ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ, 2020, том 56, № 9, с. 1471-1475
КРАТКИЕ СООБЩЕНИЯ
УДК 547.388.3 + 547.597 + 547.598.5 + 542.943.5
ПРЕВРАЩЕНИЯ ПЕРОКСИДНЫХ ПРОДУКТОВ
ОЗОНОЛИЗА (-)-α-ПИНЕНА И (+)-3-КАРЕНА
ПОД ДЕЙСТВИЕМ ГИДРАЗИДА
п-ГИДРОКСИБЕНЗОЙНОЙ КИСЛОТЫ
© 2020 г. Ю. В. Мясоедова*, Э. Р. Нуриева, Л. Р. Гарифуллина, Г. Ю. Ишмуратов
ФГБУН «Уфимский Институт химии Уфимского федерального исследовательского центра РАН»,
450054, Россия, Республика Башкортостан, г. Уфа, пр. Октября 71
*e-mail: legostaevayuv@yandex.ru
Поступила в редакцию 08 июня 2020 г.
После доработки 21 июня 2020 г.
Принята к публикации 26 июня 2020 г.
При обработке пероксидных продуктов озонолиза тризамещенных бициклических монотерпенов
(-)-α-пинена и (+)-3-карена гидразидом п-гидроксибензойной кислоты с высокими выходами образуются
в CH2Cl2 или ТГФ соответствующие кетокислоты, а в МеОН - кетоэфиры.
Ключевые слова: озонолиз, (-)-α-пинен, (+)-3-карен, гидразид п-гидроксибензойной кислоты.
DOI: 10.31857/S0514749220090207
Терпены, а также их производные являются из-
озонирования, а также, главным образом, от ре-
вестными биологически активными веществами,
агентов, разрушающих промежуточно образую-
поэтому функционализация терпеновых субстра-
щиеся пероксиды [6, 7]. Таких реагентов доста-
тов не теряет актуальности, а получение из них но-
точно много, причем, по нашему мнению, интерес
вых соединений и изучение их полезных свойств -
в качестве восстановителей пероксидных соеди-
активно развивающееся направление современной
нений представляют производные гидразина, из-
органической химии [1-3]. Подавляющее боль-
вестного своими восстановительными свойства-
шинство терпенов имеют в структуре двойные
ми. Данная работа является продолжением серии
связи, отличающиеся положением (эндо- или экзо-
исследований по изучению гидразидов кислот в
циклические), степенью замещенности (моно-,
качестве восстановителей пероксидных продук-
ди-, три- и тетразамещенные), а также наличи-
тов озонолиза природных монотерпенов [8-10] и
ем заместителей. Озонолитическое расщепление
посвящена изучению гидразида п-гидроксибен-
двойных связей является эффективным способом
зойной кислоты как восстановителя пероксидных
введения в ненасыщенные субстраты функцио-
продуктов озонолиза бициклических циклоалке-
нальных групп и широко применяется в направ-
нов с тризамещенной эндоциклической двойной
ленном синтезе практически важных веществ
связью - (-)-α-пинена 1 (ее 86%) и (+)-3-карена 2
[4, 5].
(ее 100%), легко доступных из хвойных растений
Механизм реакции озонолиза хорошо изучен:
семейства сосновых Pinaceae. Так как раствори-
известно, что итог реакции зависит от таких фак-
тель оказывает существенное влияние на строение
торов как используемый растворитель, условия
образующихся пероксидных продуктов озонолиза,
1471
1472
МЯСОЕДОВА и др.
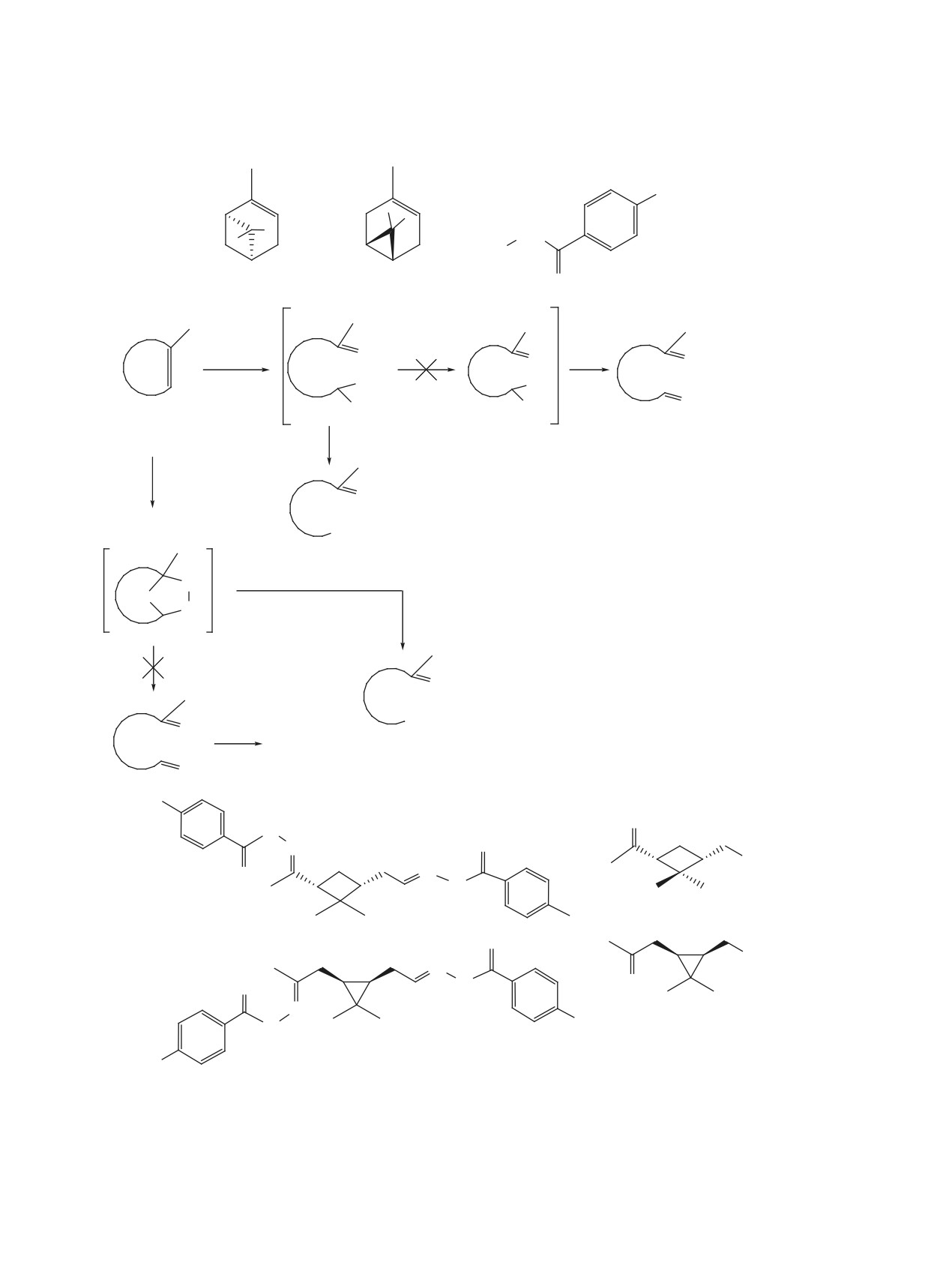
Схема 1.
OH
NH
H2N
O
1
2
3
3
O
O3
O
NNHC(O)-p-OH-C6H4
MeOH
OOH
OH
OMe
OMe
NNHC(O)-p-OH-C6H4
1, 2
3
-H2O
4, 5
CH2Cl2
O3
or THF
O
CO2Me
6, 7
3
O
O
перегруппировка
O
3
O
CO2H
O
4, 5
8, 9
O
HO
H
O
N
N
O
CO2R'
O
N
N
H
6, 8
OH
4
O
CO2R'
N
N
O
O
H
N
7, 9
OH
N
H
HO
5
R' = Me (6, 7); H (8, 9).
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 9 2020
ПРЕВР
АЩЕНИЯ ПЕРОКСИДНЫХ ПРОДУКТОВ ОЗОНОЛИЗА (-)-α-ПИНЕНА И (+)-3-КАРЕНА
1473
Использованный растворитель и выходы полученных соединений.
Терпен
Растворитель
Продукт реакции
Выход, %
1
МеОН
6
86
1
CH2Cl2
8
89
1
ТГФ
8
54
2
МеОН
7
72
2
CH2Cl2
9
76
2
ТГФ
9
78
а также конечных продуктов реакции, превраще-
CHCl3, промывали насыщенным раствором NaCl,
ния выполнялись в протонодонорном (МеОН) и
сушили Na2SO4 и упаривали.
апротонных (CH2Cl2, ТГФ) растворителях.
При проведении реакции в метаноле из α-пине-
Исходя из ранее полученных результатов на
на 1 получили 0.63 г (86%) кетоэфира 6, из 3-каре-
примере гидразидов бензойной [9] и изоникотино-
на 2 - 0.53 г (72%) кетоэфира 7. ИК и ЯМР спектры
вой [10] кислот можно предположить, что вероят-
соединений 6 и 7 идентичны описанным в [11].
ными продуктами реакции в метаноле могут быть
Метил [(1R,3R)-3-ацетил-2,2-диметилцикло-
дигидразоны 4, 5 либо кетоэфиры 6, 7, а в ТГФ или
бутил]ацетат (6). Rf 0.44 (гексан-метил-трет-
СH2Сl2 - дигидразоны 4, 5 либо кетокислоты 8 и 9
бутиловый эфир, 2:1), [α]D20 -24.8° (с 0.73, CH2Cl2).
(схема 1). О механизмах этих реакций нами более
подробно написано в работе [9].
Метил
[(1S,3R)-2,2-диметил-3-(2-оксопро-
0.42 (гексан-
пил)циклопропил]ацетат (7). Rf
В результате проведенных экспериментов уста-
метил-трет-бутиловый эфир, 2:1), [α]D20
-19.9
новлено, что продуктами реакции с выходами от
(c 16.50, CH2Cl2).
54 до 89% в апротонных растворителях являют-
ся кетокислоты 8 и 9, а в метаноле их метиловые
При проведении реакции в CH2Cl2 из α-пинена
1 получили 0.61 г (89%) кетокислоты 8, из 3-каре-
эфиры 6 и 7. Диацилгидразоны 4 или 5 ни в одном
на 2 - 0.52 г (76%) кетокислоты 9.
из растворителей не образуются (см. таблицу).
При проведении реакции в тетрагидрофуране
Таким образом, гидразид п-гидроксибензойной
из α-пинена 1 получили 0.37 г (54%) кетокислоты
кислоты является эффективным реагентом для
превращения пероксидных продуктов озоноли-
8, из 3-карена 2 - 0.49 г (72%) кетокислоты 9.
за тризамещенных бициклических монотерпенов
[(1R,3R)-(3-Ацетил-2,2-диметилциклобу-
(-)-α-пинена и (+)-3-карена в кетокарбоксильные
тил)]уксусная кислота
(8). Rf
0.21 (гексан-
соединения, очевидно, за счет дегидратации ме-
метил-трет-бутиловый эфир, 4:1), [α]D20 -39.8°
токсигидропероксидов или перегруппировки озо-
(с 0.82, CH2Cl2).
нидов.
[(1R,3S)-(2,2-Диметил-3-(2-оксопропил)ци-
Общая методика проведения эксперимента.
клопропил)]уксусная кислота (9). Rf 0.19 (гек-
Через раствор 0.5 г (3.7 ммоль) α-пинена 1 или
сан-метил-трет-бутиловый эфир, 4:1), [α]D20 -14°
3-карена 2 в 20 мл абс. МеОН или ТГФ или
(с 2.23, CH2Cl2).
CH2Cl2 при 0°С барботировали О3/О2 смесь до по-
ИК и ЯМР спектры соединений 8 и 9 идентич-
глощения 4 ммоль О3. Реакционную смесь проду-
ны описанным в [12].
вали аргоном. Добавляли (0°С) 1.7 г (11.0 ммоль)
гидразида п-оксибензойной кислоты 3, перемеши-
ИК спектры записывали на приборе IR
вали при комнатной температуре до исчезнове-
Prestige-21 (Fourier Transform Spectrophotometer -
ния пероксидов (контроль йод-крахмальная про-
Shimadzu) в тонком слое. Спектры ЯМР реги-
ба), растворитель отгоняли, остаток растворяли в
стрировали на спектрометре Bruker Avance III 500
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 9 2020
1474
МЯСОЕДОВА и др.
[рабочие частоты 500.13 (1Н), 125.76 (13С) МГц]
[Ishmuratov G.Yu., Legostaeva Yu.V., Botsman L.P.,
в CDCl3, внутренний стандарт - ТМС. Оптическое
Tolstikov G.A. Russ. J. Org. Chem. 2010, 46, 1593-
вращение измеряли на поляриметре Perkin Elmer
1621.] doi 10.1134/S1070428010110011
241-MC. Контроль методом ТСХ проводили на
7.
Мясоедова Ю.В., Назаров И.С., Ишмуратов Г.Ю.
SiO2 марки Sorbfil (Россия).
ЖОрХ. 2019, 55, 67-99. [Myasoedova Yu.V., Naza-
БЛАГОДАРНОСТИ
rov I.S., Ishmuratov G.Yu. Russ. J. Org. Chem. 2019,
55, 47-73.] doi 10.1134/S107042801901007X
В работе использовали оборудование Центра
8.
Легостаева Ю.В., Гарифуллина Л.Р., Назаров И.С.,
коллективного пользования
«Химия» УфИХ
Кравченко А.А., Ишмуратова Н.М.,
Ишмура-
УФИЦ РАН.
тов Г.Ю. ХПС. 2017, 5, 758-761. [Legostaeva Yu.V.,
ФОНДОВАЯ ПОДДЕРЖКА
Garifullina L.R., Nazarov I.S., Kravchenko A.A.,
Работа выполнена при финансовой поддерж-
Ishmuratova N.M., Ishmuratov G.Yu. Chem. Nat.
ке программы РАН «Фундаментальные основы
Compd. 2017, 53, 891-894.] doi 10.1007/s10600-017-
химии», тема № 8 «Хемо-, регио- и стереоселек-
2149-2
тивные превращения терпеноидов, стероидов
9.
Мясоедова Ю.В., Гарифуллина Л.Р., Нуриева Э.Р.,
и липидов в направленном синтезе низкомоле-
Ишмуратова Н.М., Ишмуратов Г.Ю. ХПС. 2020,
кулярных биорегуляторов»
(№ госрегистрации
56, 227-230. [Myasoedova Yu.V., Garifullina L.R.,
АААА-А17-117011910023-2, 2017 г.).
Nurieva E.R., Ishmuratova N.M., Ishmuratov G.Yu.
Chem. Nat. Compd. 2020, 56, 259-263.] doi 10.1007/
КОНФЛИКТ ИНТЕРЕСОВ
s10600-020-03002-5
Авторы заявляют об отсутствии конфликта ин-
10.
Легостаева Ю.В., Гарифуллина Л.Р., Назаров И.С.,
тересов.
Ишмуратов Г.Ю. ЖОрХ.
2018,
54,
145-146.
СПИСОК ЛИТЕРАТУРЫ
[Legostaeva Yu.V., Garifullina L.R., Nazarov I.S.,
1. Племенков В.В. ХРС. 2006, 3, 55-72.
Ishmuratov G.Yu. Russ. J. Org. Chem. 2018, 54, 146-
148.] doi 10.1134/S1070428018010165
2. Фролова Л.Л., Безуглая Л.В., Попов А.В., Ку-
чин А.В., Вендило Н.В. Изв. Коми научного центра
11.
Ишмуратов Г.Ю., Легостаева Ю.В., Боцман Л.П.,
УрО РАН. 2012, 1, 11-23.
Яковлева М.П., Шаханова О.О., Муслухов Р.Р.,
3. Шадеркина В.А., Шадеркин И.А. Экспер. Клин.
Толстиков Г.А. ХПС. 2009, 45, 272-275. [Ishmura-
Урол. 2019, 1, 77-80. doi 10.29188/2222-8543-2019-
tov G.Yu., Legostaeva Yu.V., Botsman L.P., Yakovle-
11-1-77-80
va M.P., Shakhanova O.O., Muslukhov R.R., Tolsti-
4. Van Ornum S.G., Champeau R.M., Pariza R. Chem.
kov G.A. Chem. Nat. Compd. 2009, 45, 318-321.] doi
Rev. 2006, 106, 2990-3001. doi 10.1021/cr040682z
10.1007/s10600-009-9354-6
5. Ишмуратов Г.Ю., Легостаева Ю.В., Гарифул-
12.
Ишмуратов Г.Ю., Легостаева Ю.В., Гарифул-
лина Л.Р., Боцман Л.П., Яковлева М.П., Толсти-
лина Л.Р., Боцман Л.П., Муслухов Р.Р., Толсти-
ков Г.А. ХПС. 2015, 51, 177-196. [Ishmuratov G.Yu.,
ков Г.А. ЖОрХ. 2014, 50, 1095-1101. [Ishmura-
Legostaeva Yu.V., Garifullina L.R., Botsman L.P.,
Yakovleva M.P., Tolstikov G.A. Chem. Nat. Compd.
tov G.Yu., Legostaeva Yu.V., Garifullina L.R.,
2015, 51, 199-219.] doi 10.1007/s10600-015-1246-3
Botsman L.P., Muslukhov R.R., Tolstikov G.A. Russ.
6. Ишмуратов Г.Ю., Легостаева Ю.В., Боцман Л.П.,
J. Org. Chem. 2014, 50, 1075-1081.] doi 10.1134/
Толстиков Г.А. ЖОрХ.
2010,
46,
1591-1617.
S1070428014080016
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 9 2020
ПРЕВР
АЩЕНИЯ ПЕРОКСИДНЫХ ПРОДУКТОВ ОЗОНОЛИЗА (-)-α-ПИНЕНА И (+)-3-КАРЕНА
1475
Transformations of Peroxide Products from Ozonolysis
of (-)-α-Pinene and (+)-3-Carene by p-Hydroxybenzoic
Acid Hydrazide
Yu. V. Myasoedova*, E. R. Nurieva, L. R. Garifullina, and G. Yu. Ishmuratov
Ufa Institute of Chemistry, Ufa Researcher Centre, RAS,
450054, Russia, Republic of Bashkortostan, Ufa, pr. Oktyabrya 71
*е-mail: legostaevayuv@yandex.ru
Received June 8, 2020; revised June 21, 2020; accepted June 26, 2020
When the peroxide products of ozonolysis of trisubstituted bicyclic monoterpenes (-)-α-pinene and (+)-3-carene
are treated with p-hydroxybenzoic acid hydrazide, the corresponding ketoacids (in CH2Cl2 or THF) and ke-
toesters (in MeOH) are formed with good yields.
Keywords: ozonolysis, (-)-α-pinene, (+)-3-carene, p-hydroxybenzoic acid hydrazide
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 9 2020