ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ, 2021, том 57, № 5, с. 737-741
КРАТКИЕ СООБЩЕНИЯ
УДК 547.022 + 661.7 + 615.28
ПOЛУЧЕНИЕ ПРОДУКТОВ КОНДЕНСАЦИИ,
ПОКАЗЫВАЮЩИХ БИОЛОГИЧЕСКУЮ АКТИВНОСТЬ
НА ОСНОВЕ ФЕНИЛТИОЗОЛИДИНА И АЛЬДЕГИДОВ
© 2021 г. Г. Ш. Дурускари*, А. М. Магеррамов
Бакинский государственный университет, Азербайджан, 1148 Баку, ул. З. Халилова, 23
*e-mail: gduruskari@mail.ru
Поступила в редакцию 14.01.2021 г.
После доработки 21.01.2021 г.
Принята к публикации 22.01.2021 г.
На основе 3-амино-5-фенилтиозолидин-2-иминиий бромида были синтезированы биологически активные
вещества и изучена их биологическая активность. Структуры полученных соединений подтверждены
методами 1Н и 13С ЯМР спектроскопий и методом РСА.
Ключевые слова: альдегид, Шиффовы основания, биологическая активность
DOI: 10.31857/S0514749221050062
Соединения, содержащие тиазолидиновый
Синтез соответствующих Шиффовых осно-
фрагмент, проявляют антимикробную и антиокис-
ваний на основе 3-амино-5-фенил-тиазолидин-2-
лительную активность [1, 2]. Метод синтеза соеди-
иминий-бромида с различными альдегидами пока-
нений, проявляющих широкий спектр биологиче-
зан на схеме 1.
ской активности, достаточно сложен и получается
3-[(4-Хлорбензилиден)амино]-5-фенилтиазо-
на основе недоступных исходных веществ. В связи
лидин-2-иминий бромид (1). К 0.4 г (0.001 моль)
с этим данные методы практически невыгодны, но
3-амино-5-фенилтиазолидин-2-иминий-бро-
расширение исследований в этой области целена-
мида добавляли этиловый спирт, а зaтем 0.27 г
правленно. Изучение биологических активностей
(0.001 моль) 4-хлорбензальдегида. Смесь переме-
данных соединений значимо для медицины.
шивали при кипении в течение 2 ч. Полученные
На основе проведенных нами работ [3] были
белые кристаллы отфильтровывали и промыва-
получены продукты конденсации - Шиффовы
ли ацeтоном. Выход 0.5 г (78%), т.пл. 258-259°С.
основания по реакции 3-амино-5-фенил-тиазоли-
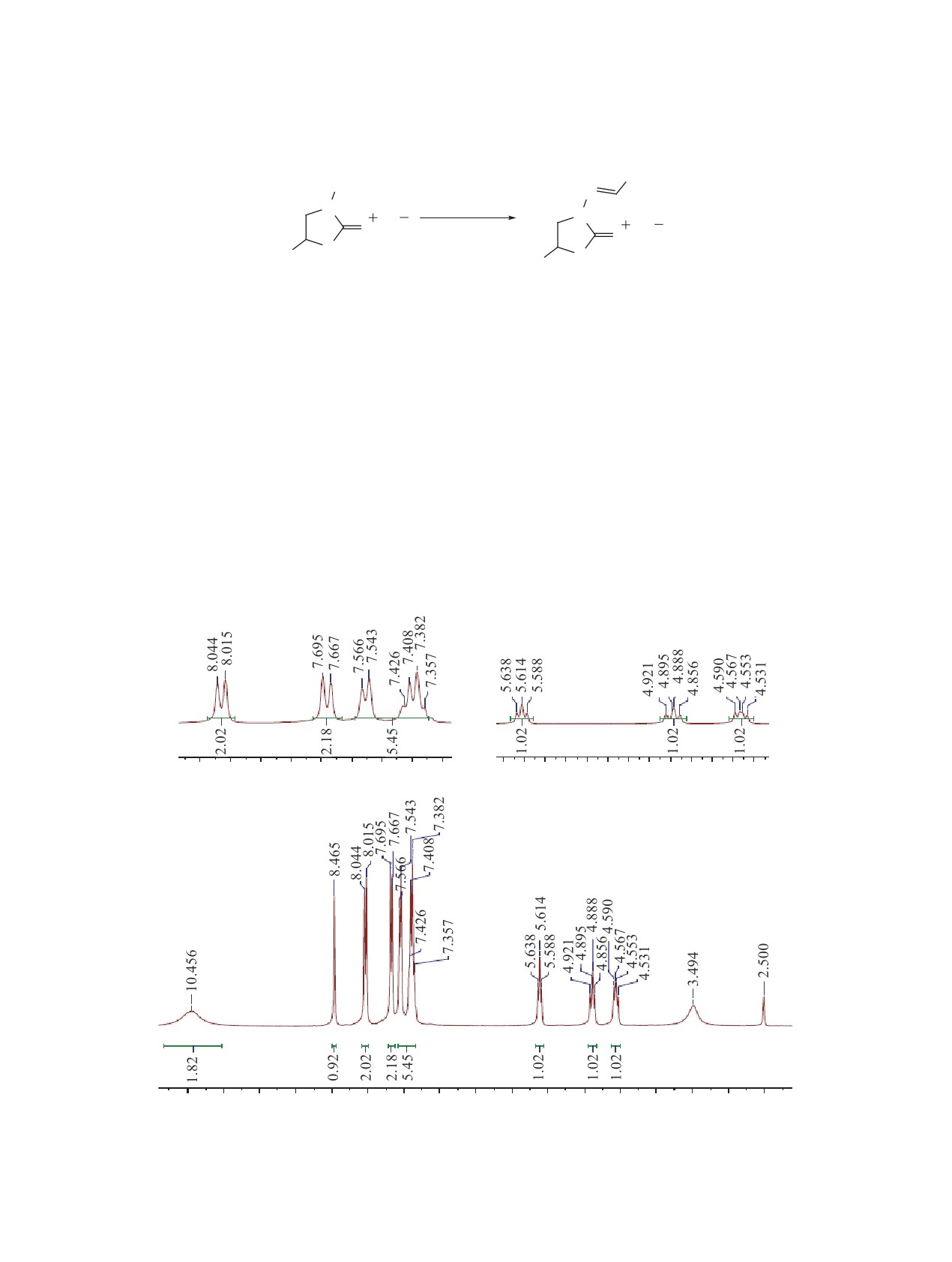
Спектр ЯМР 1H (300 МГц, DMSO-d6), δ, м.д.: 4.56
дин-2-иминий-бромида с другими различными
к (1H, CH2, 3JHH 6.9 Гц), 4.89 т (1H, CH2, 3JHH
альдегидами. Продукты реакции были осаждены
7.8 Гц), 5.61 т (1Hаром, 3JHH 7.2 Гц), 7.36-8.04
в виде монокристалла. Был изучен эффект унич-
м (9Hаром), 8.47 с (1H, CH=), 10.46 с (1H, NH=).
тожения продуктов-паразитов воспалительных
Спектр ЯМР 13C (75 MГц, DMSO-d6), δ, м.д.: 45.40,
процессов, таких как Staphylococcus aureus, грам-
55.95, 125.13, 127.77, 128.85, 129.06, 130.49, 131.84,
негативные бактерии Esherichia coli, пигментобра-
132.15, 137.40, 149.94, 167.96. Масс-спектр (ESI),
зующий грамнегативные палочки Pseudomonas
m/z: 316.82 [C16H15ClN3S]+ и 79.88 Br-. Найдено,
aeruginoza,
дрожжевые бактерии Candida
%: С 60.00; Н 4.69; N 13.20. С16Н15BrClN3S.
albicans.
Вычислено, %: С 60.66; Н 4.74; N 13.27.
737
738
ДУРУСКАРИ, МАГЕРРАМОВ
Схема 1
Ar
NH2
N
N
ArCHO, EtOH
N
NH2Br
кипячение, 2 ч
NH2Br
S
Ph
S
Ph
1-5
Ar = 4-Cl-C6H4 (1), C6H5 (2), 4-CH3-C6H4 (3),
4-F-C6H4 (4), 4-CF3-C6H4 (5).
3-[(Бензилиден)амино]-5-фенилтиазолидин-
m/z: 282.30 [C16H16N3S]+ и 79.88 Br-. Найдено, %:
2-иминий бромид (2). Методика синтеза анало-
С 53.00; Н 4.40; N 11.53. С16Н15BrN3S. Вычислено,
гична методике синтеза для соединения (1). Выход
%: С 53.04; Н 4.41; N 11.60.
0.2 г (76%), светло желтые кристаллы, т.пл. 246°С.
3-[(4-Метилбензилиден)амино]-5-фенилтиа-
Спектр ЯМР 1H (300 МГц, DMSO-d6), δ, м.д.: 4.58
золидин-2-иминий бромид (3). Методика синте-
к (1H, CH2, 3JHH 6.9 Гц), 4.89 т (1H, CH2, 3JHH
за аналогична методике синтеза для соединения
8.1 Гц), 5.60 т (1Hаром, 3JHH 7.5 Гц), 7.37-8.07 м
(10Hаром), 8.44 с (1H, CH=), 10.35 с (1H, NH=).
(1). Выход 0.3 г (54%), белые кристаллы, т.пл.
Спектр ЯМР 13C (75 MГц, DMSO-d6), δ, м.д.: 45.36,
228°С. Спектр ЯМР 1H (300 МГц, DMSO-d6), δ,
55.91, 127.76, 128.65, 128.82, 128.86, 129.09, 131.54,
м.д.: 2.33 с (3H, CH3), 4.55 к (1H, CH2, 3JHH 6.6 Гц),
132.85, 137.48, 151.11, 167.84. Масс-спектр (ESI),
4.88 т (1H, CH2, 3JHH 8.1 Гц), 5.60 т (1Наром, 3JHH
8.0
7.8
7.6
7.4
5.7
5.5
5.3
5.1
4.9
4.7
4.5
10.0
9.0
8.0
7.0
6.0
5.0
4.0
3.0
Спектр ЯМР 1Н соединения 1
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 57 № 5 2021
ПOЛУЧЕНИЕ ПРОДУКТОВ КОНДЕНСАЦИИ
739
Антимикробная активность соединений 1-5
Исследуемое вещество
Тест-культура
Срок экспозиции, мин
1
2
3
4
5
10
–
-
-
-
-
20
-
-
-
-
-
Staphylococcus aureus
40
-
-
-
-
-
60
-
-
-
-
-
10
–
-
-
-
-
20
–
-
-
-
-
Esherichia coli
40
-
-
-
-
-
60
-
-
-
-
-
10
–
-
-
-
-
20
–
-
-
-
-
Pseudomonas aeruginoza
40
-
-
-
-
-
60
-
-
-
-
-
10
–
-
-
-
-
20
–
-
-
-
-
Candida albicans
40
-
-
-
-
-
60
-
-
-
-
-
7.5 Гц), 7.28-7.98 м (9Hаром), 8.41 с (1H, CH=), 10.33
соединения (1). Выход 0.4 г (73%), белые кристал-
с (1H, NH=). Спектр ЯМР 13C (75 MГц, DMSO-d6),
лы, т.пл. 230-232°С. Спектр ЯМР 1H (300 МГц,
δ, м.д.: 21.27, 45.36, 55.90, 127.79, 128.69, 129.09,
DMSO-d6), δ, м.д.: 4.58 к (1H, CH2, 3JHH 6.6 Гц),
129.46, 130.21, 137.50, 141.68, 151.04, 167.50.
4.89 т (1H, CH2, 3JHH 8.4 Гц), 5.60 т (1Hаром, 3JHH
Масс-спектр (ESI), m/z:
296.40
[C17H18N3S]+ и
7.5 Гц), 7.39-8.29 м (9Hаром), 8.51 с (1H, CH=), 10.51
79.88 Br-. Найдено, %: С 54.19; Н 4.73; N 11.00.
с (1H, NH=). Спектр ЯМР 13C (75 MГц, DMSO-d6),
С17Н18BrN3S. Вычислено, %: С 54.26; Н 4.79; N
δ, м.д.: 45.45, 56.03, 125.74, 125.80, 127.86, 128.95,
11.17.
129.15, 129.22, 130.72, 131.14, 136.85, 137.50,
149.54, 168.62. Масс-спектр (ESI), m/z:
350.38
3-[(4-Фторбензилиден)амино]-5-фенилтиа-
[C17H15F3N3S]+ и 79.88 Br-. Найдено, %: С 47.41;
золидин-2-иминий бромид (4). Методика синте-
Н 3.42; N 9.74. С17Н15BrF3N3S. Вычислено, %: С
за аналогична методике синтеза для соединения
47.44; Н 3.49; N 9.76.
(1). Выход 0.35 г (64%), белые кристаллы, т.пл.
271-272°С. Спектр ЯМР 1H (300 МГц, DMSO-d6),
Данные соединения были синтезированны
δ, м.д.: 4.56 к (1H, CH2, 3JHH 6.6 Гц), 4.87 т (1H,
более удобным методом, что показывает доста-
CH2, 3JHH 7.8 Гц), 5.60 т (1Hаром, 3JHH 7.8 Гц),
точно хорошие антимикробные свойства. Для
7.32-8.16 м (9Hаром), 8.45 с (1H, CH=), 10.37 с
изучения этих свойств проведены анализы с ме-
(1H, NH=). Спектр ЯМР 13C (75 MГц, DMSO-d6),
тодами тест-культуры и разбавления по сериям.
δ, м.д.: 45.39, 55.97, 116.05, 127.81, 128.91, 129.13,
Полученные результаты представлены в таблице.
129.60, 131.05, 131.17, 137.55, 150.00, 167.89.
В результате можно утверждать, что синтези-
Масс-спектр (ESI), m/z: 300.36 [C16H15FN3S]+ и
рованные вещества более эффективны, чем эти-
79.88 Br-. Найдено, %: С 50.50; Н 3.89; N 11.00.
ловый спирт, взятый в качестве контроля. Данные
С16Н15BrFN3S. Вычислено, %: С 50.52; Н 3.95; N
вещества как в концентрированной, так и в разбав-
11.05.
ленных формах (1:100, 1:200, 1:400, 1:800) пода-
3-[(4-Трифторметил)бензилиден]амино-5-
вляют развитие вредных микроорганизмов, даже
фенилтиазолидин-2-иминий бромид
(5). Ме-
штамм Pseudomonas aeruginosa, считаемый самым
тодика синтеза аналогична методике синтеза для
сильным.
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 57 № 5 2021
740
ДУРУСКАРИ, МАГЕРРАМОВ
Все реагенты закуплены от фирм Merck и
низмов, даже считаемый самым сильным штамм
Fluka и использовались без дальнейшей очистки.
Pseudomonas aeruginosa.
Спектры ЯМР 1Н и 13С регистрировали на спек-
КОНФЛИКТ ИНТЕРЕСОВ
трометре Bruker Avance 300 МГц (на частотах 300
и 75 МГц соответственно). Кристаллическое стро-
Авторы заявляют об отсутствии конфликта ин-
ение синтезированных соединений было снято ме-
тересов
тодом (РСА) при помощи аппарата X-REY SMART
СПИСОК ЛИТЕРАТУРЫ
APEX II. Температуры плавления измеряли на
аппарате Stuart 30. Ход реакции контролировали
1. Katayama H., Morisue S. Tetrahedron. 2017, 73, 3541-
3546. doi 10.1016/j.tet.2017.05.04
методом тонкослойной хроматографии (ТСХ) на
аллюминиевых пластинках с силикагелем 60 F254.
2. Veale E., O’Brien J., McCabe T., Gunnlaugsson T.
Tetrahedron.
2008,
64,
6794-6800. doi
10.1016/
ВЫВОДЫ
j.tet.2008.04.097
Синтезированные вещества более эффектив-
3. Дурускари Г.С., Аскерова А.Р., Алыева Х.Н., Муса-
ные, чем этиловый спирт, взятый в качестве кон-
ева С.А., Магеррамов А.М. ЖОрХ. 2020, 56, 636-
троля. Данные вещества как в концентрированной,
640. [Duruskari G.S., Asgarova A.R., Aliyeva K.N.,
так и в разбавленных формах (1:100, 1:200, 1:400,
Musayeva S.A., Maharramov A.M. Russ. J. Org. Chem.
1:800) подавляют развитие вредных микроорга-
2020, 56, 712-715.] doi 10.1134/S1070428020040223
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 57 № 5 2021
ПOЛУЧЕНИЕ ПРОДУКТОВ КОНДЕНСАЦИИ
741
Obtaining of Condensation Products Showing Biological
Activity Based on Phenylthiazolidine and Aldehydes
G. Sh. Duruskari* and A. M. Maharramov
Baku State University, ul. Z. Khalilova, 23, Baku, 1148 Azerbaijan
*e-mail: gduruskari@mail.ru
Received January 14, 2021; revised January 21, 2021; accepted January 22, 2021
On the base of 3-amino-5-phenylthiazolidine-2-iminium bromide was synthesized the biological activity sub-
stances and studied them biological activity. Structures of synthesized compounds confirmed by 1H, 13C NMR
spectroscopy and method X-RAY structural analysis.
Keywords: aldehyde, Shiff bases, biological activity
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 57 № 5 2021