ПАРАЗИТОЛОГИЯ, 2019, том 53, № 4, с. 342-347.
УДК 595.122 : 59.084:591.044
МЕТОДЫ ИЗУЧЕНИЯ
ХЕМОРЕАКЦИЙ ЦЕРКАРИЙ ТРЕМАТОД
© 2019 г. В. В. Прокофьев*
Псковский государственный университет,
пл. Ленина, д. 2, Псков
180000, Россия
*e-mail: prok58@mail.ru
Поступила в редакцию 10.03.2019 г.
После доработки 31.05.2019 г.
Принята к публикации 07.06.2019 г.
Экспериментально подбирали наиболее подходящие методики для исследования хемореакций
церкарий трематод. Для изучения контактных реакций наиболее эффективным оказалось ис-
пользование агаровых блоков, пропитанных метаболитами вторых промежуточных хозяев, а для
дистантньх рекаций - использование микроаквариумов с узкими каналами, в которых создается
градиент сигнала.
Ключевые слова: трематоды, церкарии, хемореакции, методы.
DOI: 10.1134/S0031184719040057
В сложном жизненном цикле трематод (Trematoda, Digenea) личинка (церкария) по-
ловозрелых особей гермафродитного поколения (марит) выполняет расселительную
функцию. В ее задачи входят поиск и проникновение в организм второго промежу-
точного или дефинитивного хозяев. При этом церкария ориентируется в пространстве
при помощи системы таксисов и кинезов (см. обзоры: Haas, 2003; Chaisson, Hallem,
2012). Они позволяют личинке найти «пространство хозяина» и/или пребывать в этом
пространстве, т.е. там где встреча с потенциальным животным-хозяином наиболее ве-
роятна, а при появлении хозяина в непосредственной близости - обнаружить и напасть
на него (Combes, 2001).
Одним из наименее изученных аспектов биологии церкарий является вопрос о на-
личии и особенностях проявления у них хемореакций. Такое положение во многом
объясняется методическими сложностями проведения подобных исследований, в част-
ности, трудностью выбора критериев наличия или отсутствия у этих личинок хемчув-
ствительности в условиях эксперимента. Немногие исследования, которые посвящены
анализу этого явления, выполнены на «пресноводных» трематодах, жизнедеятельность
личинок которых походит в пресноводных бассейнах (Fried, King 1989; Haas et al., 1995,
2002; Körner, Haas 1998a, 1998b и др.). Установлено, что следует различать дистант-
342
ную и контактную хемочувствительность. Дистантная, благодаря которой церкария
ищет хозяина, выявлена у личинок некоторых эхиностоматид (Pseudechinoparyphium
echinatum, Echinostoma revolutum) (Haas, 2003), которые для своего дальнейшего раз-
вития должны заразить моллюска. Ориентация идет по выделяемым моллюсками ме-
таболитам (компоненты слизи, аминокислоты, моча, аммиак и др.), градиент которых,
после выделения, в условиях спокойного пресного водоема какое-то время сохраняет-
ся в толще воды (Haas et al., 1995; Körner, Haas, 1998a, 1998b, Haberl et al., 2000).
Контактными реакциями обладают, по-видимому, многие, если не все церкарии.
С помощью этих реакций идет распознавание подходящего хозяина при контакте с ним
или выбраковка неподходящего, поиск места внедрения и сам процесс внедрения. До
настоящего времени хемочувствительность при контакте с хозяином изучена только
для ряда видов Schistosomatidae и Diplostomidae (Haas, 2003). Распознавание ведет-
ся по целому комплексу макромолекул, ассоциированных с покровами хозяина. Это
жирные кислоты, церамиды, хлистерол, L-аргинин и др. для церкарий шистосоматид,
заражающих млекопитающих и птиц; и углеводы, гликопротеины, жирные кислоты
и др. для диплостомид, инвазирующих рыб (Haas, 2003).
Работы же по хемочувствительности морских видов трематод, включая те, которые
реализуют свои жизненные циклы в экосистемах литорали и верхней сублиторали,
отсутствуют, что и побудило нас приступить к их исследованию. На первом этапе не-
обходимо было разработать адекватные методики проведения экспериментов с цер-
кариями морских трематод. Их описанию и посвящена статья. В качестве модельных
объектов были выбраны церкарии Himasthla elongata (Mehlis, 1831) (Himasthlidae,
Echinostomatoidea) и Cryptocotyle lingua (Creplin, 1825) Fischoeder, 1903 (Heterophyidae).
В условиях Белого моря, где проводилось исследование, вторым промежуточным хозя-
ином, которого заражают церкарии, для Н. elongata являются двустворки Mytilus edulis
Linnaeus, 1758 (Mytilidae), а для С. lingua - молодь разных видов прибрежных рыб.
МАТЕРИАЛ И МЕТОДИКА
Работа выполнена на Беломорской биологической станции ЗИН РАН («Картеш»), расположен-
ной в губе Чупа Белого моря, в июле-августе 2017-2018 гг. Источником церкарий для экспери-
ментов служили литоральные моллюски Littorina littorea (Linnaeus, 1758), зараженные партени-
тами трематод Н. elongata и С. lingua. Моллюсков собирали вблизи биостанции, индивидуально
помещали в пластиковые емкости объемом 70 мл и выставляли на 0.5-1 ч на солнце или под свет
лампы накаливания (20 000-30 000 лк).
После этого емкости просматривали с помощью стереомикроскопа МСП-1 и отбирали ли-
торин, выделивших церкарий. Этих моллюсков содержали в садке в естественных условиях
(в бухте Кривозерская у причала ББС) и по мере необходимости использовали для получения
церкарий, необходимых для эксперимента, по методике, описанной выше.
Контактные реакции церкарий изучали с помощью агаровых моделей. Для этого перед про-
ведением опыта предварительно готовили 1.5% бакто-агар. После застывания агара из него вы-
резали бруски размером 3х3х1.5 мм. Блоки помещали на 1 сутки в сосуд с водой температурой
10-12 ºС, где находились либо вторые промежуточные хозяева исследуемых церкарий (мидии
или маслюки), либо слизь с покровов трески. В эту воду выделялись метаболиты хозяев, и ага-
ровые блоки, соответственно, пропитывались этими веществами. Вода с метаболитами хозяев
определялась нами как «кондиционированная». Затем блоки, выдержанные в «кондициониро-
ванной» воде, использовали для проведения экспериментов.
343
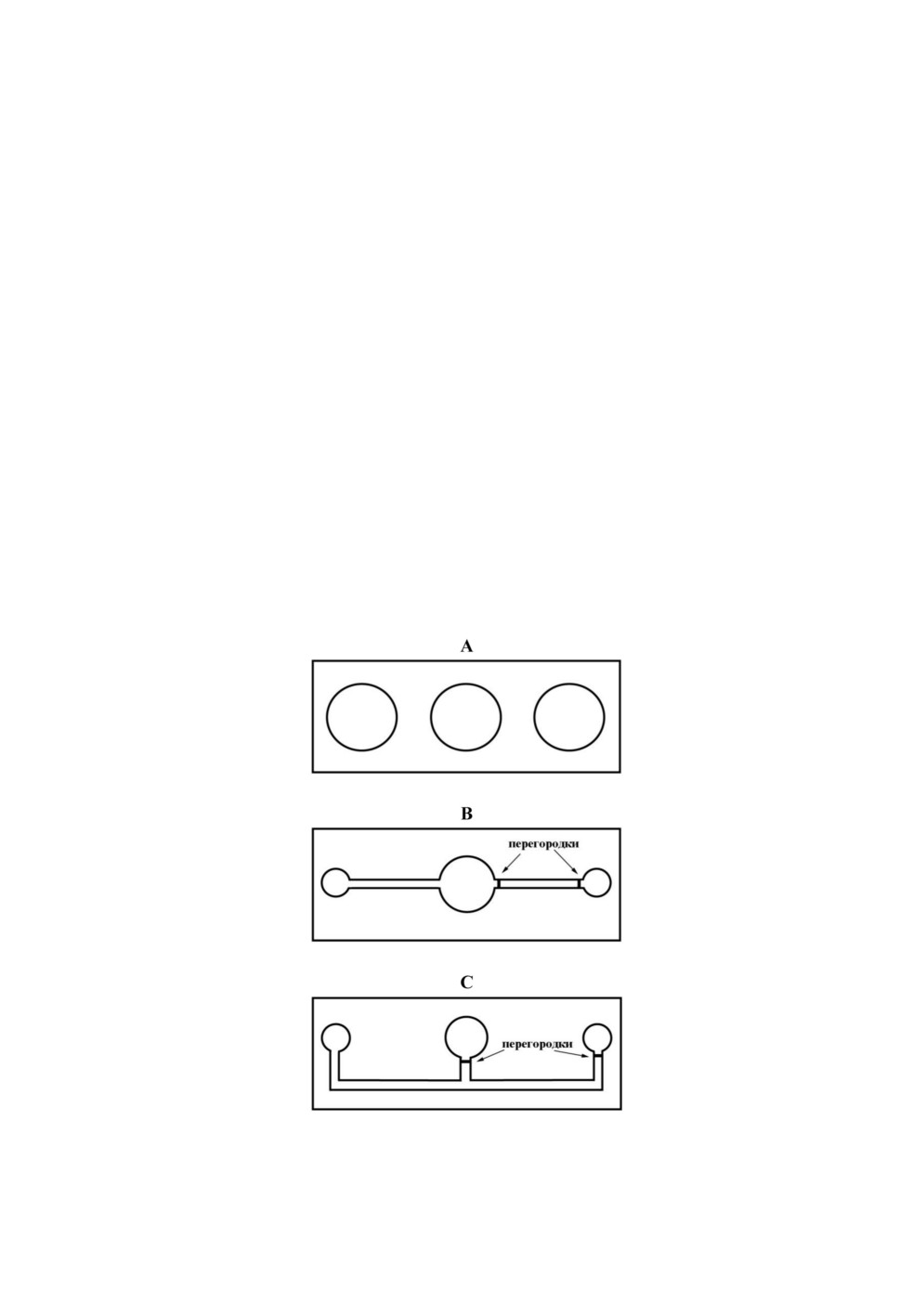
Для изучения контактных реакций церкарий была изготовлена специальная установка, вклю-
чающая три отдельных микроаквариума глубиной 5 мм и диаметром 18 мм каждый, объеди-
ненных в одном блоке (80x30x8 мм) (Рис.1A). Подобная конструкция ранее была предложена
Хаасом с соавторами (Haas et al., 1995). Однако она включала лишь один микроаквариум. Объ-
единение грех микроаквариумов в едином блоке позволяло, при необходимости, одновременно
проводить два опыта и один контроль.
При проведении наблюдений «кондиционированный» брусок агара помещали в один из ми-
кроаквариумов с фильтрованной морской водой при температуре 18-20 ºС. Туда же выпускали
церкарий в количестве 10 экз. В другой микроаквариум помещали контрольный «чистый» агаро-
вый брусок. Блок микроаквариумов располагали на столике бинокуляргого микроскопа МБС-10
и производили видеосъемку в течение 5 мин. Каждое наблюдение повторяли 5 раз. Наличие хе-
мореакции определяли по прикосновению церкарии к бруску с последующим кратковременным
прикреплением к нему. Для этого отснятое наблюдение просматривали на мониторе компьютера
и подсчитывали число касаний церкариями блока в течение 5 мин. Затем делили число касаний
на число личинок и получали число касаний на одну церкарию. Подобные подсчеты проводили
для всех 5 наблюдений и определяли среднее число касаний на одну церкарию.
Кроме агара, в качестве модели использовали полоски (10x3 мм) нитроцеллюлозной мембра-
ны (Protran). Метод основан на связывании белков и гликопротеинов с молекулами нитроцел-
люлозы на поверхности мембраны за счет гидрофобных и электростатических взаимодействий.
Для получения модели на участок мембраны наносили каплю «кондиционированной» воды и
оставляли до высыхания. В результате белки и гликонротеины, содержащиеся в «кондициониро-
ванной» воде, прочно соединялись с поверхностью мембраны. Для блокирования чистых (не об-
работанных «кондиционированной» водой) участков мембраны от неспецифичных связываний
с посторонними веществами, мембрану помещали на 30 мин. в разбавленный раствор обезжи-
ренного сухого молока с добавлением детергента Triton Х-100. При этом белок из разбавленного
раствора прикрепляется к мембране на всех участках, где не прикрепился целевой белок. Таким
образом исключалось прикрепление к мембране посторонних химических веществ и достига-
лось получение более достоверных результатов. При проведении наблюдений выполняли те же
манипуляции, что и с агаровыми брусками, но последние, при этом, заменяли обработанными
полосками мембраны.
В целях разделения метаболитов «кондиционированных» вод на фракции была произведена
попытка использовать диализные мембраны. Для этого в мешочек из диализной мембраны на-
ливали «кондиционированную» воду в объеме 1 мл. Затем мешочек на сутки помещали в сосуд
с дистиллированной водой объемом 1 мл при температуре 20 ºС, где находились агаровые бло-
ки. За счет разницы в осмотическом давлении метаболиты из мешочка через поры выходили
в воду. Поры диализной мембраны пропускали вещества молекулярной массой не более 20 кДа.
Соответственно, блоки впитывали лишь метаболиты, прошедшие через мембрану. Затем блоки
переносили в микроаквариумы и исследовали хемореакции церкарий.
Для изучения дистантных хемореакций церкарий использовали модифицированную установ-
ку, предложенную Хаасом с соавторами (Haas et al., 1995). Она включала два блока по три микро-
аквариума в каждом (Рис. 1B, 1C). Каждый блок имел размеры 80x30х8 мм. Диаметр каждого
микроаквариума, расположенного в центре блока, составлял 15 мм, диаметр каждого бокового
микроаквариума - 5 мм.
Аквариумы соединялись между собой посредством прямых (Рис. 1B) либо изогнутых
(Рис. 1C) каналов. Глубина микроаквариумов и каналов составляла 5 мл. Модифицированная
установка отличалась от установки Хааса с соавторами (Haas et al., 1995) не только размерами,
но и тем, что мы вместо внутреннего, вращающегося цилиндра с прорезью в каждом микро-
аквариуме, поворотом которого достигались открытия-закрытия связи микроаквариума с кана-
лом, применяли тонкие пластиковые либо бумажные перегородки (Рис. 1B, 1C). Использование
344
перегородок, в отличие от цилиндров, практически исключало микрозавихрения воды и, соот-
ветственно, позволяло сохранять более равномерный градиент химического сигнала.
Следует заметить, что при исследовании дистантных хемореакций микроскопических живот-
ных, к каковым относятся церкарии, серьезной проблемой является создание четко выраженно-
го градиента тестируемого химического вещества. Особенно актуально это для малых объемов
воды, когда даже незначительное сотрясение или изменение температуры приводит к движению
воды и «смазыванию» градиента. Наличие узких каналов в предложенных микроаквариумах по-
зволяет существенно снизить эффект перемешивания воды и сохранить более четкий градиент
исследуемого вещества.
Перед проведением опыта выход одного из боковых аквариумов (для удобства, как правило,
правого) закрывали перегородкой из стандартной фильтровальной бумаги (размер пор 12-15 мкм).
В этот аквариум помещали источник химического сигнала. Наличие перегородки, с одной сто-
роны, не препятствовало поступлению в канал химических веществ, выделяемых источником,
а с другой - не давало возможности церкариям напрямую контактировать с ним, т.е. исключало
возможность контактной реакции. Второй боковой аквариум оставался открытым, в него ничего
не помещали, и поэтому он служил в качестве контроля.
При проведении экспериментов канал центрального аквариума (Рис. 1B, 1C) перекрывали
пластиковой перегородкой, установку заполняли фильтрованной морской водой с температу-
рой 18-20 ºС. В правый микроаквариум помещали источник химического сигнала (несколько
капель «кондиционированной» воды, крови или лимфы либо кусочек ткани второго промежу-
точного хозяина) и выдерживали в течение 5 мин. За это время в правом канале создавался гра-
диент сигнала. Затем в центральный микроаквариум выпускали 10 экз. исследуемых церкарий,
аккуратно удаляли пластиковую перегородку, соединяющую его с каналом, и через 10 мин.
Рисунок 1. Микроаквариумы для исследования контактных (A) и дистантных (B, C)
хемореакций церкарий (пояснения в тексте).
345
подсчитывали число личинок в правом и левом каналах. Опыты повторяли 5 раз для всех ис-
следуемых церкарий.
При статистической обработке результатов экспериментов достоверность различий оценива-
ли при помощи медианного теста (m-test) для исходных данных и при помощи однофакторного
дисперсионного анализа (One-way ANOVA) для данных, трансформированных методом Бокса-
Кокса (Box-Cox transformed data).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты проведенных наблюдений и последующей их статистической обработ-
ки показали, что исследованные церкарии в той или иной степени реагируют на ме-
таболиты заражаемых животных. При этом контактные реакции отчетливо проявля-
лись лишь при использовании «кондиционированных» агаровых блоков. Церкарии
Н. elongata достоверно (m-test, Р < 0.01) реагировали на метаболиты мидии. Личинки
С. lingua демонстрировали выраженную реакцию только при контакте с метаболитами
трески (ANOVA, Р < 0.05), в то время как на метаболиты колюшки и маслюка досто-
верной реакции обнаружить не удалось (ANOVA, Р = 0.06).
Кроме контактной реакции личинки Н. elongata демонстрировали и отчетливую дис-
тантную хемореакцию на метаболиты мидии (ANOVA, Р < 0.01). Подобная реакция
у церкарий С. lingua выражена на слизь трески, маслюка (ANOVA, Р < 0.01), но не на
слизь колюшки (ANOVA, Р = 0.36).
Выявить заметную реакцию исследуемых церкарий на мембранные модели не уда-
лось. По-видимому, это связано с очень низкой концентрацией метаболитов иссле-
дуемых животных на поверхности мембран. Использование «кондиционированной»
воды, пропущенной через диализные фильтры, также не дало результатов. Возможно
личинки реагируют на вещества с молекулярной массой более 20 кДа либо концентра-
ция веществ, проходящих через поры фильтра, слишком мала, чтобы исследуемые цер-
карии смогли их распознать. Последнее представляется более вероятным, поскольку
изученные к настоящему времени хемочувствительные церкарии при поиске хозяина
реагируют на низкомолекулярные соединения (Haas, 2003). Так, церкарии Diplostomum
spathaceum (Rudolphi, 1819) демонстрировали продолжительный контакт с агарозой,
пропитанной гидрофильными экстрактами кожи рыбы массой менее 3 кДа (Haas et at.,
2002).
Полученные результаты позволяют заключить, что наиболее подходящими из числа
описанных методами исследования хемочувствительносги церкарий морских трема-
тод оказались: для контактных реакций - применение агаровых моделей, пропитанных
метаболитами хозяев, а для дистантных - микроаквариумов с узкими каналами, в ко-
торых создается градиент сигнала. Эти методы показали достаточно высокую эффек-
тивность и могут быть рекомендованы как основные для исследования хемореакций
церкарий, что не исключает необходимость проводить поиск и отработку других мето-
дических подходов к изучению этой черты поведения личинок трематод.
БЛАГОДАРНОСТИ
Работа выполнена в рамках проекта РНФ № 18-14-00170.
346
СПИСОК ЛИТЕРАТУРЫ
Chaisson К.Е., Hallem Е.А. 2012. Chemosensory behaviors of parasites. Trends in Parasitology 28 (10): 427-436.
Combes C. 2001. Parasitism, the ecology and evolution of intimate interactions. The University of Chicago Press,
Chicago and London, 728 p.
Fried U., King W. 1989. Attraction of Echinostoma revolulum cercariae to Biomphalaria glabrata dialysate. Journal
of Parasitology 75: 55-57.
Haas W. 2003. Parasitic worms: strategies of host finding, recognition and invasion. Zoology 106: 349-364.
Haas W., Korner M., Hutterer E., Wegner M., Haberl B. 1995. Finding and recognition of the snails intermediate host
3 species of echinostome cercariae. Parasitology 110: 133-142.
Haas W., Stiegeler P., Keating A., Kullmann В., Rabenau H., Schonamsgruber E., Haberl B. 2002. Diplostomum
spathaceum cercariae respond to a unique profile of cues during recognition of their fish host. International
Journal for Parasitology 32: 1145-1154.
Haberl, В., Korner M., Spengler Y„ Hertel J., Kalbe M., Haas W. 2000. Host-finding in Echinostoma caproni:
miracidia and cercariae use different signals to identify the same snail species. Parasitology 120: 479-486.
Korner M., Haas W. 1998a. Chemo-orientation of echinostome cercariae towards their snail hosts: amino acids
signal a low host-specificity. International Journal for Parasitology 28: 511-516.
Korner M., Haas W. 1998b. Chemo-orientation of echinostome cercariae towards their snail hosts: the stimulating
structure of amino acids and other attractants. International Journal for Parasitology 28: 517-525.
METHODS EFFECTIVE IN THE STUDY
OF CHEMO-ORIENTATION BEHAVIOR IN TREMATODE CERCARIAE
V. V. Prokofiev
Keywords: trematodes, cercariae, chemo-orientation, methods
SUMMARY
The most appropriate methods for experimental study of cercarial response to host chemical signals
were tested. The use of agar blocks impregnated with the second intermediate host metabolites was
found to be the most effective for the study of contact responses, and the use of experimental chambers
with narrow channels with gradient of chemicals, for the study of distant responses.
347