Письма в ЖЭТФ, том 118, вып. 9, с. 683 - 688
© 2023 г. 10 ноября
Первопринципные исследования адсорбции Li и Na на поверхности
монослоя MgCl2
+∗1)
С. В. Устюжанина+, А. А. Кистанов
+Институт проблем сверхпластичности металлов РАН, 450001 Уфа, Россия
∗Лаборатория Металлы и сплавы при экстремальных воздействиях,
Уфимский университет науки и технологий, 450076 Уфа, Россия
Поступила в редакцию 14 августа 2023 г.
После переработки 4 октября 2023 г.
Принята к публикации 5 октября 2023 г.
C использованием первопринципных расчетов исследована динамическая устойчивость нового моно-
слоя дихлорида магния (MgCl2) и образование в нем точечных дефектов. Изучена возможность исполь-
зования монослоя MgCl2 в литий(Li)- и натрий(Na)-ионных батареях. Показано, что монослой MgCl2
обладает динамической стабильностью, но может содержать точечные дефекты. Эти точечные дефекты
могут улучшить адсорбционную способность монослоя MgCl2 по отношению к атомам Li и Na. Резуль-
таты, показанные в этой работе, делают монослой MgCl2 перспективным материалом для применения
в Li- и Na-ионных батареях.
DOI: 10.31857/S1234567823210097, EDN: ptdeba
Введение. Недавно была предсказана и исследо-
Однако, насколько известно, нет исследований по
вана новая группа двумерных (2Д) материалов, дву-
возможному применению монослоя MgCl2 в качестве
мерных дихлоридов переходных металлов [1]. Кро-
материала для применения в Li- и Na-ионных бата-
ме того, повышенное внимание уделяется другим 2Д
реях. Кроме того, недостаточно изучено влияние об-
хлоридам металлов, таким как 2Д MgCl2, в связи с
разования типичных точечных дефектов в монослое
их исключительными оптоэлектронными и магнит-
MgCl2 на его адсорбционную способность по отноше-
ными свойствами [2, 3]. К примеру, в работе [4] было
нию к атомам Li и Na. Поэтому в данной работе вли-
показано, что монослой обладает шириной запрещен-
яние типичных точечных дефектов и возможность
ной зоны, равной 6.08 эВ.
применения монослоя MgCl2 в Li- и Na-ионных ба-
В настоящее время также растет спрос на Li- и
тареях исследуется с помощью теории функционала
Na-ионные аккумуляторы для различных примене-
плотности с использованием первопринципных рас-
ний, в том числе для электромобилей, возобновля-
четов.
емых источников энергии и систем хранения энер-
Вычислительные методы. Структура моно-
гии [5, 6]. В последнее время интерес исследовате-
слоя MgCl2 была спроектирована на основе гео-
лей направлен на новый класс хлоридов лития из-
метрии примитивной элементарной ячейки монослоя
за их очень высокой окислительной стабильности
MgCl2, имеющейся в базе данных 2DMatPedia (ID
[7]. Различные хлориды переходных металлов, такие
2dm-3734) [11], и найденных ранее 2Д дихлоридов
как NiCl2 и KNiCl3, были протестированы в каче-
переходных металлов [1], а также эксперименталь-
стве материалов катода в Li- и Na-ионных батаре-
ных данных [12] по монослою MgCl2. Расчеты про-
ях и показали многообещающие результаты благода-
водились методом плоских волн, реализованным в
ря их сравнительно высокой емкости и напряжению
пакете Vienna Ab initio Simulation Package [13]. Рас-
[8, 9]. Кроме того, мезопористый углерод, наполнен-
четы по оптимизации геометрии были выполнены с
ный CuCl2, был предложен в качестве катодного ма-
использованием обменно-корреляционного функци-
териала для литий-ионных аккумуляторов с высокой
онала Пердью-Берка-Эрнзергофа (PBE) в прибли-
емкостью из-за его обратимой реакции переноса двух
жении обобщенного градиента (GGA) [14]. Оптими-
электронов, обеспечивающей очень высокую обрати-
зация была остановлена, как только все компонен-
мую емкость [10].
ты всех атомных сил стали меньше 10-4 эВ/Å, а из-
менение полной энергии было меньше 10-8 эВ. Пер-
1)e-mail andrei.kistanov.ufa@gmail.com
вая зона Бриллюэна была отобрана с сеткой k-точек
Письма в ЖЭТФ том 118 вып. 9 - 10
2023
683
684
С.В.Устюжанина, А.А.Кистанов
10 × 10 × 1 для элементарной ячейки и сеткой k-
точек 3 × 3 × 1 для суперячейки. Энергия обрезки
потенциала была выбрана равной 520 эВ. Периоди-
ческие граничные условия применялись вдоль попе-
речных направлений в плоскости, а вакуумное про-
странство 20Å вводилось в направлении, перпенди-
кулярном плоскости поверхности. Для построения
фононного спектра, расчеты, основанные на теории
возмущений функционала плотности (DFPT), с по-
мощью программного пакета Phonopy [15], были вы-
полнены для суперячейки монослоя MgCl2 размером
3×3×1 с использованием сетки k-точек 2×2×1. По-
правка DFT-D3 [16] использовалась для учета Ван-
дер-Ваальсовых взаимодействий между атомами Li
и Na и поверхностью монослоя MgCl2. Для исследо-
вания моно вакансионных (МВ) дефектов и энергии
адсорбции рассматривалась супер ячейка MgCl2 раз-
мером 4 × 4 × 1 элементарных ячеек.
Энергия образования Eform МВ дефектов в моно-
слое MgCl2 рассчитывалась следующим образом:
Eform = Eperfect - Edefect - NMgEMg - NClECl,
(1)
где Eperfect и Edefect - полные энергии чистого и со-
держащего МВ монослоя MgCl2, EMg и ECl - энер-
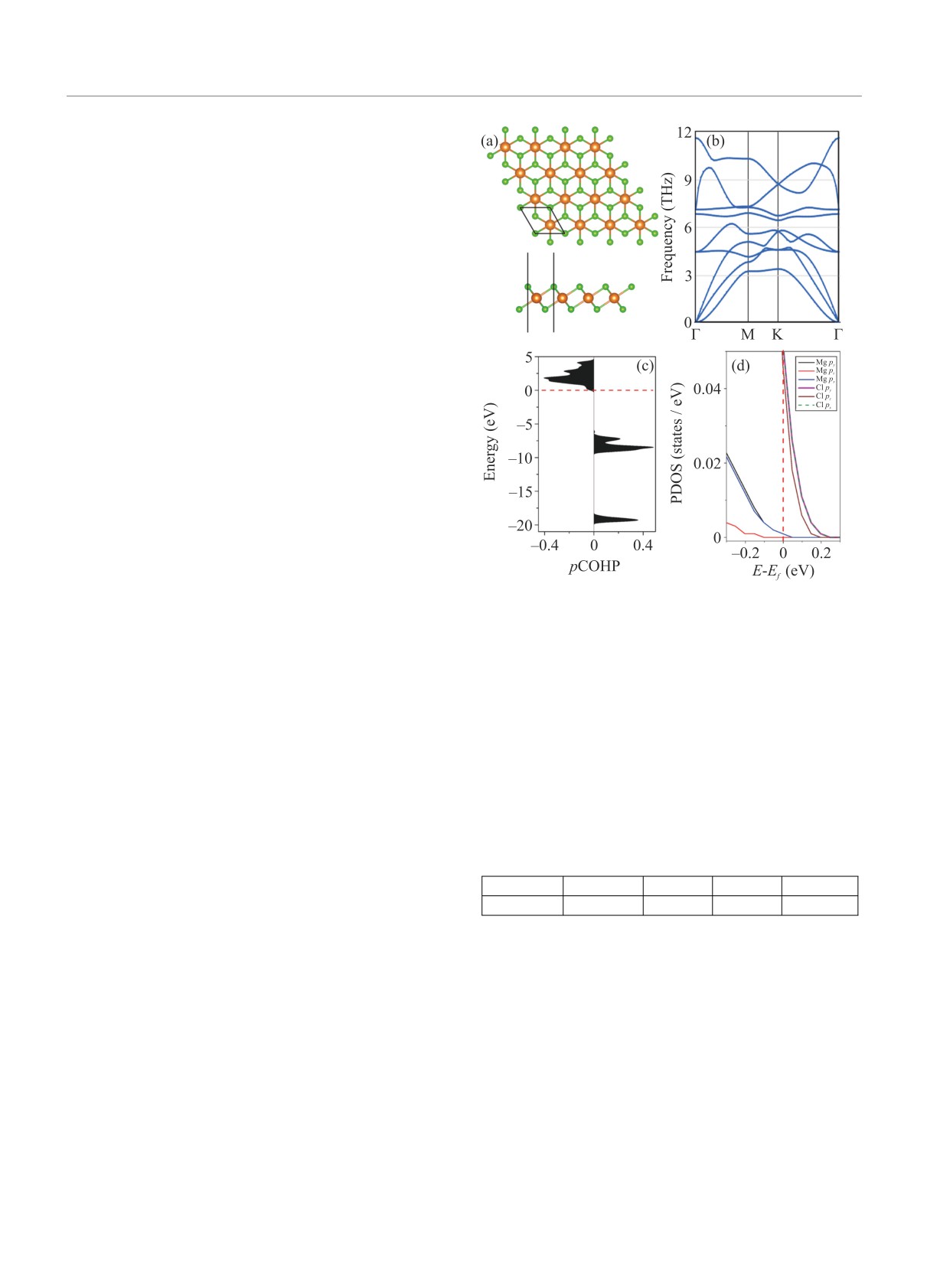
Рис. 1. (Цветной онлайн) Структура элементарной
гии атомов Mg и Cl, соответственно, рассчитанные
ячейки (а), фононный спектр (b), pCOHP (c) и PDOS
из объемных фаз материалов.
(d), где уровень Ферми показан красной пунктирной
Энергия адсорбции атомов Li и Na на поверхно-
линией, для монослоя MgCl2
сти монослоя MgCl2 рассчитывалась следующим об-
разом:
дисперсионные кривые монослоя MgCl2 положитель-
Ea = EMgCl2/mol - EMgCl2 - Eatom,
(2)
ны во всей зоне Бриллюэна, что свидетельствует о
. Стоит
динамической устойчивости монослоя MgCl2
где EMgCl2/mol - полная энергия монослоя MgCl2,
отметить, что ранее, в работе [21], уже был расчитан
адсорбированного Li(Na), EMgCl2 и Eatom - полные
фононный спектр монослоя MgCl2, наши результаты
энергии исходного монослоя MgCl2 и свободного ато-
показывают высокую сходимость с ранее представ-
ма Li(Na), соответственно.
ленными.
Заселенность кристаллических орбиталей Га-
мильтона (Crystal Orbital Hamilton Populations -
Таблица 1. Структурные параметры монослоя MgCl2
COHP) [17] рассчитывалась с помощью программы
a,Å
b,Å
α
β
γ
LOBSTER [18].
3.64
3.64
90
90
120
Результаты и обсуждения. На рисунке 1а по-
казана структура элементарной ячейки монослоя
MgCl2. Он принадлежит к тригональной простран-
В 2Д материалах обычно присутствуют различ-
ственной группе симметрии 164 P-3m1 и состоит из
ные точечные дефекты, которые самопроизвольно
одного атома Mg и двух атомов Cl. Оптимизирован-
образуются в процессе их изготовления и эксплуата-
ные структурные параметры монослоя MgCl2 собра-
ции [22-24]. Поэтому здесь рассматривается устойчи-
ны в табл. 1. Полученные данные по расчету пара-
вость и образование точечных дефектов в монослое
метров решетки монослоя MgCl2 a = b = 3.64Å
MgCl2, в частности, МВ дефектов. В данной работе
аналогичны ранее представленным результатам [19]
рассматриваются следующие дефекты: МВ атома Cl
и соотносятся с экспериментальными данными [20].
(МВСl) и МВ атома Mg (МВМg). Термическая устой-
Для подтверждения динамической стабильности мо-
чивость этих МВ-дефектов в монослое MgCl2 оцени-
нослоя MgCl2 рассчитан его фононный спектр, ко-
вается по энергии их образования Eform. Установле-
торый показан на рис.1b. Видно, что все фононные
но, что дефект МВСl имеет низкую Eform = 5.86 эВ,
Письма в ЖЭТФ том 118 вып. 9 - 10
2023
Первопринципные исследования адсорбции Li и Na...
685
Рис. 2. (Цветной онлайн) Три наиболее энергетически выгодные конфигурации атомов Li и Na на поверхности моно-
слоя MgCl2 , положение атомов Li и Na показано, как P1, P2 и P3
в то время как дефект МВМg имеет гораздо более
лее энергетически выгодные конфигурации (P1-P3)
высокую Eform = 7.90 эВ, что сравнимо с Eform МВ
атомов Li и Na на поверхности монослоя MgCl2 из
в графене (7.50 эВ) [25] и МВ дефектами в хлоридах
всех рассмотренных в данной работе. Из рисунка 2
металлов (до 7.37 эВ) [1]. Кроме того, прочность свя-
следует, что Ea Li и Na на поверхности монослоя
зи в материале можно приблизительно оценить при
MgCl2 для конфигурации Р3 (рис. 2c) значительно
помощи COHP анализа [26, 27]. Зная площадь под
ниже таковой для случаеа Р1 (рис. 2а) и Р2 (рис. 2b),
кривой pCOHP, можно дать оценку энергии связи
на ∼ 0.1 эВ в случае Li и на ∼ 0.2 эВ в случае Na. Кро-
в материале. pCOHP и для монослоя MgCl2 пред-
ме того, обнаружено, что полная энергия систем Li-
ставлен на рис. 1c. Из рисунке 1c также видно, что
MgCl2 и Na-MgCl2, представленных на рис. 2c (кон-
состояния в интервале энергий от -0.2 эВ до 4.7 эВ
фигурация P3), ниже таковой для систем Li-MgCl2
являются разрыхляющими и не дают вклад в хими-
и Na-MgCl2, представленных на рис. 2а, b. Далее, в
ческую связь Mg с Cl. Согласно рис. 1d, где пред-
работе рассматривался только случай для наиболее
ставлена диаграмма парционной плотности состоя-
энергетически выгодной конфигурации Li и Na на
ний (PDOS) монослоя MgCl2, данными разрыхляю-
поверхности монослоя MgCl2, т.е. конфигурация P3
щими орбиталями являются 2p-орбитали Cl и 2px- и
(рис. 2c). Далее, на рис. 3а показана данная энерге-
2py-орбитали Mg. Полученное значение площади под
тически выгодная конфигурация атома Li, адсорби-
кривой pCOHP (-IpCOHP), иными словами энер-
рованного на поверхности монослоя MgCl2. Атом Li
гия связи Cl-Mg, составляет ∼ 0.84 эВ. Таким обра-
расположен над атомом Mg на расстоянии 0.15Å от
зом, для удаления одного атома хлора с образовани-
поверхности. Видно, что адсорбированный атом Li
ем МВСl, требующее разрыва трех связей с ближай-
смещает атом Mg из положения равновесия. Расчет-
шими атомами Mg, потребуется ∼ 2.52 эВ, что суще-
ная энергия адсорбции Ea одного атома Li на поверх-
ственно ниже энергии формирования МВСl, получен-
ности монослоя MgCl2 оказалась равной -0.37 эВ
ной согласно формулы (1). Стоит отметить, что дан-
(см. табл. 2). Учитывая обнаруженную сравнительно
ные по расчетам Eform МВ и COHP анализа дают ре-
низкую энергию образования МВ дефектов в моно-
зультаты, отличающиеся более чем в 2 раза. Необхо-
слое MgCl2 и наблюдаемое смещение атома Mg, ак-
димо подчеркнуть тот факт, что химический потен-
тивированное адсорбцией Li, важно учитывать вза-
циал атомов Mg и Cl в объемной фазе отличается от
имодействие Li с поверхностью монослоя MgCl2, со-
такового в их соединении [28], что может приводить к
держащей МВ дефект. На рисунке 3b показана кон-
меньшей точности в оценке результатов, полученных
фигурация атома Li, адсорбированного на монослое
для энергии формирования МВCl. Тем не менее, оба
MgCl2, содержащем МВСl, при расположении Li на
метода подтверждают низкую энергию формирова-
дефекте МВСl. В этом случае атом Li находится в
ния моновакансий в монослое MgCl2, относительно
шестиугольнике на расстоянии 0.97Å, при этом зна-
других 2Д материалов, таких как графен.
чение Ea составляет -1.94 эВ (см. табл. 2). На ри-
Были рассмотрены различные атомные конфи-
сунке 3c показана адсорбция атома Li на монослое
гурации атомов Li и Na на поверхности монослоя
MgCl2, содержащем МВМg дефект. После оптими-
MgCl2. В частности, рассмотрены позиции атомов
зации геометрии структуры атом Li занимает сво-
Li и Na - над атомом Cl первого слоя, над атомом
бодное место на МВМg. В этом случае значение Ea
Mg второго слоя, над атомом Cl третьего слоя, над
составляет -6.67 эВ (см. табл.2), что свидетельству-
центром связи Cl-Mg и над центром шестичленно-
ет об экзотермическом и самопроизвольном процессе
го кольца. На рисунке 2 представлены три наибо-
адсорбции атома Li на монослое MgCl2, содержащем
Письма в ЖЭТФ том 118 вып. 9 - 10
2023
686
С.В.Устюжанина, А.А.Кистанов
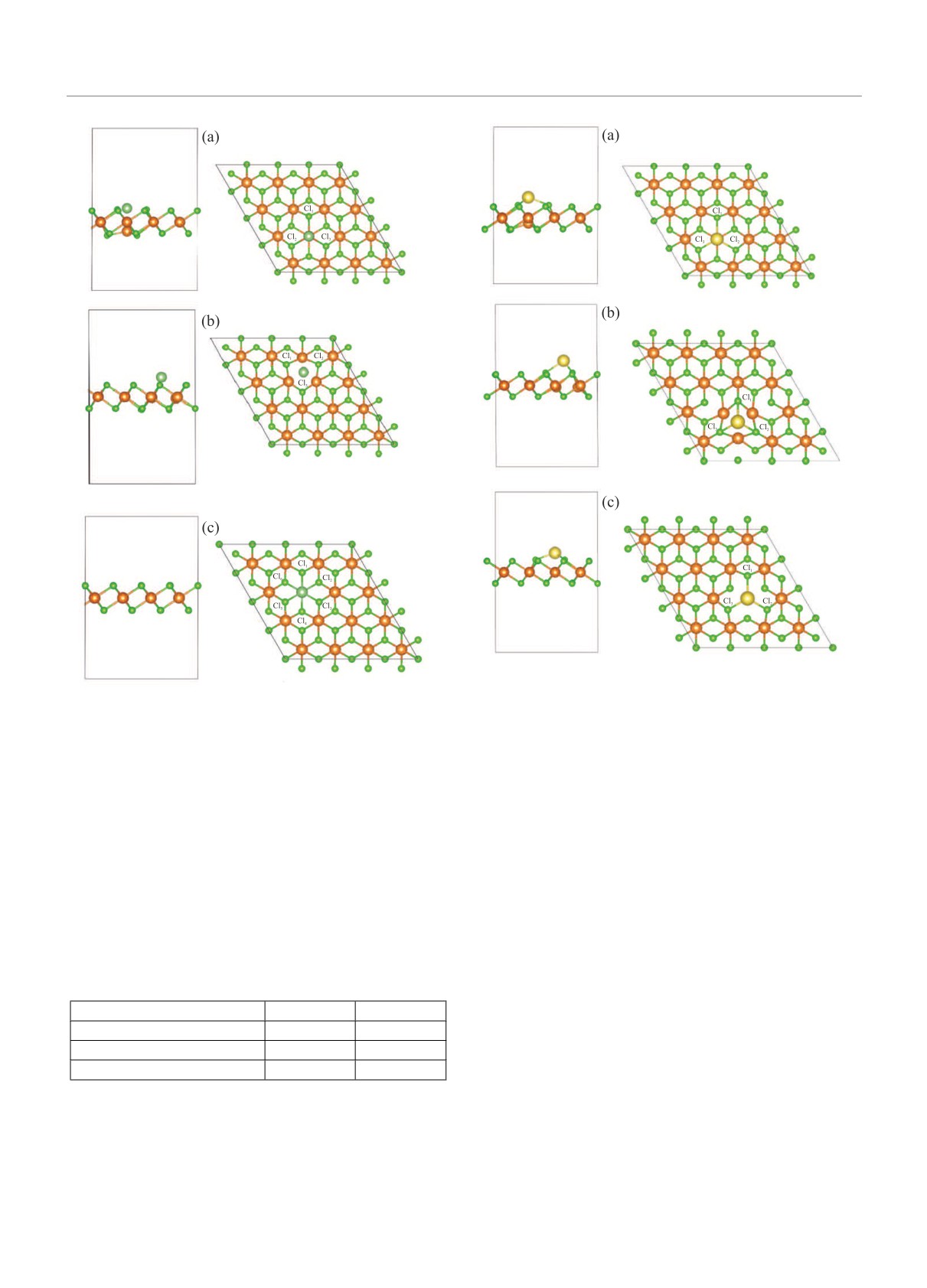
Рис. 4. (Цветной онлайн) Чистый (а), содержащий
МВСl (b) и содержащий МВMg (c) монослой MgCl2 с
Рис. 3. (Цветной онлайн) Чистый (а), содержащий
адсорбированным атомом Na
МВСl (b) и содержащий МВMg (c) монослой MgCl2 с
адсорбиров анным атомом Li
Mg на расстоянии 1.15Å от поверхности. Видно, что
МВМg. Как известно, тепловое самовозгорание ма-
адсорбированный атом Na смещает атом Mg из по-
териалов может ускоряться биохимическим или ад-
ложения равновесия, как это было в случае с атомом
сорбционным самонагревом [29], ввиду чего суще-
Li. Расчетная энергия адсорбции Ea одного атома Na
ствует опасность самовозгарания устройств, таких
на поверхности монослоя MgCl2 равна -0.38 эВ (см.
как Li- и Na-ионные батареи. Таким образом, Li- и
табл. 2). На рисунке 4b показана конфигурация ато-
Na-ионные батареи на основе монослоя MgCl2, ввиду
ма Na, адсорбированного на монослое MgCl2, содер-
больших отрицательных энергиях абсорбции атомов
жащем МВСl, когда атом Na находится на дефекте
Li и Na на его поверхности, могут быть подвержены
МВСl. В этом случае атом Na находится в шести-
данному эффекту.
угольнике на расстоянии 1.42Å от поверхности мо-
носля MgCl2, при этом значение Ea равно -1.59 эВ
Таблица 2. Энергия адсорбции Li и Na на монослое MgCl2
(см. табл. 2). На рисунке 4c показана адсорбция ато-
Li
Na
ма Na на монослое MgCl2, содержащем СВМg. После
Монослой MgCl2
-0.37 эВ
-0.38 эВ
оптимизации геометрии структуры атом Na занима-
Монослой MgCl2 с МВСl
-1.94 эВ
-1.59 эВ
ет свободное место на МВМg. В этом случае значение
Монослой MgCl2 с МВMg
-6.67 эВ
-5.68 эВ
Ea составляет всего -5.68 эВ (см. табл.2), что свиде-
тельствует об экзотермическом и самопроизвольном
На рисунке 4а показана наиболее энергетически
процессе адсорбции атома Na на монослое MgCl2, со-
выгодная конфигурация атома Na на поверхности
держащем МВМg.
монослоя MgCl2. Атом Na расположен над атомом
Стоит отметить, что Ea атома Na на монослое
Письма в ЖЭТФ том 118 вып. 9 - 10
2023
Первопринципные исследования адсорбции Li и Na...
687
Таблица 3. Величина переноса заряда Δq и донорно-акцепторные характеристики атомов Li и Na, а также соседних атомов Cl.
Положительное/отрицательное Δq характеризует потерю/приобретение электронов. Нумерация атомов согласно рис. 3 и 4
Δq [e]
Δq [e]
Δq [e]
Δq [e]
Δq [e]
Δq [e]
Δq [e]
Li/Na
Cl1
Cl2
Cl3
Cl4
Cl5
Cl6
Li на MgCl2
1
-0.032
-0.034
-0.034
(донор)
(акцептор)
(акцептор)
(акцептор)
Li MgCl2 с МВCl
1
-0.063
-0.064
-0.067
(донор)
(акцептор)
(акцептор)
(акцептор)
Li MgCl2 с МВMg
1
0.112
0.111
0.113
0.112
0.110
0.11
(донор)
(донор)
(донор)
(донор)
(донор)
(донор)
(донор)
Na на MgCl2
0.867
-0.005
-0.005
-0.007
(донор)
(акцептор)
(акцептор)
(акцептор)
Na MgCl2 с МВCl
0.907
-0.038
-0.036
-0.036
(донор)
(акцептор)
(акцептор)
(акцептор)
Na MgCl2 с МВMg
0.890
0.059
0.060
0.060
(донор)
(донор)
(донор)
(донор)
MgCl2, содержащем МВCl и МВМg несколько выше
нонный спектр монослоя MgCl2 показал его струк-
таковой для атома Li. Для объяснения полученных
турную стабильность, что важно для его приме-
результатов проведен анализ зарядового распределе-
нения. Показано также, что монослой MgCl2 мо-
ния на атомах кристаллической решетки при помо-
жет содержать МВ дефекты из-за сравнительно низ-
щи анализа Бадера [30] с использованием кода Хен-
кой энергии образования в нем этих дефектов. Во-
кельмана [31]. Представленные в табл. 3 результаты
вторых, показано, что энергия адсорбции Ea ато-
данного анализа показывают, что Li и Na являют-
ма Li и атома Na на поверхности монослоя MgCl2
ся сильными донорами во всех рассмотренных слу-
сравнительно велики, -0.37 эВ и -0.38 эВ, соответ-
чаях, в то время как ближайшие к атомам Li и Na
ственно, а наличие МВ-дефектов на поверхности мо-
атомы Cl меняют свою роль с акцепторной (в слу-
нослоя MgCl2 приводит к значительному уменьше-
чае адсорбции атомов Li и Na на монослое MgCl2,
нию энергии адсорбции Ea до -6.67 эВ (для Li) и до
содержащем МВCl) на донорную (в случае адсорб-
-5.68 эВ (для Na). Следовательно, монослой MgCl2
ции атомов Li и Na на монослое MgCl2, содержащем
может быть универсальным кандидатом для приме-
МВМg). Наибольшее различие в Ea Li и Na наблюда-
нения в качестве анодного материала, применяемых
ется для монослоя MgCl2, содержащего МВМg. При
в Li- и Na-ионных батареях.
этом значительный вклад в адсорбцию Li и Na вно-
Для А. А. Кистанова исследование выполне-
сят близлежашие к ним атомы Cl. Согласно табл. 3,
но за счет гранта Российского научного фонда
атомы Cl являются достаточно слабыми донорами
(Δq
= 0.060e) в случае адсорбции атома Na, в то
время как при адсорбции атома Li атомы Cl явля-
Исследования проводились на оборудовании кол-
ются сильными донорами (Δq= -0.112e). При этом
лективной исследовательской базы объединенного
атом Li занимает вакантную позицию Mg и имеет
суперкомпьютерного центра Российской академии
6 ближайших соседних атомов Cl, в то время как
наук.
атом Na остается на поверхности монослоя MgCl2 и
имеет только 3 ближайших соседних атомов Cl. Та-
ким образом, перенос заряда от атомов Li(Na) к по-
1. A. A. Kistanov, S. A. Shcherbinin, R. Botella,
верхности монослоя MgCl2 через ближайшие атомы
A. Davletshin, and W. Cao, J. Phys. Chem. Lett.
Cl, а также роль этих атомов Cl в каждом конкрет-
13, 2165 (2022);
ном случае имеют решающее значение при адсорб-
ции атомов Li и Na на монослое MgCl2.
2. I. T. Lima, R. Vasconcelos, R. Gargano, and
Выводы. В заключение, в данной работе при
E. N. C. Paurad, New J. Chem.
44,
8833
(2020);
помощи первопринципных расчетов были проведе-
ны исследования недавно обнаруженного монослоя
3. G. Bhattacharyya, I. Choudhuri, P. Bhauriyal,
MgCl2 для его возможного применения в Li- и Na-
P. Garg, and B. Pathak, Nanoscale 10, 22280 (2018);
ионных батареях. Во-первых, смоделированный фо-
Письма в ЖЭТФ том 118 вып. 9 - 10
2023
688
С.В.Устюжанина, А.А.Кистанов
4.
F. Lu, W. Wang, X. Luo, X. Xie, Y. Cheng, H. Dong,
18.
R. Nelson, C. Ertural, J. George, V.L. Deringer,
H. Liu, and W.-H. Wang, Appl. Phys. Lett. 108, 132104
G. Hautier, and R. Dronskowski, J. Comput Chem.
5.
W. Mrozik, M. A. Rajaeifar, O. Heidrich, and
19.
G. Bhattacharyya, I. Choudhuri, P. Bhauriyal,
P. Christensen, Energy Environ. Sci. 14, 6099 (2021);
P. Garg and B. Pathak, Nanoscale 10, 22280 (2018);
6.
A.A. Kistanov, D. R. Kripalani, Y. Cai, S. V. Dmitriev,
20.
J.
Zhu and U. Schwingenschlogl,
ACS
K. Zhou, and Y.-W. Zhang, J. Mater. Chem. A 7, 2901
Appl. Mater. Interfaces
6,
11675
(2014);
7.
I. Kochetkov, T. T. Zuo, R. Ruess, B. Singh, L. Zhou,
21.
H. R.
Mahida,
A.
Patel,
D.
Singh,
K. Kaup, J. Janek, and L. Nazar, Energy Environ. Sci.
Y. Sonvane, P. B. Thakor, and R.
Ahuja,
Superlattices Microstruct.
162,
107132
(2022);
8.
K. Giagloglou,
J. L.
Payne, Ch. Crouch,
R.K. B. Gover, P. A. Connor, and J. T. S. Irvinl,
22.
H.-P. Komsa and A. V. Krasheninnikov, Physics
J.
Electrochem. Soc.
165, A3510
(2018);
and theory of defects in
2D materials: the role
of reduced dimensionality, Amsterdam
(2022), p. 7;
9.
Y. Li, L. Shi, X. Gao, J. Wang, Y. Hu, X. Wu,
and Z. Wen, Chem. Eng. J.
421,
127853
(2021);
23.
S. Abdolhosseinzadeh, Ch. Zhang, R. Schneider,
M.
Shakoorioskooie,
F.
Nüesch,
and
10.
T. Li, Z. X. Chen, Y. L. Cao, X. P. Ai, and
J. Heier, Adv. Mater.
34,
2103660
(2022);
H.X. Yang, Electrochim. Acta
68,
202
(2012);
24.
A. A. Kistanov, V. R. Nikitenko, and O. V. Prezhdo,
11.
J. Zhou, L. Shen, M. D. Costa, K. A. Persson,
J.
Phys. Chem. Lett.
12,
620
(2021);
S. P. Ong, P. Huck, Y. Lu, X. Ma, Y. Chen,
H. Tang, and Y. P. Feng, Sci. Data 6,
86
(2019);
25.
A. V. Krasheninnikov, P. O. Lehtinen, A. S. Foster, and
R. M. Nieminen, Chem. Phys. Lett. 418, 132 (2006);
12.
D. H. Fairbrother, J. G. Roberts, and G. A. Somorjai,
Surf. Sci. 399(1), 109 (1998);
26.
X. Yu, H. Shao, X. Wang, Y. Zhu, D. Fang,
and J. Hong, J. Mater. Chem. A 8,
3128
(2020);
13.
G. Kresse, and J. Furthmuller, Phys. Rev. B 54, 11169
27.
Л. С. Чумакова, А.В. Бакулин, С. Е. Куль-
14.
J. P. Perdew, K. Burke, and M. Ernzerhof,
кова,
ЖЭТФ
161(6),
874
(2022);
Phys.
Rev.
Lett.
77,
3865
(1996).
28.
А. В. Бакулин, С. Е. Кулькова, ЖЭТФ 6(12), 1136
15.
A. Togo, L. Chaput, T. Tadano, and I. Tanaka,
J. Phys. Condens. Matter
35,
353001
(2023);
29.
А. С. Харламенков, Пожаровзрывобезопасность/Fire
and Explosion Safety. 31(3), 96 (2022).
16.
S.
Grimme, J. Antony, S. Ehrlich, and
H. Krieg, J. Chem. Phys.
132,
154104
(2010);
30.
R. F. W. Bader, Atoms in Molecules. A Quantum
Theory, Clarendon Press, Oxford, UK (1990).
17.
V.L. Deringer, A. L. Tchougreeff, and R. Dronskowski,
31.
W. Tang, E. Sanville, and G. Henkelman,
J.
Phys. Chem. A
115(21),
5461
(2011);
J. Phys.: Condens. Matter.
21,
084204
(2009);
Письма в ЖЭТФ том 118 вып. 9 - 10
2023