ВВЕДЕНИЕ
Почвенное органическое вещество (ПОВ) представляет собой резервуар углерода, азота и других питательных элементов для растений, поддерживая агроэкологические функции почвы [17, 31]. Потеря органического углерода (Сорг) при сельскохозяйственном использовании земель оказывает негативное влияние на физические, химические и биологические свойства почв и является одним из наиболее серьезных факторов, ведущих к их деградации [25, 57, 61]. Доступным способом одновременного восстановления запасов ПОВ и депонирования секвестрированного углерода является внесение растительных остатков в почву [14, 15, 21, 25, 40, 42]. Наиболее распространенным и доступным для использования типом растительных остатков является солома [26, 55, 59, 61], внесение которой обеспечивает повторное вовлечение в биогеохимический круговорот до 50% азота, фосфора и калия и поступление нескольких тонн на гектар органического вещества [14, 25, 37, 41]. Кроме того, в связи с экономическим развитием солома сельскохозяйственных культур превратилась из ценного сырья и корма для скота в органические отходы, требующие утилизации [37, 42]. Практикуемое сжигание соломы недопустимо с природоохранных позиций. Таким образом, заделывание соломы в почву позволяет решить одновременно три задачи: компенсировать потери ПОВ, утилизировать растениеводческие отходы и повысить плодородие почвы [25, 40].
Почва является олиготрофной средой, в которой подавляющая часть микроорганизмов обитает в условиях дефицита субстрата [28, 47]. Послеуборочные растительные остатки зерновых и зернобобовых культур характеризуются повышенным содержанием целлюлозы, гемицеллюлозы и лигнина, являясь энергетическим субстратом для гетеротрофных микроорганизмов [16, 41]. При внесении растительных остатков в почву происходит увеличение эмиссии СО2 и биомассы почвенных микроорганизмов [4, 59, 61, 63]. Таким образом, заделка соломы, как агротехнологический прием биологизации земледелия, активизирует почвенную микробиоту [47], что, с одной стороны, повышает микробный пул ПОВ, но, с другой стороны, может активизировать прайминг-эффект дополнительной минерализации Сорг [25, 55, 61].
Внесение растительных остатков является важным приемом почвенной секвестрации углерода, составляя в среднем 168 ± 67 кг С/(га год) [52]. Сохранность секвестрируемого с растительными остатками органического вещества во многом определяется численностью и структурой почвенного микробного сообщества, в том числе соотношением грибы/бактерии [10, 24, 43, 49, 50]. Преобладание микобиоты и высокие значения отношения грибы/бактерии обычно выявляют в почвах с повышенной секвестрирующей способностью и более низкими значениями C/N [43, 49, 50, 55]. Уменьшение отношения грибы/бактерии указывает на снижение секвестрирующей способности почв [34, 43].
Применение минеральных удобрений является обязательным условием получения высоких урожаев [31, 36], но их внесение, чаще всего, негативно отражается на микробиологических показателях почвы [22, 30, 31, 35]. Обнаружено уменьшение таксономического разнообразия прокариот и грибов в почве и ризосфере удобренных сельскохозяйственных растений [20, 30, 46, 48, 62]. Можно предположить, что совместное внесение минеральных удобрений и соломы будет не только устранять негативные эффекты, но и оптимизировать численность и структуру почвенных микроорганизмов.
Цель работы – оценка влияния свежего органического вещества соломы на численность клеток и копий рибосомальных генов, а также величину и структуру биомассы различных групп микроорганизмов в дерново-подзолистой почве в условиях длительного полевого эксперимента.
ОБЪЕКТЫ И МЕТОДЫ
Почва. Исследования проводили с образцами агродерново-подзолистой супесчаной почвы (Umbric Retisol), отобранными в многолетнем полевом опыте, заложенном в 1997 г. на опытном поле Всероссийского научно-исследовательского института органических удобрений и торфа (ВНИИОУ) – филиале ФГБНУ “Верхневолжский ФАНЦ” в Судогодском районе Владимирской области (56°3′16″ N, 40°29′28″ E), в пятипольном зернопропашном севообороте: озимая пшеница, люпин (на зерно), картофель, ячмень, однолетние травы (люпин + овес). Условия проведения длительных опытов ВНИИОУ подробно описаны в работе [7]. Климат территории умеренно континентальный с теплым летом (средняя температура июля +18°C) и умеренно холодной зимой (средняя температура января −12°C). Среднегодовое количество осадков составляет от 500 до 550 мм.
Для проведения данного исследования выбрали следующие варианты опыта: контроль без удобрений (V1 и V5); N54P51K57 (среднегодовая доза) (V2 и V6); N54P51K57 + солома озимой пшеницы, люпина, ячменя по 3 т/га (V3 и V7); солома озимой пшеницы, люпина, ячменя по 3 т/га (V4 и V8). Суммарно с начала полевого опыта в пахотный слой почвы в вариантах V3, V4, V7, V8 внесено 42 т/га соломы. Площадь делянок составляла 42–47 м2. Минеральные удобрения вносили ежегодно весной под предпосевную культивацию. Солому измельчали во время уборки зерна комбайном АМПО-500, равномерно распределяли по площади делянок согласно схеме опыта и заделывали в верхний слой 0–10 см тяжелой дисковой бороной. Через 3–4 нед. производили вспашку с равномерным распределением в толще 0–20 см прокомпостированной соломы [14]. Образцы почвы для анализов отбирали в агроценозе ячменя в июне (1-й срок отбора, V1–V4) и августе (V5–V8) из слоя 0–15 см в трехкратной повторности. Почвенные пробы для микробиологических анализов отбирали с соблюдением требований по контролю контаминации. Пробы почвы для определения биомассы микроорганизмов хранили в стерильных емкостях в течение месяца в холодильнике при температуре +4°С, а для молекулярно-генетических анализов – в морозильной камере при –70°С. Для определения химических свойств почв использовали воздушно-сухие образцы.
Химические свойства почвы. Содержание органического углерода (Сорг) и общего азота (Nобщ) в почве определяли на автоматическом HCNS-анализаторе Leco 932 (США). Величины водного pH почвы измеряли потенциометрическим способом при соотношении почва/вода, равном 1/2.5. Содержание подвижных соединений фосфора (Pподв) и калия (Kподв) определяли по методу Кирсанова.
Определение углерода микробной биомассы, базального дыхания и метаболического коэффициента. Углерод микробной биомассы (Смик) оценивали методом субстрат-индуцированного дыхания (СИД) [3]. Навеску почвы помещали во флакон и добавляли водный раствор глюкозы. Обогащенный образец почвы инкубировали (3.5–5 ч, +22°С) и измеряли концентрацию СО2 на газовом хроматографе КристаллЛюкс 4000М (Россия). Углерод микробной биомассы рассчитывали по формуле:
Базальное дыхание (БД) определяли так же, как СИД, только вместо раствора глюкозы в почву добавляли дистиллированную воду. Время инкубации флаконов с почвой 24 ч. Скорость БД выражали в мкг С–СО2/(г почвы ч).
Микробный дыхательный коэффициент (qCO2) рассчитывали по формуле:
Биомассу прокариот оценивали с помощью метода люминесцентной микроскопии с применением флуоресцентного красителя акридина оранжевого (микроскоп Биомед 5 ПР ЛЮМ (Россия)) при увеличении 1000× с масляной иммерсией [5]. Десорбцию клеток с почвы проводили при помощи ультразвуковой установки УЗДН-1 (2 мин, сила тока 0.40 А, частота 22 кГц). Число клеток прокариот на 1 г субстрата рассчитывали по формуле:
Биомассу грибов определяли методом люминесцентной микроскопии с применением флуоресцентного красителя калькофлуора белого [5]. Учет спор и длины мицелия осуществляли на люминесцентном микроскопе Биомед 5 ПР ЛЮМ (Россия) при увеличении 400×. Десорбцию клеток с почвы проводили при помощи вортекса MSV-3500 (Латвия) при скорости 3500 об./мин в течение 10 мин. Расчет количества грибных спор на 1 г субстрата вели по формуле:
Экстракция тотальной ДНК из почвы и количественная ПЦР в реальном времени. Тотальную ДНК выделяли из 0.25 г образцов почвы с использованием набора DNeasy PowerSoil ProKit (Qiagen, Германия) и гомогенизатора Precellys 24 (Bertin Technologies, Франция) при скорости 6500 об./мин в течение 40 с. Количественную оценку содержания рибосомальных генов микроорганизмов осуществляли методом полимеразной цепной реакции (ПЦР) в реальном времени. Для амплификации целевых участков ДНК разных групп микроорганизмов использовали следующие праймеры: Eub338/Eub518 – для бактерий, arc915f/arc1059r – для архей, ITS1f/5.8S – для грибов [46, 48]. Проводили калибровку зависимости интенсивности флуоресценции от логарифма концентрации ДНК стандартных растворов, по которой определяли численность копий генов в образцах с помощью программного обеспечения CFX Manager. В качестве контроля для бактерий использовали растворы клонированных фрагментов рибосомального оперона Escherichia coli, для архей – штамма FG-07 Halobacterium salinarum, для грибов – Saccharomyces cerevisiae Meyen 1 B-D1606. Реакцию проводили по следующему протоколу: 1) +95°C – 3 мин; 2) денатурация двухцепочечной ДНК при +95°C – 10 с; 3) отжиг праймеров на матрице при +50°C – 10 с; 4) удлинение цепи ДНК при +72°C – 20 с; 5) считывание значений флуоресценции, 49-кратное повторение этапов 2‒5. Анализ кривых плавления проводили для проверки размера амплифицированных продуктов. ПЦР проводили для трех повторностей образца с пересчетом на средние значения содержания копий генов в грамме почвы.
Статистический анализ и визуализация экспериментальных данных проводили в программной среде R 4.2.1. Соответствие экспериментальных данных нормальному распределению проверяли критерием Шапиро–Уилка (p > 0.05). Для оценки различий между средними значениями разных вариантов эксперимента осуществляли дисперсионный анализ методом One-Way ANOVA с проверкой нормальности распределения ошибок, гомогенности дисперсий и идентичности размера выборок. Поправку на множественные сравнения делали с помощью post-hoc теста Тьюки. Силу и достоверность связей между химическими и микробиологическими свойствами почв оценивали с помощью коэффициента корреляции Пирсона. В качестве поправки на множественные сравнения использовали поправку Холма–Бонферрони. Для многомерного анализа данных использовали метод главных компонент.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Химические свойства почвы. Внесение минеральных удобрений и соломы приводило к незначительному уменьшению рН по сравнению с контролем (табл. 1). Содержание Cорг изменялось от 0.49 в вариантах с минеральными удобрениями до 0.72% в образцах с соломой. Содержание Nобщ варьировало от 0.05 до 0.07%, отношение C/N находилось в диапазоне от 9.0 до 11.8. Для обоих сроков отбора выявлено увеличение C/N, Cорг и Nобщ в ряду: контроль < NPK < NPK + солома < солома. Содержание Kподв менялось от 54 до 107 мг/кг; Рподв – от 98 до 173 мг/кг; аммонийного азота – от 5.07 до 8.5 мг/кг. Минимальные значения Kподв и Рподв отмечены для контроля, а максимальные – для вариантов NPK и NPK + солома.
Таблица 1.
Основные химические свойства агродерново-подзолистой почвы
| Индекс | Срок отбора | Наличие соломы | Наличие удобрений | Сорг | Nобщ | С/N | pHводн | N–NH4 | Pподв | Кподв |
|---|---|---|---|---|---|---|---|---|---|---|
| % | мг/кг | |||||||||
| V1 | Июнь | – | – | 0.55 | 0.06 | 9.2 | 6.29 | 5.07 | 98 | 54 |
| V2 | – | + | 0.60 | 0.06 | 9.7 | 5.81 | 7.36 | 170 | 107 | |
| V3 | + | + | 0.67 | 0.07 | 9.9 | 5.49 | 8.50 | 173 | 107 | |
| V4 | + | – | 0.70 | 0.06 | 11.2 | 5.72 | 6.86 | 105 | 67 | |
| V5 | Август | – | – | 0.49 | 0.05 | 9.2 | 5.99 | 5.79 | 106 | 64 |
| V6 | – | + | 0.62 | 0.07 | 9.0 | 5.76 | 5.57 | 160 | 88 | |
| V7 | + | + | 0.65 | 0.06 | 10.0 | 5.57 | 6.21 | 158 | 81 | |
| V8 | + | – | 0.72 | 0.06 | 11.8 | 5.78 | 5.14 | 114 | 62 | |
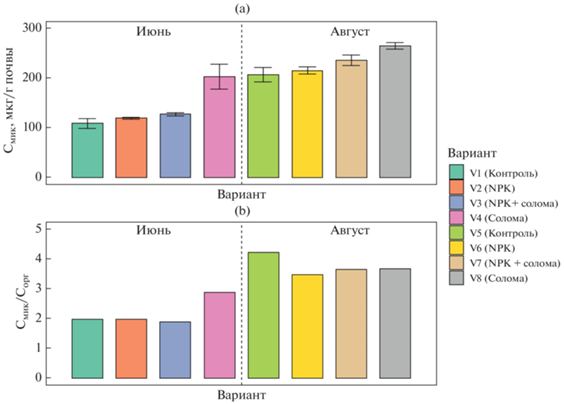
Значения углерода микробной биомассы (Смик) варьировали от 109 до 265 мкг С/г почвы (рис. 1). Увеличение значений Смик происходило только в вариантах с заделыванием соломы, причем наибольший рост биомассы (1.25–2 раза) отмечен в вариантах без внесения минеральных удобрений. Таким образом, подтверждается гипотеза о том, что заделывание в почву соломы повышает углерод микробной биомассы [26, 45, 59]. Подобный существенный рост значений Смик выявлен для второго срока отбора образцов. В целом, наблюдалось последовательное увеличение содержания Смик в ряду: контроль < NPK < NPK + солома < солома. Определяющими факторами уровня биомассы микроорганизмов в проанализированных почвах были срок отбора (F = 504, p < 0.0001) и заделка соломы (F = 136, p < 0.0001).
Для вариантов первого срока отбора заделка соломы увеличивала содержание Смик почти в 2 раза, в то время как внесение минеральных удобрений и одновременное добавление к почве соломы с NPK приводило к росту углерода микробной биомассы лишь на 5–10% по сравнению с контролем. Данный результат говорит об ингибировании части микробного сообщества минеральными удобрениями и подтверждается в предыдущих исследованиях [30, 48, 54]. Значения Смик в образцах второго срока отбора были идентичны (в случае контроля и NPK) либо выше (на 20% для варианта NPK + солома и на 30% для варианта с заделыванием соломы без минеральных удобрений) по сравнению с результатами для аналогичных вариантов первого срока. Таким образом, свежее органического вещество соломы стимулировало рост микробной биомассы и нивелировало ингибирующее действие минеральных удобрений, что отмечено в работах [29, 47]. Следует подчеркнуть, что величины углерода микробной биомассы в почвах значительно варьировали в зависимости от срока отбора, что характерно и для модельных экспериментов с внесением в почву соломы [54].
C помощью метода люминесцентной микроскопии определена структура биомассы микроорганизмов. Суммарная биомасса прокариот (одноклеточных и мицелиальных) составляла от 1.07 до 2.96 мкг/г почвы. Биомасса одноклеточных прокариот варьировала от 0.86 до 2.78 мкг/г почвы, а численность их клеток – от 4.00 × 108 до 1.32 × 109 кл./г почвы соответственно (табл. 2). Минимальные значения выявлены для контроля, а максимальные – для варианта NPK + солома. Полученные результаты сопоставимы с данными для широкого спектра дерново-подзолистых почв средней полосы России [12] и были в 1.5–2 раза выше, чем численность клеток прокариот в серых лесных и аллювиально-луговых почвах юга Московской области [18].
Таблица 2.
Структура биомассы почвенных микроорганизмов
| Индекс | Срок отбора | Наличие соломы | Наличие удобрений | Грибы | Прокариоты | Суммарная биомасса микроорганизмов (грибы и прокариот) | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| мицелий (преимуществ d = 3 мкм) |
споры (диаметр, мкм) | общая биомасса спор, мкг/г почвы | доля мелких (2–3 мкм) спор по массе, % | суммарная биомасса грибов, мкг/г почвы | численность клеток прокариот, × 109 кл./г почвы | биомасса одноклеточных прокариот, мкг/г почвы | длина актиномицетного мицелия, м/г почвы | биомасса актиномицетного мицелия, мкг/г почвы | доля мицелия актиномицетов в биомассе прокариот, % | общая биомасса прокариот, мкг/г почвы | ||||||||||||
| биомасса, мкг/г почвы | длина, м/г почвы | доля мицелия грибов, % | 2 | 3 | 5 | |||||||||||||||||
| численность, шт/г почвы × 104 | масса, мкг/г почвы | численность, шт/г почвы × 104 | масса, мкг/г почвы | численность, шт/г почвы × 103 | масса, мкг/г почвы | |||||||||||||||||
| V1 | Июнь | – | – | 121 ± ± 22 | 82.65 ± ±14.88 | 48.4 | 9.92 ± ±1.79 | 34 ± 6 | 6.45 ± ± 1.16 | 75 ± 14 | 2.08 ± ± 0.37 | 20 ± 4 | 129 ± ± 23 | 84.5 | 250 ± ± 45 | 0.40 ± ± 0.07 | 0.86 ± ± 0.15 | 5.73 ± ± 1.03 | 0.21 ± ± 0.04 | 19.63 ± ± 3.53 | 1.07 ± ± 0.19 | 251.07 ± ± 45 |
| V2 | – | + | 49 ± ± 9 | 33.9 ± ± 6.10 | 31.6 | 13.81 ± ± 2.49 | 47 ± 8 | 4.52 ± ± 0.81 | 52 ± 9 | 0.69 ± ± 0.12 | 7 ± 1 | 106 ± ± 19 | 93.4 | 155 ± ± 28 | 0.51 ± ± 0.09 | 1.09 ± ± 0.20 | 20.47 ± ± 3.68 | 0.76 ± ± 0.14 | 41.08 ± ± 7.39 | 1.85 ± ± 0.33 | 156.85 ± ± 28 | |
| V3 | + | + | 80 ± ± 14 | 55.14 ± ± 9.93 | 62.5 | 8.64 ± ± 1.56 | 29 ± 5 | 1.61 ± ± 0.29 | 19 ± 3 | – | – | 48 ± ± 9 | 100 | 128 ± ± 23 | 0.50 ± ± 0.09 | 1.07 ± ± 0.19 | 2.24 ± ± 0.40 | 0.08 ± ± 0.01 | 6.96 ± ± 1.25 | 1.15 ± ± 0.21 | 129.15 ± ± 23 | |
| V4 | + | – | 174 ± ± 31 | 119.59 ± ± 21.53 | 77.3 | 73.40 ± ± 13.21 | 25 ± 5 | 2.26 ± ± 0.41 | 26 ± 5 | – | – | 51 ± ± 9 | 100 | 225 ± ± 41 | 0.57 ± ± 0.10 | 1.22 ± ± 0.22 | 1.79 ± ± 0.32 | 0.07 ± ± 0.01 | 5.43 ± ± 0.98 | 1.29 ± ± 0.23 | 226.29 ± ± 42 | |
| V5 | Август | – | – | 74 ± ± 13 | 58.72 ± ±10.57 | 41.6 | 11.21 ± ± 2.02 | 38 ± 7 | 4.51 ± ± 0.81 | 66 ± 11 | – | – | 104 ± ± 19 | 100 | 178 ± ± 32 | 0.77 ± ±0.14 | 1.62 ± ± 0.29 | 13.89 ± ± 2.50 | 0.51 ± ± 0.09 | 23.94 ± ± 4.31 | 2.13 ± ± 0.38 | 180.13 ± ± 33 |
| V6 | – | + | 52 ± ± 9 | 41.25 ± ± 7.43 | 38.2 | 8.19 ± ± 1.47 | 28 ± 5 | 3.82 ± ± 0.69 | 56 ± 10 | – | – | 84 ± ± 15 | 100 | 136 ± ± 24 | 1.04 ± ±0.19 | 2.20 ± ± 0.40 | 3.73 ± ± 0.67 | 0.14 ± ± 0.03 | 5.98 ± ±1.08 | 2.34 ± ± 0.42 | 138.34 ± ± 25 | |
| V7 | + | + | 66 ± ± 12 | 52.03 ± ± 9.36 | 73.3 | 6.04 ± ± 1.09 | 20 ± 4 | 2.78 ± ± 0.50 | 40 ± 8 | – | – | 24 ± ± 4 | 100 | 90 ± ± 16 | 1.32 ± ± 0.24 | 2.78 ± ± 0.50 | 4.78 ± ± 0.86 | 0.18 ± ± 0.03 | 6.08 ± ±1.09 | 2.96 ± ± 0.53 | 92.96 ± ± 17 | |
| V8 | + | – | 108 ± ± 19 | 85.11 ± ± 15.32 | 45.4 | 9.92 ± ± 1.79 | 34 ± 6 | 6.59 ± ± 1.19 | 96 ± 17 | – | – | 130 ± ± 23 | 100 | 238 ± ± 43 | 0.56 ± ±0.10 | 1.19 ± ± 0.21 | 8.36 ± ± 1.50 | 0.31 ± ± 0.06 | 20.67 ± ±3.72 | 1.50 ± ± 0.27 | 239.5 ± ±43 | |
Доля мицелия актиномицетов в биомассе прокариот варьировала от 5% для вариантов с минеральными удобрениями и соломой до 21% для варианта с соломой второго срока отбора и контроля. Биомасса прокариот в большинстве образцов была представлена, преимущественно, одноклеточными формами. Длина актиномицетных гиф коррелировала с его долей в биомассе прокариот и составляла от 1.79 до 20.47 м/г почвы. Доля мелких клеток (наноформ) прокариот, которые включены в общую численность прокариот, была незначительна и увеличивалась от 3 до 8% в ряду: контроль < NPK < NPK + солома < солома.
Биомасса грибов изменялась от 90 в варианте с минеральными удобрениями и соломой до 250 мкг/г почвы в контроле. Полученные значения биомассы грибов в 1.5 раза меньше, чем в залежных дерново-подзолистых почвах Московской области [8], но в 1.5–2 раза больше по сравнению таковыми для темно-гумусовых лесных почв Костромской области [13]. Доля мицелия – активного компонента грибной биомассы – варьировала от 31.6 до 77.3%. Наименьшая длина грибных гиф (33.9 м/г почвы) выявлена в варианте с внесением минеральных удобрений, а наибольшая (119.59 м/г почвы) – в варианте с внесением соломы. Все показатели, характеризующие биомассу грибов, снижались ко второму сроку отбора. Внесение минеральных удобрений уменьшало длину мицелия микобиоты, как и в других исследованиях [34], а присутствие соломы, наоборот, увеличивало данный показатель. В целом, длина мицелия грибов в изученных вариантах была сопоставима с таковой для залежных дерново-подзолистых почв Московской области [8], но была почти в 3 раза меньше, чем для залежных выщелоченных черноземов Нижегородской области [12]. Численность одноклеточных грибных пропагул (спор и дрожжей) в образцах составляла 105–106 кл./г почвы.
Соотношение Смик/Сорг варьировало от 1.89 в варианте NPK + солома до 4.22 в контроле, с преобладанием в первом сроке отбора. Данный показатель характеризует физиологическое состояние почвенного микробиома и является индикатором доступности почвенного углерода для микроорганизмов [1, 10]. Уменьшение значений этого соотношения в почве указывает на тенденцию к стабилизации ПОВ и наличие экологических условий, препятствующих потреблению субстрата микроорганизмами [18, 23].
Активность базального дыхания почвенных микроорганизмов варьировала от 0.24 в 0.71 мкг С–СО2/(г ч) (рис. 2), что соответствует значениям для пахотных дерново-подзолистых почв Костромской области [2]. Для обоих сроков отбора образцов отмечено повышение БД в ряду контроль < NPK < NPK + солома < солома. Во второй срок отбора активность БД повышалась по сравнению с первым отбором для всех образцов. Факторами, определяющими интенсивность БД, в первую очередь являлась заделка соломы (F = 145, p < 0.0001), срок отбора образцов (F = 69, p < 0.0001) и внесение минеральных удобрений (F = 63, p < 0.0001).
Рис. 2.
Активность базального дыхания микроорганизмов (мкг С–СО2/г ч) (a) и величины дыхательного коэффициента (мкг С–СО2 (мг Смик ч)) (b).
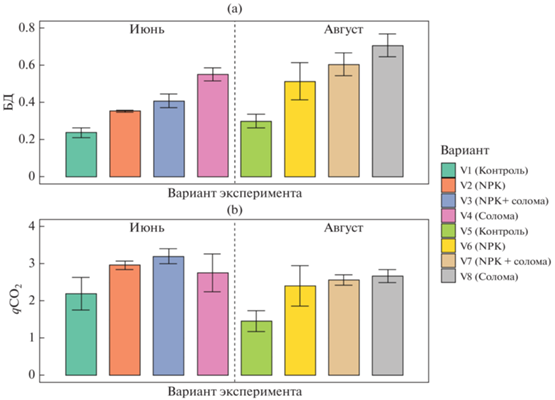
Для обоих сроков отбора внесение свежего органического вещества соломы приводило к резкому росту (в 2.5 раза) значений БД по сравнению с контролем, что соответствует результатам других исследований [61]. Одновременное внесение соломы с минеральными удобрениями также повышало БД по сравнению с контролем, но давало меньший эффект (в 1.7–2 раза). Таким образом, внесение минеральных удобрений значительно снижает БД, индуцированное при добавлении растительных остатков в почву. Такой вывод подтверждают другие исследования [38]. Ранее продемонстрирована бóльшая отрицательная корреляция между внесением NPK и содержанием Смик по сравнению с БД [27]. Судя по результатам нашей работы, внесение минеральных удобрений снижает интенсивность роста Смик, вызванную заделыванием соломы [27, 40].
Значения дыхательного коэффициента (qСО2) изменялись от 1.46 до 3.2, что характерно для пахотных дерново-подзолистых почв средней полосы России [15]. В среднем для двух сроков отбора характерна тенденция к увеличению значений qСО2 в ряду: контроль < NPK < солома < NPK + + солома. Таким образом, подтверждена гипотеза об увеличении дыхательного коэффициента при заделке соломы [15, 58]. Для qCO2 определяющими факторами являлись внесение минеральных удобрений (F = 27, p < 0.0001), срок отбора образцов (F = 19, p < 0.0001) и внесение соломы (F = 18, p < 0.0001).
Численность копий рибосомальных генов архей варьировала в диапазоне от 6.75 × 107 до 4.44 × × 108 копий генов/г почвы; численность генов бактерий – от 1.96 × 109 до 5.98 × 109 копий генов/г почвы; численность генов грибов – от 3.74 × 108 до 1.31 × 109 копий генов/г почвы (рис. 3). Применение соломы значительно повышало численность копий генов грибов и бактерий до 2 раз, а также архей до 1.5 раз. Данные результаты по порядку значений соответствовали таковым для сельскохозяйственных почв южной Бразилии с внесением соломы [44].
Рис. 3.
Численность генов микроорганизмов в почве методом количественной ПЦР (копий генов/г почвы): бактерии (a), грибы (b), археи (c), соотношение грибы/бактерии (d).
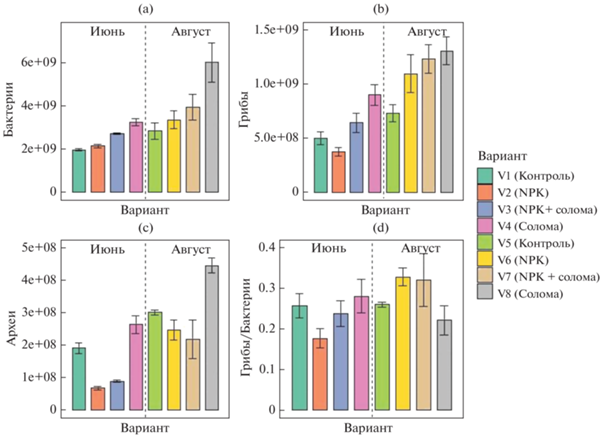
Внесение минеральных удобрений резко (в 1.5–3 раза) снижало численность архей по сравнению с контрольным вариантом, в том числе в варианте NPK + солома. При этом внесение соломы позволяло нивелировать негативное воздействие минеральных удобрений на микобиоту, что показано и в других работах [44, 48]. Численность копий рибосомальных генов бактерий не зависела отприменения минеральных удобрений.
Главным фактором, в наибольшей степени оказывающим влияние на численность копий генов всех рассматриваемых групп микроорганизмов, был срок отбора образцов (F = 174 для архей, F = 72 для бактерий и F = 122 для грибов; для всех вариантов p < 0.0001) (рис. 4). Применение соломы оказывало ведущее влияние на численность бактерий и грибов (F = 62, p < 0.0001), а количество копий генов архей в значительной степени определялось внесением минеральных удобрений (F = 163, p < 0.0001).
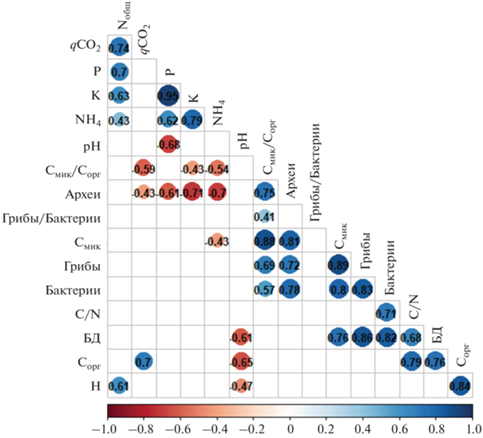
Рис. 4.
Матрица корреляций между химическими и микробиологическими свойствами почв. Числами указаны коэффициенты корреляции. Значения приведены только для коэффициентов корреляции с p < 0.05.
Полученные значения численности копий генов 16S рРНК архей и бактерий, а также ITS грибов были на 1–2 порядка ниже, чем для агрочерноземов Ставропольского края [9] и серых лесных почв юга Московской области [18]. Положительный эффект от внесения свежего органического вещества растительных остатков на численность генов почвенных микроорганизмов был показан ранее в длительных полевых экспериментах в Швеции [56].
Соотношение грибы/бактерии. По результатам люминесцентной микроскопии в микробной биомассе почвы доминировали грибы, доля которых колебалась от 79.7% для варианта NPK + солома до 94.0% в контроле. Соответственно, соотношение грибы/бактерии по методу люминесцентной микроскопии изменялось от 4 в вариантах с NPK и NPK + солома до 15 в вариантах с заделыванием соломы и контроле. Однако по результатам количественной ПЦР соотношение грибы/бактерии варьировало в диапазоне от 0.17 в вариантах с минеральными удобрениями до 0.33 в варианте с соломой. Факторами, в наибольшей степени определяющими соотношение грибы/бактерии, были срок отбора образцов (F = 35, p < 0.0001) и внесение минеральных удобрений (F = 30, p < 0.0001).
По двум примененным методам (люминесцентная микроскопия и количественная ПЦР) получены сильно отличающиеся значения соотношений грибы/бактерии в почвах. В первую очередь это обусловлено тем, что количественная ПЦР не отражает информацию о количестве клеток и биомассе микроорганизмов, в отличие от метода люминесцентной микроскопии. Для разных таксонов содержание рибосомальных генов неодинаково и может варьировать в диапазоне от 1 до 16 [19, 51]. Кроме того, за счет мицелиального строения в клетках грибов содержится гораздо меньше ДНК на единицу биомассы по сравнению с прокариотами [39].
Матрица корреляций между химическими и биологическими свойствами почв. Интенсивность БД характеризовалась высокой положительной корреляцией с количеством копий генов грибов (r = 0.88) и бактерий (r = 0.83), а также Смик и Сорг (r = 0.76). Смик положительно коррелировал с количеством копий генов грибов (r = 0.89), архей (r = 0.81) и бактерий (r = 0.80). Таким образом, хотя численность копий генов микроорганизмов не тождественна Смик, эти показатели характеризуются высокой положительно корреляцией, поэтому численность генов прокариот и грибов может являться хорошим дополнительным микробиологическим индикатором состояния почв.
Отрицательная корреляция обнаружена между численностью копий генов архей и содержанием аммонийного азота (r = –0.70), а также между qCO2 и отношением Смик/Сорг (r = –0.59). Негативное влияние аммонийного азота на численность копий генов архей может быть связано с тем, что преобладающей среди них группой являются представители филума Thaumarchaeota, развитие которых происходит в условиях низких концентраций аммония [19, 32]. Кроме того, в случае окисления аммония археи и бактерии выступают конкурентами за ресурсы [32]. Внесение соломы в почву существенно стимулирует нитрификацию аммонийного азота археями филума Thaumarchaeota, по сравнению с аммонийокисляющими бета- и гаммапротеобактериям [56, 60].
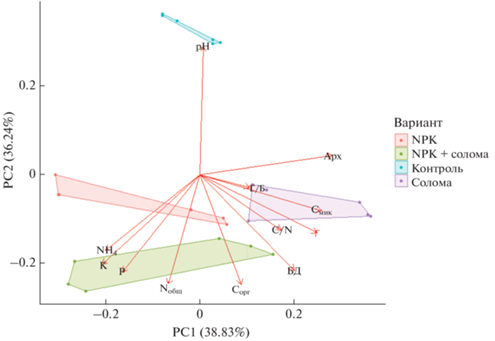
Метод главных компонент. На основе анализа химических и микробиологических показателей агродерново-подзолистой почвы, рассмотренные варианты были разделены на 4 непересекающихся кластера (рис. 5). Внесение соломы способствовало росту значений C/N, Смик, численности грибов и соотношению грибы/бактерии. Соотношение грибы/бактерии связывают с углеродсеквестрирующей способностью почвы: рост грибной биомассы и соотношений грибы/бактерии положительно сказывается на накоплении ПОВ [43, 55]. При этом следует отметить уменьшение прироста грибной биомассы при совместном внесении соломы и минеральных удобрений [29]. Тем не менее, большинство рассмотренных микробиологических показателей агродерново-подзолистой почвы (Смик/Сорг, биомасса прокариот, БД, численность копий рибосомальных генов микроорганизмов) по отдельности характеризовалось значительным временным варьированием, которое часто оказывало даже больший эффект по сравнению с внесением соломы или минеральных удобрений [31]. Этот факт подчеркивает зависимость функционирования микробного сообщества почвы от гидротермических условий и стадии вегетации растений. Например, отмечены различия в величинах целлюлазной активности в почве под вико-овсяной смесью, выращиваемой в мае и сентябре [6]. Кроме того, следует иметь в виду возможность волнообразной динамики целлюлазной активности и численности прокариотов и микромицетов со строгой зависимостью числа и пиков осцилляций от внесения минеральных или органических удобрений [6, 33, 53].
ЗАКЛЮЧЕНИЕ
Многократная заделка соломы оказывала положительное действие на большинство микробиологических параметров агродерново-подзолистой почвы. Минеральные удобрения, напротив, уменьшали величину qСО2, биомассу грибов и численность копий генов 16S рРНК архей. Поэтому заделка свежего органического вещества соломы может быть использована для повышения микробиологической активности почвы и ее плодородия, а также для устранения негативного влияния минеральных удобрений на почвенную микробиоту. Для части микробиологических показателей (Смик, Смик/Сорг, биомасса прокариот, БД, численность копий генов 16S рРНК бактерий и ITS рРНК грибов) фактор временной динамики превышал влияние как минеральных удобрений, так и соломы.