Адсорбент благородных металлов на основе сополимеров дивинилсульфида и 4-винилпиридина
75
Журнал прикладной химии. 2019. Т. 92. Вып. 1
УДК 541.64:547.425
АДСОРБЕНТ БЛАГОРОДНЫХ МЕТАЛЛОВ НА ОСНОВЕ СОПОЛИМЕРОВ
ДИВИНИЛСУЛЬФИДА И 4-ВИНИЛПИРИДИНА
© Н. С. Шаглаева1, Д. Б. Багинов1, Е. Г. Филатова1, Ю. Н. Пожидаев1,
Т. А. Подгорбунская1, Л. М. Станевич2
1 Иркутский национальный исследовательский технический университет
2 Иркутский государственный медицинский университет
E-mail: ShaglaevaNS@yandex.ru
Поступила в Редакцию 10 апреля 2018 г.
После доработки 25 сентября 2018 г.
Принята к публикации 27 сентября 2018 г.
Радикальной сополимеризацией дивинилсульфида с 4-винилпиридином синтезированы сополимеры
пространственной структуры, имеющие в своей структуре «пиридиновые» атомы азота и суль-
фидную серу. Установлено, что сополимеры характеризуются высокими значениями статических
сорбционных емкостей, которые для Au(III), Ag(I), Pt(IV) и Pd(II) достигают 1200, 340, 1040, 520 мг·г-1
соответственно. Полученные результаты свидетельствуют о перспективности использования ди-
винилсульфида в качестве сшивающего мономера при синтезе ионообменных смол.
Ключевые слова: дивинилсульфид, 4-винилпиридин, сополимеры, сорбционная емкость, ионообменные
смолы.
DOI: 10.1134/S0044461819010109
Ионообменные смолы, или иониты, находят широ-
Радикальной сополимеризацией ДВС с 4-винил-
кое применение в промышленности для извлечения
пиридином (ВП) осуществлен синтез ионита, содер-
благородных и редких металлов. Из 94 марок смол,
жащего в полимерной цепи «пиридиновый» атом
допущенных к применению, в России выпускается
азота и сульфидную серу, что обеспечивает высокую
только катионит КУ-2-8. Сырьевая база для синтеза
сорбционную активность продуктов сополимериза-
смол постоянно сокращается, поэтому необходимо
ции по отношению к ионам благородных металлов.
восстановление российского производства основ-
Подобным путем получены аниониты на основе ВП и
ных видов ионообменных смол на обновленной тех-
технического дивинилбензола с сорбционной обмен-
нологической платформе. Дивинилсульфид (ДВС)
ной емкостью 7.18 мэкв·г-1 (0.1 М HCl), проведение
является одним из перспективных мономеров для
аналогичной реакции с п-дивинилбензолом позво-
создания ионообменных смол, поскольку наличие
ляет увеличить емкость ионита до 7.90 мэкв·г-1 [4].
в каркасе полимерной матрицы атомов сульфидной
Способ получения дивинилбензола многостадийный
серы ДВС («мягких» легкополяризуемых центров
и протекает с образованием изомеров дивинильного
основности и комплексообразования) будет придавать
мономера, в то время как технология синтеза ДВС
иониту комплексообразующее сродство высокой се-
проста и осуществляется в одну стадию из ацетиле-
лективности по отношению к редким и благородным
на и сульфида калия в среде диметилсульфоксида с
металлам.
выходом 82%. Основное преимущество сорбентов
ДВС синтезируется реакцией ацетилена с серово-
ДВС-ВП перед сорбентом дивинилбензол-ВП заклю-
дородом или сульфидом натрия [1, 2]. Главным пре-
чается в простоте получения ДВС.
имуществом данного способа получения серосодер-
Склонность ионов благородных металлов к обра-
жащего мономера является доступность и дешевизна
зованию устойчивых комплексов с N- и S-донорными
исходных веществ. На основе ДВС получена серия
лигандами [5] активно используется при создании со-
ионитов со свойствами, значительно превосходящими
рбционных материалов. Так, функциональные смолы,
существующие или принципиально новыми [3].
содержащие гуанилтиомочевину, 2-меркапто-1-ме-
76
Шаглаева Н. С. и др.
тилимидазол, проявили высокую селективность по
Радикальная сополимеризация дивинилсульфида
отношению к золоту(I) и серебру(I) из аммиачных
и 4-винилпиридина. Радикальную сополимеризацию
растворов. При этом они не сорбировали аммиачные
ДВС и ВП проводили ампульным методом в присут-
комплексы меди(II). Кинетику сорбции золота(I) на
ствии ДАК при 60°С. В стеклянную ампулу помеща-
этих смолах улучшали путем иммобилизации лиган-
ли рассчитанные количества ДВС, ВП и ДАК, реак-
дов N,N-диметилэтаноламина, которые отвечали за
ционную смесь выдерживали в массе сомономеров
повышение гидрофильности полимерного материала.
в атмосфере азота при температуре 60°С в течение
Степень сорбции степени золота составляла 99.5% [6].
4 ч. Полученный сополимер после синтеза после-
В качестве сорбентов для ионов Ag(I), Au(III), Pd(II)
довательно промывали растворителями (бензолом,
и Pt(II) исследовали серию из восемнадцати сополи-
ацетоном и водой) в аппарате Сокслета и сушили в
меров 4-винилпиридина или 4-метил-4′-винилбипи-
вакууме до постоянной массы. Составы полученных
ридина с различными сшивающими агентами. Такие
сополимеров рассчитывали по данным элементного
хелатные полимеры обладают значительной селектив-
анализа. Степень набухания сополимера ДВС-ВП
ностью сорбции для Au(III) по Ag(I) и Pd(II) по Pt(II) [7].
определяли весовым методом.
Новая хелатная смола была синтезирована из ма-
Удельную поверхность сополимеров определяли
крорезистентного полистирол-дивинилбензольного
методом низкотемпературной адсорбции-десорбции
сополимера, включающего функциональную группу
азота [12] на приборе СОРБТОМЕТР-М. Суммарный
β-гидроксидитиокоричной кислоты. Результаты ис-
объем пор W вычисляли по уравнению W = Хmax/ρ,
следования адсорбционной способности показали,
где Хmax — максимальный объем сорбированного
что синтезированная смола оказалась высокоселек-
газа (г·г-1), ρ - плотность газа (г·см-3).
тивной для серебра(I), ртути(II), золота(III) и плати-
ИК спектры регистрировали в KBr и в вазели-
ны(IV) в сильнокислотном водном растворе [8].
новом масле на спектрометре IFS-25. УФ спектры
Серия высокоэффективных сорбентов благород-
регистрировали на приборе Specord UV-VIS.
ных металлов получена золь-гель синтезом на основе
Стандартные растворы ионов благородных метал-
кремнийорганических N,S-функциональных мономе-
лов концентрацией 10 мг·мл-1 готовили растворением
ров. Отличительной особенностью таких полимеров
препаратов H2PtCl6·6H2O («чистый», ОАО AURAT),
наряду с незаурядной комплексообразующей актив-
PdCl2·2H2O («чистый», ОАО AURAT), HAuCl4·4H2O
ностью является высокая химическая и термическая
(х.ч., ОАО AURAT) в соляной кислоте 3 моль·л-1,
стабильность [9-11].
Ag(NO3)·4H2O («чистый», ООО РЕАХИМ) раство-
В целом N- и S-содержащие ионообменные и ком-
ряли в азотной кислоте 3 моль·л-1.
плексообразующие сорбенты занимают лидирую-
Сорбцию благородных металлов из растворов со-
щие позиции среди обширной группы полимерных
ляной кислоты различной концентрации осущест-
материалов, предложенных для извлечения ионов
вляли в статических условиях при температуре 25°С.
благородных металлов.
Для перемешивания растворов использовали аппа-
Цель настоящей работы — получение сополиме-
рат для встряхивания марки 6410 М (300 качаний в
ров ДВС с 4-ВП и изучение адсорбции благородных
1 мин). Концентрацию ионов благородных металлов
металлов ионитами на основе синтезированных со-
в растворах варьировали от 10-4 до 10-2 моль·л-1. Во
полимеров.
всех случаях использовали свежеприготовленные рас-
творы. Сорбент ДВС-ВП в статическом варианте сор-
бции использовали без предварительного набухания.
Экспериментальная часть
Масса воздушно-сухого сорбента 0.02 г, объем рас-
Дивинилсульфид синтезировали по способу [1].
твора 50 мл. По окончании сорбции сополимер отде-
Непосредственно перед опытом его очищали пере-
ляли от раствора фильтрованием. Содержание золота
гонкой.
в растворах после сорбции определяли атомно-абсор-
4-Винилпиридин - коммерческий продукт фирмы
бционным методом на приборе С-115М1 (НПП Укр-
Sigma-Aldrich. Очистку проводили вакуумной пере-
росприбор), палладия и платины — фотометрическим
гонкой 58°С/5 мм рт ст., nD20 1.5499. Чистоту моно-
методом по реакции образования их хлороловянных
меров контролировали хроматографически.
комплексов [13]. Измерение оптической плотности
Динитрил азобисизомасляной кислоты (ДАК) —
проводили на электрофотоколориметре КФК-3-1.
коммерческий продукт фирмы Sigma-Aldrich. Про-
Эффективность процесса извлечения ионов ме-
дукт предварительно очищали перекристаллизацией
таллов из раствора оценивали по степени извлечения
из этанола.
W (%), которую рассчитывали как отношение раз-
Адсорбент благородных металлов на основе сополимеров дивинилсульфида и 4-винилпиридина
77
ности исходной сисх (мг∙л-1) и конечной скон (мг∙л-1)
азотной кислот и гидроксида натрия не вызывает де-
концентраций ионов металла в растворе к исходной
струкцию каркаса). Сополимеры хорошо набухают в
концентрации ионов металла:
органических растворителях: в ацетоне — на 500%,
в гексане на — 300%. Набухаемость сополимеров
в водном растворе кислоты и щелочи значительно
ниже и составляет до 100 и 60% соответственно. Ва-
рьируя количество ДВС в сополимере, можно целена-
Статическую сорбционную емкость А (мг·г-1) рас-
правленно увеличивать степень сшивки, что приводит
считывали по формуле
к понижению степени набухания, и появляется воз-
можность использования сополимеров в колоночных
процессах извлечения ионов благородных металлов.
Удельная поверхность по азоту 2.3 м2·г-1, суммарный
где с0 и с — исходная и равновесная концентрации
объем пор 0.22 см3·г-1 полученных сополимеров со-
иона металла в растворе (мг·л-1), V — объем раство-
поставимы с аналогичными показателями известных
ра (л), m — масса сорбента (г).
сополимеров схожей структуры [14, 15].
Аналогично исследовали сорбцию ионов серебра
Процесс сополимеризации протекает с хорошим
из растворов азотной кислоты. Остаточную концен-
выходом при любых соотношениях мономерной сме-
трацию серебра в растворах определяли атомно-аб-
си (табл. 1). Составы сополимеров, рассчитанные по
сорбционным методом на приборе С-115М1.
содержанию азота и серы, удовлетворительно со-
При проведении сорбции Pt(IV), Pd(II), Au(III) из
гласуются между собой. Количество звеньев ДВС в
растворов серной кислоты исходные хлоридные рас-
сополимере уменьшается с понижением его концен-
творы благородных металлов смешивали с водными
трации в исходной смеси. С увеличением содержания
растворами серной кислоты необходимой концентра-
ДВС в исходной смеси наблюдается уменьшение
ции. Процесс сорбции и анализ растворов осущест-
выхода целевого продукта.
вляли аналогично исследованию в солянокислых
В ИК спектрах сополимеров отсутствуют полосы
растворах.
поглощения, характерные для виниловой группы при
960, 1580 и 1640 см-1, но остаются неизменными по-
Обсуждение результатов
лосы поглощения пиридинового кольца (1600, 1555,
Радикальной сополимеризацией ДВС с ВП по-
1490, 1068 см-1). Полоса поглощения при 660 см-1 мо-
лучены нерастворимые сополимеры, которые пред-
жет быть отнесена к валентным колебаниям связи С-S.
ставляют собой порошки желтого цвета и обладают
Образование нерастворимого продукта и данные
высокой механической прочностью и осмотической
ИК спектроскопии свидетельствуют о том, что сопо-
стабильностью, устойчивы к действию солей, раз-
лимеризация ДВС с ВП протекает с раскрытием двух
бавленных кислот и щелочей (кипячение образцов
двойных связей в ДВС, что приводит к образованию
в течение 6 ч в 10%-ных растворах соляной, серной,
сополимера, имеющего сетчатую структуру:
Предварительными экспериментами было пока-
в виде катиона Ag+. Извлечение ионов Pt, Pd и Au
зано, что сополимер ДВС-ВП, содержащий 8.78%
исследовано в растворах соляной и серной кислот, в
азота и 12.67% серы (табл. 1, опыт № 3), обладает
которых эти металлы существуют в виде ацидоком-
более высокой сорбционной активностью. Поэтому
плексов различного состава [5, 16-18].
детальное исследование сорбционных свойств осу-
Для ацидокомплексов Pt, Pd, Au с увеличением
ществлено для этого образца сополимера.
концентрации кислот отмечается некоторое снижение
Изучение адсорбции ионов серебра рассматривае-
степени извлечения ионов металлов, за исключением
мым сополимером ДВС-ВП осуществлено в раство-
тетрахлоридного комплекса золота в сернокислой сре-
рах азотной кислоты, где этот металл присутствует
де (рис. 1). В большей степени снижение степени из-
78
Шаглаева Н. С. и др.
Таблица 1
Сополимеризация дивинилсульфида с 4-винилпиридином (ДАК = 0.5 мас% , 60°С, 6 ч)
Состав исходной смеси, мол%
Содержание азота и серы, мас%
Состав сополимера, мол%
№ опыта
Выход, %
ВП
ДВС
N
S
ВП
ДВС
1
20.0
80.0
5.01
23.42
32.11
67.89
65
2
40.1
59.9
7.90
16.83
54.36
45.64
75
3
50.0
50.0
8.78
12.67
61.23
38.77
92
4
80.0
20.0
12.11
3.45
88.75
11.25
80
влечения ионов металлов проявляется для хлороком-
плексов Pt, Pd τ1/2 = 30 мин для хлорокомплексов Au
плексов платины и золота в растворе соляной кислоты
τ1/2 = 5-10 мин.
(рис. 1). Приведенный характер зависимости свиде-
Изотермы адсорбции в 1 М растворах кислот
тельствует в пользу анионного обмена по пиридиново-
(рис. 2) характеризуют распределение ионов метал-
му атому азота и проявления конкурирующего влияния
лов в жидкой и твердой фазах в состоянии равнове-
анионов кислоты с учетом их размеров и подвижности.
сия и позволяют рассчитать значения сорбционной
Не исключается и координационное взаимодействие
емкости (табл. 2).
ионов металлов по атомам азота и серы, что в большей
В целом сополимеры ДВС-ВП характеризуют-
степени характерно для катионной формы серебра.
ся высокими значениями статических сорбционных
Время установления сорбционного равновесия
емкостей, которые для Au(III), Ag(I), Pt(IV) и Pd(II)
при извлечении металлов из 1 М растворов кислот
достигают 1200, 340, 1040, 520 мг·г-1 соответственно.
составляет 60 мин для катиона серебра при време-
Высокая сорбционная активность рассматривае-
ни полусорбции τ1/2 = 15 мин; для анионных ком- мых сополимеров (табл. 2) определяется достаточно
Рис. 1. Влияние природы и концентрации кислот на
степень извлечения ионовAu(III) в H2SO4 (1) и HCl (3),
Рис. 2. Изотермы адсорбции ионов Ag в HNO3 1 М (а),
Ag(I) в HNO3 (2), Pd(II) в H2SO4 (4) и HCl (5), Pt(IV) в
Au, Pt, Pd в HCl 1 М (а) и H2SO4 1 М (б) (mсорб = 10 мг,
H2SO4 (6) и HCl (7).
V = 20 мл, t = 2 ч).
Адсорбент благородных металлов на основе сополимеров дивинилсульфида и 4-винилпиридина
79
высоким содержанием атомов азота и серы в составе
Таблица 2
сополимера (табл. 1, опыт № 3). В соответствии с
Значения статической сорбционной емкости А
удельным содержанием азота и серы в составе со-
в растворах кислот 1 моль·л-1
полимера рассчитаны теоретические значения пол-
ной сорбционной емкости по благородным металлам
А, мг·г-1/ммоль·г-1
Металл
исходя из предположения о взаимодействии ионов
HCl
H2SO4
благородных металлов с атомами азота и серы в со-
отношении 1:1 (табл. 3). Сопоставление экспери-
Pt
670/3.44
570/2.92
ментальных (табл. 2) и теоретически достижимых
Pd
410/3.88
520/4.91
(табл. 3) значений сорбционной емкости сополимера
Au
730/3.71
1200/6.09
ДВС-ВП по ионам благородных металлов свиде-
Ag
330/3.06 (HNO3)
тельствует о высокой степени заполнения химически
активных центров на поверхности адсорбента.
Полученные результаты свидетельствуют о том,
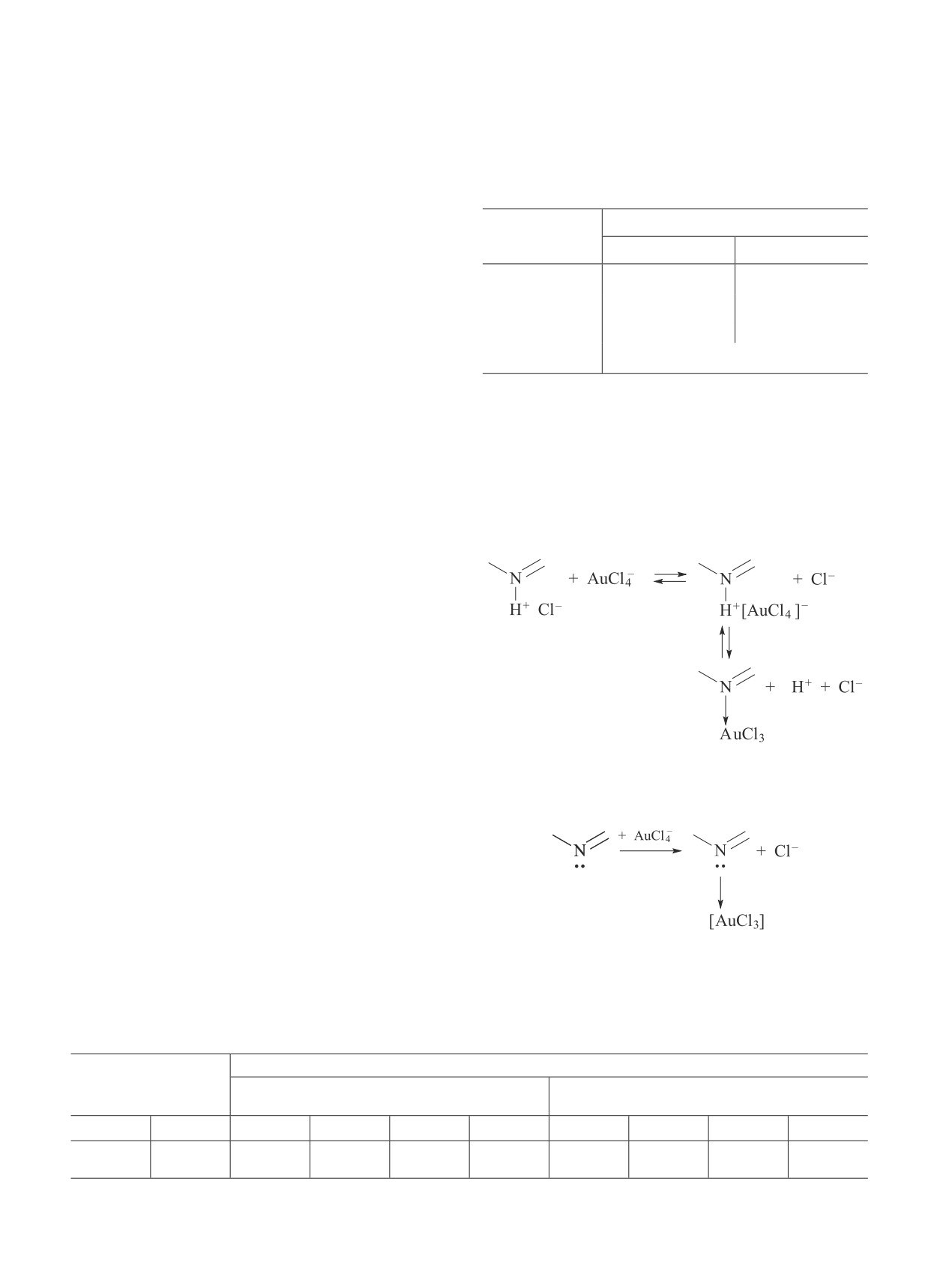
ацидокомплексов, вначале имеет место анионный об-
что исследованные сополимеры ДВС и 4-ВП не усту-
мен, а затем происходит координация. Таким образом,
пают по эффективности сорбционного извлечения
взаимодействие по атому азота можно представить
благородных металлов известным комплексообразу-
следующей схемой: по протонированной форме сое-
ющим и ионообменным сорбентам, содержащим в
динения сорбция проходит вначале по ионному меха-
своем составе сходные химически активные группы,
низму, а затем происходит вытеснение хлорид-иона
в том числе гетероциклические амины [19-21].
из первой координационной сферы металла:
Для выяснения механизма сорбционного взаимо-
действия изучены ИК спектры исходных сополиме-
ров и сополимеров, обработанных минеральными
кислотами, и их концентратов после сорбции. В ИК
спектре сополимера, обработанного соляной кисло-
той 1 М, появляется широкая полоса поглощения в
области 2600-3000 см-1, характерная для аммоние-
вого катиона. Смещение полосы поглощения с 1600
к 1630 см-1 также свидетельствует об образовании
протонированного атома азота в пиридиновом фраг-
менте сополимера. Такие же изменения сохраняются
и в ИК спектрах сополимера, насыщенного ионами
Сорбция на непротонированной форме происходит
благородных металлов. Полученные данные позво-
только в результате замещения хлорид-ионов лиганд-
ляют предполагать, что для ацидокомплексов Pt, Pd,
ными группами комплекса:
Au сорбция происходит за счет ионного обмена с
последующим вытеснением лигандов из внутренней
сферы хлорокомплекса металла.
По аналогии с литературными данными по извле-
чению ионов переходных, в том числе благородных,
металлов сорбентами со сходными функциональны-
ми группами [22-25] можно предположить, что при
Смещение полосы поглощения ДВС-фрагмента в
сорбции металлов, находящихся в растворе в виде
полимерной матрице с 660 до 700 см-1 свидетельству-
Таблица 3
Теоретические значения полной сорбционной емкости сополимера ДВС-ВП
Полная сорбционная емкость, мг·г-1
Удельное содержание,
вычислено по удельному содержанию азота в
вычислено по удельному содержанию серы в
ммоль·г-1
сорбенте
сорбенте
N
S
Ag(I)
Au(III)
Pt(IV)
Pd(II)
Ag(I)
Au(III)
Pt(IV)
Pd(II)
6.27
3.96
677
1236
1223
665
428
780
772
420
80
Шаглаева Н. С. и др.
ет об участии атомов серы сополимера в процессах
ev Yu. N., Raspopina O. Yu., Belousova L. I., Voron-
сорбции металлов.
kov M. G. // Russ. J. Gen. Chem. 1999. V. 69. N 9.
Установлено, что в условиях извлечения благород-
P. 1391-1394].
[10]
Pozhidaev Y., Vlasova N., Voronkov M., Vasilyeva I. //
ных металлов в 1 М растворах кислот не сорбируются
Advanced Sci. Lett. 2013. V. 19. N 2. P. 615-618.
железо, кобальт, никель, цинк. При исходной концен-
[11]
Пожидаев Ю. Н., Оборина E. H., Белоусова Л. И.,
трации 1 мг·мл-1 медь извлекается на 18%.
Власова Н. Н., Воронков М. Г. // ДАН. 2004. Т. 399.
Вып. 6. С. 788-790 [Pozhidaev Yu. N., Oborina E. N.,
Выводы
Belousova L. I., Vlasova N. N., Voronkov M. G. //
Doklady Chem. 2004. V. 399. N 4-6. Р. 250-252].
1. Радикальной сополимеризацией дивинилсуль-
[12]
Rouquerol F., Rouquerol J., Llewellyn P., Maurin G.,
фида с 4-винилпиридином в присутствии динитрила
Sing K. Adsorption by Powders and Porous Solids.
азобисизомасляной кислоты с выходом до 92% по-
Oxford; Amsterdam: Acad. Press, 2013. 646 p.
лучены сетчатые сополимеры, имеющие удельную
[13]
Марченко З., Бальцежак М. К. Методы спектро-
поверхность по азоту 2.3 м2·г-1, суммарный объем
фотометрии в УФ и видимой областях в неорга-
пор 0.22 см3·г-1.
ническом анализе: Пер. с польск. М.: БИНОМ.
2. Сополимеры дивинилсульфид-4-винилпиридин
Лаборатория знаний, 2007. 711 с.
характеризуются высокими значениями статических
[14]
Светлов А. К., Раховская С. М., Хомутов Л. И.,
сорбционных емкостей, которые для Au(III), Ag(I),
Боримская В. С. // Коллоид. журн. 1971. Т. 33.
Pt(IV) и Pd(II) достигают 1200, 340, 1040, 520 мг·г-1
С. 264-267.
[15]
Вокина О. Г., Царик Л. Я., Калабина А. В., Куза-
соответственно.
ев А. И. // Высокомолекуляр. соединения. 1982.
3. Взаимодействие ионов благородных металлов
Т. 24А. № 7. С. 1378-1385 [Vokina O. G., Tsa-
с поверхностью адсорбента является результатом
rik L. Ya., Kalabina A. V., Kuzayev A. I. // Polym. Sci.
образования ионно-координированных комплексов
1982. V. 24. N 7. P. 1742-1748].
с атомами азота и серы химически активных групп
[16]
Livingstone S. E. The Chemistry of Ruthenium,
сополимера.
Rhodium, Palladium, Osmium, Iridium and Platinum.
Приведенные в статье результаты были получены
Oxford; NewYork: Pergamon Press, 1973. 224 p.
в рамках выполнения государственного задания Мин-
[17]
Симонова С. А., Бурмистрова Н. М., Афонин М. В.
обрнауки России № 4.5867.2017/8.9 и гранта РФФИ
// Рос. хим. журн. 2006. Т. L. № 4. С. 19-25.
№ 16-08-00198а.
[18]
Адеева Л. Н., Миронов А. В. // Вестн. Омского ун-
та. 2013. № 4. С. 128-131.
[19]
Мясоедова Г. В., Захарченко Е. А., Моходоева О. Б.,
Список литературы
Кубракова И. В., Никашина В. А. // ЖАХ. 2005.
[1] Pat. GB 1369280 (publ. 1974). Divinyl sulfide. С. А.
Т. 60. № 5. С. 536-542.
1975. V. 83. 27563.
[20]
Симонова С. А., Бурмистрова Н. М., Бажано-
[2] Vitkovskaya N., Kobychev V.,Skitnevskaya A., Orel V.,
ва И. С., Тевлина А. С., Коновалов Л. B. // ЖПХ.
Bobkov A., Zubarev A., Trofimov B. // Tetrahedron Lett.
1998. Т. 71. № 4. С. 573-579 [Simanova S. A.,
2017. V. 58. N 1. P. 92-96.
Burmistrova N. M., Bazhanova I. S., Tevlina A. S.,
[3] Трофимов Б. А., Амосова С. В. Дивинилсульфид и
Konovalov L. V. // Russ. J. Appl. Chem. 1998. V. 71.
его производные. Новосибирск: Наука, 1983. 264 c.
N 4. P. 588-594].
[4] Салдадзе К. M., Копылова-Валова В. Д. Комплексо-
[21]
Моходоева О. Б., Мясоедова Г. В., Кубракова И. В.
образующие иониты. М.: Химия, 1980. 336 с.
// ЖАХ. 2007. Т. 62. № 7. С. 679-695 [Mokhodo-
[5] Massey A. G., Thompson N. R., Johnson B. F. G. The
eva O. B., Myasoedova G. V., Kubrakova I. V. // J.
Chemistry of Copper, Silver and Gold. Oxford; New
Analyt. Chem. 2007. V. 62. N 7. P. 607-622].
York: Pergamon Press, 1973. 197 p.
[22]
Ehrlich H. V., Buslaeva T. M., Maryutina T. A. // Russ.
[6] Pilśniak-Rabiega M., Trochimczuk A. W. // Hydrometal-
J. Inorg. Chem. 2017. V. 62. N 14. P. 1797-1818.
lurgy. 2014. V. 146. P. 111-118.
[23]
Борягина И. В., Волчкова Е. В., Буслаева Т. М.,
[7] Talanova G. G., Zhong, L., Kravchenko O. V., Yatsimir-
Васильева М. В., Эрлих Г. В. // Цв. металлы. 2012.
skii K. B., Bartsch R. A. // J. Appl. Polym. Sci. 2011.
№ 5. С. 59-64.
V. 80. N 2. P. 207-213.
[24]
Boryagina I. V., Volchkova E. V., Buslaeva T. M.,
[8] Liu C. Y., Lih J. J. Z. // Fresenius′ Zeitschrift für
Lobanova U. A., Ehrlich H. V. // Precious Metals.
analytische Chemie. 1988. Bd 332. N 2. S. 171-175.
V. 33. N 1. P. 45-47.
[9] Власова Н. Н., Пожидаев Ю. Н., Распонина О. Ю.,
[25]
Эрлих Г. В., Лисичкин Г. В. // ЖОХ. 2017. Т. 87. № 6.
Белоусова Л. И., Вороноков М. Г. // // ЖОХ. 1999.
С. 1001-1027 [Ehrlich H. V., Lisichkin G. V. // Russ.
Т. 69. № 9. С. 1446-1449 [Vlasova N. N., Pozhida-
J. Gen. Chem. 2017. V. 87. N 6. P. 1220-1245].