Журнал прикладной химии. 2019. Т. 92. Вып. 10
СОРБЦИОННЫЕ И ИОНООБМЕННЫЕ ПРОЦЕССЫ
УДК 552.5
ФИЗИКО-ХИМИЧЕСКИЕ И СОРБЦИОННЫЕ СВОЙСТВА
ОБРАЗЦОВ ПРИРОДНОГО УГЛЯ РАЗЛИЧНОЙ СТЕПЕНИ МЕТАМОРФИЗМА
© В. Г. Смирнов1, В. В. Дырдин1, А. Ю. Манаков2*,
Н. И. Федорова3, Н. В. Шикина4, З. Р. Исмагилов3,4
1 Кузбасский государственный технический университет им. Т. Ф. Горбачева,
650000, г. Кемерово, ул. Весенняя, д. 28
2 Институт неорганической химии им. А. В. Николаева СО РАН,
630090, г. Новосибирск, пр. Академика Лаврентьева, д. 3
3 Институт углехимии и химического материаловедения ФИЦ угля и углехимии,
650000, г. Кемерово, Советский пр., д. 18
4 Институт катализа им. Г. К. Борескова СО РАН,
630090, г. Новосибирск, пр. Академика Лаврентьева, д. 5
* Е-mail: manakov@niic.nsc.ru
Поступила в Редакцию 25 мая 2019 г.
После доработки 7 июня 2019 г.
Принята к публикации 26 июня 2019 г.
Исследована пористость восьми образцов природных углей, у которых в ряду возрастания степени
метаморфизма содержание углерода в органической массе увеличивается от 80 до 93%, а кислорода
уменьшается от 14 до 2%. Использованы методы низкотемпературной сорбции азота и ртутной
порометрии, а также исследована изотерма сорбции воды (+27°С). На основе каждого метода
рассчитан объем пор, емкость монослоя при сорбции воды и сорбции азота, вычислена площадь по-
верхности пор. По уравнению сорбции Дента рассчитано количество прочно- и слабосвязанной воды,
сорбированной каждым образцом, и показано, что количество прочносвязанной воды монотонно
зависит от количества кислорода в органической массе. Для исследованных образцов природного
угля объем сорбированной воды близок к суммарному объему пор, определенному методом ртутной
порометрии, и на порядок превосходит объем пор, измеренный методом низкотемпературной сорбции
азота. Обсуждаются причины наблюдаемого несоответствия.
Ключевые слова: cорбция воды; сорбция метана; природный уголь; порометрия; диффузия
DOI: 10.1134/S0044461819100116
При формировании природного угля из раститель-
температура, формируются химическая структура
ных остатков происходит обуглероживание органиче-
органической массы угля и внутренняя текстура пор
ской массы, сопровождающееся потерей кислород- и
[1-4]. Актуальной задачей является исследование фи-
водородсодержащих групп. Из угольного пласта в
зико-химических свойств углей и текстуры внутрен-
процессе созревания угля выделяются углекислый
ней поверхности угольных пор [1-6]. Данные свой-
газ, метан, легкие углеводороды, водород и другие
ства влияют на сорбцию природными углями жидких
газы, а также вода. Под влиянием геологических ус-
и газообразных веществ и могут иметь определяющее
ловий, к которым относятся высокие механические
значение для разработки технологий комплексной
напряжения в пласте, а также газовое давление и
переработки угля, извлечения из природного угля
1320
Физико-химические и сорбционные свойства образцов природного угля различной степени метаморфизма
1321
ценных химических компонентов и добычи метана
что в исследованных углях оба типа воды являются
из угольных пластов. Изучение текстуры пор при-
незамерзающими, т. е. четкого фазового перехода
родного угля проводится методами низкотемператур-
вода-лед для них не фиксируется. Можно отметить,
ной сорбции азота либо сорбцией других газов при
что в работах [25-28] обсуждается возможное влия-
низких и комнатных температурах, а также методом
ние метана, выделяющегося при разложении газовых
ртутной порометрии [7-15]. Часто в ряду увеличения
гидратов, а также метана, находящегося в виде твер-
степени метаморфизма природного угля обнаружива-
дого раствора в угле, на газодинамические явления
ется U-образная зависимость [15, 16] сорбционной
в краевой зоне угольных пластов. В работах [19, 29]
емкости углей, причем низкая сорбционная емкость
показано, что для образцов угля в ряду метаморфизма
углей средних степеней метаморфизма обусловлена
сорбционная емкость по воде и диоксиду углерода
в основном наполненностью пор смолистыми веще-
монотонно зависит от содержания кислорода в орга-
ствами, выделяющимися при превращениях уголь-
нической массе, а количество прочносвязанной воды
ного вещества.
линейно зависит от концентрации поверхностных
Для процессов коксования существенное значе-
функциональных групп угля.
ние имеет количество свободной и связанной воды
От текстуры пор и внутреннего пространства угля
[16-22], содержащейся в образцах природного угля.
зависит диффузионная проницаемость угля, которую
Присутствие воды в угле изменяет его сорбционные
можно определить по скорости насыщения угля во-
и фильтрационные свойства. Бурые угли в естествен-
дой. Сорбция углем молекул воды [7-9, 20, 21] вклю-
ном состоянии содержат от 20 до 60 мас% влаги, что
чает следующие стадии: молекулярную диффузию
существенно снижает эффективность их сжигания и
воды в газовой фазе через крупные поры, кнудсе-
соответственно затрудняет их использование в виде
новскую диффузию через мезопоры, поверхностную
топлива. Для каменных углей и антрацитов макси-
диффузию молекул внутри сорбированного слоя и
мальное количество сорбированной воды составляет
диффузию через микропоры. Величина эффективного
5-10 мас%. Свойства сорбированной углем воды из-
коэффициента диффузии определяется самой медлен-
учаются методами ЯМР [17-20] и адсорбционными
ной стадией, лимитирующей скорость насыщения
методами [20, 21]. Чтобы описать изотерму сорбции
угля водой. Коэффициент диффузии воды в маломе-
воды на углеродных материалах [20, 21], применяют,
таморфизованных углях меньше [20, 21], чем в углях
в частности, модель Дента, позволяющую разделить
с более высокой степенью метаморфизма.
вклад сорбционных центров двух типов, различа-
В представленной работе для образцов угля в ряду
ющихся энергией взаимодействия сорбент-сорбат
метаморфизма проведен технический и петрографи-
[16-22]. Центрами первого типа, с высокой энергией
ческий анализ, определена концентрация поверх-
связи (47-54 кДж·моль-1), являются гидрофильные
ностных функциональных групп. Методами низко-
участки поверхности угля, такие как кислородсодер-
температурной сорбции азота, ртутной порометрии
жащие функциональные группы типа СО, СООН,
изучены сорбционные свойства углей, для этих же
OH. Согласно современным представлениям, эти
углей измерены количественные и кинетические за-
функциональные группы угля находятся на перифе-
кономерности сорбции воды. Наиболее интересным
рии макромолекул, тем самым формируя полярную
из полученных результатов является продемонстри-
поверхность микро- и мезопор угольного вещества.
рованная для всего ряда образцов зависимость сорб-
Адсорбированную на этих центрах воду и называ-
ционной емкости угля от типа сорбата.
ют прочносвязанной. Поверхность прочносвязанной
воды может сорбировать дополнительные порции
Экспериментальная часть
воды и выступает в качестве центров сорбции второго
типа. Такая вода называется слабосвязанной и харак-
На угольных шахтах Кузбасса отобраны образ-
теризуется энергией (44-47 кДж·моль-1), близкой к
цы каменных углей разной степени метаморфизма.
теплоте конденсации воды в жидкость [17-21].
На шахте им. А. Д. Рубана отобран длиннопламен-
Свойства связанной углями воды существенно
ный уголь (Д), на шахте им. С. М. Кирова и шахте
отличаются от свойств объемной воды. Так, в ра-
им. 7 Ноября отобраны образцы газового угля, ко-
ботах [23-26] для нескольких образцов природного
торым в настоящей работе присвоены коды (Гк) и
угля изучено влияние типа адсорбированной воды
(Гн), на шахте Усковская отобран уголь марки газо-
на способность этой воды образовывать газовые ги-
вый-жирный (ГЖ), шахте Костромовская — жирный
драты. Показано, что образовывать гидраты может
(Ж), шахте Первомайская — коксующийся (К), на
только слабосвязанная вода. Интересно отметить,
угольном предприятии Сибэнергоуголь отобраны об-
1322
Смирнов В. Г. и др.
разцы тощего (Т) угля и антрацита (А). Отобранные
ли в пластиковые бюксы и переносили в эксикаторы
образцы в лабораторных условиях высушивали на
с заданной величиной парциального давления паров
воздухе в течение 2-3 дней, затем измельчали и рас-
воды. Значение относительной влажности воздуха
сеивали по размерам частиц. Для аналитических
задавали насыщенным водно-солевым раствором,
исследований (технический анализ, анализ функ-
помещенным в каждый эксикатор: Na2CO3 — 0.91,
циональных групп на поверхности угля и азотная
KCl — 0.84, NaCl — 0.75, KI — 0.69, MnCl2 — 0.56,
порометрия) использовали фракцию 0.063-0.250 мм.
NaI — 0.38, CaBr2 — 0.17, дистиллированная во-
В остальных экспериментах использовалась фрак-
да — 1.00, здесь цифры соответствуют равновесному
ция 1.0-2.0 мм. В табл. 1 приведены результаты тех-
значению относительной влажности над насыщен-
нического анализа углей, взятых для исследования.
ным раствором данной соли. Содержание воды в
Содержание общей золы Ad в расчете на сухую массу
углях определяли по изменению массы образцов.
угля определяли в соответствии с ГОСТ 12596-67.
Взвешивание производили раз в 12 ч в первые трое
Образцы угля после взвешивания помещали в му-
суток, затем раз в сутки и далее раз в несколько суток.
фельную печь, остаток дожигали до постоянной мас-
Эксикаторы находились при постоянной температуре
сы при 800 ± 25°С и затем взвешивали. Содержание
27 ± 2°С на протяжении всего исследования, точность
летучих веществ в каждой марке угля определяли
взвешивания составляла 0.01% массы. На рис. 1 точ-
в соответствии с ГОСТ 6382-2001. Образец угля
ками показаны значения влажности образцов угля,
известной массы нагревали без доступа кислоро-
установившиеся после выдержки 3-5 мес в эксика-
да воздуха до температуры 900°С в течение 7 мин.
торах, т. е. за время, достаточное для достижения
Выход летучих (Vdaf, %) рассчитывали как потерю
постоянной массы.
массы образца за минусом потери массы при сушке.
Элементный состав (Cdaf, Hdaf) определяли в CHNS-
Обсуждение результатов
анализаторе ThermoFlash2000. Содержание кислорода
и азота рассчитывали по разности общей массы и
Результаты исследования свойств углей суммиро-
массы углерода, водорода и серы. Содержание об-
ваны в табл. 1 и 2. Образцы угля в табл. 1 расположе-
щей серы определяли согласно ГОСТ 8606-93 (ИСО
ны в порядке увеличения степени метаморфизма от
334-92) «Определение общей серы. Метод Эшка».
молодых к зрелым углям. В этом ряду увеличивается
Содержание поверхностных групп угля проводилось
содержание углерода, уменьшается содержание кис-
с использованием следующих процедур: карбониль-
лорода и водорода, падает выход летучих веществ.
ных — по реакции с гидрохлоридом гидроксиламина,
Величина зольности углей имеет малую корреляцию
карбоксильных — используя ацетатный метод, сумму
со степенью метаморфизма.
карбоксильных и гидроксильных групп — посред-
Содержание реакционноспособного кислорода
ством ионного обмена с гидроксидом натрия.
(Or, табл. 2) определяли как сумму кислорода в форме
Для каждого образца природного угля измеря-
фенольных, карбонильных и карбоксильных групп,
ли изотермы сорбции и десорбции азота при 77.4 K
детектируемых на поверхности угля. Исходя из кон-
(-195.75°C) на приборе ASAP-2020, оборудованном
центрации функциональных групп, выраженной в
вакуумной установкой. Адсорбционные и десорб-
мг-экв·г-1 (на сухую обеззоленную массу угля daf),
ционные измерения проводили в интервале относи-
рассчитали количество кислорода (мг·г-1; daf), нахо-
тельных давлений p/p0 = 10-3-0.995. Ртутная пороме-
дящегося в этих функциональных группах (табл. 2).
трия образцов угля проведена на приборе AutoPoreIV
Для образцов угля разной степени метаморфизма
9500 (Micromeritics Instruments Corporation, USA)
обычно наблюдается линейная связь между количе-
при давлениях ртути Hg 0.1-60000 psi (0.0007-
ством реакционного и общим количеством кислорода
414 МПа) и при комнатной температуре. Метод
[29].
основан на уравнении Юнга-Лапласа, устанавли-
Результаты, полученные при исследовании углей
вающем зависимость от давления нагнетания (ΔР)
методами азотной и ртутной порометрии, суммирова-
радиуса пор (rp), в которые проникает жидкость,
ны в табл. 3. Для всех образцов угля вблизи значения
характеризующаяся поверхностным натяжением
p/p0 = 1.0 ветви изотерм сорбции азота круто подни-
маются вверх. Объем пор образцов угля (табл. 3, V0.99,
(γ) и краевым углом смачивания (θ):
V0.91) рассчитан как объем адсорбированного азота
Для построения изотермы сорбции воды навески
при относительном давлении паров 0.99 и 0.91 при
угля в течение 6 ч высушивали в вакууме при 110°С,
допущении, что плотность азота в сорбированном
затем охлаждали до комнатной температуры, помеща-
состоянии равна плотности жидкого азота. На основе
Физико-химические и сорбционные свойства образцов природного угля различной степени метаморфизма
1323
Таблица 1
Технический анализ образцов угля, взятых для исследования
Зольность
Выход летучих
Масса углерода
Масса водорода
Сера аналитическая
Кислород + азот
Уголь, код
Ad,%
Vdaf, %
Cdaf, %
Hdaf, %
Sа, %
O + N, %
Д
9.8
42.8
80.11
5.46
0.22
14.21
Гк
3.3
43.6
80.58
5.41
0.51
13.50
Гн
5.3
44.1
84.80
5.74
0.46
9.00
ГЖ
8.6
38.5
82.71
5.34
0.39
11.56
Ж
6.5
37.9
85.57
5.74
0.58
8.11
К
5.1
20.5
89.66
5.08
0.58
4.68
Т
16.9
6.9
92.88
3.76
0.57
2.79
А
13.0
6.5
93.10
3.69
0.87
2.34
изотерм сорбции азота (N2, Vp) методом Брунауэра-
соответствует диапазон пор, определенный методом
Эммета-Теллера (БЭТ) рассчитана площадь по-
БДХ), а также 0.1-10.0 и 10-300 мкм. Диапазоны
верхности пор (SБЭТ), приведенная в табл. 3, здесь
размеров указаны индексами у символа объема (V) в
же указана константа БЭТ (CБЭТ). Метод Барретта-
заголовках столбца. Ртутная порометрия применима
Джойнера-Халенды (БДХ) использовался для расчета
для определения пор диаметром от 3 нм до 200 мкм,
объема мезопор (VБДХ), в табл. 3 приведено значение,
однако заполнение ртутью мелких пор, размером
рассчитанное по десорбционной ветви. Объем ми-
менее 0.01 мкм, происходит при давлении 100 МПа
кропор, рассчитанный t-методом Хелси, имеет пре-
и выше, при таком давлении возможна деформация
небрежимо малое значение (< 0.0001 см·г-3), поэтому
стенок пор и разрушение внутренних перегородок
в табл. 3 не указан. В табл. 3 помещены данные по
в природном угле. Исследуемый образец вакуумиро-
измерению объема пор угольных образцов методом
ван, и давление газа внутри пор отсутствует, в этом
ртутной порометрии (Hg, Vp), разделенные на диа-
случае при давлении жидкой ртути, равном атмос-
пазоны размеров 0.002-0.10 мкм (этому диапазону
ферному, заполняются поры радиусом 7.6 мкм. Более
Таблица 2
Кислородсодержащие функциональные группы исследуемых углей
Концентрация функциональных групп
Кислород в функциональных группах
(на сухую обеззоленную массу угля), мг-экв·г-1
(на сухую обеззоленную массу угля), мг·г-1
Уголь, код
COOH
CO
COOH + OH
COOH
CO
COOH + OH
Д
—
0.259
0.154
2.07
2.46
Гк
0.010
0.217
0.137
0.32
1.74
2.19
Гн
—
0.090
0.090
0.72
1.44
ГЖ
—
0.135
0.074
1.08
1.18
Ж
—
0.128
0.060
1.02
0.96
К
< 0.01
0.101
0.036
< 0.32
0.81
0.58
Т
< 0.01
0.172
0.050
< 0.32
1.38
0.80
А
< 0.01
0.109
0.047
< 0.32
0.87
0.75
1324
Смирнов В. Г. и др.
низкое давление ртути позволяет определить рас-
пределение по размерам макропор, а при высоком
давлении ртути изучается распределение по размерам
микропор.
Известно, что в модели Дента [20, 21] количе-
ство воды, адсорбированной на центрах первого
(m1 — прочносвязанная вода) и второго (m2 — слабо-
связанная вода) типов, а также общее количество
сорбированной воды m = m1 + m2, отнесенные к сор-
бционной емкости монослоя m0, описываются урав-
нениями
(1)
(2)
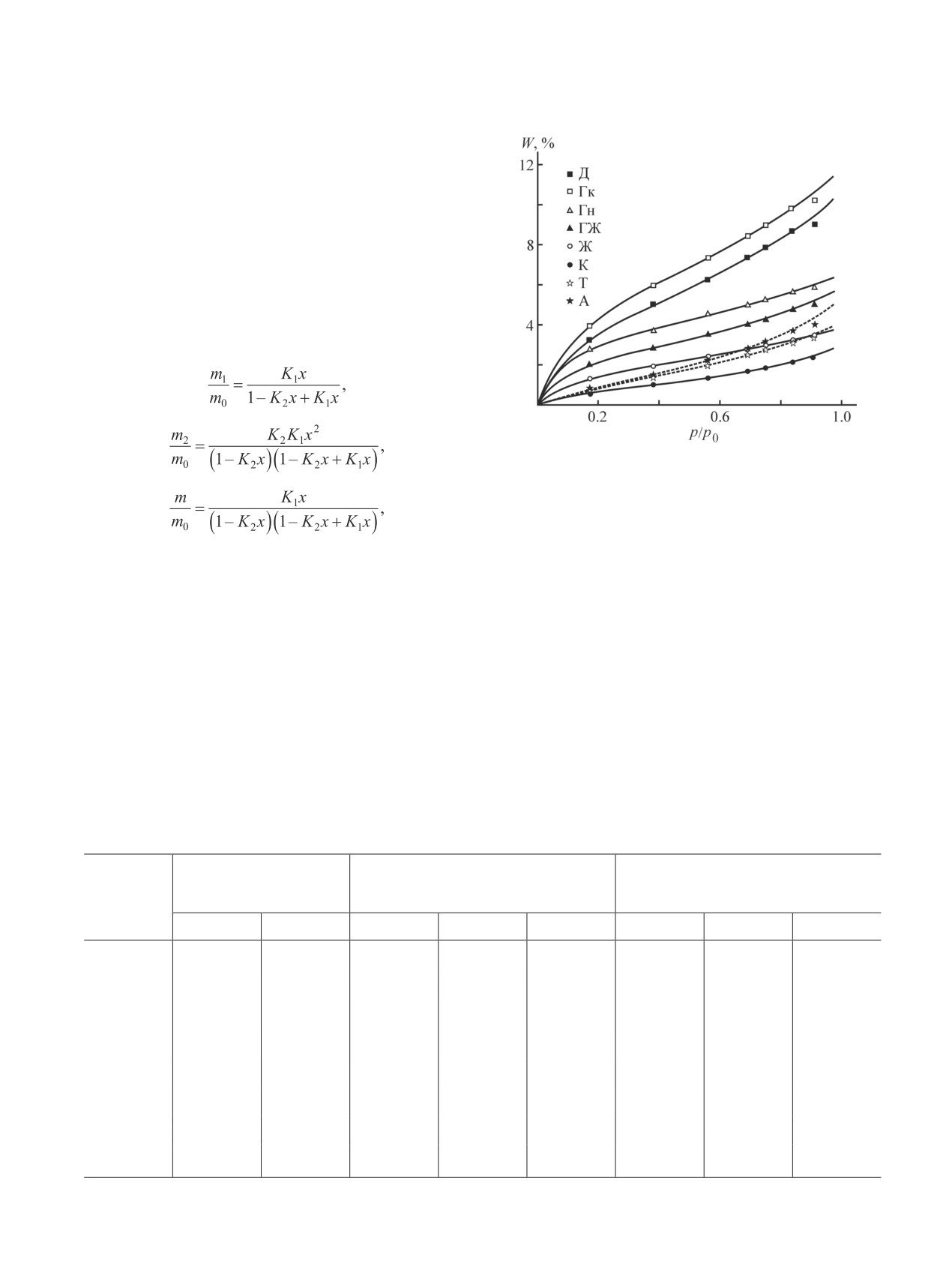
Рис. 1. Изотермы сорбции воды образцами природного
угля.
(3)
Точки — экспериментальные данные, сплошные и пун-
ктирные линии — аппроксимация по изотерме Дента.
где x = p/p0 — относительное парциальное давление
Экспериментальные точки на изотермах сорбции
паров воды.
воды (рис. 1) в интервале относительной влажности
Значения K1 и K2 позволяют оценить энергию ад-
воздуха 0-0.84 для каждого образца природного угля
сорбции молекул воды на центрах первого (E1) и
аппроксимировали теоретическим уравнением (3),
второго (E2) типа в сравнении с энергией (EL) кон-
для чего подбирали константы K1 и K2, а также вели-
денсации молекул воды, находящихся в объеме жид-
чину емкости монослоя m0. Рассчитанные изотермы
кости:
сорбции показаны на рис. 1 сплошными и пунктир-
ными линиями. При приближении относительной
ΔE1 = E1 - EL = (RT/M)lnK1,
(4)
влажности воздуха к значению p/p0 = 1 объем сорби-
ΔE2 = E2 - EL = (RT/M)lnK2.
(5)
рованной воды для каждого из образцов стремится
Таблица 3
Результаты анализа текстуры пор исследуемых углей
Объем сорбированного углем азота
Измеренный ртутной порометрией объ-
Сорбция азота,
при разном парциальном давлении паров
ем пор, см3·г-1, имеющих размеры, мкм,
метод БЭТ
Уголь, код
и рассчитанный методом БДХ, см3·г-1
в указанном диапазоне
SБЭТ, м2·г-1
СБЭТ
V0.99
V0.91
VБДХ
V0.002-0.1
V0.1-10.0
V10-300
Д
2.282
76.56
0.0049
0.0030
0.0047
0.0546
0.0175
0.0474
Гк
0.570
23.94
0.0019
0.0010
0.0020
0.0490
0.0096
0.0393
Гн
0.228
-218.9
0.0014
0.0003
0.0014
0.0397
0.0059
0.0522
ГЖ
1.480
87.80
0.0047
0.0023
0.0047
0.0427
0.0201
0.0960
Ж
0.550
65.38
0.0023
0.0010
0.0023
0.0248
0.0091
0.1855
К
0.558
-6755.8
0.0019
0.0007
0.0017
0.0433
0.0040
0.1621
Т
2.853
99.90
0.0050
0.0031
0.0039
0.0436
0.0084
0.0868
А
2.134
87.84
0.0051
0.0026
0.0045
0.0446
0.0089
0.0883
Физико-химические и сорбционные свойства образцов природного угля различной степени метаморфизма
1325
Таблица 4
Расчетные значения коэффициентов изотермы Дента
Разница энергии
Параметры сорбции, %,
Константы Дента:
сорбции на угле для
Удельная
при p/p0 =1.0: m0 — емкость монослоя,
K1 - для прочно-,
ΔE1 — прочно-,
площадь
m — масса сорбированной воды,
Уголь,
K2 — для
ΔE2 — слабосвязанной
поверхности
m1, m2 — массы прочно- и слабосвязанной
код
слабосвязанной воды
воды и энергии испарения
пор
воды
жидкой воды, кДж·моль-1
SSAH2O,
м2·г-1
m0
m
m1
m2
K1
K2
ΔE1
ΔE2
Д
5.13
10.61
4.81
5.80
6.96
0.546
4.84
-1.51
180
Гк
6.13
11.73
5.75
5.98
7.41
0.510
5.00
-1.68
215
Гн
3.71
6.50
3.54
2.96
11.39
0.455
6.07
-1.96
130
ГЖ
2.63
5.85
2.53
3.32
11.22
0.567
6.03
-1.41
92
Ж
2.03
3.86
1.91
1.95
7.23
0.508
4.93
-1.69
71
K
0.98
3.00
0.93
2.07
5.56
0.691
4.28
-0.92
34
T
1.92
4.13
1.66
2.47
2.62
0.597
2.39
-1.29
67
A
1.85
5.32
1.68
3.64
3.05
0.685
2.79
-0.94
65
к конечному пределу, который мы принимаем как
ние БЭТ. Полученные значения SSAH2O по порядку
максимальное количество сорбированной воды.
величины близки к ранее рассчитанным на основе
В табл. 4 приведены значения констант уравнения
экспериментальных изотерм сорбции воды методом
Дента K1, K2, сорбционная емкость монослоя воды на
БЭТ и из емкости монослоя в уравнении Дента [20,
поверхности пор m0, а также: m = m1 + m2 — общее
21].
количество воды, выраженное в процентах от массы
По скорости насыщения угля водой определяли
угля; m1 — количество воды, сорбированной на цен-
эффективный коэффициент диффузии молекул воды
трах первого типа, m2 — количество воды на центрах
внутри частиц природного угля. Кривые зависимости
второго типа, рассчитанные по изотерме Дента при
влажности образцов угля от времени содержали ли-
p/p0 = 1; ΔE1 и ΔE2 — рассчитанная по формулам (4),
нейный участок на начальном этапе после помещения
(5) разность энергии сорбции воды на центрах пер-
угля в эксикатор с заданной влажностью воздуха, а за-
вого и второго типа и теплоты конденсации воды в
тем, через 150-200 ч выходили на этап насыщения, на
жидкое состояние. Площадь поверхности пор SSAH2O
котором практически прекращалось изменение массы
вычислена формуле
образцов угля. При изучении процесса насыщения во-
дой частицы природного угля (0.5-1.0 мм) принимали
SSAH2O = ωH2O(m0/M)Na
гомогенными и сферическими со средним значением
диаметра 0.75 мм. Экспериментальную зависимость
исходя из полученных значений сорбционной емко-
влажности от времени q(t) аппроксимировали функ-
сти монослоя воды m0 в предположении, что моле-
цией, являющейся решением нестационарного урав-
кулы воды расположены в один слой и минималь-
нения Фика, которое для сферически симметричных
ная площадь, занимаемая одной молекулой, равна
частиц записывали в следующем виде:
ωH2O =0.105 нм2 [7-9], M — молярная масса воды,
Na — число Авогадро. Величину SSAH2O можно от-
(6)
нести к поверхности пор образцов угля по аналогии
с расчетом поверхности сорбентов методом БЭТ, ко-
торый широко применяется при анализе, например
В начальный период, когда
где q(t),
[7-9, 20, 21], изотерм сорбции азота и расчете удель-
ной поверхности твердых тел, а уравнение Дента
q0 — текущая и равновесная влажность, решение
(3), если положить K2 = 1, превращается в уравне-
уравнения (6) аппроксимировали [8] выражением
1326
Смирнов В. Г. и др.
Таблица 5
Коэффициент диффузии исследуемых образцов угля
Эффективный
Коэффициент диффузии
Расчетная константа
Среднеквадратичное
Уголь,
коэффициент диффузии
молекул воды через уголь,
уравнения (7)
отклонение
код
De, 10-6, c-1
D, 10-14, м2·c-1
B, 10-3, с-1/2
ΔB, 10-3, с-1/2
Д
0.216
3.04
0.465
0.014
Гк
0.162
2.27
0.402
0.019
Гн
0.235
3.30
0.485
0.030
ГЖ
0.361
5.08
0.601
0.019
Ж
0.308
4.33
0.555
0.007
T
0.460
6.46
0.678
0.028
материалы [8], имеющие молекулярно-ситовые свой-
(7)
ства.
Данные технического анализа углей, а также со-
держание в органической массе углерода, водорода
Начальный этап изменения влажности угля сразу
и кислорода, выход летучих соответствуют маркам
после помещения в один из восьми эксикаторов с
образцов угля, взятых для исследования. Вместе
заданным значением влажности воздуха аппрокси-
с тем результаты исследования текстуры пор при-
мировали уравнением (7) и рассчитали константу B.
родных углей стандартными методами, такими как
В табл. 5 для каждого образца угля приведено зна-
низкотемпературная сорбция азота, сорбция воды
чение константы B, усредненное по результатам из-
при комнатной температуре и ртутная порометрия,
мерения во всех эксикаторах, а также ΔB — сред-
существенно различны для разных методов исследо-
неквадратичное отклонение от среднего значения.
вания (рис. 2). Известно [7-9], что для многих твер-
Для каждого образца угля вычислен эффективный
дых тел кумулятивные кривые распределения пор
коэффициент диффузии e
в который вхо-
по размерам, построенные по результатам низкотем-
дит D — усредненный коэффициент диффузии воды
пературной сорбции азота и ртутной порометрии,
через угольное вещество и r — размер частиц.
С увеличением степени метаморфизма исследу-
емых углей (табл. 5) коэффициент диффузии D воз-
растает. По величине коэффициента диффузии можно
сделать вывод о типе физических взаимодействий,
которые определяют процесс диффузии. Насыщение
природного угля водой происходит в несколько ста-
дий, включающих диффузию паров воды в крупных
порах, кнудсеновскую диффузию и диффузию в слое
сорбированных молекул в мезопорах, а также диффу-
зию молекул через микропористую сплошную среду.
Эффективный коэффициент диффузии определяется
самыми медленными стадиями, которыми являются
[8] диффузия в микропорах и поверхностная диффу-
зия в слое сорбированных молекул. Коэффициенты
диффузии разных типов различаются на несколько
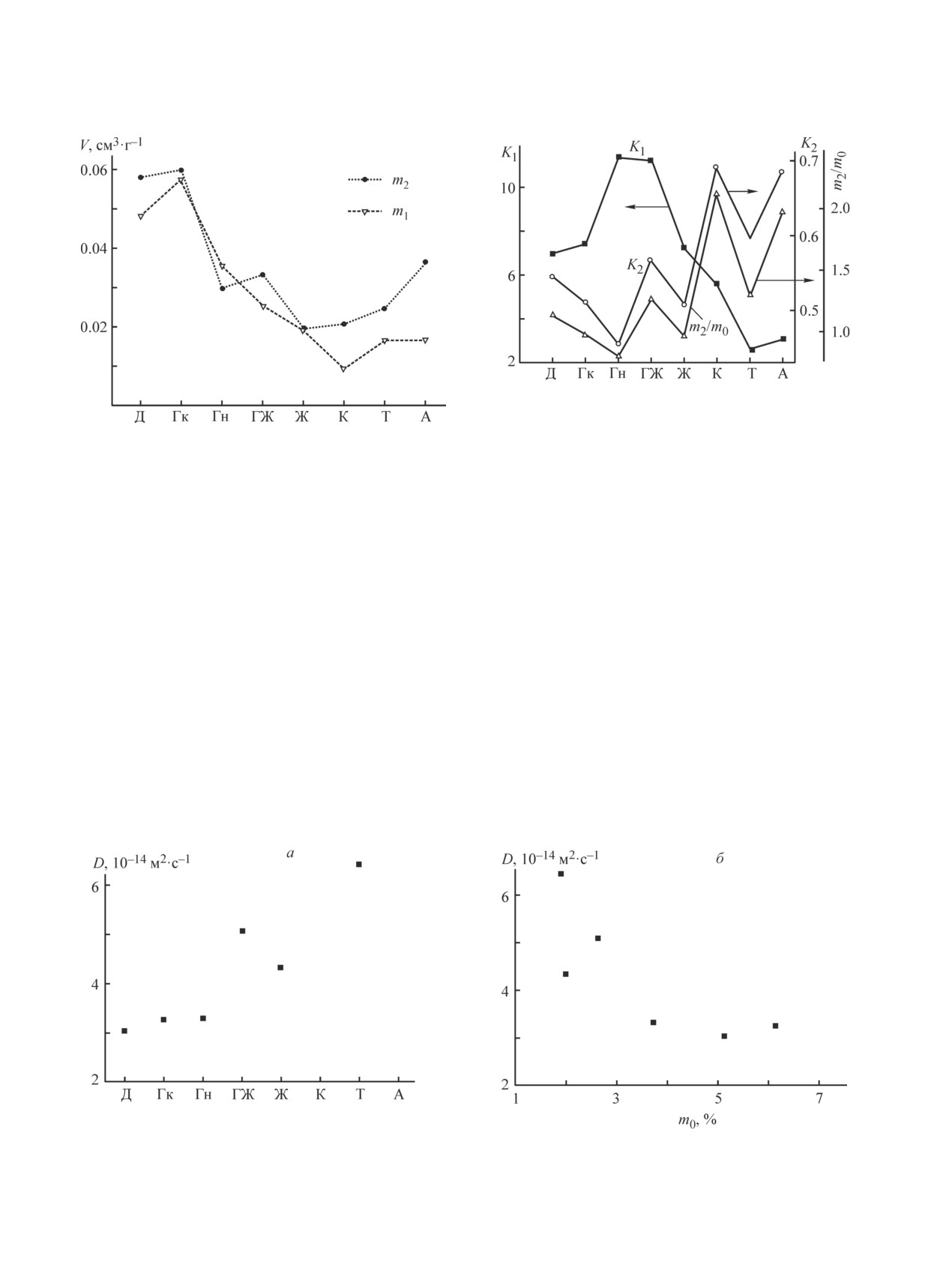
Рис. 2. Сравнение максимального объема сорбирован-
порядков, поэтому достаточно уверенно идентифици-
ной воды, объема ртути, заполняющей поры размером
руется характер диффузии. В нашем случае получен-
0.002-10 мкм, объема сорбированного азота при от-
ные значения коэффициента диффузии соответствуют
носительном давлении паров 0.99 для исследованных
диффузии воды через микропористые углеродные
образцов угля.
Физико-химические и сорбционные свойства образцов природного угля различной степени метаморфизма
1327
плотные графитоподобные кристаллиты, на поверх-
ность которых вытесняются кислородсодержащие
функциональные группы и алифатические цепочки,
образующие менее плотные фрагменты структуры с
большим количеством микро- и мезопор, имеющих
мягкие стенки и входы, за счет чего поры способны
«дышать». Кроме того, наличие на стенках этих пор
полярных функциональных групп делает возможной
их различную реакцию на появление сорбата с раз-
ной полярностью. В целом свойства такой структуры
зависят от условий, в которых находится уголь, и от
природы сорбата.
При измерениях методом сорбции азота использу-
ется неполярный сорбат, сами измерения проводят-
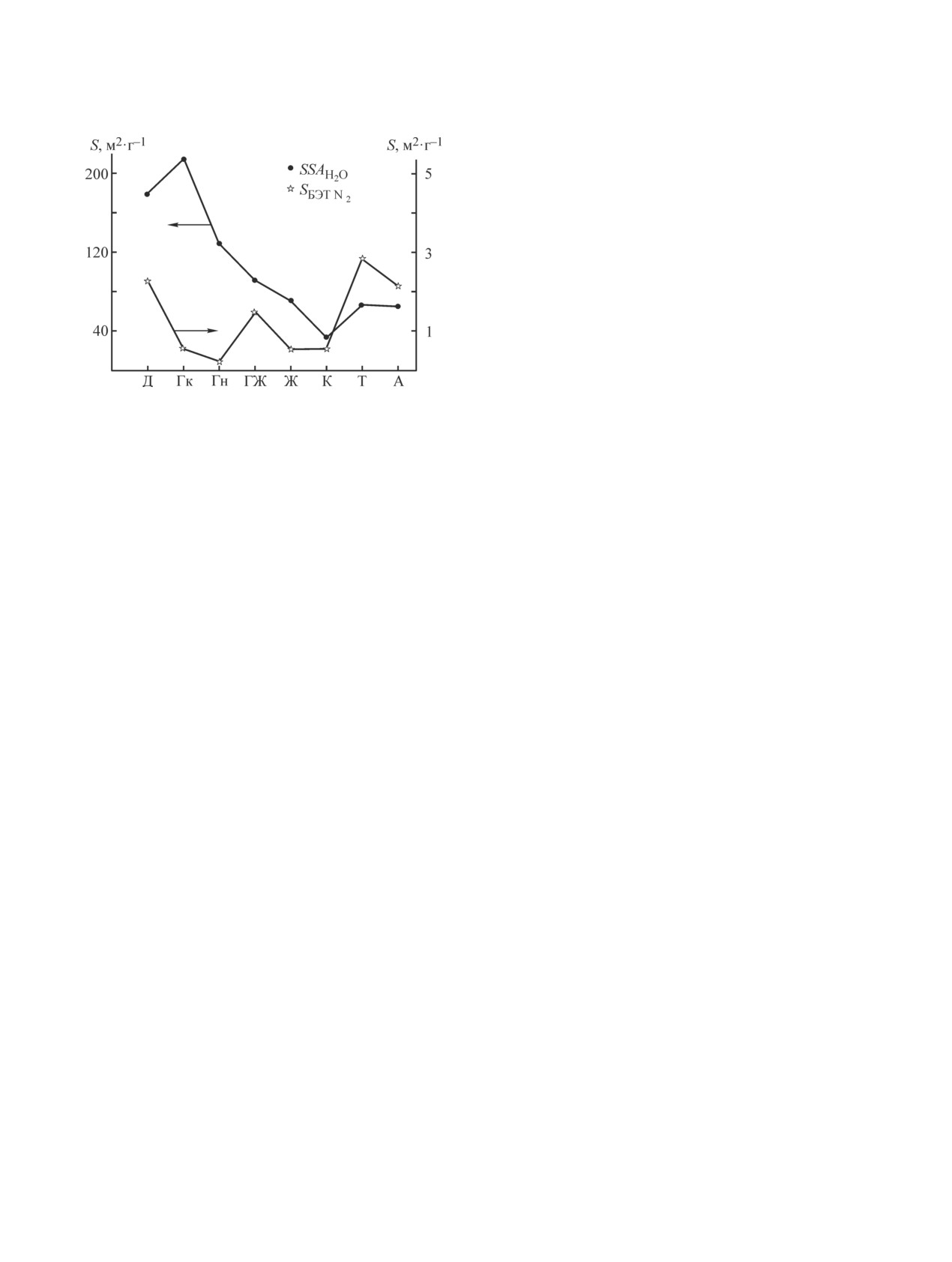
Рис. 3. Удельная поверхность пор, рассчитанная из изо-
ся при криогенных температурах. В этих условиях
терм сорбции воды и из изотерм сорбции азота для
исследованных образцов угля.
«дышащая» часть структуры угольного вещества
застывает, имеющиеся на стенках пор полярные
функциональные группы предпочтительно взаимо-
совпадают. В нашем случае для всех образцов угля
действуют между собой, не давая поре раскрыть-
объем азота, сорбированного при давлении паров
ся. За счет этого существенная доля пористости не
0.99, примерно на порядок меньше объема сорбиру-
обнаруживается, измеряемый объем пор оказыва-
емой воды и объема ртути, заполняющей поры разме-
ется заниженным. При ртутной порометрии проис-
ром 0.002-0.1 мкм, т. е. микро- и мезопоры (рис. 2).
ходит нагнетание жидкой ртути в мезо- и микропо-
Объемы сорбированной воды и вошедшей в поры
ры природного угля под давлением, достигающим
ртути значительно ближе по величине. Для углей
сотни МПа, эксперимент проводится при обычных
малой степени метаморфизма (длиннопламенный Д,
температурах. Происходит деформация стенок пор,
газовый Г) объем сорбированной воды в 1.4-2.0 раза
разрушение внутренних перегородок, частично от-
больше объема ртути, заполняющей поры, а для бо-
крывается доступ к закрытой пористости углей. Под
лее метаморфизованных углей объем ртути близок к
действием высоких механических напряжений воз-
объему воды или даже превосходит его. Более значи-
можно уплотнение рыхлого вещества, прилегающего
тельные различия наблюдаются для величин площади
к стенкам пор. Все эти процессы могут приводить к
поверхности пор (рис. 3), вычисляемых из емкости
завышению значений объема пор, измеренного ме-
монослоя, рассчитанного методами БЭТ (сорбция
тодом ртутной порометрии, в сравнении с реальным
азота) и Дента (сорбция воды). Для углей низкой сте-
объемом пор. Вместе с тем сорбат и в данном случае
пени метаморфизма определенная по сорбции воды
неполярный, соответственно не способен заполнять
площадь поверхности пор на два порядка выше, чем
внутреннее пространство «дышащих» пор, закрытое
определенная по сорбции азота. Для углей с высокой
состояние которых стабилизировано взаимодействи-
степенью метаморфизма различие в значениях пло-
ем имеющихся на их стенках полярных функциональ-
щади, измеренной этими способами, снижается, но
ных групп. В случае сорбции воды все имеющиеся
все равно превосходит один порядок величин.
полярные группы угля эффективно гидратируются.
Рассмотрим возможные причины необычных со-
Молекулы воды занимают существующие и генериру-
рбционных свойств природных углей. Для такого
ют новые микропоры, деформируя участки угольной
рода сорбентов существенные различия в характе-
бахромы. Тепловые колебания молекул стенок пор
ристиках текстуры пор, измеряемых при комнатной
обеспечивают периодическое увеличение размеров
температуре, при температуре жидкого азота, а также
пор, что облегчает доступ во внутреннее простран-
методом ртутной порометрии могут быть связаны с
ство угля при комнатной температуре. Чем более раз-
особенностями их строения, в частности отсутстви-
вита бахрома угольных молекул и больше дипольный
ем жесткого каркаса сорбента и существенно разной
момент поверхности угля, тем выше энергия сорбции
химической природой различных структурных фраг-
первых слоев воды, ниже коэффициент диффузии
ментов. Уголь является природным углеводородным
и больше максимальное количество воды, которое
полимером нерегулярного строения, внутри которого
может сорбировать уголь из воздуха. Все рассмо-
ароматические участки формируют относительно
тренные факторы и приводят к различию объемов
1328
Смирнов В. Г. и др.
пор, определенных по сорбции воды и методом ртут-
зициях. В свою очередь емкость монослоя проявляет
ной порометрии (рис. 2). В углях с низкой степенью
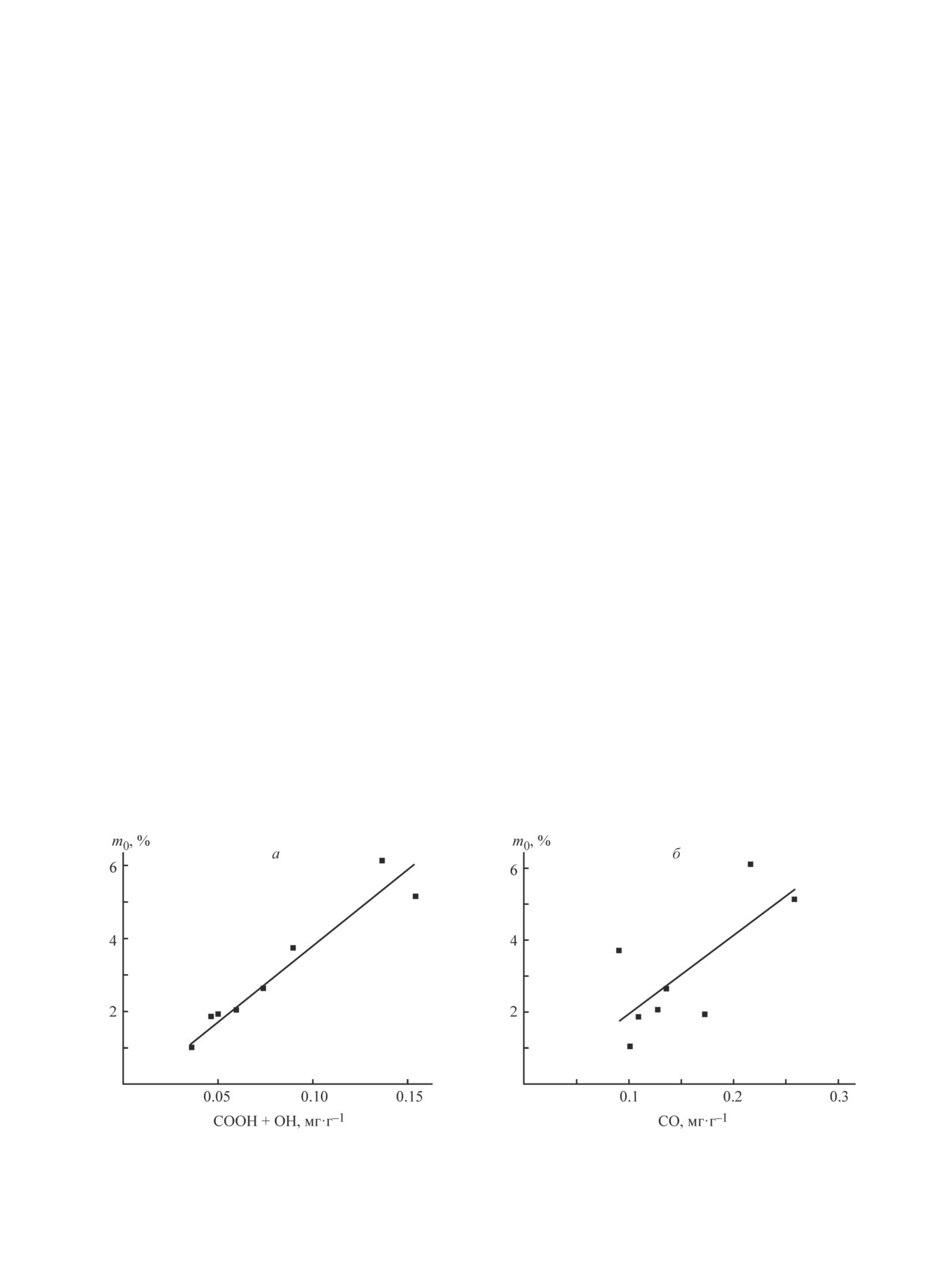
высокую степень корреляции (R2 = 0.93) с концен-
метаморфизма имеется большое количество поляр-
трацией кислородсодержащих групп СООН + ОН
ных функциональных групп, что благоприятствует
(рис. 4, а) и не очень высокую корреляцию (R2 = 0.45)
сорбции воды. При вдавливании ртути значительная
с группами СО (рис. 4, б). Таким образом, количество
часть потенциальной пористости не проявляется.
сорбированной воды напрямую связано с содержа-
При повышении степени метаморфизма в угольном
нием кислорода в органической массе угля и кон-
веществе появляется все больше гидрофобных пор,
центрацией карбоксильных и гидроксильных групп,
в которых вода не сорбируется. Объем пор, опреде-
которые формируют активные сорбционные центры
ленный методом ртутной порометрии, становится
первого типа. Это соответствует литературным дан-
равен или даже превышает объем, определенный
ным [17-19, 22].
по сорбции воды. Подобным образом можно объяс-
Представленный на рис. 2 объем сорбированной
нить и наблюдаемые особенности определенной раз-
воды в соответствии с выполненными в табл. 4 рас-
ными методами удельной поверхности пор (рис. 3).
четами состоит из прочно- и слабосвязанной воды
Известно, что в общем случае площадь поверхности
(рис. 5). Для образцов угля марок: длиннопламенный,
пор пропорциональна сорбционной емкости моно-
газовый, жирный — объемы прочно- и слабосвязан-
слоя. Это полностью справедливо для сорбции азо-
ной воды примерно равны, а для углей коксовый,
та, однако, как отмечено выше, значительная часть
тощий, антрацит объем слабосвязанной воды в 1.5-
«дышащих» пор при этом не раскрывается. Вместе
2.2 раза превосходит объем прочносвязанной воды.
с тем сорбция «монослоя» воды происходит, строго
Данный результат можно соотнести со значительным
говоря, не на всей поверхности, а на имеющихся на
снижением доли кислородсодержащих функциональ-
этой поверхности функциональных группах, причем
ных групп в органической массе угля и на внутренней
при малых относительных давлениях воды часть пор
поверхности пор, а также с растущими размерами пор
здесь также может не раскрыться. Все это и приводит
у углей высокой степени метаморфизма.
к наблюдаемой на рис. 3 картине.
Логарифм коэффициентов K1 и K2, входящих в
Более детально рассмотрим результаты экспе-
уравнение Дента, определяет энергию связи молекул
риментов по исследованию изотерм сорбции воды.
сорбированной воды на центрах первого и второго
Прежде всего отметим, что рассчитанная с исполь-
типа (4), (5). В ряду исследованных углей коэффи-
зованием изотермы Дента емкость монослоя во всех
циент K1 имеет наименьшее значение у зрелых углей
случаях близка к количеству прочносвязанной воды
марок К, Т, А (рис. 6). Наибольшее значение K1 су-
(табл. 4). Это вполне ожидаемо, фактически и та и
щественно превосходит единицу и у углей марок Г и
другая величина соответствует количеству воды на
ГЖ достигает величин 11.2 и 11.4, что соответствует
заполняющихся в первую очередь сорбционных по-
энергии связи сорбированной воды, на 15% превосхо-
Рис. 4. Сорбционная емкость монослоя, сопоставленная с концентрацией кислородсодержащих функциональных
групп.
Физико-химические и сорбционные свойства образцов природного угля различной степени метаморфизма
1329
Рис. 6. Значения параметров уравнения Дента и отноше-
ния количества слабосвязанной воды к емкости монос-
лоя в ряду образцов угля разной степени метаморфизма.
Рис. 5. Сравнение количеств прочно- и слабосвязанной
воды на углях различного типа.
дящей энергию конденсации. Высокая энергия связи
нице, тем больше энергия сорбции и тем больше
в первом сорбированном слое уплотняет молекулы
количество воды, сорбированной на центрах второго
воды, нарушает их взаимную координацию, прису-
типа. Это соответствует тому, что профиль значений
щую жидкой воде. Это приводит к тому, что энергия
коэффициента K2 в ряду метаморфизма углей (рис. 6)
сорбции следующих слоев воды меньше, чем тепло-
имеет вид, аналогичный профилю m2/m0 — отно-
та конденсации, а коэффициент K2 меньше едини-
шения количества слабосвязанной воды к емкости
цы. Между коэффициентами K1 и K2 наблюдается
монослоя.
обратная корреляция: для образцов угля с высоким
По порядку величины абсолютное значение изме-
K1 значение K2 в среднем ниже, и, следовательно,
ренного коэффициента диффузии молекул воды во
меньше энергия сорбции молекул воды на центрах
внутреннем пространстве угля соответствует молеку-
второго типа. Чем ниже энергия сорбции, тем меньше
лярной диффузии через микропоры [7]. Коэффициент
количество воды, сорбируемой на центрах второго
диффузии молекул воды через уголь имеет наимень-
типа, отнесенное к емкости монослоя. Чем выше
шее значение для образцов угля марок Д, Гк, Гн, а
значение коэффициента K2, т. е. чем ближе он к еди-
у более зрелых углей марок ГЖ, Ж, Т коэффици-
Рис. 7. Коэффициент диффузии молекул воды через уголь в ряду метаморфизма углей (а) и сопоставленный с ем-
костью монослоя (б).
1330
Смирнов В. Г. и др.
ент диффузии выше примерно в 2 раза (рис. 7, а).
чины близко к значению коэффициента диффузии
Коэффициент диффузии имеет большую величину у
молекул воды через микропористые углеродные по-
образцов, которые сорбируют мало воды (рис. 7, б).
лимеры.
Это можно связать с тем, что для углей низкой сте-
пени метаморфизма значительную долю пористого
Финансирование работы
объема составляют микропоры, которые формируют-
ся линейными участками углеводородных цепочек,
Работа выполнена при поддержке проекта № 18
находящихся на периферии угольных макромолекул.
«Изучение физико-химических свойств гидратосо-
Увеличение доли микропористого объема приводит
держащих пород для развития дистанционных ме-
к росту среднего пути, проходимого молекулой воды
тодов обнаружения и характеристики природных
в процессе диффузии до мест сорбции. Полярные
скоплений газовых гидратов» комплексной програм-
кислородсодержащие функциональные группы, на-
мы фундаментальных исследований Сибирского от-
ходящиеся на поверхности угля, связывают молекулы
деления Российской академии наук.
воды, замедляя диффузию. Низкое значение коэф-
фициента диффузии измерено в углях с высоким
Конфликт интересов
выходом летучих веществ и высоким содержанием
кислорода.
Авторы заявляют об отсутствии конфликта инте-
ресов, требующего раскрытия в данной статье.
Выводы
Информация об авторах
У исследованных образцов угля в ряду метамор-
физма увеличивается доля углерода, снижается доля
Смирнов Вячеслав Геннадьевич, к. ф.-м. н., доцент,
кислорода и водорода в органической массе, умень-
шается выход летучих веществ. С увеличением сте-
Дырдин Валерий Васильевич, д.т.н., проф., ORCID:
пени метаморфизма угля снижается концентрация
кислородсодержащих функциональных групп на по-
Манаков Андрей Юрьевич, д.х.н., г.н.с., ORCID:
верхности угля, а также содержание кислорода в не-
активной форме. Это соответствует характеристикам
Федорова Наталья Ивановна, к.х.н., в.н.с.,
марок отобранных образцов угля.
Показано, что измеренные различными метода-
Шикина Надежда Васильевна, вед. инж., ORCID:
ми (сорбция азота, сорбция воды, ртутная пороме-
трия) объемы микро- и мезопор угля существенно
Исмагилов Зинфер Ришатович, чл.-корр. РАН,
различаются. В качестве возможной причины этого
обсуждается модель «дышащих» пор, заполнение
9216
которых сорбатом сильно зависит от его полярности
и температуры эксперимента.
Список литературы
Изотермы сорбции воды природным углем изме-
рены экспериментально и аппроксимированы уравне-
[1] Гюльмалиев А. М., Головин Г. С., Гладун Т. Г.
Теоретические основы химии угля. М. : Изд-во
нием Дента. Молодые угли марок Д и Г сорбируют до
МГГУ, 2003. С. 7-32.
10% воды, наименьшее количество воды сорбируют
[2] Русьянова Н. Д. Углехимия. М. : Наука, 2000. С. 17-
образцы марки К — 3%. Оценена энергия сорбция
59.
воды на центрах первого и второго типа. Центры
[3] Van Krevelen D. W. Coal: typology, physics, chemistry,
первого типа характеризуются высокой энергией со-
constitution. Amsterdam; London; New York; Tokyo:
рбции, которая для молодых углей марок Д, Г, ГЖ, Ж
Elsevier, 1993. 979 р.
на 240-340 кДж·кг-1, а для зрелых углей марок Т, А
[4] Исмагилов З. Р., Шикина Н. В., Журавлева Н. В.,
на 130-160 кДж·кг-1 больше, чем теплота конденса-
Потокина Р. Р., Теряева Т. Н., Керженцев М. А.
ции воды в жидкое состояние (2430 кДж·кг-1).
Пористая структура углей Усинского месторожде-
Рассчитанный по скорости насыщения образ-
ния Печорского угольного бассейна // ХТТ. 2014.
цов угля водой коэффициент диффузии воды в угле
№ 4. С. 3-11. DOI: 10.7868/S0023117714040057
монотонно увеличивается с ростом степени мета-
[Ismagilov Z. R., Shikina N. V., Kerzhentsev M. A.,
морфизма углей. Характерное значение коэффици-
Zhuravleva N. V., Potokina R. R., Teryaeva T. N.
ента диффузии D ≈ 4·10-14 м2·с-1 по порядку вели-
Porous structure of coals from the usinsk deposit in the
Физико-химические и сорбционные свойства образцов природного угля различной степени метаморфизма
1331
Pechora Coal Basin // Solid Fuel Chem. 2014. V. 48.
coal // J. Nat. Gas Sci. Eng. 2015. V. 22. P. 203-213.
N 4. P. 215-223. DOI: 10.3103/S0361521914040053].
[5] Улановский М. Л. Взаимосвязь свойств углей с из-
[16] Смирнов В. Г., Манаков А. Ю., Дырдин В. В.,
менением содержания водорода при углефикации
Хицова Л. М., Михайлова Е. С., Исмагилов З. Р.
// Кокс и химия. 2011. № 2. C. 2-9 [Ulanovskii M. L.
Термогравиметрический анализ десорбции влаги
Relation between coal properties and the change
из природных углей // Кокс и химия. 2017. № 10.
in hydrogen content on coalification // Coke and
C. 2-7 [Smirnov V. G., Dyrdin V. V., Manakov A. Y.,
Chem. 2011. V. 54. N 2. P. 33-39. DOI: 10.3103/
Khitsova L. M., Mikhaylova E. S., Ismagilov Z. R.
S1068364X11020074].
Thermogravimetric Analysis of Moisture Desorption
[6] Nie B., Liu X., Yang L., Meng J., Li X. Pore structure
from Coal // Coke and Chem. 2017. V. 60. N 10.
characterization of different rank coals using gas ad-
P. 375-379. DOI: 10.3103/S1068364X17100076].
sorption and scanning electron microscopy // Fuel.
[17] Tahmasebi A., Han Y., Yin F., Li X. A review on
2015. V. 158. P. 908-917. http://dx.doi.org/10.1016/j.
water in low rank coals: The existence, interaction
fuel.2015.06.050
with coal structure and effects on coal utilization //
[7] Грег. С., Синг К. Адсорбция, удельная поверх-
ность, пористость: Пер. с англ. 2-е изд. М.: Мир,
org/10.1016/j.fuproc.2012.09.051
1984. С. 13-37, 186-202, 261-294 [Gregg S. J.,
[18] McCutcheon A. L., Barton W. A., Wilson M. A.
Sing K. S. W. C. Adsorption, surface area and porosity.
Characterization of Water Adsorbed on Bituminous
2nd Ed. London: Acad. Press, 1982. 303 p.].
Coals // Energy & Fuels. 2003. V. 17. P. 107-112.
[8] Ruthven D. M., Farooq S., Knaebel K. S. Pressure
DOI: 10.1021/ef020101d
Swing Adsorption. USA: VCH Publ., 1994. P. 11-
[19] Norinaga K., Kumagai H., Hayashi Ju., Chiba T.
63.
Classification of Water Sorbed in Coal on the Basis of
[9] Фенелонов В. Б. Введение в физическую химию
Congelation Characteristics // Energy & Fuels. 1998.
формирования супрамолекулярной структуры ад-
сорбентов и катализаторов. 2-е изд. Новосибирск:
[20] Charrière D., Behra P. Water sorption on coals //
Изд-во СО РАН, 2004. С. 58-93, 299-324.
J. Colloid Interface Sci. 2010. V. 344. P. 460-467.
[10] Thommes M., Kaneko K., Neimark A. V., Olivier J. P.,
doi:10.1016/j.jcis.2009.11.064
Rodriguez-Reinoso F., Rouquerol J., Kenneth S. W.
[21] Švábová M., Weishauptová Z., Prˇibyl O. Water vapour
Sing. Physisorption of gases, with special reference to
adsorption on coal // Fuel. 2011. V. 90. P.1892-1899.
the evaluation of surface area and pore size distribu-
doi:10.1016/j.fuel.2011.01.005
tion (IUPAC Technical Report) // Pure Appl. Chem.
[22] Allardice D. J., Clemow L. M., Favas G., Jack-
2015. V. 87. N 9-10. P. 1051-1069. DOI: 10.1515/
son W. R., Marshall M., Sakurovs R. The character-
pac-2014-1117
isation of different forms of water in low rank coals
[11] Alexeev A. D., Vasylenko T. A., Ul′yanova E. V. Phase
and some hydrothermally dried products // Fuel. 2001.
states of methane in fossil coals // Solid State
2361(02)00339-3
org/10.1016/j.ssc.2004.03.034
[23] Smirnov V. G., Manakov A. Y., Ukraintseva E. A.,
[12] Cai Y., Liu D., Pan Z., Yao Y., Li J., Qiu Y. Pore struc-
Villevald G. V., Karpova T. D., Dyrdin V. V.,
ture and its impact on CH4 adsorption capacity and
Lyrshchikov S. Y., Ismagilov Z. R., Terekhova I. S.,
flow capability of bituminous and subbituminous coals
Ogienko A. G. Formation and decomposition of meth-
from Northeast China // Fuel. 2013. V. 103. P. 258-
ane hydrate in coal // Fuel. 2016. V. 166. P. 188-195.
[13] Kędzior S., Jelonek I. Reservoir parameters and macer-
[24] Smirnov V. G., Dyrdin V. V., Manakov A. Y., Rodiono-
al composition of coal in different Carboniferous litho-
va T. V., Villevald G. V., Ismagilov Z. R., Mikhai-
stratigraphical series of the Upper Silesian Coal Basin,
lova E. S., Malysheva V. Y. The formation of the cabon
Poland // Int. J. Coal. Geol. 2013. V. 111. P. 98-105.
dioxide hydrate from water sorbed by coals // Fuel.
[14] Frolkov G. D., Frolkov A. G. Correlation between the
fuel.2018.04.131
Sudden and Regular Releases of CoalBed Methane
[25] Дырдин В. В., Смирнов В. Г., Ким Т. Л., Мана-
and the Structures of the Organic Matter of Natural
ков А. Ю., Фофанов А. А., Картаполова И. С.
Coals // Solid Fuel Chem. 2011. V. 45. N 1. P. 7-11.
Изменение термодинамических параметров систе-
DOI: 10.3103/S0361521911010046
мы угольная матрица-газ-влага при сбросе давле-
[15] Liu H., Mou J., Cheng Y. Impact of pore structure on
ния и фазовых превращениях газогидратов // Изв.
gas adsorption and diffusion dynamics for long-flame
вузов. Физика. 2017. Т. 60. № 2. С. 8-15 [Dyrdin V. V,
1332
Смирнов В. Г. и др.
Smirnov V. G., Kim T. L., Manakov A. Yu., Fofanov A.
[27] Айруни А. Т. Прогнозирование и предотвращение
A., Kartopolova I. S. Thermodynamic changes in the
газодинамических явлений в угольных шахтах. М.:
coal matrix-gas-moisture system under pressure re-
Наука, 1987. С. 189-236.
lease and phase transformation of gas hydrates // Russ.
[28] Алексеев А. Д. Физика углей и горных процессов.
Киев: Наук. думка, 2010. C. 93-155.
[29] Nishino J. Adsorption of water vapor and carbon di-
org/10.1007/s11182-017-1063-1].
[26] Смирнов В. Г., Дырдин В. В., Манаков А. Ю.,
oxide at carboxylic functional groups on the surface
Ким Т. Л., Шепелева С. А. // Изв. вузов. Горн. журн.
2014. № 1. С. 128-135.
org/10.1016/S0016-2361(00)00136-8