Литийпроводящие твердые электролиты в системе Li7La3Zr2O12-Li5La3Nb2O12, синтезированные золь-гель методом
1543
Журнал прикладной химии. 2019. Т. 92. Вып. 12
УДК 544.6.018.462.4
ЛИТИЙПРОВОДЯЩИЕ ТВЕРДЫЕ ЭЛЕКТРОЛИТЫ В СИСТЕМЕ
Li7La3Zr2O12-Li5La3Nb2O12, СИНТЕЗИРОВАННЫЕ ЗОЛЬ-ГЕЛЬ МЕТОДОМ
© Е. А. Ильина, Е. Д. Лялин, Б. Д. Антонов, А. А. Панкратов
Институт высокотемпературной электрохимии Уральского отделения РАН,
620990, г. Екатеринбург, ул. Академическая, д. 20
E-mail: koksharova.zh@mail.ru
Поступила в Редакцию 5 августа 2019 г.
После доработки 8 сентября 2019 г.
Принята к публикации 27 сентября 2019 г.
Синтез твердых электролитов Li7-xLa3Zr2-xNbxO12 (x = 0.0-2.0) был проведен золь-гель методом,
в качестве одного из исходных соединений использовали Nb2O5. Предложенная методика синтеза по-
зволила снизить температуру и время отжига по сравнению с твердофазным методом синтеза с 1200
в течение 36 ч до 1150°C в течение 1 ч. В ходе работы было исследовано влияние допирования соедине-
ния Li7La3Zr2O12 по подрешетке Zr ниобием (Nb5+) на его кристаллическую структуру, морфологию и
электропроводность. Установлено, что полученные соединения с x > 0.1 являлись однофазными и име-
ли кубическую структуру Ia-3d. С помощью растровой электронной микроскопии изучены морфология
и размер зерен полученных твердых электролитов; средний размер зерен керамических образцов равен
1-4 мкм. Сопротивление твердых электролитов Li7-xLa3Zr2-xNbxO12 (x = 0.0-2.0) измерено методом
электрохимического импеданса. Определено, что Li6.75La3Zr1.75Nb0.25O12 обладает наиболее высоким
значением общей литий-ионной проводимости при 25°C — 4.0·10-5 См·см-1. Показана возможность
и перспективность использования золь-гель метода для получения твердых электролитов на основе
Li7La3Zr2O12, допированных ионами Nb5+.
Ключевые слова: твердый электролит; Li7La3Zr2O12; гранатоподобная структура; золь-гель синтез;
литий-ионная проводимость; электрохимический импеданс
DOI: 10.1134/S0044461819120041
Литиевые и литий-ионные источники тока обла-
На данный момент особое внимание обращено на
дают высокой удельной энергоемкостью и имеют
твердые электролиты с гранатоподобной структурой.
широкую область применения, что делает их одними
Соединения Li5La3M2O12 (M = Ta, Nb) с кубической
из наиболее перспективных источников тока в на-
структурой и литий-ионной удельной проводимостью
стоящее время. Одним из актуальных направлений
~10-6 См·см-1 при 25°C являются первыми примера-
исследования является поиск твердых электролитов
ми суперионных проводников, имеющих гранатопо-
для данных аккумуляторов, которые должны обладать
добную структуру, которые положили начало грана-
высокими значениями униполярной литий-ионной
топодобному семейству твердых электролитов [6-8].
проводимости, химической устойчивостью к катод-
В 2007 г. исследователям удалось получить много-
ным и анодным материалам и высокой плотностью
обещающий твердый электролит — Li7La3Zr2O12
керамических мембран, а также разработка мето-
(LLZ), который не только обладает высокой элек-
дики синтеза данных материалов при более низких
тропроводностью (общая удельная проводимость
темпераутрах и времени спекания, что в свою оче-
кубической модификации при комнатной температуре
редь позволит снизить энергозатраты, связанные с
составляет ~10-4 См·см-1), но и является устойчивым
получением твердого электролита. Огромный инте-
к металлическому литию [9]. LLZ имеет две струк-
рес к литийпроводящим твердым электролитам под-
турные модификации: кубическую и тетрагональную.
тверждается многочисленными статьями обзорного
Кубическая структура обладает более высокими зна-
и экспериментального характера [1-5].
чениями проводимости при комнатной температуре
1544
Ильина Е. А. и др.
по сравнению с тетрагональной (удельная проводи-
La2O3 (ч.д.а.), Nb2O5 (ос.ч.) и ZrO(NO3)2·2H2O
мость тетрагональной модификации LLZ составля-
(ч.д.а.). La2O3 и Nb2O5 предварительно прокаливали
ет ~10-6-10-7 См·см-1 при 25°С). Стоит отметить,
при 1000°C в течение 1 ч. Li2CO3 брали с 10%-ным
что стабилизация высокопроводящей кубической
избытком, так как при высоких температурах воз-
модификации LLZ возможна только при введении
можны потери Li2O вследствие его летучести [9].
некоторых допантов, таких как Al3+ (ионный радиус
Исходные реактивы Li2CO3 и La2O3 растворяли в раз-
0.57 Å), Ga3+ (0.62 Å), Y3+ (0.97 Å), Nb (0.66 Å) и др.
бавленной азотной кислоте (ос.ч.). ZrO(NO3)2·2H2O
[1, 10-14]. При этом замещение части ионов цир-
и C6H8O7·H2O (х.ч.) растворяли в небольшом коли-
кония (ионный радиус 0.82 Å) на ниобий (ионный
честве дистиллированной воды. Количество введен-
радиус 0.66 Å) представляется одним из наиболее
ной в синтез лимонной кислоты составляло двойной
перспективных, так как ионные радиусы данных эле-
избыток по сравнению с эквивалентным содержа-
ментов имеют близкие значения.
нием всех металлов в синтезируемом соединении.
Синтез твердых электролитов на основе LLZ с
Полученные растворы смешивали и затем добавля-
добавкой Nb производится зачастую по твердофаз-
ли труднорастворимый оксид ниобия. Полученную
ной методике с выдержкой при высоких темпера-
смесь выпаривали до образования прозрачного геля.
турах в течение длительного времени (1200°C, 36 ч
Гель высушивали при ~200°C. Полученный продукт
[14], 1150°C, 25 ч [15]). Синтез по золь-гель методике
поэтапно отжигали на воздухе при температурах 700,
приводит к получению керамики с более мелким раз-
800 и 900°C в течение 1 ч для удаления органиче-
мером частиц, что позволяет получить конечный про-
ских остатков и сажи, а также формирования основ-
дукт с более высокими значениями электропровод-
ной фазы. После каждой стадии отжига порошок
ности, а также снизить температуру и время спекания
перетирали в агатовой ступке. Полученный порошок
керамических мембран [1, 16]. Так, в работе [17]
подвергался одноосному прессованию при давле-
золь-гель синтез LLZ, допированного ионами алю-
нии 240 МПа, после достижения заданного давления
миния и молибдена, позволил эффективно снизить
образцы выдерживали в течение 1 мин для релакса-
температуру спекания керамики, повысив ее ионную
ции напряжений. Спрессованные образцы отжигали
проводимость и плотность. В работе [18] была осу-
при 1150°C в течение 1 ч на воздухе на Pt-подожке.
ществлена попытка синтеза золь-гель методом при
Спекание проводили в засыпке из порошка того же
низких температурах (700°C) твердых электролитов
состава, для того чтобы уменьшить возможные поте-
Li7La3(Zr2-x,Nbx)O12 (x = 0.05, 0.25, 0.5, 1.0 и 1.5) с
ри оксида лития вследствие его летучести.
использованием Nb(OC2H5)5, однако высокие зна-
Критерием оценки полноты прохождения синтеза
чения проводимости керамики не были достигнуты
служили данные рентгенофазового анализа (РФА).
(удельная электропроводность твердого электролита
РФА проводили с помощью рентгеновского дифрак-
Li7La3ZrNbO12 составила 1·10-7 См·см-1 при комнат-
тометра Rigaku D/MAX-2200VL/PC (Rigaku, Япония),
ной температуре). В работе [19] при синтезе циркона-
CuKα-излучение, интервал углов рассеяния 2θ = 10-
та лития Li2ZrO3 карбонат лития растворяли в HNO3,
65°. Идентификацию соединений проводили сопостав-
затем добавляли нерастворимый ZrO2 и этиленгли-
лением полученных данных с базой данных PDF-2.
коль. Полученную смесь выпаривали и поэтапно от-
Микрофотографии поверхности образцов LLZ
жигали. Благодаря предложенной методике удалось
получали с помощью электронного микроскопа
получить конечный продукт с более мелким размером
TESCAN MIRA 3 LMU (TESCAN, Чехия).
частиц при более низкой температуре конечного от-
Для измерения электропроводности в качестве
жига по сравнению с твердофазным синтезом.
электродов на торцы образцов наносили галлий-се-
Целью данной работы являлся синтез твердых
ребряную пасту. Электропроводность измеряли ме-
электролитов Li7-xLa3Zr2-xNbxO12 в широком концен-
тодом электрохимического импеданса с помощью
трационном диапазоне золь-гель методом и исследова-
измерителя E7-25 (MNIPI, Беларусь) в частотном
ние структуры, фазового состава, морфологии и элек-
диапазоне 0.025-1000 кГц. Измерения проводили в
тропроводности полученных твердых электролитов.
интервале температур 20-210°C в двухэлектродной
электрохимической ячейке с серебряными токоотво-
дами на воздухе.
Экспериментальная часть
Обсуждение результатов
В качестве исходных материалов для синтеза твер-
дых электролитов Li7-xLa3Zr2-xNbxO12 (x = 0-2.0)
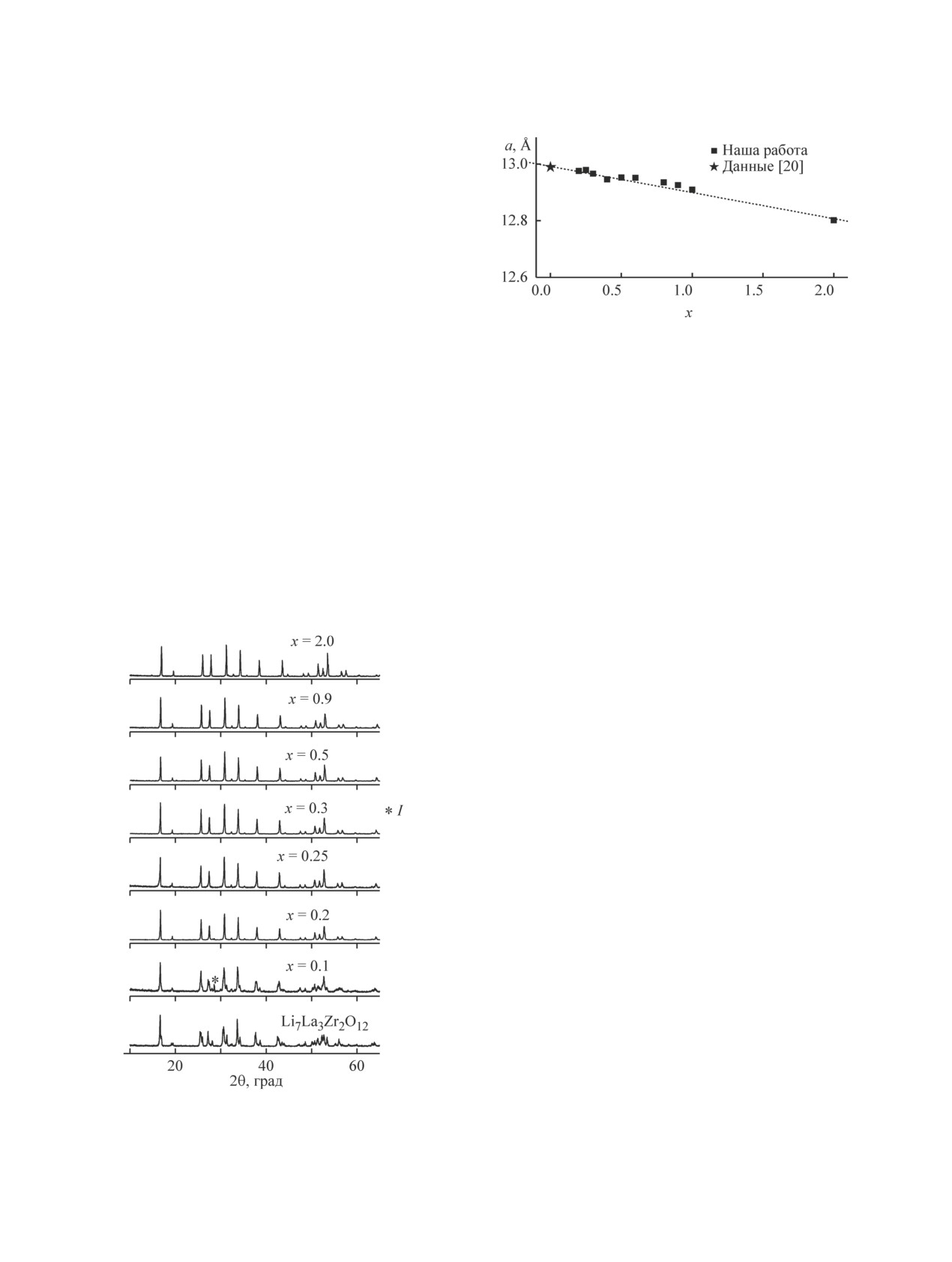
Согласно данным РФА (рис. 1) без добавки ниобия
золь-гель методом использовали Li2CO3 (ос.ч.),
получен однофазный Li7La3Zr2O12 тетрагональной
Литийпроводящие твердые электролиты в системе Li7La3Zr2O12-Li5La3Nb2O12, синтезированные золь-гель методом
1545
модификации. При x = 0.1 наблюдается смесь тетра-
гональной и кубической модификаций LLZ, а также
дополнительный примесный пик, относящийся к
La2Zr2O7. Стоит отметить, что при получении твер-
дых электролитов Li7-xLa3Zr2-xNbxO12 с помощью
твердофазного метода синтеза состав с x = 0.1 так-
же был неоднофазным и представлял собой смесь
двух структурных модификаций LLZ [15]. Составы
с x > 0.1, полученные в данной работе, являлись од-
нофазными и имели кубическую структуру Ia-3d,
характерную для соединения Li5La3Nb2O12, синте-
Рис. 2. Зависимость параметра решетки а в системе
Li7-xLa3Zr2-xNbxO12 от содержания Nb.
зированного твердофазным методом в работах [5-7].
С помощью ренгеноструктурного анализа были
рассчитаны параметры решетки соединений с x > 0.1
12.8020(4) Å и близок по значению к данным [8],
в системе Li7-xLa3Zr2-xNbxO12 (x = 0-2.0), имеющих
полученным для указанного соединения при твердо-
кубическую структуру. Для кубического Li7La3Zr2O12
фазном синтезе — 12.801(2) Å.
параметр решетки а, равный 12.9894(4) Å, приведен
Морфология и размер керамических зерен твер-
из литературных данных [20]. Из рис. 2 видно, что
дых электролитов в системе Li7-xLa3Zr2-xNbxO12, по-
параметр решетки a постепенно уменьшается при
лученных с помощью золь-гель метода, были изучены
замещении Zr4+ на Nb5+, что обусловлено меньшим
с помощью растровой электронной микроскопии
ионным радиусом ниобия, а также уменьшением ко-
(РЭМ). На рис. 3 представлены микрофотографии
личества Li+ в системе Li7-xLa3Zr2-xNbxO12. Параметр
исследуемых твердых электролитов с x = 0.25, 0.5
кристаллической решетки а для Li5La3Nb2O12, полу-
и 0.8, снятые в режиме отраженных (слева) и вто-
ченного с помощью золь-гель метода синтеза, равен
ричных электронов (справа). Съемка в режиме отра-
женных электронов позволяет выявить присутствие
нескольких фаз в составе исследуемых образцов по
изменению цвета керамических зерен. Из представ-
ленных на рис. 3 данных можно сделать вывод об
однофазности синтезированных твердых электроли-
тов. Изображения, полученные в режиме вторичных
электронов, более четко отображают морфологию ке-
рамического зерна. Средний размер зерен для соста-
вов с х = 0.25, 0.5 и 0.8 составляет 1-4 мкм. Однако
при большем увеличении (рис. 3, в) можно предполо-
жить, что наблюдаемые керамические зерна состоят
из более мелких частиц (<1 мкм). Таким образом,
предложенная растворная методика синтеза твердых
электролитов в системе Li7La3Zr2O12-Li5La3Nb2O12
позволила получить керамические мембраны с раз-
мером зерна ~1-4 мкм.
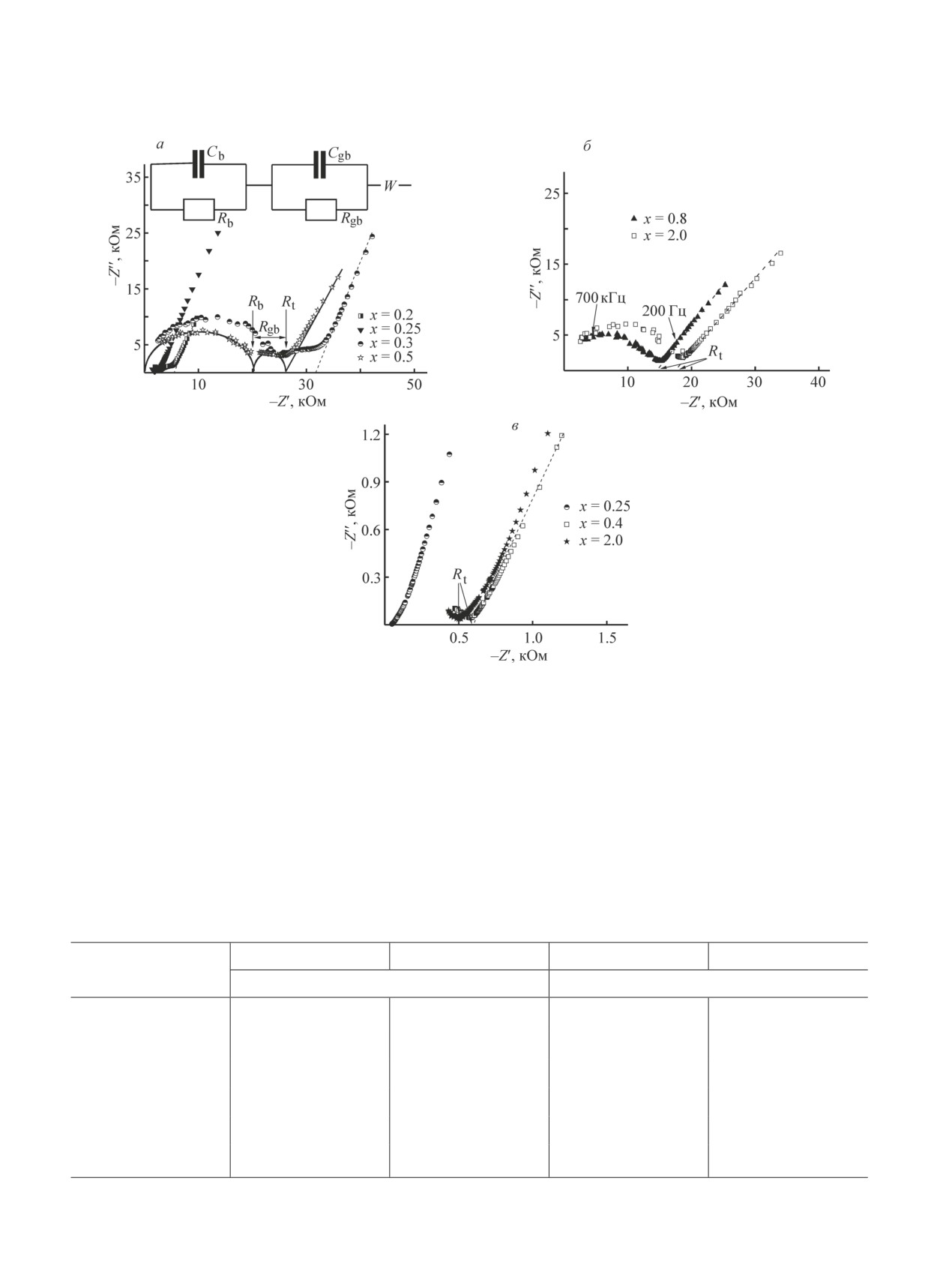
Типичные годографы импеданса электролитов
Li7-xLa3Zr2-xNbxO12 при 25 и 130°C представлены на
рис. 4. В спектрах импеданса для соединений с x < 0.6
можно выделить две полуокружности. Пересечение
полуокружности с осью реальных сопротивлений
вблизи начала координат можно связать с сопро-
тивлением объема твердого электролита (Rb), в то
время как вторая полуокружность в низкочастотной
области относится к сопротивлению границ зерен
Рис. 1. Дифрактограммы твердых электролитов
Li7-xLa3Zr2-xNbxO12 (x = 0-2.0) после отжига
(Rgb), а низкочастотный луч относится к импедансу
при 1150°C в течение 1 ч.
Варбурга (рис. 4, а). В таблице приведены значе-
I — La2Zr2O7.
ния сопротивления и удельной электропроводности
1546
Ильина Е. А. и др.
а
Такое поведение обусловлено фазовым переходом
твердого электролита на основе LLZ из тетрагональ-
ной модификации в кубическую. Уменьшение со-
противления границ зерен у Li7-xLa3Zr2-xNbxO12 при
переходе от x > 0.1 может быть также обусловлено
увеличением плотности керамической мембраны от
~3.0 (x = 0.1) до ~3.8 г·см-3 (x > 0.1). Затем для соеди-
нения Li6.75La3Zr1.75Nb0.25O12 происходит небольшое
увеличение проводимости объема и границ зерен.
10 мкм
Для составов с x = 0.3-0.5 σb и σgb имеют более низ-
кие значения и практически не изменяются.
б
Для образцов с x > 0.5 спектр импеданса при
комнатной температуре не удалось разделить на
две полуокружности, так как они сливались в одну
(рис. 4, б). При температурах выше 100°C для всех
исследуемых электролитов наблюдается только луч
(рис. 4, в). Таким образом, разделить вклады сопро-
тивлений объема и границ зерен электролита при
измерениях в частотном диапазоне 0.025-1000 кГц
10 мкм
не представляется возможным для всех полученных
соединений. Общее сопротивление (Rt) твердых элек-
в
тролитов Li7-xLa3Zr2-xNbxO12 определяли по пересе-
чению низкочастотного луча (импеданс Варбурга) с
осью реальных сопротивлений.
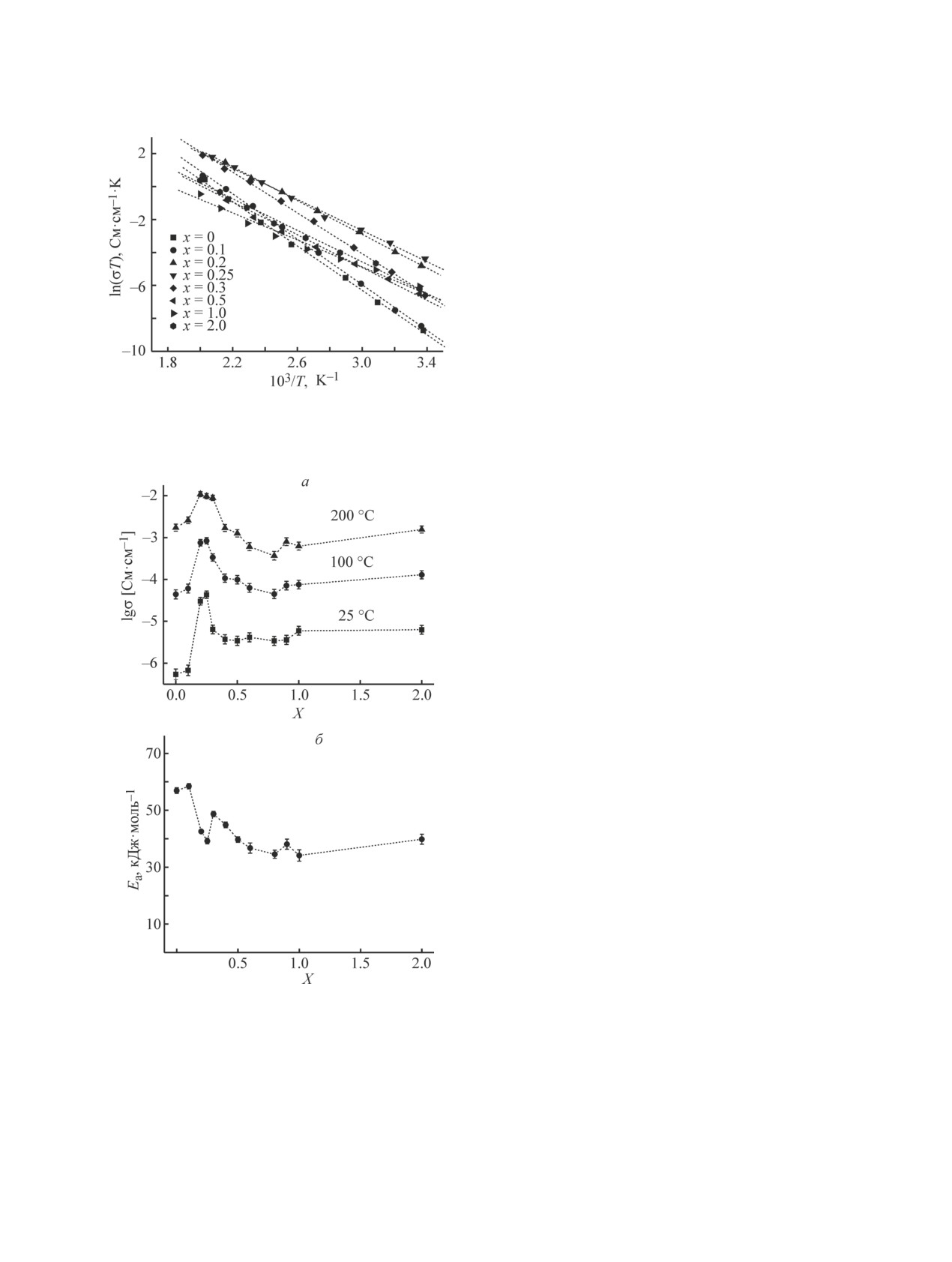
Температурные зависимости общей электропро-
водности для некоторых исследуемых составов в
координатах Аррениуса представлены на рис. 5. В ис-
следуемом интервале температур все зависимости
являются прямолинейными; перегибы, связанные с
5 мкм
фазовыми переходами, отсутствуют. При увеличении
содержания ниобия от 0.0 до 0.25 в исследуемых
г
твердых электролитах происходит рост электропро-
водности, а затем ее снижение. Наблюдаемый на кон-
центрационной зависимости электропроводности
(рис. 6, а) рост проводимости на два порядка вели-
чины при изменении содержания ниобия от 0.1 до
0.2 связан с фазовым переходом из тетрагональной
модификации в кубическую. Максимальной вели-
чиной удельной литий-ионной проводимости при
комнатной температуре обладает твердый электро-
10 мкм
лит Li6.75La3Zr1.75Nb0.25O12 — 4.0·10-5 См·см-1. Рост
электропроводности в системе Li7-xLa3Zr2-xNbxO12
Рис. 3. РЭМ-микрофотографии поверхности твердых
авторы работы [14] связывают с повышением под-
электролитов Li7-xLa3Zr2-xNbxO12 с x = 0.25 (а),
вижности носителей заряда в структуре твердого
0.5 (б, в), 0.8 (г).
электролита для состава с x = 0.25 по сравнению с
Изображения получены в режиме отраженных (слева)
x = 0. При дальнейшем увеличении содержания нио-
и вторичных электронов (справа).
бия в LLZ наблюдается снижение удельной электро-
объема и границ зерен исследуемых электролитов с
проводности до ~10-6 См·см-1. При более высоких
x = 0.1-0.5 при 25°C. Наблюдается резкое увеличение
температурах ее значения для составов с x = 0.4-2.0
удельной проводимости для состава с x = 0.2: для
близки. Удельная проводимость твердого электро-
объемной проводимости (σb) — на один порядок, а
лита Li5La3Nb2O12, полученного золь-гель методом
для межзеренной (σgb) — на два порядка величины.
синтеза, составила 6.8·10-6 См·см-1 при 25°C, что в
Литийпроводящие твердые электролиты в системе Li7La3Zr2O12-Li5La3Nb2O12, синтезированные золь-гель методом
1547
Рис. 4. Годографы импеданса твердых электролитов Li7-xLa3Zr2-xNbxO12, измеренные при 25 (а, б) и 130°C (в).
несколько раз больше значения (3.4·10-6 См·см-1),
уменьшается при увеличении количества нио-
полученного в работе [8] при твердофазном синтезе
бия до содержания, соответствующего x = 0.25
данного соединения.
(39.2 ± 1.0 кДж·моль-1), затем наблюдается неболь-
Значения энергии активации находили из углов
шой скачок для состава с x = 0.3. Для твердых элек-
наклона линейных графиков зависимости ln(σT)-1/T
тролитов с x = 0.5-2.0 энергия активации имеет близ-
методом наименьших квадратов. Энергия актива-
кие значения с величиной, полученной для состава с
ции проводимости в системе Li7-xLa3Zr2-xNbxO12
x = 0.25 (рис. 6, б).
Значения сопротивлений и удельной проводимости объема (Rb, σb) и границ зерен (Rgb, σgb) твердых
электролитов Li7-xLa3Zr2-xNbxO12 (x = 0.1-0.5) при 25°C
Rb
Rgb
σb
σgb
x
Ом
См·см-1
0.1
25470
214860
5.0·10-6
6.0·10-7
0.2
2870
2630
5.1·10-5
5.5·10-5
0.25
1920
1400
6.6·10-5
9.1·10-5
0.3
24590
8300
5.8·10-6
1.7·10-5
0.4
21300
9600
5.7·10-6
1.3·10-5
0.5
19500
6400
6.3·10-6
1.9·10-5
1548
Ильина Е. А. и др.
литы Li7-xLa3Zr2-xNbxO12 (x = 0.0-2.0). Применение
данной методики позволило снизить температуру и
время отжига керамических образцов по сравнению с
твердофазным методом синтеза с 1200 в течение 36 ч
до 1150°C в течение 1 ч, а также получить твердые
электролиты в системе Li7La3Zr2O12-Li5La3Nb2O12
со средним размером керамических зерен ~1-4 мкм.
С помощью РФА было установлено, что образец с
x = 0.1 представлял собой смесь тетрагональной и
кубической модификации Li7La3Zr2O12, однако боль-
шее введение Nb5+ способствовало формированию
однофазных образцов с кубической модификаций
Ia-3d. Сопротивление керамики Li7-xLa3Zr2-xNbxO12
(x = 0.0-2.0) измерено методом электрохимическо-
Рис. 5. Температурные зависимости электропроводно-
го импеданса в интервале температур 20-210°C.
сти твердых электролитов Li7-xLa3Zr2-xNbxO12 в коор-
динатах Аррениуса.
Установлено, что общая литий-ионная проводимость
твердых электролитов Li7-xLa3Zr2-xNbxO12 увеличи-
вается при небольшом введении ниобия и достигает
максимального значения (4.0·10-5 См·см-1 при 25°C)
для состава с x = 0.25. Рост электропроводности в
исследуемой системе связан с повышением подвиж-
ности носителей заряда (Li+) в структуре твердого
электролита для состава с x = 0.25 по сравнению с
x = 0. При увеличении содержания ниобия (x > 0.25)
в синтезируемых твердых электролитах наблюда-
лось снижение удельной электропроводности до
~10-6 См·см-1 при комнатной температуре. Таким
образом, в ходе работы показана перспективность
использования золь-гель метода для получения твер-
дых электролитов на основе Li7La3Zr2O12, допирован-
ных ионами Nb5+. Полученные твердые электролиты
могут быть использованы в литий-ионных аккумуля-
торах.
Благодарности
Аттестацию полученных материалов проводили с
использованием оборудования ЦКП «Состав веще-
ства» ИВТЭ УрО РАН.
Финансирование работы
Исследование выполнено при финансовой под-
держке гранта Президента РФ № МК-1382.2019.3.
Рис. 6. Концентрационные зависимости общей прово-
при различных
димости образцов Li7-xLa3Zr2-xNbxO12
Конфликт интересов
температурах (а) и энергия активации электропровод-
ности (б).
Авторы заявляют об отсутствии конфликта инте-
ресов, требующего раскрытия в данной статье.
Выводы
Информация об авторах
В ходе работы золь-гель методом синтеза с исполь-
зованием в качестве одного из исходных соединений
Ильина Евгения Алексеевна, к.х.н., н.с., ORCID:
Nb2O5 получены литийпроводящие твердые электро-
Литийпроводящие твердые электролиты в системе Li7La3Zr2O12-Li5La3Nb2O12, синтезированные золь-гель методом
1549
Лялин Ефим Дмитриевич, лаборант, ORCID:
[11] Li Y., Han J., Wang C.-A., Vogel S. C., Xie H., Xu M.,
Goodenough J. B. Ionic distribution and conductivity
Антонов Борис Дмитриевич, к.х.н., с.н.с., ORCID:
in lithium garnet Li7La3Zr2O12 // J. Power Sources.
2012. V. 209. P. 278-281.
Панкратов Александр Александрович, к.х.н., н.с.,
[12] Bernuy-Lopez C., Manalastas W., Lopez del Amo J. M.,
Aguadero A., Aguesse F., Kilner J. A. Atmosphere
controlled processing of Ga-substituted garnets for
Список литературы
high Li-ion conductivity ceramics // Chem. Mater.
2014. V. 26. P. 3610-3617.
[1] Ramakumar S., Deviannapoorani C., Dhivya L.,
Shankar L.S., Murugan R. Lithium garnets: Synthesis,
[13] Li Y., Han J.-T., Wang C.-A., Xie H., Goodenough J. B.
structure, Li+ conductivity, Li+ dynamics and
Optimizing Li+ conductivity in a garnet framework //
applications // Prog. Mater. Sci. 2017. V. 88. P. 325-
J. Mater. Chem. 2012. V. 22. P. 15357-15361.
[2] Ярославцев А. Б. Основные направления разра-
[14] Ohta S., Kobayashi T., Asaoka T. High lithium
ботки и исследования твердых электролитов //
ionic conductivity in the garnet-type oxide
Успехи химии. 2016. Т. 85. № 11. С. 1255-1276
Li7-xLa3(Zr2-xNbx)O12 (x = 0-2) // J. Power Sources.
[Yaroslavtsev A. B. Solid electrolytes: Main prospects
2011. V. 196. P. 3342-3345.
of research and development // Russ. Chem. Rev.
2016. V. 85. P. 1255-1276.
[15] Zhao P., Xiang Y., Wen Y., Li M., Zhu X.,
Zhao S., Jin Z., Ming H., Cao G. Garnet-like
[3] Kammampata S. P., Thangadurai V. Cruising in
Li7-xLa3Zr2-xNbxO12 (x = 0-0.7) solid state
ceramics — discovering new structures for all-
electrolytes enhanced by self-consolidation strategy
solid-state batteries — fundamentals, materials, and
// J. Eur. Ceram. Soc. 2018. V. 38. P. 5454-5462.
performances // Ionics. 2018. V. 24. P. 639-660.
[16] Il′ina E. A., Andreev O. L., Antonov B. D.,
[4] Liu Q., Geng Z., Han C., Fu Y., Li S., He Y., Li
Batalov N. N. Morphology and transport properties
B. Challenges and perspectives of garnet solid
of the solid electrolyte Li7La3Zr2O12 prepared by
electrolytes for all solid-state lithium batteries // J.
the solid-state and citrate-nitrate methods // J. Power
Power Sources. 2018. V. 389. P. 120-134.
Sources. 2012. V. 201. P. 169-173.
[5] Zheng F., Kotobuki M., Song S., Lai M.O., Lu L.
[17] Li Y., Yang T., Wu W., Cao Z., He W., Gao Y., Liu J., Li
Review on solid electrolytes for all-solid-state lithium-
G. Effect of Al-Mo codoping on the structure and ionic
ion batteries // J. Power Sources. 2018. V. 389. P. 198-
conductivity of sol-gel derived Li7La3Zr2O12 ceramics
// Ionics. 2018. V. 24. P. 3305-3315.
[6] Hyooma H., Hayashi K. Crystal structures of
La3Li5M2O12 (M = Nb, Ta) // Mater. Res. Bull. 1988.
[18] Rosero-Navarro N.C., Yamashita T., Miura A.,
V. 23. P. 1399-1407.
Higuchi M., Tadanaga K. Preparation of
Li7La3(Zr2-x, Nbx)O12 (x
=
0-1.5)
and
[7] Mazza D. Remarks on a ternary phase in the La2O3-
Li3BO3/LiBO2 composites at low temperatures using a
Me2O5-Li2O system (Me = Nb, Ta) // Mater. Lett.
sol-gel process // Solid State Ionics. 2016. V. 285. P.
1988. V. 7. P. 205-207.
[19] Sherstobitova E. A., Gubkin A. F., Bobrikov I. A.,
[8] Thangadurai V., Kaack H., Weppner W. Novel fast
Kalashnova A. V., Pantyukhina M. I. Bottle-necked
lithium ion conduction in garnet-type Li5La3M2O12
ionic transport in Li2ZrO3: high temperature
(M = Nb, Ta) // J. Am. Ceram. Soc. 2003. V. 86.
neutron diffraction and impedance spectroscopy //
P. 437-440.
Electrochim. Acta. 2016. V. 209. P. 574-581.
[9] Murugan R., Thangadurai V., Weppner W. Fast lithium
[20] Rettenwander D., Redhammer G., Preishuber-Pflugl F.,
ion conduction in garnet-type Li7La3Zr2O12 // Angew.
Cheng L., Miara L., Wagner R., Welzl A., Suard E.,
Chem. Int. Ed. 2007. V. 46. P. 7778-7781.
Doeff M.M., Wilkening M., Fleig J., Amthauer G.
Structural and electrochemical consequences of Al and
[10] Raskovalov A.A., Il′ina E.A., Antonov B.D. Structure
Ga co-substitution in Li7La3Zr2O12 solid electrolytes
and transport properties of Li7La3Zr2-0.75xAlxO12
// Chem. Mater. 2016. V. 28. N 7. P. 2384-2392.
superionic solid electrolytes // J. Power Sources. 2013.
V. 238. P. 48-52.