Журнал прикладной химии. 2019. Т. 92. Вып. 3
СОРБЦИОННЫЕ И ИОНООБМЕННЫЕ ПРОЦЕССЫ
УДК 541.64:532.7
ДИНАМИКА СОРБЦИИ МОЧЕВОЙ КИСЛОТЫ НА МОЛЕКУЛЯРНО
ИМПРИНТИРОВАННОМ СОРБЕНТЕ
© И. С. Гаркушина1, И. В. Полякова1, О. А. Писарев1,2
1 Институт высокомолекулярных соединений РАН, Санкт-Петербург
2 Санкт-Петербургский политехнический университет Петра Великого
E-mail: chrom79@yandex.ru
Поступила в Редакцию 27 сентября 2018 г.
После доработки 19 января 2019 г.
Принята к публикации 28 января 2019 г.
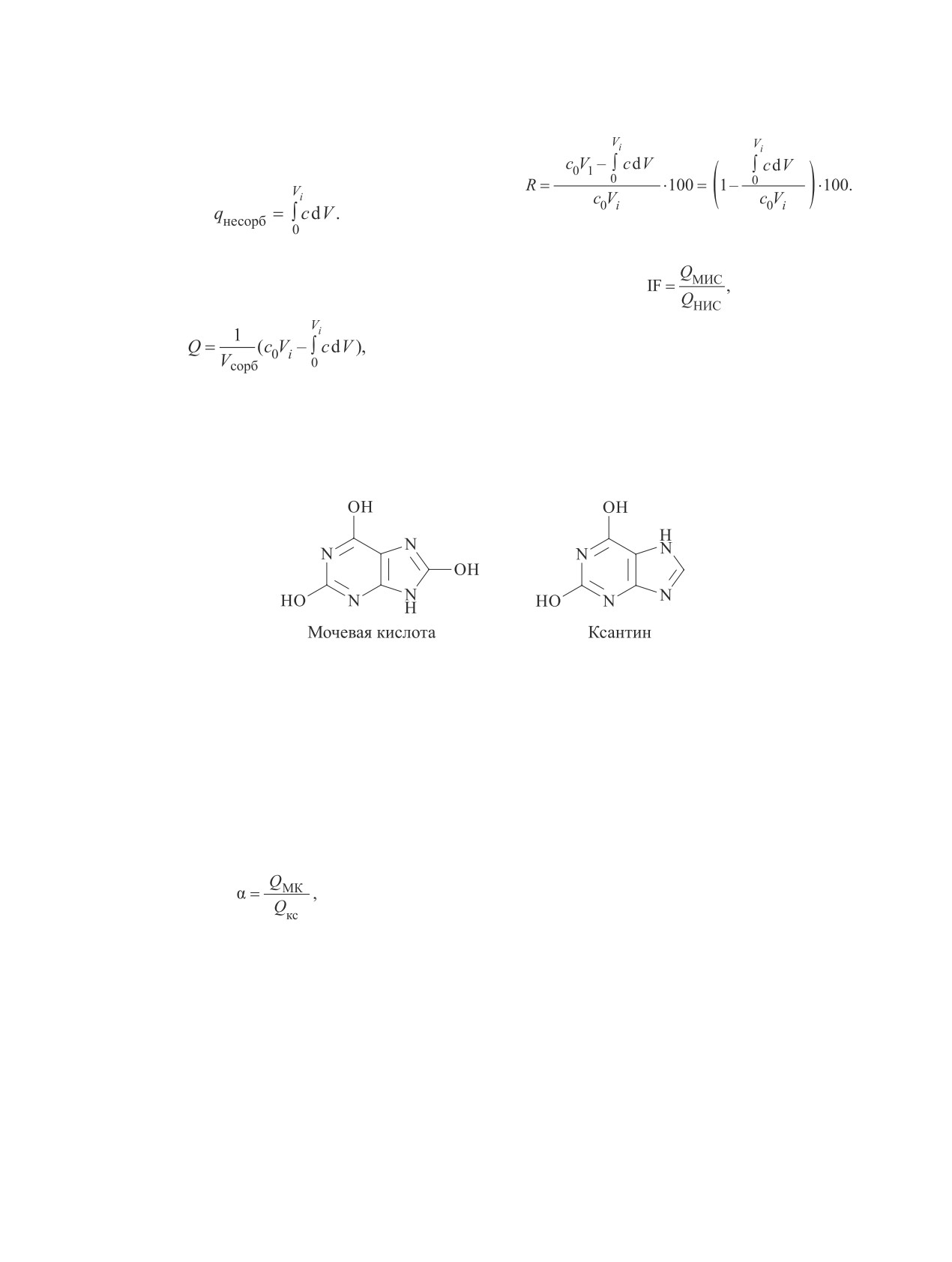
С целью создания эффективного сорбционного метода извлечения мочевой кислоты из плазмы крови
исследована динамика сорбции мочевой кислоты гранульным молекулярно импринтированным поли-
мерным сорбентом на основе 2-гидроксиэтилметакрилата и диметакрилата этиленгликоля и его
неимпринтированным аналогом. Установлены интервалы скоростей подвижной фазы, в которых
реализуется равновесный режим динамики сорбции мочевой кислоты на молекулярно импринтиро-
ванном сорбенте МИС-40. Определен оптимальный режим динамического сорбционного процесса на
МИС-40, при котором степень извлечения мочевой кислоты из физиологического раствора составляла
60%, а коэффициент селективности равнялся 2.08.
Ключевые слова: молекулярное импринтирование, полимерные сорбенты, динамика сорбции, мочевая
кислота.
DOI: 10.1134/S0044461819030150
Молекулярный импринтинг является современ-
Вместе с тем в настоящее время в медицинской
ным методом создания высокоселективных сорбентов
промышленности РФ для осуществления большин-
[1-3]. Молекулярно импринтированные сорбенты
ства процессов гемо- и плазмосорбции в качестве
(МИС) представляют собой синтетические материа-
сорбентов применяются соединения на основе ак-
лы, которые селективно взаимодействуют с целевой
тивированных углей [6]. Активированные угли яв-
молекулой в присутствии близких по химической
ляются неселективными сорбентами. Наряду с ток-
структуре соединений [4, 5]. Эти материалы получа-
сическими веществами они сорбируют множество
ют при полимеризации функционального мономера и
физиологически активных компонентов, которые
сшивающего агента в присутствии целевой молекулы
необходимы для жизнедеятельности организма че-
(темплата). В результате после удаления темплата в
ловека.
полимерной сетке формируются специфичные сай-
Одной из нерешенных задач, где необходимо ис-
ты (импринт-центры), обладающие «молекулярной
пользование высокоселективных сорбентов в экс-
памятью» о целевой молекуле. В отличие от природ-
тракорпоральных установках для гемо- и плазмо-
ных рецепторов МИС обладают структурной ста-
сорбции, является создание эффективных методов
бильностью в широком интервале рН, ионной силы,
извлечения из крови избыточной мочевой кислоты
температуры и содержания органических раствори-
(МК). Мочевая кислота — конечный продукт пу-
телей.
ринового метаболизма в организме человека. При
393
394
Гаркушина И. С. и др.
высокой концентрации мочевой кислоты (свыше
тель. Общий объем реакционной смеси составлял
420 мкмоль·л-1) в организме человека возникает ги-
50 мл при соотношении объема суспензионной сре-
перурикемия и как следствие гиперурикемии подагра.
ды и мономерной смеси 5:1. Реакцию сополимери-
Поэтому разработка препаративного процесса селек-
зации инициировали путем введения 0.16 г АИБН.
тивной сорбции мочевой кислоты является актуаль-
Сополимеризацию осуществляли при 65-70°С в те-
ной задачей.
чение 1 ч при постоянном перемешивании (скорость
Ключевым этапом нахождения оптимальных ус-
вращения мешалки составляла 200-300 об·мин-1).
ловий осуществления препаративной селективной
Синтезированные сферические гранулы извлека-
сорбции целевого биологически активного вещества
ли из колбы и промывали водой. Темплат мочевой
(в частности, и МК) является систематическое изуче-
кислоты удаляли из полимерной матрицы путем
ние его динамики сорбции.
последовательной промывки изопропиловым спир-
Цель работы состояла в исследовании динами-
том, затем смесью 0.1 М раствора HCl и изопропи-
ки сорбции мочевой кислоты МИС на основе 2-ги-
лового спирта 50/50 (об%). Полноту удаления моче-
дроксиэтилметакрилата (ГЭМА) и диметакрилата
вой кислоты из полимерной сетки контролировали
этиленгликоля (ДМЭГ) и его неимпринтированным
с помощью количественного определения мочевой
аналогом. Выбор сомономеров, с одной стороны, был
кислоты при λ = 293 нм на приборе СФ-256 УВИ
обусловлен их гемосовместимостью [6], с другой —
(ЛОМО Фотоника, Россия). Для этого использовалась
тем, что использование ГЭМА в качестве мономера
предварительно построенная калибровочная кри-
приводило к синтезу молекулярно импринтирован-
вая, которая обладала прямолинейным участком до
ных полимеров, позволяющих осуществлять селек-
с = 0.04 ммоль·л-1. Процесс удаления темплата осу-
тивную сорбцию целевых компонентов из водных
ществляли до полного отсутствия мочевой кислоты
сред [7].
в промывных растворах. Затем образцы сорбентов
промывали последовательно водой и изопропиловым
спиртом, сушили в вакуумной печи при 50°С до до-
Экспериментальная часть
стижения постоянной массы. Сорбенты, синтезиро-
МИС были синтезированы методом радикальной
ванные в присутствии 20, 30, 40 и 60 мас% мочевой
суспензионной сополимеризации ГЭМА (98%, Sigma-
кислоты, обозначены как МИС-20, МИС-30, МИС-40
Aldrich, Германия) и ДМЭГ (98%, Sigma-Aldrich,
и МИС-60 соответственно.
Германия) при соотношении ГЭМА/ДМЭГ, рав-
В качестве сорбента сравнения использовали
ном 50/50 (мол%). Мочевая кислота (о.х.ч., Вектон,
неимпринтированный сорбент (НИС). Он был син-
Россия) вводилась в полимеризационную смесь в
тезирован в аналогичных c МИС условиях, но без вве-
качестве темплата при соотношениях 20, 30, 40 и
дения мочевой кислоты в полимеризационную смесь.
60 мас% к массе сомономеров. В качестве суспен-
Использовали гранулы МИС и НИС диаметром
зионной среды использовали насыщенный раствор
~(100-300) мкм, так как именно этот диапазон разме-
NaCl (Вектон, Россия), в который для стабилизации
ров позволяет обеспечивать хорошую протекаемость
суспензии добавляли 1 мас% растворимого крахмала
препаративных гемосорбционных колонок при низ-
(Вектон, Россия). Порообразователем являлся гептан
ком давлении.
(х.ч., Вектон, Россия) в соотношении 10 об% к объ-
Изображения поверхности сорбентов, полученные
ему сомономеров. Радикальную сополимеризацию
методом сканирующей электронной микроскопии
ГЭМА и ДМЭГ инициировали 2,2′-азобисизобутиро-
(СЭМ), свидетельствовали о формировании структур-
нитрилом (АИБН) (99%, Chemical Line, Россия), его
но сегрегированных полимерных матриц, содержа-
концентрация в полимеризационной смеси составля-
щих пространство между глобулами (транспортные
ла 1 мас% к массе сомономеров.
поры) и микроглобулы, пронизанные микропорами
При синтезе МИС на первом этапе 3.3, 4.95, 6.6
(рис. 1).
или 9.9 г мочевой кислоты (20, 30, 40 и 60 мас%
В работах [8, 9] было изучено равновесие сорбции
соответственно) растворяли в смеси, состоящей из
мочевой кислоты на МИС-20, МИС-30, МИС-40 и
6.5 мл ГЭМА, 10 мл ДМЭГ и 1.65 мл гептана. Раствор
МИС-60 и показано, что в сравнении с неимпринти-
крахмала в насыщенном NaCl предварительно на-
рованными сорбентами МИС сорбируют мочевую
гревали до 50°С в цилиндрической колбе емкостью
кислоту с более высокими значениями равновесной
100 мл, снабженной механической лопастной мешал-
сорбционной емкости. При начальной концентра-
кой. Далее в нагретую суспензионную среду вносили
ции мочевой кислоты в сорбционной среде, равной
раствор, содержащий сомономеры и порообразова-
500 мкмоль·л-1 (именно эта начальная концентра-
Динамика сорбции мочевой кислоты на молекулярно импринтированном сорбенте
395
Рис. 1. СЭМ-изображения поверхности полимерных сорбентов на основе ГЭМА-ДМЭГ.
а — НИС, б — МИС-40.
ция использована нами при получении фронтальных
Эксперименты по исследованию влияния скорости
динамических кривых), максимальная равновесная
протекания подвижной фазы на динамику сорб-
сорбционная емкость была реализована на MИС-40
ции мочевой кислоты проводили на колонках НИС
и составляла ~4 мкмоль·мл-1, тогда как на МИС-20,
и МИС-40 с H = 3.0 см при скоростях, равных 0.1,
МИС-30, МИС-60 и НИС она составляла ~2.5, 3.1,
0.25 и 0.5 мл·мин-1. Для построения фронтальных
1.6 и 1 мкмоль·мл-1 соответственно. В связи с этим в
динамических кривых пробы (4 мл) на выходе из
сравнении с НИС динамика сорбции мочевой кисло-
колонок отбирали через равные интервалы времени.
ты систематически изучена на МИС-40.
Концентрацию мочевой кислоты в пробах опреде-
Концентрация 500 мкмоль·л-1 в плазме крови че-
ляли при λ = 293 нм. После каждого динамического
ловека соответствует уровню выраженной гипер-
сорбционного эксперимента колонки регенерировали
урикемии [10]. Для приготовления физиологиче-
путем последовательной промывки изопропиловым
ского раствора мочевой кислоты концентрацией
спиртом, затем смесью 0.1 н раствора HCl и изо-
500 мкмоль·л-1 навеску мочевой кислоты 8.4 мг рас-
пропилового спирта 50/50 (об%) и затем отмывали
творяли в 100 мл 0.9% NaCl с добавлением 0.03 г
раствором 0.9% NaCl с добавлением 0.03 г Li2CO3.
Li2CO3 для образования урата лития, растворимого
Контроль отмывки от сорбированной мочевой кис-
в воде.
лоты осуществляли при λ = 293 нм.
Динамику сорбции мочевой кислоты изучали с
С целью дальнейшего использования в препара-
использованием стеклянных колонок, заполненных
тивных гемосорбционных колонках большого диа-
сорбентами НИС (колонка НИС) и МИС-40 (колон-
метра скорости протекания подвижной фазы были
ка МИС-40). Диаметр колонок — 1.4 см. Колонки
пересчитаны в величины, не зависящие от площади
набивали сорбентами в набухшем состоянии. Для
сечения колонки. Эти величины составляли 4.8, 12.0
набухания сорбенты НИС и МИС-40 были поме-
и 24.0 мл·см-2·ч-1 соответственно.
щены на 16 ч в стеклянные стаканы, заполненные
Фронтальные динамические кривые строили в
раствором 0.9% NaCl с добавлением 0.03 г Li2CO3.
координатах с/с0 от V, где с и с0 — концентрация
Предварительными экспериментами было показано,
мочевой кислоты в элюате и в исходном растворе
что 16 ч достаточно для достижения равновесия при
(мкмоль·мл-1).
набухании. Набухшими гранулами сорбентов запол-
Количество (мкмоль) мочевой кислоты qисх, вно-
няли стеклянные колонки (H = 1.5, 3.0 и 4.3 см), а
симое в сорбционную колонку до насыщения сорбен-
затем промывали физиологическим раствором до
та, рассчитывали как
равномерного распределения гранул в сорбционном
qисх = с0Vi,
(1)
слое. Эксперименты по исследованию влияния вы-
соты сорбирующего слоя на динамику сорбции мо-
где Vi - объем исходного раствора мочевой кислоты,
чевой кислоты проводили с постоянной скоростью
который необходимо было пропустить через колонку
протекания подвижной фазы, равной 0.25 мл·мин-1.
до насыщения сорбента.
396
Гаркушина И. С. и др.
Количество (мкмоль) мочевой кислоты, не сорби-
рованное сорбционной колонкой:
(4)
(2)
Импринтинг-фактор рассчитывали согласно фор-
Равновесные динамические сорбционные емкости
муле
синтезированных сорбентов в расчете на 1 мл сорбен-
,
(5)
та вычисляли следующим образом:
где QМИС и QНИС — равновесные динамические сорб-
(3)
ционные емкости МИС-40 и НИС соответственно.
С целью изучения селективности сорбции МК на
где Vсорб — объем сорбента (мл).
МИС-40 была исследована динамика сорбции ксан-
Относительная ошибка определения динамиче-
тина («чистый», Вектон, Россия, ММ = 152). Ксантин
ской емкости сорбции составляла 3.4-4.2%.
является наиболее близким структурным аналогом
Тогда степень извлечения мочевой кислоты R (%)
мочевой кислоты:
из физиологического раствора
Физиологический раствор ксантина готовили так-
ющихся веществ. Оптимальные условия выделения
же с начальной концентрацией скс = 500 мкмоль·л-1.
целевого компонента достигаются при его перемеще-
Для этого навеску ксантина 7.6 мг растворяли в
нии по сорбционной колонке в равновесном динами-
100 мл 0.9% NaCl с добавлением 0.03 г Li2CO3. Для
ческом режиме [11].
определения равновесной концентрации использо-
С целью нахождения условий реализации равно-
вали предварительно построенные калибровочные
весного режима динамики сорбции мочевой кислоты
кривые при λ = 267 нм, которые носили линейный
было исследовано влияние высоты сорбционных ко-
характер вплоть до скс = 0.2 ммоль·л-1.
лонок МИС-40 и НИС на их динамические сорбци-
Коэффициент селективности сорбции мочевой
онные свойства.
кислоты рассчитывали по формуле
На НИС наблюдались хорошо известные в пре-
паративной хроматографии биологически активных
веществ при низком давлении зависимости вида
(6)
динамических сорбционных кривых от высоты ко-
лонки (рис. 2). Выходная кривая динамики сорбции
где QМК и Qкс — динамические емкости сорбции
мочевой кислоты на колонке НИС с H = 1.5 см рез-
мочевой кислоты и ксантина соответственно, рассчи-
ко асимметричная, она характеризуется достаточно
танные по формуле (4).
резким подъемом на начальном участке и медленно
приближается к состоянию равновесия (рис. 2, а,
кривая 1). Эти особенности характерны для нерав-
Обсуждение результатов
новесного режима динамики сорбции, при котором
Эффективность сорбционных процессов, исполь-
насыщение колонки далеко от полного, несмотря на
зуемых для препаративного или промышленного вы-
высокую концентрацию вытекающего из колонки
деления целевых веществ, определяется, с одной сто-
вещества. Равновесный режим динамики сорбции
роны, равновесной избирательностью сорбционного
мочевой кислоты на НИС достигался при увеличе-
процесса, а с другой — условиями обострения или
нии высоты колонки — динамическая фронтальная
размывания концентрационных профилей сорбиру-
кривая приобретала S-образный симметричный вид
Динамика сорбции мочевой кислоты на молекулярно импринтированном сорбенте
397
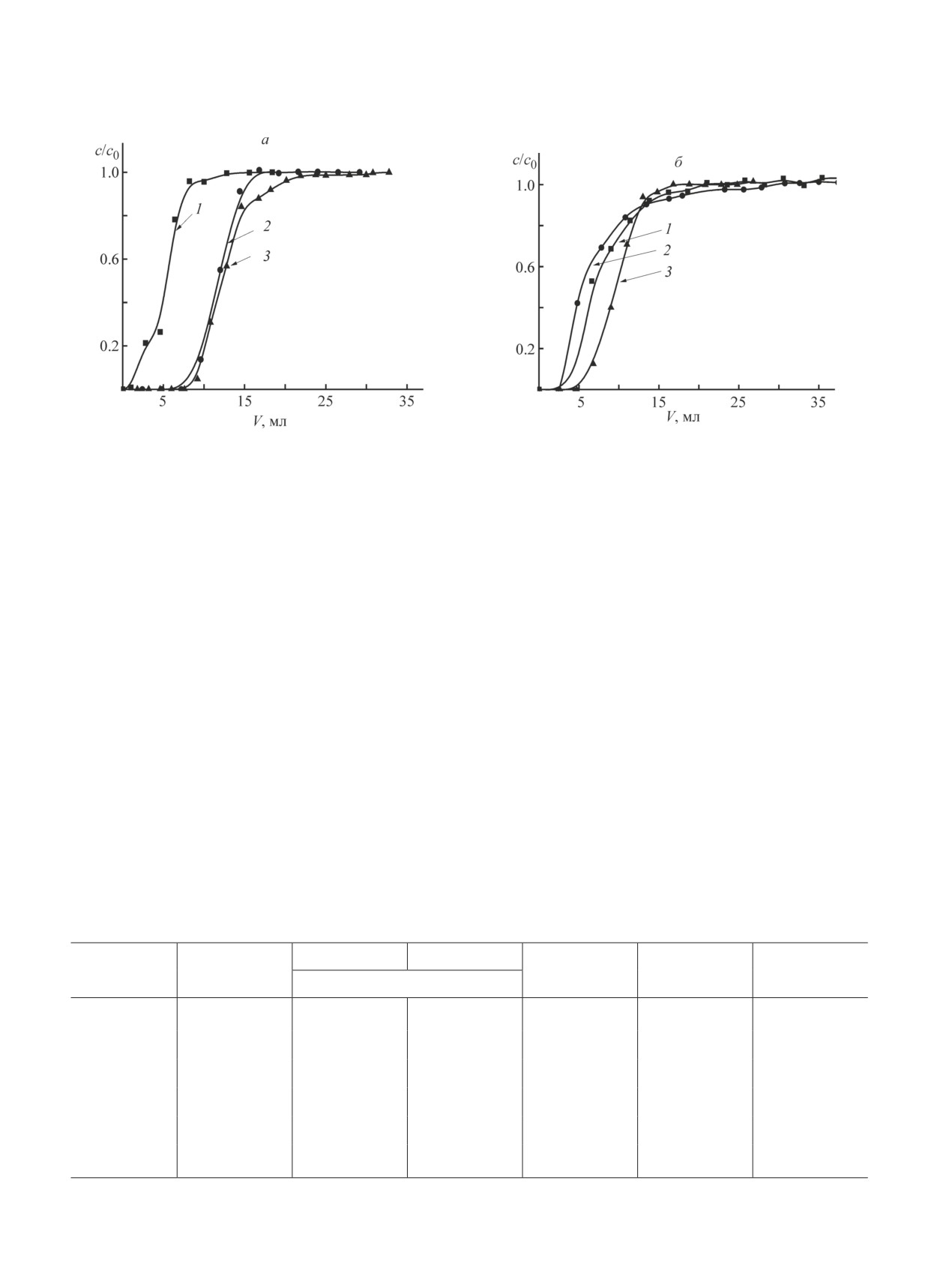
Рис. 2. Динамика сорбции мочевой кислоты на НИС (а) и МИС-40 (б).
Скорость протекания подвижной фазы 12 мл·см-2·ч-1.
V — объем раствора мочевой кислоты, пропущенного через колонку.
H (см): 1 — 1.5, 2 — 3.0, 3 — 4.3.
со значительным увеличением объема «проскока»
ванных сорбентов, которые содержат как специфиче-
(рис. 2, а, кривые 2, 3), при этом степень извлечения
ские, так и неспецифические сорбционные центры.
R монотонно возрастала и достигала 57% (табл. 1).
При сорбции мочевой кислоты на колонке МИС-40
В отличие от НИС характер фронтальных кривых
с H = 1.5 см превалировал вклад специфичного связы-
динамики сорбции мочевой кислоты на МИС-40 сви-
вания в сорбцию, о чем свидетельствовало значение
детельствовал о протекании процесса в равновесном
импринтинг-фактора (IF > 1). По всей видимости,
режиме для всех значений высоты сорбционной ко-
при малом объеме колонки в первую очередь реали-
лонки (рис. 2, б). Значения qсорб и соответственно зна-
зовывалась специфичная сорбция на легко доступных
чения R возрастали с увеличением высоты колонки
импринт-сайтах в межглобулярном пространстве ге-
(табл. 1). Однако при H = 3.0 см динамическая кривая
теросетчатого сорбента [5].
сорбции была более «размыта», чем при H = 1.5 см
При увеличении высоты колонки до H = 3 см ко-
(рис. 3, б, кривые 1, 2). Такое «неправильное» пове-
личество сорбированной мочевой кислоты и соот-
дение динамических сорбционных кривых, по всей
ветственно значения R увеличивались, однако при
видимости, может быть объяснено особенностями
этом превалировал вклад неспецифичного связыва-
структурной организации молекулярно импринтиро-
ния в сорбцию мочевой кислоты импринтирован-
Таблица 1
Влияние высоты сорбционной колонки на характеристики динамической сорбции мочевой кислоты
Скорость протекания подвижной фазы 12 мл·см-2·ч-1, qисх ≅ 12.0 мкмоль
qнесорб
qсорб
Сорбент
H, см
Q, мкмоль·мл-1
IF
R, %
мкмоль
НИС
1.5
9.5
2.5
2.0
20
3.0
6.4
5.6
2.2
—
47
4.3
5.2
6.8
1.6
57
МИС-40
1.5
8.3
3.7
2.6
1.32 ± 0.12
31
3.0
7.3
4.7
1.6
0.71 ± 0.05
39
4.3
7.2
4.8
1.0
0.53 ± 0.05
50
398
Гаркушина И. С. и др.
ным сорбентом (IF < 1). Можно полагать, что в этом
протекания раствора — эффективность сорбцион-
случае высоты колонки было недостаточно, чтобы
ной колонки ухудшалась при наименьшей скорости
обеспечить полное заполнениие неспецифичных
(4.8 мл·см-2·ч-1), т. е. имел место быстрый проскок
сорбционных центров, которые преимущественно
и потеря сорбционной емкости (рис. 3, а, кривая 1;
расположены во внутриглобулярном пространстве
табл. 2). Однако обычно низкая скорость протекания
полимерной сетки. Это и приводило к некоторому
подвижной фазы способствует улучшению внутри-
размыванию концентрационного фронта мочевой
диффузионного гетерогенного массопереноса [11].
кислоты. Дальнейшее увеличение высоты колонки
Можно полагать, что вклад в сорбцию внутридиффу-
до H = 4.3 см способствовало «задействованию» всех
зионного массопереноса к свободным сорбционным
неспецифичных сорбционных центров и соответ-
центрам во внутриглобулярном пространстве был
ственно увеличению суммарного объема задержки
затруднен из-за плохой проницаемости НИС. В ре-
мочевой кислоты (рис. 2, б, кривая 3).
зультате сорбция осуществлялась преимущественно
Таким образом, при скорости протекания под-
в транспортных порах, обычно содержащих не более
вижной фазы, равной 12 мл·см-2·ч-1, увеличение H
5-10% сорбционных центров [11]. Повышение скоро-
приводило к уменьшению специфичной емкости
сти протекания подвижной фазы до 12.0 мл·см-2·ч-1
мочевой кислоты. Это свидетельствует о том, что
значительно улучшало эффективность сорбционной
характер кривых динамики сорбции зависел главным
колонки, при которой достигались максимальные
образом от особенностей структурной организации
сорбционная емкость и степень извлечения мочевой
молекулярно импринтированных сорбентов. Эти осо-
кислоты из раствора (рис. 3, а, кривая 2; табл. 2).
бенности определяли доступность специфических
Можно полагать, что увеличение протекания подвиж-
и неспецифических сорбционных центров и наибо-
ной фазы усиливало вихревые потоки в транспорт-
лее ощутимо проявлялись на колонке с Н = 3.0 см.
ных порах, что создавало дополнительное давление
Поэтому с целью оптимизации динамической сорб-
жидкости внутри полимерной матрицы и улучшало
ции мочевой кислоты на НИС и МИС-40 было про-
ее проницаемость и, следовательно, внутридиффузи-
ведено исследование влияния скорости протекания
онный массоперенос в микроглобулы к труднодоступ-
подвижной фазы на выходные кривые динамики со-
ным сорбционным центрам. Дальнейшее повышение
рбции при Н = 3.0 см (рис. 3, табл. 2). Кроме того,
скорости до 24.0 мл·см-2·ч-1 приводило к более бы-
отношение высоты колонки к диаметру, равное 2-2.5,
строму проскоку мочевой кислоты с колонки и потере
наиболее широко используется в клинике при про-
сорбционной емкости (рис. 3, а, кривая 3; табл. 2).
ведении гемо- и плазмосорбционных процессов [6].
Следует отметить, что описанные эффекты требуют
Неспецифичная сорбция мочевой кислоты на
дополнительных систематических исследований.
НИС характеризовалась необычной зависимостью
В отличие от НИС динамика сорбции мочевой
степени извлечения мочевой кислоты от скорости
кислоты на МИС-40 описывалась обычной зависимо-
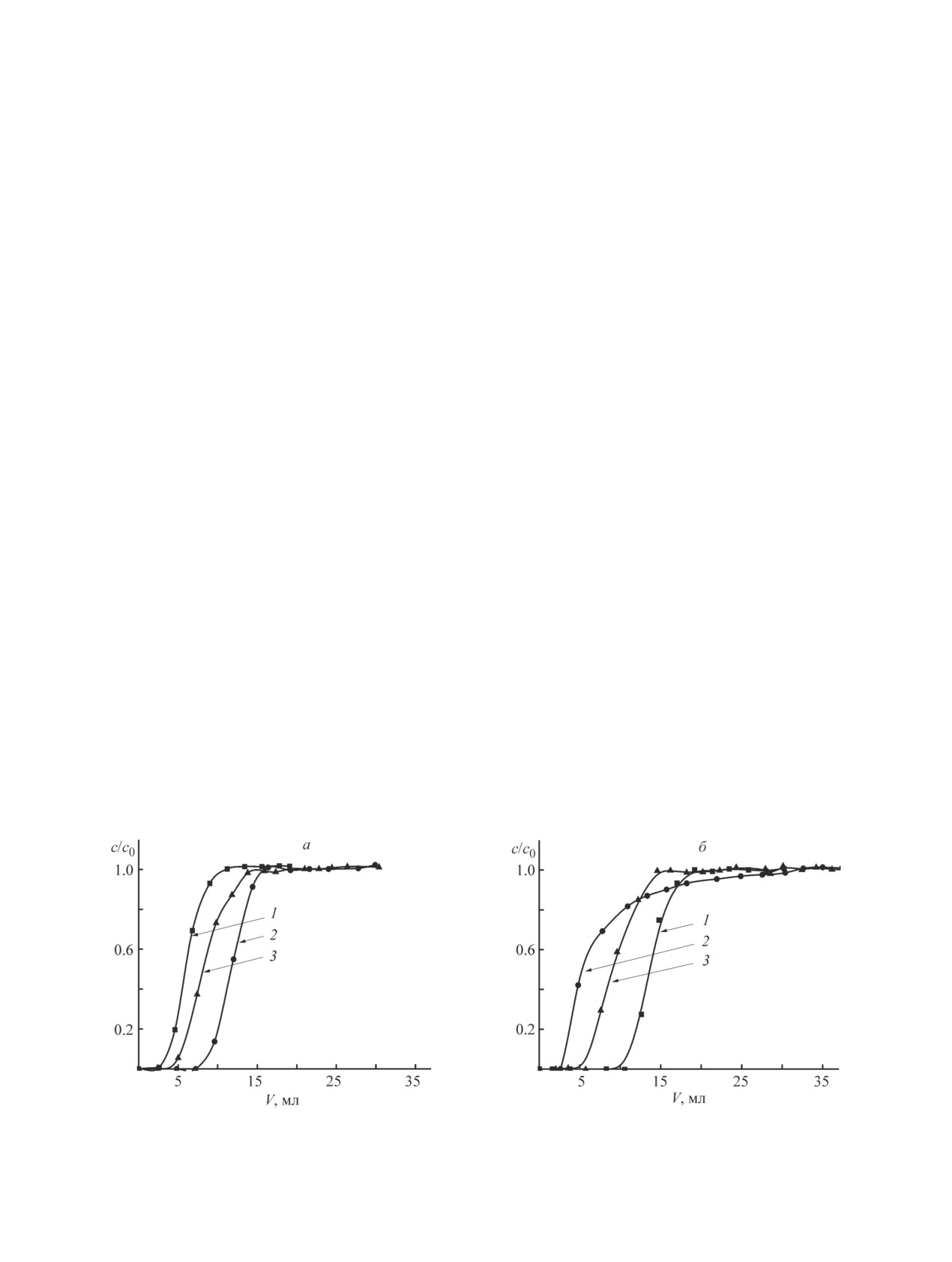
Рис. 3. Динамика сорбции мочевой кислоты на колонках НИС (а) и МИС-40 (б), H = 3.0 см.
V — объем раствора мочевой кислоты, пропущенного через колонку.
Скорость протекания подвижной фазы (мл·см-2·ч-1): 1 — 4.8, 2 — 12.0, 3 — 24.0.
Динамика сорбции мочевой кислоты на молекулярно импринтированном сорбенте
399
Таблица 2
Влияние скорости протекания раствора мочевой кислоты на характеристики динамической сорбции
мочевой кислоты на НИС и МИС-40, H = 3.0 см, qисх ≅ 12.0 мкмоль
qнесорб
qсорб
Сорбент
v, мл·см-2·ч-1
Q, мкмоль·мл-1
IF
R, %
мкмоль
НИС
4.8
8.9
3.1
1.2
54
12.0
6.4
5.6
2.2
—
70
24.0
7.7
4.3
1.7
57
МИС-40
4.8
4.9
7.1
2.5
2.08 ± 0.11
60
12.0
7.3
4.7
1.6
0.71 ± 0.06
39
24.0
7.3
4.7
1.6
0.94 ± 0.07
39
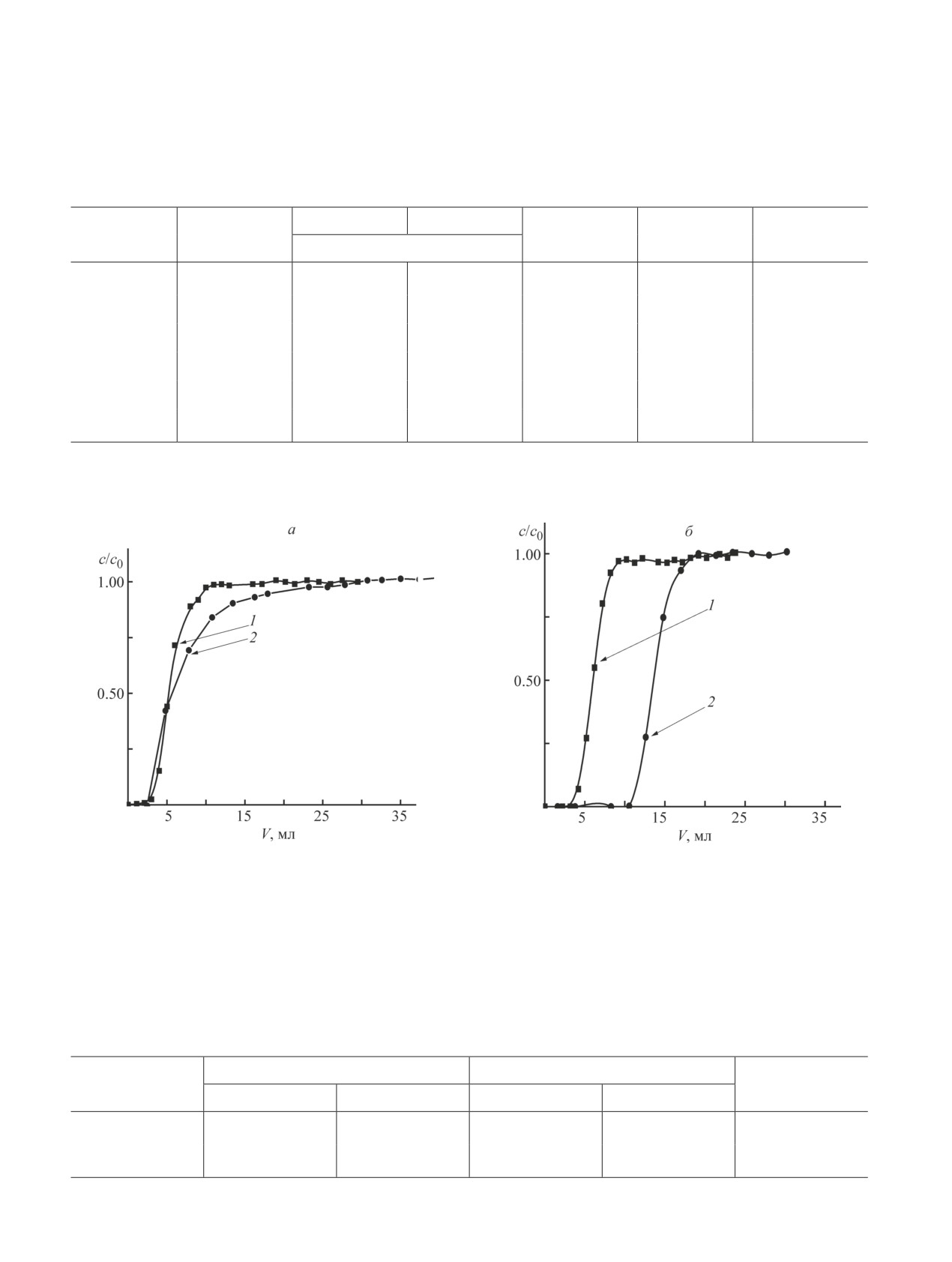
Рис. 4. Динамика сорбции мочевой кислоты и ксантина на НИС (а) и МИС-40 (б).
Скорость протекания подвижной фазы 4.8 мл·см-2·ч-1, H =3.0 см.
1 — ксантин, 2 — мочевая кислота.
Таблица 3
Характеристики динамической сорбции ксантина и мочевой кислоты на НИС и МИС-40
Скорость протекания подвижной фазы 4.8 мл·см-2·ч-1, H = 3.0 см, qисх ≅ 12.0 мкмоль
Ксантин
Мочевая кислота
Сорбент
α
qсорб, мкмоль
Q, мкмоль·мл-1
qсорб, мкмоль
Q, мкмоль·мл-1
НИС
2.8
1.1
3.1
1.2
1.09 ± 0.09
МИС-40
3.1
1.2
7.1
2.5
2.08 ± 0.11
400
Гаркушина И. С. и др.
стью эффективности колонки от скорости протекания
2. На молекулярно импринтированном сорбенте
подвижной фазы (рис. 3, б; табл. 2). При скорости
МИС-40 наблюдался равновесный режим динамики
протекания, равной 4.8 мл·см-2·ч-1, степень извле-
сорбции мочевой кислоты в интервале скоростей
чения мочевой кислоты практически в 1.5 раза пре-
протекания подвижной фазы 4.8-24.0 мл·см-2·ч-1.
вышала степень извлечения при бóльших скоростях.
3. Оптимизированы условия динамического сорб-
Также при этой скорости достигалось значительное
ционного извлечения мочевой кислоты из физиологи-
превалирование вклада специфичного связывания
ческого раствора на молекулярно импринтированном
над неспецифичным (IF > 1). Дальнейшее увеличение
сорбенте МИС-40. Установлено, что наиболее опти-
скорости подвижной фазы приводило к превалирова-
мальный режим сорбции при максимально полной
нию вклада неспецифичного связывания в сорбцию
реализации специфичной емкости достигался при
(IF < 1). Это, по всей видимости, свидетельствовало о
скорости протекания раствора 4.8 мл·см-2·ч-1 на ко-
распределении специфичных импринт-центров преи-
лонке с высотой 3.0 см.
мущественно на поверхности микроглобул в матрице
4. Изучение динамики сорбции мочевой кислоты и
МИС-40.
ксантина показало, что МИС-40 проявляет специфич-
Следует отметить, что скорость протекания под-
ную селективность по отношению к мочевой кислоте
вижной фазы, равная 4.8 мл·см-2·ч-1, соответствует
за счет большего термодинамического сродства им-
скорости 350-450 мл·ч-1 при использовании колонок
принт-сайтов к молекуле мочевой кислоты.
диаметром 5 см. Эта скорость протекания подвижной
фазы наиболее часто используется в клинике при
Финансирование работы
проведении гемо- и плазмосорбционных процессов
[6].
Работа выполнена при поддержке Российского
Селективность сорбции на МИС должна реали-
фонда фундаментальных исследований, грант № 19-
зовываться за счет высокого термодинамического
03-00618.
сродства импринт-сайтов к целевой молекуле, ис-
пользуемой в качестве темплата при синтезе МИС.
Список литературы
Поэтому были изучены фронтальные кривые динами-
ки сорбции мочевой кислоты и ксантина - наиболее
[1] Spivak D. A., Shea K. I. // J. Mol. Recognit. 2012.
близкого структурного аналога мочевой кислоты на
V. 25. N 2. P. 320-382.
[2] Chen L., Wang X., Lu W., Wu X., Li J. // Chem. Soc.
колонках НИС и МИС-40 при H = 3.0 см и скоро-
Rev. 2016. V. 45. N 8. P. 2137-2211.
сти протекания подвижной фазы 4.8 мл·см-2·ч-1, а
[3] Cieplak M., Kutner W. // Trends Biotechnol. 2016.
также рассчитаны коэффициенты селективности α
V. 34. N 11. P. 922-941.
(рис. 4, а, б; табл. 3).
[4] Zaidi S. A. // Biomater. Sci. 2017 V. 5. N 3. P. 388-
Неспецифичная сорбция мочевой кислоты и ксан-
402.
тина на НИС характеризовалась одинаковыми вели-
[5] Pisarev O. A., Polyakova I. V. // React. Funct. Polym.
чинами объемов задержки, при этом наблюдалось
2018. V. 130. N 9. P. 98-110.
незначительно большее сродство НИС к мочевой
[6] Севастьянов В. А. Физико-химические свойства
кислоте по сравнению с ксантином (α = 1.09). Это
и гемосовместимость биоматериалов / Под ред.
свидетельствовало о том, что ксантин в основном
В. А. Севастьянова и М. П. Кирпичникова. М.:
сорбировался на неспецифичных сорбционных сай-
Медицина, 2011. 129 с.
тах. При сорбции мочевой кислоты и ксантина на
[7] Гаркушина И. С., Полякова И. В., Писарев О. А. //
ЖПХ. 2014. Т. 87. № 8. С. 1147-1153 [Garkushi-
МИС-40 объем задержки мочевой кислоты резко воз-
na I. S., Polyakova I. V., Pisarev O. A. // Russ. J. Appl.
растал, а величина α достигала значения 2.08.
Chem. 2014. V. 87. N 8. P. 1126-1132].
[8] Лещинская А. П., Ежова Н. М., Писарев О. А. //
ЖПХ. 2015. Т. 88. № 5. С. 778-784 [Leshinskaya
Выводы
A. P., Ezhova N. M., Pisarev O. A. // Russ. J. Appl.
Chem. 2015. V. 88. N 2. P. 820-825].
1. Радикальной суспензионной сополимеризацией
[9] Leshchinskaya A. P., Ezhova N. M., Pisarev O. A. //
2-гидроксиэтилметакрилата и диметакрилата этилен-
React. Funct. Polym. 2016. V. 102. N 1. P. 101-109.
гликоля синтезированы гранульные молекулярно им-
[10] Stellato D., Morrone L. F., Di Giorgio C., Gesualdo L.
принтированные полимерные сорбенты при введении
// Int. Emerg. Med. 2012. V. 7. N 1. P. 5-18.
темплата мочевой кислоты, а также их неимпринти-
[11] Pisarev O. A., Polyakova I. V. // Trends Chromatogr.
рованный аналог.
2013. V. 7. N 1. P. 85-106.