1112
Кулешов В. Н. и др.
Журнал прикладной химии. 2020. Т. 93. Вып. 8
УДК 544.478-03
ВЫСОКОЭФФЕКТИВНЫЕ ЭЛЕКТРОДЫ
ДЛЯ ЩЕЛОЧНОГО ЭЛЕКТРОЛИЗА ВОДЫ
© В. Н. Кулешов, Н. В. Кулешов, С. В. Курочкин
Национальный исследовательский университет «МЭИ»,
111250, г. Москва, Красноказарменная ул., д. 14
E-mail: KuleshovNV@mpei.ru
Поступила в Редакцию 25 сентября 2019 г.
После доработки 12 мая 2020 г.
Принята к публикации 5 июня 2020 г.
В работе представлено новое пористое покрытие электродов для электролизеров воды со щелочным
электролитом, а также способы его модифицирования катализаторами реакции выделения водорода
и кислорода. Покрытие сформировано из суспензии никель-кобальтового порошка в гальванической
ванне для нанесения никель-кобальтового покрытия и характеризуется игольчатой структурой и
развитой удельной поверхностью. Никель-кобальтовый порошок получен термическим разложением
смешанного формиата никеля-кобальта в среде 1,4-бутандиола, являющегося модифицирующей до-
бавкой гальванических ванн никелирования. Приведены результаты исследований новых электродных
материалов физико-химическими и электрохимическими методами.
Ключевые слова: щелочной электролиз; пористое никель-кобальтовое покрытие электродов; терми-
ческое разложение формиатов металлов в среде многоатомных спиртов
DOI: 10.31857/S004446182008006X
Электролизеры воды со щелочным электроли-
Ni-Co-S или платиной [5]. В частности, в работе [6]
том многие десятилетия используются в атомной
красный фосфор осаждали на металлическую пену
и тепловой энергетике, в водородном цикле нако-
(Ni-Fe) при температуре 600°С, однако авторы отме-
пления энергии, вырабатываемой возобновляемыми
чают, что подобные системы обладают недостаточ-
источниками энергии. Основным преимуществом
ной стабильностью, вследствие чего каталитическая
технологии щелочного электролиза перед электро-
активность электродов значительно снижается через
лизом с твердополимерным электролитом является
несколько десятков часов работы.
отсутствие металлов платиновых группы в составе
Другим направлением разработок высокоэффек-
электрокатализаторов. Кроме того, щелочные элек-
тивных электродов является формирование пористо-
тролизеры могут функционировать при температурах
го никелевого покрытия на поверхности никелевой
окружающей среды ниже -40°С, в то время как твер-
сетчатой подложки методом совместного осажде-
дополимерные электролизеры необратимо теряют
ния частиц никеля и электролитического никеля из
работоспособность при отрицательных температурах.
гальванической ванны никелирования, содержащей
Данный фактор позволяет эффективно использовать
суспензию никелевого порошка. Для дополнитель-
щелочной электролиз на удаленных энергообъектах,
ного снижения перенапряжения выделения водорода
расположенных в условиях Крайнего Севера или на
и кислорода пористое никелевое покрытие модифи-
орбитальных космических станциях.
цировали катализаторами катодных процессов Ni-Px
Энергоэффективность электролизера в первую
и Ni-Mo, а также катализаторами анодных процес-
очередь определяется свойствами диафрагменного
сов — никель-кобальтовой шпинелью NiCo2O4 [7].
материала [1, 2] и электрокаталитической активно-
Электроды, полученные данным способом, обладают
стью катода и анода. Известны работы по приме-
высокой активностью и стабильностью. Коммерчески
нению в щелочном электролизе никелевой пены [3,
доступные никелевые порошки электролитический
4], поверхность которой модифицируют сплавом
(ПНЭ) и карбонильный (ПНК-ОТ2) имеют доста-
Высокоэффективные электроды для щелочного электролиза воды
1113
точно большие размеры частиц: ПНЭ — от 50 до
Получаемый порошок пирофорен и мгновенно
100 мкм, а порошок ПНК-ОТ — 2 до 20 мкм, что огра-
окисляется при контакте с воздухом, поэтому его пе-
ничивает дальнейшее развитие электрохимически
реносили в гальваническую ванну в виде суспензии
активной поверхности и размеров активных центров.
в 1,4-бутандиоле. 1,4-Бутандиол является одной из
Увеличение активной электрохимической поверх-
стандартных рассеивающих добавок к электролиту
ности электрода и снижение размеров активных цен-
для никелирования, позволяющей получать более
тров до субмикрометрового уровня возможно за счет
равномерные покрытия.
применения более мелкодисперсного порошка для
Пористое никель-кобальтовое покрытие наноси-
формирования пористого никелевого покрытия из
ли из электролита состава (г·л-1): NiSO4∙7H2O —
гальванической ванны. Известны способы получе-
350, NiCl2∙6H2O — 60, CoSO4 — 170, CoCl2 — 30,
ния каталитических нанопорошков серебра, железа,
H3BO3 — 60, суспензия никель-кобальтового порош-
кобальта, никеля, меди термическим разложением
ка — 100. Аноды марки АН-2 расположены с двух
формиатов и оксалатов этих металлов [8-10].
сторон покрываемой сетки. Основа электродов с по-
Цель работы — улучшение характеристик элект-
ристым покрытием — никелевая просечно-вытяжная
родов с пористым никелевым покрытием, разработан-
сетка с размером ячейки 1 × 2 мм. Перед началом
ных ранее [7], за счет использования субмикрометро-
нанесения покрытия сетку обезжиривали, протравли-
вого никель-кобальтового порошка, синтезируемого
вали азотной кислотой и подвергали циклированию в
термическим разложением смешанного формиата
гальванической ванне.
никеля-кобальта. Использование в качестве основы
Формирование пористого никель-кобальтового
порошка с субмикрометровым размером частиц по-
покрытия проводили в течение 1 ч при плотности
зволяет увеличить удельную рабочую поверхность
тока 12.3 мА·см-2 и рабочей температуре электролита
пористого покрытия, развить пористость и увеличить
50°C. В процессе электролиза происходит одновре-
число активных центров, необходимых для дальней-
менная адгезия частиц никеля-кобальта и восста-
шего модифицирования катодной реакции выделения
новление ионов никеля и кобальта из электролита,
водорода и кислорода.
что приводит к надежному закреплению порошка
на поверхности сетки и его укрупнению до субми-
крометровых размеров. Сформированное пористое
Экспериментальная часть
покрытие непирофорно.
Смешанный формиат никеля-кобальта осаждали
Электроды с пористым покрытием Ni-Co допол-
формиатом натрия из водного раствора хлоридов
нительно модифицировали катализаторами катод-
никеля и кобальта, взятых в молярном соотношении
ных (Ni-Co-Px) и анодных процессов (NiCo2O4).
1:1. Формиат натрия брали в избытке по отношению к
Для химического осаждения Ni-Co-Px электрод с
стехиометрическому молярному количеству хлоридов
пористым никель-кобальтовым покрытием погру-
никеля и кобальта. Отфильтрованный и промытый
жали в раствор состава (г·л-1): NiCl2∙6H2O — 20,
осадок высушивали при температуре 50°С, затем
CoCl2·6H2O — 10; NaH2PO2∙10H2O — 10. Осаждение
измельчали с помощью планетарной мельницы SPEX
проводили при температуре 30°С, время осаждения
(США) и отсеивали на виброгрохоте Sieve Shaker
1 ч. Формирование никель-кобальтовой шпинели про-
M100 (Великобритания) с ситом 20 мкм.
водили термическим разложением нитратов никеля
В качестве рабочей среды для термического разло-
и кобальта. Сетку с пористым никель-кобальтовым
жения смешанного формиата никеля-кобальта выбран
покрытием погружали в раствор Ni(NO3)2 и Co(NO3)2
двухосновный спирт — 1,4-бутандиол с температурой
в изопропиловом спирте. Нитраты никеля и кобальта
кипения 235°С. Термическое разложение проводи-
брали в молярном соотношении 1:2. Пропитанный
ли в закрытом реакторе при постоянном перемеши-
раствором нитратов электрод с пористым покрытием
вании, пропуская через раствор диоксид углерода
помещали в кварцевую трубку, нагревали до тем-
(CO2). Разложение формиата никеля-кобальта про-
пературы 250°С, выдерживали в течение 2 ч, затем
исходит в восстановительной атмосфере CO и H2 по
повышали температуру со скоростью 1 град/5 мин
реакциям [8]
до 300°С и дополнительно выдерживали еще 3 ч.
Для формирования плотного слоя шпинели операцию
Me(HCOO)2 → Me + CO + CO2 + H2O,
(1)
повторяли 3 раза.
Me(HCOO)2 → Me + 2CO2 + H2,
(2)
Микрофотографии получены на сканирую-
щем электронном микроскопе JEOL JSM-6380 LA
где Me — Ni и Co.
(Япония). Анализ процентного содержания кобальта
1114
Кулешов В. Н. и др.
в электроосажденном покрытии на просечно-вытяж-
исследований методом контактно-эталонной пороме-
ной сетке проводили по градуировочной зависимо-
трии (рис. 3).
сти методом лазерной атомно-эмиссионной спек-
Пористое покрытие, полученное осаждением из
троскопии SPEX LAES Matrix (Россия). Удельную
суспензии порошка Ni-Co, характеризуется отно-
площадь поверхности электродов исследовали ме-
сительно узким интервалом распределения пор по
тодом контактно-эталонной порометрии на прибо-
радиусам в области 1-2 мкм и удельной пористостью
ре Porotech (Канада). Исследования электрохимиче-
до 2.3 см3·г-1. При модифицировании пористого по-
ской активности полученных электродов проводили
крытия катализатором реакции выделения водорода
в трехэлектродной ячейке с помощью потенциостата
Ni-Co-Px удельная пористость покрытия изменяется
SolartronParstat 1587 (Великобритания) при 80°C в
незначительно, но развитие пористости обусловле-
0.1 М растворе KOH . В качестве электрода сравнения
но нанопорами с радиусами в интервале 40-80 нм.
использовали ртутно-оксидный электрод, вспомога-
Удельная пористость электродов, модифицирован-
тельный электрод — платиновый площадью 2 см2 и
ных катализатором реакции выделения кислорода
толщиной 1 мм.
NiCo2O4, также незначительно отличается от немо-
дифицированного пористого покрытия. При этом
катализатор на основе никель-кобальтовой шпинели
характеризуется наиболее широким интервалом рас-
Обсуждение результатов
пределения пор по радиусам — 1-5 мкм.
Частицы пористого покрытия имеют игольчатую
Сопоставление поляризационных кривых реакции
структуру (рис. 1, а) с длиной, значительно превы-
выделения водорода на никелевой сетке (рис. 4, а,
шающей поперечное сечение. Структура катализа-
кривая 1) и на пористом никель-кобальтовом покры-
тора катодных процессов Ni-Co-Px (рис. 1, б) также
тии (рис. 4, а, кривая 2) и реакции выделения кис-
имеет развитую поверхность и повторяет игольчатую
лорода на никелевой сетке (рис. 4, б, кривая 1) и на
структуру пористого покрытия, но размер частиц
пористом никель-кобальтовом покрытии (рис. 4, б,
уменьшается.
кривая 2) показывает, что электроды с пористым ни-
Содержание кобальта в пористом никель-кобаль-
кель-кобальтовым покрытием характеризуются бо-
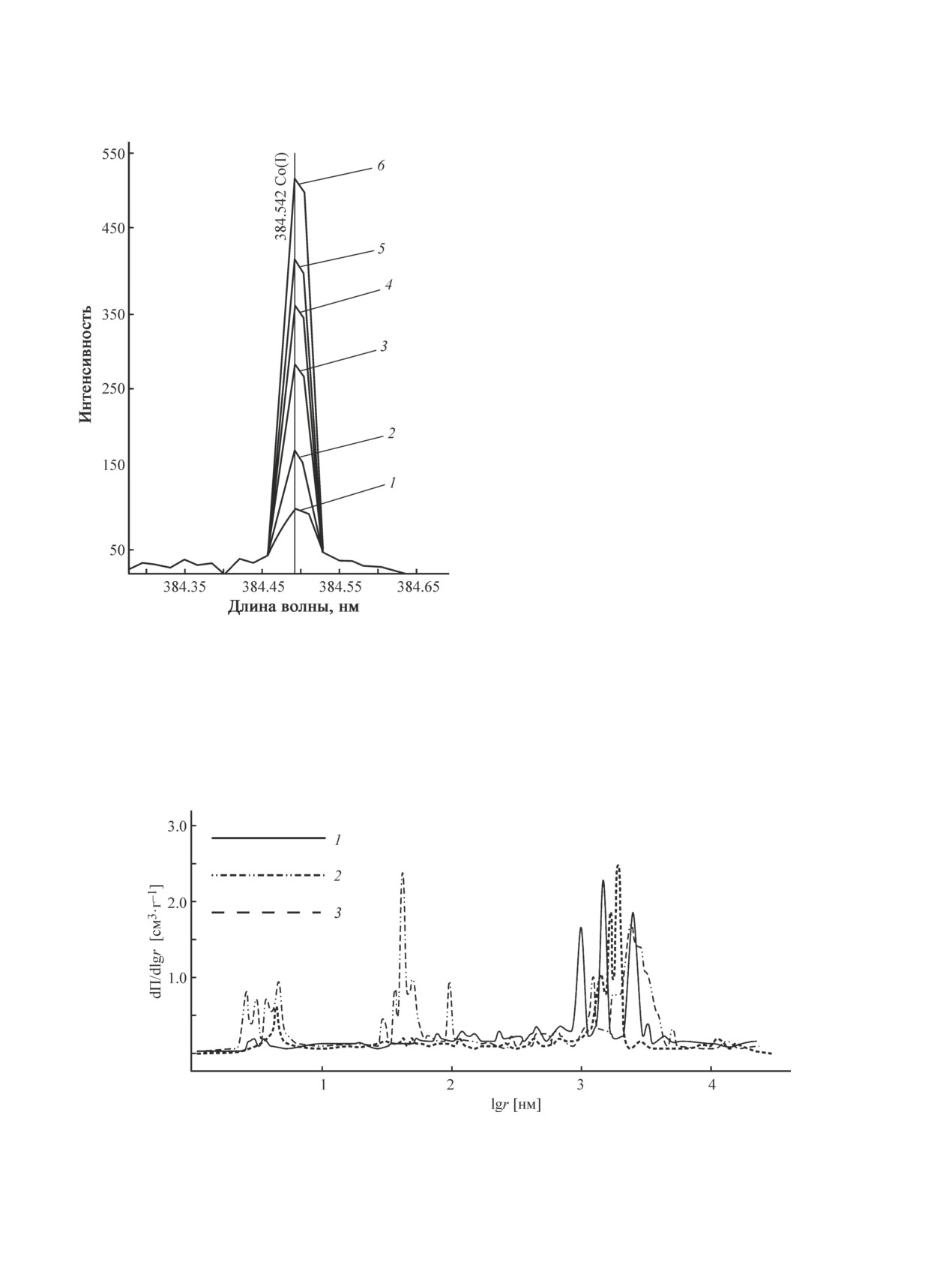
товом покрытии составляет 17 мас%, на рис. 2 при-
лее развитой удельной поверхностью по сравнению
ведены спектры атомной эмиссии, полученные для
с гладкой никелевой сеткой (подложкой электрода
построения градуировочной зависимости.
без покрытия). Изменение угла наклона поляриза-
Данные микроскопии о развитии поверхности
ционных кривых позволяет судить об изменении ме-
и снижении размера частиц при модифицировании
ханизма реакций выделения водорода и кислорода.
пористого никель-кобальтового покрытия катализа-
В реакциях выделения водорода перенапряжение
тором Ni-Co-Px хорошо коррелируют с результатами
может быть снижено на 110-120 мВ при 300 мА·см-2.
Рис. 1. Микрофотографии электродов.
Пористое покрытие, полученное осаждением никель-кобальтового порошка: а — исходное, б — модифицированное
катализатором Ni-Co-Px.
Высокоэффективные электроды для щелочного электролиза воды
1115
Увеличение активности может быть объяснено фор-
мированием кристаллической решетки с более высо-
кой энергией связи атомов Ni-Co с атомами водоро-
да по сравнению с чистым никелем. Использование
электродов с никель-кобальтовым покрытием позво-
ляет снизить перенапряжение выделения кислорода
на 100-110 мВ при 300 мА·см-2. Из более ранних ис-
следований [11] известно, что снижению перенапря-
жения выделения кислорода способствует образова-
ние переходных оксидов металлов, например Ni2O3.
Можно предположить, что снижение перенапряжения
может быть связано с образованием развитой струк-
туры поверхностных оксидов на активных центрах
пористого никель-кобальтового покрытия.
Модифицирование электродов катализатором
Ni-Co-Px позволяет снизить перенапряжение реак-
ции выделения водорода на 80-100 мВ относитель-
но немодифицированного пористого покрытия и на
200-220 мВ относительно гладкой никелевой сетки
без покрытия при 300 мА·см-2. Тангенс угла накло-
на поляризационных кривых (параметр b уравнения
Тафеля реакции выделения водорода на пористом
никель-кобальтовом покрытии, модифицированном
катализатором Ni-Co-Px) отличается от параметра b,
рассчитанного для реакции, протекающей на нике-
Рис. 2. Атомно-эмиссионный спектр кобальта в составе
левой сетке и электроде с пористым никель-кобаль-
пористого электрода, полученного электроосаждением
товым покрытием (см. таблицу). Каталитический
смешанного порошка Ni-Co.
эффект катализатора Ni-Co-Px может быть объяснен
Содержание кобальта в образцах, приготовленных для
образованием поверхностно-полимерных гидрок-
построения градуировочной зависимости (%): 1 — 3,
2 — 7, 3 — 13, 4 — 17, 5 — 20, 6 — 28.
сильных и других активных аморфных пленок.
Рис. 3. Дифференциальное распределение пор по радиусам.
Электрод с пористым никель-кобальтовым покрытием: 1 — исходный, 2 — модифицированный Ni-Co-Px, 3 — моди-
фицированный NiCo2O4.
1116
Кулешов В. Н. и др.
Рис. 4. Поляризационные кривые катализаторов.
а — реакция выделения водорода.
1 — никелевая сетка; 2 — пористое Ni-Co-покрытие; 3 — пористое Ni-Co-покрытие, модифицированное Ni-Co-Px.
б — реакция выделения кислорода.
1 — никелевая сетка; 2 — пористое Ni-Co-покрытие; 3 — пористое Ni-Co-покрытие, модифицированное NiCo2O4.
Параметры уравнения Тафеля реакций выделения водорода и кислорода
Катализаторы катодных процессов
Катализаторы анодных процессов
катализатор
b, мВ
i0, мА·см-2
катализатор
b, мВ
i0, мА·см-2
Ni-Сетка (гладкий никель)
-102
0.008
Ni-Сетка (гладкий никель)
95
9.666·10-3
Пористое покрытие
-82
0.044
Пористое покрытие
72
3.468·10-3
Пористое покрытие + Ni-Co-Px
-55
0.052
Пористое покрытие + NiCo2O4
66
3.892·10-3
Перенапряжение реакции выделения кислорода
ров воды со щелочным электролитом. Установлено,
может быть снижено дополнительным модифициро-
что по сравнению с сетчатой никелевой подложкой
ванием пористого электрода катализатором реакции
пористое покрытие позволяет снизить перенапряже-
выделения кислорода — никель-кобальтовой шпи-
ние выделения водорода на 100-110 мВ, а перена-
нелью (рис. 4, б, кривая 3) на 40-50 мВ по сравне-
пряжение выделения кислорода на 100-110 мВ при
нию с немодифицированным пористым покрытием
плотности тока 300 мА·см-2. Показано, что допол-
(рис. 4, б, кривая 2) и на 210-220 мВ по сравнению
нительное модифицирование нового пористого по-
с гладкой никелевой сеткой без покрытия (рис. 4, б,
крытия катализатором катодных процессов Ni-Co-Px
кривая 1) при 300 мА·см-2. Сравнение параметров b
позволяет дополнительно снизить перенапряжение
уравнения Тафеля может свидетельствовать о том,
выделения водорода на 80-100 мВ при 300 мА·см-2.
что механизм реакции выделения кислорода на элек-
Модифицирование пористого никель-кобальтово-
тродах с пористым никель-кобальтовым покрытием и
го покрытия катализаторами анодных процессов
покрытием, модифицированным никель-кобальтовой
NiCo2O4 позволяет дополнительно снизить перена-
шпинелью, имеет схожий характер и отличается от
пряжение реакции выделения кислорода на 40-50 мВ
механизма реакции выделения кислорода на гладкой
при 300 мА·см-2.
никелевой сетке без покрытия.
Благодарности
Выводы
Исследования проведены в рамках госзадания
Разработано пористое никель-кобальтовое покры-
№ 13.2052.2017 (проектная часть) Министерства на-
тие сетчатых никелевых электродов для электролизе- уки и высшего образования Российской Федерации.
Высокоэффективные электроды для щелочного электролиза воды
1117
Конфликт интересов
nanosheets on Co3O4 nanoarrays as an advanced overall
water splitting electrocatalyst in alkaline solution //
Авторы заявляют об отсутствии конфликта инте-
J. Alloys Compd. 2019. V. 791. P. 328-335. https://
ресов, требующего раскрытия в данной статье.
[5]
Pierozynski B., Mikolajczyk T., Luba M., Zolfaghari A.
Информация об авторах
Kinetics of oxygen evolution reaction on nickel foam
and platinum-modified nickel foam materials in
Кулешов Николай Васильевич, проф., д.т.н.,
alkaline solution // J. Electroanal. Chem. 2019. V. 847.
P. 113-194.
Кулешов Владимир Николаевич, доц., к.т.н.,
[6]
Ma Z., Li R., Wang M., Meng H., Zhang F., Bao X.,
Курочкин Семен Васильевич,
Tang B., Wang X. Self-supported porous Ni-Fe-P
composite as an efficient electrocatalyst for hydrogen
evolution reaction in both acidic and alkaline medium
// Electrochim. Acta. 2016. V. 219. P. 194-203. http://
Список литературы
[1]
Кулешов Н. В., Кулешов В. Н., Довбыш С. А.,
[7]
Kuleshov V., Kuleshov N., Grigoriev S., Udris E.,
Курочкин С. В., Удрис Е. Я., Славнов Ю. А.
Millet P., Grigoriev A. Development and
Полимерные диафрагмы на основе полисульфона
characterization of new nickel coatings for application
для электрохимических устройств со щелочным
in alkaline water electrolysis // Int. J. Hydrogen
электролитом // ЖПХ. 2018. Т. 91. № 6. С. 802-
Energy. 2016. V. 41. P. 36-45.
805 [Kuleshov N. V., Kuleshov V. N., Dovbysh S. A.,
Kurochkin S. V., Udris E. Y., Slavnov Y. A. Polysulfone-
[8]
based polymeric diaphragms for electrochemical
Анкудинов А.
Синтез нанопорошков никеля в дина-
devices with alkaline electrolyte // Russ. J. Appl. Chem.
мических условиях // Рос. нанотехнологии. 2018.
2018. V. 91. N 6. P. 930-933.
Т. 13. № 11-12. С. 3-7.
[2]
Vermeiren Ph., Adriansens W., Moreels JP., Leysen R.
[9]
Shishido T., Takehira K. Preparation of highly
Evaluation of the Zirfon separator for use in alkaline
dispersed Ni catalysts for H2 production for polymer
water electrolysis and Ni-H2 batteries // Int. J.
electrolyte fuel cells // J. Japan Petrol. Inst. 2015.
Hydrogen Energy. 1998. V. 23. N 5. P. 321-324. https://
V. 58. N 6. P. 353-364.
[3]
Zhang D., He W., Zhang Z., Xu X. Structure-design and
[10]
Шпильрайн Э., Малышенко С., Кулешов Г. Введение
synthesis of Nickel-Cobalt-Sulfur arrays on nickel foam
в водородную энергетику. М.: Энергоатомиздат,
for efficient hydrogen evolution // J. Alloys Compd.
1984. С. 82-84.
2019. V. 785. P. 468-474.
[11]
Łosiewicz B., Popczyk M. Effect of heat treatment
on the structure of Ni-P electrocoatings // Solid
[4]
Xiong T., Li G., Young D., Tan Z., Yin X., M Y., Hu F.
State Phenom. 2015. V. 228. P. 148-152. https://
In-situ surface-derivation of Ni-Mo bimetal sulfides