1118
Шевцов Д. С. и др.
Журнал прикладной химии. 2020. Т. 93. Вып. 8
УДК 620.197.3
ИНГИБИРОВАНИЕ КОРРОЗИИ МЕДИ N-АРИЛАМИНОТРИАЗОЛАМИ
В ВОДНЫХ ХЛОРИДНЫХ РАСТВОРАХ И В АТМОСФЕРНЫХ УСЛОВИЯХ
© Д. С. Шевцов1, Х. С. Шихалиев1*, Е. С. Комарова1, А. А. Кружилин2,
Г. О. Киприянова1, А. Ю. Потапов1, И. Д. Зарцын1, О. А. Козадеров1,
Ч. Прабхакар3, А. Трипати3
1 Воронежский государственный университет,
394018, г. Воронеж, Университетская пл., д. 1
2 Воронежский государственный аграрный университет,
394087, г. Воронеж, ул. Мичурина, д. 1
3 Национальный технологический институт Курукшетра,
Харьяна, 136119, Индия
Поступила в Редакцию 21 мая 2019 г.
После доработки 16 марта 2020 г.
Принята к публикации 25 мая 2020 г.
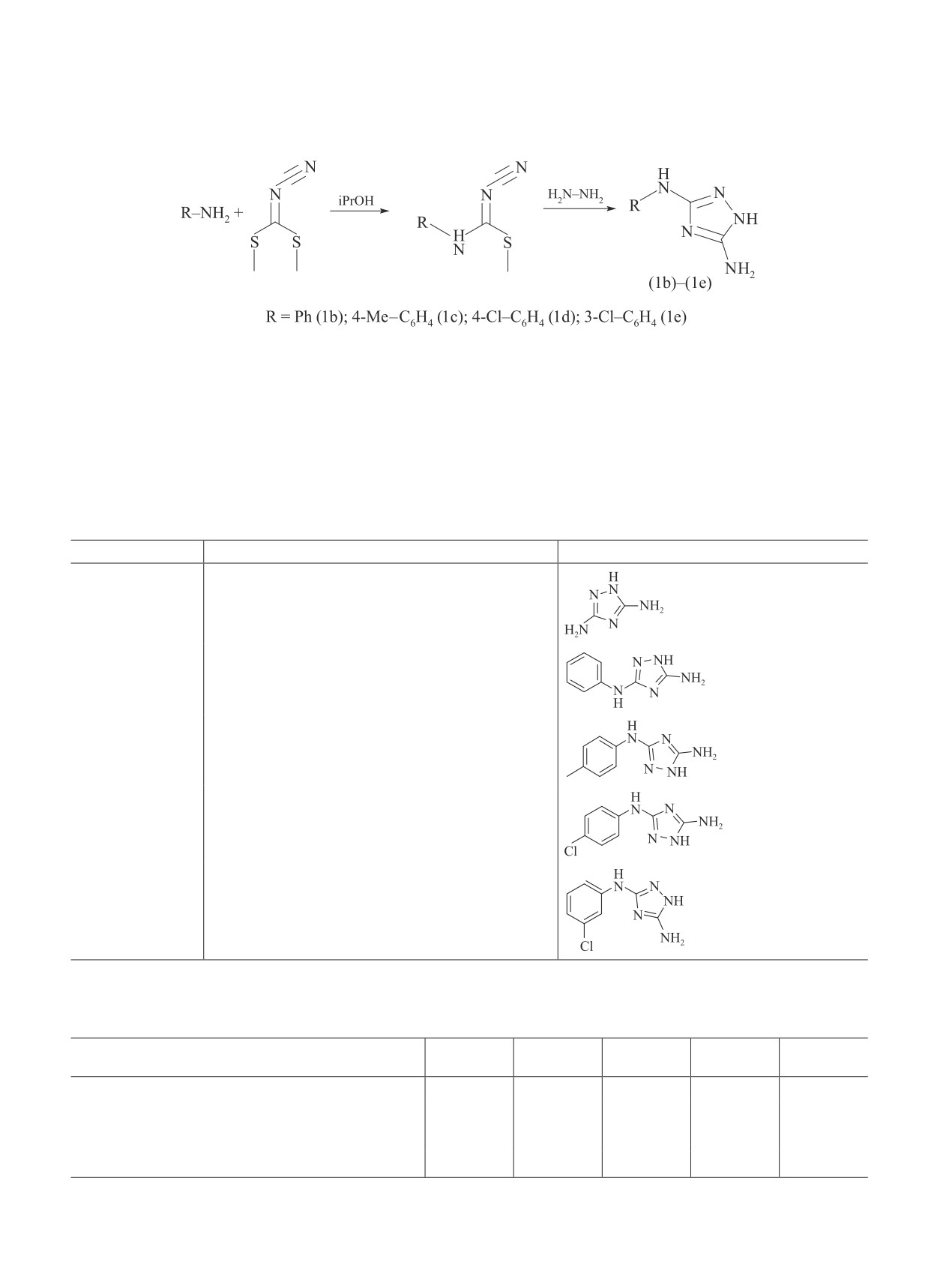
Взаимодействием S,S-диметилцианодитиоимидокарбамата с некоторыми анилинами получены со-
ответствующие 3-(N-ариламино)-5-амино-1Н-1,2,4-триазолы. Изучено их ингибирующее действие
на коррозию меди марки М1 в кислых и нейтральных хлоридсодержащих средах с применением элек-
трохимических и ускоренных натурных методов. Максимальная степень защиты для коммерчески
доступного 3,5-диамино-1H-1,2,4-триазола и синтезированных 3-фениламино-, 3-(4-метилфенилами-
но)-, 3-(4-хлорфениламино)- и 3-(3-хлорфениламино)производных 5-амино-1Н-1,2,4-триазола дости-
гает 70-87%. В кислой среде синтезированные вещества эффективнее 3,5-диаминопроизводного и
обеспечивают степень защиты до 92-96%. Аналогичные результаты получены в ходе экспериментов
в камере соляного тумана.
Ключевые слова: синтез in situ; медь; ингибиторы коррозии; хлориды; 3-(N-ариламино)-5-ами-
но-1Н-1,2,4-триазолы
DOI: 10.31857/S0044461820080071
При эксплуатации металлов в различных средах
Наиболее изученным ингибитором коррозии ме-
одним из распространенных подходов к уменьшению
ди класса азолов является 1,2,3-бензотриазол [5-7],
скорости их коррозии является применение орга-
широко применяемый для защиты цветных метал-
нических ингибиторов данного процесса. Широкое
лов и в настоящее время. Однако не только произ-
применение для защиты меди и сплавов на ее основе
водные бензотриазола, но и некоторые другие, бо-
получили такие органические соединения, как азолы
лее гидрофильные триазолы привлекают внимание
[1, 2]. Несмотря на обширную номенклатуру уже
исследователей для защиты меди и ее сплавов. Так,
известных соединений с доказанным защитным дей-
3-амино-1,2,4-триазол эффективнее бензотриазола
ствием, синтез новых перспективных ингибиторов
предотвращает образование питтинга на меди в бо-
коррозии как для конкретного металла в конкретной
ратном буферном растворе, содержащем хлориды
среде, так и универсальных ингибиторов для ряда
или сульфаты [8]. Зачастую повышение эффектив-
металлов и сплавов, эксплуатируемых в различных
ности таких ингибиторов достигается введением в
условиях, по-прежнему является актуальным направ-
триазольный цикл гидрофобного заместителя. Это
лением исследований [3, 4].
снижает их растворимость в воде и может приводить
Ингибирование коррозии меди N-ариламинотриазолами в водных хлоридных растворах и в атмосферных условиях
1119
к нарушению работы оборудования, в том числе за
Электрохимические исследования проводили
счет образования агломератов частиц с последующим
в боратном буферном растворе рН 7.40 на основе
засорением проводящих каналов [9, 10]. Получение
дистиллированной воды с добавкой 10 мМ NaCl.
ингибиторов коррозии с высокими защитными свой-
Поляризационные кривые регистрировали в трех-
ствами и удовлетворительной растворимостью явля-
электродной электрохимической ячейке с неразде-
ется важной научно-практической задачей.
ленными электродными пространствами на потен-
Цель работы
— синтез соединений класса
циостате IPC-PRO. Рабочий электрод, изготовленный
3-(N-ариламино)-5-амино-1Н-1,2,4-триазолов и изу-
из меди М1 (площадь 0.75 cм2), предварительно за-
чение их защитного действия по отношению к меди
чищали на наждачных бумагах до крупности К3000
в водных нейтральных и кислых растворах, содер-
и обезжиривали ацетоном. Потенциалы электрода (Е)
жащих хлорид-ионы, в сравнении с коммерчески
измеряли относительно хлоридсеребряного электрода
доступными аналогами.
и пересчитывали на нормальную водородную шкалу.
Вспомогательный электрод — платина.
После удаления образованной на воздухе пленки
Экспериментальная часть
оксида меди при Е = -0.60 В в течение 15 мин по-
3,5-Диамино-1H-1,2,4-триазол (1a) производ-
тенциостат отключали до установления потенциала
ства Sigma-Aldrich, inc. CAS 1455-77-2 использо-
свободной коррозии (Екор). Далее при перемешивании
вали в качестве коммерчески доступного продукта.
вводили раствор NaCl (сCl- = 10 ммоль·л-1) и иссле-
S,S-Диметилцианодитиоимидокарбамат получали по
дуемые ингибиторы в концентрации синг = 0.01, 0.10
методике, описанной в [11].
и 1.00 ммоль·л-1. После установления нового значе-
Общая методика синтеза 3-(N-ариламино)-
ния Екор регистрировали поляризационные кривые
5-амино-1Н-1,2,4-триазолов (1b)-(1e). К 0.1 моль
с разверткой потенциала 0.2 мВ·с-1 в катодном и
S,S-диметилцианодитиоимидокарбамата приливали
анодном направлениях. Потенциал активации (Еакт)
0.1 моль соответствующего анилина. Смесь кипяти-
определяли по резкому росту тока на анодном участке
ли в течение 3-4 ч в изопропиловом спирте. После
поляризационной кривой с последующей визуальной
полной конверсии амина к смеси добавили 0.2 моль
идентификацией питтинга на поверхности электрода.
гидразин-гидрата и кипятили в течение 1 ч. Осадок
Погрешность в измерении Еакт составила 0.03 В.
отфильтровали и промыли горячим изопропанолом.
Для расчета скорости коррозии по достижении
Спектры ЯМР 1H были получены на приборе
стационарного состояния производили поляризацию
Bruker DRX-500 (рабочая частота 500 и 125.8 МГц)
электрода в интервале ±30 мВ от значения Екор в по-
в импульсном Фурье-режиме в ДМСО-d6. Отнесение
тенциодинамическом режиме со скоростью развертки
сигналов проведено относительно остаточных сигна-
0.2 мВ·с-1.
лов протона дейтерорастворителя или тетраметилси-
Поляризационное сопротивление (Rp) определяли
лана как внутреннего стандарта. Хроматографический
как наклон поляризационной кривой в точке Екор в
анализ чистоты полученного соединения проводили
координатах ΔE (E-Екор)-i. Получали зависимость в
на жидкостном хроматографе Agilent 1260 Infinity с
координатах 2.3Rpi-ΔE. Коэффициенты ba и bc (тафе-
УФ- и масс-детектированием (времяпролетный де-
левские наклоны анодной и катодной полуреакций)
тектор масс высокого разрешения Agilent 6230 TOF
определяли с помощью программы TableCurve 2D как
LC/MS, ионизация электрораспылением). Условия хро-
параметры аппроксимации уравнения
матографирования: колонка Gemini C18 (4.6 × 50 мм);
диаметр частиц сорбента 5 мкм; линейное гради-
ентное элюирование; подвижная фаза: элюент А —
MeCN-Н2О, 2.5:97.5, 0.1% CF3COOH, элюент В —
Скорость коррозии рассчитывали по уравне-
MeCN, 0.1% CF3COOH, скорость потока подвижной
фазы 3.75 мл·мин-1; температура колонки 40°С; объем
нию
с учетом полученных коэффициентов.
инжекции 1.5 мкл. Температуры плавления опре-
делены на приборе Stuart SMP30. Промежуточный
Подобная методика расчета скорости коррозии была
контроль полноты конверсии и чистоты получаемых
предложена Мансфельдом [12] и апробирована для
веществ осуществляли методом ТСХ на пластинках
меди в нейтральном хлоридном растворе [13, 14].
Silufol UV-254. В качестве элюента использовали
Эффективность ингибирующего действия производ-
системы хлороформ-метанол; проявление хрома-
ных 5-амино-1H-1,2,4-триазола оценивали по степени
тограмм осуществлялось в УФ-свете и парах иода.
защиты:
1120
Шевцов Д. С. и др.
где iкор,0 и iкор,инг — плотность тока коррозии в отсут-
где k0 и kинг — скорость коррозии в растворе HCl в от-
сутствие и в присутствии ингибитора соответственно.
ствие и в присутствии ингибитора соответственно.
Параметр k0 составлял 40-44 г·м-2·сут-1. Иссле-
Натурными испытаниями в камере соляного ту-
дование антикоррозионного действия проводили
мана моделировали атмосферную коррозию меди с
для систем с концентрацией ингибитора 1.0, 5.0 и
целью выявить ингибирующий эффект производных
10.0 ммоль·л-1.
5-амино-1H-1,2,4-триазола для межоперационной
защиты медных изделий. Исследования проводили
на медных пластинах, которые предварительно зачи-
Обсуждение результатов
щали на наждачной бумаге различной зернистости,
Целевые 3-(N-ариламино)-5-амино-1Н-1,2,4-
полировали и обезжиривали ацетоном. Защитную
триазолы (1b)-(1e) синтезировали в две стадии:
пленку ингибиторов получали выдержкой пластин
реакцией соответствующих анилинов с S,S-диме-
в водном растворе с добавкой ингибиторов в тече-
тилцианодитиоимидокарбаматом и последующим
ние 60 мин при температуре 60°C. Образцы высу-
взаимодействием промежуточных продуктов с гидра-
шивали и помещали в камеру, внутри которой еже-
зин-гидратом. В ходе мониторинга условий синтеза
часно распыляли 5%-ный водный раствор NaCl
аминотриазолов (1b)-(1e) установлено, что стадия
(pH 6.5-7.2, ГОСТ Р 52763-2007) и поддерживали
относительную влажность воздуха 95-100%. Осмотр
получения N-циано-1-карбимидотиоатов протекает
образцов проводили 3 раза в сутки, чтобы определить
практически количественно. При точном контроле
конверсии исходных соединений это позволяет избе-
время появления первого коррозионного поражения
жать необходимости выделения и очистки образую-
(τкор).
щихся промежуточных N-циано-1-карбимидотиоатов
Коррозионные испытания проводили в соот-
и проводить вторую стадию процесса с добавлением
ветствии с ГОСТ 9.905-82 «Методы коррозион-
гидразин-гидрата непосредственно в реакционный
ных испытаний» на медных пластинах площадью
сосуд. Благодаря этому удается снизить массовые
S = 20 × 50 мм2 и толщиной d = 0.2 мм. Каждый об-
потери и сократить общее время синтеза целевых
разец предварительно полировали мелкозернистой
соединений. В результате получены 3-(N-ариламино)-
шлифовальной бумагой К1000, промывали дистилли-
рованной водой, этанолом и сушили фильтровальной
5-амино-1Н-1,2,4-триазолы (1b)-(1e) (табл. 1, 2), ана-
бумагой. Эксперименты продолжительностью 7 сут
логичные по чистоте и характеристикам продуктам,
получаемым постадийно (см. схему).
проводили с тремя образцами одновременно в не-
Спектры ЯМР 1H синтезированных соединений
перемешиваемом, естественно аэрируемом 1%-ном
(табл. 3) содержат характерные сигналы NH-протона
водном растворе HCl. После испытаний пластины
соответствующих триазольных циклов в области
промывали дистиллированной водой и обрабатыва-
11.05-11.25 м. д. Протон вторичных аминогрупп,
ли в соответствии с ГОСТ 9.907-83 «Методы уда-
связанных с бензольным и триазольным циклами,
ления продуктов после коррозионных испытаний».
находится в области 8.40-8.92 м. д. Наборы про-
Скорость коррозии определяли по потере массы об-
тонов ароматических систем присутствуют в виде
разцов и рассчитывали по формуле
соответствующих триплетов и дублетов в районе
6.70-7.75 м. д.
При введении изученных ингибирующих до-
бавок в хлоридный раствор не было выявлено од-
где m0 и m — масса образца до и после коррозионных
нонаправленного изменения Екор (табл. 4). При
испытаний соответственно.
добавлении 3,5-диамино-1H-1,2,4-триазолов до
Эффективность ингибирующего действия про-
достижения концентрации в растворе синг ≤ 0.10 и
изводных 5-амино-1H-1,2,4-триазола оценивали по
синг = 1.00 ммоль·л-1 для 3-(4-хлорфениламино)-5--
величине коэффициента торможения
амино-1Н-1,2,4-триазола не выявлено различимого
изменения Екор. Только для 3-фениламино-5-ами-
но-1Н-1,2,4-триазола отмечено смещение в анодную
область на более чем 50 мВ. Для остальных добавок
и степени защиты
получено смещение Екор в катодную сторону.
Ингибирование коррозии меди N-ариламинотриазолами в водных хлоридных растворах и в атмосферных условиях
1121
Схема синтеза N-замещенных 1H-1,2,4-триазол-3,5-диаминов
В электрохимических исследованиях не пред-
Электрохимическое поведение медного электрода
ставлены данные для 3-(3-хлорфениламино)-5-ами-
в присутствии 3,5-диамино-1H-1,2,4-триазола (рис. 1)
но-1Н-1,2,4-триазола по причине его разложения на
отличается от случаев с добавкой соединений (1b)-
стадии приготовления рабочего раствора для последу-
(1d). Плотность тока на анодном участке поляриза-
ющего разбавления, что ограничивает его применение.
ционной кривой для концентрации 0.01 ммоль·л-1
Таблица 1
Структуры исследованных 3-(N-ариламино)-5-амино-1Н-1,2,4-триазолов
Обозначение
Название
Структурная формула
(1a)
3,5-Диамино-1H-1,2,4-триазол
(1b)
3-Фениламино-5-амино-1Н-1,2,4-триазол
(1c)
3-(4-Метилфениламино)-5-амино-1Н-1,2,4-триазол
(1d)
3-(4-Хлорфениламино)-5-амино-1Н-1,2,4-триазол
(1e)
3-(3-Хлорфениламино)-5-амино-1Н-1,2,4-триазол
Таблица 2
Физико-химические характеристики синтезированных 3-(N-ариламино)-5-амино-1Н-1,2,4-триазолов
Брутто-
Вычислено
Найдено
Соединение
Тпл, °C
Выход, %
формула
[М + H]+
[М + Н]+
3-Фениламино-5-амино-1Н-1,2,4-триазол
C8H9N5
175.0961
175.0963
166-169
95
3-(4-Метилфениламино)-5-амино-1Н-1,2,4-триазол
C9H11N5
190.1065
190.1107
162-164
84
3-(4-Хлорфениламино)-5-амино-1Н-1,2,4-триазол
C8H8ClN5
209.0511
209.0541
161-163
77
3-(3-Хлорфениламино)-5-амино-1Н-1,2,4-триазол
C8H8ClN5
209.0511
209.0527
158-160
73
1122
Шевцов Д. С. и др.
Таблица 3
Спектры ЯМР 1Н синтезированных 3-(N-ариламино)-5-амино-1Н-1,2,4-триазолов
Соединение
Спектр ЯМР 1Н, δ, м. д. (J, Гц)
3-Фениламино-5-амино-1Н-1,2,4-триазол
5.87 (2H, уш. с., NH2), 6.71 (1H, т., J = 7.3, CH-аром.), 7.15 (2H, т.,
J = 7.8, CH-аром.), 7.49 (2H, д., J = 7.9, CH-аром.), 8.62 (с., 1H,
NH), 11.20 (уш. с., 1H, NH-триаз.)
3-(4-Метилфениламино)-5-амино-1Н-1,2,4-триазол
2.18 (3H, с., CH3), 5.80 (2H, уш. с., NH2), 6.71 (2H, д., J = 7.9,
CH-аром.), 7.38 (2H, д., J = 7.9, CH-аром.), 8.40 (с., 1H, NH),
11.05 (уш. с., 1H, NH-триаз.)
3-(4-Хлорфениламино)-5-амино-1Н-1,2,4-триазол
5.90 (2H, уш. с., NH2), 7.12 (2H, т., J = 7.8, CH-аром.), 7.57 (2H, д.,
J = 7.9, CH-аром.), 8.60 (с, 1H, NH), 11.15 (уш. с., 1H, NH-триаз.)
3-(3-Хлорфениламино)-5-амино-1Н-1,2,4-триазол
5.90 (2H, уш. с., NH2), 6.71 (1H, д., CH-аром.), 7.15 (1H, т.,
J = 7.8, CH-аром.), 7.31 (1H, д., J = 7.9, CH-аром.), 7.74 (1H, с.,
CH-аром.); 8.92 (с., 1H, NH), 11.25 (уш. с., 1H, NH-триаз.)
вначале изменяется аналогично контрольному опыту
отмечено значительное, более 0.10 В, увеличение
в отсутствие ингибитора. При дальнейшем увели-
области поляризуемости медного электрода.
чении поляризации наблюдается превышение плот-
Однако при введении 1.00 ммоль·л-1 3,5-диами-
ности тока в интервале ≈0.21-0.40 В, после чего
но-1H-1,2,4-триазола на анодном участке поляризаци-
поляризационные кривые неразличимы. Катодный
онной кривой наблюдается интенсивное возрастание
участок поляризационной кривой имеет более широ-
плотности тока. Максимум тока получен при более
кую (на 20-30 мВ) область поляризуемости относи-
отрицательных значениях потенциала. Плотность
тельно контрольного эксперимента. При увеличении
тока превышает значение контрольного опыта до
концентрации до 0.10 ммоль·л-1 начальный участок
5 раз. Катодная поляризационная кривая аналогична
анодной поляризационной кривой смещен к нулевым
контрольной.
значениям плотности тока вплоть до формирования
Степень защиты (Zинг) 3,5-диамино-1H-1,2,4-три-
максимума при потенциале ≈0.38 В. Дальнейший
азола в нейтральных хлоридсодержащих растворах
ход анодной поляризационной кривой аналогичен
монотонно убывает с ростом концентрации вещества
контрольному эксперименту. На катодном участке
от 0.01 до 1.00 ммоль·л-1 (табл. 4). Натурные испыта-
Таблица 4
Результаты электрохимических измерений меди в боратном буферном растворе (рН 7.4) + 10 ммоль·л-1 NaCl
с добавкой 5-амино-1H-1,2,4-триазолов
Потенциал
Концентрация
Поляризационное
Плотность тока
Степень
свободной
Соединение
ингибитора синг,
сопротивление
коррозии
защиты
коррозии
ммоль·л-1
Rp, кОм∙cм2
iкор, мкA∙см-2
Zинг, %
Eкор, В
Без добавки ингибитора
—
0.172
41.9 ± 4.6
1.2 ± 0.3
—
3,5-Диамино-1H-1,2,4-триазол
0.01
0.185
58.6 ± 5.2
0.36 ± 0.17
70
0.10
0.175
32.0 ± 4.3
0.46 ± 0.13
62
1.00
0.090
39.9 ± 3.8
0.7 ± 0.2
42
3-Фениламино-5-амино-1Н-1,2,4-триазол
0.10
0.246
61.3 ± 7.2
0.62 ± 0.16
48
1.00
0.216
72.6 ± 9.6
0.44 ± 0.12
63
3-(4-Метилфениламино)-5-амино-1Н-
0.10
0.117
58.5 ± 6.2
0.81 ± 0.15
33
1,2,4-триазол
1.00
0.116
99.9 ± 9.4
0.25 ± 0.09
79
3-(4-Хлорфениламино)-5-амино-1Н-1,2,4-
0.10
0.141
221 ± 13
0.41 ± 0.13
66
триазол
1.00
0.188
340 ± 18
0.16 ± 0.06
87
Ингибирование коррозии меди N-ариламинотриазолами в водных хлоридных растворах и в атмосферных условиях
1123
контрольного эксперимента без обработки веществом
(1a) (табл. 5). Значение τкор = 2 ч для концентрации
10.0 ммоль·л-1 рассматривается как аналогичное
контрольному опыту без добавки вещества (1a) при
интервале проводимых осмотров в 1 ч. Натурные
испытания в кислой среде при этом позволяют сде-
лать вывод об увеличении степени защиты (Zk) с
ростом концентрации ингибитора в интервале 1.00-
10.0 ммоль·л-1 (табл. 5).
Закономерности изменения анодных и катодных
участков поляризационных кривых для 3-фенилами-
но-5-амино-1Н-1,2,4-триазола и 3-(4-метилфенил-
амино)-5-амино-1Н-1,2,4-триазола аналогичны
(рис. 2, 3), несмотря на различие в значениях Екор. Для
обеих добавок не отмечено формирования максимума
тока на анодной поляризационной кривой. Смещение
Еакт в положительную область превышает 0.20 В
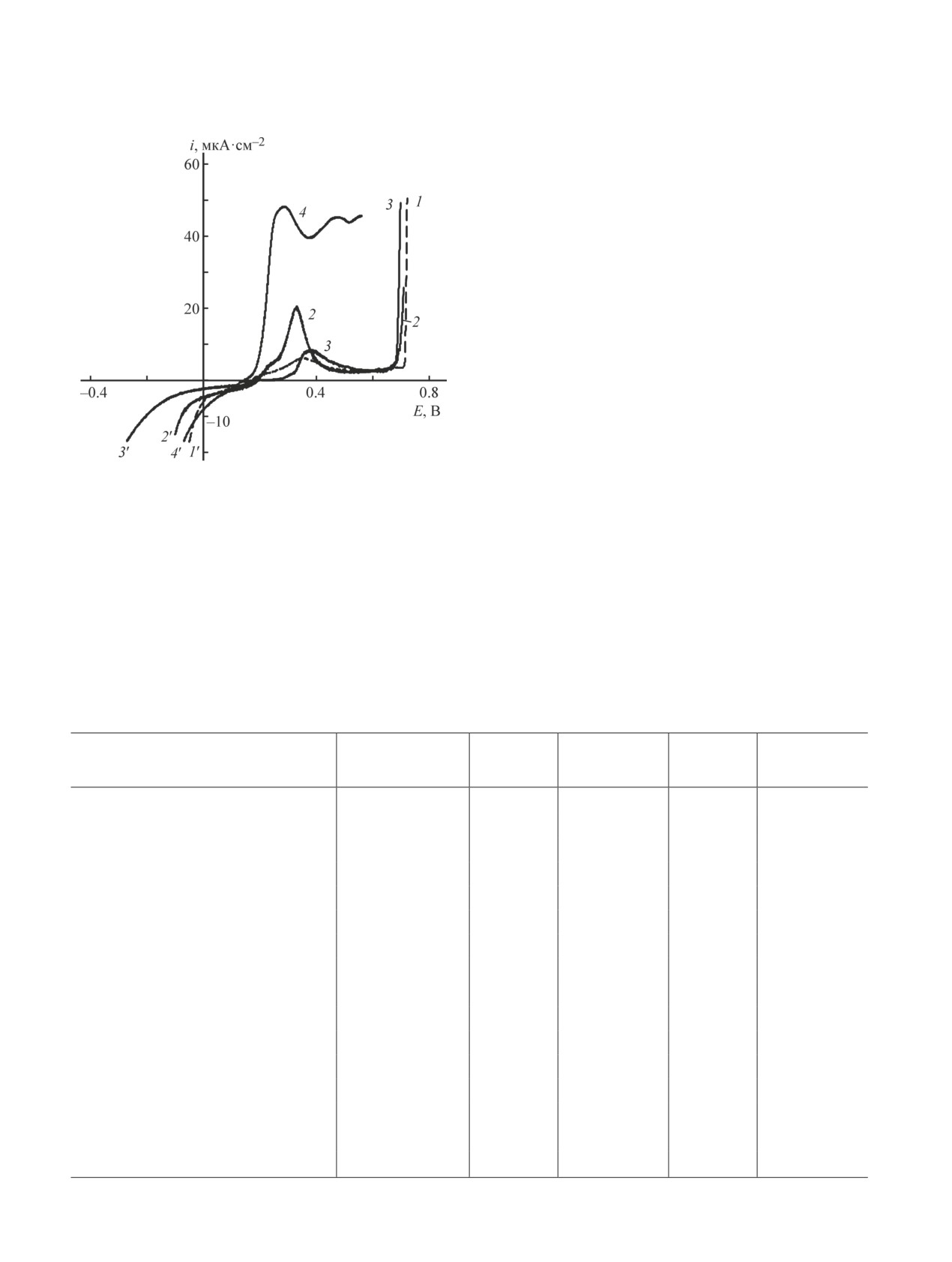
Рис. 1. Анодные и катодные поляризационные кри-
[за исключением концентрации 0.10 ммоль·л-1 для
вые меди в боратном буферном растворе (рН 7.4) +
3-(4-метилфениламино)-5-амино-1Н-1,2,4-триазола].
+ 10 ммоль·л-1 NaCl без ингибитора (1, 1′) и с добавкой
Также наблюдается увеличение области поляризуе-
3,5-диамино-1H-1,2,4-триазола (2, 2′ — 0.01, 3, 3ʹ —
мости электрода на катодных участках поляризаци-
0.10, 4, 4ʹ — 1.00 ммоль·л-1).
онных кривых на величину свыше 0.10 для 3-фе-
ниламино-5-амино-1Н-1,2,4-триазола и 0.25 В для
ния в камере соляного тумана с контролем параметра
3-(4-метилфениламино)-5-амино-1Н-1,2,4-триазола.
τкор в интервале концентраций 1.00-10.0 ммоль·л-1
Выявленные закономерности на поляризационных
не обнаруживают защитного действия относительно кривых позволяют прогнозировать защитное дей-
Таблица 5
Результаты коррозионных тестов в кислоте и в камере соляного тумана
Концентрация
Скорость
Степень
Время
Коэффициент
Соединение
ингибитора cинг,
коррозии,
защиты
до появления
торможения γ
ммоль·л-1
г·м2∙сут-1
Zk, %
коррозии τкор, ч
Без добавки ингибитора
—
44.0
1.0
—
3
3,5-Диамино-1H-1,2,4-триазол
1.0
10.4
1.3
20.4
4
5.0
8.5
1.6
35.5
4
10.0
3.3
4.0
74.7
2
3-Фениламино-5-амино-1Н-1,2,4-
1.0
18.6
2.4
57.7
60
триазол
5.0
20.9
2.1
52.5
62
10.0
2.0
22
95.5
61
3-(4-Метилфениламино)-5-амино-1Н-
1.0
17.1
1.3
22.8
66
1,2,4-триазол
5.0
4.7
4.7
78.8
80
10.0
1.7
12.8
92.2
122
3-(4-Хлорфениламино)-5-амино-1Н-
1.0
15.3
1.2
18.4
36
1,2,4-триазол
5.0
8.8
2.1
53.0
46
10.0
3.9
4.8
79.3
62
3-(3-Хлорфениламино)-5-амино-1Н-
1.0
4.4
2.0
51.1
70
1,2,4-триазол
5.0
0.6
14.2
92.9
90
10.0
0.3
26.3
96.2
93
1124
Шевцов Д. С. и др.
интервале концентраций 1-10 ммоль·л-1, а для
3-(4-метилфениламино)-5-амино-1Н-1,2,4-триазола
защитный эффект выше и увеличивается с ростом
концентрации.
В кислых растворах также выявлено ингибиро-
вание коррозии. Степень защиты возрастает в ин-
тервале концентраций 1-10 ммоль·л-1 и достигает
92-95%.
Анодный участок поляризационной кривой меди
с добавкой 0.10 ммоль·л-1 3-(4-хлорфениламино)-5--
амино-1Н-1,2,4-триазола отличается от всех прочих
полученных зависимостей (рис. 4). На начальном
участке до потенциала ≈0.27 В плотность тока ниже
относительно контрольного опыта. При дальнейшем
увеличении потенциала наблюдается интенсивное
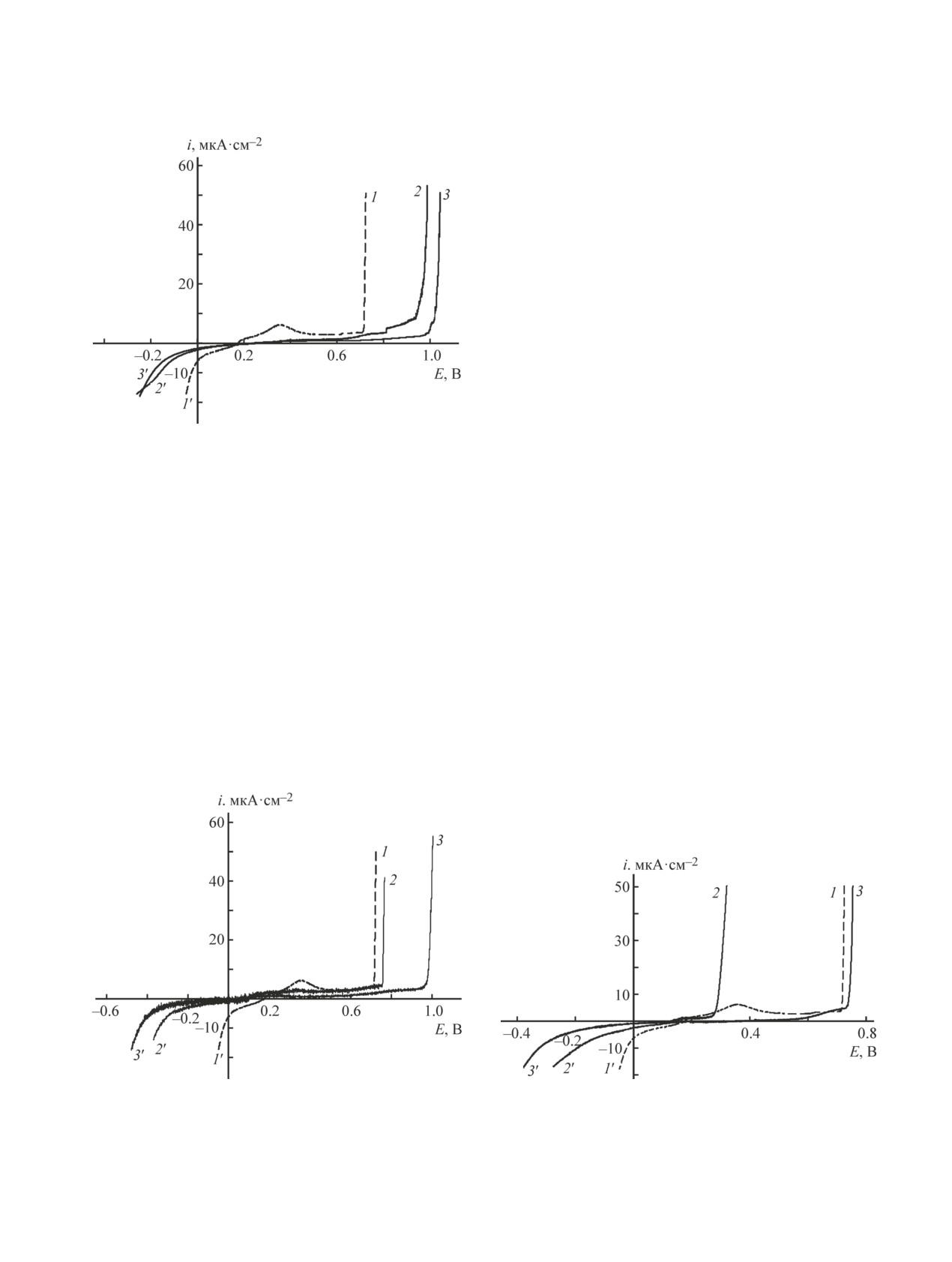
Рис. 2. Анодные и катодные поляризационные кривые
увеличение плотности тока без формирования мак-
меди в боратном буферном растворе (рН 7.4) +
симума вплоть до плотности тока 250 мкА∙см-2. При
+ 10 ммоль·л-1 NaCl без ингибитора (1, 1ʹ) и с добав-
концентрации 1.00 ммоль·л-1 получен продолжитель-
кой 3-фениламино-5-амино-1Н-1,2,4-триазола
ный участок на анодном участке поляризационной
(2, 2ʹ — 0.10; 3, 3ʹ — 1.00 ммоль·л-1).
кривой со значениями тока, близкими к нулю, вплоть
до потенциала 0.57 В. Максимум плотности тока не
ствие соединений (1b)-(1c) в нейтральных средах.
совпадает с контроль-
зафиксирован. Значение Еакт
Выявлено возрастание ингибирующего эффекта с
ным опытом. На катодных участках поляризационных
ростом концентрации. Коррозионные эксперимен-
кривых наблюдается увеличение области поляри-
ты в камере соляного тумана также демонстрируют
зуемости электрода на величину свыше 0.10 В для
более чем 20-кратный защитный эффект для сое-
изученных концентраций 3-(4-хлорфениламино)-5--
динений (1b), (1c) и (1e) и более чем 10-кратный
амино-1Н-1,2,4-триазола.
для соединения (1d) относительно незащищенно-
Полученные значения токов коррозии для
го металла независимо от концентрации ингибито-
3-(4-хлорфениламино)-5-амино-1Н-1,2,4-триазола
ра. Следует отметить, что для 3-фениламино-5-а-
являются наименьшими для всех изученных соеди-
мино-1Н-1,2,4-триазола результаты аналогичны в
нений при сопоставимых концентрациях. Результаты
коррозионных тестов в камере соляного тумана со-
поставимы с данными опытов для веществ, рассмо-
тренных выше. Защитный эффект более 50% в кислой
Рис. 3. Анодные и катодные поляризационные кривые
Рис. 4. Анодные и катодные поляризационные кри-
меди в боратном буферном растворе (рН 7.4) +
вые меди в боратном буферном растворе (рН 7.4) +
+ 10 ммоль·л-1 NaCl без ингибитора (1, 1ʹ) и с добав-
+ 10 ммоль·л-1 NaCl без ингибитора (1, 1ʹ) и с добав-
кой 3-(4-метилфениламино)-5-амино-1Н-1,2,4-триазо-
кой 3-(4-хлорфениламино)-5-амино-1Н-1,2,4-триазола
ла (2, 2ʹ — 0.10; 3, 3ʹ — 1.00 ммоль·л-1).
(2, 2ʹ — 0.10; 3, 3ʹ — 1.00 ммоль·л-1).
Ингибирование коррозии меди N-ариламинотриазолами в водных хлоридных растворах и в атмосферных условиях
1125
среде получен только при концентрации 3-(4-хлор-
Информация об авторах
фениламино)-5-амино-1Н-1,2,4-триазола не менее
Шевцов Дмитрий Сергеевич,
5 ммоль·л-1.
Шихалиев Хидмет Сафарович, д.х.н., проф.,
Выводы
Комарова Екатерина Сергеевна,
С применением оптимизированного каскадного
однореакторного взаимодействия S,S-диметилциано-
Кружилин Алексей Александрович, к.х.н., ORCID:
дитиоимидокарбамата с ариламинами и гидразином
проведен синтез 3-фениламино-, 3-(4-метилфенил-
Потапов Андрей Юрьевич, д.х.н., проф., ORCID:
амино)-, 3-(4-хлорфениламино)- и 3-(3-хлорфени-
ламино)производных 5-амино-1Н-1,2,4-триазола с
Киприянова Галина Олеговна, к.х.н., ORCID:
выходом более 75%.
Полученные соединения обладают ингибирующим
Зарцын Илья Давидович, д.х.н., проф., ORCID:
действием по отношению к меди в нейтральных и
кислых хлоридсодержащих средах. Для нейтральной
Козадеров Олег Александрович, д.х.н., доц.,
водной среды максимальная степень защиты близка
для всех изученных соединений и достигает 70-87%.
Прабхакар Четти (Prabhakar Chetti), доц.,
Для 3,5-диамино-1H-1,2,4-триазола получено сни-
жение защитного действия при увеличении концен-
Трипати Ануж (Tripathi Anuj),
трации в растворе в интервале 0.01-1.00 ммоль·л-1.
В кислой среде степень защиты для синтезированных
соединений выше относительно коммерчески до-
ступного 3,5-диамино-1H-1,2,4-триазола и достигает
92-96% для 3-фениламино-, 3-(4-метилфениламино)-
Список литературы
и 3-(3-хлорфениламино)производных при концентра-
ции 10 ммоль·л-1. Результаты испытаний в камере
[1] Kear G., Barker B. D., Walsh F. C. Electrochemical
соляного тумана аналогичны данным для кислой
corrosion of unalloyed copper in chloride media — a
critical review // Corros. Sci. 2004. V. 46. P. 109-135.
среды. Время до образования первых продуктов кор-
розии в 9-60 раз превышает значения для 3,5-диами-
[2] Finsgar M., Milosev I. Inhibition of copper corrosion
но-1H-1,2,4-триазола в зависимости от концентрации
by 1,2,3-benzotriazole: A review // Corros. Sci. 2010.
и структуры новых производных.
V. 52. P. 2737-2749.
Применение 3-(3-хлорфениламино)-5-ами-
но-1Н-1,2,4-триазола в качестве ингибитора кор-
[3] Khiati Z., Othman A. A., Sanchez-Moreno M.,
розии меди целесообразно при непосредственном
Bernard M.-C., Joiret S., Sutter E. M. M., Vivier V.
растворении в рабочей среде по причине высокой
Corrosion inhibition of copper in neutral chloride media
вероятности разложения на стадии приготовле-
by a novel derivative of 1,2,4-triazole // Corros. Sci.
ния концентратов с содержанием вещества более
2011. V. 53. P. 3092-3099.
10 ммоль·л-1.
[4] Finšgar M. EQCM and XPS analysis of 1, 2, 4-triazole
and 3-amino-1,2,4-triazole as copper corrosion
Финансирование работы
inhibitors in chloride solution // Corros. Sci. 2013. V. 77.
Работа по синтезу 3-(N-ариламино)-5-амино-1Н-
[5] Skrypnikova E. A., Kaluzhina S. A., Agafonova L. E.
1,2,4-триазолов и оптимизации условий процесса их
Inhibition of copper pitting corrosion in alkaline
получения выполнена при поддержке Минобрнауки
sulphate media by benzotriazole at elevated
России в рамках государственного задания высшим
temperatures // lnt. J. Corros. Scale Inhib. 2014. V. 3.
учебным заведениям в сфере научной деятельности
N 1. P. 59-65.
на 2017-2019 годы, проект № 4.3633.2017/4.6.
Работа по электрохимическим и натурным кор-
[6] Dugdale I., Cotton J. B. An electrochemical
розионным испытаниям выполнена при финансо-
investigation on the prevention of staining of copper by
вой поддержке Научно-технического совета (SERB,
benzotriazole // Corros. Sci. 1963. V. 2. N 1. Р. 69-75.
Нью-Дели, Индия, грант SB/FT/CS-101/2014).
1126
Шевцов Д. С. и др.
[7]
Poling G. W. Reflection infra-red studies of films
[11]
Wittenbrook L. S., Smith G. L., Timmons R. J.
Chemistry of N-cyanodithioimidocarbonic acid. II.
Synthesis of 3-halo-1,2,4-thiadiazoles // J. Org. Chem.
1973. V. 38. N 3. P. 465-471.
[8]
Takenouti H.
Aminotriazole as corrosion inhibitor of
[12]
Mansfeld F. The polarization resistance technique for
Cu-30Ni alloy in 3% NaCl in presence of ammoniac
measuring corrosion currents // Advances in corrosion
science and technology. Springer, Boston, MA. 1976.
P. 163-262.
[9]
Moussa M. N. H., El-Far A. A., El-Shafei A. A. The
use of water-soluble hydrazones as inhibitors for the
[13]
Mansfeld F. Tafel slopes and corrosion rates obtained
corrosion of C-steel in acidic medium // Mater. Chem.
in the pre-Tafel region of polarization curves // Corros.
Phys. 2007. V. 105. P. 105-113.
Sci. 2005. V. 47. N 12. P. 3178-3186.
[10]
Rivera-Grau L. M., Casales M., Regla I., Ortega-
[14]
Shih H., Mansfeld F. Software for quantitative analysis
Toledo D. M., Ascencio-Gutierrez J. A., Porcayo-
of polarization curves // Computer Modeling in
Calderon J., Martinez-Gomez L. Effect of organic
Corrosion. ASTM International. 1992. P. 174-185.
corrosion inhibitors on the corrosion performance
of 1018 carbon steel in 3% NaCl solution // lnt. J.
Electrochem. Sci. 2013. V. 8. P. 2491-2503.