1188
Хрущева М. Л. и др.
Журнал прикладной химии. 2020. Т. 93. Вып. 8
УДК 615.074:54.061:543.51
НОВЫЕ МАТРИЧНЫЕ СОЕДИНЕНИЯ
ДЛЯ ДЕТЕКТИРОВАНИЯ КАРБОКСИЛСОДЕРЖАЩИХ
НЕСТЕРОИДНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ
МЕТОДОМ МАСС-СПЕКТРОМЕТРИИ МАЛДИ
© М. Л. Хрущева1*, М. С. Кривошеина2, М. Д. Матвеева2,
Д. И. Жиляев3, Р. С. Борисов2,3**
1 ФГБУ «Научный центр экспертизы средств медицинского применения»
Министерства здравоохранения Российской Федерации,
127051, г. Москва, Петровский бул., д. 8, стр. 2
2 Институт нефтехимического синтеза им. А. В. Топчиева РАН,
119991, г. Москва, Ленинский проспект, д. 29
3 Российский университет дружбы народов,
117198, г. Москва, ул. Миклухо-Маклая, д. 6
E-mail: *khrushchevaml@expmed.ru; **borisov@ips.ac.ru
Поступила в Редакцию 17 апреля 2020 г.
После доработки 14 мая 2020 г.
Принята к публикации 21 мая 2020 г.
Изучена возможность применения метода масс-спектрометрии с матрично-активированной ла-
зерной десорбцией/ионизацией (МАЛДИ) для экспрессного детектирования карбоксилсодержащих
нестероидных противовоспалительных средств. Сравнение результатов, полученных с помощью
ранее описанных и вновь предложенных в качестве матричных соединений 4-(диметиламино)бен-
зальдегида и N,N-диметил-п-фенилендиамина, показало, что последние обеспечивают регистрацию
масс-спектров, содержащих интенсивные пики депротонированных молекул всех использованных в
работе лекарственных средств. Сравнение времени, необходимого для их детектирования различными
масс-спектрометрическими методами, показало, что при потоковом анализе масс-спектрометрия
МАЛДИ обеспечивает наибольшую производительность.
Ключевые слова: нестероидные противовоспалительные средства; карбоксилсодержащие соединения;
контроль качества; подлинность; детектирование; депротонирующие матрицы; масс-спектроме-
трия МАЛДИ; отрицательно заряженные ионы
DOI: 10.31857/S0044461820080150
Нестероидные противовоспалительные средства
нием обезболивающего и противовоспалительного
(НПВС) представляют собой группу лекарственных
действий. По своей химической структуре НПВС об-
средств, которые широко применяются в клинической
ладают в разной степени выраженными кислотными
практике при ревматических, неврологических, трав-
или основными свойствами в зависимости от наличия
матологических заболеваниях, а также в кардиологии
функциональных групп. Основные лекарственные
в качестве средств антиагрегантной терапии. НПВС
препараты, содержащие кислотные и другие функ-
ежедневно принимают более 30 млн людей в мире, в
циональные группы, включают производные салици-
том числе около 20% больных, получающих лечение
ловой, уксусной, пропионовой кислот, производные
в стационарах [1].
пиразолона и оксикамы [1].
К группе нестероидных противовоспалительных
Сегодняшний российский рынок НПВС явля-
средств относятся лекарственные препараты различ-
ется преимущественно монокомпонентным, при-
ного химического строения с различным соотноше-
чем лидирующее положение занимают карбоксил-
Новые матричные соединения для детектирования...
1189
содержащие лекарственные препараты, такие как
информативностью в упомянутом перечне методов
диклофенак, мелоксикам, ибупрофен, кетопрофен
анализа обладает ТСХ, идентификационные возмож-
и кеторолак. Благодаря кампании импортозамеще-
ности которой в большинстве случаев опираются на
ния с 2016 г. было увеличено число предложений
определение фактора подвижности аналита и фик-
препаратов отечественного производства, однако
сацию изменения цвета пятна при специфической
насыщение рынка достигается за счет выпуска не
дериватизации [4]. В целях надежной и достоверной
оригинальных, а уже имеющихся препаратов [2].
идентификации разделенных компонентов целесо-
В связи с этим актуальной является задача контро-
образно использовать сочетание ТСХ с масс-спек-
ля качества производимых препаратов, в том чис-
трометрическим детектированием (МС) [5]. Однако
ле контроля подлинности лекарственных средств
такая комбинация еще не нашла широкого приме-
и содержания в них примесей. В качестве основ-
нения при анализе лекарственных препаратов, хотя
ных методов подтверждения подлинности НПВС,
существуют работы, в которых описано эффективное
согласно Государственной фармакопее Российской
использование сочетания ТСХ и масс-спектрометрии
Федерации XIV изд. (ГФ РФ XIV), применяются УФ-
для практических целей. В частности, именно этот
и ИК-спектроскопия.* УФ-спектроскопия считается
метод был использован для определения НПВС в
наиболее доступным методом анализа, однако обла-
объектах окружающей среды [6] и в биологических
дает низкой информативностью, что снижает надеж-
объектах [7]. Основными недостатками применения
ность полученных результатов. Информативность
метода являются относительная сложность пробопод-
метода ИК-спектроскопии выше за счет возможности
готовки и подбор условий разделения [8].
получения большего количества характеристических
Более экспрессным подходом к подтверждению
сигналов — полос поглощения, что увеличивает уро-
подлинности фармацевтических субстанций и лекар-
вень достоверности идентификации и позволяет про-
ственных препаратов является применение масс-спек-
водить экспрессный потоковый анализ. Вместе с тем
трометрии с ионизацией при атмосферном давлении
применение этого метода при подтверждении под-
или непосредственно на воздухе без использования
линности субстанций требует трудоемкой процедуры
дополнительного хроматографического разделения.
пробоподготовки готовых лекарственных форм (по-
Однако применение для этого большинства методов
лучение прессованной таблетки с KBr) и их анализа.
ионизации при атмосферном давлении (ионизация
Идентификация аналитов затруднена присутствием
электрораспылением, фотоионизация и т. д.) ослож-
органических соединений (углеводов, полиалкилен-
няется выраженными матричными эффектами [9].
гликолей, производных карбоновых кислот и т. д.), а
Более удобными являются способы ионизации при
также наличием оболочки, не содержащей действую-
нормальных условиях (прямой анализ в реальном
щих веществ субстанций.
времени, десорбционная ионизация электрораспыле-
Альтернативными методами анализа могут быть
нием и т. д.), практически не требующие проведения
различные хроматографические методы, в том числе
предварительной пробоподготовки [10]. Однако их
тонкослойная (ТСХ),** газовая (ГХ) и высокоэф-
широкому применению в аналитической практике
фективная жидкостная хроматография (ВЭЖХ) [3].
препятствует довольно малая распространенность
В последних двух случаях используются разнообраз-
соответствующей приборной базы.
ные типы детекторов (пламенно-ионизационный и
Еще одним перспективным методом для экспресс-
катарометр для ГХ, ультрафиолетовый спектрофо-
ного подтверждения подлинности фармацевтических
тометрический*** и детектор светорассеяния для
субстанций является масс-спектрометрия с матрич-
ВЭЖХ). Следует отметить, что далеко не все упомя-
но-активированной лазерной десорбцией/ионизацией
нутые методы внесены ГФ РФ XIV в статьи, регла-
(МАЛДИ). Изначально предназначенный для анализа
ментирующие контроль качества НПВС. Наименьшей
высокомолекулярных соединений, в настоящее время
этот метод все шире применяется для детектирова-
ния малых молекул, в том числе биологически ак-
* ФС.2.1.0145.18. Нимесулид; ФС.2.1.0138.18.
Напроксен; ФС.2.1.0107.18. Кетопрофен; ФС.2.1.0100.18.
тивных веществ [11]. Большим его преимуществом
Ибупрофен; ФС.2.1.0022.15. Кеторолак; ФС.2.1.0094.18.
является возможность использования автоматизи-
Диклофенак. Государственная фармакопея Российской
рованных алгоритмов сбора данных при облучении
Федерации. XIV изд. Т. 3. М., 2018.
лазером мишеней с большим числом нанесенных на
** ФС.2.1.0107.18. Кетопрофен. Государственная фар-
них аналитов (например, стандартные мишени для
макопея Российской Федерации. XIV изд. Т. 3. М., 2018.
масс-спектров МАЛДИ Bruker позволяют наносить
*** ФС.2.1.0022.15. Кеторолак. Государственная фар-
макопея Российской Федерации. XIV изд. Т. 3. М., 2018.
на них одновременно 384 образца).
1190
Хрущева М. Л. и др.
Одним из основных препятствий к широкому
виде фармацевтической субстанции. Для проведения
применению этого метода является необходимость
анализа готовили его раствор в ТГФ концентрацией
подбора матричных соединений для анализа кон-
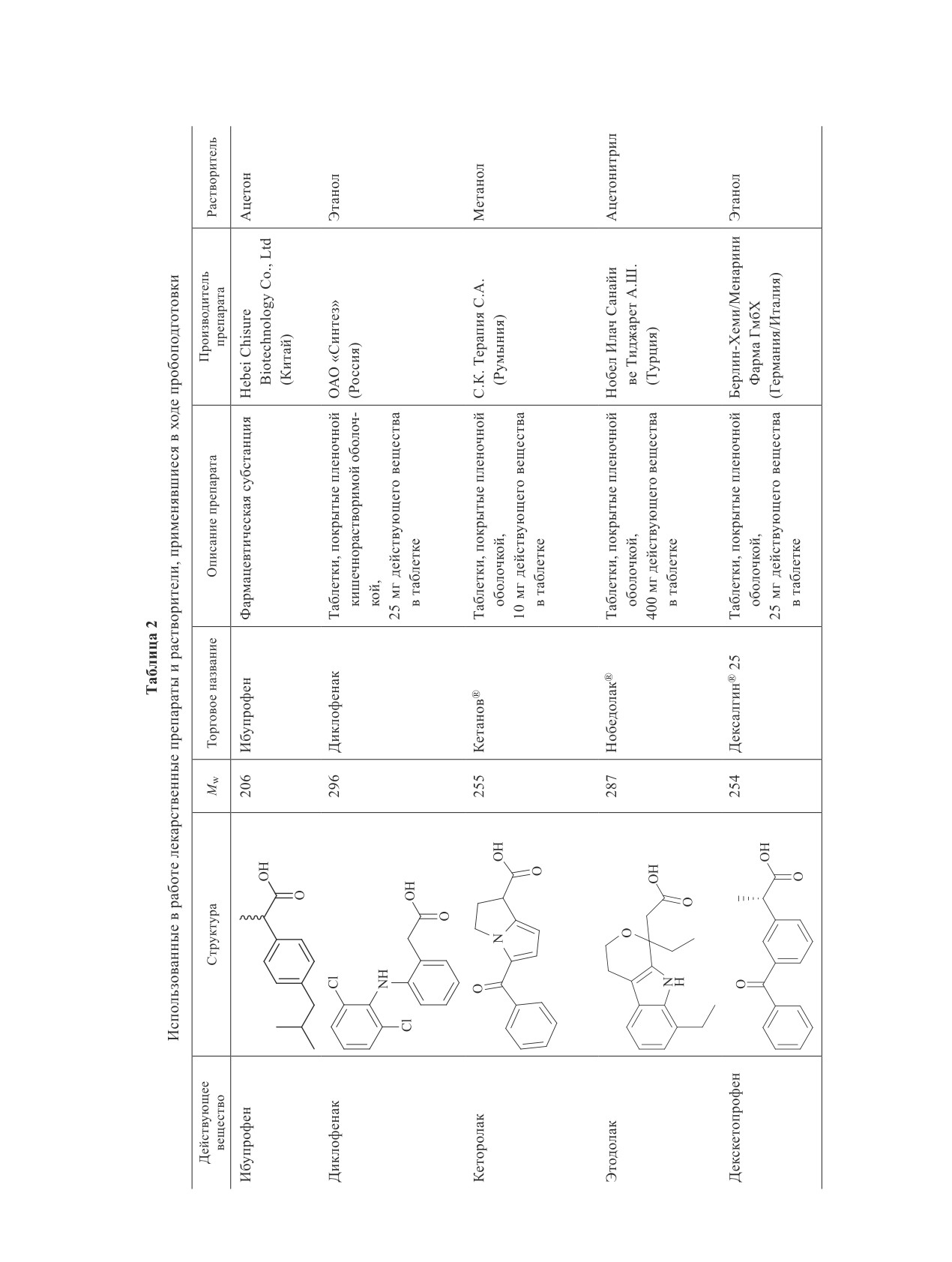
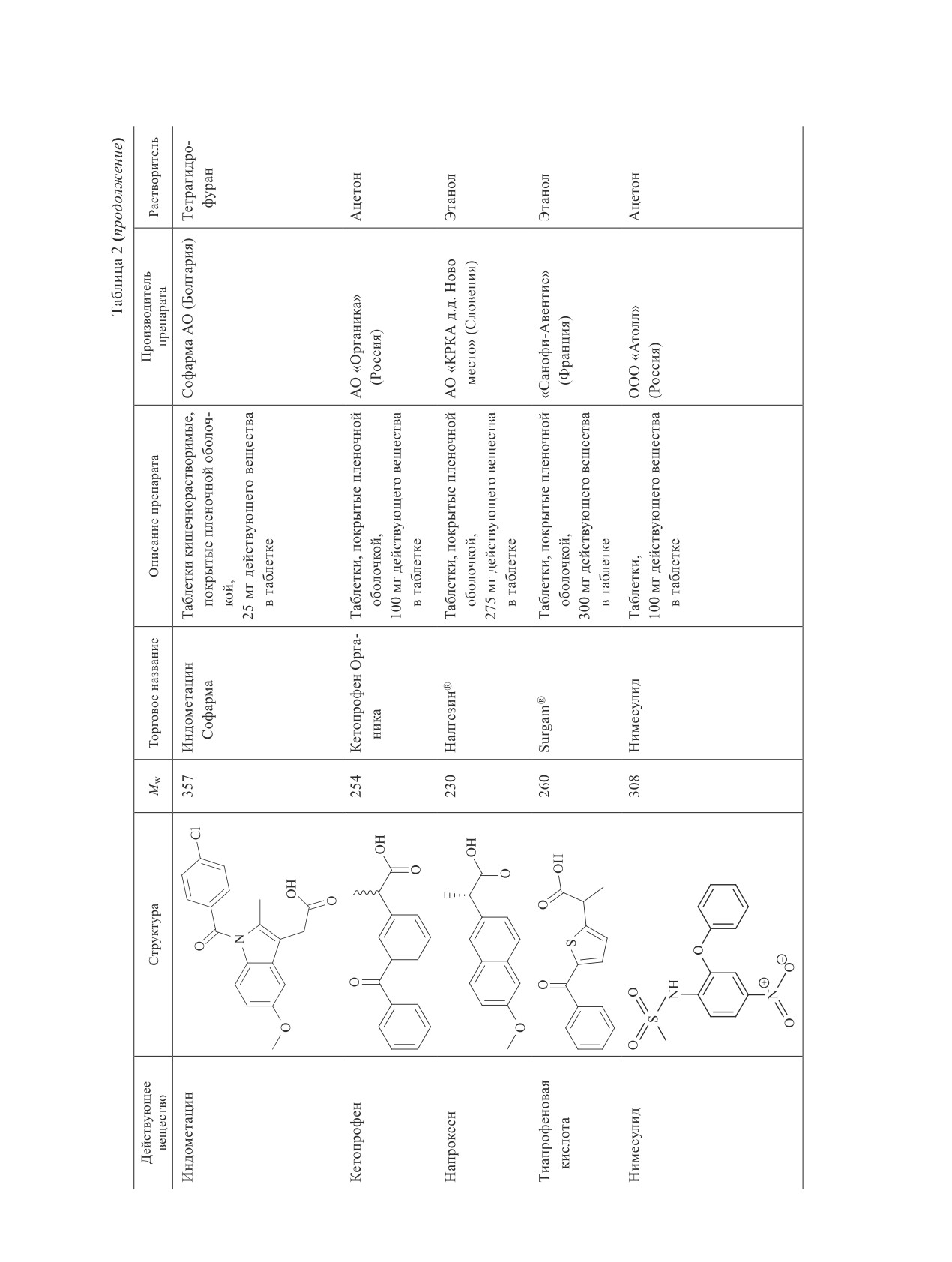
10 мг·мл-1. Диклофенак (2), кеторолак (3), этодолак
кретных классов аналитов с целью обеспечения наи-
(4), декскетопрофен (5), индометацин (6), кетопрофен
лучшей чувствительности, а иногда и селективности
(7), напроксен (8), тиапрофеновая кислота (9), ниме-
метода [12, 13]. Наибольшее число работ в области
сулид (10) извлекали из лекарственных препаратов в
исследования органических соединений методом
таблетированной форме, приобретенных в аптечной
масс-спектрометрии с МАЛДИ выполнено с исполь-
сети (табл. 2).
зованием режима регистрации положительно заря-
Растворы действующих веществ (2)-(10) готови-
женных ионов. Такие ионы наиболее стабильны и
ли следующим образом: приобретенные в аптечной
в условиях МАЛДИ образуются в результате прото-
сети лекарственные препараты (табл. 2) измельчали
нирования или катионирования молекул аналитов.
в агатовой ступке до порошка; порошок помеща-
В некоторых случаях используются подходы, позво-
ли в виалы из силанизированного стекла емкостью
ляющие заранее формировать положительно заря-
2 мл, вносили 1 мл соответствующего растворителя
женный фрагмент в молекуле [14]. Однако высокой
(табл. 2) и выдерживали в шейкере при комнатной
чувствительности можно достичь и при регистрации
температуре в течение 60 мин.
отрицательно заряженных ионов. Как показали недав-
10 мкл каждого из растворов аналитов смешива-
ние исследования, такие ионы могут легко генериро-
ли с 30 мкл раствора матричного соединения в ТГФ
ваться в случае кислот и соединений с повышенной
(30 мг·мл-1) и наносили на стальную мишень MTP
кислотностью, если для этого использовать матрицы
384 ground steel (Bruker Daltonics Inc.). Для реги-
с высоким сродством к протону и, следовательно,
страции масс-спектров с наноструктурированной
обеспечивающие отщепление протона от молекулы
поверхности растворы аналитов без добавления ма-
аналита [15].
трицы наносили на мишень MSP 96 NALDI (Bruker
К настоящему времени описано лишь несколько
Daltonics Inc.).
таких депротонирующих матричных соединений.
Определение пределов обнаружения соедине-
Например, для детектирования карбоновых кислот,
ния (1) методом масс-спектрометрии МАЛДИ про-
некоторых фенолов и кислот было предложено ис-
водили путем последовательного двукратного разбав-
пользовать 9-аминоакридин [16] и 3-аминохинолин
ления раствора аналита (10 мг·мл-1) с последующей
[17].
регистрацией его масс-спектра с помощью соответ-
Цель работы — изучение возможности примене-
ствующего матричного соединения. При определении
ния некоторых ранее описанных и оценка потенциала
пределов обнаружения аналитов за минимальное
новых предлагаемых нами матриц для детектирова-
отношение сигнал/шум принимали значение 3.
ния карбоксилсодержащих нестероидных противо-
Для оценки времени анализа, необходимого для
воспалительных средств методом масс-спектроме-
детектирования аналитов методом ГХ/МС, к 100 мкл
трии с МАЛДИ.
раствора соединения (1) в ацетонитриле (2 мг·мл-1)
добавляли 10 мкл N,O-бис(триметилсилил)трифтор-
ацетамида и выдерживали на шейкере в течение
Экспериментальная часть
5 мин при 70°С. После силилирования 1 мкл дерива-
В работе использовали матричные соединения,
тизированного экстракта вводили в инжектор газово-
характеристика которых представлена в табл. 1. В ка-
го хроматографа.
честве растворителей использовали метанол, эта-
Для оценки времени анализа, необходимого для
нол, ацетон, тетрагидрофуран (ТГФ), ацетонитрил
детектирования аналитов методом ВЭЖХ/МС, рас-
(все вышеперечисленные вещества производства
твор соединения (1) в ацетонитриле (1 мг·мл-1) филь-
Реахим, х.ч.), а также, для проведения анализа ме-
тровали с помощью шприцевого фильтра (0.22 мкм,
тодом ВЭЖХ, ацетонитрил (ФизЛабПрибор, Россия,
Hawach Scientific) и вводили 1 мкл фильтрата в источ-
HPLC grade). Для силилирования использовался
ник ионов с помощью автосамплера жидкостного
N,O-бис(триметилсилил)трифторацетамид, содержа-
хроматографа без использования хроматографиче-
щий 1% триметилсилилхлорида (Sigma-Aldrich, кат.
ской колонки.
№ T6381 США, derivatization grade, CAS 25561-30-2).
Масс-спектры МАЛДИ получали на масс-спек-
Ибупрофен (1) был предоставлен Центром коллек-
трометре Bruker autoflex speed (Bruker Daltonics
тивного пользования (научно-образовательным цен-
Inc.), оснащенном твердотельным УФ-лазером с
тром) Российского универститета дружбы народов в
λ = 355 нм, в режиме регистрации положительно
Новые матричные соединения для детектирования...
1191
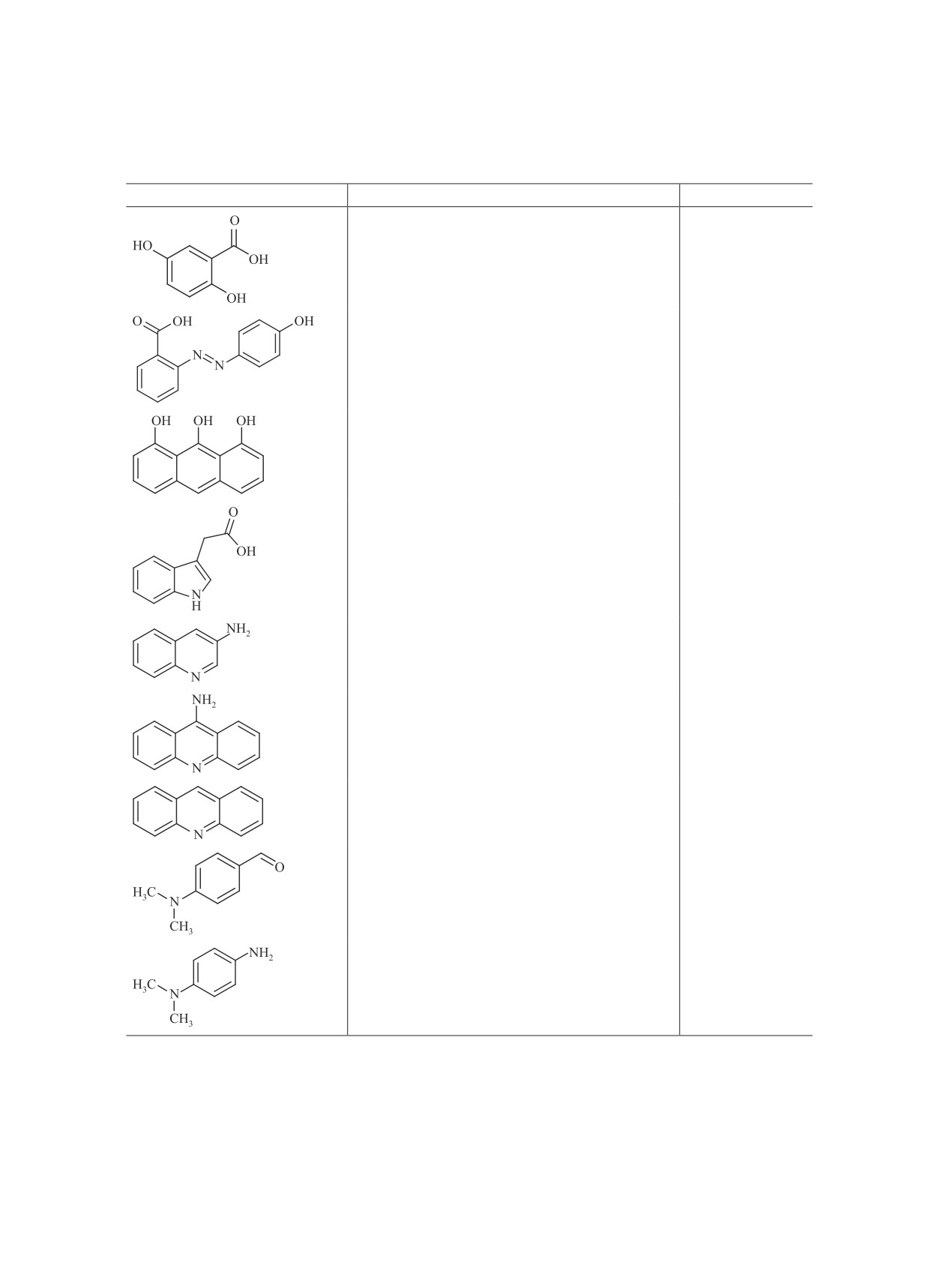
Таблица 1
Матричные соединения, использованные в работе
Структура
Название
Сокращение
2,5-Дигидроксибензойная кислота
DHB
2-(4-Гидроксифенилазо)бензойная кислота
HABA
1,8,9-Антрацентриол
AT
3-Индолакриловая кислота
IAA
3-Аминохинолин
AQ
9-Аминоакридин
AA
Акридин
AC
4-(Диметиламино)бензальдегид
DMABA
N,N-Диметил-п-фенилендиамин
DMAPA
и отрицательно заряженных ионов с использова-
ным квадрупольным масс-анализатором, в режиме ре-
нием рефлектрона. Максимальная энергия лазера
гистрации отрицательно заряженных ионов. Анализ
8 кДж·м-2. Масс-спектры ионизации электрораспы-
методом ГХ/МС проводили с помощью хромато-
лением (ИЭР) регистрировали на масс-спектрометре
масс-спектрометра Thermo Focus DSQ II (капилляр-
Shimadzu LCMS-8040 (Shimadzu), оснащенном трой-
ная колонка Varian VF-5ms, длина 15 м, внутренний
Новые матричные соединения для детектирования...
1193
1194
Хрущева М. Л. и др.
диаметр 0.25 мм, толщина слоя неподвижной фазы
заметные пики, соответствующие продуктам де-
0.25 мкм, газ-носитель — гелий). Режим работы:
протонирования молекул аналитов. Но все же для
температура инжектора 250°С, начальная темпера-
большинства матриц, таких как DHB, HABA, AT,
тура термостата хроматографа 45°С, затем изотерма
IAA, обычно обеспечивающих перенос протона на
в течение 1 мин, нагрев со скоростью 15 град·мин-1
молекулу аналита, интенсивность зарегистрирован-
до 250°С. Режим работы масс-спектрометра: энергия
ных пиков отрицательно заряженных ионов была на
ионизации электронами 70 эВ, температура источни-
уровне шумов. Аналогичная картина наблюдалась
ка ионов 250°С, сканирование в диапазоне 10-800 Да
и для случая безматричной НАЛДИ, где основным
со скоростью 1.5 скан·с-1, разрешение единичное по
механизмом ионизации является передача протона
всему диапазону масс.
от слабокислых силанольных групп на поверхности
нанонитей. Существенно лучшие результаты были
получены с использованием депротонирующих ма-
Обсуждение результатов
триц: интенсивность соответствующих пиков ионов и
Как уже отмечалось, одним из основных недостат-
соотношение сигнал/шум были в десятки и сотни раз
ков метода масс-спектрометрии МАЛДИ является
выше. Сопоставительный анализ полученных данных
необходимость эмпирического подбора матричных
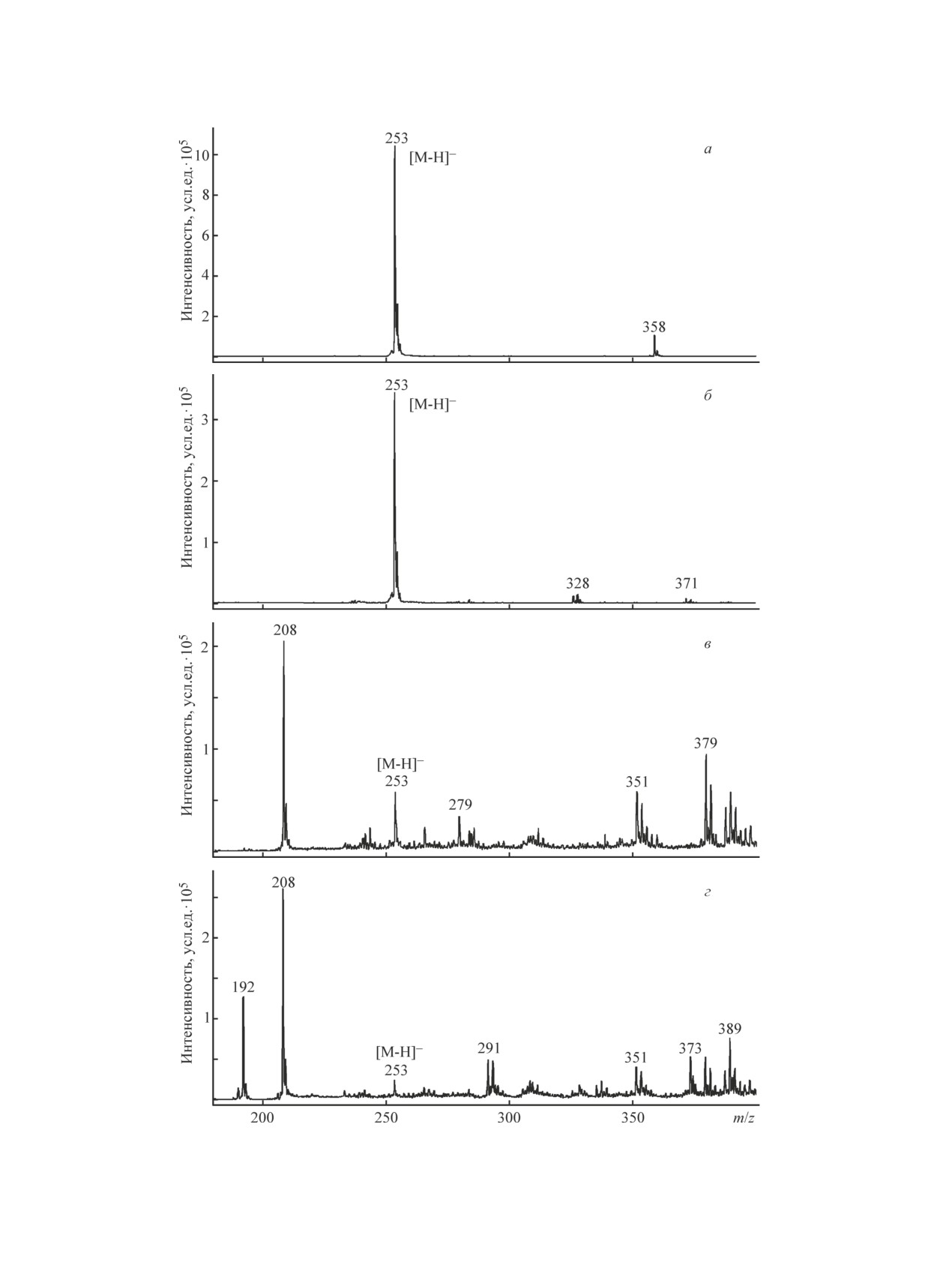
показал, что наиболее универсальными матричными
соединений. В настоящем исследовании, направлен-
соединениями являются AQ и ранее не описанные в
ном на разработку способа анализа НПВС, изуче-
качестве матричных соединений DMABA и DMAPA
на возможность использования как традиционных
(см. рисунок, табл. 3). Совершенно очевидно, что
матриц (DHB, HABA, AT, IAA, AQ, AA) (табл. 1),
такие соединения обладают высоким сродством к
так и впервые апробированных нами матричных
протону, обеспечивающим легкое отщепление кис-
соединений (AС, DMABA, DMAPA). Поскольку
лого протона от молекулы аналита, причем в газовой
большинство НПВС являются низкомолекулярны-
фазе факела МАЛДИ равновесие [аналит — H]-/[мат-
ми соединениями, ионы-продукты их ионизации
рица + Н]+ существенно сдвинуто в сторону генери-
попадают в область низких массовых чисел, в ко-
рования отрицательно заряженных депротонирован-
торой наблюдаются интенсивные пики продуктов
ных молекул.
ионизации и фрагментации матричных соединений.
В ходе работы были проведены исследования по
Поэтому помимо МАЛДИ был исследован способ
установлению наилучшей матрицы из названных
проведения анализа методом масс-спектрометрии
трех. Для соединения (1) методом последователь-
с поверхностно-активированной лазерной десорб-
ного разбавления были определены пределы обна-
цией/ионизацией с использованием коммерчески до-
ружения: при использовании в качестве матричного
ступных мишеней с наноструктурированной поверх-
соединения AQ он составил 4·10-2 мг·мл-1, а при
ностью (НАЛДИ).
применении DMABA и DMAPA — 1·10-3 и 2·10-3
Регистрация масс-спектров МАЛДИ положи-
соответственно.
тельно заряженных ионов с использованием всех
Необходимо отметить, что использование де-
апробированных в работе традиционных матрич-
протонирующих матриц позволяет регистрировать
ных соединений и мишеней НАЛДИ дала ожидае-
масс-спектры МАЛДИ для НПВС, не содержащих
мо неудовлетворительный результат: большинство
карбоксильных групп. Например, присутствующая
полученных масс-спектров не содержали сигналов,
в препарате нимесулид (10) сульфамидная груп-
соответствующих аналитам. В тех случаях, когда
па также обеспечивает генерацию депротонирован-
в масс-спектрах присутствовали пики протониро-
ных ионов. При этом, как и в случае соединений
ванных [соединение (2)] или катионированных мо-
(1)-(9), масс-спектр положительно заряженных ио-
лекул [соединения (1), (7), (9)], отношение сигнал/
нов нимесулида содержал лишь малоинтенсивные
шум для них не превышало 40. Очевидно, что нали-
пики ионов протонированных и катионированных
чие в молекулах аналитов полярных карбоксильных
молекул.
групп существенно снижает вероятность их участия
Поскольку одним из аргументов в пользу исполь-
в ионизационных процессах, связанных с протони-
зования масс-спектрометрии МАЛДИ являлась экс-
рованием, а их взаимодействие с катионами метал-
прессность метода, на примере анализа образца (1)
лов приводит к образованию солей, а не заряженных
была проведена сравнительная оценка временных
комплексов.
затрат, необходимых для подтверждения наличия
Напротив, масс-спектры отрицательно заря-
активного вещества другими масс-спектрометриче-
женных ионов в большинстве случаев содержали
скими методами (ГХ/МС и ВЭЖХ/МС-ИЭР). В пер-
Новые матричные соединения для детектирования...
1195
Масс-спектры МАЛДИ действующего вещества лекарственного препарата Кетопрофен Органика, полученные
с помощью матричных соединений: 4-(диметиламино)бензальдегида (а), N,N-диметил-п-фенилендиамина (б),
3-аминохинолина (в), 9-аминоакридина (г).
1196
Хрущева М. Л. и др.
Таблица 3
Результаты применения различных матричных соединений для регистрации масс-спектров отрицательных
ионов исследованных соединений*
Матричные соединения
N,N-
2,5-дигидрок-
2-(4-гидрокси-
3-индол-
4-(диметил-
Соединение
1,8,9-антра-
3-амино-
9-амино-
диметил-п-
сибензойная
фенилазо)бен-
акриловая
акридин
амино)бенз-
центриол
хинолин
акридин
фенилен-
кислота
зойная кислота
кислота
альдегид
диамин
Ибупрофен
-
-
-
-
++
+
+
+++
++
Диклофенак
-
-
-
-
+
-
-
++
++
Кеторолак
-
+
-
+
+
-
-
++
+
Этодолак
-
+
+
-
++
-
-
+++
+++
Декскетопрофен
-
-
-
-
+
-
-
+++
++
Индометацин
-
-
-
-
++
+
-
+++
++
Кетопрофен
-
-
-
-
+
+
-
+++
+++
Напроксен
-
-
-
-
+
-
-
+++
++
Тиапрофеновая
–
-
+
-
++
+
-
+++
++
кислота
Нимесулид
-
-
+
-
++
++
+
+++
+++
* «-» — пик депротонированной молекулы отсутствует в масс-спектре; «+» — пик депротонированной молекулы
присутствует в масс-спектре, однако его интенсивность меньше, чем интенсивности других пиков ионов в масс-спектре;
«++» — пик депротонированной молекулы присутствует в масс-спектре, и его интенсивность сравнима с интенсивностя-
ми других пиков ионов в масс-спектре; «+++» — пик депротонированной молекулы присутствует в масс-спектре, и его
интенсивность существенно выше интенсивностей других пиков ионов в масс-спектре.
вом случае помимо сравнительно продолжительного
Выводы
времени анализа (14 мин) потребовалось проведение
дополнительной стадии пробоподготовки, а именно
Таким образом, метод масс-спектрометрии с
силилирования, что увеличило суммарное время,
МАЛДИ может быть использован для экспрессного
необходимое для тестирования одного образца до
установления подлинности фармацевтических суб-
19 мин. Во втором случае анализ потребовал суще-
станций и лекарственных препаратов, а также каче-
ственно меньшего времени, так как использовался
ственного определения кислотосодержащих несте-
режим непосредственного введения раствора аналита
роидных противовоспалительных средств в образцах
в источник ионов. Общее время, требующееся для
различного генезиса (биологических, природных).
анализа одного образца, включающее растворение
Для НПВС, содержащих карбоксильные или суль-
пробы, ее фильтрование и регистрацию масс-спек-
фамидные группы, предложено использовать депро-
тра, составило в среднем 9 мин, что меньше вре-
тонирующие матрицы, которые обеспечивают высо-
мени, необходимого для регистрации масс-спектра
кую чувствительность метода масс-спектрометрии с
МАЛДИ (11 мин с учетом шлюзования мишени).
МАЛДИ в режиме регистрации отрицательно заря-
Вместе с тем переход к потоковому анализу боль-
женных ионов. Очевидно, что предложенный способ
шого числа образцов методом масс-спектрометрии
позволяет селективно детектировать вещества кисло-
с МАЛДИ позволил существенно снизить общие за-
го характера на фоне других компонентов, не претер-
траты времени до 3 мин на образец, что обусловлено
певающих процесс депротонирования. Среди апроби-
необходимостью лишь однократного шлюзования
рованных в работе протон-отщепляющих матричных
мишени с нанесенными на нее несколькими образ-
соединений выявлены наиболее эффективные из них,
цами и автоматической регистрацией масс-спектра.
которыми являются 4-(диметиламино)бензальдегид и
В то же время в случае ВЭЖХ/МС-ИЭР установлено,
N,N-диметил-п-фенилендиамин. Данные соединения
что потенциал снижения времязатрат значительно
можно рекомендовать для применения в качестве
меньше, и анализ одной пробы в потоковом режиме
матричных при использовании комбинации методов
занял 6 мин.
ТСХ/МАЛДИ-МС.
Новые матричные соединения для детектирования...
1197
Благодарности
Различия в фармакокинетике ибупрофена в моно-
и многокомпонентных препаратах // Ведомости
Работа выполнена с использованием оборудования
НЦЭСМП. 2017. Т. 7. № 2. С. 117-121.
ЦКП «Аналитический центр проблем глубокой пере-
[4]
Pyka A. Detection progress of selected drugs in TLC //
работки нефти и нефтехимии» ИНХС РАН.
Biomed. Res. Int. 2014. ID 732078.
[5]
Ferey J., Da Silva D., Lafite P., Daniellou R.,
Финансирование работы
Maunit B. TLC-UV hyphenated with MALDI-TOFMS
for the screening of invertase substrates in plant
Работа выполнена в рамках государственного
extracts // Talanta. 2017. V. 170. P. 419-424.
задания ФГБУ НЦЭСМП Министерства здраво-
охранения России № 056-00003-20-00 на проведение
[6]
Seigel A., Schröck A., Hauser R., Spangenberg B.
прикладных научных исследований (номер государ-
Sensitive quantification of diclofenac and ibuprofen
ственного учета НИР AAAA-A18-118021590049-0),
using thin layer chromatography coupled with a vibrio
подбор матричных соединений для детектирования
fisheri bioluminescence assay // J. Liq. Chromatogr.
карбоксилсодержащих НПВС проводился при фи-
Rel. Techn. 2011. V. 34. N 10-11. P. 817-828. https://
нансовой поддержке Российского фонда фундамен-
[7]
Ваталев А. А., Киреева А. В., Куклин В. Н. Химико-
тальных исследований в рамках проекта 19-33-60037
токсикологическое исследование некоторых не-
Перспектива.
стероидных противовоспалительных средств //
[8]
Гильдеева Г. Н., Плетень Б. А., Дорофеев В. Л.
Конфликт интересов
Анализ воспроизведенных лекарственных средств
Хрущева М. Л. является научным редактором
группы НПВС методом тонкослойной хроматогра-
Журнала прикладной химии, другие соавторы заявля-
фии // Фармация. 2010. № 2. C. 23-24.
ют об отсутствии конфликта интересов, требующего
[9]
Taylor P. J. Matrix effects: The Achilles heel of
раскрытия в данной статье.
quantitative high-performance liquid chromatography-
electrospray-tandem mass spectrometry // Clinical
Biochem. 2005. V. 38. N 4. P. 328-334.
Информация об авторах
[10]
Wells J. M.,
Roth M. J.,
Keil A. D.,
Хрущева Мария Леонидовна, к.х.н.,
Grossenbacher J. W., Justes D. R., Patterson G. E.,
Barket D. J. Implementation of DART and DESI
Кривошеина Мария Сергеевна,
ionization on a fieldable mass spectrometer // J. Am.
Soc. Mass Spectrom. 2008. V. 19. N 10. P. 1419-1424.
Матвеева Мария Дмитриева, к.х.н.,
[11]
Ostermann K. M., Luf A., Lutsch N. M., Dieplinger R.,
Жиляев Дмитрий Игоревич, к.х.н.,
Mechtler T. Р., Metz T. F., Schmid R., Kasper D. C.
MALDI Orbitrap mass spectrometry for fast and
simplified analysis of novel street and designer drugs //
Борисов Роман Сергеевич, к.х.н.,
Clinica Chimica Acta. 2014. V. 433. P. 254-258.
[12]
Zaikin V. G., Borisov R. S., Polovkov N. Yu.,
Slyundina M. S. Reactive matrices for matrix-assisted
Список литературы
laser desorption/ionization mass spectrometry of
[1] Шостак Н. А., Клименко А. А. Нестероидные про-
primary amines // Eur. J. Mass Spectrom. 2015. V. 21.
тивовоспалительные препараты — современные
аспекты их применения // Клиницист. 2013. № 3-4.
[13]
Слюндина М. С., Половков Н. Ю., Борисов Р. С.,
С. 53-61.
Заикин В. Г. Триптамин: реакционная матри-
[2] Олейникова Т. А., Пожидаева Д. Н. Анализ тен-
ца в масс-спектрометрии МАЛДИ // Масс-
денций развития фармацевтического рынка не-
спектрометрия. 2016. Т. 13. № 4. С. 220-224
стероидных противовоспалительных препаратов
[Slyundina M. S., Polovkov N. Y., Borisov R. S.,
в России // Ремедиум. 2018. № 5. С. 14-20. http://
Zaikin V. G. Tryptamine: A reactive matrix for
MALDI mass spectrometry // J. Anal. Chem. 2017.
[3] Красных Л. М., Смирнов В. В., Василенко Г. Ф.,
V. 72. N 13. P. 1295-1299.
Горошко О. А., Егоренков Е. А., Зозина В. И.
1198
Хрущева М. Л. и др.
[14] Borisov R. S., Zhilyaev D. I., Polovkov N. Yu.,
[16] Vermillion-Salsbury R. L.,
Hercules D. M.
Zaikin V. G. Simple approach to derivatization
9-Aminoacridine as a matrix for negative mode
of alcohols and phenols for the analysis by
matrix-assisted laser desorption/ionization // Rapid
matrix(surface)-assisted laser desorption/ionization
Commun. Mass Spectrom. 2002. V. 16. P. 1575-1581.
time-of-flight mass spectrometry // Rapid Commun.
Mass Spectrom. 2014. V. 28. P. 2231-2236. https://
[17] Rohmer M., Meyer B., Mank M., Stahl B., Bahr U.,
Karas M. 3-Aminoquinoline acting as matrix and
[15] Calvano C. D., Monopoli A., Cataldi T. R. I.,
derivatizing agent for MALDI MS analysis of
oligosaccharides // Anal. Chem. 2010. V. 82. N 9.
weight compounds: An endless story? // Anal. Bioanal.
Chem. 2018. V. 410. P. 4015-4038.