Особенности сорбции родия(III) из хлоридных растворов на ионите с тиомочевинными функциональными группами
1311
Журнал прикладной химии. 2020. Т. 93. Вып. 9
УДК 546.97:544.726
ОСОБЕННОСТИ СОРБЦИИ РОДИЯ(III) ИЗ ХЛОРИДНЫХ РАСТВОРОВ
НА ИОНИТЕ С ТИОМОЧЕВИННЫМИ ФУНКЦИОНАЛЬНЫМИ ГРУППАМИ
© С. А. Егоров, А. А. Блохин, Ю. В. Мурашкин
Санкт-Петербургский государственный технологический институт (технический университет),
190013, г. Санкт-Петербург, Московский пр., д. 26
Поступила в Редакцию 10 февраля 2020 г.
После доработки 5 апреля 2020 г.
Принята к публикации 17 апреля 2020 г.
Изучена сорбция родия(III) на комплексообразующих ионитах Purolite S914 с тиомочевинными, Purolite
S920 с изотиомочевинными, Purolite S924 с тиольными функциональными группами и Purolite S924/K,
содержащем одновременно тиольные и карбоксильные группы (далее S914, S920, S924 и S924/K со-
ответственно) из 4 М растворов хлороводородной кислоты, предварительно выдержанных или при
комнатной температуре, или при температуре ~80°С, в присутствии (г·л-1): Fe(III) — 6.0, Al(III) —
4.2, Zn(II) — 5.2, Sn(IV) — 4.1 и Ce(III) — 2.0. Установлено, что по способности к сорбции родия(III)
иониты S914 и S920 существенно превосходят иониты S924 и S924/K, а предварительное выдержива-
ние растворов при температуре ~80°С приводит к повышению емкости этих ионитов по родию(III)
и возрастанию скорости сорбции родия(III) на ионите S914. Скорость сорбции родия(III) на ионите
S914 независимо от способа предварительной подготовки растворов при комнатной температуре
низка и заметно возрастает при повышении температуры сорбции до 60°С. Показана возможность
глубокого извлечения родия(III) (до 99%) из многокомпонентных хлоридных растворов, предварительно
выдержанных при температуре ~80°С, на ионите S914 с тиомочевинными функциональными группами
в динамических и статических условиях при 56°С.
Ключевые слова: родий; хлоридные растворы; температурная обработка; сорбция; десорбция; ио-
ниты
DOI: 10.31857/S0044461820090078
Одним из наиболее эффективных методов извле-
чем реакции обмена молекул воды, находящихся во
чения палладия(II) и платины(II) и (IV) из хлоридных
внутренней координационной сфере аквахлоридных
растворов сложного состава является сорбционный
комплексов родия(III), на хлорид-ион или иные лиган-
метод, основанный на использовании ионитов с тио-
ды протекают с весьма низкой скоростью. При этом
мочевинными или изотиомочевинными функцио-
координационно-насыщенный гексахлоридный ком-
нальными группами [1-4]. Однако применение таких
плекс родия(III) [RhCl6]3- существенно более лабилен
ионитов не обеспечивает приемлемого извлечения ро-
и, следовательно, реакционноспособен по сравнению
дия(III), остаточная концентрация которого в раство-
с аквахлоридными комплексами [8]. Представлялось,
рах после сорбции может достигать 10 мг∙л-1 и более
что предварительный перевод основной части ро-
[3, 4]. По мнению авторов [2, 4, 5], это вызвано суще-
дия(III) в гексахлоридную форму позволит повысить
ственно более низкой скоростью сорбции родия(III)
полноту его сорбционного извлечения. В работе [9]
по сравнению со скоростью сорбции палладия(II) и
на основании изучения электронных спектров по-
платины(II) и (IV) на тио- и изотиомочевинных ио-
глощения родия(III) в растворах хлороводородной
нитах. Действительно, хорошо известна [6, 7] кине-
кислоты было показано, что повышение температуры
тическая инертность аквахлоридных комплексов ро-
приводит к ускорению реакций обмена молекул воды,
дия(III) [Rh(H2O)nCl6-n]n-3, в виде которых родий(III)
находящихся во внутренней координационной сфере
присутствует в реальных хлоридных растворах, при-
аквахлоридных комплексов родия(III), на хлорид-ион
1312
Егоров С. А. и др.
и существенному повышению доли родия(III), при-
выдержанных как при комнатной, так и при повы-
сутствующего в виде гексахлоридного комплекса.
шенной температуре. Навески ионитов в контакте с
Ранее авторами [10] было установлено, что предва-
растворами выдерживали при комнатной температу-
рительное выдерживание хлоридных растворов при
ре (20-22°С) в течение 14 сут при перемешивании
повышенной температуре позволяет существенно
в дневные часы на шейкере Memmert WNB 14. По
повысить полноту извлечения родия(III) при сорбции
истечении указанного времени растворы отделяли
его на макропористом слабоосновном анионите на
от ионитов и проводили их анализ на родий(III). По
стирольной матрице с первичными, вторичными и
изменению концентрации родия(III) с учетом наве-
третичными аминогруппами. Поскольку для одно-
ски ионита и объема раствора рассчитывали значе-
временного извлечения палладия(II), платины(II) и
ния массовой емкости ионитов [г родия(III)/г сухого
родия(III) было бы целесообразно использовать один
ионита], которые затем с учетом удельного объема
и тот же сорбент, представлялось полезным оценить,
ионитов пересчитывали на объемную емкость [г ро-
не позволит ли этот прием улучшить показатели сорб-
дия(III)/л набухшего ионита].
ционного извлечения родия(III) и при использовании
Кинетику сорбции родия(III) изучали методом
ионитов с тиомочевинными или изотиомочевинными
ограниченного объема. Использовали ионит S914
функциональными группами. Кроме того, определен-
фракции 0.63-1.0 мм во влажном (набухшем) состоя-
ные перспективы могут иметь и иониты с тиольными
нии. Сорбцию вели из 4 М раствора HCl с концентра-
функциональными группами, которые, например, про-
цией родия(III) 0.2 г·л-1. Раствор после приготовления
являют высокую избирательность к палладию(II) [11].
в одном случае был выдержан при комнатной темпе-
Цель работы — исследование сорбции родия(III)
ратуре в течение 14 сут, в другом — при температуре
из хлоридных растворов, предварительно выдержан-
~80°С в течение 7 ч. В стакан вводили исходный рас-
ных как при комнатной, так и при повышенной тем-
твор объемом 100 мл, стакан с раствором помещали
пературе, на ионитах, содержащих в качестве функци-
в термостат и выдерживали до достижения заданной
ональных групп тиомочевинные, изотиомочевинные
температуры. Затем навеску ионита 1 г (в пересчете
и тиольные группы, и выявление возможности и ус-
на сухую массу) помещали в ячейку с отверстия-
ловий применения этих ионитов для извлечения ро-
ми, конструкция которой приведена в монографи-
дия(III) из многокомпонентных хлоридных растворов.
и,* укрепленную на оси механической мешалки, и
приводили в контакт с раствором, после чего сразу
включали мешалку. Скорость вращения мешалки под-
Экспериментальная часть
держивали равной 300 об·мин-1. Через определенные
В работе были исследованы макропористые иони-
промежутки времени отбирали пробы раствора для
ты, синтезированные на стирольной матрице: Purolite
анализа на родий(III). Суммарный объем отобранных
S914 с тиомочевинными, Purolite S920 с изотиомо-
проб не превышал 5% от общего объема раствора.
чевинными, Purolite S924 с тиольными функцио-
Эксперименты по извлечению родия(III) из мно-
нальными группами и Purolite S924/K, содержащий
гокомпонентных хлоридных растворов в статиче-
одновременно тиольные и карбоксильные группы,
ских условиях в двухступенчатом режиме проводи-
далее обозначенные как S914, S920, S924 и S924/K
ли следующим образом: в колбы отбирали по 30 мл
соответственно. Все иониты предварительно были
растворов, предварительно выдержанных или при
переведены в протонированную форму обработкой
комнатной температуре, или при температуре 80°С.
1 М раствором хлороводородной кислоты с последу-
Затем в растворы вводили ионит S914 в соотношении
ющей промывкой дистиллированной водой.
масса ионита (г в пересчете на сухой ионит):объем
Рабочие растворы после приготовления выдер-
раствора (мл), равном 1:100. Ионит и раствор переме-
живали при комнатной температуре в течение 14 сут
шивали механической мешалкой в колбе в термостате
или при температуре 80 ± 3°С в стеклянной колбе,
в течение 4 ч (время контакта ионита с раствором на
снабженной обратным холодильником, на колбона-
одной ступени) или при температуре 20°С, или при
гревателе в течение 7 ч [9].
температуре 56°С при той же скорости вращения ме-
Эксперименты по изучению сорбции и десорбции
шалки, что и при изучении кинетики сорбции. По ис-
родия(III) проводили в статических и динамических
течении указанного времени контакта ионит отделяли
условиях. Эксперименты в статических условиях про-
от раствора и раствор анализировали на родий(III).
водили по следующей методике: навески ионитов c
фиксированной влажностью массой 0.15 г (в пересче-
те на сухой ионит) помещали в колбы и заливали
* Гельферих Ф. Иониты. Основы ионного обмена. М.:
15 мл растворов заданного состава, предварительно
ИЛ, 1962. C. 279-280.
Особенности сорбции родия(III) из хлоридных растворов на ионите с тиомочевинными функциональными группами
1313
Затем к раствору добавляли навеску свежего ионита
натной температуре, устанавливается лишь спустя
и описанные выше операции повторяли.
6 мес. Таким образом, в экспериментах по изуче-
Эксперименты в динамических условиях про-
нию сорбции родия(III) из растворов, не прошедших
водили в колонке, заполненной 7 мл ионита S914
активирование путем выдерживания при повышенной
фракции 0.4-0.63 мм, при соотношении высоты слоя
температуре, равновесие не было достигнуто.
ионита и внутреннего диаметра колонки, равном 7:1.
Поэтому оценка влияния температуры, при которой
Растворы в колонку подавали по направлению снизу
предварительно были выдержаны рабочие растворы,
вверх. Скорость пропускания растворов при сорб-
на емкостные характеристики ионитов по родию(III),
ции и десорбции поддерживали равной 7 мл·ч-1, или
проведенная на основании данных, представленных
1 уд. об.·ч-1 (уд. об. — удельный объем, т. е. объем
на рис. 1, носит достаточно условный характер.
раствора, отнесенный к объему находящегося в ко-
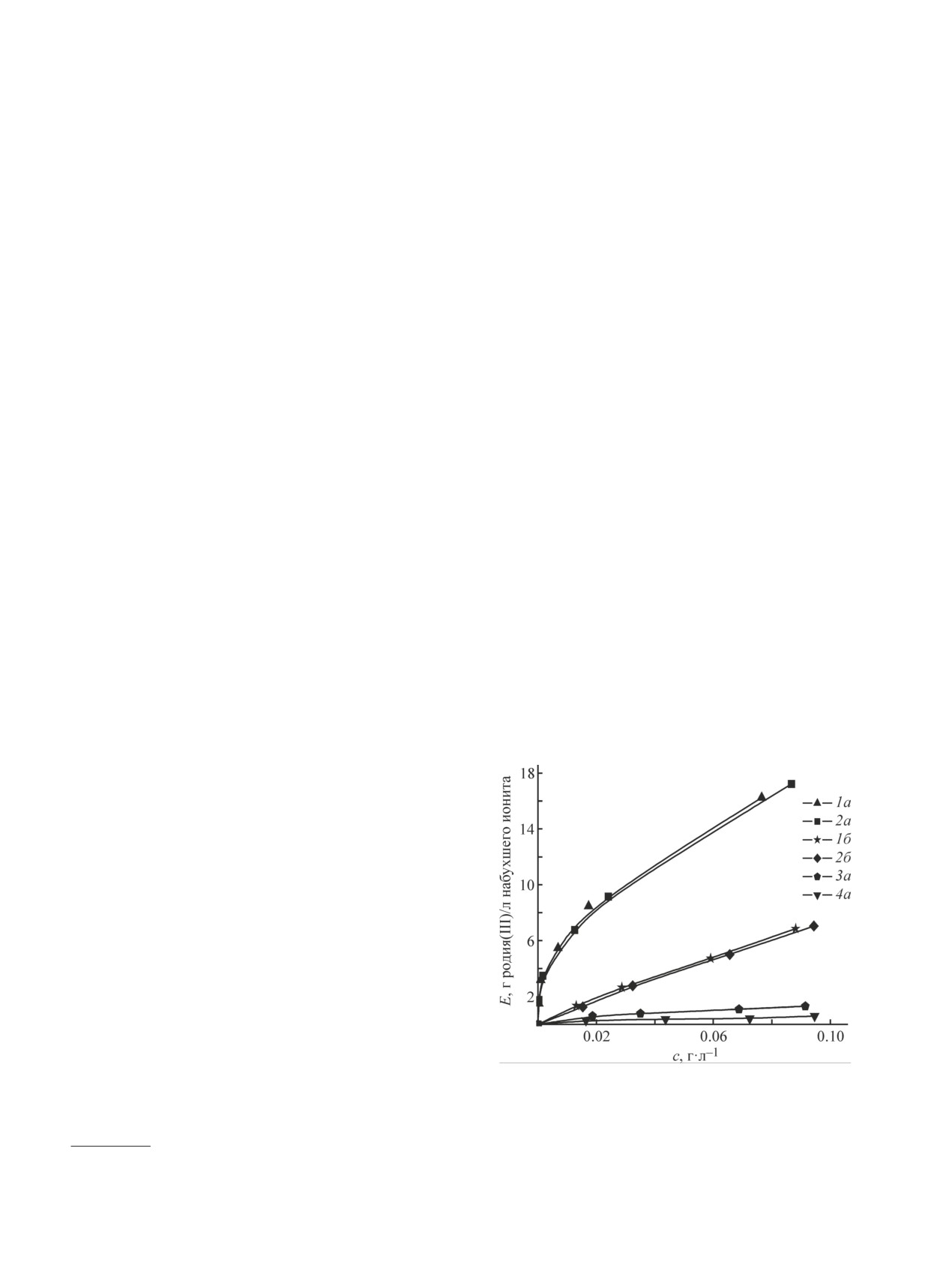
Из всех опробованных ионитов наибольшей се-
лонке ионита). При осуществлении операции сорбции
лективностью к родию(III) обладают иониты S914 и
и десорбции при повышенной температуре колонку
S920 с тиомочевинными и изотиомочевинными груп-
помещали в термостат. Пробы раствора отбирали на
пами соответственно (рис. 1). Предварительная тем-
выходе из колонки и анализировали на родий(III).
пературная обработка родийсодержащих хлоридных
Для определения концентрации родия(III) исполь-
растворов приводит к увеличению емкости ионитов
зовали фотоколориметрический метод анализа, ос-
S914 и S920 по родию(III) в 3-7 раз в зависимости от
нованный на измерении светопоглощения комплекса
концентрации родия(III) в растворах после контакта с
родия(III) с иодидом олова(II).* При определении
ионитами относительно их емкости, достигаемой при
родия(III) в тиомочевинных растворах пробы пред-
сорбции из растворов, выдержанных при комнатной
варительно обрабатывали царской водкой для разло-
температуре. Зависимости значений емкости этих
жения тиомочевины.
ионитов по родию(III) от его концентрации в раство-
рах, прошедших предварительную температурную
обработку, которые, с учетом того что при сорбции из
Обсуждение результатов
таких растворов равновесие было достигнуто, по сути
Для оценки избирательности и емкостных ха-
представляют собой изотермы сорбции родия(III),
рактеристик исследуемых ионитов по отношению к
имеют выпуклую форму. Иониты S924 и S924/К, в
родию(III) и влияния предварительной температур-
состав функциональных групп которых входят тиоль-
ной обработки растворов были изучены зависимо-
ные группы, родий(III) из данных растворов практи-
сти значений емкости ионитов по родию(III) от его
чески не сорбируют.
концентрации в растворах после контакта с ионита-
ми в течение заданного времени — 14 сут (рис. 1).
Исходные модельные растворы имели одинаковый
состав по макрокомпоненту — 4 моль·л-1 HCl и со-
путствующим компонентам, обычно присутствую-
щим в реальных технологических растворах (г·л-1):
Fe(III) — 6.0, Al(III) — 4.2, Zn(II) — 5.2, Sn(IV) — 4.1
и Ce(III) — 2.0. Концентрация родия(III) в исходных
растворах изменялась от 0.052 до 0.31 г·л-1. В одной
серии экспериментов исходные растворы после при-
готовления предварительно выдерживали при ком-
натной температуре в течение 14 сут, в другой — при
температуре ~80°С в течение 7 ч. Следует отметить,
что, как показали предварительные эксперименты,
заданного времени контакта ионитов с растворами
(14 сут) с избытком хватает для установления равно-
весия при сорбции из растворов, выдержанных при
Рис. 1. Зависимости значений емкости ионитов S914
повышенной температуре, в то время как равновесие
(1а, 1б), S920 (2а, 2б), S924 (3а), S924/К (4а) по ро-
при сорбции из растворов, выдержанных при ком-
дию(III) от его концентрации в растворах после контак-
та с ионитами в течение 14 сут из хлоридных растворов,
* Марченко З., Бальцежак М. Методы спектрофотоме-
предварительно выдержанных при температуре ~80°С
трии в УФ и видимой областях в неорганическом анализе.
в течение 7 ч (1а-4а) и при комнатной температуре в
М.: БИНОМ. Лаборатория знаний, 2009. С. 328-329.
течение 14 сут (1б, 2б).
1314
Егоров С. А. и др.
В связи с тем что эффект предварительной темпе-
кинетики сорбционного процесса), что свидетель-
ратурной обработки может сказываться на скорости
ствует о существенном вкладе скорости химической
сорбции родия(III) на ионитах с тиомочевинными и
реакции в общую скорость этого процесса. Уместно
изотиомочевинными группами, на примере ионита
также отметить, что гранулы ионитов S914 и S920
S914 были проведены сравнительные эксперименты
после насыщения последних родием(III) окрашива-
по изучению кинетики сорбции родия(III) из 4 М рас-
ются в желтый цвет, характерный для комплексов ро-
твора HCl, выдержанного при комнатной температуре
дия(III) с тиомочевиной [кислые хлоридные растворы
и при температуре ~80°С (рис. 2).
родия(III) имеют красный цвет]. Это дает основание
Предварительное выдерживание родийсодержаще-
полагать, что родий(III) сорбируется ионитами это-
го раствора при повышенной температуре действи-
го типа в основном не по анионообменному меха-
тельно приводит к некоторому возрастанию скорости
низму, а по механизму комплексообразования с их
сорбции родия(III), причем эта тенденция приобрета-
функциональными группами, т. е. путем замещения
ет более выраженный характер по мере увеличения
хлорид-ионов, содержащихся во внутренней коор-
времени контакта ионита с раствором (рис. 2). Кроме
динационной сфере родия(III), на фиксированные
того, независимо от способа предварительной подго-
тиомочевинные или изотиомочевинные группы.
товки раствора скорость сорбции родия(III) на ионите
С целью оценки влияния температуры сорбции и
S914 при комнатной температуре низка и существен-
температуры предварительного выдерживания рас-
но возрастает при повышении температуры до 60°С.
творов на достигаемое извлечение родия(III) из мно-
В работе [12] показано, что скорость образования
гокомпонентных хлоридных растворов была изучена
тиомочевинных комплексов родия(III) в растворах
сорбция родия(III) на ионите S914 в статических ус-
также низка при комнатной температуре, но заметно
ловиях в двухступенчатом режиме при температурах
увеличивается при повышении температуры. Исходя
20 и 56°С. В качестве исходных растворов исполь-
из этих данных, можно предположить, что столь вы-
зовались модельные растворы того же состава по
раженное влияние температуры на скорость сорб-
хлороводородной кислоте и сопутствующим компо-
ции родия(III) на ионите S914 обусловлено прежде
нентам, что и в экспериментах по исследованию за-
всего особенностями взаимодействия родия(III) с
висимостей значений емкости ионитов по родию(III)
фиксированными в матрице ионита тиомочевинны-
от его концентрации в растворах, с концентрацией ро-
ми группами. Действительно, как показано в работе
дия(III) в одном случае 0.237, в другом — 0.210 г·л-1,
[13], значения эффективной энергии активации про-
один из которых был выдержан при комнатной темпе-
цесса сорбции родия(III) на ионите S914 составляют
ратуре, другой — при температуре ~80°С. К одному
47.5-60.4 кДж·моль-1 (в зависимости от того, какая
и тому же раствору на каждой ступени добавляли
математическая модель использовалась для описания
навеску свежего ионита. Полученные данные пред-
ставлены в таблице.
Максимального значения степень извлечения ро-
дия(III), равного 99.0%, достигает за две ступени
сорбции при температуре 56°С из раствора, предвари-
тельно выдержанного при повышенной температуре
(см. таблицу). В этих же условиях степень извлечения
родия(III) из раствора, выдержанного при комнатной
температуре, составляет 91.9%. Таким образом, и при
осуществлении сорбции родия(III) при повышенной
температуре предварительная температурная обра-
ботка растворов дает положительный эффект.
Для более полной оценки влияния температурного
режима сорбции на показатели извлечения родия(III)
на ионите S914 в завершение работы были проведе-
ны эксперименты в динамических условиях (рис. 3).
Сорбцию вели из растворов того же состава по со-
путствующим компонентам, что и в предыдущем
Рис. 2. Зависимости емкости ионита S914 по родию(III)
эксперименте. Концентрация родия(III) в первой пор-
от времени контакта с 4 М раствором HCl при темпера-
туре 20 (1а, 1б) и 60°С (2а, 2б).
ции исходного раствора составила 0.20, во второй —
Раствор был предварительно выдержан при комнатной
0.25 г·л-1. Оба раствора были предварительно выдер-
температуре (1а, 2а) и при температуре ~80°С (1б, 2б).
жаны при температуре 80°С. В первом эксперименте
Особенности сорбции родия(III) из хлоридных растворов на ионите с тиомочевинными функциональными группами
1315
Сорбция родия(III) на ионите S914 в статических условиях в двухступенчатом режиме
сRh(III), г·л-1
Суммарная степень
Температура
Исходный раствор
Число ступеней
извлечения родия,
сорбции, °С
в исходном
в растворе после
%
растворе
контакта с ионитом
Выдержанный при тем-
20
1
0.237
0.162
31.6
пературе ~80°С
2
0.237
0.153
35.4
56
1
0.210
0.009
95.7
2
0.210
0.002
99.0
Выдержанный при ком-
56
1
0.210
0.021
90.0
натной температуре
2
0.210
0.017
91.9
сорбцию вели при комнатной температуре, во втором
Таким образом, при сорбции родия(III) на ионите
— при 56°С. После насыщения родием(III) ионит про-
S914 в динамических условиях при температуре 56°С
мыли 2 М раствором HCl. Десорбцию в соответствии
из многокомпонентных хлоридных растворов, пред-
с рекомендациями [1, 2, 12] проводили раствором тио-
варительно выдержанных при повышенной темпера-
мочевины 70 г·л-1 в 0.3 М HCl при температуре 56°С.
туре, происходит существенное повышение полноты
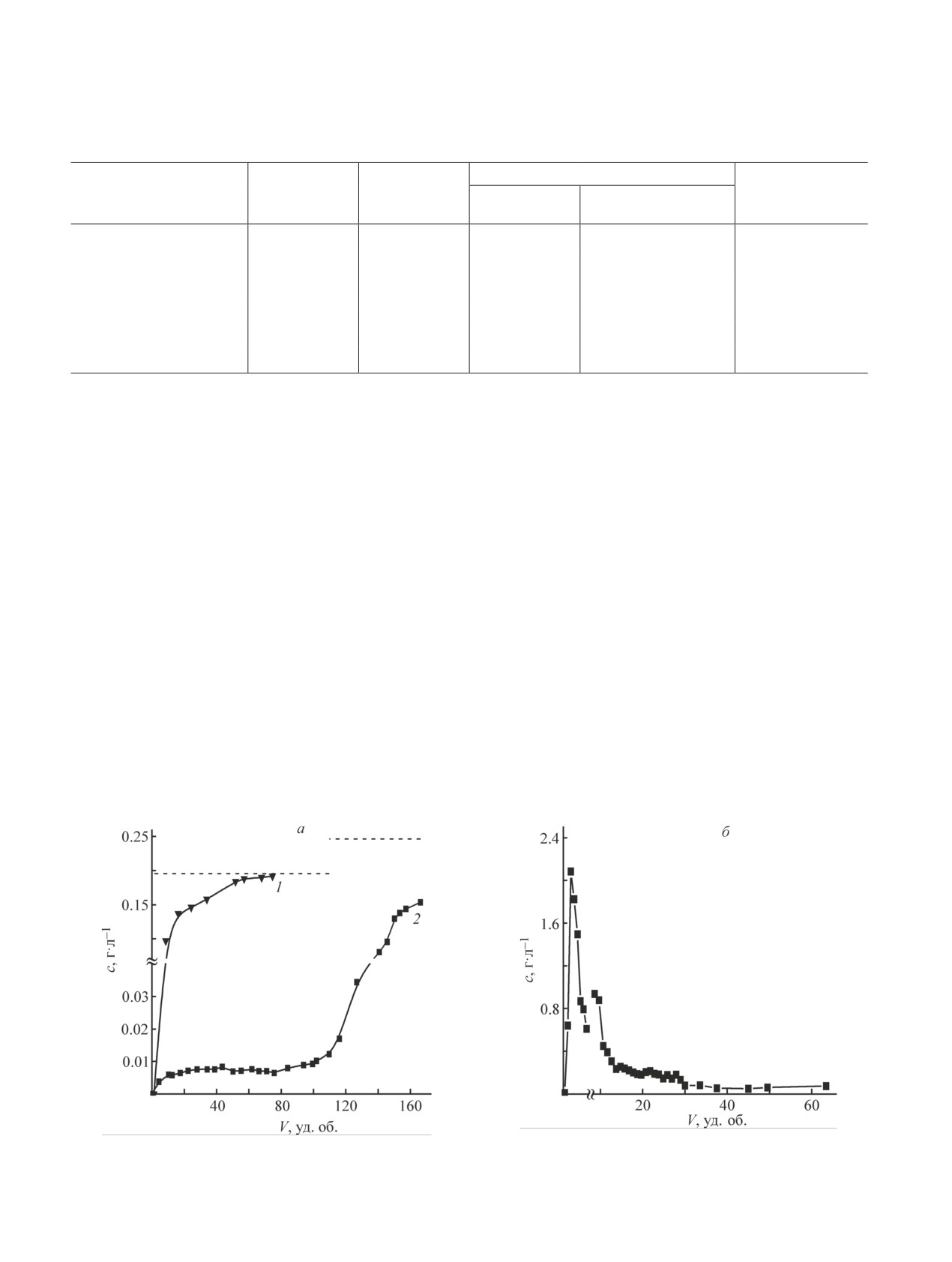
При проведении сорбции при температуре 20°С
извлечения родия(III) по сравнению с достигаемой
проскок родия(III) наблюдался уже в первых пор-
при его сорбции из тех же растворов при комнатной
циях пропущенного раствора, и концентрация его в
температуре.
растворе на выходе из колонки по мере дальнейшего
Десорбция родия(III) была проведена из ионита,
пропускания раствора резко нарастала, при темпера-
насыщенного при сорбции из раствора при температу-
туре 56°С концентрация родия(III) в первых 75 уд.
ре 56°С. В процессе десорбции (рис. 3, б) произошло
об. пропущенного раствора не превысила 6-7 мг·л-1
концентрирование родия(III), его концентрация в
(рис. 3, а). По мере дальнейшего пропускания раство-
наиболее богатой фракции элюата составила 2.1 г·л-1,
ра концентрация родия(III) в растворе на выходе из
в усредненном элюате — 0.5 г·л-1, что в 10.5 и
колонки постепенно увеличивалась. Явный проскок
2.5 раза соответственно превосходит его концентра-
родия(III) наступил после пропускания 110 уд. об.
цию в растворе, подаваемом на сорбцию. При этом
раствора. Средняя концентрация родия(III) в первых
применение подкисленного раствора тиомочевины
110 уд. об. пропущенного раствора составила 8 мг·л-1,
не обеспечило полную десорбцию родия(III) из ио-
что соответствует степени его извлечения ~96%.
нита с тиомочевинными функциональными группа-
Насыщение ионита родием(III) не было достигнуто.
ми: степень десорбции родия(III) составила ~48%.
Риc. 3. Выходные кривые сорбции родия(III) на ионите S914 при температуре 20 (1) и 56°С (2) (а) и десорбции ро-
дия(III) раствором тиомочевины 70 г·л-1 в 0.3 М HCl из ионита, насыщенного родием(III) при температуре 56°С (б)
(при проведении десорбции после пропускания первых 8 уд. об. раствора эксперимент был прерван на 14 ч).
1316
Егоров С. А. и др.
Выводы
тиновых металлов из отработанного электро-
лита процесса электрорафинирования золота //
Выявлена способность ионитов S914 с тиомо-
Драгоценные камни. Драгоценные металлы. 2008.
чевинными и S920 с изотиомочевинными функци-
№ 11. С. 170-173.
ональными группами к избирательной сорбции ро-
[4]
Nikoloski A. N., Ang K-L., Li D. Recovery of platinum,
дия(III) из 4 М растворов хлороводородной кислоты,
palladium and rhodium from acidic chloride leach
содержащих Fe(III), Al(III), Zn(II), Sn(IV) и Ce(III) в
solution using ion exchange resins // Hydrometallurgy.
концентрациях, более чем на порядок превосходящих
2015. V. 152. P. 20-32.
концентрацию родия(III). Показано, что предвари-
тельное выдерживание родийсодержащих растворов
[5]
Борбат В. Ф., Ярощик И. С., Шиндлер А. А. Термо-
динамика и кинетика сорбции родия(III) из соля-
при повышенной температуре (~80°С) способствует
нокислых растворов хелатными смолами // Вестн.
повышению емкости этих ионитов по родию(III) и
Омск. ун-та. 2010. № 4. С. 101-104.
ускорению его сорбции на ионите S914. Установлено,
[6]
Benguerel Е., Demopoulos G., Harris G. О. В.
что в связи с низкой скоростью сорбции родия(III)
Speciation and separation of rhodium(III)
на ионите S914 при комнатной температуре и суще-
from chloride solutions: A critical review //
ственном ее ускорении при повышении температуры
Hydrometallurgy. 1996. V. 40. N 1-2. P. 135-152.
до 60°С сорбционное извлечение родия(III) с помо-
щью этого ионита следует проводить при повышен-
[7]
Буслаева Т. М., Симанова С. А. Состояние плати-
ной температуре. Показано, что предварительное
новых металлов в солянокислых и хлоридных вод-
активирование родия(III) путем выдерживания рас-
ных растворах. Палладий, платина, родий, иридий
творов при температуре ~80°С и последующее про-
// Координац. химия. 1999. Т. 25. № 3. С. 165-176.
ведение его сорбции при повышенной температуре
[8]
Nikoloski A. N., Ang K.-L. Review of the application
(56°С) позволяет заметно повысить полноту извле-
of ion exchange resins for the recovery of platinum-
чения родия(III) при сорбции на ионите S914 как в
group metals from hydrochloric acid solutions //
Mineral Process. Extr. Metall. Rev. 2014. V. 35. N 6.
статических, так и динамических условиях.
P. 369-389.
Конфликт интересов
[9]
Егоров С. А., Блохин А. А., Мурашкин Ю. В.
Влияние температурной и ультразвуковой обра-
Авторы заявляют об отсутствии конфликта инте-
ботки на состояние родия(III) в солянокислых
ресов, требующего раскрытия в данной статье.
растворах // V Междунар. конф. по химии и хим.
технологии: Сб. материалов. Ереван, 2017. С. 304-
Информация об авторах
306.
[10]
Tatarnikov A. V., Sokolskaya I., Shneerson Ya. M.,
Егоров Сергей Александрович,
Lapin A. Yu., Goncharov P. M. Treatment of platinum
flotation products // Platinum Metals Rev. 2004. V. 48.
Блохин Александр Андреевич, д.т.н., проф.,
N 3. P. 125-132.
Мурашкин Юрий Васильевич, к.х.н., доцент,
[11]
Hubicki Z., Wolowicz A. A comparative study of
chelating and cationic ion exchange resins for the
removal of palladium(II) complexes from acidic
chloride media // J. Hazard. Mater. 2009. V. 164.
Список литературы
N 2-3. P. 1414-1419.
[1] Warshawsky A. Integrated ion exchange and liquid-
liquid extraction process for the separation of platinum
[12]
Блохин А. А., Молошнева О. В., Мурашкин Ю. В.,
group metals (PGM) // Separation and Purification
Воронина С. Н. Кинетика десорбции родия из ком-
Methods. 1982. V. 11. N 2. P. 95-130.
плексообразующего ионита с тиомочевинными
функциональными группами раствором тиомоче-
[2] Warshawsky A., Fieberg M., Mihalik P., Murphy T. G.,
вины // Сорбцион. и хроматогр. процессы. 2011.
B Y. The separation of platinum group metals (PGM)
Т. 11. № 4. С. 467-472.
in chloride media by isothioronium resins // Sep. Purif.
[13]
Егоров С. А., Куразова В. А., Блохин А. А., Мураш-
Meth. 1980. V. 9. N 2. P. 209-265.
кин Ю. В. Кинетика сорбции родия(III) из хло-
ридных растворов на ионите с тиомочевинными
[3] Блохин А. А., Гельман Г. Е., Клеандров В. Т.,
функциональными группами // Изв. СПбГТИ (ТУ).
Мурашкин Ю. В. Сорбционное извлечение пла-
2019. № 49 (75). С. 3-8.