Журнал прикладной химии. 2021. Т. 94. Вып. 1
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ И МАТЕРИАЛЫ НА ИХ ОСНОВЕ
УДК 662.74:552
ПРОСТОЙ СПОСОБ ОЦЕНКИ ПАРАМЕТРА РАСТВОРИМОСТИ
МАЛЫХ МОЛЕКУЛ И ПОЛИМЕРНЫХ МАТЕРИАЛОВ
© А. М. Гюльмалиев, Л. А. Зекель, А. У. Дандаев, А. Е. Батов,
М. Х. Кадиева, Э. Э. Магомадов, Х. М. Кадиев
Институт нефтехимического синтеза им. А. В. Топчиева РАН,
119991, ГСП-1, г. Москва, Ленинский пр., д. 29
Поступила в Редакцию 15 апреля 2020 г.
После доработки 30 сентября 2020 г.
Принята к публикации 6 ноября 2020 г.
Исследование относится к проблеме подбора растворителя для органических полимеров при их хими-
ческой переработке. На основе метода расчета параметра растворимости малых молекул и поли-
мерных материалов А. А. Аскадского с использованием структурных элементов молекул предложены
простые расчетные схемы. На примере малых молекул и полимеров показано, что построенные ме-
тоды по точности не уступают методам Аскадского, Смолла и Ван Кревелена. Предложенные схемы
позволяют вычислить параметр растворимости и найти приемлемые растворители полимерного
материала с известным значением параметра растворимости. Схемы апробированы на конкретных
примерах и показана возможность их применения для подбора растворителя.
Ключевые слова: параметр растворимости; полимеры; растворитель; матрица структурных единиц
DOI: 10.31857/S0044461821010084
Разработка эффективных методов утилизации по-
установил, что растворение одного вещества в ряде
лимерных отходов, количество которых с каждым
растворителей связано с их «внутренним давлением»
годом все больше растет [1], необходима для решения
[2]. Он назвал величину энергии испарения 1 см3
двух важных задач одновременно — получения сырья
вещества
«плотностью энергии когезии» и
для повторного органического синтеза и улучшения
ввел в рассмотрение параметр δ, характеризующий
экологической обстановки. Одним из перспектив-
растворимость данного вещества:
ных методов вторичной переработки синтетических
органических и биополимерных материалов является
процесс их гидрокаталитической переработки. На
,
(1)
первом этапе процесса проводится подготовка сырья
к гидрогенизации путем перевода полимерных мате-
где ∆E0 = ∆H0 - RT, ∆H0 — скрытая теплота испаре-
риалов в жидкое состояние термообработкой в среде
ния жидкости, R — газовая постоянная, Т — абсолют-
органических растворителей. В качестве раствори-
ная температура, V — мольный объем.
телей можно использовать как отдельные индиви-
Согласно определению Гильдебранда два веще-
дуальные соединения, так и их смеси. Еще в 1951 г.,
ства будут растворяться друг в друге, если параметры
исследуя физическую природу растворимости поли-
растворимости их близки. При поиске лучших орга-
меров в различных растворителях, Дж. Гильдебранд
нических растворителей полимера часто оказывается
55
56
Гюльмалиев А. М. и др.
достаточным совпадение параметров растворимости
,
(3)
Гильдебранда δ самого полимера и жидкости с точ-
ностью до ±1.5 (кал·см-3)0.5 [2, 3]. Для полимеров
di — длина связи между двумя атомами, Ri — ван--
регулярного строения параметр δ вычисляется для
дер-ваальсовы радиусы соседних валентно-связанных
элементарного фрагмента.
атомов.***
Для малых молекул параметр растворимости δ
определяется по экспериментальным данным, тогда
Для оценки относительной доли занятого объема
как теплоту испарения ∆H0 для макромолекул экспе-
в общем объеме вещества используется коэффициент
риментально определить невозможно из-за того, что
молекулярной упаковки k [4]:
при температуре кипения они разлагаются. В литера-
туре к настоящему времени предложены различные
,
(4)
варианты расчетной схемы параметра δ.* Все они ба-
зируются на методе Гильдебранда с различными под-
где NA — число Авогадро, Vобщий — мольный объем
ходами к расчету параметра ∆H0. В связи c этим ин-
молекулы, Vсобственный — собственный объем 1 моль
тересно отметить метод Смолла и Ван Кревелена,**
молекулы.
в котором авторы ввели в рассмотрение структурные
В итоге расчет параметра растворимости δ сводит-
инкременты органических соединений и в предпо-
ся к формуле [6]
ложении, что их константы притяжения Fi и объемы
Vi являются аддитивными величинами, для расчета
(5)
параметра растворимости δ предложили формулу
Уравнение (4) примечательно тем, что оно приме-
нимо в равной степени как к малым молекулам, так
и полимерам. Величины ΔEi* = kE — энергия когезии
Следует отметить, что теоретическая оценка вели-
жидкости и ΔV для различных типов структурных
чины ∆H0, характеризирующей энергию межмолеку-
элементов органических молекул табулированы.
лярных взаимодействий, не простая задача. Поэтому
При практическом применении формулы (5) воз-
разными авторами для расчета ∆H0 применяются
никают следующие затруднения: расчетная схема
различные приближения. В настоящее время широко
параметра растворимости δ для конкретных случаев
применяется метод расчета Хансена, согласно которо-
достаточно трудоемкая, применение метода к смеси
му энергию межмолекулярных взаимодействий разде-
растворителей требует дополнительных исследований.
ляют на составляющие компоненты (дисперсионные,
Цель работы — упростить расчетную схему по
полярные и водородные связи), что является сложной
формуле (5), сделав ее более простой для поиска эф-
задачей [4, 5]. Авторами [6] на основе фундаменталь-
фективных растворителей полимерных материалов,
ных представлений о строении вещества выведен
сохранив при этом точность вычисления параметра
алгоритм расчета параметра растворимости δ как
растворимости δ.
для малых органических молекул-растворителей,
так и различных классов полимерных молекул. Для
вычисления мольных объемов по аддитивной схеме
Методы исследования
V = ∑ΔVi, где ΔVi — инкремент объема i-того атома,
Суть нашего подхода заключается в следующем:
вычисляется как объем сферы этого атома минус объ-
введение в рассмотрение набор структурных эле-
емы шаровых сегментов, отсекаемых на этой сфере
ментов — базисных функций для расчета величин
соседними валентно-связанными атомами:
∑ΔEi*, NA∑ΔVi и получение линейных корреляционных
i
i
,
(2)
уравнений по данным тестовых молекул. Для иллю-
страции расчетного метода перечень некоторых струк-
где hi — высота сегмента,
турных элементов и их обозначения приведены в табл. 1.
Выбор базиса, состоящего из таких структурных
элементов, хорош тем, что в нем учитываются все
атомы, входящие в молекулу, гибридные состояния
* Нестеров А. Е. Свойства растворов и смесей поли-
меров. Справочник по физической химии полимеров. Т. 1.
sp2 и sp3 базисных углеродных атомов, их окруже-
Киев: Наук. думка, 1984. С. 19-24.
** Там же.
*** Там же.
Простой способ оценки параметра растворимости малых молекул и полимерных материалов
57
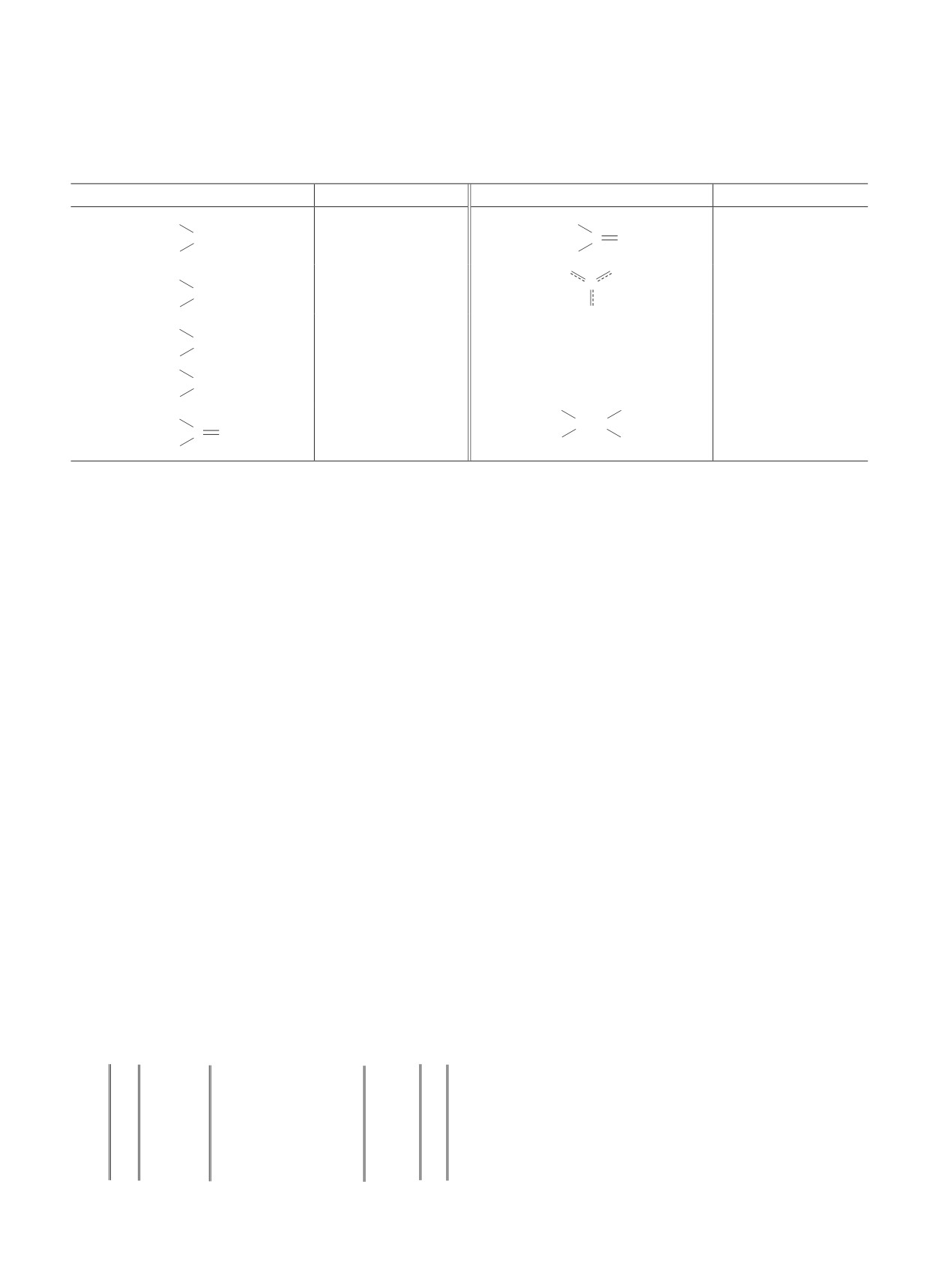
Таблица 1
Перечень некоторых структурных элементов для расчета параметра растворимости
Структурный элемент
Код
Структурный элемент
Код
H
C33
H
C21
H—C—
H—C
H
H
C32
C20
C
H—C—
H
C31
—OH
OH
H—C—
C30
—COOH
COOH
H—C—
H
C22
СОС
—COC—
H—C
H
ние водородными атомами. Отметим, что поскольку
где ‖ξ‖ — вектор структурных единиц n, ǁxǁ — прямо-
величины энергия и объем являются аддитивными,
угольная матрица размерностью (m∙n), ǁΨǁ — вектор
расчет их линейной функции в базисе структурных
тестовых молекул размерностью m, ǁxTǁ — транспо-
элементов из табл. 1 оправдан.
нированная к ǁxǁ матрица.
Эффективность такого базиса для расчета тер-
Матрица ǁxǁ приведена в табл. 2. Мы рассмотрели
модинамических функций, которые также являются
два варианта определения δ по тестовым соедине-
аддитивными, показана в работах [7-9]. Принятые
ниям.
структурные элементы (табл. 1) близки к структур-
Вариант I. По формуле (5) для ∆E = ∑ΔEi* и
i
ным элементам в методе Смолла и Ван Кревелена
∆V = NA∑ΔVi использовали данные из [4, 6]. Резуль-
[6], однако предлагаемая расчетная схема параметра
i
растворимости на их основе отличается.
таты расчета ∆E, ∆V и расчетного значения параметра
растворимости δI, а также для сопоставления их экс-
периментальные значения δэ [6] приведены в табл. 3.
Обсуждение результатов
Как видно из данных табл. 3, согласие расчет-
Любое аддитивное свойство вещества Ψ может
ных (δI) и экспериментальных (δэ) данных хорошее.
быть представлено в виде линейной функции свойств
Решением матричного уравнения (7) получены сле-
ее составляющих ξi:
дующие корреляционные уравнения:
— для расчета энергии взаимодействия по струк-
Ψj = ∑
nxiξi; j = 1, 2, …, m,
(6)
турным элементам
i
где n — количество структурных единиц; xi — коли-
∆E = ∑ΔEi* = 453.16128C33 + 726.115C32 +
i
чество i-той структурной единицы (дескриптора) в
+ 725.8986C31 + 17.499414C22 +
тестовой молекуле j и ξi — ее вклад в свойство Ψ; m —
(8)
+ 721.42582C21 + 855.25794C20 +
число тестовых молекул, подобранных для нахожде-
+ 4057.4583OH + 1377.3061COC +
ния значения i-того структурного элемента, m ≥ n.
Величины ξi определяются из матричного уравне-
+ 5052.8387COOH,
ния методом наименьших квадратов:
— для расчета молекулярного объема по структур-
ǁξǁ = ǁxTxǁ-1ǁxTΨǁ,
(7)
ным элементам
∆V = NA∑ΔVi = 14.4304C33 +
Ψ1
x11 x12 . . . x1n
ξ1
i
Ψ2
x21 x22 . . . x2n
ξ2
+ 10.1957C32 + 6.1709C31 +
(9)
ǁΨǁ =
; ǁxmnǁ =
; ǁξǁ =
,
+ 13.1753C22 + 8.6829C21 +
+ 4.5999C20 + 8.2510OH + 5.8365COC +
Ψm
xm1 xm2 . . . xmn
ξn
+ 18.9696COOH.
58
Гюльмалиев А. М. и др.
Таблица 2
Матрица структурных единиц тестовых молекул
xi
Молекула
C33
C32
C31
C22
C21
C20
OH
COC
COOH
Пентан
2
3
0
0
0
0
0
0
0
Гексан
2
4
0
0
0
0
0
0
0
Гептан
2
5
0
0
0
0
0
0
0
Октан
2
6
0
0
0
0
0
0
0
Нонан
2
7
0
0
0
0
0
0
0
Декан
2
8
0
0
0
0
0
0
0
Бензол
0
0
0
0
6
0
0
0
0
Нафтал
0
0
0
0
8
2
0
0
0
Толуол
1
0
0
0
5
1
0
0
0
Мезитлен
3
0
0
0
3
3
0
0
0
Стирол
0
0
0
1
6
1
0
0
0
Этанол
1
1
0
0
0
0
1
0
0
Уксусная кислота
1
0
0
0
0
0
0
0
1
Диэтиловый эфир
2
2
0
0
0
0
0
1
0
Изопен
3
1
1
0
0
0
0
0
0
Изопрен
1
0
0
2
1
1
0
0
0
Этиленгликоль
0
2
0
0
0
0
2
0
0
Фенол
0
0
0
0
5
1
1
0
0
Глицерин
0
2
1
0
0
0
3
0
0
Метанол
1
0
0
0
0
0
1
0
0
Диоксан
0
4
0
0
0
0
0
2
0
Уравнения (8) и (9) удобны тем, что для любо-
ΔE = 1440.9501C33 + 1074.2385C32 +
го органического соединения, содержащего такие
+ 78.072296C31 + 714.43777C22 +
структурные элементы, можно с хорошей точностью
+ 1217.1359C21 + 981.93910C20 +
(11)
вычислить δp = √ΔE/ΔV . Кроме того, по коэффициен-
+ 5995.9107OH + 1865.1030COC +
там при структурных элементах можно целенаправ-
+ 7608.3699COOH,
ленно подобрать растворитель с заданным значением
параметра δ.
— для расчета молекулярного объема
Вариант II. Для получения корреляционных урав-
нений используются экспериментальные значения
ΔV = 31.295590C33 + 16.790905C32 +
параметра растворимости δэ (кал·см-3)0.5 и мольные
6.5089851C31 + 26.054514C22 +
объемы V (см3·моль-1) тестовых молекул [6]. Энергия
+ 14.978392C21 +.76970526C20 +
(12)
межмолекулярного взаимодействия определяется по
+ 10.907515OH + 9.2999546COC +
формуле
+ 25.704410COOH.
ΔEi = ΔViδi2.
(10)
По формулам (10)-(12) вычисляются значения δII,
Аналогично первому варианту решением матрич-
ΔЕ и ΔV (табл. 4). Как видно из данных табл. 4, согла-
ного уравнения (7) получены следующие корреляци-
сие вычисленных значений δII с экспериментальными
онные уравнения:
данными удовлетворительное.
— для расчета энергии межмолекулярного взаи-
На рисунке сопоставлены результаты расчетов
модействия
δ тестовых молекул по трем вариантам δI, δII, δА с
Простой способ оценки параметра растворимости малых молекул и полимерных материалов
59
Таблица 3
Результаты расчетов по структурным элементам xi энергии взаимодействия ∆E = ∑ΔEi*, молекулярного объема
i
∆V = NA∑ΔVi, параметра растворимости δI
i
∆V,
δI
δэ [6]
Молекула
xi
∆E, кал
см3·моль-1
(кал·см-3)0.5
Пентан
2
3
0
0
0
0
0
0
0
3084.7
59.448
7.20
7.02
Гексан
2
4
0
0
0
0
0
0
0
3810.8
69.644
7.40
7.3
Гептан
2
5
0
0
0
0
0
0
0
4536.9
79.839
7.54
7.45
Октан
2
6
0
0
0
0
0
0
0
5263.0
90.035
7.65
7.55
Нонан
2
7
0
0
0
0
0
0
0
5989.1
100.23
7.73
7.65
Декан
2
8
0
0
0
0
0
0
0
6715.2
110.43
7.80
7.75
Бензол
0
0
0
0
6
0
0
0
0
4328.6
52.097
9.12
9.15
Нафталин
0
0
0
0
8
2
0
0
0
7481.9
78.663
9.75
9.9
Толуол
1
0
0
0
5
1
0
0
0
4915.5
62.445
8.87
8.9
Мезитлен
3
0
0
0
3
3
0
0
0
6089.5
83.140
8.56
8.8
Стирол
0
0
0
1
6
1
0
0
0
5201.3
69.872
8.63
8.66
Этанол
1
1
0
0
0
0
1
0
0
5236.7
32.886
12.62
12.7
Уксусная кислота
1
0
0
0
0
0
0
0
1
5506.0
33.400
12.84
12.6
Диэтиловый эфир
2
2
0
0
0
0
0
1
0
3735.9
55.089
8.23
7.4
Изопентан
3
1
1
0
0
0
0
0
0
2811.5
59.658
6.86
7.05
Изопрен
1
0
0
2
1
1
0
0
0
2064.8
54.064
6.18
7.25
Этиленгликоль
0
2
0
0
0
0
2
0
0
9567.1
36.911
16.10
15.7
Фенол
0
0
0
0
5
1
1
0
0
8519.8
56.274
12.30
12.1
Глицерин
0
2
1
0
0
0
3
0
0
14351.0
51.342
16.72
16.5
Метанол
1
0
0
0
0
0
1
0
0
4510.6
22.690
14.10
14.5
Диоксан
0
4
0
0
0
0
0
2
0
5659.1
52.456
10.39
10.0
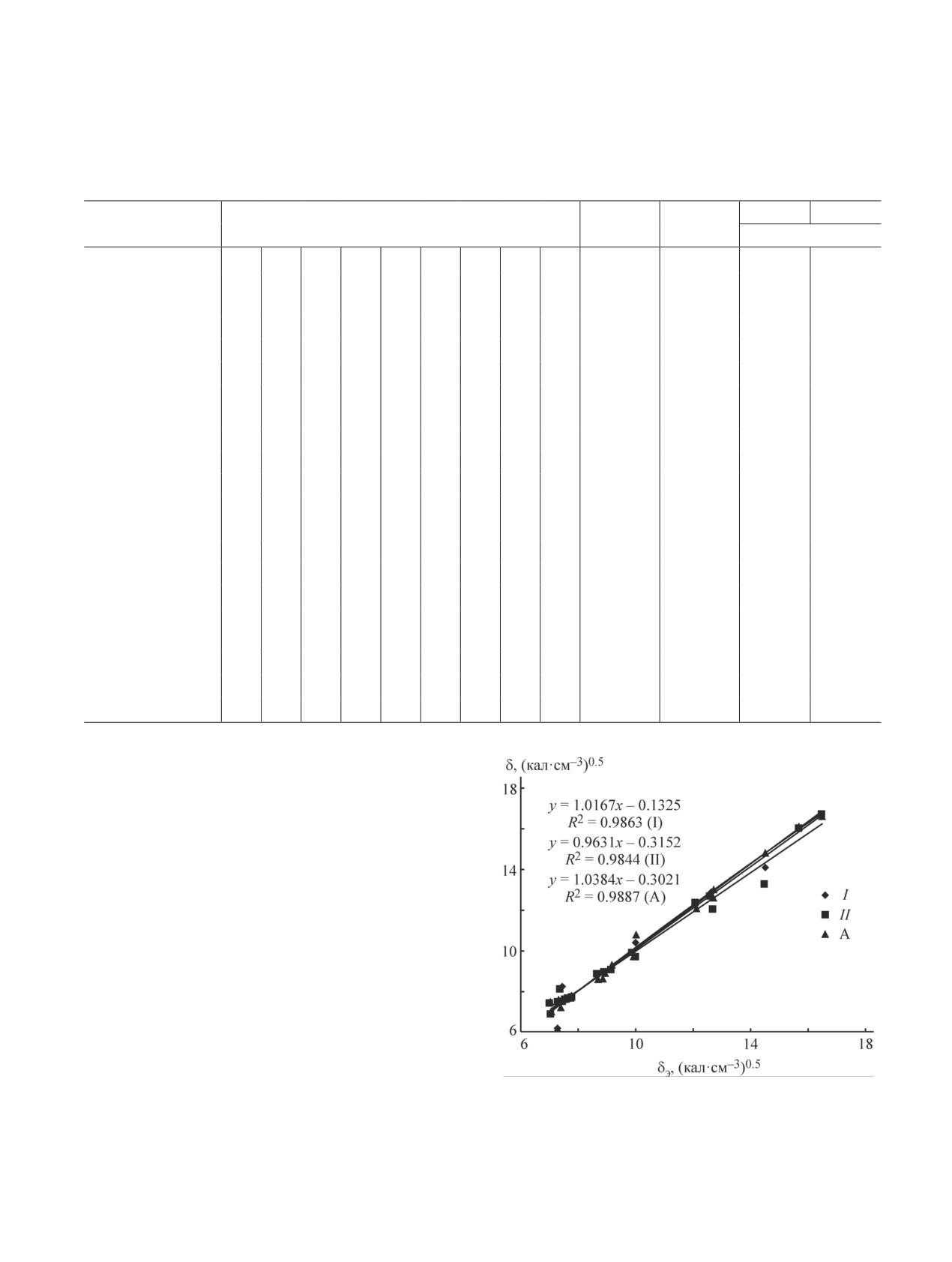
экспериментальными данными. Результаты сравне-
согласно [10], состоит из двух звеньев, который пред-
ния показывают, что все три способа практически
ставлен в табл. 5. Там же приведены структурные
приводят к одинаковым результатам.
единицы, входящие в состав элементарного фрагмен-
В качестве примера в рамках предложенной мето-
та, и их количества. Ниже в качестве примера приве-
дики расчета рассмотрим параметр растворимости
дена расчетная схема параметра δ для целлюлозы по
целлюлозы. Элементарный фрагмент целлюлозы,
варианту I:
Структурная
C33
C32
C31
C22
C21
C20
OH COC COOH
∑
единица
Число структурных
0
2
10
0
0
0
6
4
0
единиц
∆E
453.2
726.1
725.9
17.5
721.4
855.3
4057.5
1377.3
5052.8
38568.4
∆V
14.43
10.20
6.17
13.17
8.68
4.60
8.26
5.84
18.97
145.02
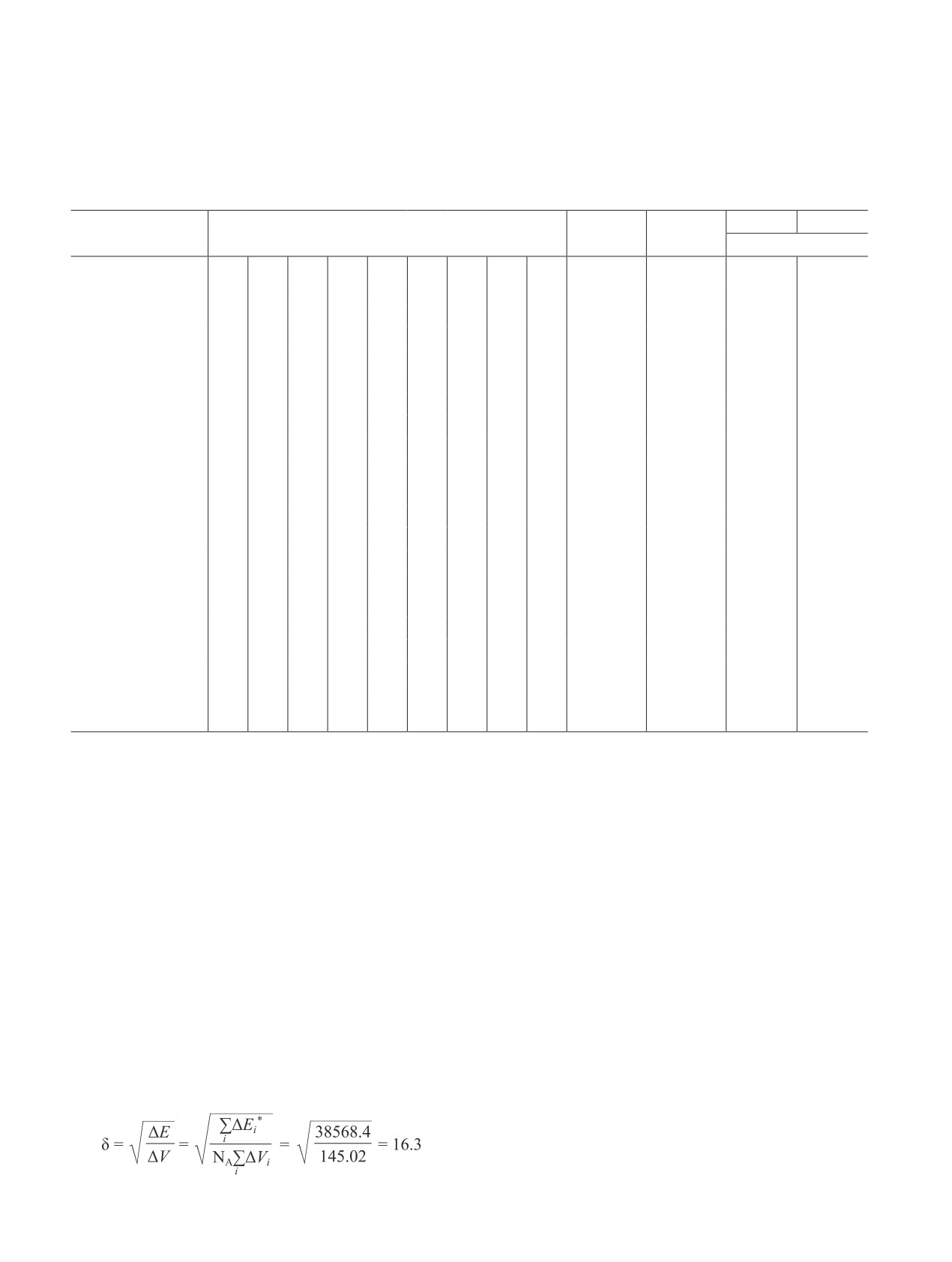
Далее по формуле (5) вычисляется δ:
В практическом применении расчетная схема
параметра растворимости δ в базисе структурных
единиц проще, чем в атомном базисе по формулам
(2)-(5) [4].
В табл. 5 также приведены результаты расчета
параметра δ «простых» молекул глицерина и мета-
60
Гюльмалиев А. М. и др.
Таблица 4
Результаты расчетов по структурным элементам xi энергии межмолекулярного взаимодействия ∆E,
мольного объема ∆V, параметра растворимости δII по варианту II.
∆V,
δII
δэ
Молекула
xi
∆E, кал
см3·моль-1
(кал·см-3)0.5
Пентан
2
3
0
0
0
0
0
0
0
6105
113.0
7.351
7.02
Гексан
2
4
0
0
0
0
0
0
0
7179
129.8
7.438
7.3
Гептан
2
5
0
0
0
0
0
0
0
8253
146.5
7.505
7.45
Октан
2
6
0
0
0
0
0
0
0
9327
163.3
7.557
7.55
Нонан
2
7
0
0
0
0
0
0
0
10400
180.1
7.599
7.65
Декан
2
8
0
0
0
0
0
0
0
11480
196.9
7.634
7.75
Бензол
0
0
0
0
6
0
0
0
0
7303
89.87
9.014
9.15
Нафталин
0
0
0
0
8
2
0
0
0
11700
121.4
9.819
9.9
Толуол
1
0
0
0
5
1
0
0
0
8509
107.0
8.919
8.9
Мезитлен
3
0
0
0
3
3
0
0
0
10920
141.1
8.796
8.8
Стирол
0
0
0
1
6
1
0
0
0
8999
116.7
8.782
8.66
Этанол
1
1
0
0
0
0
1
0
0
8511
58.99
12.01
12.7
Уксусная кислота
1
0
0
0
0
0
0
0
1
9049
57.00
12.60
12.6
Диэтиловый эфир
2
2
0
0
0
0
0
1
0
6895
105.5
8.086
7.4
Изопентан
3
1
1
0
0
0
0
0
0
5475
117.2
6.835
7.05
Изопрен
1
0
0
2
1
1
0
0
0
5069
99.15
7.150
7.25
Этиленгликоль
0
2
0
0
0
0
2
0
0
14140
55.40
15.98
15.7
Фенол
0
0
0
0
5
1
1
0
0
13060
86.57
12.28
12.1
Глицерин
0
2
1
0
0
0
3
0
0
20210
72.81
16.66
16.5
Метанол
1
0
0
0
0
0
1
0
0
7437
42.20
13.27
14.5
Диоксан
0
4
0
0
0
0
0
2
0
8027
85.76
9.675
10.0
нола. Из-за близости их с параметром растворимости
целлюлозы можно предположить, что они должны
быть ее растворителями. Однако на практике может
оказаться, что это не так. Дело в том, что в полярных
веществах существуют различные типы по природе
межмолекулярных взаимодействий: дисперсионные,
полярные и водородные. Их суммарная энергия ха-
рактеризуется термодинамической функцией — сво-
бодной энергией Гиббса ΔG(T) = ΔH(T) - TΔS(T).
Составляющие cлагаемые энтальпия ΔH(T) и энтро-
пия ΔS(T) определяют характер растворения полиме-
ра в растворителе. Если обозначить энергию Гиббса
полимера — ∆GП, растворителя — ∆GР и смеси —
∆GП-Р, то можно записать
∆GР.Р = ∆GП-Р - (∆GП + ∆GР).
Сопоставление результатов расчетов параметра рас-
Процесс растворения самопроизвольный и до-
творимости δ тремя способами с экспериментальными
стигает равновесия при минимуме ∆GР.Р и макси-
данными.
муме энтропии ∆SР.Р. Отсюда вытекают следующие
I — по варианту I, II — по варианту II,
выводы.
А — методом Аскадского [4].
Простой способ оценки параметра растворимости малых молекул и полимерных материалов
61
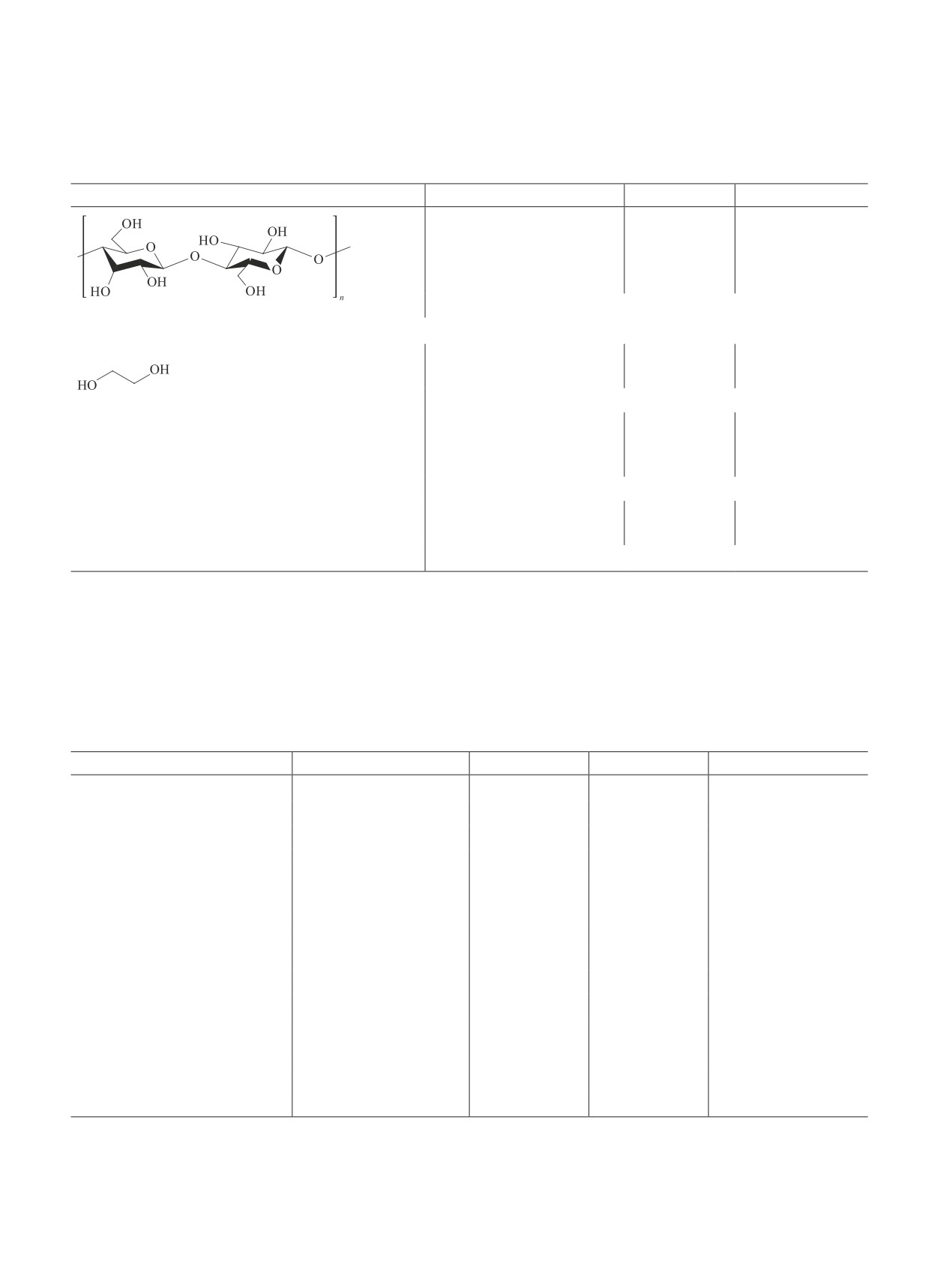
Таблица 5
Результаты расчета параметра растворимости δ целлюлозы и простых молекул
Целлюлоза
Структурная единица
Код
Количество
OH
ОН
6
—O—
СОС
4
CH2
С32
2
CH
С31
10
δI = 15.72, δII = 15.18
Простые молекулы
Этиленгликоль
OH
OH
2
CH2
C32
2
δI = 16.10, δII = 15.82
Глицерин
OH
OH
3
HOCH2—CHOH—CH2OH
CH2
C32
2
CH
С31
1
δI = 16.72, δII = 16.54
Метанол
OH
OH
1
CH3OH
CH3
C33
1
δI = 14.1, δII = 13.83
Таблица 6
Сопоставление результатов расчета параметра растворимости δ по вариантам I и II с литературными данными
для некоторых простых соединений и неполярных полимеров*
Соединение
По методу Аскадского [4]
По варианту I
По варианту II
По эксперименту** [4]
н-Тетрадекан
7.8
7.97
7.72
7.95
Этилбензол
7.7
8.8
8.8
8.8
Изопропилбензол
8.4
8.6
8.3
8.86
Циклогексанол
10.95
11.3
10.6
11.4
н-Пропанол
11.9
12.3
11.5
11.9
Изопропиловый спирт
10.9
11.5
10.6
10.7
н-Валериановая кислота
10.1
9.96
10.69
10.8; 10.69
Полиэтилен
7.9
8.44
8.0
—
Полистирол
9.1
9.6
9.1
8.6-9.1
Полиизобутилен
7.9
7.2
6.9
7.8-8.05
Полифенилен
9.8
10.2
10.6
—
Изопреновый каучук
—
8.53
8.59
8.25
Бутадиеновый каучук
—
8.76
8.51
8.1
Полипропилен
10.7
7.9
6.9
8.2
* Cоединения, которые не вошли в перечень тестовых при построении методов.
** Кондратов А. П., Журавлева Г. Н. Физика и химия материалов и технологических процессов. М.: МГУП имени
Ивана Федорова, 2016. C. 11-13.
62
Гюльмалиев А. М. и др.
— Так как при разрушении кристаллической
параметра растворимости смеси растворителей, что
структуры энтропия возрастает, то для одного и
будет предметом следующего сообщения.
того же полимера в его аморфном состоянии вели-
чина ∆GР.Р будет меньше, чем в кристаллическом.
Финансирование работы
Поскольку энтропия является мерой беспорядка, при
Исследование выполнено на базе Института
растворении энтропия системы полимер-раствори-
нефтехимического синтеза РАН за счет гранта
тель ∆SР.Р возрастает, следовательно, растворитель
Российского научного фонда (проект № 17-73-30046).
аморфной структуры может и не являться раство-
рителем кристаллической структуры. По-видимому,
этим обусловлена нерастворимость целлюлозы при
Конфликт интересов
близких значениях параметра растворимости.
Авторы заявляют об отсутствии конфликта инте-
— Вклад различных типов взаимодействий в эн-
ресов, требующего раскрытия в данной статье.
тальпию системы разный, поэтому превалирование
одних типов взаимодействий может существенно вли-
Информация о вкладе авторов
ять на энтальпию системы и изменить тепловой эф-
фект процесса растворения, а также температурную
А. М. Гюльмалиев разработал методы I и II,
область растворения, которая в методе Гильдебранда
алгоритмы расчета параметра растворимости;
учитывается неявно.
Л. А. Зекель собрал исходные данные для тестовых
В методе Гильдебранда параметр δ характеризует
молекул и полимерных материалов; А. У. Дандаев вы-
суммарное взаимодействие, поэтому из равенства
полнял практические расчеты методом II; А. Е. Батов
параметров растворимости полимера и растворителя
провел сравнительный анализ результатов расчета по
нельзя сделать прогноз о растворимости полимера.
рассмотренным методам; М. Х. Кадиева выполнила
Отметим, что в методе Аскадского энергии этих ти-
практические расчеты методом I; Э. Э. Магомадов
пов взаимодействий в расчетную схему вводятся с
разработал компьютерную программу для расчета на
помощью различных инкрементов [4].
алгоритмическом языке Basic; Х. М. Кадиев руково-
Проведем оценку возможности переноса полу-
дил постановкой задачи, выбором объекта исследова-
ченных значений коэффициентов на произвольные
ния и обсуждения результатов исследования.
соединения. В табл. 6 приведены расчетные значения
параметра δ для некоторых простых молекул и не-
полярных полимеров, которые не вошли в перечень
Информация об авторах
тестовых соединений при построении расчетных
Агаджан Мирза-оглы Гюльмалиев, д.х.н.,
методов. Сопоставление этих результатов с данными
метода Аскадского и эксперимента показывает их
Зекель Леонид Абрамович, к.т.н.,
удовлетворительное согласие.
Дандаев Асхаб Умалтович, к.х.н.,
Выводы
Батов Александр Евгеньевич, к.х.н.,
Результаты проведенных исследований показыва-
ют, что предложенные методы для расчета параметра
Кадиева Малкан Хусаиновна, к.х.н.,
растворимости простым способом по точности не
уступают относительно строгому методу Аскадского
Магомадов Эльдар Элиевич, к.х.н.,
и могут быть успешно применены к системам непо-
лярный полимер-неполярный растворитель со значе-
Кадиев Хусаин Магамедович, д.х.н.,
ниями δратворитель ≅ δполимер. Использование структур-
ных единиц удобно тем, что по величине их вклада в
∆E и ∆V можно предварительно прогнозировать моле-
кулярную структуру растворителя. Кроме того, базис
Список литературы
из структурных единиц более удобен для дальнейших
[1] Ла Мантиа Ф. Вторичная переработка полимеров.
исследований с включением в расчетную схему раз-
СПб: Профессия, 2006. С. 87-91.
личных физико-химических показателей соединений
[2] Hildebrand J. H., Prausnitz J. M., Scott R. L. Regular
с целью повышения точности определения парамет-
and Related Solutions. New York: Van Nostrand, 1970.
ра δ. Методы также можно применять для расчета
P. 70-76.
Простой способ оценки параметра растворимости малых молекул и полимерных материалов
63
[3]
Van Krevelen D. W. Properties of polymers. Their
[8] Gyulmaliev A. M., Popova V. P., Romantsova I. I.,
correlation with chemical structure. Their numerical
Krichko A. A. Calculation of thermodynamic function
estimation and prediction from additive group
of coal liquids // Fuel. 1992. V. 71. N 11. P. 1329-
contributions. Amsterdam: Elsevier, 1997. P. 189-227.
[4]
Аскадский А. А., Кондращенко В. И. Компьютерное
[9] Кадиев Х. М., Гюльмалиев А. М., Кубрин Н. А.
материаловедение полимеров. В 3 т. Т. 1. Атомно-
Аддитивный метод расчета термодинамических
молекулярный уровень. М.: Науч. мир, 1999. С. 350-
функций тяжелого сырья // Нефтехимия. 2016.
390.
T. 56. № 6. С. 584-589.
[5]
Hansen C. M. The universality of the solubility
parameter // Ind. Eng. Chem. Product Res. Develop.
[Kadiev Kh. M., Gyulʹmaliev A. M., Kubrin N. A. An
1969. N 8 (1). P. 2-11.
additive method for calculating the thermodynamic
functions of heavy feedstock // Petrol. Chem. 2016.
[6]
Аскадский А. А., Матвеев Ю. И. Химическое строе-
V. 56. N 9. P. 807-813.
ние и физические свойства полимеров. М.: Химия,
1983. С. 190-210.
[10] Алешина А., Глазкова С. В., Луговская Л. А.,
[7]
Гюльмалиев А. М., Головин Г. С., Гладун Т. Г. Теоре-
Подойникова М. В., Фофанов А. Д., Силина Е. В.,
тические основы химии угля. М.: Изд-во МГГУ,
Современные представления о строении целлюло-
2003. С. 321-325.
зы (обзор) // Химия раст. сырья. 2001. № 1. С. 5-36.