Синтез высокодисперсных алюмомагниевых оксидов на основе продукта центробежной термической активации гиббсита
163
Журнал прикладной химии. 2021. Т. 94. Вып. 2
УДК 54.057 + 54.021
СИНТЕЗ ВЫСОКОДИСПЕРСНЫХ АЛЮМОМАГНИЕВЫХ ОКСИДОВ
НА ОСНОВЕ ПРОДУКТА ЦЕНТРОБЕЖНОЙ ТЕРМИЧЕСКОЙ АКТИВАЦИИ
ГИББСИТА
© А. В. Жужгов, В. Ю. Кругляков, Е. А. Супрун, Р. С. Проценко, Л. А. Исупова
Институт катализа им. Г. К. Борескова СО РАН,
630090, г. Новосибирск, пр. Академика Лаврентьева, д. 5
E-mail: faleks2010@gmail.com
Поступила в Редакцию 4 августа 2020 г.
После доработки 28 октября 2020 г.
Принята к публикации 6 ноября 2020 г.
С использованием методов рентгеновского, термического, микроскопического, адсорбционного и хи-
мического анализа изучена возможность получения алюмината магния при взаимодействии продукта
центробежной термической активации гиббсита и насыщенного водного раствора нитрата магния
при комнатной температуре и 150°С. Показано, что взаимодействие при 150°С реагентов, взятых в
стехиометрическом соотношении по катионам, приводит к образованию фазы слоистого двойного
гидроксида состава MgAl2(OH)1.85(NO3)0.88·0.13H2O, термообработка которого при температуре
550°C обеспечивает формирование стехиометрической шпинели MgAl2O4 с удельной поверхностью
~150 м2·г-1. Традиционная пропитка продукта центробежной термической активации гиббсита
по влагоемкости концентрированным раствором нитрата магния при комнатной температуре и
последующая термообработка при 550°С приводит к образованию твердого раствора на основе
низкотемпературной формы γ-Al2O3 с удельной площадью поверхности ~180 м2·г-1, содержащего
~4.55 мас% магния. Полученные образцы различаются морфологией частиц и содержанием магния на
поверхности. По сравнению с традиционным методом соосаждения способ позволяет существенно
сократить количество исходных реагентов, технологических стадий, а также минимизировать или
полностью исключить образование сточных вод.
Ключевые слова: продукт центробежной термической активации гиббсита; алюминат магния;
синтез
DOI: 10.31857/S0044461821020043
Катализаторы и носители на основе алюминатов
приготовления алюмомагниевых шпинелей, осно-
щелочноземельных металлов, в частности, таких как
ванный на способе высокотемпературного прокали-
алюминаты магния (MgAl2O4) со структурой шпи-
вания механических смесей оксидов и (или) гидрок-
нели, представляют значительный практический ин-
сидов соответствующих металлов при температурах
терес благодаря нейтральным кислотно-основным
1100-1300°С и выше в окислительной либо инертной
характеристикам поверхности и очень высокой тер-
атмосфере [8-10], энергозатратен и не позволяет го-
мической стабильности, что важно при разработке
товить высокодисперсные порошки.
новых и усовершенствовании существующих ката-
Распространенным способом приготовления алю-
лизаторов для процессов гидрирования/дегидриро-
минатов магния является метод совместного осаж-
вания, а также катализаторов высокотемпературных
дения (золь-гель технология) гидроксокомплексов
окислительных процессов [1-7]. Алюминаты находят
Al3+ и Mg2+ из смешанных водных растворов солей
также широкое применение в качестве огнеупоров,
различной природы [1, 2, 4-6, 9-11]. Образующиеся
структурированной керамики, обладают повышен-
осадки после соосаждения в виде гелей декантируют,
ной механической прочностью, термической и хи-
фильтруют, промывают от примесей анионов, сушат
мической устойчивостью [1-3]. Традиционный метод
в интервале температур 80-110°C и прокаливают
164
Жужгов А. В. и др.
при температурах 500-600°C и выше, в результате
гидрохимическая обработка продуктов механической
чего формируются алюминаты магния со структурой
активации смеси гидроксидов магния и алюминия
шпинели. В литературе существует многообразие
в воде при 20-95°С в течение 0.25-2 ч приводит к
вариантов приготовления Mg-алюминиевых систем
образованию слоистого двойного гидроксида маг-
с применением золь-гель технологии путем варьи-
ния и алюминия состава [MgxAl(1-x)(OH)2](OH)(1-x),
рования времени и температуры старения осадков,
дальнейшее термическое разложение которого при
соотношения катионов магния и алюминия, использо-
температуре не ниже 800°C позволяет получать алю-
вания стадии отмывки или ее исключения, изменения
минат магния при более низкой температуре синтеза
порядка и скорости приливания одного раствора к
по сравнению с термическим разложением механи-
другому и т. д. Преимуществом метода соосаждения
чески активированной смеси, что обеспечивает более
(и в целом осаждения), например, перед способом вы-
высокую удельную поверхность оксида.
сокотемпературного спекания оксидно-гидроксидных
В работах [18, 19] подробно исследованы про-
смесей является более низкая температура образова-
цессы «старения» механически активированного
ния алюминатов магния. Однако метод осаждения
гиббсита в водных растворах азотнокислых солей
характеризуется многостадийностью и использова-
M2+(NO3)2 (где M2+ — Zn, Cu, Ni, Co) при комнатной
нием большого количества растворов солей, кислот
температуре и в условиях автоклавной обработки.
или щелочей. Соосажденные гели содержат примеси
Показано, что «старение» гиббсита при комнатной
анионов (нитратов, сульфатов, хлоридов, карбонатов
температуре не обеспечивает формирования сложных
и т. д.), которые могут быть удалены только с исполь-
соединений алюминия с соответствующим катионом.
зованием большого объема промывных вод.
Образование слоистых двойных гидроксидов наблю-
Часто для модифицирования кислотно-основных
дается только при использовании механохимически
свойств поверхности оксида алюминия использу-
активированных образцов гиббсита в условиях авто-
ется метод пропитки растворами различных солей
клава при температуре 150°C в течение 48 ч.
магния (нитратов, хлоридов, карбонатов, а также
Механохимическая активация исходных реагентов
органических растворов этих солей) по влагоемко-
перед спеканием позволяет снизить температуру про-
сти предварительно подготовленных носителей или
каливания по сравнению с керамическим методом,
их предшественников — гидроксидов алюминия.
а также исключить стадию осаждения и образова-
После термообработки при температурах выше 600-
ния сточных вод, что характерно для метода осажде-
800°C это приводит к образованию магнийсодержа-
ния. Вместе с тем механохимический метод требует
щих шпинелеподобных структур («протошпинелей»)
специального оборудования и широкого распростра-
[7, 12, 13]. Недостатком метода пропитки по влагоем-
нения для получения материалов на промышленном
кости является ограничение по вводимой концентра-
уровне не получил.
ции катионов Mg2+, связанное с ограниченным вла-
Помимо механохимической активации порошка
гопоглощением носителя и пределом растворимости
гиббсита среди известных способов, получивших
соли в пропиточном растворе.
наиболее широкое практическое применение в про-
В литературе описаны подходы к получению би-
изводстве носителей, катализаторов и осушителей,
нарных Al-Mg-соединений, основанные на физиче-
получил метод термоактивации. Разновидностями
ских методах интенсификации процессов. Например,
метода, в частности, являются методы термохимиче-
в работах [14-16] описаны способы получения алю-
ской активации [20, 21] и центробежной термоакти-
мината магния с микрометровым размером частиц
вации, разработанные в ИК СО РАН [22]. Продукты
обработкой в автоклаве при температурах 350-450°С
термоактивации гиббсита по сравнению с исходным
смеси гидроксида алюминия и оксида магния в при-
гиббситом характеризуются повышенной химической
сутствии добавок или соосажденных гидроксидов.
активностью по отношению к электролитам — более
Полученный хорошо окристаллизованный алюминат
высокими степенями растворения в кислотах и ще-
магния перспективен для использования в качестве
лочах [22, 23]. Благодаря этим свойствам продукты
сырья при синтезе монокристаллов [14].
быстрого нагрева порошка гиббсита могут быть пер-
В работе [17] описан механохимический метод
спективными для получения алюмината магния со
получения порошка однофазного алюмината маг-
структурой шпинели. Можно было ожидать, что при
ния, заключающийся в механохимической обработке
взаимодействии продуктов термоактивации с раство-
смеси гидроксидов магния и алюминия, взятых в сте-
рами солей магния образуются двойные гидроксиды,
хиометрическом соотношении по катионам, и после-
что обеспечит получение алюмомагниевой шпинели
дующем ее прокаливании при 1000°С. Показано, что
в мягких условиях и без осаждения.
Синтез высокодисперсных алюмомагниевых оксидов на основе продукта центробежной термической активации гиббсита
165
Цель работы — изучение возможности получения
ной термической активации гиббсита массой 3 г
алюмината магния при взаимодействии продукта
по каплям прилили насыщенный раствор Mg(NO3)2
центробежной термоактивации гиббсита и раствора
объемом 1.52 мл с содержанием Mg2+ 77 г·л-1, что
Mg(NO3)2 при нормальном и повышенном давлении.
соответствовало расчетному содержанию Mg2+ в ок-
сиде алюминия около 4.5 мас%, или массовому отно-
шению Al3+/Mg2+ = 11.88. Такое содержание магния в
Экспериментальная часть
образце обусловлено, с одной стороны, растворимо-
В качестве исходного сырья для получения про-
стью Mg(NO3)2, а с другой — объемом пор продук-
дукта центробежной термической активации гибб-
та центробежной термической активации гиббсита.
сита марки ИК-02-76 (ТУ 2175-040-03533913-2007)
После стадии пропитки образец сушили при 110°C
использовали гиббсит производства ОАО
в течение 12 ч и затем прокаливали на воздухе при
«Ачинский глиноземный комбинат» марки ГД 000
температуре 550°C в течение 4 ч. Полученный обра-
(ТУ 1711-99-039-2000). Содержание примесей в ис-
зец обозначен как Mg-ЦТА-ГБП/550.
ходном гиббсите (мас%): Fe — 0.002, Na — 0.11,
Рентгенофазовый анализ (РФА) проводили с по-
K — 0.033 и Si — 0.014. Величина удельной площади
мощью дифрактометра D-500 (Siemens) с использова-
поверхности исходного порошка составляла не более
нием CuKα-излучения и графитового монохроматора
1 м2·г-1. Потери при прокаливании при 850°C соста-
на отраженном пучке. Образцы сканировали с шагом
вили 34 мас%. В качестве исходного Mg-содержащего
0.05° в области значений углов 2θ = 10-70° и време-
сырья использовали Mg(NO3)2·6H2O (ч.д.а., ОOО
нем накопления 3 с. Идентификацию фаз осуществля-
«Кемикал Елементс Юкрейн»).
ли путем сравнения экспериментальных дифракто-
Термоактивацию гиббсита проводили в центро-
грамм с дифрактограммами баз данных ICDD и PDF 2.
бежном флаш-реакторе барабанного типа (ЦЕФЛАР)
Термический анализ образцов выполняли на
при температуре теплоэлектронагревателей 540°С,
синхронном термоанализаторе STA 449 С Jupiter
скорости вращения барабана 60 об·мин-1 и расходе
(Netzsch) в интервале температур 20-1200-1400°C
исходного порошка 50 кг·ч-1. Потери при прокали-
со скоростью нагрева 10 град·мин-1 с использованием
вании полученного продукта термоактивации при
навесок 30 мг.
850°C составили 12.5 мас%. После проведения термо-
Морфологию поверхностного слоя образцов ис-
активации порошок подвергали помолу на шаровой
следовали на растровом электронном микроскопе
мельнице в течение 12 ч, что обеспечивало получение
JSM-6460 LV (JEOL) с энергией электронов зонда
порошка со средним размером частиц около 50 мкм.
20-25 кэВ. Микроскоп укомплектован рентгенов-
Для синтеза в гидротермальных условиях бы-
ским энергодисперсионным спектрометром INCA
ла приготовлена суспензия из термоактивирован-
Energy-350 (Oxford Instruments), позволяющим опре-
ного в реакторе ЦЕФЛАР гиббсита и раствора
делять элементный состав образцов в слое глубиной
Mg(NO3)2, так, чтобы соотношение катионов соот-
до 5 мкм.
ветствовало стехиометрическому алюминату магния.
Величину удельной площади поверхности
Суспензию с исходным значением pH около 5.0 под-
(Sуд, м2·г-1) измеряли методом сорбции аргона при
вергали гидротермальной обработке при 150 ± 1°C
77 K и последующей термодесорбции по четы-
(P = 3.5 ± 0.1 атм) в течение 4 ч при перемешивании
рем точкам сорбционного равновесия на приборе
со скоростью 120 об·мин-1. После автоклавной обра-
СОРБИ-М 4.1 (ЗАО «МЕТА») с использованием про-
ботки сформировавшийся гель сушили при 110°C в
граммы soft Sorbi-M Version 4.2. В качестве газа-но-
течение 12 ч до состояния ксерогеля. Последующую
сителя в смеси использовали гелий. Расчет значений
термообработку проводили на воздухе при темпера-
туре 550°C в течение 4 ч. Полученные образцы после
Химический состав образцов определяли методом
сушки при 110°C и прокаливания при 550°C промар-
атомно-эмиссионной спектроскопии с индуктивно
кированы как Mg-ЦТА-ГБ/110 и Mg-ЦТА-ГБ/550
связанной плазмой на приборе OPTIMA 4300 DV
соответственно.
(Perkin Elmer).
Для сравнения приготовлен образец с исполь-
зованием традиционного метода однократной про-
Обсуждение результатов
питки по влагоемкости продукта центробежной тер-
мической активации гиббсита водным раствором
Согласно результатам рентгенофазового ана-
Mg(NO3)2. Влагоемкость этого продукта составила
лиза, исходный гиббсит хорошо окристаллизован
около 0.45 мл·г-1. К порошку продукта центробеж-
(рис. 1, а), наличие каких-либо других фазовых вклю-
166
Жужгов А. В. и др.
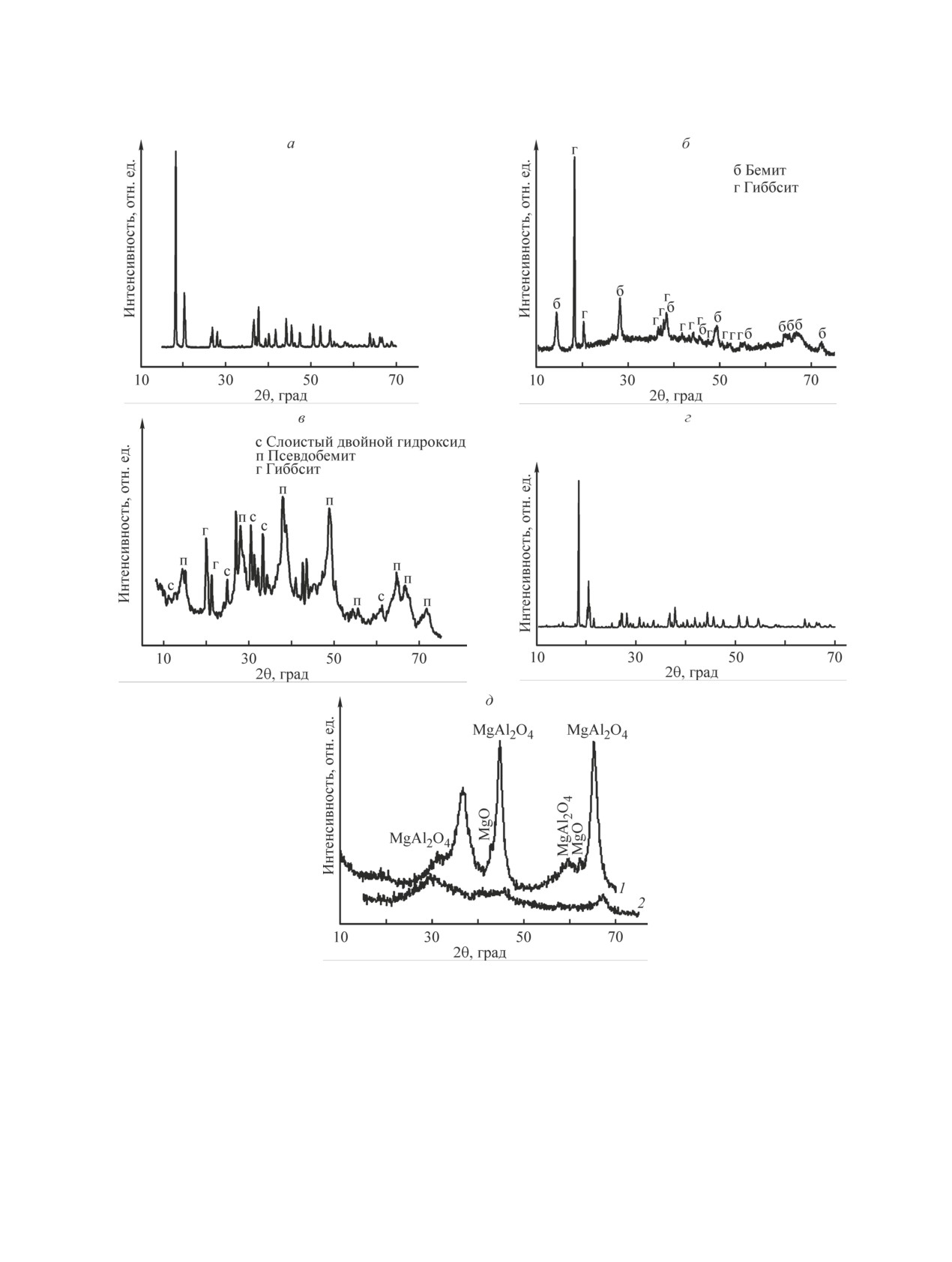
Рис. 1. Дифрактограммы исходного гиббсита (а); продукта центробежной термической активации гиббсита (б); про-
дукта центробежной термической активации гиббсита после его гидротермальной обработки в растворе Mg(NO3)2
и сушки при 110°С (в); исходного гиббсита после его гидротермальной обработки в растворе Mg(NO3)2 и сушки
при 110°C (г); продукта центробежной термической активации гиббсита после его гидротермальной обработки
в растворе Mg(NO3)2, сушки при 110°С и прокаливания при 550°С (1) и продукта центробежной термической
активации гиббсита после пропитки по влагоемкости раствором Mg(NO3)2, сушки при 110°С и термообработки
при 550°С (2) (д).
чений в нем не обнаружено. На дифрактограмме про-
свидетельствующее о наличии рентгеноаморфного
дукта центробежной термической активации наблю-
продукта, рефлексы от кристаллического бемита
даются размытое «гало» в области углов 2θ = 20-40°,
(γ-AlOOH), образующегося в процессе термоакти-
Синтез высокодисперсных алюмомагниевых оксидов на основе продукта центробежной термической активации гиббсита
167
вации в крупных частицах гиббсита, а также пики
представляет собой твердый раствор на базе низ-
исходного недоразложившегося гиббсита (рис. 1, б).
котемпературной формы оксида алюминия, о чем
Рентгеновская порошковая дифрактограмма про-
свидетельствует увеличенный (a = 7.970 Å) относи-
дукта гидротермальной обработки термоактивирован-
тельно γ-Al2O3 (a = 7.915 Å, PDF № 47-1308) пара-
ного гиббсита в растворе Mg(NO3)2 и последующей
метр решетки. Увеличение параметра связано с тем,
сушки полученного геля на воздухе при 110°C в
что размер катиона магния больше размера катиона
течение 12 ч (образец Mg-ЦТА-ГБ/110) содержит
алюминия. Величина изменения зависит не только
рефлексы, характерные для псевдобемита и слоистого
от содержания магния в твердом растворе, но и от
двойного гидроксида магния (см. таблицу, рис. 1, в).
способа его введения, что может быть обусловлено
Сохраняются рефлексы от исходного гиббсита, не
неоднородностью распределения магния в некото-
участвующего в процессе взаимодействия при ука-
рых случаях [24, 25]. Определенное нами значение
занных условиях гидротермальной обработки. Это
параметра для твердого раствора, содержащего ~5%
обусловлено тем, что исходный гиббсит, как отмечено
магния, согласуется с описанным в литературе значе-
выше, инертен в химическом отношении, что под-
нием для однородного раствора на основе γ-Al2O3 с
тверждается как литературными данными [18-23],
близким содержанием магния [24].
так и проведенным нами экспериментом. Так, после
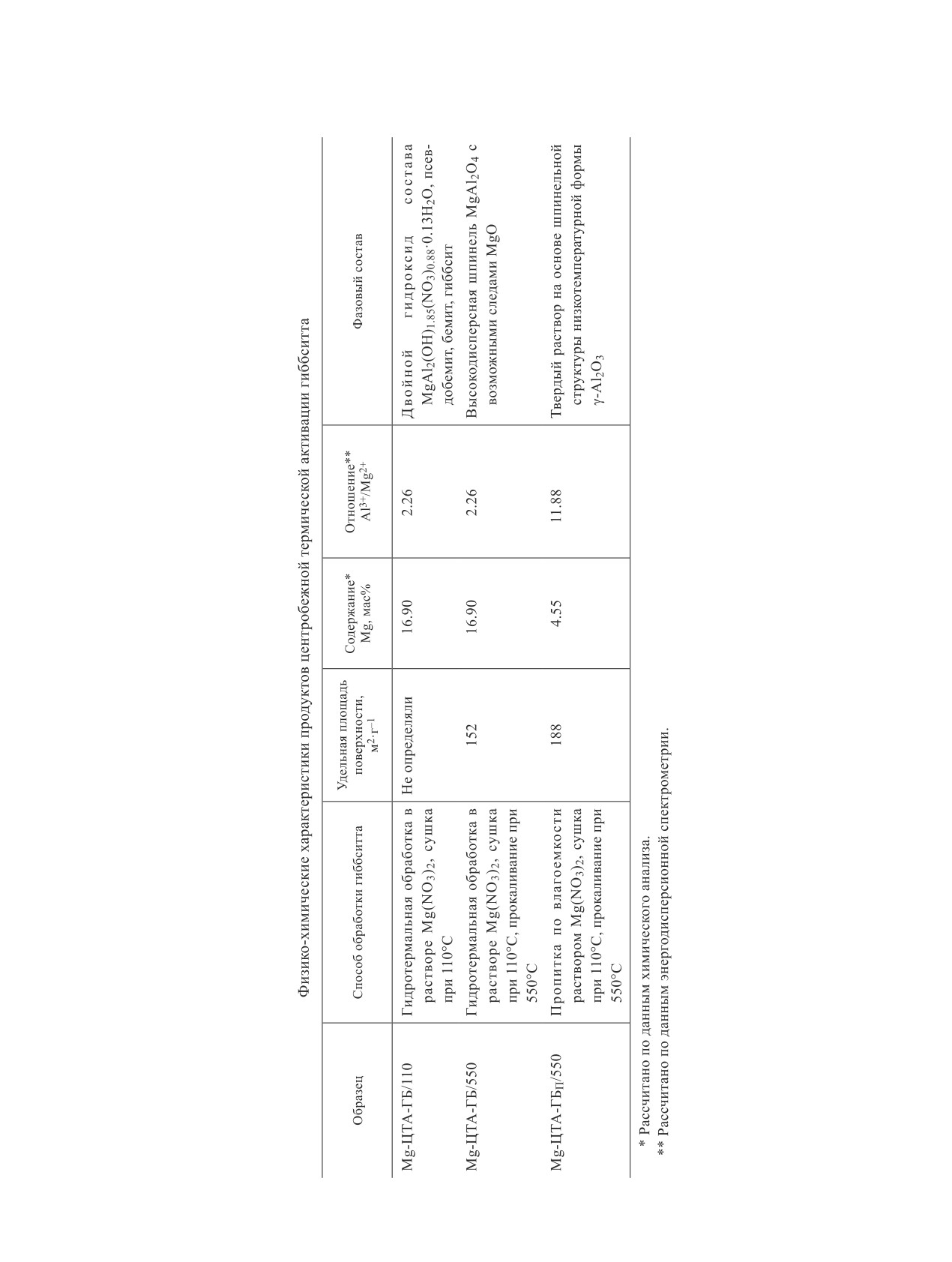
Термический анализ исходного гиббсита выявил
автоклавной обработки исходного гиббсита в водном
следующие эндотермические эффекты: эндотермиче-
растворе Mg(NO3)2 при 150°С в течение 4 ч дифрак-
кий эффект с минимумом при 97°C, обусловленный
ционная картина этого образца (рис. 1, г) практически
удалением слабосвязанной молекулярной воды; два
полностью идентична спектру исходного гиббсита
эндотермических эффекта с минимумами при 238 и
(рис. 1, а). Не исключено, что в продукте взаимодей-
256°C, свидетельствующие о начальной стадии разло-
ствия помимо примесной фазы гиббсита сохраняется
жения кристаллитов гиббсита пластинчатой формы с
и примесь фазы бемита, выявить которую сложно
образованием бемита; основной эндотермический эф-
из-за близости рефлексов фаз псевдобемита и бемита.
фект дегидратации фазы гиббсита (с минимумом при
Рентгеновская порошковая дифрактограмма про-
314°C) и эндотермический эффект разложения фазы
каленного продукта гидротермального взаимодей-
бемита с минимумом при 536°C (рис. 2, а). При на-
ствия (Mg-ЦТА-ГБ/550) (рис. 1, д, спектр 1) содержит
греве продукта центробежной термической активации
характерные дифракционные пики, соответствую-
гиббсита (рис. 2, б) появляется эндотермический эф-
щие алюминату магния MgAl2O4 с параметром ре-
фект с минимумом при 103°C, обусловленный удале-
шетки a = 8.093 Å, что несколько больше таблич-
нием молекулярной воды из рентгеноаморфной алю-
ного значения для высокотемпературного MgAl2O4
мооксидной составляющей продукта термоактивации.
(a = 8.080 Å, PDF № 21-1152). Увеличение отно-
Сохраняются эндотермический эффект с минимумом
сительно табличного значения параметра решетки
при 267°C, обусловленный дегидратацией остаточ-
может свидетельствовать, например, о возможном
ной фазы гиббсита до χ-Al2O3, и эндотермический
анионном модифицировании полученной нами низ-
тепловой эффект с минимумом при 495°C, связан-
котемпературной шпинели. Оценка среднего размера
ный с разложением бемита до γ-Al2O3. Присутствие
кристаллитов из данных рентгеновского анализа дает
гиббсита и бемита в продукте центробежной терми-
величину ~7 нм. Помимо пиков, соответствующих
ческой активации гиббсита показано выше методом
алюминату магния, на дифрактограмме наблюдаются
РФА (рис.1, б). Наличие экзотермического теплово-
малоинтенсивные пики, скорее всего присущие фазе
го эффекта с максимумом при 826°C может свиде-
MgO (см. таблицу, рис. 1, д, спектр 1). Нельзя исклю-
тельствовать о кристаллизации рентгеноаморфной
чить возможное присутствие в образце фазы оксида
фазы в низкотемпературные формы Al2O3 [20, 23].
алюминия, выявить которую в спектре на фоне алю-
Термограмма продукта гидротермального взаи-
мината магния не удается из-за перекрывания основ-
модействия после термообработки при 110°С (об-
ных пиков, поскольку примесь гиббсита в продукте
разец Mg-ЦТА-ГБ/110) существенно отличается от
центробежной термической активации гиббсита не
термограммы продукта центробежной термической
вступает во взаимодействие, и на рентгенограмме
активации гиббсита наличием эффектов, обуслов-
присутствуют пики оксида магния.
ленных разложением слоистых двойных гидроксидов
Образец, полученный пропиткой по влагоемко-
(рис. 2, в). При термическом анализе слоистого двой-
сти продукта центробежной термической активации
ного гидроксида, получаемого методом совместного
гиббсита раствором Mg(NO3)2 (Mg-ЦТА-ГБП/550),
осаждения Al3+ и Mg2+, на термограммах можно вы-
по данным РФА (см. таблицу, рис. 1, д, спектр 2)
делить три области потери веса [1, 2, 6]: низкотемпе-
Синтез высокодисперсных алюмомагниевых оксидов на основе продукта центробежной термической активации гиббсита
169
Рис. 2. Данные синхронного термического анализа.
а — исходный кристаллический гиббсит, б — продукт центробежной термической активации гиббсита, в — высушен-
ный при 110°С продукт гидротермальной обработки суспензии термоактивированного гиббсита в растворе Mg(NO3)2
(Mg-ЦТА-ГБ/110).
ратурная область (до 150°С) соответствует удалению
гидроксилирования бруситоподобных слоев и удале-
физически адсорбированной воды, в интервале тем-
нию межслоевых анионов NO3-; широкий размытый
ператур 200-300°С происходит удаление межслоевой
экзотермический эффект в области 500-600°С соот-
воды, а высокотемпературную область 350-500°С от-
ветствует кристаллизации фазы шпинели. Это согла-
носят к дегидроксилированию бруситоподобных сло-
суется с данными рентгенофазового анализа, так как
ев и удалению межслоевых анионов (A)n-. В нашем
после прокаливания высушенного продукта гидро-
случае термограмма высушенного продукта гидротер-
термальной обработки (Mg-ЦТА-ГБ/110) при 550°C
мальной обработки (Mg-ЦТА-ГБ/110) характеризует-
образуется алюминат магния (рис. 1, д, спектр 1).
ся набором следующих тепловых эффектов: в области
Согласно результатам микроскопического ана-
температур 45-103°C происходит удаление слабосвя-
лиза, образец Mg-ЦТА-ГБП/550, полученный про-
занной воды; эндотермический эффект с миниму-
питкой по влагоемкости продукта центробежной
мом при 166°C связан с началом процесса удаления
термической активации гиббсита водным раство-
межслоевой воды из структуры слоистого двойного
ром Mg(NO3)2 и прокаленный при 550°С, состоит
гидроксида; эндотермический эффект с минимумом
из кубических частиц преимущественным разме-
при 271°C обусловлен дегидратацией примесной
ром 30-40 мкм, кроме того, присутствуют и частицы
фазы гиббсита, присутствующей в продукте термо-
размерами 10-15 мкм (рис. 3, а). Напротив, обра-
активации до его гидротермальной обработки в рас-
зец Mg-ЦТА-ГБ/550, полученный автоклавной об-
творе Mg(NO3)2 (рис. 2, в); эндотермический эффект
работкой этих исходных реагентов и прокаленный
с минимумом при 377°C соответствует процессу де-
при 550°С, в основном состоит из частиц размерами
170
Жужгов А. В. и др.
Рис. 3. Электронно-микроскопические изображения образцов Mg-ЦТА-ГБП/550 (а, в, д) и Mg-ЦТА-ГБ/550 (б, г, е).
10-15 мкм с встречающимися в незначительном ко-
частицы исходного гиббсита (рис. 3, в, д), то образец
личестве частицами размером 30-40 мкм (рис. 3, б).
Mg-ЦТА-ГБ/550 образован вытянутыми иглоподоб-
Приготовленные образцы различаются также мор-
ными частицами (рис. 3, г, е), что более характерно
фологией поверхности частиц (рис. 3, в-е). Так, если
для шпинели, получаемой из двойных гидроксидов
Mg-ЦТА-ГБП/550 больше напоминает по морфологии
[1, 2, 8].
Синтез высокодисперсных алюмомагниевых оксидов на основе продукта центробежной термической активации гиббсита
171
Близкие размеры кристаллитов, определенные из
Выводы
данных об уширении линий рентгеновской дифрак-
Гидротермальная обработка продукта центро-
ции (~7 нм) и данных о величине удельной площади
бежной термической активации гиббсита в рас-
поверхности образцов (~9-10 нм), позволяют рассма-
творе нитрата магния при 150°С приводит к об-
тривать их как монокристаллические. Поскольку раз-
разованию слоистого двойного гидроксида,
мер частиц, определенный из данных микроскопии,
который может быть представлен составом
намного превышает размер таких монокристаллитов,
MgAl2(OH)1.85(NO3)0.88·0.13H2O. Термообработка
можно сделать вывод, что частицы состоят из кри-
полученного слоистого двойного гидроксида при тем-
сталлитов и содержат открытые поры.
пературе 550°C обеспечивает формирование высоко-
Анализ результатов элементного соста-
дисперсной шпинели MgAl2O4 с удельной поверх-
ва различных участков поверхности образцов
ностью ~150 м2·г-1. Вычисленный параметр ячейки
Mg-ЦТА-ГБП/550 и Mg-ЦТА-ГБ/550, полученных
a = 8.093 Å несколько превышает значение для вы-
методом энергодисперсионной рентгеновской спек-
сокотемпературной шпинели MgAl2O4 (a = 8.080 Å).
троскопии при энергии электронов зонда до 25 кэВ,
Взаимодействие гиббсита с раствором соли магния в
что соответствует толщине анализируемого слоя до
данных условиях не происходит.
5 мкм, показал, что среднее массовое отношение ка-
Пропитка продукта центробежной термической
тионов Al/Mg в образце Mg-ЦТА-ГБП/550 составляет
активации гиббсита по влагоемкости водным раство-
около 11, а в образце Mg-ЦТА-ГБ/550 — 2.26 (см.
ром Mg(NO3)2 при температуре окружающей среды с
таблицу). Это соответствует массовому отношению
последующей термообработкой при 550°C не приво-
этих металлов по условиям приготовления и также
дит к образованию MgAl2O4. Наблюдается образова-
может свидетельствовать о равномерном распределе-
ние твердого раствора на основе низкотемпературной
нии магния по глубине частиц в обоих образцах. По
формы Al2O3 с содержанием магния 4.55 мас%, пара-
данным химического анализа содержание магния в
метром ячейки a = 7.970 Å и удельной поверхностью
образцах Mg-ЦТА-ГБП/550 и Mg-ЦТА-ГБ/550 состав-
~180 м2·г-1.
ляет 4.55 и 16.90 мас% (см. таблицу) соответственно,
Полученные образцы различаются морфологией
что согласуется с данными, полученными методом
частиц и содержанием магния на поверхности, что
энергодисперсионной рентгеновской спектроскопии,
представляет интерес для различных приложений.
а также с рассчитанным при приготовлении содержа-
Если частицы твердого раствора сохраняют размеры
нием этих элементов.
и форму частиц продукта центробежной термической
Слоистая структура двойных гидроксидов сфор-
активации гиббсита и, следовательно, гиббсита, то
мирована из бруситоподобных пакетов, состоящих
частицы шпинели образованы кристаллитами, форма
из двух слоев плотноупакованных OH-групп, между
которых соответствует двойным гидроксидам. Данные
которыми расположен слой катионов Al3+ и Mg2+.
свидетельствуют о пористом характере этих частиц.
Общая формула слоистого двойного гидроксида
Проведенные исследования демонстрируют ши-
может быть представлена следующей формулой
рокие возможности получения смешанных оксидов
[1, 2]:
различного состава и морфологии в зависимости от
[M2+M3+(OH)2]q+(A)n-·mH2O,
условий взаимодействия продуктов термоактивации
гиббсита и растворов солей, что представляет инте-
где M2+ — катионы двухвалентных металлов Co2+,
рес для приготовления Mg-содержащих носителей
Ni2+, Zn2+, Mg2+ и т. д.; M3+ — катионы трехвалент-
и катализаторов с необходимыми свойствами. По
ных металлов Al3+, Cr3+, Fe3+. Положительный заряд
сравнению с традиционным методом соосаждения
пакетов компенсируется слоем отрицательно заряжен-
это позволяет существенно сократить количество ис-
ных частиц (A)n-, например, OH-, NO3-, CO32-, SO42-
ходных реагентов, технологических стадий, а также
и т. д. На основании данных термического анализа, а
минимизировать или полностью исключить образо-
также фазового анализа и электронной микроскопии,
вание промывных вод.
сформированный на стадии гидротермальной обра-
ботки при синтезе Mg-ЦТА-ГБ/550 слоистый двойной
гидроксид алюминия и магния может быть пред-
Финансирование работы
ставлен составом MgAl2(OH)1.85(NO3)0.88·0.13H2O.
Отметим, что содержание NO3- рассчитано из общего
Работа выполнена в рамках государственно-
количества растворенного Mg(NO3)2, используемого
го задания Института катализа СО РАН, проект
для приготовления водного раствора.
АААА-А21-121011490008-3.
172
Жужгов А. В. и др.
Конфликт интересов
[5]
Панкина Г. В., Чернавский П. А., Лунин В. В. Би-
металлические катализаторы Co-Fe/носитель:
Авторы заявляют об отсутствии конфликта инте-
динамика гидрирования CO // ЖФХ. 2013. Т. 87.
ресов, требующего раскрытия в данной статье.
№ 10. С. 1647-1652.
[Pankina G. B., Chernavsky P. А., Lunin V. V.
Информация о вкладе авторов
Dynamics of hydrogenation for bimetallic Co-Fe/
Carrier catalysts // Russ. J. Phys. Chem. A. 2013.
А. В. Жужгов и В. Ю. Кругляков разработали ме-
V. 87. N 10. P. 1622-1626.
тодику эксперимента, участвовали в приготовлении
образцов, анализе полученных результатов и подго-
[6]
Бельская О. Б., Степанова Л. Н., Гуляева Т. И.,
товке текста статьи; Е. А. Супрун выполнил элек-
Голинский Д. В., Белый А. С., Лихолобов В. А.
тронно-микроскопическое исследование образцов;
Исследование катализаторов Pt/MgAlOx в реакции
Р. С. Проценко участвовал в проведении экспери-
дегидрирования н-декана // Кинетика и катализ.
ментов по гидротермальному синтезу; Л. А. Исупова
2015. Т. 56. № 5. С. 663-671.
сформулировала цель работы и заключение, участво-
вала в подготовке окончательного варианта статьи.
[Belskaya O. B., Stepanova L. N., Gulyaeva T. I.,
Golinskii D. V., Belyi A. S., Likholobov V. A. Study of
Pt/MgAlOx catalysts in n-decane dehydrogenation //
Информация об авторах
Kinet. Catal. 2015. V. 56. N 5. P. 655-662.
Жужгов Алексей Викторович, к.х.н.,
[7]
Sadykov V. A, Chub O. V., Chesalov Yu. A.,
Mezentseva N. V., Pavlova S. N., Arapova M. V.,
Кругляков Василий Юрьевич, к.т.н.,
Rogov V. A., Simonov M. N., Roger A. C.,
Parhomenko K. V., Veen A. C. V. Mechanism of ethanol
Супрун Евгений Александрович, к.х.н.,
steam reforming over Pt/(Ni + Ru)-promoted oxides
by FTIRS in situ // Top. Catal. 2016. V. 59. P. 1332-
Проценко Роман Станиславович,
[8]
Иванова А. С., Скрипченко Е. В., Мороз Э. М., Лит-
вак Г. С., Кустова Г. Н., Криворучко О. П. Исследо-
Исупова Любовь Александровна, д.х.н.,
вание твердофазных превращений при термообра-
ботке индивидуальных и смешанных гидроксидов
магния и алюминия // Изв. СО АН СССР. 1989.
Т. 6. № 6. С. 116-122.
Список литературы
[9]
Thesis F. L., Ayoko G. A., Frost R. L. Synthesis of
[1] Evans D. G., Slade R. C. T. Structural aspects of layered
layered double hydroxides containing Mg2+, Zn2+,
double hydroxides // Struct. Bond. 2006. V. 119.
Ca2+ and Al3+ layer cations by co-precipitation
methods — A review // Appl. Surf. Sci. 2018. V. 134.
[2] Li F., Duan X. Applications of layered double
P. 1481-1492.
hydroxides // Struct. Bond. 2006. V. 119. P. 193-223.
[10]
Othman M. R., Helwani Z., Martunus F.,
[3] Gareth R., OʹHare W., OʹHare D. Towards
Fernando W. J. N. Synthetic hydrotalcites from
understanding, control and application of layered
different routes and their application as catalysts and
double hydroxide chemistry // J. Mater. Chem. 2006.
gas adsorbents: A review // App. Organometal. Chem.
2009. V. 23. P. 335-346.
[4] Боканегра С. А., Гуэото-Руи А., Селза О. А., де
Мигуэль С. Р. Шпинель MgAl2O4, приготовленная
[11]
Криворучко О. П., Буянов Р. А., Парамзин С. М.,
методом механохимического синтеза, как носи-
Золотовский Б. П. Взаимодействие механохими-
тель полиметаллических катализаторов дегидри-
чески активированных гидроксидов Al3+ с кри-
рования парафинов // Катализ в пром-сти. 2012.
сталлическими оксидами двухвалентного металла
№ 5. С. 63-74 [Bocanegra S. A., Guerrero-Ruiz А.,
// Кинетика и катализ. 1988. Т. 29. № 1. С. 252-253
Scelza O. A., de Miguel С. Р. MgAl2O4 spinel prepared
[Krivoruchko O. P., Buyanov R. A., Paramsin S. M.,
by mechanochemical synthesis used as a support of
multimetallic catalysts for paraffin dehydrogenation //
Catal. Ind. 2013. N 5. P. 61-73.
P. 223-224].
Синтез высокодисперсных алюмомагниевых оксидов на основе продукта центробежной термической активации гиббсита
173
[12]
Koo K. Y., Roh H. S., Seo Y. T., Seo D. J., Yoon W. L.,
[21]
Буянов Р. А., Криворучко О. П., Золотовский Б. П.
Park S. B. Coke study on MgO-promoted Ni/Al2O3
О природе термохимической активации кристал-
catalyst in combined H2O and CO2 reforming of
лических гидроксидов // Изв. СО АН СССР. Сер.
methane for gas to liquid (GTL) process // Appl. Catal.
хим. наук. 1986. № 11. Вып. 4. С. 39-44.
A: General. 2008. V. 340. P. 183-190.
[22]
Танашев Ю. Ю., Мороз Э. М., Исупова Л. А.,
Иванова А. С., Литвак Г. С., Амосов Ю. И., Руди-
[13]
Arbag H. Effect of impregnation sequence of Mg on
на Н. А., Шмаков А. Н., Степанов А. Г., Хари-
performance of mesoporous alumina supported Ni
на И. В., Кулько Е. В., Данилевич В. В., Бала-
catalyst in dry reforming of methane // Appl. Catal. A:
шев В. А., Кругляков В. Ю., Золотарский И. А.,
Int. J. Hydrogen Energy. 2018. V. 43. P. 6561-6574.
Пармон В. Н. Получение оксидов алюминия на
основе продуктов быстрого терморазложения
[14]
Пат. РФ 2630112 (опубл. 2017). Способ получения
гидраргиллита в центробежном флаш-реакто-
мелкокристаллического алюмината магния.
ре. Физико-химические свойства продуктов
[15]
Комлев А. A., Гусаров В. В. Механизм формиро-
центробежной термоактивации гидраргиллита
вания нанокристаллов со структурой шпинели
// Кинетика и катализ. 2007. Т. 48. № 1. С. 161-
в системе MgO-Al2O3-H2O в гидротермальных
170 [Tanashev Yu. Yu., Moroz E. M., Isupova L. A.,
условия // ЖОХ. 2011. Т. 81. Вып. 11. С. 1769-
Ivanova A. S., Litvak G. S., Amosov Yu. I., Rudina N. A.,
1717 [Komlev A. A., Gusarov V. V. Mechanism of
Shmako A. N., Stepanov A. G., Kharina I. V.,
the nanocrystals formation of the spinel structure in
Kulʹko E. V., Danilevich V. V., Balashov V. A.,
the MgO-Al2O3-H2O system under hydrothermal
Kruglyakov V. Yu., Zolotarskii I. A., Parmon V. N
.
conditions // Russ. J. Gen. Chem. 2011. V. 81. N 11.
Synthesis of aluminum oxides from the products of
P. 2222-2230.
the rapid thermal decomposition of hydrargillite in a
centrifugal flash reactor. Physicochemical properties
[16]
Xu Z. P., Lu G. Q. Hydrothermal synthesis of layered
of the products obtained by the centrifugal thermal
hydroxides (LDHs) from mixed MgO and Al2O3: LDH
activation of hydrargillite // Kinet. Catal. 2007. V. 48.
formation mechanism // Chem. Mater. 2005. V. 17.
N 1. P. 153-161.
[17]
Карагедов Г. Р. Механохимически стимулирован-
[23]
Воробьев Ю. К., Шкрабина Р. А., Мороз Э. М.,
ный синтез алюмомагниевой шпинели и ее низ-
Фенелонов В. Б., Заграфская Р. В., Камбарова Т. Д.,
котемпературное спекание в плотную керамику //
Левицкий Э. А. Синтез алюмооксидных сое-
Химия в интересах устойчив. развития. 2020. Т. 28.
динений-носителей и компонентов катализато-
№ 1. C. 10-17.
ров. Физико-химическое исследование продук-
тов термического диспергирования гиббсита //
[Karagedov G. R. Mechanochemically stimulated
Кинетика и катализ. 1981. Т. 22. № 6. С. 1595-
synthesis and low temperature sintering of MgAl2O4
1602 [Vorobev Yu. K., Shkrabina R. A., Moroz E. M.,
// Chem Sus. Dev. 2020. N 1. Р. 8-15.
Fenelonov V. B., Zagrafskaya R. V., Kambarova T. D.,
Levitskii E. A. Synthesis of aluminum-oxides-catalyst
[18]
Williams G. R., Moorhouse S. J., Timothy J. P.,
and constituents-physicochemical study of the
Fogg A. M., Rees N. H., OʹHare D. A. New insights
products of the thermal dispersion of gibbsite // Kinet.
into the intercalation chemistry of Al(OH)3 // Dalton
Catal. 1981. V. 22. N 6. P. 1275-1281].
Trans. 2011. V. 40. P. 6012-6022.
[24]
Arapova M. V., Pavlova S. N., Larina T. V.,
Glazneva T. S., Rogov V. A., Krieger T. A.,
[19]
Fogg A. M., Williams G. R., Chester R., OʹHare D. A.
Sadykov V. A., Smorygo O., Parkhomenko K.,
Novel family of layered double hydroxides —
Roger A.-C. Hydrogen and syngas production via
[MAl4(OH)12](NO3)2·xH2O (M = Co, Ni, Cu, Zn) //
ethanol steam reforming over supported nickelates
J. Mater. Chem. 2004. V. 14. P. 2369-2371.
// Proc. of the Energy and Mater. Res. Conf. (EMRS
2015) / Ed. A. Mendes-Vilas. Boca Raton, USA:
[20]
Ingram-Jones V. J., Davies R. C. T., Southern J. C.,
Brown Walker Press, 2015. P. 131-135.
Salvador S. Dehydroxylation sequences of gibbsite
[25]
Penkova A., Bobadilla L. F., Romero-Sarria F.,
and boehmite: Study of differences between soak
Centeno M. A., Odriozola J. A. Pyridine adsorption on
and flash calcinations and of particle-size effects // J.
NiSn/MgO-Al2O3: An FTIR spectroscopic study of
Mater. Chem. 1996. V. 6. N 1. P. 73-79.
surface acidity //Appl. Surf. Sci. 2014. V. 317. P. 241-