Журнал прикладной химии. 2021. Т. 94. Вып. 2
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ И МАТЕРИАЛЫ НА ИХ ОСНОВЕ
УДК 541.64+541.18
НАНОКОМПОЗИТЫ СЕРЕБРА НА ОСНОВЕ СОПОЛИМЕРОВ
N,N-ДИАЛЛИЛ-Nʹ-АЦИЛГИДРАЗИНОВ С АКРИЛОВЫМИ МОНОМЕРАМИ
© М. Н. Горбунова, Т. Д. Батуева, Д. В. Ерошенко, Д. М. Кисельков
Институт технической химии УрО РАН,
614013, г. Пермь, ул. Королева, д. 3
E-mail: mngorb@yandex.ru
Поступила в Pедакцию 13 июля 2020 г.
После доработки 28 августа 2020 г.
Принята к публикации 8 сентября 2020 г.
Cополимеры N,N-диаллил-Nʹ-ацетилгидразина и N,N-диаллил-Nʹ-бензоилгидразина с акриловой кисло-
той, акрилонитрилом и акриламидом были синтезированы методом радикальной сополимеризации в
присутствии радикального инициатора азобисизобутиронитрила. Боргидридным методом получены
новые полимерные нанокомпозиты, содержащие наночастицы серебра размерами 31-55 нм, стаби-
лизированные синтезированными сополимерами N,N-диаллил-Nʹ-ацилгидразинов. Наличие гетеро-
атомных фрагментов и функциональных групп (карбоксильных, амидных, нитрильных, ацетильных,
бензоильных, гидразиновых) в полимерной цепи способствует специфическому взаимодействию с ча-
стицами серебра, регулируя размеры частиц на наноуровне и обеспечивая их равномерное распределе-
ние в полимерной матрице. Структурные особенности нанокомпозитов исследованы с использованием
УФ-, ИК-, ЯМР-спектроскопии и сканирующей электронной микроскопии. Полученные нанокомпозиты
обладают цитотоксической активностью в отношении клеток меланомы MS и рабдомиосаркомы RD
и являются перспективными в качестве лекарственных средств нового поколения, предназначенных
для терапии раковых опухолей.
Ключевые слова: N,N-диаллил-Nʹ-ацилгидразины; акриловые мономеры; радикальная сополимеризация;
нанокомпозиты; цитотоксическая активность
DOI: 10.31857/S0044461821020080
На основе нанокомпозитов создаются разнообраз-
образованию материалов с принципиально новыми
ные новые функциональные материалы для фото-
функциональными свойствами. При создании по-
ники, катализаторы, препараты для биотехнологии,
лимерных наноматериалов актуальными остаются
фармацевтической промышленности и сельского
вопросы равномерного распределения наночастиц в
хозяйства [1-3]. В таких материалах реализуется вы-
объеме материалов, создания устойчивых нанокомпо-
годное для полимеров и наночастиц серебра взаимо-
зитов, управления структурой, составом и размерами
действие компонентов: с одной стороны, полимеры
наночастиц.
выступают в качестве стабилизаторов наночастиц,
Полимерная матрица выступает в качестве стаби-
обусловливающих уникальные свойства нанокомпо-
лизирующего компонента, предотвращая агрегацию
зитов (биологические, каталитические, оптические,
металлических наночастиц. При этом на стабиль-
магнитные, электрические), с другой — включение
ность частиц значительное влияние оказывает при-
наночастиц в традиционные полимеры приводит к
рода полимера [4].
206
Нанокомпозиты серебра на основе сополимеров N,N-диаллил-Nʹ-ацилгидразинов с акриловыми мономерами
207
Перспективными высокомолекулярными соеди-
Акриловую кислоту (АК) (Alfa Aesar) очищали
нениями для стабилизации частиц серебра являются
перегонкой, использовали фракцию с т. кип. 138°С,
сополимеры N,N-диаллил-Nʹ-ацилгидразинов (ДАГ),
nD20 1.4202. Акрилонитрил (АН) (Alfa Aesar) очища-
поскольку они обладают высокой сорбционной спо-
ли перегонкой, использовали фракцию с т. кип. 78°С,
собностью по отношению к ионам металлов, кото-
nD20 1.3910. Акриламид (АА) (Alfa Aesar) перекри-
рая усиливается в случае формирования хелатных
сталлизовывали из ацетона и сушили в вакуум-шкафу
комплексов. Введение в полимерную матрицу разно-
до постоянной массы, т. пл. 84°С.
образных функциональных групп (карбоксильных,
Динитрил азодиизомасляной кислоты (ДАК)
амидных, нитрильных) способствует специфическо-
трижды перекристаллизовывали из метанола, сушили
му взаимодействию полимерных цепей с частицами
в вакууме при комнатной температуре до постоянной
серебра, регулируя размеры частиц на наноуровне и
массы, т. пл. 103°С, с разложением.
обеспечивая их равномерное распределение в поли-
Сополимеризацию N,N-диаллил-Nʹ-ацилгидрази-
мерной матрице.
нов с акриловой кислотой, акрилонитрилом и акрил-
Цель работы — получение нанокомпозитов,
амидом проводили в массе и в растворе органических
состоящих из наночастиц серебра и сополимеров
растворителей в присутствии радикального инициа-
N,N-диаллил-Nʹ-ацилгидразинов с акриловой кисло-
тора ДАК. Cополимеры очищали двукратным пере-
той, акрилонитрилом и акриламидом, исследование
осаждением из раствора в осадитель. Растворитель и
их цитотоксической активности.
осадитель подбирали для каждой системы отдельно:
для сополимера ДААГ-АК — метанол/диэтиловый
эфир; для сополимера ДААГ-АН — ацетон/метанол;
Экспериментальная часть
для сополимеров ДААГ-АА, ДАБЕГ-АК, ДАБЕГ-
N,N-Диаллил-Nʹ-ацетилгидразин (ДААГ) и N,N-
АН и ДАБЕГ-АА — ДМСО/метанол. Сополимеры
диаллил-Nʹ-бензоилгидразин (ДАБЕГ) синтезировали
сушили в вакууме при 40-50°С до постоянной массы.
из аллилхлорида и соответствующих ацилгидрази-
Состав сополимеров рассчитывали по результатам
нов по методике [5]. Для исследования использова-
элементного анализа.
ли: ДААГ — фракцию с т. кип. 120°С/5 мм рт. ст.,
Эффективные константы сополимеризации r1 и
nD20 1.4771, ДАБЕГ — фракцию с т. пл. 108°С (аце-
r2 рассчитывали методами Файнемана-Росса [6] и
тон:вода = 1:1). Чистоту контролировали элементным
Келена-Тюдоша [7].
анализом и методом ЯМР 13С. Основные спектраль-
Синтез нанокомпозитов серебра и сополимеров
ные характеристики N,N-диаллил-Nʹ-ацилгидразинов
N,N-диаллил-Nʹ-ацилгидразинов проводили следу-
представлены в табл. 1.
ющим образом. Сополимер (10-3 моль) растворяли в
Таблица 1
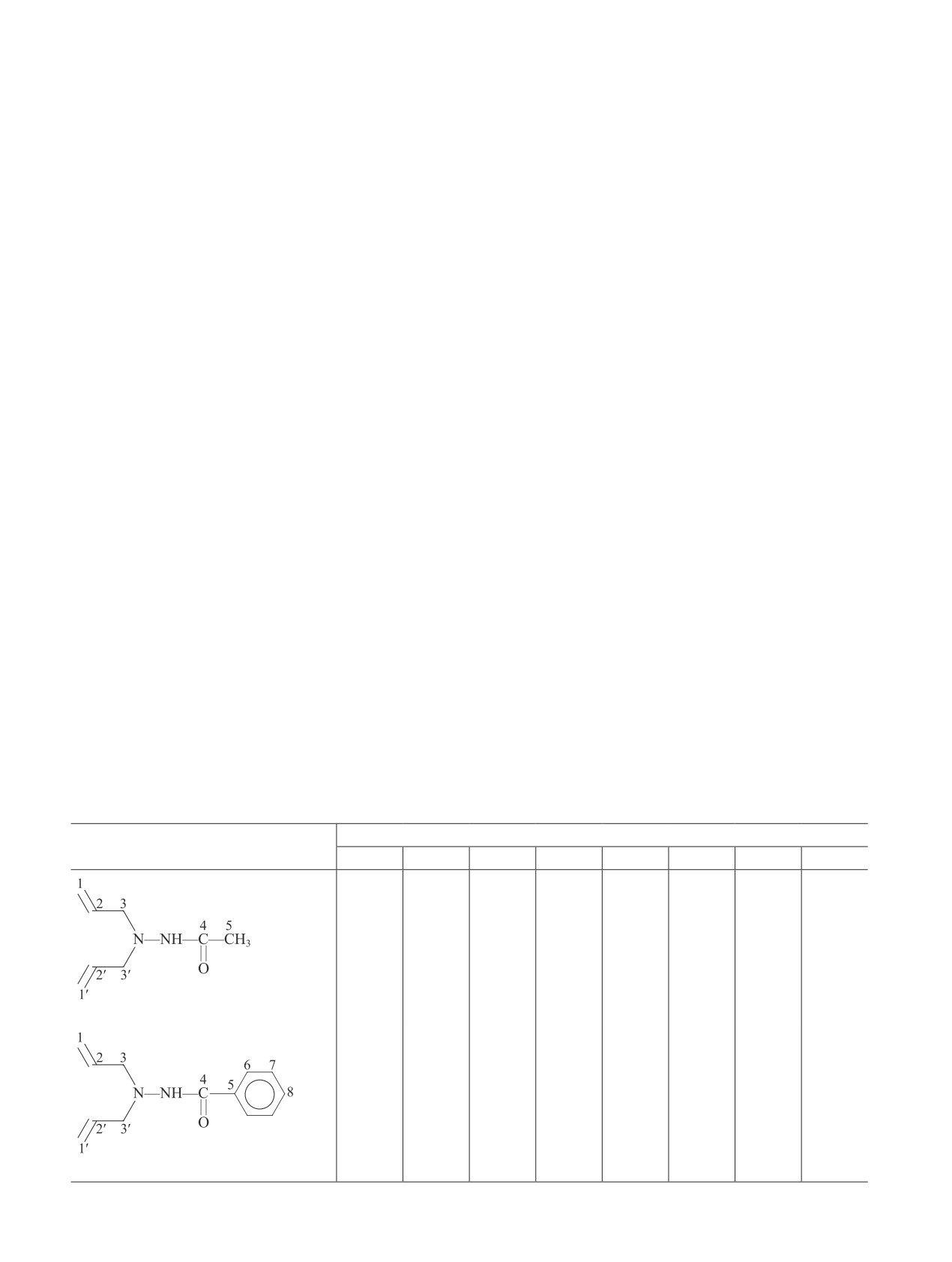
Основные спектральные характеристики N,N-диаллил-Nʹ-ацилгидразинов
Химический сдвиг δ, м. д., в спектре ЯМР 13С атомов
Соединение
С1,1ʹ
C2,2ʹ
C3,3ʹ
C4
C5
C6
C7
C8
119.7
132.4
60.9
175.1
20.1
N,N-Диаллил-Nʹ-ацетилгидразин
117.4
134.9
58.8
165.3
134.1
117.1
128.1
131.0
N,N-Диаллил-Nʹ-бензоилгидразин
208
Горбунова М. Н. и др.
20 мл метилового спирта или ацетона, к полученному
делена при 544 нм. В качестве количественного по-
раствору добавляли 1%-ный раствор нитрата серебра
казателя цитотоксичности по кривой доза-эффект
(0.17 г, 10-3 моль) и перемешивали смесь 1 ч при ком-
рассчитывали концентрацию тестируемого соедине-
натной температуре. Затем порциями добавляли бор-
ния, которая вызывает гибель 50% клеток (IC50). Все
гидрид натрия (0.038 г, 10-3 моль) в течение 10 мин.
эксперименты проводили в 3-кратной повторности.
Полученный темный раствор перемешивали в те-
чение 10 ч при комнатной температуре. Композиты
Обсуждение результатов
выделяли диализом и сушили в вакуумном шкафу.
ИК-спектры регистрировали на спектрометре IFS
Как было установлено ранее в работе [9], в при-
66/S Bruker в вазелиновом масле. Спектры ЯМР 1H и
сутствии радикальных инициаторов (динитрил азо-
13С регистрировали на спектрометре Bruker Avance II.
диизомасляной кислоты, перекись бензоила) N,N-
Спектры записаны в режимах с широкополосной
диаллил-Nʹ-ацилгидразины вступают в реакции
развязкой по протонам и в режиме JMOD. В качестве
гомо- и сополимеризации с виниловыми мономерами
растворителя использовали ДМСО-d6, внутренний
и диоксидом серы.
стандарт — тетраметилсилан. Спектры поглоще-
Cополимеры N,N-диаллил-Nʹ-ацетилгидразина
ния регистрировали на спектрофотометре СФ 2000.
и N,N-диаллил-Nʹ-бензоилгидразина с акриловой
Содержание Ag в водных растворах определяли
кислотой, акрилонитрилом и акриламидом были син-
на атомно-абсорбционном спектрометре iCE 3500
тезированы методом радикальной сополимеризации
(Thermo Fisher Scientific). Микрофотографии полу-
в присутствии ДАК. Исследования сополимериза-
чали на сканирующем электронном микроскопе FEI
ции N,N-диаллил-Nʹ-ацилгидразинов с акриловыми
QUANTA FEG 650 microscope (Netherlands).
мономерами показали, что при сополимеризации
Цитотоксичность синтезированных наноком-
независимо от среды образующиеся продукты имеют
позитов была определена по МТТ-тесту. Культуры
клеток человека А549 (аденокарцинома легкого),
RD (рабдомиосаркома) и MS (меланома), полу-
ченные из НИИ экспериментальной диагностики
и терапии опухолей Российского онкологического
научного центра им. Н. Н. Блохина РАМН, выра-
щивались в среде DMEM (для A549 и RD) и RPMI
1640 (для MS) с добавлением 10% эмбриональной
телячьей сыворотки, 2 мM L-глутамина и 1% гента-
мицина в качестве антибиотика при 37°C и 5% CO2 в
CO2-инкубаторе Isotemp Barnstead (США). Для оцен-
ки цитотоксического действия соединений в 96-лу-
ночный планшет Corning Costar (США) вносили клет-
ки A549, RD и MS в концентрации 1·104 кл/200 мкл
и инкубировали при 37°C во влажной атмосфере с
5% CO2. Через 24 ч к монослою клеток добавляли
испытуемые нанокомпозиты, растворенные в ДМСО,
в интервале концентраций 1.56–100 мкмоль·л-1.
В качестве контроля использовали лунки с добав-
лением 0.1% ДМСО. Аналогичным образом была
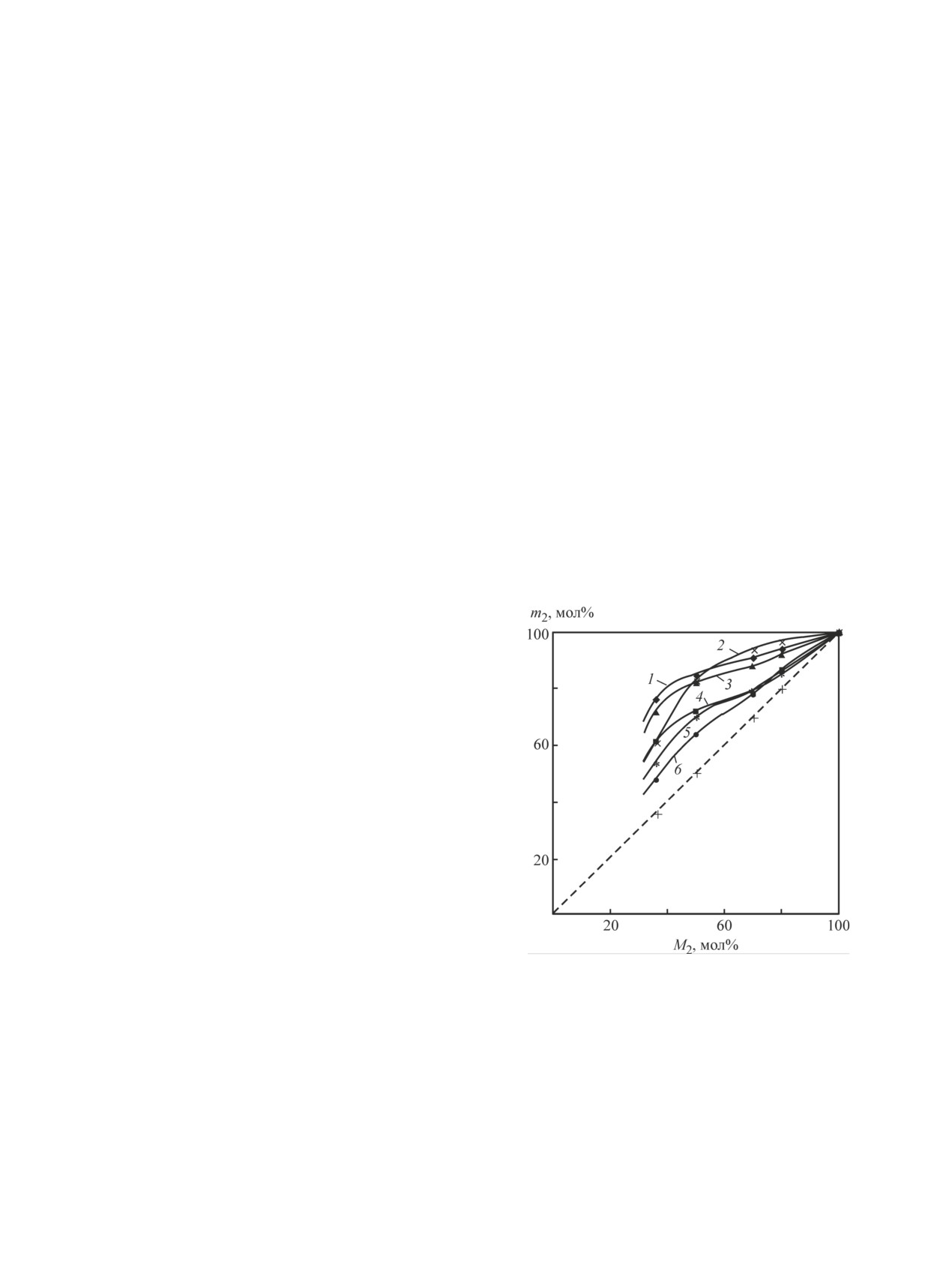
Рис. 1. Зависимость состава сополимера N,N-диал-
исследована цитотоксичность алкалоида с высокой
лил-Nʹ-ацетилгидразина (1-3) и N,N-диаллил-Nʹ-
противоопухолевой активностью камптотецина и
бензоилгидразина (4-6) с акриловой кислотой (1, 4),
антибиотика с противоопухолевой активностью док-
акрилонитрилом (2, 5) и акриламидом (3, 6) от состава
исходной смеси мономеров.
сорубицина. Камптотецин (ACROS organics) и док-
сорубицин гидрохлорид (TOCRIS bioscience) исполь-
[Динитрил азодиизомасляной кислоты] = 3 мас%,
T = 80°C.
зовали без дополнительной очистки. Выживаемость
M2 и m2 — содержание акрилового мономера в исходной
клеток оценивали через 72 ч инкубации клеток с ис-
смеси и в сополимере соответственно.
следуемыми нанокомпозитами с помощью МТТ-теста
1, 4 — в массе; 2, 5 — диметилсульфоксид, [М1 + М2] =
[8] на спектрофотометре FLUOstar OPTIMA BMG
= 2.2 моль·л-1; 3, 6 — метанол, [М1 + М2] = 2 моль·л-1;
Labtech (Германия), оптическая плотность была опре-
[М1 + М2] — суммарная концентрация мономеров.
Нанокомпозиты серебра на основе сополимеров N,N-диаллил-Nʹ-ацилгидразинов с акриловыми мономерами
209
статистическое распределение сомономерных звеньев
так и N,N-диаллил-Nʹ-ацетилгидразина. В этом слу-
в макромолекуле. При сополимеризации акриловый
чае радикал акрилонитрила предпочтительно ре-
мономер значительно активнее ДАГ, поэтому при
агирует со «своим» мономером, и происходит об-
всех исходных соотношениях мономеров образую-
разование длинных блоков последовательностей
щиеся сополимеры обогащены звеньями акрилового
акрилонитрила с включениями звеньев N,N-диаллил-
мономера (рис. 1). Поскольку молекула N,N-диаллил-
Nʹ-ацетилгидразина.
Nʹ-ацилгидразинов практически не способна присо-
В спектрах ЯМР 13С сополимеров N,N-диаллил-
единиться к растущему радикалу, оканчивающемуся
Nʹ-ацилгидразинов с акриловыми мономерами, син-
звеном ДАГ [5, 9], при любом соотношении мономе-
тезированных в присутствии инициатора ДАК при
ров в исходной смеси сополимеры не могут содер-
температуре 60-90°С, сигналы атомов двойной связи
жать звеньев ДАГ более 50 мол%.
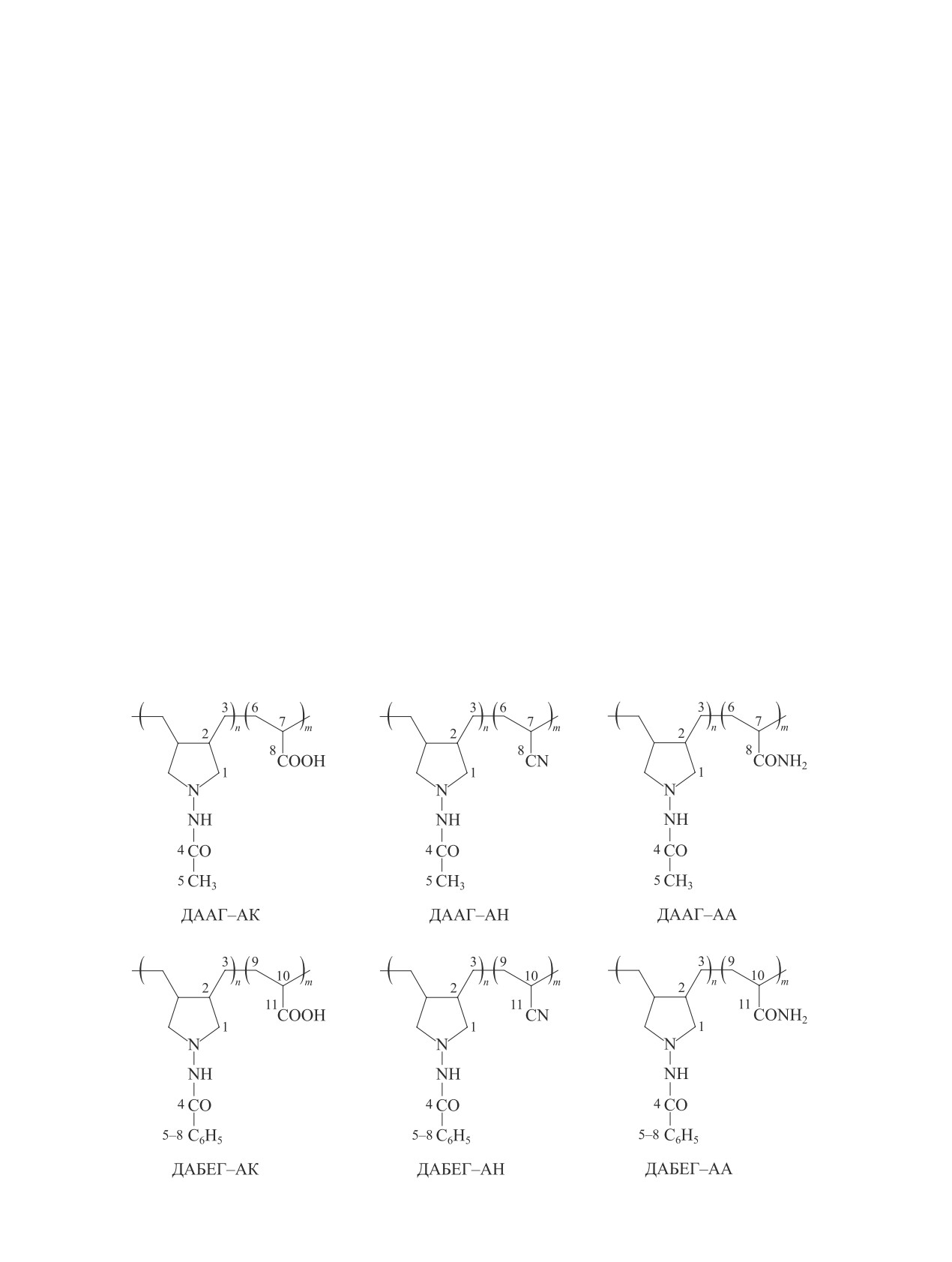
отсутствуют (см. схему, табл. 3). N,N-Диаллил-Nʹ-
Зависимость состава сополимера от состава исход-
ацетилгидразин и N,N-диаллил-Nʹ-бензоилгидразин
ной мономерной смеси для системы ДААГ (М1)-АН
вступают в реакции сополимеризации с акриловы-
формально соответствует крайне редко встречаю-
ми мономерами с участием обеих двойных связей
щемуся случаю, когда обе эффективные константы
с образованием пирролидиновых структур. Звенья
сополимеризации r1 > 1 и r2 > 1 (табл. 2). Численные
N,N-диаллил-Nʹ-ацилгидразинов, представляющие
значения эффективных констант сополимеризации,
собой пирролидиновые циклы, состоят из смеси цис-,
рассчитанные методом Файнемана-Росса, равны
транс-стереоизомеров со значительным преоблада-
r1 = 1.1 и r2 = 8.42 соответственно. В этом случае
нием транс-изомерных гетероциклов.
в системе наблюдается тенденция к последователь-
Сополимер N,N-диаллил-Nʹ-бензоилгидразина с
ной гомополимеризации мономеров, что, вероятно,
акрилонитрилом практически не содержит длинных
связано c низкой реакционной способностью ради-
блоков звеньев акрилонитрила и имеет упорядочен-
калов N,N-диаллил-Nʹ-ацетилгидразина. Тем не ме-
ную структуру, в то время как в структуре сополиме-
нее анализ ЯМР 13С спектра сополимера подтвердил
ра N,N-диаллил-Nʹ-ацетилгидразина с акрилонитри-
наличие в сополимере звеньев как акрилонитрила,
лом преобладают блочные фрагменты винилового
Сополимеры N,N-диаллил-Nʹ-ацетилгидразина и N,N-диаллил-Nʹ-бензоилгидразина с акриловой кислотой,
акрилонитрилом и акриламидом
210
Горбунова М. Н. и др.
Таблица 2
Значения эффективных констант сополимеризации N,N-диаллил-Nʹ-ацилгидразинов (М1) с акриловыми
мономерами (динитрил азодиизомасляной кислоты, 80°С)
Условия
М1
М2
r1
r2
r1r2
r1/r2
сополимеризации
N,N-Диаллил-Nʹ-
В массе
Акриловая кислота
0.12 ± 0.03
3.58 ± 0.74
0.429
0.033
ацетилгидразин
Диметилсульфоксид
Акрилонитрил
1.10 ± 0.31
8.42 ± 0.98
9.262
0.131
Метанол
Акриламид
0.12 ± 0.11
2.54 ± 0.55
0.305
0.047
N,N-Диаллил-Nʹ-
В массе
Акриловая кислота
0.01 ± 0.00
1.27 ± 0.23
0.012
0.008
бензоилгидразин
Диметилсульфоксид
Акрилонитрил
0.05 ± 0.01
1.21 ± 0.14
0.061
0.041
Метанол
Акриламид
0.59 ± 0.21
1.62 ± 0.22
0.956
0.364
мономера с включениями звеньев N,N-диаллил-Nʹ-
лые порошки. Все сополимеры растворимы в ДМСО,
ацетилгидразина.
сополимеры N,N-диаллил-Nʹ-ацетилгидразина с акри-
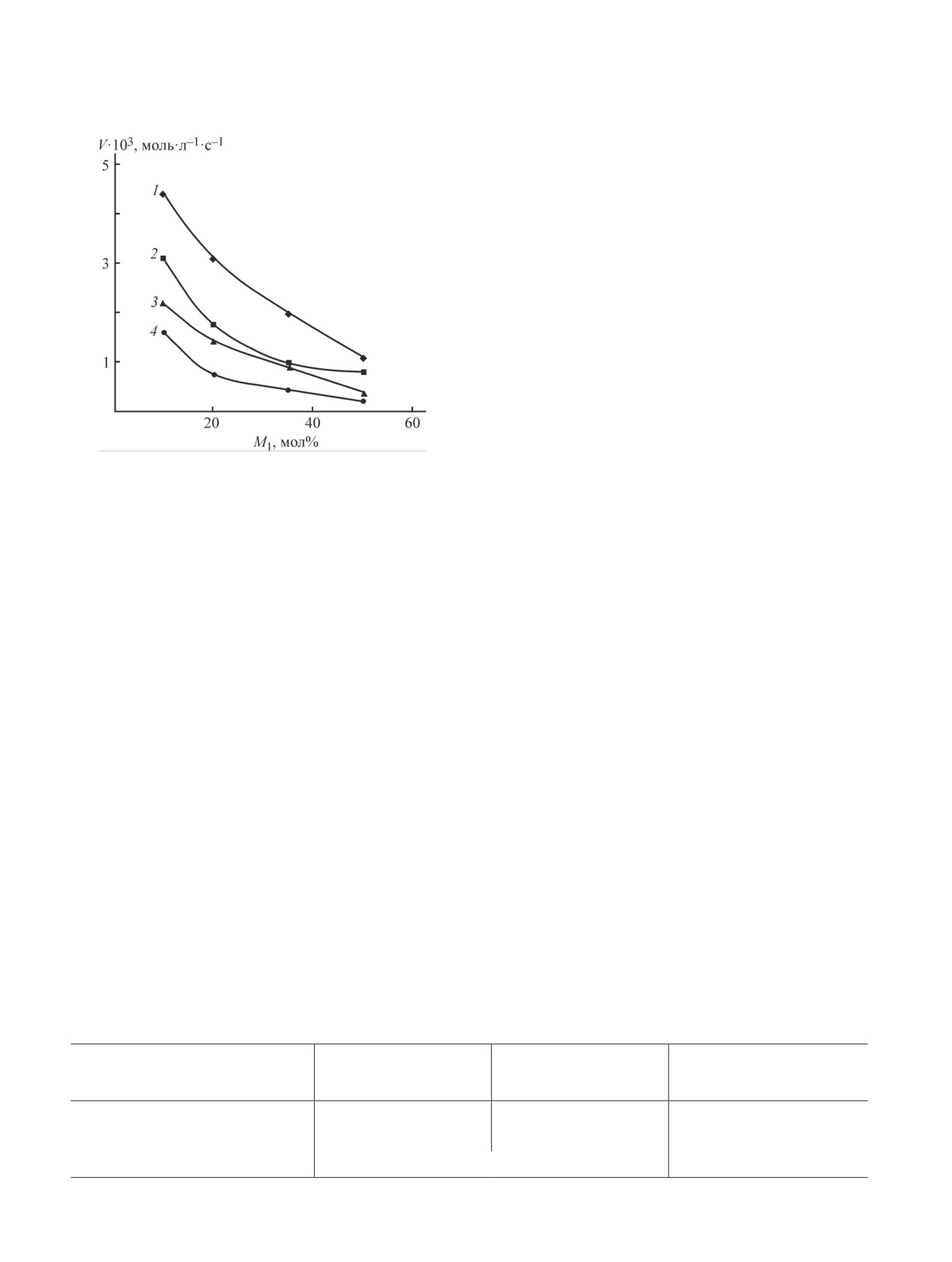
Кинетические исследования показали, что при
ловой кислотой и акриламидом растворимы также в
увеличении содержания N,N-диаллил-Nʹ-ацил-
воде, сополимер N,N-диаллил-Nʹ-бензоилгидразина с
гидразинов (М1) в исходной мономерной смеси зна-
акриловой кислотой растворим в ацетоне.
чения скорости сополимеризации всех исследуемых
Для синтеза нанокомпозитов серебра были выбра-
систем снижаются (рис. 2). Скорость сополимери-
ны растворимые в воде сополимеры N,N-диаллил-
зации N,N-диаллил-Nʹ-ацетилгидразина выше, чем
Nʹ-ацетилгидразина с акриловой кислотой и акрил-
N,N-диаллил-Nʹ-бензоилгидразина.
амидом и растворимые в ацетоне сополимеры
Сополимеры N,N-диаллил-Nʹ-ацилгидразинов с
N,N-диаллил-Nʹ-бензоилгидразина с акриловой кис-
акриловыми мономерами представляют собой свет- лотой. Синтез нанокомпозитов серебра проводили
Таблица 3
Спектры ЯМР 13С сополимеров N,N-диаллил-Nʹ-ацилгидразинов с акриловыми мономерами
(диметилсульфоксид-d6, тетраметилсилан, 25°С)
Химический сдвиг и мультиплетность сигналов δ, м. д., атомов
Соединение
С1
С2
С3
С4
C5
С6
С7
С8
С9
С10
С11
N,N-Диаллил-Nʹ-
58.7
32.2
52.4
173.0
20.4
42.2
55.8
174.76
ацетилгидразин-
60.0
33.3
53.5
с
к
т
д
175.15
акриловая кислота
т
д
т
с
N,N-Диаллил-Nʹ-
58.9
40.4
30.9
173.0
20.6
26.9
33.2
120.3
ацетилгидразин-
60.2
40.8
32.1
с
к
т
т
c
акрилонитрил
т
д
т
N,N-Диаллил-Nʹ-
58.4
42.5
36.1
172.8
20.9
31.8
48.7
177.0
ацетилгидразин-
60.2
43.9
36.6
с
к
т
т
c
акриламид
т
д
т
N,N-Диаллил-Nʹ-
57.8
40.7
49.7
165.2
134.1
127.4
128.5
128.9
43.1
45.3
174.3
бензоилгидразин-
59.2
41.3
50.8
с
с
д
д
д
т
д
c
акриловая кислота
т
д
т
N,N-Диаллил-Nʹ-
57.9
40.4
29.8
164.8
134.2
127.1
128.1
131.0
32.7
28.0
120.0
бензоилгидразин-
61.0
41.8
31.2
с
с
д
д
д
33.8
д
121.2
акрилонитрил
т
д
т
т
с
N,N-Диаллил-Nʹ-
58.5
40.7
35.8
167.9
133.4
127.7
128.0
131.1
34.5
49.6
177.2
бензоилгидразин-
59.3
42.0
37.2
с
с
д
д
д
т
т
с
акриламид
т
д
т
Примечание. с — синглет, д — дублет, т — триплет, к — квадруплет.
Нанокомпозиты серебра на основе сополимеров N,N-диаллил-Nʹ-ацилгидразинов с акриловыми мономерами
211
восстановлению ионной формы серебра, находящего-
ся в координационном взаимодействии с макромоле-
кулами сополимеров, до металлического состояния,
при этом постепенно изменяется цвет раствора от
светлого до темно-коричневого. Нанокомпозиты были
выделены методом диализа. В зависимости от сопо-
лимера образуются нанокомпозиты с содержанием
серебра от 5 до 15%. Соотношение нитрата серебра,
восстановителя и сополимера влияет на концентра-
цию серебра в нанокомпозитах. Характеристики ис-
следуемых нанокомпозитов серебра, полученных
методом диализа, представлены в табл. 4.
Образование нанокомпозитов сопровождается
заметным изменением химической структуры поли-
мерной матрицы. Обзорные ИК-спектры сополиме-
ров N,N-диаллил-Nʹ-ацетилгидразина с акриловой
кислотой и акриламидом и их нанокомпозитов се-
Рис. 2. Зависимость начальной скорости сополиме-
ребра представлены в дополнительных материалах
ризации N,N-диаллил-Nʹ-ацетилгидразина (1, 2)
и N,N-диаллил-Nʹ-бензоилгидразина (3, 4) с акриловой
(ESM_1).
кислотой (1, 3) и акрилонитрилом (2, 4) от состава ис-
В ИК-спектрах полученных нанокомпозитов на ос-
ходной смеси мономеров.
нове сополимеров N,N-диаллил-Nʹ-ацилгидразинов с
[Динитрил азодиизомасляной кислоты] = 3 мас%,
акриловой кислотой наблюдается заметное снижение
T = 80°C.
интенсивности полос поглощения валентных колеба-
M1 — содержание N,N-диаллил-Nʹ-ацилгидразинов в ис-
ний карбонильной группы ДАГ при 1671 см-1 и кар-
ходной смеси.
боксильной группы акриловой кислоты при 1728 см-1
1, 3 — в массе; 2, 4 — диметилсульфоксид, [М1 + М2] =
= 2.2 моль·л-1; [М1 + М2] — суммарная концентрация
и небольшой сдвиг этих полос в длинноволновую
мономеров.
область. Кроме того, исчезает полоса поглощения
валентных колебаний NH-группы при 1555 см-1 и
восстановлением нитрата серебра боргидридом на-
появляется интенсивная полоса поглощения валент-
трия в растворе сополимера. При смешивании рас-
ных колебаний карбоксилат-аниона при 1394 см-1.
творов сополимеров и нитрата серебра образуется
В ИК-спектрах полученных нанокомпозитов на
хлопьевидный осадок белого цвета, который при
основе сополимера N,N-диаллил-Nʹ-ацетилгидразина
дальнейшем перемешивании разрушается. Можно
с акриламидом наблюдается исчезновение плеча при
говорить, что исследуемые сополимеры на первой
1720 см-1, соответствующего валентными колебани-
стадии образуют с нитратом серебра устойчивую су-
ям карбонильной группы акриламида, а также сни-
спензию в виде мелкой взвеси в растворе, что связано
жение интенсивности полосы поглощения валентных
с возникающим координационным взаимодействием
колебаний карбонильной группы N,N-диаллил-Nʹ-
карбоксильных, амидных, гидразиновых, ацетильных
ацетилгидразина при 1670 см-1 и сдвиг этой полосы
и бензоильных фрагментов макромолекул с ионами
в область 1657 см-1. Аналогично нанокомпозитам на
серебра. Добавление боргидрида натрия приводит к
основе сополимеров с акриловой кислотой проис-
Таблица 4
Характеристики исследуемых нанокомпозитов серебра на основе сополимеров N,N-диаллил-Nʹ-ацетилгидразина
с акриловой кислотой и акриламидом и N,N-диаллил-Nʹ-бензоилгидразина с акриловой кислотой
N,N-Диаллил-Nʹ-
N,N-Диаллил-Nʹ-
N,N-Диаллил-Nʹ-
Характеристика
ацетилгидразин-акриловая
ацетилгидразин-
бензоилгидразин-акриловая
кислота
акриламид
кислота
Содержание Ag, мас%
5
11
8
Средний размер частиц, нм
51
31
55
Растворители для нанокомпозитов
Вода, диметилсульфоксид
Ацетон, диметилсульфоксид
212
Горбунова М. Н. и др.
ходит исчезновение полосы поглощения валентных
области 400-409 нм, в спектрах спиртовых раство-
колебаний NH-группы при 1555 см-1 и появляет-
ров нанокомпозитов на основе сополимеров N,N-
ся полоса поглощения валентных колебаний C—O
диаллил-Nʹ-ацилгидразинов с акриловой кислотой
при 1389 см-1. Можно отметить также заметное уве-
пик наблюдается в области 450 нм (рис. 3). Вид спек-
личение полос поглощения валентных колебаний
тров поглощения и полуширина максимума свиде-
NН2-группы при 3401 и 3208 см-1 и их сдвиг в об-
тельствуют об образовании золей с изолированными
ласть 3306 и 3182 см-1 соответственно. Подобные
наночастицами серебра [10].
изменения подтверждают взаимодействие полимер-
Результаты сканирующей электронной микроско-
ной матрицы с поверхностью наночастиц серебра,
пии подтверждают получение нанокомпозитов с уз-
обеспечивающее их стабилизацию.
кодисперсным распределением наночастиц серебра в
Исходя из вышеприведенных данных связывание
полимерной матрице (рис. 4). Установлено, что в ре-
ионов серебра теоретически возможно по кислороду
зультате образуются наночастицы сферической фор-
и азоту в звеньях N,N-диаллил-Nʹ-ацилгидразинов и
мы со средним диаметром 51, 31 и 55 нм для сопо-
в звеньях акриловой кислоты и акриламида. Можно
лимеров N,N-диаллил-Nʹ-ацетилгидразин-акриловая
предположить, что частичный отрицательный заряд
кислота, N,N-диаллил-Nʹ-ацетилгидразин-акриламид
на атоме азота в амидной группе будет чрезвычайно
и N,N-диаллил-Nʹ-бензоилгидразин-акриловая кис-
низок вследствие сопряжения несвязывающей элек-
лота соответственно. При стабилизации наночастиц
тронной пары атома азота с карбонильной группой.
сополимерами N,N-диаллил-Nʹ-ацилгидразинов с
Это позволяет считать, что атом азота в амидной
группе не способен эффективно вступать в координа-
цию с ионом металла. И координация иона серебра с
амидной группой возможна только по карбонильно-
му атому кислорода, в то время как взаимодействие
с карбоксилат-анионом возможно по двум атомам
кислорода.
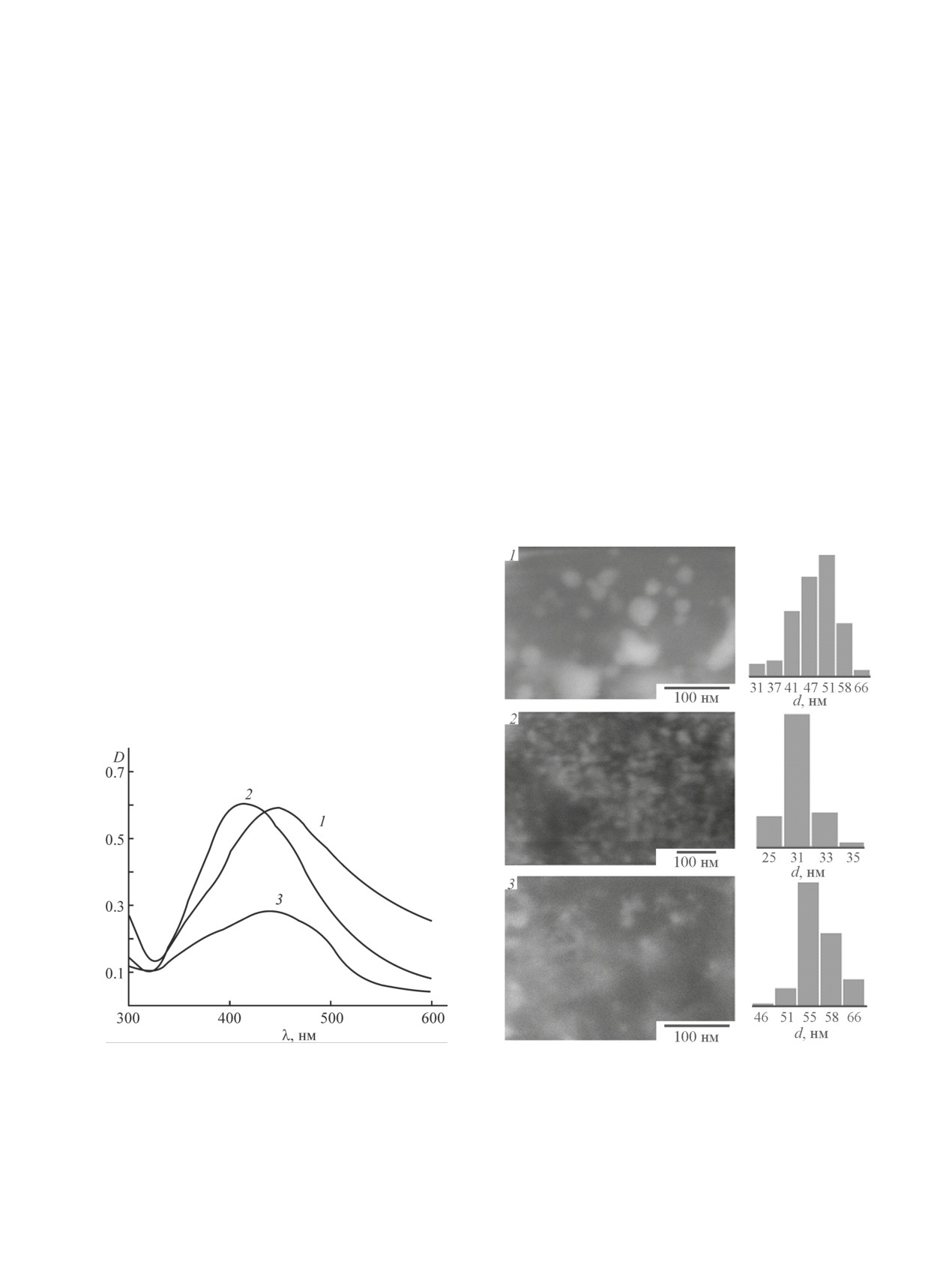
В УФ-спектрах водного раствора нанокомпози-
та на основе сополимера N,N-диаллил-Nʹ-ацетил-
гидразина с акриламидом наблюдается характерная
полоса плазмонного поглощения с максимумом в
Рис. 3. УФ-спектры поглощения растворов нанокомпо-
Рис. 4. Микрофотографии, полученные сканирующей
зитов серебра с сополимерами.
электронной микроскопией, наночастиц серебра и
1 — N,N-диаллил-Nʹ-ацетилгидразин-акриловая кис-
гистограммы распределения наночастиц серебра по
лота, этанол, с = 0.8·10-3 моль·л-1; 2 — N,N-диаллил-
размерам в нанокомпозитах на основе сополимеров
Nʹ-ацетилгидразин-акриламид, вода, с = 10-3 моль·л-1;
N,N-диаллил-Nʹ-ацетилгидразин-акриловая кислота (1),
3 — N,N-диаллил-Nʹ-бензоилгидразин-акриловая кислота,
N,N-диаллил-Nʹ-ацетилгидразин-акриламид (2), N,N-
этанол, с = 0.5·10-3 моль·л-1.
диаллил-Nʹ-бензоилгидразин-акриловая кислота (3).
Нанокомпозиты серебра на основе сополимеров N,N-диаллил-Nʹ-ацилгидразинов с акриловыми мономерами
213
Таблица 5
Цитотоксическая активность нанокомпозитов на основе сополимеров N,N-диаллил-Nʹ-ацилгидразинов
Концентрация тестируемого соединения, вызывающая гибель 50% клеток, IC50,
Нанокомпозит
мкмоль·л-1
RD (рабдомиосаркома)
A549 (аденокарцинома легкого)
MS (меланома)
N,N-Диаллил-Nʹ-ацетилгидразин-
8.30 ± 90.78
Не определяли
10.25 ± 0.02
акриловая кислота
N,N-Диаллил-Nʹ-ацетилгидразин-
8.86 ± 3.54
26.3 ± 1.78
6.25 ± 0.02
акриламид
N,N-Диаллил-Nʹ-бензоилгидразин-
2.07 ± 0.26
35.8 ± 8.24
0.25 ± 0.04
акриловая кислота
Камптотецин
1.72 ± 0.37
1.31 ± 0.03
0.77 ± 0.34
Доксорубицин
1.28 ± 0.03
2.04 ± 0.22
1.29 ± 0.16
акриловой кислотой наблюдается некоторая агрегация
тотоксической активности самих сополимеров в отно-
частиц, но размер агрегатов остается ниже 100 нм.
шении исследуемых клеток (IC50 > 100 мкмоль·л-1),
В последние годы опубликован ряд обзоров и
можно говорить об основном вкладе наночастиц сере-
статей, посвященных цитотоксической активности
бра в цитотоксическую активность нанокомпозитов.
серебра в отношении опухолевых клеток [11-18].
Наночастицы серебра исследованы в качестве про-
Выводы
тивораковых терапевтических средств для лечения
лейкемии, рака молочной железы, гепатоцеллюляр-
Cополимеры N,N-диаллил-Nʹ-ацетилгидразина
ной карциномы, рака легкого, рака кожи и орального
и N,N-диаллил-Nʹ-бензоилгидразина с акриловой
рака [14]. В этом плане применение металлполи-
кислотой, акрилонитрилом и акриламидом получены
мерных конструкций для противораковой терапии
методом радикальной сополимеризации в массе и
открывает уникальные возможности для борьбы
растворе органических растворителей в присутствии
с теми видами опухолей, которые не поддавались
динитрила азодиизомасляной кислоты. При сополиме-
лечению известными препаратами. Можно пред-
ризации N,N-диаллил-Nʹ-ацилгидразинов с акриловы-
положить, что используемые в качестве наноста-
ми мономерами независимо от среды образующиеся
билизирующих матриц сополимеры N,N-диаллил-
продукты имеют статистическое распределение со-
Nʹ-ацилгидразинов будут не только предотвращать
мономерных звеньев в макромолекуле, причем при
агрегацию частиц, но и обеспечивать пролонгирован-
всех исходных соотношениях мономеров образу-
ное биологическое действие, облегчать биодоступ-
ющиеся сополимеры обогащены звеньями акрило-
ность и, вероятно, позволят корректировать токсич-
вого мономера. N,N-Диаллил- Nʹ-ацилгидразины
ность наночастиц.
вступают в реакции сополимеризации с акриловыми
Результаты исследований цитотоксической ак-
мономерами с участием обеих двойных связей с об-
тивности показали, что нанокомпозиты обладают
разованием пирролидиновых структур, состоящих
высокой активностью в отношении клеток мелано-
из смеси цис-, транс-стереоизомеров со значитель-
мы MS и рабдомиосаркомы RD (табл. 5), причем по
ным преобладанием транс-изомерных гетероциклов.
уровню активности полученные нанокомпозиты не
Сополимеры N,N-диаллил-Nʹ-ацилгидразинов
уступают алкалоиду с высокой противоопухолевой
с акриловыми мономерами выступают в качестве
активностью камптотецину и антибиотику с проти-
подходящих стабилизаторов наночастиц серебра.
воопухолевой активностью доксорубицину.
Результаты сканирующей электронной микроско-
Исходя из представленных в литературе данных о
пии подтверждают образование серебряных нано-
цитотоксической активности наночастиц серебра, ста-
частиц сферической формы со средним диаметром
билизированных цитратом (в отношении дрожжевых
51, 31 и 55 нм для сополимеров N,N-диаллил-Nʹ-
клеток Saccharomyces cerevisiae 3-5 мкмоль·л-1 [19], в
ацетилгидразина с акриловой кислотой, акриламидом
отношении клеток аденокарциномы легких человека
и N,N-диаллил-Nʹ-бензоилгидразина с акриловой
A549 95 мкг·мл-1 [20]), и полученной нами низкой ци-
кислотой соответственно.
214
Горбунова М. Н. и др.
Высокая цитотоксическая активность полученных
[2]
Sustainable polymer composites and nanocomposites.
нанокомпозитов в отношении клеток меланомы MS и
Ch. Impact of nanoparticle shape, size, and properties
рабдомиосаркомы RD делает их перспективными для
of silver nanocomposites and their applications / Eds
S. Inamuddin, R. Thomas, Kumar Mishra, A. M. Asiri.
разработки новых высокоэффективных противоопу-
Springer, Cham, 2019. P. 1067-1091.
холевых лекарственных средств.
[3]
Крутяков Ю. А., Кудринский А. А., Оленин А. Ю.,
Лисичкин Г. В. Синтез и свойства наночастиц се-
Благодарности
ребра: достижения и перспективы // Успехи хи-
Авторы благодарят Центр коллективного пользо-
мии. 2008. Т. 77. № 3. С. 242-269 [Krutyakov
вания ПФИЦ УрО РАН «Исследование материалов и
Yu. A., Kudrinskiy A. A., Olenin A. Yu., Lisichkin G. V.
вещества» за спектральные, аналитические и биоло-
Synthesis and properties of silver nanoparticles:
гические исследования.
Advances and prospects // Russ. Chem. Rev. 2008.
Финансирование работы
[4]
Вегера А. В., Зимон А. Д. Синтез и физико-химиче-
ские свойства наночастиц серебра, стабилизиро-
Работа выполнена при финансовой поддерж-
ванных кислотным желатином // ЖПХ. 2006. Т. 79.
ке Российского фонда фундаментальных иссле-
№ 9. С. 1419-1422 [Vegera A. V., Zimon A. D. Synthesis
дований и Правительства Пермского края (грант
and physicochemical properties of silver nanoparticles
№ 19-43-590019-р_а).
stabilized by acid gelatin // Russ. J. Appl. Chem. 2006.
V. 79. N 9. P. 1403-1406.
Конфликт интересов
[5]
Гусев В. Ю., Воробьева А. И., Радушев А. В.,
Авторы заявляют об отсутствии конфликта инте-
Колесов С. В., Маслухов Р. Р., Толстиков А. Г.
ресов, требующего раскрытия в данной статье.
Диаллилацилгидразины как мономеры для по-
лифункциональных водорастворимых полиме-
ров // Изв. АН. Сер. хим. 2003. № 12. C. 2603-
Дополнительные материалы
2605 [Gusev V. Yu., Radushev A. V., Tolstikov A. G.,
Vorobʹeva A. I., Kolesov S. V., Muslukhov R. R.
Дополнительные материалы к статье представле-
Diallylacylhydrazines as monomers for polyfunctional
ны в файле ESM_1.
water-soluble polymers // Russ. Chem. Bull. 2003.
Информация об авторах
[6]
Finemann M., Ross S. D. Linear method for determining
Горбунова Марина Николаевна, к.х.н., ст.н.с. ИТХ
monomer reactivity ratios in copolymerization // J.
УрО РАН,
Polym. Sci. 1950. V. 5. P. 259-262.
Батуева Татьяна Дмитриевна, к.х.н., с.н.с. ИТХ
[7]
Kelen T., Tüdős F. Analysis of the linear methods for
УрО РАН,
determining copolymerization reactivity ratios. I. A new
improved linear graphic method // J. Macromol. Sci.,
Ерошенко Дарья Владимировна, к.б.н., н.с. ИТХ
Chem. 1975. V. 9. N 1. P. 1-27.
УрО РАН,
[8]
Scudiero D. A., Shoemaker R. H., Paull K. D., Monks A.,
Tierney S., Notziger T. H., Currens M. T., Seniff D.,
Кисельков Дмитрий Михайлович, к.т.н., н.с. ИТХ
Boyd M. K. Evaluation of a soluble tetrazolium/
УрО РАН,
formazan assay for cell growth and drug sensitivity in
culture using human and other tumor cell lines // Cancer
Res. 1988. V. 48. P. 4827-4833.
[9]
Воробьева А. И., Горбунова М. Н., Гусев В. Ю.,
Список литературы
Муслухов Р. Р., Колесов С. В., Толстиков А. Г.
[1] Nanomaterials and polymer nanocomposites. Raw
Сополимеры на основе диаллилгидразинов //
materials to applications. Ch. 2. Silver Nanomaterials
ЖПХ. 2004. T. 77. № 7. C. 1174-1179 [Vorobʹeva A. I.,
and Their Polymer Nanocomposites / Ed. by N. Karak.
Gorbunova M. N., Gusev V. Y., Muslukhov R. R.,
Elsevier, 2019. P. 47-89.
Kolesov S. V., Tolstikov A. G., Monakov Yu. B.
Copolymers based on diallylhydrazines // Russ. J.
Нанокомпозиты серебра на основе сополимеров N,N-диаллил-Nʹ-ацилгидразинов с акриловыми мономерами
215
Appl. Chem. 2004. V. 77. N 7. P. 1160-1164. https://
[15]
Zhang T., Wang L., Chen Q., Chen Ch. Cytotoxic
potential of silver nanoparticles // Yonsei Med. J.
[10]
Карпов С. В., Слабко В. В. Оптические и фотофи-
2014. V. 55. P. 283-291.
зические свойства фрактально-структурированных
золей металлов. Новосибирск: Изд-во СО РАН,
[16]
Goodman A. M., Cao Y., Urban C., Neumann O., Ayala-
2003. C. 89-122.
[11]
Ostad S. N., Dehnad S., Nazari Z. E., Fini Sh. T.,
Halas N. J
. The Surprising in vivo instability of near-
Mokhtari N., Shakibaie M., Shahverdi A. R. Cytotoxic
IR-absorbing hollow Au-Ag nanoshells // ACS Nano.
activities of silver nanoparticles and silver ions in
2014. V. 8. P. 3222-3231.
parent and tamoxifen-resistant T47D human breast
cancer cells and their combination effects with
[17]
Braun G. B., Friman T., Pang H.-B., Pallaoro A.,
tamoxifen against resistant cells // Avicenna J. Med.
Hurtado de Mendoza T., Willmore A.-M. A.,
Biotechnol. 2010. V. 2. N 4. Р. 187-196.
Kotamraju V. R., Mann A. P., She Zh.-G.,
[12]
Ананян М. А., Демченко А. Г., Садыкова В. С.,
Sugahara K. N., Reich N. O., Teesalu T., Ruoslahti E.
Люндуп А. В., Громовых Т. И., Фельдман Н. Б.,
Etchable plasmonic nanoparticle probes to image and
Луценко С. В. Получение стабилизированных на-
quantify cellular internalization // Nat. Mater. 2014.
ночастиц серебра и изучение их антимикробной и
V. 13. P. 904-911.
цитотоксической активности в отношении клеток
гепатомы человека линии HepG2 // Рос. нанотехно-
[18]
Ong C., Lim J. Z. Z., Ng C.-T., Li J. J., Yung L.-Y. L.,
логии. 2019. Т. 14. № 5-6. С. 91-98 [Ananyan M. A.,
Bay B.-H
. Silver nanoparticles in cancer: Therapeutic
Demchenko A. G., Sadykova V. S., Lyundup A. V.,
efficacy and toxicity // Curr. Med. Chem. 2013. V. 20.
Gromovykh T. I., Feldman N. B., Lutsenko S. V.
P. 772-781.
Preparation of stabilized silver nanoparticles and study
of their antimicrobial and cytotoxic activity on the
[19]
Klimov A. I., Zherebin P. M., Gusev A. A.,
human hepatoma HepG2 cell line // Nanotechnologies
Kudrinskiy A. A., Krutyakov Y. A. The silver ions
in Russia. 2019. V. 14. P. 273-279.
contribution into the cytotoxic activity of silver and
silver halides nanoparticles // IOP Conf. Ser.: Mater.
[13]
Mohanta Y. K., Panda S. K., Jayabalan R., Sharma N.,
Sci. Eng. 2015. 012034/1-012034/9
Bastia A. K., Mohanta T. K. Antimicrobial, antioxidant
and cytotoxic activity of silver nanoparticles
[20]
Mala R., Ruby Celsia A.S., Malathi Devi S.,
synthesized by leaf extract of Erythrina suberosa
Geerthika S. Comparison on bactericidal and cytotoxic
(Roxb.) // Frontiers Mol. Biosci. 2017. V. 4. P. 14/1-
effect of silver nanoparticles synthesized by different
methods // IOP Conf. Ser.: Mater. Sci. Eng. 2017.
[14]
Wei L., Lu J., Xu H., Patel A., Chen Z. S., Chen G.
012155/1-012155/11.
Silver nanoparticles: Synthesis, properties, and
therapeutic applications // Drug. Discov. Today. 2015.
V. 20. P. 595-601.