Журнал прикладной химии. 2021. Т. 94. Вып. 6
СОРБЦИОННЫЕ И ИОНООБМЕННЫЕ ПРОЦЕССЫ
УДК 544.726:661.862′053.2
СОРБЦИОННОЕ УДАЛЕНИЕ ЖЕЛЕЗА(III)
ИЗ РАСТВОРОВ СУЛЬФАТА АЛЮМИНИЯ
© А. А. Блохин1, Ю. В. Мурашкин1, М. А. Михайленко2
1 Санкт-Петербургский государственный технологический институт (технический университет),
190013, г. Санкт-Петербург, Московский пр., д. 26
2 Представительство компании Purolite Ltd в CНГ,
113096, г. Москва, Люсиновская ул., д. 36
E-mail: blokhin@list.ru
Поступила в Редакцию 24 апреля 2021 г.
После доработки 24 мая 2021 г.
Принята к публикации 10 июня 2021 г.
Исследована сорбция алюминия(III) и железа(III) из индивидуальных растворов и примесных количеств
железа(III) из растворов Al2(SO4)3 на макропористых фосфоновокислотном катионите Purolite
MTS9560 и иминодиацетатных ионитах Purolite MTS9300 и Purolite S991. Показано, что все три
ионита имеют более высокое сродство к железу(III) относительно алюминия(III). Установлено,
что наиболее высокую избирательность к железу(III) при сорбции из раствора сульфата алюминия
катионит Purolite MTS9560 проявляет после введения в раствор серной кислоты до ее концентра-
ции 2.2-2.5 моль·л-1, а иминодиацетатные иониты — при сорбции из раствора с рН 2.2-2.6. Ионит
Purolite MTS9300, синтезированный на стирольной матрице, по способности к сорбции железа(III)
превосходит ионит Purolite S991, синтезированный на акрилатной матрице. Установлено, что при
пропускании раствора с концентрацией Al2(SO4)3 184 и железа(III) 2.9 г·л-1, рН 2.3, через колонку с
ионитом Purolite MTS9300 происходит глубокое удаление примеси железа(III) до его остаточной
концентрации не более 0.002 г·л-1. Практически полная десорбция железа(III) из ионита достигается
при пропускании через колонку 1 М раствора серной кислоты.
Ключевые слова: сульфат алюминия; алюминий(III); железо(III); ионный обмен; сорбция; десорбция;
иониты
DOI: 10.31857/S0044461821060141
Сульфат алюминия широко применяется в про-
В зависимости от маркировки сульфата алюми-
цессах водоподготовки, в текстильном производстве,
ния предъявляются определенные требования к его
строительстве, пищевой промышленности, косметике
чистоте. К числу примесей, содержание которых в
и бытовой химии, а также как прекурсор при синтезе
сульфате алюминия всегда регламентируется, отно-
других востребованных соединений алюминия.*
сится примесь железа. Так, согласно ГОСТ 12966-85
«Алюминия сульфат технический очищенный.
Технические условия», в техническом сульфате алю-
миния как первого, так и высшего сорта содержание
iesCB8435192_EN.htm#Purpose%20and%20effect%20of%20
aluminum%20sulfate
примеси железа не должно превышать 0.02 мас%
805
806
Блохин А. А. и др.
в пересчете на оксид железа(III), или 0.007 мас% в
сульфат-иона железо(III) присутствует в виде отри-
пересчете на железо. Еще более жесткие требования
цательно заряженных сульфатных комплексов,* что
к чистоте по примеси железа (0.001-0.002 мас%)
может сказаться на результатах сорбции.
предъявляются к алюмокалиевым и алюмоаммоний-
Цель работы — исследование сорбции железа(III)
ным квасцам, синтез которых основан на применении
из растворов Al2(SO4)3 на ионитах с фосфоновокис-
сульфата алюминия. Между тем содержание при-
лыми и иминодиацетатными функциональными груп-
меси железа в сульфате алюминия, получаемом в
пами, выбор ионита и оценка результатов, достига-
результате обработки серной кислотой природного и
емых при сорбционной очистке растворов Al2(SO4)3
техногенного сырья, обычно существенно превышает
от примеси железа(III) на выбранном ионите.
приведенные выше значения [1].
Применение метода кристаллизации из растворов
Экспериментальная часть
[1] и метода, основанного на избирательном осажде-
нии гидроксида железа(III) [2], не обеспечивает глу-
При проведении экспериментов по сорбции и при
бокой очистки соединений алюминия от примеси же-
аналитическом сопровождении работы использова-
леза. Применение методов жидкостной экстракции с
лись Al2(SO4)3∙18H2O и Fe2(SO4)3∙9H2O (оба — pure,
использованием в качестве экстрагентов карбоновых
PanReac AppliChem ITW Reagents), KCNS, K2S2O8
кислот [1], алкилфосфорных кислот и алкилфосфо-
и дитизон (все — for analysis, PanReac AppliChem
новых кислот, например, ди-2-этилгексилфосфорной
ITW Reagents), гликокол (for analysis, Merck KGaA),
кислоты (Д2ЭГФК) [1, 3] и моно-2-этилгексилового
раствор H2SO4 94.6%-ный (х.ч., ОХК «Щекиноазот»),
эфира 2-этилгексилфосфоновой кислоты (P507) [4],
cтандарт-титры (фиксаналы) раствора Трилона Б
а для очистки растворов AlCl3 третичных аминов и
(Комплексона III) (АО «Реактив»).
бинарных экстрагентов — смесей Д2ЭГФК и четвер-
В работе были опробованы монофункциональный
тичных аммониевых оснований [5] хотя и позволяет
катионит с фосфоновокислыми группами Purolite
осуществлять достаточно полную очистку растворов
MTS9560 и два иминодиацетатных ионита Purolite
солей алюминия от железа(III), но сопряжено с за-
MTS9300 и Purolite S991 (Purolite Ltd), далее обо-
грязнением перерабатываемых и сбросных растворов
значенные как MTS9560, MTS9300 и S991. Все три
зачастую токсичными органическими веществами —
ионита макропористые, иониты MTS9560 и MTS9300
компонентами экстрагентов. В работе [1] рассмотрена
синтезированы на стирольной, S991 — на акрилатной
возможность применения ионообменных сорбентов
матрице.
различной функциональности для удаления желе-
В экспериментах, проводимых в статических усло-
за(III) из растворов Al2(SO4)3. Предпочтение было
виях, навески ионитов по 0.2 г в пересчете на сухую
отдано карбоксильному катиониту КБ-2х8, однако
массу помещали в колбы и приводили в контакт с
детальные исследования показали, что он может быть
20 мл раствора, содержащего Fe(III) и (или) Al(III),
использован только для предварительной очистки
содержимое колб перемешивали в шейкере Memmert
растворов Al2(SO4)3 от железа(III) до остаточного
ONE 14 в течение 48 ч. По истечении указанного
содержания последнего не менее 1 г∙л-1. В патентах
времени растворы отделяли от ионитов, проводили
[6, 7] приведено описание сорбционных способов
их анализ на сорбируемые компоненты и измеряли
удаления железа(III) из растворов Al(NO3)3, основан-
значения рН. По изменению концентрации ионов
ных на применении иминодиацетатного ионита [6]
металлов в растворе (с учетом навески ионита и
или фосфоновокислотного катионита, содержащего
объема раствора) рассчитывали значения массовой
для улучшения кинетических характеристик наряду
емкости анионитов (мг или ммоль иона металла/г
с фосфоновокислыми функциональными группами
сухого ионита), которые затем с учетом удельного
сульфогруппы [7]. Применение обоих способов обе-
объема ионитов пересчитывали на объемную емкость
спечивает достаточно глубокую очистку растворов
(мг или ммоль иона металла/мл набухшего ионита).
Al(NO3)3 от железа(III). В то же время сведений о
Степень извлечения рассчитывали как долю погло-
применении таких ионитов для удаления железа(III)
щенного ионитами иона металла от его содержания в
из растворов Al2(SO4)3 нами не было найдено. При
исходном растворе. Эксперимент в динамических ус-
рассмотрении возможности применения сорбцион-
ловиях проводили в стеклянной колонке, заполненной
ных способов для удаления железа(III) из растворов
Al2(SO4)3 следует принимать во внимание, что если
* Martell A. E., Smith R. M. Critical stability constants.
с нитрат-ионом железо(III) анионных комплексов не
V. 4. Inorganic Complexes. New York: Springer Science +
образует, то в растворах с высокой концентрацией
Business Media, 1977. P. 50, 83.
Сорбционное удаление железа(III) из растворов сульфата алюминия
807
20 мл ионита при соотношении высоты слоя аниони-
рошем соответствии с данными, относящимися к
та и внутреннего диаметра колонки 10:1. Скорость
фосфоновокислотным катионитам, сведений об от-
пропускания растворов при сорбции составила 1.5,
носительном сродстве иминодиацетатных ионитов к
при десорбции — 0.75 уд. об.∙ч-1 (уд. об. — удельный
железу(III) и алюминию(III) в доступной литературе
объем раствора, т. е. объем раствора, отнесенный к
нами не было найдено.
объему сорбента, находящемуся в колонке). Как при
Из опробованных ионитов наиболее высока ем-
сорбции, так и при десорбции растворы подавали в
кость по железу(III) катионита MTS9560, однако он
колонку по направлению снизу вверх. В растворах
же из всех ионитов в наибольшей степени сорбирует
на выходе из колонки определяли концентрацию же-
и алюминий(III). Судя по характеру полученных зави-
леза(III).
симостей, а именно исходя из того, что способность
Концентрацию алюминия и железа(III) в исходных
катионита MTS9560 к сорбции железа(III) при сни-
растворах и индивидуальных растворах при прове-
жении рН растворов уменьшается менее резко, чем
дении предварительных экспериментов определяли
его способность к сорбции алюминия(III), можно
комплексонометрическим титрованием,* концен-
предполагать, что он будет более эффективно сорби-
трацию железа(III) в растворах Al2(SO4)3 — коло-
ровать железо(III) из растворов сульфата алюминия
риметрически роданидным методом.** Измерения
после их подкисления. Наиболее высокие различия
проводили на фотоэлектрическом фотометре КФК-3
в способности к сорбции железа(III) и алюминия(III)
ЗОМЗ (АО «ЗОМЗ»). Значения рН растворов опреде-
проявляет иминодиацетатный ионит, синтезирован-
ляли при помощи универсального электрода ЭСК-106
ный на стирольной основе, MTS9300. При сорбции
(ООО «Измерительная техника») на иономере рН-410
из слабокислых растворов его емкость по железу(III)
(ООО «НПО Аквилон»).
в интервале рН 1.5-2.4 достаточно велика, в то время
как заметные количества алюминия он начинает сор-
бировать только при достижении рН не менее 2.0-2.5.
Обсуждение результатов
Несколько ниже различия в сродстве железа(III) и
На начальном этапе работы были проведены экс-
алюминия(III) к иминодиацетатному иониту S991,
перименты по изучению сорбции алюминия(III) и
синтезированному на акрилатной матрице.
железа(III) на отобранных ионитах из индивидуаль-
Сорбция железа(III) на ионитах MTS9560,
ных растворов, содержащих тот или иной компонент.
MTS9300 и S991 была исследована непосредственно
Для получения сопоставимых данных эксперименты
из раствора Al2(SO4)3 с концентрацией по Al2(SO4)3
по сорбции проводили путем контакта различных ио-
146 г∙л-1 и железу(III) 1.3 г∙л-1. Исходя из результатов
нитов с растворами с одинаковой концентрацией алю-
исследования сорбции железа(III) и алюминия(III)
миния(III) или железа(III) по 0.025 ± 0.001 моль∙л-1,
из их индивидуальных растворов, при поиске опти-
фоновым электролитом служил сульфат натрия,
мальных условий сорбции железа(III) на катионите
концентрация которого поддерживалась равной
MTS9560 эксперименты проводили при подкислении
0.5 моль∙л-1. Переменным параметром являлись зна-
раствора Al2(SO4)3 различными количествами серной
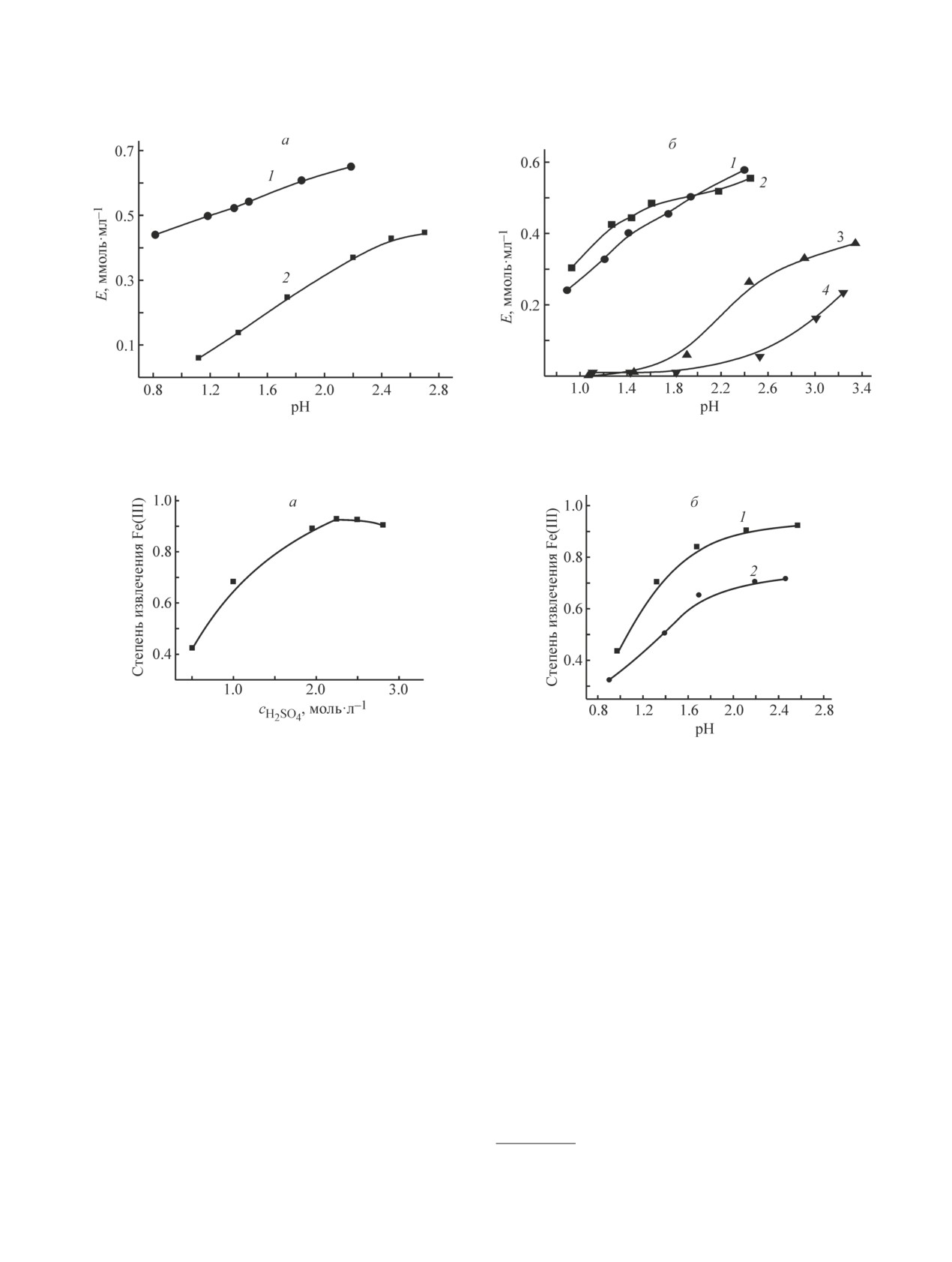
чения рН растворов (рис. 1).
кислоты [при поддержании постоянной концентрации
Емкость ионитов как по алюминию(III), так и же-
Al2(SO4)3], на иминодиацетатных ионитах — в срав-
лезу(III) возрастает при повышении рН растворов,
нительно узком интервале рН раствора (рис. 2, а, б).
при этом все иониты в исследованном интервале рН
Все три ионита проявляют способность к сорбции
растворов проявляют большее сродство к железу(III),
железа(III) из раствора с высокой концентрацией
чем к алюминию(III) (рис. 1), что находится в хо-
Al2(SO4)3. Это позволяет сделать заключение, что при
контакте с фосфоновокислыми и иминодиацетатными
функциональными группами ионитов сульфатные
* Шварценбах Г., Флашка Г. Комплексонометрическое
комплексы, в виде которых железо(III) находится в
титрование /Пер. с нем. Ю.И. Ванштейна. М.: Химия,
растворах с высокой концентрацией сульфат-иона,
1970. С. 191-192, 239-240 [Schwarzenbach G., Flaschka H.
Die komplexometrische Titration. Stuttgard: Ferdinand Enke
разрушаются вследствие связывания железа(III) функ-
Verlag, 1965].
циональными группами ионитов в комплексные со-
** Марченко З., Бальцежак М. Методы спектрофотоме-
единения, существенно более устойчивые, чем его
трии в УФ и видимой областях в неорганическом анализе /
сульфатные комплексы. Полученные результаты под-
Пер. с пол. под ред. Ю. А. Золотова. М.: БИНОМ. Лаборатория
твердили справедливость предположений, сделанных
знаний, 2009. С. 178-180 [Marczenko Z., Balcerzak M.
на основании результатов предварительных экспери-
Spektrofotometryczne metody w analizie nieorganicznej.
Warszawa: Wydawnictwo Naukowe PWN SA, 1998].
ментов. Действительно, полнота извлечения желе-
808
Блохин А. А. и др.
Рис. 1. Зависимость емкости катионита MTS9560 по железу(III) (1а) и алюминию(III) (2а) и ионитов S991 по же-
лезу(III) (1б) и алюминию(III) (3б) и MTS9300 по железу(III) (2б) и алюминию(III) (4б) от рН 0.5 М раствора Na2SO4.
Рис. 2. Зависимость степени извлечения железа(III) на катионите MTS9560 от концентрации серной кислоты (а) и
на ионитах MTS9300 (1б) и S991 (2б) от рН раствора с концентрацией по Al2(SO4)3 146 г∙л-1 и исходной концен-
трацией железа(III) 1.3 г∙л-1.
за(III) на фосфоновокислотном катионите MTS9560
виде раствора, или в виде твердой соли необходимо
из раствора Al2(SO4)3 заметно возрастает при повы-
после проведения очистки от железа(III) на фосфо-
шении кислотности раствора и достигает максималь-
новокислотном катионите нейтрализовать введенную
ных значений при концентрации серной кислоты
в растворы серную кислоту, поскольку содержание
2.2-2.5 моль∙л-1 (рис. 2, а). Способность иминоди-
серной кислоты в сульфате алюминия нормирует-
ацетатного ионита MTS9300 к сорбции железа(III)
ся.* Кроме того, десорбция железа(III) из фосфоно-
из раствора Al2(SO4)3 монотонно увеличивается при
вокислотных катионитов вызывает определенные
повышении рН растворов и достигает максимальных
затруднения [8]. Значения рН растворов, оптималь-
значений при рН 2.2-2.6, причем степень извлечения
ные для выделения железа(III) на ионите MTS9300,
железа(III) на этом ионите при рН 2.2-2.6 сравнима
соответствуют значениям рН растворов Al2(SO4)3,
со степенью извлечения железа(III) на катионите
получаемых в результате переработки различных ви-
MTS9560 при сорбции из растворов, подкисленных
дов минерального сырья, в том числе отработанных
серной кислотой (рис. 2, б). Избирательность к же-
катализаторов гидрообработки нефти. Таким образом,
лезу(III) ионита S991 на фоне Al2(SO4)3 заметно ниже.
при использовании ионита MTS9300 для очистки
Подкисление растворов — это дополнительная и
нежелательная операция: для дальнейшего исполь-
* ГОСТ 12966-85. Алюминия сульфат технический
зования сульфата алюминия или непосредственно в очищенный. Технические условия.
Сорбционное удаление железа(III) из растворов сульфата алюминия
809
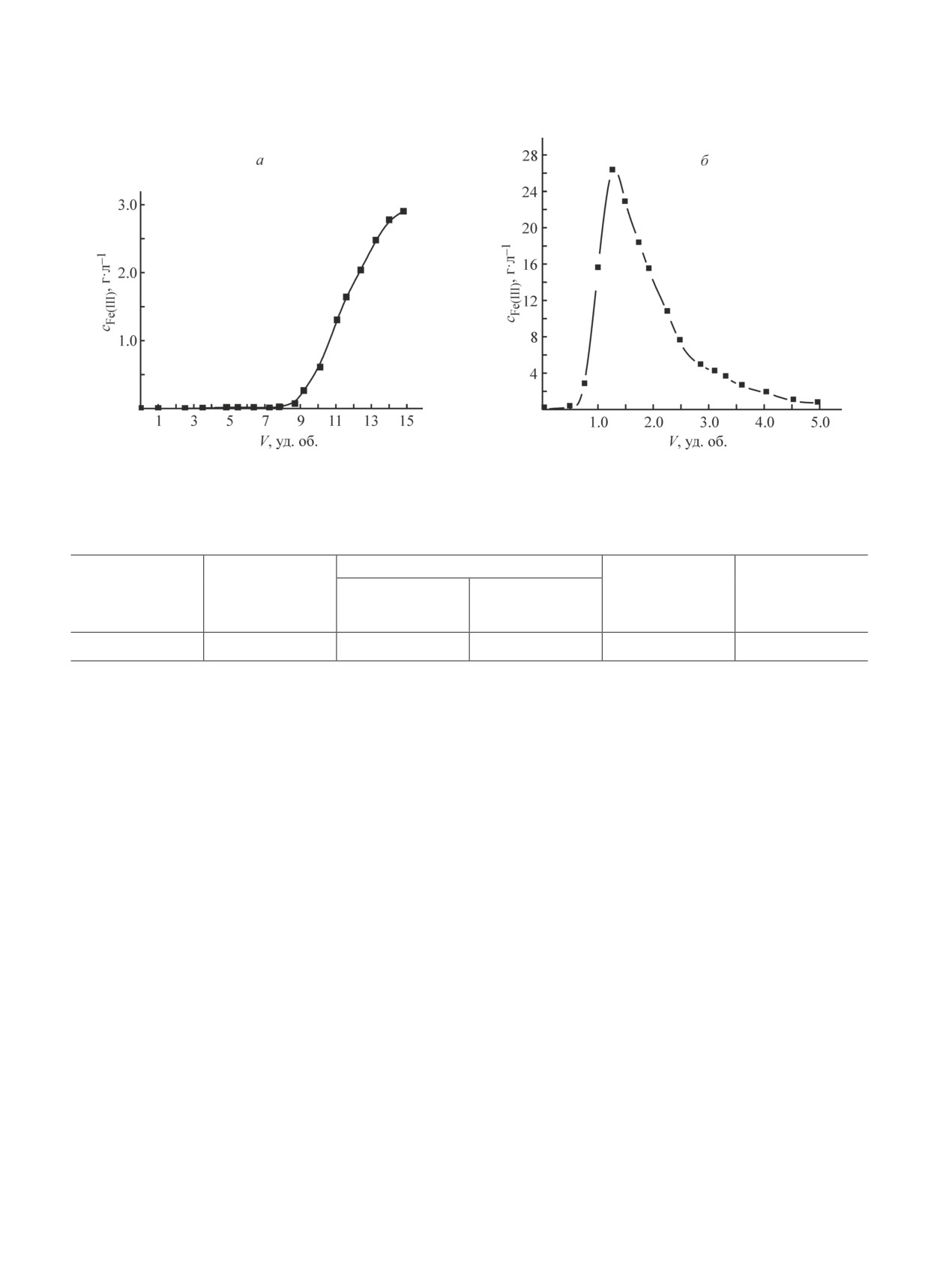
Рис. 3. Выходные кривые сорбции железа(III) на ионите MTS9300 из раствора с концентрацией Al2(SO4)3 184 г∙л-1
и железа(III) 2.9 г∙л-1, рН 2.3 (а) и десорбции железа(III) 1 М раствором Н2SO4 (б).
Сводные параметры сорбции и десорбции железа(III) на иминодиацетатном ионите MTS9300
-1 ионита
Сорбировано железа(III), мг∙мл
Остаточная
Коэффициент
Десорбировано
динамическая
полная
Дисбаланс,
концентрация
очистки
железа(III),
обменная емкость
динамическая
мг∙мл-1 ионита
железа(III), г∙л-1
от железа(III)
мг∙мл-1 ионита
до проскока
обменная емкость
≤0.002
≥ 1450
24.6
33.0
34.2
1.2
растворов Al2(SO4)3 не требуется какой-либо кор-
о возможности многократного использования ионита
ректировки кислотности этих растворов. Десорбция
в циклах сорбции-десорбции.
железа(III) из иминодиацетатных ионитов не долж-
Поскольку в реальных растворах Al2(SO4)3 часть
на вызывать затруднения. Исходя из этого иониту
примеси железа может присутствовать в степени
MTS9300 и было отдано предпочтение.
окисления 2+, перед проведением очистки следует
Для оценки результатов, которые могут быть
предусмотреть операцию окисления железа(II) H2O2
достигнуты при удалении железа(III) из растворов
или персульфатом аммония.
Al2(SO4)3 при использовании иминодиацетатного
ионита MTS9300, были проведены эксперименты
Выводы
по сорбции-десорбции железа(III) в динамических
условиях. Исходный раствор представлял собой мо-
Установлено, что для эффективной сорбции желе-
дельный раствор сульфата алюминия с концентраци-
за(III) из раствора Al2(SO4)3 на фосфоновокислотном
ей Al2(SO4)3 184 г∙л-1, железа(III) 2.9 г∙л-1, что соот-
катионите необходимо предварительно подкислять
ветствует содержанию железа в Al2(SO4)3 1.58 мас%,
раствор до достижения в нем концентрации серной
и рН 2.3. После насыщения железом(III) ионит был
кислоты 2.2-2.5 моль∙л-1, в то время как иминодиаце-
промыт 5 уд. об. дистиллированной воды для отмыв-
татный ионит Purolite MTS9300 проявляет наиболее
ки от исходного раствора. Десорбция железа прове-
высокую избирательность к железу(III) при сорбции
дена 1 М раствором Н2SO4 (~100 г∙л-1).
из раствора Al2(SO4)3 с рН 2.2-2.6. Показано, что в
В ходе пропускания раствора Al2(SO4)3 через ио-
результате пропускания раствора Al2(SO4)3, содер-
нит MTS9300 происходило глубокое удаление при-
жащего 2.9 г∙л-1 железа(III), через колонку с ионитом
меси железа(III) (см. таблицу, рис. 3). Обработка ио-
Purolite MTS9300 концентрация железа(III) в первых
нита 1 М раствором Н2SO4 обеспечила практически
9 уд. об. пропущенного раствора уменьшается не
полную десорбцию железа(III), что свидетельствует
менее чем в
1450 раз. Сорбированное железо(III)
810
Блохин А. А. и др.
практически полностью элюируется из ионита 1 М
[2] Пат РФ 2480413 (опубл. 2013). Способ очистки от
раствором Н2SO4.
железа кислых растворов солей, содержащих нитрат
алюминия.
[3] Hu G., Wu Y., Chen D., Wang Y., Qi T., Wan L. Selective
Финансирование работы
removal of iron(III) from highly salted chloride acidic
Исследование выполнено за счет гранта Россий-
solutions by solvent extraction using di(2-ethylhexyl)
ского научного фонда (проект № 21-79-30029).
phosphate // Chem. Sci. Eng. 2021. V. 15. N 3. P. 528-
[4] Wang L., Wang Y., Cui L., Gao J., Guo Y., Cheng F. A
Конфликт интересов
sustainable approach for advanced removal of iron from
Авторы заявляют об отсутствии конфликта инте-
CFA sulfuric acid leach liquor by solvent extraction
ресов, требующего раскрытия в данной статье.
with P507 // Sep. Purif. Technol. 2020. V.251. ID
Информация об авторах
[5] Sun X., Sun Y., Yu J. Removal of ferric ions from
aluminum solutions by solvent extraction. Part I: Iron
Блохин Александр Андреевич, д.т.н., проф.,
removal // Sep. Purif. Technol. 2016. V.159. P. 18-22.
Мурашкин Юрий Васильевич, к.х.н., доцент,
[6] Пат. РФ 2453368 (опубл. 2012). Способ сорбционно-
го извлечения железа из растворов нитратных солей.
Михайленко Михаил Анатольевич, к.х.н., руково-
[7] Пат. РФ 2489353 (опубл. 2013). Способ очистки
дитель направления гидрометаллургии, представи-
солей алюминия от железа.
тельство Purolite Ltd в СНГ,
[8] Sole K. C., Mooiman M. B., Hardwick E. Ion exchange
in hydrometallurgical processing: An overview and
selected applications // Sep. Purif. Rev. 2017. V. 47.
N 2. P. 159-178.
Список литературы
[1] Лайнер Ю. А. Комплексная переработка алюминий-
содержащего сырья кислотными способами. М.:
Наука, 1982. С. 117-126.