Синтез фармацевтической субстанции основного сукцината висмута(III) высокой чистоты
857
Журнал прикладной химии. 2021. Т. 94. Вып. 7
УДК 542.06:661.887:661.743.2
СИНТЕЗ ФАРМАЦЕВТИЧЕСКОЙ СУБСТАНЦИИ
ОСНОВНОГО СУКЦИНАТА ВИСМУТА(III) ВЫСОКОЙ ЧИСТОТЫ
© Е. В. Тимакова1,2, Е. И. Бунькова1,2, Л. И. Афонина1,2,
Ю. М. Юхин1, В. А. Володин3,4
1 Институт химии твердого тела и механохимии СО РАН,
630128, г. Новосибирск, ул. Кутателадзе, д. 18
2 Новосибирский государственный технический университет,
630073, г. Новосибирск, пр. К. Маркса, д. 20
3 Институт физики полупроводников им. А. В. Ржанова СО РАН,
630090, г. Новосибирск, пр. Академика Лаврентьева, д. 13
4 Новосибирский государственный университет,
630090, г. Новосибирск, ул. Пирогова, д. 2
Е-mail: timakova@solid.nsc.ru
Поступила в Редакцию 21 апреля 2021 г.
После доработки 24 июня 2021 г.
Принята к публикации 7 июля 2021 г.
Для получения фармацевтической субстанции основного сукцината висмута состава С2Н4(СООBiO)2,
отвечающего требованиям высокой чистоты по содержанию примесных металлов, исследованы
процессы взаимодействия твердого тригидрата пентанитрата тригидроксо-пентаоксо-гексависму-
та(III) состава [Bi6O5(OH)3](NO3)5·3H2O и моноклинной модификации оксида висмута α-Bi2O3 с
раствором янтарной кислоты. Предложен способ получения основного сукцината висмута(III), вклю-
чающий стадии гидролитической переработки технологического азотнокислого раствора висмута с
получением высокочистого соединения состава [Bi6O5(OH)3](NO3)5·3H2O, его обработки раствором
NaOH с получением мелкокристаллического α-Bi2O3 и последующего взаимодействия оксида висмута
с раствором янтарной кислоты. Состав субстанции подтвержден методами рентгенофазового и
химического анализа, ИК- и КР-спектроскопии, термогравиметрии; определено содержание примес-
ных металлов атомно-абсорбционным методом.
Ключевые слова: фармацевтическая субстанция; янтарная кислота; оксонитрат висмута(III); оксид
висмута(III); основной сукцинат висмута(III); способ получения; примесные металлы
DOI: 10.31857/S0044461821070069
Соединения висмута с природными карбоновыми
эффективны также при лечении лейшманиоза [4].
кислотами, обладающими физиологической актив-
Янтарная (сукциновая) кислота и ее соли (сукцинаты)
ностью, имеют широкие перспективы применения
представляют собой универсальный внутриклеточ-
в медицинских целях в качестве фармацевтических
ный метаболит, широко участвующий в обменных
антимикробных субстанций [1, 2]. Препараты, содер-
реакциях в организме. Физиологическая значимость
жащие соли висмута с лимонной и салициловой кис-
янтарной кислоты в клеточном обмене обусловлена
лотами, применяются при лечении хеликобактерной
ее участием в цикле трикарбоновых кислот (цикл
инфекции в случае неэффективности эрадикационной
Кребса) и процессах окислительного фосфорилиро-
терапии первой линии [3]. В рамках терапии второй
вания [5].
линии среди рекомендованных висмутовых соедине-
Соли янтарной кислоты обычно получают в ре-
ний возможно использование и сукцината висмута.
зультате осаждения из растворов [6-8]. Так, сукцина-
Соли висмута с производными янтарной кислоты
ты редкоземельных металлов осаждаются при добав-
858
Тимакова Е. В. и др.
лении водного раствора сукцината натрия к растворам
лых растворов не удается достичь эффективной сте-
хлоридов или нитратов соответствующих металлов
пени очистки целевого продукта от сопутствующих
[6], сукцинат меди(II) можно получить при добавле-
металлов. Это связано с образованием тяжелыми
нии раствора натриевой соли в раствор сульфата меди
металлами нерастворимых соединений со многи-
[7]. Сукцинаты d-элементов высокой степени чисто-
ми органическими кислотами, входящими в состав
ты, применяемых в качестве биологически активных
висмутовых субстанций. Использование в качестве
веществ комплексного действия, получают добавле-
висмутсодержащих прекурсоров оксонитратов раз-
нием твердого водорастворимого сульфата соответ-
личного состава, получаемых путем гидролитиче-
ствующего d-металла в раствор сукцината натрия [8].
ской переработки висмутовых растворов, позволяет
Основная висмутовая соль янтарной кислоты яв-
решить эту проблему.
ляется фармацевтической субстанцией препаратов,
Цель работы — получение фармацевтической суб-
которые применяются в ряде стран для лечения ан-
станции основного сукцината висмута(III) высокой
гин, ларингитов и фарингитов. Субстанция имеет
чистоты и физико-химические исследования полу-
состав C4H4Bi2O6 и представляет собой белый по-
ченной субстанции.
рошок, нерастворимый в воде и 96%-ном этиловом
спирте, растворимый в разбавленной соляной кисло-
Экспериментальная часть
те; содержание висмута составляет 72.2-75.8 мас%.*
В России данная субстанция не зарегистрирована,
Для приготовления раствора висмута использо-
так же как и препараты на ее основе. Литературные
вали Bi2O3 квалификации ч., а также металлический
данные относительно способов получения и физи-
висмут марки Ви 1, ГОСТ 10928-90 (ТОО «Казцинк»)
ко-химических исследований основного сукцината
с содержанием висмута 98.3%. В работе использовали
висмута отсутствуют. Это делает актуальным разра-
янтарную кислоту (х.ч., ООО «Компонент-Реактив»,
ботку способов получения данного соединения с воз-
а также HNO3 (х.ч., ООО «Технологическая лабора-
можностью организации его производства в России.
тория Гиредмет») и NaOH (ч.д.а., ООО «Компонент-
К лекарственным препаратам предъявляются вы-
Реактив»). Для приготовления раствора (NH4)2CO3
сокие требования по качеству, среди которых осо-
использовали аммиак водный (х.ч., ООО «Компонент-
бое место занимает чистота продукта. Для висмут-
Реактив») и NH4HCO3 (х.ч., КАО «Азот»).
содержащих субстанций чистота в первую очередь
Исходный раствор нитрата висмута (420 г·л-1 Bi3+,
определяется содержанием нитрат-ионов и примесей
100 г·л-1 свободной HNO3) готовили растворением
сопутствующих висмуту металлов, таких как свинец,
оксида висмута в азотной кислоте концентрацией
серебро, железо, медь и цинк, и зависит от способов
7 моль·л-1. Гидролитическое осаждение висмута из
получения.
растворов минеральных кислот, а также исследование
Содержание нитрат-ионов в висмутовых субстан-
процессов твердый прекурсор-раствор проводили во
циях не должно превышать 0.4%, поскольку образу-
фторопластовых или стеклянных сосудах, снабжен-
ющаяся в желудке из нитрат-ионов азотная кислота
ных мешалками, термостатирование которых осу-
способна оказывать негативное воздействие, а полу-
ществляли на водяных банях.
чающиеся из нее в результате окислительно-восста-
Гидрат гексанитрат тетрагидроксо-тетраоксо-гек-
новительных реакций нитрит-ионы и их производные
сависмута(III) состава [Bi6O4(OH)4](NO3)6·H2O полу-
обладают канцерогенным действием, которому также
чали разбавлением 50 мл раствора нитрата висмута
способствует присутствие тяжелых металлов [9].
нагретой до 60°С дистиллированной водой объемом
Процесс получения соединений висмута для тех-
950 мл при перемешивании смеси в течение 30 мин
ники и медицины связан с гидролитической перера-
при температуре 60-70°С. Маточный раствор сливали
боткой азотнокислых растворов висмута, поскольку
декантацией, осадок отфильтровывали. Тригидрат
HNO3 является лучшим растворителем металличе-
пентанитрат тригидроксо-пентаоксо-гексависму-
ского висмута и его сплавов. Осаждение соединений
та(III) состава [Bi6O5(OH)3](NO3)5·3H2O получали
проводят разбавлением висмутсодержащих растворов
двукратной промывкой [Bi6O4(OH)4](NO3)6·H2O ди-
водой или добавлением к ним органических кислот
стиллированной водой при температуре 60 ± 2°С.
и их солей. В наших ранних работах показано, что в
Осадок отфильтровывали и сушили на воздухе.
результате получения фармацевтических субстанций
Для получения оксида висмута использовали сле-
висмута осаждением из технологических азотнокис-
дующие способы:
1) 50 мл исходного раствора нитрата висмута при
* Pharmacopee Francaise. Bismuth (sous-succinate de).
перемешивании добавляли постепенно к раствору
Синтез фармацевтической субстанции основного сукцината висмута(III) высокой чистоты
859
NaOH (2 моль·л-1) объемом 220 мл, рН раствора под-
плексе STA 449 F1 Jupiter (Netzsch) в динамическом
держивали равным 12;
режиме при нагревании в атмосфере Ar/O2 (80/20;
2) 14 г [Bi6O5(OH)3](NO3)5∙3H2O при перемеши-
O2 — 10 мл·мин-1; Ar — 40 мл·мин-1). Навески мас-
вании добавляли к 30 мл 2 моль·л-1 раствора NaOH
сой 180-200 мг помещали в тигли из сплава Pt-10%
при температуре 22 ± 2°С, pH 12.
Rh и нагревали со скоростью 10 град·мин-1 до 350-
Синтезы проводили в течение 1 ч. Полученный
500°С. Масс-спектры газообразных продуктов, обра-
осадок желтого цвета отфильтровывали, промывали
зующихся в процессе термообработки, записывали в
дистиллированной водой до нейтральной реакции
режиме мультиионного детектирования для m/z, рав-
рН среды по универсальной индикаторной бумаге,
ных 18 и 44, с помощью квадрупольного масс-спек-
отфильтровывали и сушили на воздухе. Для получе-
трометра QMS 403D (Netzsch). Исследование образ-
ния основного сукцината висмута навеску янтарной
цов методом растровой электронной микроскопии
кислоты массой 1.5-2.5 г растворяли в 50 мл дистил-
(РЭМ) проводили с использованием сканирующего
лированной воды при перемешивании. К полученно-
электронного микроскопа Hitachi TM 1000.
му раствору при температуре синтеза 70°С добавляли
5 г α-Bi2O3 и перемешивали смесь в течение 1 ч.
Обсуждение результатов
Предварительно проведенные исследования с исполь-
зованием рентгенофазового и химического анализов
Процесс получения лекарственной субстанции
показали, что для образования основного сукцината
основного сукцината висмута осуществляли при ис-
висмута достаточно 1 ч. Полученный осадок отфиль-
пользовании в качестве исходного сырья металличе-
тровывали, промывали дистиллированной водой и
ского висмута. Процесс получения целесообразно
сушили на воздухе.
представить в виде следующих основных стадий:
Определение макроколичеств Bi(III) в раство-
1) окисление металлического висмута до оксида;
рах проводили титрованием раствором комплек-
2) приготовление висмутсодержащего раствора
сона III с индикатором ксиленоловым оранжевым.
путем растворения технического Bi2O3 в азотной
Микроколичества висмута определяли фотоколо-
кислоте;
риметрически с иодидом натрия.* Содержание
3) очистка висмута от примесных металлов при
углерода и водорода в синтезированных образцах
гидролитическом осаждении в виде соединения со-
определяли модифицированным методом Прегля с
става [Bi6O5(OH)3](NO3)5·3H2O;
гравиметрическим окончанием анализа. Определение
4) получение субстанции основного сукцината
содержания примесных металлов осуществляли атом-
висмута взаимодействием твердого висмутсодержа-
но-абсорбционным методом на спектрофотометре
щего прекурсора с раствором янтарной кислоты.
Varian AA 280FS.
В производстве соединений висмута обычно ис-
Для определения фазового состава образцов
пользуют азотнокислые растворы, которые получают
использовали метод рентгеновской дифракции.
растворением гранул металла в HNO3 концентрацией
Рентгенограммы образцов регистрировали на диф-
7-9 моль·л-1. Использование для этих целей Bi2O3
рактометре Bruker D8 Advance в геометрии Брэгга-
является более экологически оправданным. В этом
Брентано с характеристичным излучением СuKα
случае удается сократить расход азотной кислоты, не-
в диапазоне углов 4° < 2θ < 70° с шагом 0.02°.
обходимой для приготовления раствора, и устранить
Интерпретацию полученных данных РФА проводи-
выделение в атмосферу токсичных оксидов азота
ли с помощью базы данных ICDD PDF-4 (2011 г.).
[10].
Инфракрасные спектры поглощения в средней ИК-
На первой стадии процесса проводят окисление
области (4000-400 см-1) записывали на ИК-Фурье-
металлического висмута марки Ви 1 кислородом
спектрометре Scimitar FTS 2000 (Digilab), образцы
воздуха при введении в расплав при 320°С оксида
готовили в виде таблеток с прокаленным KВr. КР-
висмута (20 мас%) с последующим повышением тем-
спектры снимали на спектрометре T64000 (Horiba
пературы до 600°С [11]. Далее полученный Bi2O3
Jobin Yvon) с Ar+ лазером [длина волны 514.5 нм,
технической чистоты растворяют в азотной кислоте
геометрия Z(XY)-Z]. Термический анализ образцов
концентрацией 7 моль·л-1 для приготовления тех-
проводили на синхронном термоаналитическом ком-
нологического висмутсодержащего азотнокислого
раствора. Основная задача следующего этапа — про-
ведение глубокой очистки висмута от примесных
* Коростелев П. П. Фотометрический и комплексоме-
металлов, содержащихся в технологическом растворе,
трический анализ в металлургии. М.: Металлургия, 1984.
С. 41-45, С. 221-224.
в результате гидролитического его осаждения.
860
Тимакова Е. В. и др.
Ранее показано [10], что высокие значения коэф-
Учитывая, что в результате взаимодействия про-
фициентов очистки висмута от примесных металлов
исходит существенное подкисление среды за счет
достигаются при гидролизе азотнокислых растворов.
образования HNO3, реакцию (2) можно представить
Это делает возможным широко использовать данный
в виде последовательности следующих стадий:
процесс для синтеза соединений висмута высокой
[Bi6O5(OH)3](NO3)5∙3H2Oтв + 13Н+ =
чистоты, в том числе и используемых в медицине.
(3)
= 6Bi3+ + 5NO3- + 11Н2О,
Гидролиз при повышенной температуре не менее
60°С позволяет получать легко фильтруемый осадок
2Bi3+ + Н2О + С2Н4(СОО-)2 =
состава [Bi6O4(OH)4](NO3)6·H2O и эффективно его
(4)
= С2Н4(СООBiO)2
+ 2Н+ .
отделять от раствора, содержащего ионы примесных
металлов.
Возможность образования основного сукцината
Осаждаемый при этом моногидрат гексанитрат
висмута в системе определяется существенно бо-
тетрагидроксо-тетраоксо-гексависмута(III) состава
лее низкой растворимостью этой соли по сравне-
[Bi6O4(OH)4](NO3)6·H2O представляет собой хорошо
нию с [Bi6O5(OH)3](NO3)5·3H2O. Так, при обработке
окристаллизованные сростки короткопризматиче-
[Bi6O5(OH)3](NO3)5·3H2O водой при температуре
ских кристаллов с наибольшим размером единичного
25°С концентрация висмута в растворе составля-
кристалла в базисной плоскости 10-30 мкм, а по тол-
ет 1.09 г·л-1, а при обработке С2Н4(СООBiO)2 —
щине 10-20 мкм (рис. 1, а). В результате промывки
1.68·10-6 г·л-1.
данного соединения водой происходит гидролитиче-
Однако проведенные исследования показали, что
ское разложение с образованием тригидрата пентани-
в рассматриваемой системе эффективного обмена
трата тригидроксо-пентаоксо-гексависмута(III) (да-
нитрат-ионов на анионы янтарной кислоты не про-
лее оксонитрата) состава [Bi6O5(OH)3](NO3)5·3H2O,
исходит. Согласно данным рентгенофазового анализа
представляющего собой удлиненно-призматические
(рис. 2, 1 и 4), образцы, полученные после обработки
кристаллы длиной в базисной плоскости 10-40 мкм,
в течение 1-3 ч твердого [Bi6O5(OH)3](NO3)5·3H2O
шириной 5-20 мкм и толщиной 1-5 мкм (рис. 1, б),
раствором янтарной кислоты, представляют собой
по реакции
смесь основного сукцината висмута и исходного пре-
курсора. Кроме того, в указанных условиях до 5%
[Bi6O4(OH)4](NO3)6·H2O + 2H2O =
(1)
висмута в виде катионов переходит в маточный рас-
= [Bi6O5(OH)3](NO3)5·3H2O + Н+ + NO3- .
твор вследствие повышения кислотности последнего
в результате образования азотной кислоты [уравне-
В результате перекристаллизации удается осу-
ние (2)]. Таким образом, не удается количественно
ществить эффективную очистку конечного про-
провести реакцию обмена и получить продукт, не
дукта от примесных металлов, захваченных в объ-
содержащий нитрат-ионы.
ем микрокристаллов в ходе осаждения первичного
Для получения фармацевтической субстанции ос-
продукта гидролиза. Оксонитрат висмута состава
новного сукцината висмута, не содержащего примесь
[Bi6O5(OH)3](NO3)5·3H2O является высокочистым
нитрат-ионов, целесообразно рассмотреть систему
продуктом гидролитической переработки и может
твердый α-Bi2O3-раствор янтарной кислоты. Оксид
быть использован в качестве прекурсора в синтезе
висмута моноклинной модификации α-Bi2O3, исполь-
соединений висмута высокой чистоты, в том числе
зуемый для обработки раствором янтарной кислоты,
для фармацевтической промышленности.
можно получить путем термического разложения
Показано, что при обработке полученного на пре-
[Bi6O5(OH)3](NO3)5·3H2O при 600°С, а также при его
дыдущей стадии твердого [Bi6O5(OH)3](NO3)5·3H2O
обработке раствором NaOH согласно реакциям [10]
раствором янтарной кислоты при молярном отно-
шении сукцинат-ионов к висмуту, равном 0.6-1.0,
[Bi6O5(OH)3](NO3)5∙3H2Oтв =
(5)
и температуре процесса 60-80°С удается получить
= 3Bi2O3 + 2.5N2O5 + 4.5Н2О,
субстанцию основного сукцината висмута состава
С2Н4(СООBiO)2. Процесс взаимодействия можно
[Bi6O5(OH)3](NO3)5∙3H2Oтв + 5NaOHр-р =
(6)
представить в виде реакции
= 3Bi2O3 + 5NaNO3 + 7Н2О .
[Bi6O5(OH)3](NO3)5∙3H2Oтв +
Термическое разложение [Bi6O5(OH)3](NO3)5×
+ 3С2Н4(СООH)2р-р =
(2)
×3H2O сопровождается выделением в атмосферу ток-
= 3С2Н4(СООBiO)2
+ 5HNO3р-р + 5H2O.
сичных оксидов азота, требует дополнительных энер-
Синтез фармацевтической субстанции основного сукцината висмута(III) высокой чистоты
861
Рис. 1. Микрофотографии [Bi6O4(OH)4](NO3)6·H2O (а), [Bi6O5(OH)3](NO3)5∙3H2O (б), образцов α-Bi2O3 после
щелочной обработки [Bi6O5(OH)3](NO3)5∙3H2O (в) и Varistor grade (HEК) (д); основных сукцинатов висмута (г, е),
синтезированных из образцов в и д соответственно.
гетических затрат вследствие высокой температуры
водой без дополнительного высушивания может быть
прокаливания, а Bi2O3 формируется в виде крупных
сразу использован на следующей стадии процесса.
оплавленных зерен, сохраняющих форму и разме-
Согласно данным рентгенофазового анализа (рис. 2, 1
ры частиц исходного оксонитрата, что существенно
и 2), образец, полученный в результате щелочной
уменьшает его реакционную способность. Наиболее
обработки соединения [Bi6O5(OH)3](NO3)5·3H2O
технологичным способом для получения α-Bi2O3
(ICDD 000-48-0575), представляет собой монофазный
является щелочное разложение оксонитрата висмута,
α-Bi2O3 (ICDD 040-03-2034).
которое осуществляется при температуре 25 ± 2°С.
При обработке α-Bi2O3 раствором янтарной кис-
В этом случае оксид висмута после отделения от
лоты при молярном отношении сукцинат-ионов к
маточного раствора и промывки дистиллированной
висмуту, равном 0.6-1.0, и температуре процесса
862
Тимакова Е. В. и др.
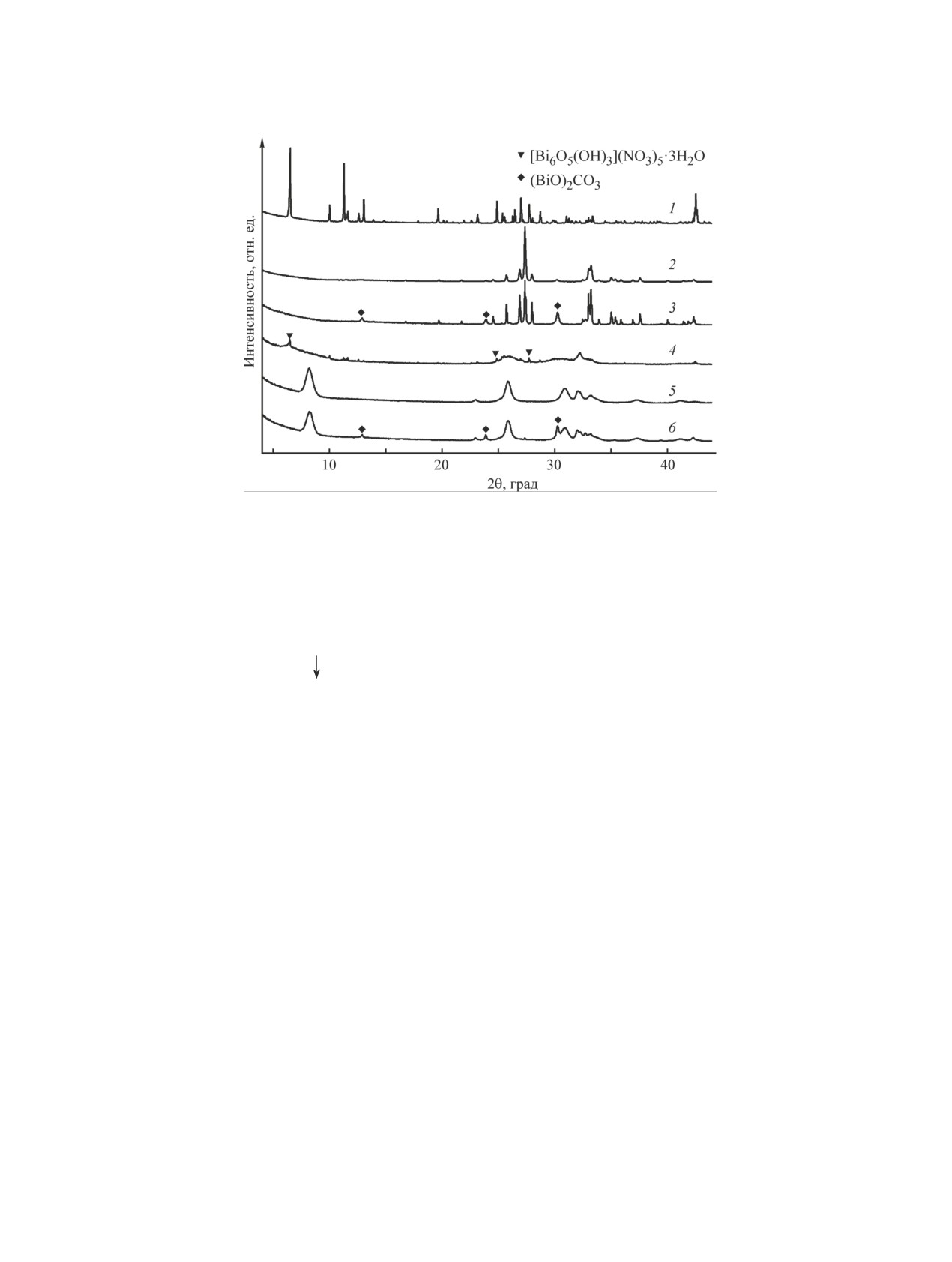
Рис. 2. Рентгенограммы [Bi6O5(OH)3](NO3)5∙3H2O (1), образцов α-Bi2O3 после щелочной обработки
[Bi6O5(OH)3](NO3)5∙3H2O (2), Varistor grade (HEK) (3) и основных сукцинатов висмута (4-6), синтезированных из
образцов 1-3 соответственно.
60-80°С в течение 1 ч образуется основной сукцинат
Для сокращения числа стадий в процессе полу-
висмута:
чения основного сукцината висмута проверена воз-
можность непосредственной обработки растворами
Bi2O3 + С2Н4(СООH)2р-р =
янтарной кислоты высокочистых промышленных
(7)
= С2Н4(СООBiO)2
+ Н2О.
образцов α-Bi2O3. Использование в качестве пре-
курсора промышленного образца оксида висмута
Данные рентгенофазового анализа подтвер-
(Varistor grade) показало, что после его обработки
ждают образование целевого продукта (рис. 2, 5):
раствором янтарной кислоты при молярном отноше-
на рентгенограмме отсутствуют дифракционные
нии сукцинат-ионов к висмуту, равном 0.6-1.0, и тем-
максимумы α-Bi2O3 (ICDD 040-03-2034) и янтар-
пературе 70°С в течение 1-5 ч полученные образцы,
ной кислоты (ICDD 000-31-1899). Данные химиче-
по данным рентгенофазового анализа, представляют
ского анализа также свидетельствуют об образова-
собой смесь основного сукцината и оксокарбона-
нии С2Н4(СООBiO)2, содержание (%): Bi — 72.9
та висмута (ICDD 000-41-1488) (рис. 2, 6). Многие
(расч. 73.85), C — 8.30 (8.48), Н — 0.65 (0.71). Следует
промышленные образцы оксида висмута в резуль-
отметить, что увеличение в реакционной смеси мо-
тате хемосорбции CO2 содержат в качестве примеси
лярного отношения сукцинат-ионов к висмуту до 5
(BiO)2CO3, который не взаимодействует с янтарной
не меняет состава продукта, и единственным продук-
кислотой. Образец, используемый нами, также содер-
том реакции остается основной сукцинат висмута.
жит в качестве примеси (BiO)2CO3 (рис. 2, 3). Таким
Согласно данным электронной микроскопии, при
образом, при непосредственном использовании про-
обработке [Bi6O5(OH)3](NO3)5∙3H2O раствором NaOH
мышленных образцов Bi2O3 в схеме производства
образуется мелкокристаллический порошок Bi2O3 в
висмутовых солей необходимо предусматривать ста-
виде рыхлых конгломератов, составленных из удли-
дию их предварительной термической обработки на
ненных плоскопризматических игольчатых кристал-
воздухе при температуре 400-500°C с целью разло-
лов с преобладающим размером в базисной плоско-
жения примеси оксокарбоната висмута до оксида.
сти до 10 мкм и толщиной 0.5-1 мкм (рис. 1, в). Его
Отметим, что в сравнении с металлическим висмутом
обработка раствором янтарной кислоты приводит
технической чистоты, который обычно используется
к образованию основного сукцината висмута. Это
в качестве исходного сырья в процессе получения
агрегаты сферических частиц размером 5-20 мкм, со-
соединений висмута, использование высокочистых
стоящих из тонких игольчатых кристаллов размером
образцов Bi2O3 существенно увеличивает конечную
не более 2-3 мкм (рис. 1, г).
стоимость целевого продукта. Используемый нами
Синтез фармацевтической субстанции основного сукцината висмута(III) высокой чистоты
863
промышленный образец α-Bi2O3 состоит из сферо-
бания в виде полосы большей интенсивности — при
литоподобных частиц размером 1-3 мкм (рис. 1, д).
1445 см-1. Разницы ∆ν(СОО-) = νаs(СОО-) - νs(СОО-)
После обработки оксида раствором янтарной кислоты
из ИК-спектра составляют 100, 140 и 150 см-1, что в
основной сукцинат висмута также образуется в виде
сравнении с данной величиной для натриевой соли
агрегатов сферических частиц (рис. 1, е).
[16] указывает преимущественно на бидентатную и
Анализ ИК- и КР-спектров основного сукцината
бидентатно-мостиковую координацию сукцинат-иона
висмута позволяет сделать выводы о координации
[17].
аниона янтарной кислоты катионами висмута и дру-
В спектрах основного сукцината висмута также
гих особенностях строения соединения. Отнесение
отсутствуют колебания δ(ОН)СООН, при этом поло-
характеристических полос в спектрах проводили пу-
са средней интенсивности в ИК-спектре соли при
тем сравнения со спектрами янтарной кислоты [12,
660 см-1 относится к деформационным колебаниям
13] и сукцинатов других металлов [14-16]. В ИК- и
карбоксилат-иона δ(СОО-). В области 1470-1400 см-1
КР-спектрах янтарной кислоты наблюдается ряд ха-
плоским деформационным колебаниям (ножнич-
рактеристических полос, которые не регистрируют-
ным) δ(СН2) соответствуют полосы при 1423 (ИК)
ся в спектрах основного сукцината висмута. Так, в
и 1430 см-1 (КР), полоса средней интенсивности при
спектрах соли не наблюдаются валентные колебания
1372 см-1 относится к веерным колебаниям ω(СН2),
ν(С О) карбонильной группы, что свидетельствует о
указанные колебания также проявляются в спектрах
координации янтарной кислоты с катионами висмута
кислоты. Колебание ν(С—С) активно как в спектрах
через карбоксильные группы. Таким образом, в рас-
кислоты, так и в ИК- и КР-спектрах соли при 926 и
сматриваемом соединении остатки янтарной кислоты
951 см-1 соответственно.
дважды депротонированы, о чем также свидетель-
Наличие широкой полосы средней интенсивно-
ствуют характеристические интенсивные полосы ко-
сти в ИК-спектре основного сукцината висмута при
лебаний карбоксилат-ионов: асимметричные валент-
524 см-1 в области валентных колебаний связи Bi—O
ные колебания νаs(СОО-) проявляются в ИК-спектре в
также подтверждает замещение протонов янтарной
виде интенсивной полосы с двумя максимумами при
кислоты на висмутсодержащие катионы и свиде-
1550 и 1540 см-1, плечом при 1500 см-1; симметрич-
тельствует о равноценности образуемых связей, в
ные νs(СОО-) валентные колебания — также в виде
КР-спектрах соли данные связи проявляются в виде
сильной полосы несколько меньшей интенсивно-
слабого плеча.
сти при 1400 см-1 (рис. 3, 1), интенсивность полос в
Отсутствие полос валентных О—Н-колебаний
КР-спектре соли, как и следует ожидать, перераспре-
воды (3700-3000 см-1), а также деформационных
деляется (рис. 3, 2). Асимметричные валентные коле-
колебаний воды (~1640 см-1) в ИК-спектре основного
бания νаs(СОО-) проявляются в виде полос средней
сукцината висмута свидетельствует о ее отсутствии в
интенсивности при 1575 и 1555 см-1, с плечом при
составе соединения, что также подтверждают данные
1540 см-1; симметричные νs(СОО-) валентные коле-
термического анализа (рис. 4).
Рис. 3. ИК- (1) и КР- (2) спектры поглощения основного сукцината висмута.
864
Тимакова Е. В. и др.
По результатам проведенных исследований раз-
работан способ получения основного сукцината
висмута [20] и проведены укрупненные лабораторные
испытания на примере переработки 1.0 кг металличе-
ского висмута марки Ви 1, содержащего (%): висму-
та — 98.3, свинца — 1.43, серебра — 5.6·10-2, ме-
ди — 9.5·10-3, железа — 6.2·10-3, цинка — 6.4·10-4,
олова — 1.0·10-3, сурьмы — 1.6·10-3. Гранулы метал-
лического висмута растворяли при перемешивании
в 2.5 л HNO3 концентрацией 7.0 моль·л-1 в тече-
ние 3 ч и получили 2.35 л раствора с концентрацией
Bi3+ 418 г·л-1. После фильтрации раствор разбавляли
(1:1) дистиллированной водой, нагревали до темпе-
ратуры 70°С, а затем добавлением к нему раствора
(NH4)2CO3 концентрацией 2.5 моль·л-1 доводили
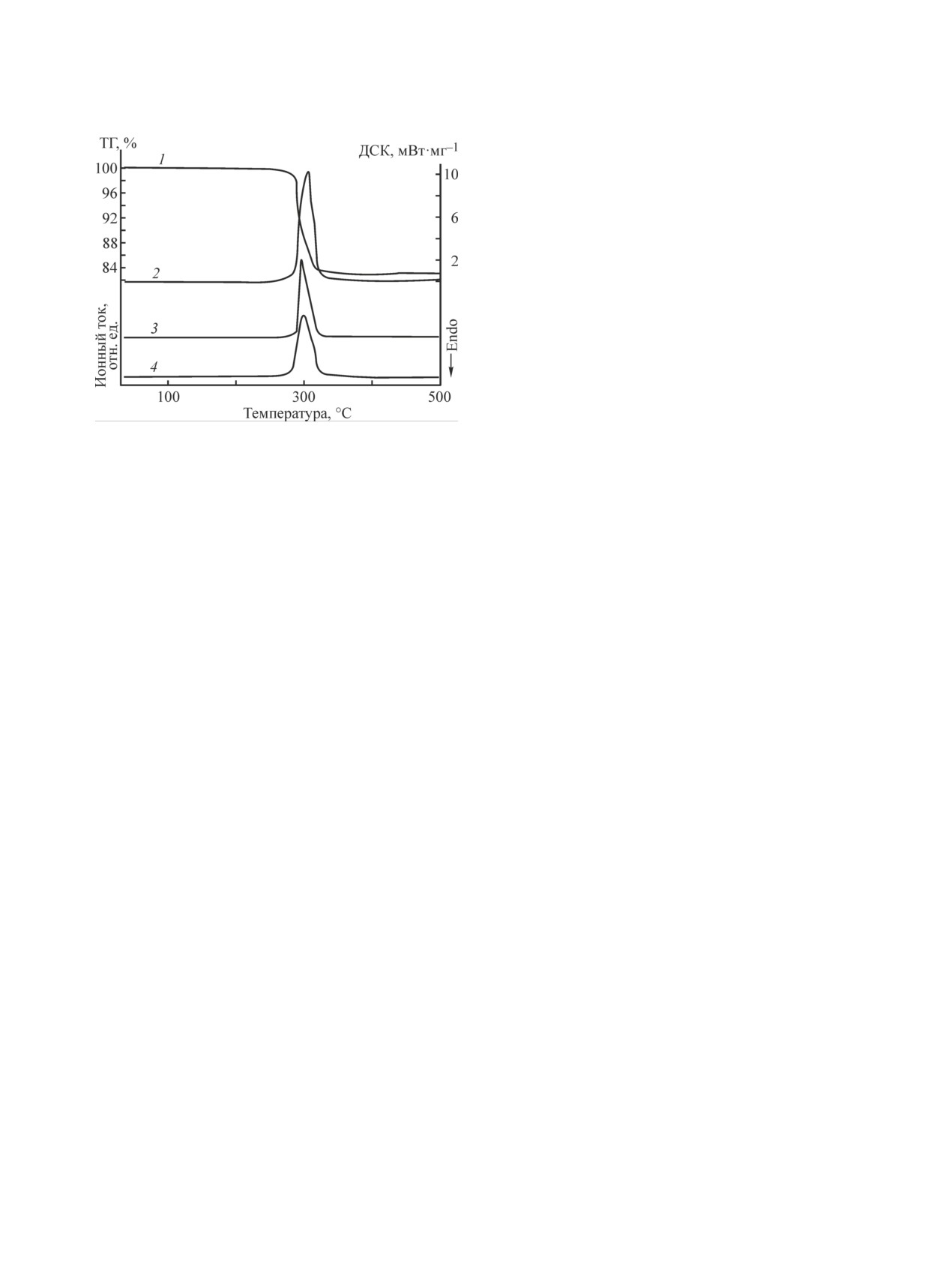
Рис. 4. Кривые термогравиметрии (1), дифференциаль-
рН смеси до 1. Пульпу перемешивали 30 мин при
но-сканирующей калориметрии (2) основного сукцината
температуре не ниже 60°С и давали отстояться в те-
висмута состава C2H4(COOBiO)2 и масс-спектры выде-
чение 1 ч. Результаты химического анализа отфиль-
ляющихся газов: Н2О (3) и СО2 (4).
трованного и высушенного образца осадка состава
[Bi6O4(OH)4](NO3)6·H2O свидетельствуют о том, что
Процесс окислительного термолиза основного
он содержит (%): висмута — 70.3, нитрат-ионов —
сукцината висмута не имеет каких-либо особен-
20.4, свинца — 5.4·10-3, серебра — 3.2·10-4, ме-
ностей в сравнении с термолизом безводных сук-
ди — 3.0·10-3, железа — 3.2·10-3, цинка — 4.0·10-4,
цинатов других металлов [16], происходит за одну
олова — 5.0·10-4, сурьмы — 6.0·10-4. Осадок
стадию, которая связана с разложением исходного со-
[Bi6O4(OH)4](NO3)6·H2O отделяли от маточника де-
единения до соответствующего оксида. Термическая
кантацией и двукратно промывали 6.0 л дистиллиро-
устойчивость C2H4(COOBiO)2 находится в линей-
ванной воды при температуре 60 ± 2°С. Образец осадка
ной зависимости от энтальпии образования оксида
промытого водой имеет состав [Bi6O5(OH)3](NO3)5×
(∆fH°(Bi2O3) = -577.8 кДж∙моль-1 [18]) в ряду метал-
×3H2O и по результатам анализа содержит (%):
лов главных подгрупп [19]. По данным термического
висмута — 71.3, нитрат-ионов — 17.4, свинца —
анализа (рис. 4), процесс окислительного термолиза
4.2·10-4, серебра — 1.5·10-4, меди — 5.0·10-4, желе-
С2Н4(СООBiO)2 протекает в интервале температур
за — 1.0·10-3, цинка — 1.0·10-4, олова — 2.0·10-4,
275-310°С и сопровождается экзоэффектом с мак-
сурьмы — 3.0·10-4. Промытый осадок висмута ни-
симумом при 305°С, соответствующим разложению
трата основного состава [Bi6O5(OH)3](NO3)5∙3H2O
органической составляющей. По данным масс-спек-
в количестве 1.38 кг обрабатывали при температу-
трометрии, в газовой фазе регистрируется наличие
ре 22 ± 2°С 3.25 л раствора NaOH концентрацией
углекислого газа (m/z = 44) и воды (m/z = 18). Потеря
2 моль·л-1 в течение 4 ч (молярное отношение ги-
массы, рассчитанная по ТГ-кривым, в соответствии
дроксида натрия к висмуту равно 1.4). После двукрат-
с уравнением (8) разложения основного сукцината
ной промывки в течение 30 мин 6.0 л дистиллирован-
висмута до оксида, составляет 17.3% (теор. 17.7%):
ной воды, нагретой до 60°С, осадок висмута оксида
состава Bi2O3 (содержание нитрат-ионов — 0.14%)
С2Н4(СООBiO)2 + 3.5O2 = Bi2O3 + 4СO2 + 2Н2О . (8)
отфильтровывали и переводили в висмута сукцинат
основной обработкой 10 л раствора янтарной кис-
Показано, что выдерживание образцов основного
лоты концентрацией 0.35 моль·л-1 при перемешива-
сукцината висмута при температуре 200°С в тече-
нии в течение 4 ч при температуре 70 ± 2°С (моляр-
ние 4 ч на воздухе, согласно данным РФА, не приво-
ное отношение янтарной кислоты к висмуту равно
дит к их заметному разложению, а при температуре
0.75). Осадок висмута сукцината основного состава
280°С за это же время образцы подвергаются полно-
C2H4(COOBiO)2 промывали двукратно 6.0 л дистил-
му окислительному термолизу с образованием α- и
лированной воды при температуре 60 ± 2°С в течение
β-Bi2O3. Таким образом, сушку готового продукта
30 мин, после чего сушили при температуре 100 ± 5°С
C2H4(COOBiO)2 можно проводить при температуре
в течение 4 ч. В результате испытаний получено
100-150°С в течение 2-4 ч.
1.30 кг висмута сукцината основного, содержащего
Синтез фармацевтической субстанции основного сукцината висмута(III) высокой чистоты
865
(%): висмута — 73.8, свинца — 1.0·10-4, серебра —
все синтезы веществ, провела сбор данных литера-
5.0·10-5, меди — 2.0·10-4, железа — 5.0·10-4, цин-
туры и оформила литературный обзор, участвовала
ка — 8.0·10-5, олова — 1.0·10-4, сурьмы — 1.0·10-4,
в написании текста статьи; Л. И. Афонина прове-
нитрат-ионов — ˂0.02. Прямое извлечение висмута в
ла исследования химического состава полученных
продукт из металлического висмута составило 97.6%.
образцов, участвовала в обработке и интерпрета-
Висмут(III) из маточных и промывных растворов
ции результатов работы, написании текста статьи;
концентрацией 1.1 г·л-1 доосаждали при рН 3 до кон-
Ю. М. Юхин консультировал по планированию и
центрации 0.005 г·л-1. Полученный при этом осадок
руководил проведением укрупненных лабораторных
можно направить на стадию приготовления исходного
испытаний, участвовал в интерпретации полученных
раствора нитрата висмута.
результатов, внес основной вклад в написание разде-
ла о способе получения основного сукцината висму-
та; В. А. Володин провел исследования образцов
Выводы
методами спектроскопии комбинационного рассеяния
Проведенные исследования показали, что фар-
и ИК, осуществил интерпретацию полученных спек-
мацевтическую субстанцию основного сукцината
троскопических данных.
висмута состава С2Н4(СООBiO)2 целесообразно по-
лучать путем обработки моноклинной модификации
Информация об авторах
α-Bi2O3 раствором янтарной кислоты при молярном
Тимакова Евгения Владимировна, к.х.н., доц.,
отношении сукцинат-ионов к висмуту, равном 0.6-1.0,
и температуре процесса 60-80°С. Экологически безо-
Бунькова Екатерина Игоревна,
пасным способом получения фармацевтической суб-
станции С2Н4(СООBiO)2 высокой степени очистки от
Афонина Любовь Игоревна, к.х.н.,
примесных металлов и нитрат-ионов является обра-
ботка раствором янтарной кислоты α-Bi2O3, получен-
ного при взаимодействии [Bi6O5(OH)3](NO3)5∙3H2O
Юхин Юрий Михайлович, д.х.н., проф.,
с раствором NaOH.
Володин Владимир Алексеевич, д.ф.-м.н., доц.,
Финансирование работы
Работа выполнена в соответствии с тематическим
Список литературы
планом Института химии твердого тела и механо-
[1] Yang Y., Ouyang R., Xu L., Guo N., Li W., Feng K.,
химии СО РАН 121032500064-8 и Новосибирского
Ouyang L., Yang Z., Zhou S., Miao Y. Bismuth
государственного технического университета
complexes: Synthesis and applications in biomedicine
ТП-ХХТ-1_21.
// J. Coord. Chem. 2015. V. 68. N 3. P. 379-397.
[2] Wang R., Li H., Ka-Yan Ip T., Sun H. Bismuth drugs as
Конфликт интересов
antimicrobial agents //Adv. Inorg. Chem. 2020. V. 75.
Авторы заявляют об отсутствии конфликта инте-
P. 183-205.
ресов, требующего раскрытия в данной статье.
[3] Dore M. P., Lu H., Graham D. Y. Role of bismuth in
improving Helicobacter pylori eradication with triple
Благодарности
therapy //Gut. 2016. V. 65. N 5. P. 870-878.
Авторы выражают благодарность ЦКП «ВТАН»
[4] Loh A., Ching Ong Y., Blair V. L. Kedzierski L.,
НГУ за предоставленное оборудование для регистра-
Andrews P. C. Bismuth (III) α-hydroxy carboxylates:
ции спектров комбинационного рассеяния света.
Highly selective toxicity of glycolates towards
Leishmania major // J. Biol. Inorg. Chem. 2015. V. 20.
P. 1193-1203.
Информация о вкладе авторов
Е. В. Тимакова разработала концепцию работы,
[5] Murphy M. P., OʹNeill L. A. J. Krebs cycle reimagined:
методику эксперимента, осуществила сбор, анализ
The emerging roles of succinate and itaconate as signal
и интерпретацию результатов работы, участвовала в
transducers //Cell. 2018. V. 174. N 4. P. 780-784.
написании текста статьи; Е. И. Бунькова выполнила
866
Тимакова Е. В. и др.
[6]
Manna S. C., Zangrando E., Bencini A., Benelli C.,
lead succinate: A promising NLO material // J. Cryst.
Chaudhuri N. R. Syntheses, crystal structures, and
Growth. 2011. V. 319. P. 96-101.
magnetic properties of [LnIII2(Succinate)3(H2O)2]×
×0.5H2O [Ln = Pr, Nd, Sm, Eu, Gd, and Dy].
[15]
Arankumar A., Ramasamy P., Vishnu K., Jayaray M. K.
Polymeric networks: Unusual ferromagnetic coupling
Growth, structural, thermal, optical, and electrical
in Gd derivative // Inorg. Chem. 2006. V. 45. N 22.
properties of potassium succinate-succinic acid crystal
// J. Mater. Sci. 2014. V. 49. P. 3598-3607.
[7]
Karthik A. D., Geetha K. Synthesis of copper precursor,
copper and its oxide nanoparticles by green chemical
[16]
Caires F. J., Lima L. S., Carvalho C. T., Ionashiro M.
reduction method and its antimicrobial activity //J.
Thermal behaviour of succinic acid, sodium succinate
Appl. Pharm. Sci. 2013. V. 3. N 5. P. 16-21.
and its compounds with some bivalent transition metal
ions // Thermochim. Acta. 2010. V. 500. P. 6-12.
[8]
Пат. РФ 2174508 (опубл. 2001). Способ получения
сукцинатов d-металлов [Pat. RU 2174508 (publ.
[17]
Deacon G. B., Phillips R. J. Relationships between the
2001). Method of preparing d-element succinate].
carbon-oxygen stretching frequencies of carboxylato
[9]
Галачиев С. М., Макоева Л. М., Джиоев Ф. К.,
complexes and the type of carboxylate coordination //
Хаева Л. Х. Возможности эндогенного образова-
Coord. Chem. Rev. 1980. V. 33. P. 227-250.
ния нитрозаминов в желудочном соке in vitro //
Изв. Самарского НЦ РАН. 2011. Т. 13. № 1 (7).
[18]
Мацкевич Н. И., Семерикова А. Н., Гельфонд Н. В.,
С. 1678-1680.
Мацкевич М. Ю., Ткачев Е. Н., Ануфриева О. И.,
[10]
Юхин Ю. М., Михайлов Ю. И. Химия висмутовых
Мартынец В. Г. Энтальпия образования ниобата
соединений и материалов. М.: Изд-во СО РАН,
висмута, замещенного эрбием // ЖНХ. 2020. T. 65.
2001. С. 122-137.
№ 5. С. 669-672.
[11]
Yukhin Y. M., Mishchenko K. V., Daminov A. S. Bismuth
preoxidation for preparing solutions of salts. // Theor.
[Matskevich N. I., Semerikova A. N., Gelfond N. V.,
Found. Chem. Eng. 2017. V. 51. P. 495-502. https://
Matskevich M. Yu., Tkachev E. N., Anufrieva O. I.,
Martynetz V. G. Enthalpy of Formation of Erbium-
[12]
De Gelder J., De Gussem K., Vandenabeele P.,
Doped Bismuth Niobate // Russ. J. Inorg. Chem. 2020.
Moens L. Reference database of Raman spectra of
V. 65. P. 743-746.
biological molecules // J. Raman Spectrosc. 2007.
[19]
Yokobayashi H., Nagase K., Muraishi K. The thermal
[13]
Krishnan S., Raj C. J., Priya S. N., Robert R.,
decomposition reactions of bivalent metal succinates
Dinakaran S., Das S. J. Optical and dielectric studies
in the solid state // Bull. Chem. Soc. Jpn. 1975. V. 48.
on succinic acid single crystals // Cryst. Res. Technol.
2008. V. 43. N 8. P. 845-850.
[20]
Пат. РФ 27402592 (опубл. 2021). Способ получения
висмута сукцината основного [Pat. RU 2740292
[14]
Dhanya V. S., Sudarsanakumar M. R., Suma S.,
(publ. 2021). Method for producing base bismuth
Prasanna S., Babu K. R., Kumar B. S., Roy S. M.
succinate].
Growth and characterization of a new polymorph of