Журнал прикладной химии. 2021. Т. 94. Вып. 9
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ И МАТЕРИАЛЫ НА ИХ ОСНОВЕ
УДК 546.05
ПОЛУЧЕНИЕ ПОЛИСИЛАЗАНА ПУТЕМ АММОНОЛИЗА ДИХЛОРСИЛАНА
В НУКЛЕОФИЛЬНОМ РАСТВОРИТЕЛЕ
© А. В. Барышева1,2, Г. М. Мочалов1,2, С. С. Суворов2
1 Нижегородский государственный технический университет им. Р. Е. Алексеева,
603950, г. Нижний Новгород, ул. Минина, д. 24
2 ООО «Фирма «ХОРСТ»,
117534, г. Москва, ул. Академика Янгеля, д.14, к. 2, кв. 257
E-mail: alex.barysheva@yandex.ru
Поступила в Редакцию 16 июня 2021 г.
После доработки 23 сентября 2021 г.
Принята к публикации 23 сентября 2021 г.
Исследован процесс получения неорганического полисилазана аммонолизом дихлорсилана в пиридине.
При увеличении потока аммиака в реактор молярная масса полисилазана уменьшается, а структура
полимерной молекулы становится более линейной. Уменьшение потока приводит не только к росту
молярной массы продукта, но и к появлению разветвленных участков полимерной цепи. Минимальное
необходимое количество пиридина, обеспечивающее высокий выход продукта, составило 2.6 моль на
1 моль дихлорсилана. Снижение температуры синтеза приводит к повышению выхода продукта.
Ключевые слова: неорганический полисилазан; пиридин; поликонденсация; ИК-спектры; аммонолиз
DOI: 10.31857/S004446182109005X
Неорганический полисилазан является перспек-
как эфиры кремниевой кислоты, хлориды кремния,
тивным материалом для получения пленок оксида и
алкоксисиланы и др. Сочетание адгезионных свойств
нитрида кремния [1, 2]. Полученные из полисилазана
с возможностью нанесения очень тонких покрытий
пленки обладают высокой твердостью (9Н), устой-
делает полисилазан перспективным материалом для
чивостью к высоким температурам и истиранию,
микроэлектроники, автомобильной и авиационной
кислотостойкостью и устойчивостью к влиянию ат-
промышленности.
мосферного воздуха [1-4].
Наиболее применяемым на практике методом син-
При использовании неорганического полисилазана
теза неорганического полисилазана является реак-
для формирования пленок оксида и нитрида крем-
ция аммонолиза раствора дихлорсилана в пиридине.
ния становится возможным создание прозрачного
Также известны способы синтеза полисилазана в
покрытия толщиной от десятков до десятых долей
других растворителях — ксилоле, дихлорметане,
микрометра. Полисилазан обладает хорошей адгезией
бензоле, тетрагидрофуране [5-9]. Во всех публика-
ко многим материалам, таким как стекло, поликар-
циях образование полисилазана проводили по реак-
бонат, полиметилметакрилат, полиэтилен, металлы
ции поликонденсации аммиака с дихлорсиланом в
и сплавы, мрамор, лаки и т. д. По адгезионным свой-
соответствии с уравнением (1) в среде растворителя.
ствам полисилазан превосходит многие другие пре-
Использование нуклеофильного растворителя су-
курсоры пленок нитрида или оксида кремния, такие
щественно повышает выход полисилазана за счет
1149
1150
Барышева А. В. и др.
связывания хлорида водорода, выделяющегося при
молекуле полисилазана приводит к образованию при
поликонденсации. Кроме того, реакция аммонолиза
пиролизе пленки смешанного состава, состоящей из
дихлорсилана в нуклеофильном растворителе про-
кремния и нитрида кремния. На практике простран-
ходит через промежуточную стадию образования
ственно-разветвленный полисилазан используют для
аддукта дихлорсилана с растворителем по реакции
формирования оксидных или оксидно-нитридных
(2) [10]. Использование аддукта позволяет существен-
пленок при полимеризации во влажной среде.
но снизить реакционную способность дихлорсилана
Возможно также изменение структуры полисила-
при взаимодействии с аммиаком. Это способствует
зана за счет реакции поликонденсации с образовани-
контролируемому протеканию реакции с образова-
ем пространственно-сшитых цепей и увеличением
нием полимерных молекул. Авторами публикаций
молекулярной массы полимера. Влияние этой реак-
было установлено, что наилучшим нуклеофильным
ции на структуру и молярную массу полисилазана
растворителем является пиридин.
исследовано в [5]. Пиридин и особенно аммиак сти-
мулируют реакцию поликонденсации, которую прово-
nSiH2Cl22Py + 3nNH3
1/n[SiH2-NH]n +
дили отдельной стадией после синтеза олигомера ли-
(1)
+ 2NH4Cl + 2Py,
нейного полисилазана в пиридине. Методика синтеза
заключалась в длительном (4 ч) нагревании раствора
SiH2Cl2 + 2Py
SiH2Cl2·2Py.
(2)
полисилазана в пиридине в присутствии избытка
аммиака. Реакция взаимодействия полисилазана с
Использование пиридина в качестве растворителя
аммиаком приводила к пространственной сшивке мо-
для длительного хранения полисилазана нежелатель-
лекул полисилазана за счет образования связей между
но, так как пиридин обладает высокой гидрофильно-
двумя атомами кремния через имидную группу с
стью и активно поглощает воду из атмосферы, а хра-
выделением водорода, при этом отношение Si:N в мо-
нение раствора полисилазана в загрязненном водой
лекуле неорганического полисилазана уменьшалось.
пиридине приводит к постепенному гидролизу по-
Отмечено, что ксилол и другие инертные раствори-
лисилазана и его гелированию. Кроме того, пиридин
тели ингибируют реакцию между полисилазаном и
катализирует реакцию конденсации полисилазана с
аммиаком. Уменьшение отношения Si:N благоприят-
выделением водорода и образованием разветвленных
ствует получению нитридокремниевых пленок при
структур с более высокой молярной массой, что так-
пиролизе пространственно-сшитого полисилазана.
же приводит к гелированию раствора. В связи с этим
Цель работы — выяснение влияния условий про-
при производстве товарного раствора полисилазана
текания реакции аммонолиза дихлорсилана (темпера-
пиридин заменяют на инертный растворитель, чаще
тура проведения процесса, концентрация реагентов в
всего на дибутиловый эфир или ксилол. Это связано
реакционной смеси и скорость прибавления реаген-
с тем, что ксилол и дибутиловый эфир ингибируют
тов в реакционную зону) на структуру полученного
реакцию конденсации полисилазана [5].
полисилазана, а также на выход продукта и произво-
Пленки, получаемые из неорганического поли-
дительность этого процесса.
силазана, характеризуются достаточно высоким
значением усадки (20% при температуре пиролиза
Экспериментальная часть
400°С) [1, 6]. Такое высокое значение усадки приво-
дит к напряжениям в полученной пленке и затем к
Для экспериментов использовали дихлорсилан
образованию дефектов. Усадка зависит от структуры
с содержанием основного компонента не менее
полимерной молекулы, а низкая усадка характерна
99.9% (ООО «Фирма «ХОРСТ»), безводный аммиак
для неорганического полисилазана с разветвленной
99.9999% (ООО «Фирма «ХОРСТ»), дибутиловый
структурой, которая формируется за счет замеще-
эфир (Acros Organics) с содержанием основного ком-
ния атома водорода в группе N—H атомом кремния.
понента 99+% и пиридин (АО «Вектон») с содержа-
При этом отношение количества атомов кремния в
нием основного компонента 99.99%. Газообразный
молекуле полисилазана к атомам азота возрастает и
азот 5.0 (99.999%) производства АО «Линде Газ Рус»
приближается к 3:1. Поскольку при пиролизе идет
для продувки реактора, влажность контролировали
реакция дегидрирования, уменьшение количества
анализатором влажности ИВГ-1, МК-С, содержание
атомов водорода в молекуле исходного полисилазана
воды в азоте не превышало 0.5 ppm.
приводит к формированию более плотной структу-
Синтез проводили в трехгорлой колбе емкостью
ры при пиролизе и уменьшению значения усадки.
2 л, оснащенной верхнеприводной мешалкой, входом
Однако увеличение отношения кремния к азоту в
для газообразного азота, дихлорсилана и аммиака,
Получение полисилазана путем аммонолиза дихлорсилана в нуклеофильном растворителе
1151
а также обратным теплообменником для улавлива-
ния паров растворителя. Из-за того что неорганиче-
ский полисилазан и дихлорсилан чувствительны к
воде, синтез проводили при непрерывной продувке
реактора потоком газообразного азота с расходом
50 мл·мин-1. Колбу помещали в ванну, заполненную
теплоносителем (рис. 1). Для поддержания заданной
температуры теплоносителя использовали термостат.
В реактор вводили пиридин и устанавливали
требуемую температуру теплоносителя в ванне с
реактором. При перемешивании в реактор вводили
110 г дихлорсилана, расход дихлорсилана составлял
2.2 г·мин-1. Значение расхода дихлорсилана было
выбрано максимально возможным при условии отсут-
ствия проскока из реактора. В результате реакции был
получен твердый белый аддукт состава SiH2Cl2∙2Py.
Аммонолиз аддукта проводили путем введения в
систему 73 г газообразного аммиака при расходе
0.5-4 г·мин-1.
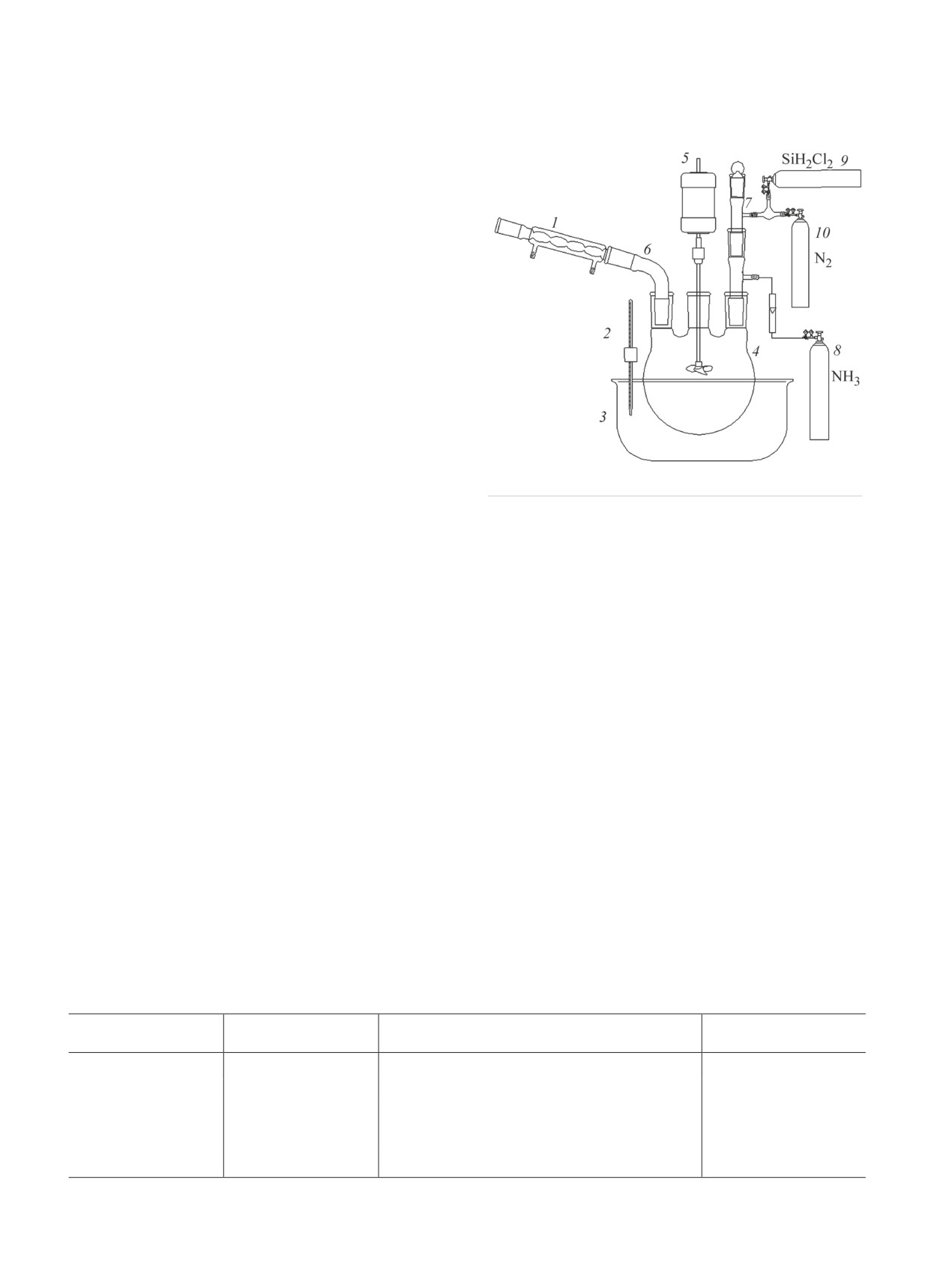
Рис. 1. Схема установки для синтеза полисилазана.
В результате реакции аммиака с аддуктом полу-
1 — обратный холодильник; 2 — термометр; 3 — охлаж-
чали растворенный в пиридине полисилазан и твер-
даемый термостат; 4 — трехгорлая колба (реактор); 5 —
дый нерастворимый в пиридине хлорид аммония.
верхнеприводная мешалка; 6, 7 — аллонж; 8 — баллон
Нерастворимый осадок NH4Cl отделяли от раствора
с аммиаком; 9 — баллон с дихлорсиланом; 10 — баллон
фильтрованием в атмосфере азота.
с азотом.
ИК-спектрометрический анализ образцов неорга-
нического полисилазана (в таблетках с KBr) проводи-
Обсуждение результатов
ли на ИК-Фурье-спектрометре Shimadzu FTIR-8400S.
На осмометре Osmomat 070 (Gonotec GmbH) опре-
Для экономии ресурсов целесообразно проводить
деляли молярную массу полисилазана, полученно-
синтез с использованием минимального количества
го с различным расходом аммиака. Для калибров-
растворителей. Пошаговое уменьшение массы пири-
ки осмометра использовали четыре калибровочных
дина с 982 до 228 г не приводило к изменению выхода
раствора с концентрациями фенолфталеина 2, 4, 8,
продукта (табл. 1). При количестве пиридина 228 г
12 ммоль·кг-1 в пиридине. Измерение проводили при
отношение его количества к количеству дихлорсила-
температуре 80°С.
на составляет 2.6 моль/моль, что на 23% превышает
Количество синтезированного полисилазана вы-
стехиометрически необходимое количество пиридина
числяли по его массовой доле в пиридине, которую
для образования аддукта с дихлорсиланом. При 147 г
определяли гравиметрическим методом после филь-
(1.7 моль/моль) пиридина выход полисилазана ожида-
трации синтез-продукта путем испарения раствори-
емо снизился, что связано с неполным связыванием
теля в вакууме из навески раствора.
дихлорсилана в аддукт.
Таблица 1
Влияние отношения мольного количества пиридина к дихлорсилану на выход полисилазана в реакции
аммонолиза дихлорсилана
Отношение мольного количества пиридина
Масса пиридина, г
Масса дихлорсилана, г
Выход полисилазана, %
к дихлорсилану
982
110
11.4
65 ± 6
621
110
7.2
69 ± 6
326
110
3.8
70 ± 6
228
110
2.6
72 ± 6
147
110
1.7
49 ± 4
1152
Барышева А. В. и др.
Максимальный достигнутый в экспериментах вы-
при температуре 20°С реакция поликонденсации при-
ход полисилазана 69% не является количественным,
водит к получению продукта с высокой молярной
что объясняется частичной потерей дихлорсилана
массой. Снижение температуры синтеза до -30°С [6]
из-за реакции его диспропорционирования до сила-
позволило получить продукт, хорошо растворимый в
на, монохлорсилана, трихлорсилана и тетрахлорида
пиридине и дибутиловом эфире.
кремния, которая катализируется пиридином [11], а
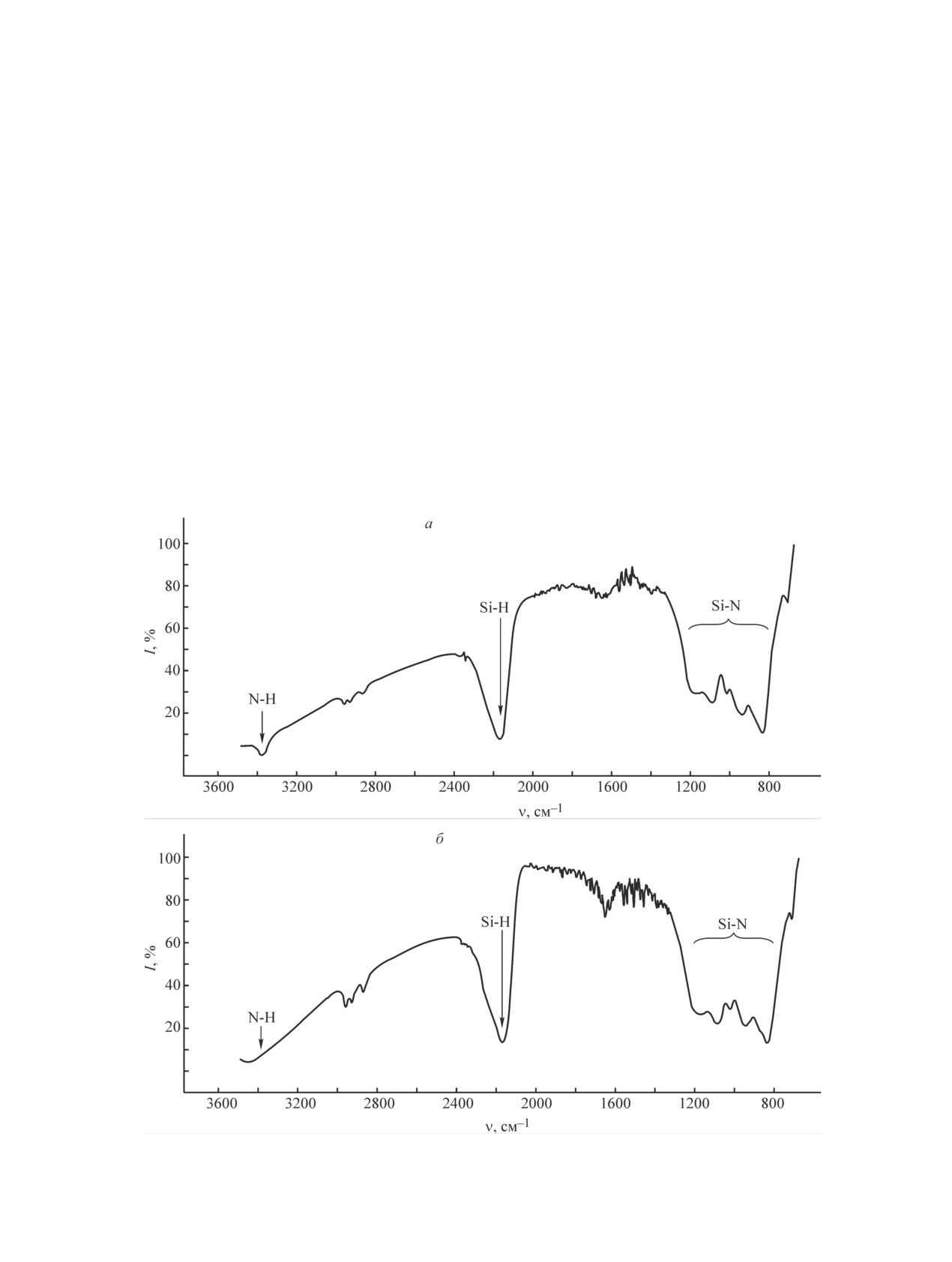
В ИК-спектре образца, полученного при макси-
также его неполным связыванием в аддукт.
мальном расходе аммиака в реакции аммонолиза
При проведении синтеза при температуре 20°С
дихлорсилана, регистрируется область, соответству-
в реакторе образовывался высокомолекулярный по-
ющая поглощению связей N—H (3380 см-1) (рис. 2).
лимер, который представляет собой желеобразный
В ИК-спектре образца, полученного с минимальным
раствор полисилазана в пиридине со взвесью хлорида
расходом аммиака, эта область практически не фикси-
аммония. Отделить раствор полисилазана в пиридине
руется. Наблюдаемый эффект можно объяснить тем,
от взвеси хлорида аммония не удалось ни отстаивани-
что при малом расходе аммиака в реакционной зоне
ем, ни фильтрованием. Попытка селективного раство-
возникает избыток дихлорсилана, который приводит
рения полисилазана в дибутиловом эфире также не
к протеканию аммонолиза по уравнению (3) с обра-
удалась, что может свидетельствовать о слишком вы-
зованием разветвленных цепей путем замены связей
сокой молекулярной массе полимера. Следовательно,
N—H на N—Si:
Рис. 2. ИК-спектры образцов неорганического полисилазана, полученного аммонолизом дихлорсилана при макси-
мальном (а) и минимальном (б) расходе аммиака.
Получение полисилазана путем аммонолиза дихлорсилана в нуклеофильном растворителе
1153
SiH2Cl
3SiH2Cl2 + NH3 + Py
N
+ 3HCl·Py.
(3)
ClH2Si
SiH2Cl
При протекании реакции по данному механизму
Силандиамин [SiH2(NH2)2] постепенно реагирует
структура получаемого полисилазана соответствует
с дихлорсиланом с образованием линейного полиси-
лазана и с сохранением связей N—H. Можно предпо-
H
ложить, что в случае высокого расхода аммиака об-
разуется большое количество молекул силандиамина,
N—Si—
(4)
которые являются точкой роста большого количества
H
n
коротких цепей полисилазана. Для подтверждения
этого предположения были определены молярные
Таким образом, при малом расходе аммиака обра-
массы полисилазана при различных массовых расхо-
зуются молекулы полисилазана с высокой степенью
дах NH3 (табл. 2).
разветвления. При большом расходе аммиака в зоне
При увеличении расхода аммиака молярная масса
ввода формируется локальная область его повышен-
полисилазана уменьшается. Это подтверждает приве-
ной концентрации, что приводит к протеканию реак-
денное выше предположение о синтезе большого ко-
ции в этой области по уравнению (5) с образованием
личества силандиамина в локальной зоне избыточной
силандиамина:
концентрации аммиака с дальнейшим образованием
SiH2Cl2 + 2NH3 + Py
H2N—SiH2—NH2 +
короткоцепочечного линейного полисилазана, в ко-
(5)
тором связи N—H сохранены. Уменьшение расхода
+ 2HCl·Py.
аммиака приводит не только к росту молярной массы
При протекании реакции по данному механизму
продукта, но и к появлению разветвленных участков
предположительно образуется линейная цепь с по-
полимерной цепи с уменьшением количества связей
лимерной структурой:
N—H в полимерной цепи.
H
H
Выводы
—
N—Si—
(6)
Руководствуясь принципами ресурсосбережения,
H
n
целесообразно проводить синтез полисилазана при
мольном соотношении растворителя пиридина и
Эти предположения позволяют объяснить причину
дихлорсилана 3:1. При реакции аммонолиза полу-
сохранения связей N—H в образце, полученном при
ченного аддукта высокий расход аммиака приводит
максимальном расходе аммиака, и их практическое
к формированию большого количества линейных
отсутствие в образце, полученном при минимальном
молекул полисилазана с относительно небольшой
расходе аммиака.
молярной массой — 610 ± 80 г·моль-1 и предпо-
ложительным соотношением кремния и азота 1:1.
Таблица 2
Малый расход аммиака приводит к формированию
Молярная масса полисилазана при различном
молекул полисилазана с высокой степенью развет-
массовом расходе аммиака в реакции аммонолиза
вления и относительно высокой молярной массой —
дихлорсилана
3000 ± 400 г·моль-1. В этом случае соотношение
Массовый расход NH3,
Молярная масса
кремния и азота приближается к 3:1.
г·мин-1
полисилазана, г·моль-1
0.5
3000 ± 400
Финансирование работы
1.0
2000 ± 300
1.2
1500 ± 200
Работа выполнена при поддержке грант-програм-
1.8
1000 ± 100
мы «УМНИК» 2019 Фонда Бортника в рамках реа-
лизации научного проекта «Разработка технологии
2.5
900 ± 100
получения товарного раствора полисилазана для фор-
4.0
610 ± 80
мирования защитных покрытий».
1154
Барышева А. В. и др.
Конфликт интересов
silica thin films formed on alicyclic poly imide film
using ultraviolet irradiation // Mater. Sci. Appl. 2014.
Авторы заявляют об отсутствии конфликта инте-
V. 5. N 3. P. 105-111.
ресов, требующего раскрытия в данной статье.
[5]
Isoda T., Kaya H., Nishii H., Funayama O., Suzuki T.,
Tashiro Y. Perhydropolysilazane precursors to silicon
Благодарности
nitride ceramic // J. Inorg. Organomet. Polym. 1992.
Авторы статьи благодарят Матвеева Александра
[6]
Pat. US
0004421 A1 (publ.
2015). Inorganic
Константиновича, директора ООО «Фирма «ХОРСТ»,
polysilazane resin.
за предоставленные материалы и оборудование.
[7]
Funayama O., Tashiro Y., Kamo A., Okumura M.,
Isoda T. Conversion mechanism of perhydropoly-
silazane into silicon nitride-basic ceramics // J. Mater.
Информация об авторах
Sci. 1994. V. 29. P. 4883-4888.
Барышева Александра Владимировна, инженер
ООО «Фирма «ХОРСТ»,
[8]
Seyferth D., Wiseman G. H., Prudʹhomme. A liquid
silazane precursor to silicon nitride // J. Am. Ceram.
Мочалов Георгий Михайлович, д.т.н., доцент, про-
Soc. 1983. V. 66. P. C-13-C-14.
фессор кафедры «Нанотехнологии и биотехнологии»
[9]
Pat. US 4950381 A (publ. 1990). Polysilazane and
НГТУ им. Р. Е. Алексеева, начальник аналитического
method for synthesis thereof.
отдела ООО «Фирма «ХОРСТ»,
[10]
Seyferth D., Wiseman G. H. High-yield ynthesis of
Si3N4/SiC ceramic materials by pyrolysis of a novel
Суворов Сергей Сергеевич, к.х.н., технический
polyorganosilazane // J. Am. Ceram. Soc. 1984. V. 67.
директор ООО «Фирма «ХОРСТ»,
P. C-132-C-133.
[11]
Campbell-Ferguson H. J., Ebsworth E. A. V.
Adducts formed between some halogenosilanes
Список литературы
and the organic bases pyridine, trimethylamine, and
tetramethylethylenediamine. Part I. Stoichiometry //
[1] Günthner M., Wang K., Bordia R. K., Motz G.
J. Chem. Soc. A. 1966. P. 1508-1514.
Conversion behaviour and resulting mechanical
properties of polysilazane-based coatings // J. Eur.
[12]
Pat. US 0106576 A1 (publ. 2014). Inorganic
Ceram. Soc. 2012. V. 32. N 9. P. 1883-1892.
polysilazane, silica film-forming coating liquid
containing same, and method for forming silica film.
[2] Zhan Y., Grottenmüller R., Li W., Javaid F., Riedel R.
[13]
Гришнова Н. Д., Мочалов Г. М., Гусев А. В.,
Evaluation of mechanical properties and hydrophobicity
Моисеев А. Н., Балановский Н. В., Харина Т. П.
of room-temperature, moisture-curable polysilazane
Каталитическая активность анионообменных
coatings // J. Appl. Polym. Sci. 2021. V. 138. N 21.
смол в реакции диспропорционирования трихлор-
силана // ЖПХ. 1999. Т. 72. № 10. С. 1667-1672
[3] Morlier A., Cros S., Garandet J. P., Alberola N.
[Grishnova N. D., Gusev A. V., Moiseev A.N.,
Structural properties of ultraviolet cured polysilazane
Mochalov G. M., Balanovsky N. V., Harina T. P.
gas barrier layers on polymer substrates // Thin Solid
Catalytic activity of anion-exchange resins in
Films. 2014. V. 550. P. 85-89.
disproportionation of trichlorosilane // Russ. J. Appl.
Chem. 1999. V. 72. N 10. P. 1761-1766].
[4] Ohishi T., Yanagida K. Preparation and gas barrier
characteristics of polysilazane derived multi-layered