Журнал прикладной химии. 2022. Т. 95. Вып. 1
ФИЗИКО-ХИМИЧЕСКИЕ ИССЛЕДОВАНИЯ СИСТЕМ И ПРОЦЕССОВ
УДК 544.135:547-315
ИССЛЕДОВАНИЕ СТРУКТУРЫ НИТРАТОВ ЦИКЛОДЕКСТРИНОВ
МЕТОДОМ РЕНТГЕНОВСКОЙ ДИФРАКЦИИ
© Ю. М. Михайлов1, Л. Б. Романова1, М. А. Рахимова1, А. В. Даровских1,*,
А. Е. Тарасов1, Д. Ю. Ковалев2, А. П. Сиротина3
1 Институт проблем химической физики РАН,
142432, Московская обл., г. Черноголовка, пр. Академика Семенова, д. 1
2 Институт структурной макрокинетики и проблем материаловедения им. А. Г. Мержанова РАН,
142432, Московская обл., г. Черноголовка, ул. Академика Осипьяна, д. 8
3 Институт нанотехнологий микроэлектроники РАН,
119991, г. Москва, Ленинский пр., д. 32а
Поступила в Редакцию 16 сентября 2021 г.
После доработки 7 декабря 2021 г.
Принята к публикации 16 декабря 2021 г.
Методом рентгеновской дифракции проведен анализ структуры нитратов α-, β- и γ-циклодекстринов.
Установлено, что с увеличением количества нитратных групп в нитратах β- и γ-циклодекстринов
происходит изменение структуры от кристаллической при степени замещения гидроксильных групп
9-12% до аморфной при степени замещения более 40%, что является следствием стерических фак-
торов и различной степени полярности функциональных групп (OH) и (ONO2). В случае с нитратами
α-циклодекстрина с увеличением степени замещения гидроксильных групп тенденция к аморфизации
вещества, характерная для нитратов β- и γ-циклодекстринов, сохраняется, однако при степени
замещения 98-100% наблюдается появление новой кристаллической фазы. Вероятно, молекулы ни-
тратов α-циклодекстринов, имеющие в своем составе только 6 глюкопиранозных звеньев, вследствие
стерических эффектов претерпевают структурные изменения, в результате которых образуется
новая молекулярная кристаллическая структура с более устойчивой конфигурацией.
Ключевые слова: нитраты циклодекстринов; степень замещения; кристаллическая структура;
аморфизация
DOI: 10.31857/S0044461822010042
Циклодекстрины и их производные — сложные
тельной дешевизны, биоразлагаемости и нетоксич-
природные циклические олигосахариды, состоящие
ности в последние десятилетия интенсивно исследу-
из остатков D-глюкопиранозы. Наибольшее распро-
ются и широко используются в различных областях
странение и коммерческое использование получи-
промышленности: пищевой, фармацевтической, кос-
ли α-, β- и γ-циклодекстрины, которые состоят из 6,
метической, химической и биохимической и др. [1].
7 или 8 глюкопиранозных звеньев соответственно.
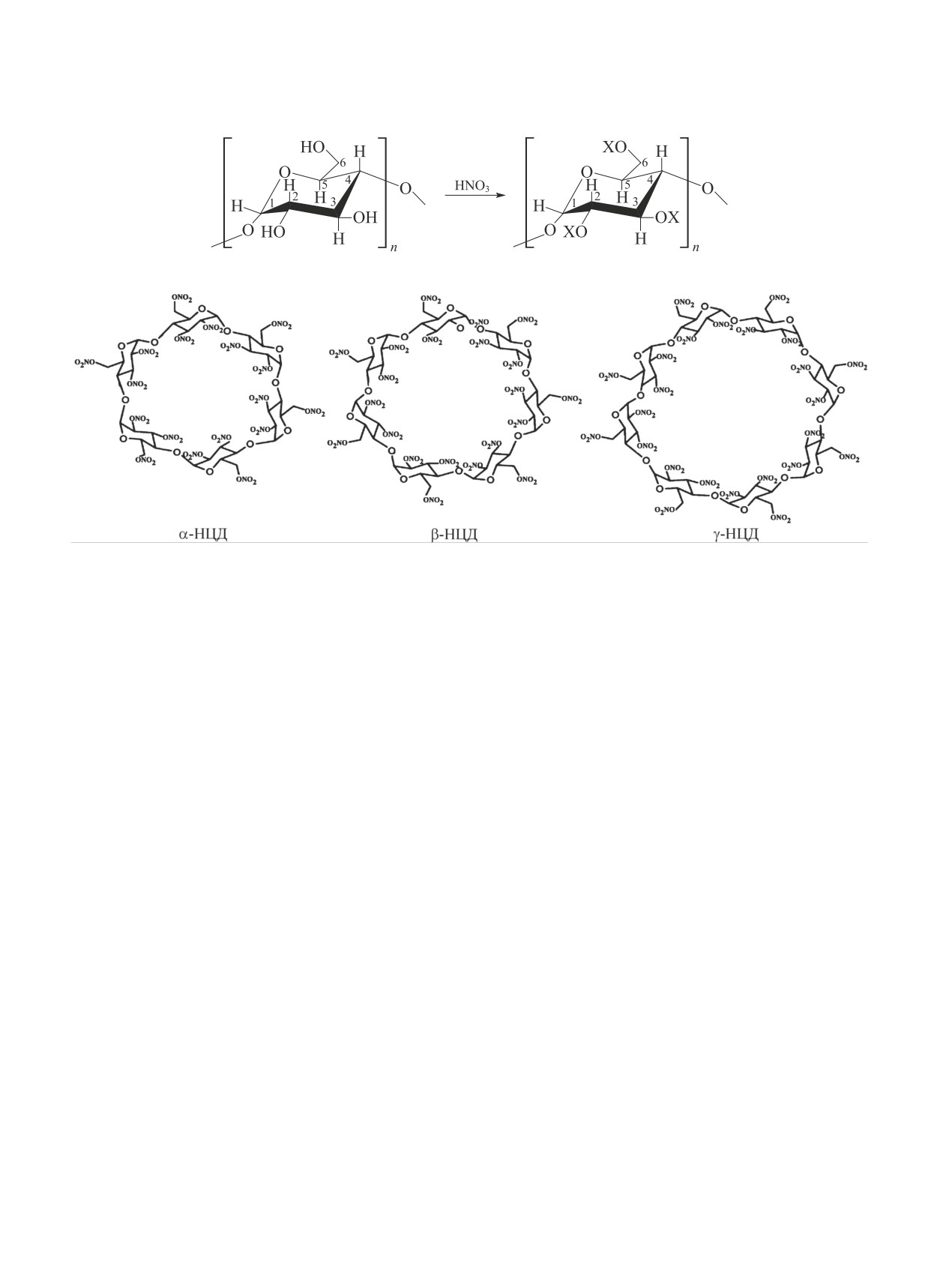
Процесс образования нитратов циклодекстринов
Циклодекстрины и их производные в силу относи- (НЦД) можно выразить следующим общим уравнением:
36
Исследование структуры нитратов циклодекстринов методом рентгеновской дифракции
37
Нитраты циклодекстринов по своему строению
клодекстрине на метильную [13-15] или гидрокси-
похожи на нитроцеллюлозу и поэтому могут пред-
пропильную [16] группу наблюдаются изменения
ставлять интерес в качестве энергоемких соединений
в структуре образующихся производных β-цикло-
[2-4]. Однако наряду с полностью нитрованными
декстринов, они становятся аморфными веществами.
циклодекстринами интерес представляют и их не-
Литературных данных о структуре нитратов цикло-
полные нитраты, которые могут быть использованы
декстринов нами найдено не было.
как индивидуальные вещества, например, в качестве
Цель работы — изучение влияния степени заме-
доноров оксида азота в лекарственных средствах или
щения гидроксильных групп на нитратные в макро-
как промежуточные соединения для дальнейших хи-
цикле α-, β- и γ-циклодекстринов на структуру полу-
мических превращений.
чаемых нитратов.
Вероятнее всего, нитраты циклодекстринов, по-
добно исходным циклодектринам, обладают такой
Экспериментальная часть
же тороидальной структурой макроциклов и имеют
наноразмерную гидрофобную полость, за счет чего
В работе использовали α-, β- и γ-циклодекстрины
могут образовывать комплексы включения с различ-
(Sigma-Aldrich, кат. номер C4642, C4767, С4892).
ными веществами [5].
Исходные циклодекстрины содержат до 18-20% кри-
Свойства циклодекстринов и некоторых произ-
сталлизационной воды в зависимости от методов
водных, в том числе их строение и структура, до-
приготовления и сушки препарата, поэтому перед
статочно хорошо изучены [1, 6]. Так, в работах по
проведением реакций нитрования циклодекстрины
изучению структуры гидратов α-циклодекстринов [7,
сушили при температуре 100°С в течение 10-50 ч
8], β-циклодекстринов [6, 9] и γ-циклодекстринов [10]
в зависимости от содержания воды в исходном ци-
установлено, что циклодекстрины имеют кристалли-
клодекстрине. Для реакций использовали α-, β- и
ческую структуру. С водой они образуют гидраты,
γ-циклодекстрины, содержащие 0.5-0.8 моль воды на
при этом происходит уплотнение структуры, сни-
1 моль циклодекстрина, т. е. ~1 мас%.
жение кристалличности и искажение макроциклов
Нитраты циклодекстринов с определенной сте-
циклодекстринов вследствие включения определен-
пенью замещения получали нитрованием соответ-
ного количества молекул воды в полость молекулы
ствующих циклодекстринов по разработанной ранее
циклодекстрина [11, 12].
методике [17]. Для проведения реакций нитрования
По данным рентгеноструктурного анализа, при
использовали концентрированную азотную кислоту
замещении водорода гидроксильных групп в β-ци- (Sigma-Aldrich, кат. номер 1.00455) с плотностью
38
Михайлов Ю. М. и др.
1.51 г·см-3, которую дополнительно очищали пере-
клодекстрина изменяется, что, очевидно, связано с
гонкой при пониженном давлении* [18], а также ее
замещением гидроксильных групп на нитратные. При
водные растворы концентрацией 75-98%. Массовую
увеличении степени замещения до 22% дифракцион-
долю азотной кислоты определяли согласно мето-
ные линии исходного β-циклодекстрина практически
дикам.**
исчезают, и на дифрактограмме наблюдается несколь-
Определение количества нитратных групп в нитра-
ко сильно размытых диффузных линий. Дальнейшее
тах циклодекстринов осуществляли по разработан-
увеличение степени замещения приводит к полной
ным ранее методикам: методом ЯМР-спектроскопии
потере кристалличности нитратом β-циклодекстри-
[18] высокого разрешения на Bruker AVANCE-3 500
на. Начиная с 40%-ной степени замещения нитрат
с рабочей частотой 500 МГц, а также методом
β-циклодекстрина является рентгеноаморфным веще-
ИК-спектроскопии [19] на FTIR-спектрофотометре
ством, т. е. может состоять как из наноразмерных кри-
Bruker Alpha (шаг сканирования 2 см-1, диапазон
сталлитов, так и (или) аморфной фазы: наблюдается
измерения 4000-360 см-1, число сканирований об-
лишь ближний порядок молекулярной структуры.
разца и фона 56) в кювете из NaCl с фиксированной
Аналогичная тенденция изменения структуры
толщиной 0.00506 см.
от кристаллической до рентгеноаморфной при за-
Степень замещения рассчитывалась как отноше-
мещении гидроксильных групп на нитратные на-
ние количества образующихся ONO2-групп в нитра-
блюдается и в случае нитратов γ-циклодекстрина
тах циклодекстринов к максимально возможному их
(см. рисунок, б). Различия между нитратами β- и
количеству (18 ONO2-групп — для нитратов α-ци-
γ-циклодекстринов заключаются лишь в том, что
клодекстрина, 21 — для нитратов β-циклодекстрина,
изменение кристаллической структуры нитратов
24 — для нитратов γ-циклодекстрина). Рассчитанная
γ-циклодекстрина при замещении гидроксильных
степень замещения является среднестатистической
групп на нитратные происходит при меньшей степени
величиной, так как получающиеся нитраты цикло-
замещения. Уже при степени замещения 8%, которая
декстринов имеют молекулярно-структурную неод-
соответствует замещению двух гидроксильных групп
нородность, в значительной степени зависящую от
из 24, дифрактограмма нитратов γ-циклодекстри-
условий проведения реакции нитрования.
на свидетельствует о рентгеноаморфном состоянии
Структура нитратов циклодекстринов с различ-
продукта. Таким образом, практически все нитраты
ной степенью замещения исследовалась методом
γ-циклодекстрина являются рентгеноаморфными ве-
рентгенофазового анализа (РФА) на дифрактометре
ществами.
ДРОН 3М (НПП «Буревестник») с монохроматором
Для нитратов α-циклодекстрина тенденция амор-
на вторичном пучке, излучение CuKα, шаг 0.02°, экс-
физации вещества с увеличением степени замещения,
позиция 4 с в точке, интервал 2θ = 5-35°. В качестве
характерная для нитратов β- и γ-циклодекстринов, со-
бесфоновой подложки использовался монокристал-
храняется (см. рисунок, в). Так, при степени замеще-
лический диск Si.
ния 9% дифракционные линии исходной фазы α-ци-
клодекстрина практически исчезают, а дальнейшее
увеличение количества нитратных групп в макро-
Обсуждение результатов
цикле приводит к полной потере кристалличности.
При увеличении количества нитратных групп в
Однако при 98-100%-ной степени замещения на диф-
нитратах циклодекстринов наблюдается аморфиза-
рактограммах нитратов α-циклодекстрина появляют-
ция структуры (см. рисунок, а). Дифрактограммы
ся дифракционные линии, которые свидетельствуют о
исходных β- и γ-циклодекстринов свидетельствуют о
наличии кристаллической структуры. Сопоставление
низкосимметричной кристаллической структуре этих
дифрактограмм исходного α-циклодекстрина и его
веществ. При степени замещения 12% в нитрате β-ци-
нитрата с 98-100%-ной степенью замещения пока-
клодекстрина происходит структурный переход (см.
зывает, что кристаллическая структура этих соедине-
рисунок), кристаллическая структура исходного β-ци-
ний различна. Установить пространственную группу
и структурные данные нитрата α-циклодекстрина,
* Чистые химические вещества. Изд. 4-е, перераб.
относящегося, по-видимому, к одной из низших син-
и доп. / Ю. В. Карякин, И. И. Ангелов. М.: Химия, 1974.
гоний, методом порошковой дифрактометрии про-
С. 162-164.
блематично и представляет собой отдельную задачу.
** ГОСТ 701-89. Кислота азотная концентрированная.
Переход от аморфной к кристаллической структуре в
Технические условия. ГОСТ 28959-91. Кислота азотная
нитратах α-циклодекстрина при практически полном
техническая. Метод определения концентрации по изме-
рению плотности.
замещении гидроксильных групп не является слу-
Исследование структуры нитратов циклодекстринов методом рентгеновской дифракции
39
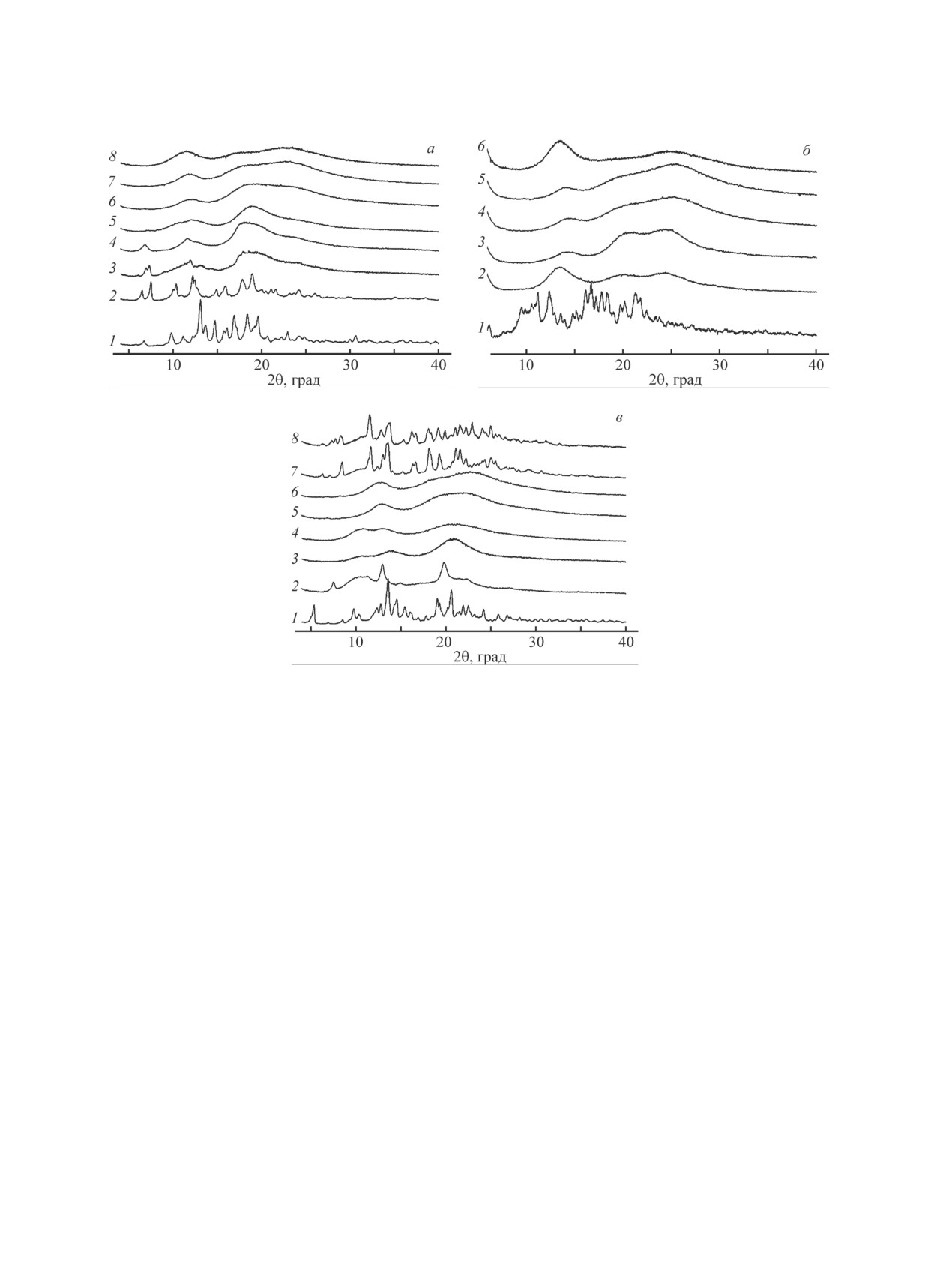
Дифрактограммы исследуемых веществ.
а) β-циклодекстрин (1) и его производные со степенью замещения гидроксильных групп на нитратные (%): 2 — 12, 3 —
22, 4 — 30, 5 — 40, 6 — 70, 7 — 80, 8 — 100; б) γ-циклодекстрин (1) и его производные со степенью замещения гидрок-
сильных групп на нитратные (%): 2 — 9, 3 — 40, 4 — 73, 5 — 80, 6 — 100; в) α-циклодекстрин (1) и его производные со
степенью замещения гидроксильных групп на нитратные (%): 2 — 14, 3 — 44, 4 — 72, 5 — 81, 6 — 93, 7 — 99, 8 — 100.
чайным артефактом. Он подтвержден анализом 7 об-
Можно предположить, что аморфизация нитра-
разцов нитратов α-циклодекстрина с 98-100%-ной
тов циклодекстринов при замещении гидроксильных
степенью замещения, полученных независимо друг
групп на нитратные является следствием различной
от друга.
степени полярности функциональных групп. В случае
Трактовка обнаруженного эффекта лежит вне
сильнополярных OH-групп макроциклы образуют
рамок настоящей работы и требует проведения до-
между собой водородные и ван-дер-ваальсовы связи,
полнительных исследований. Следует отметить, что
формируя трехмерную молекулярную периодическую
наблюдаемый переход в кристаллическое состояние
структуру. При замещении OH-групп на менее поляр-
характерен только для макроциклов нитратов α-ци-
ные ONO2-группы водородные связи и ван-дер-вааль-
клодекстрина, для нитратов β- и γ-циклодекстринов
совое взаимодействие ослабевают, и молекулярные
подобного изменения структуры нет. Вероятно, мо-
макроциклы сохраняют только ближний порядок.
лекулы нитратов α-циклодекстрина, имеющие в сво-
Возможно также, что определенный вклад в деста-
ем составе 6 глюкопиранозных звеньев, вследствие
билизацию кристаллической структуры вносит стери-
стерических эффектов претерпевают изменения, в
ческий эффект. Размер нитратных групп существенно
результате которых структура макромолекулы изме-
больше, чем гидроксильных, что препятствует сбли-
няется с формированием новой молекулярной кри-
жению и определенной пространственной ориента-
сталлической структуры с более устойчивой конфигу-
ции макроциклов и делает невозможным образование
рацией периодической пространственной структуры.
кристаллической структуры.
40
Михайлов Ю. М. и др.
Выводы
Д. Ю. Ковалев и А. П. Сиротина проводили рентге-
нофазовый анализ синтезированных нитратов цикло-
Методом рентгенофазового анализа изучена струк-
декстринов.
тура нитратов α-, β- и γ-циклодекстринов с различной
степенью замещения гидроксильных групп в цикло-
декстринах на нитратные. Установлено, что замена
Информация об авторах
гидроксильных групп на нитратные в циклодекстри-
Михайлов Юрий Михайлович, акад. РАН, д.х.н.,
нах приводит к изменению внутри- и межмолеку-
лярных связей в глюкопиранозном кольце нитратов
Романова Людмила Борисовна, к.х.н.,
циклодекстринов и, как следствие, изменению их
структуры. Для макроцикла нитрата циклодекстрина
Рахимова Мария Аркадьевна, к.х.н.,
с минимальным количеством звеньев — нитрата α-ци-
клодекстрина наблюдается переход в кристалличе-
Даровских Анна Владимировна,
ское состояние при 98-100%-ной степени замещения.
Тарасов Александр Евгеньевич, к.х.н.,
Благодарности
Ковалев Дмитрий Юрьевич, к.т.н.,
Работа выполнена с использованием оборудования
Аналитического центра коллективного пользования
Сиротина Анна Петровна,
ckp/ackp» и оборудования РЦКП ИСМАН.
Авторы выражают благодарность А. В. Черняку
за помощь в интерпретации данных ЯМР-спектро-
Список литературы
скопии.
[1]
Del Valle E. M. M. Cyclodextrins and their uses: A
review // Process Biochem. 2004. V. 39. N 9. P.1033-
Финансирование работы
[2]
Pat. US 5114506 (publ. 1992). Energetic composites of
Работа выполнена в рамках государственного
cyclodextrin nitrate esters and nitrate ester plasticizers.
задания ИПХФ РАН 0089-2019-0005 (№ государ-
[3]
Pat. US 6468370 (publ. 2002). Gas generating
ственной регистрации АААА-А19-119101690058-9),
composition for vehicle occupant protection apparatus.
государственного задания ИСМАН РАН, те-
[4]
Pat. US 6293201 (publ. 2001). Chemically reactive
ма
44.1
(№ государственной регистрации
fragmentation warhead.
АААА-А20-120021890022-5).
[5]
Mikhailov Y. M., Romanova L. B., Tarasov A. E.,
Darovskikh A. V. Inclusion complexes of cyclodextrin
nitrates with compounds containing explosive groups in
Конфликт интересов
their composition // Proceedings of 22th International
Seminar «New Trends in Research of Energetic
Авторы заявляют об отсутствии конфликта инте-
Materials». Czech Republic, Pardubice, 2019. P. 550-
ресов, требующего раскрытия в данной статье.
554.
[6]
Damodharan L., Pattabhi V. Solvent interaction with
β-cyclodextrin as observed in crystal structures // Mol.
Информация о вкладе авторов
Cryst. Liq. Cryst. 2004. V. 423. P. 17-35.
Ю. М. Михайлов и Л. Б. Романова участвовали в
постановке задач исследования, осуществляли лите-
[7]
Lindner K., Saenger W. Topography ofcyсlodextrin
inclusion complexes. XVI. Cyclic system of hydrogen
ратурный поиск; М. А. Рахимова и А. В. Даровских
bonds: Structure of α-cyclodextrinhexahydrate, form
синтезировали неполные нитраты циклодекстринов
(II): Comparison with form (I) // Acta. Cryst. 1982.
с различной степенью замещения гидроксильных
V. 38. P. 203-210.
групп на нитратные, определяли степень замеще-
ния гидроксильных групп на нитратные в исследуе-
[8]
Calabro M. L., Tommasini S., Donato P., Raneri D.,
мых циклодекстринах методом ЯМР-спектроскопии;
Stancanelli R., Ficarra P., Ficarra R., Costa C.,
А. Е. Тарасов определял степень замещения ги-
Catania S., Rustichelli C., Gamberini G. Effects of
дроксильных групп на нитратные в исследуемых
α- and β-cyclodextrin complexation on the physico-
циклодекстринах методом ИК-спектроскопии;
chemical properties and antioxidant activity of some
Исследование структуры нитратов циклодекстринов методом рентгеновской дифракции
41
3-hydroxyflavones // J. Pharm. Biomed. Anal. 2004.
[16]
Fernandes C. M., Vieira M. V., Veiga F. J. B.
V. 35. P. 365-377.
Physicochemical characterization and in vitro
dissolution behavior of nicardipine-cyclodextrins
[9]
Steiner T., Koellner G., Ali S., Zakim D., Saenger
inclusion compounds // Eur. J. Pharmacol. Sci. 2002.
W. Crystalline β-cyclodextrin·12H2O reversibly
V. 15. P. 79-88.
dehydrates to β-cyclodextrin·10.5 H2O under ambient
conditions // Biochem. Biophys. Res. Commun. 1992.
[17]
Михайлов Ю. М., Романова Л. Б., Тарасов А. Е.,
V. 188. P. 1060-1066.
Рахимова М. А., Даровских А. В., Баринова Л. С.
Исследование процесса получения нитратов ци-
[10]
Harata K. The structure of the cyclodextrin complex.
клодекстринов // ЖПХ. 2018. Т. 91. № 7. С. 1049-
XX. Crystal sructure of uncomplexed hydrated
γ-cyclodextrin // Bull. Chem. Soc. Jpn. 1987. V. 60.
[Mikhailov Y. M., Romanova L. B., Tarasov A. E.,
Rakhimova M. A., Darovskikh A. V., Barinova L. S.
[11]
Cunha-Silva L., Jose J. C. Teixeira-Dias. How
Preparation of cyclodextrin nitrates // Russ. J. Appl.
humidity affects the solid-state inclusion of
Chem. 2018. V. 91. N 7. P. 1217-1221.
2-phenoxyethanol in β-cyclodextrin: A comparison
with β-cyclodextrin // New J. Chem. 2004. V. 28.
[18]
Романова Л. Б., Баринова Л. С., Лагодзинская Г. В.,
Казаков А. И., Михайлов Ю. М. Получение и анализ
[12]
Steiner T., Koellner G. Crystalline beta-сyclodextrin
методом ЯМР нитратов бета-циклодекстрина //
hydrate at various humidities: Fast, continuous, and
ЖПХ. 2014. Т. 87. № 12. С. 1809-1815.
reversible dehydration studied by x-ray diffraction //
J. Am. Chem. Soc. 1994. V. 116. P. 5122-5128.
[Romanova L. B., Barinova L. S., Lagodzinskaya G. V.,
Kazakov A. I., Mikhailov Y. M. Preparation and NMR
[13]
Spulber M., Pinteala M., Fifere A., Moldoveanu C.,
analysis of β-cyclodextrin nitrates // Russ. J. Appl.
Mangalagiu L., Harabagiu V., Simionescu B. C.
Chem. 2014. V. 87. N 12. P. 1884-1889.
Water soluble complexes of methyl-β-cyclodextrin
and sulconazole nitrate // J. Incl. Phenom. Macrocycl.
[19]
Родин М. Д., Романова Л. Б., Даровских А. В.,
Chem. 2008. V. 62. P. 135-142.
Горбунова М. А., Тарасов А. Е. ИК-спектральная
методика определения степени нитрования β-ци-
[14]
Ren Y., Liu Y., Niu R., Liao X., Zhang J., Yang B.
клодекстрина // Журн. прикл. спектр. 2018. Т. 85.
Host-guest inclusion system of oleanolic acid with
№ 4. С. 639-644.
methyl-β-cyclodextrin: Preparation, characterization
and anticancer activity // J. Molec. Structure. 2016.
[Rodin M. D., Romanova L. B., Darovskih A. V.,
V. 1117. P. 1-7.
Gorbunova M. A. Tarasov A. E. IR-spectroscopic
method for determining the degree of nitration of
[15]
Никитин Н. А. Циклодекстрины и их комплексы
β-cyclodextrin // J. Appl. Spectrosc. 2018. V. 76. N 4.
включения (обзор литературы) // Вопр. биол., мед.
P. 639-644.
и фармацевт. химии. 2015. № 6. С. 3-11.