264
Бельская О. Б. и др.
Журнал прикладной химии. 2022. Т. 95. Вып. 2
УДК 544.478.02:546.92
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ АКТИВИРОВАННЫХ ПРОМЫШЛЕННЫХ
АЛЮМИНИЕВЫХ СПЛАВОВ С ВОДОЙ
КАК ПРЕДШЕСТВЕННИК НОСИТЕЛЯ КАТАЛИЗАТОРОВ
© О. Б. Бельская1,3, А. И. Низовский2,*, Т. И. Гуляева1,
И. В. Муромцев1, В. И. Бухтияров2
1 Центр новых химических технологий Федерального исследовательского центра
«Институт катализа им. Г. К. Борескова СО РАН»,
644040, г. Омск, ул. Нефтезаводская, д. 54
2 Федеральный исследовательский центр «Институт катализа им. Г. К. Борескова СО РАН»,
630090, г. Новосибирск, пр. Академика Лаврентьева, д. 5
3 Омский государственный технический университет,
644050, г. Омск, пр. Мира, д. 11
* E-mail: niz@catalysis.ru
Поступила в Редакцию 9 ноября 2021 г.
После доработки 10 марта 2022 г.
Принята к публикации 10 марта 2022 г.
Получены продукты взаимодействия активированных Ga-In эвтектикой технических алюминиевых
сплавов с водой. Установлено, что основными примесями в образующемся гидроксиде алюминия яв-
ляются Ga (5 мас%), In и Cu (0.6-0.7 мас%), также обнаружено присутствие Fe, Zn, Ca, Mg и Mn
в количествах менее 0.1 мас%. Предложен метод очистки загрязненной Ga-In эвтектики, использо-
ванной при активации Al, для последующего применения. Оксидная фаза, полученная на основе син-
тезированного продукта, представлена γ-Al2O3, модифицированным Ga и In. Она характеризуется
развитой поверхностью ~300 м2·г-1, мезопористой структурой и может быть использована в каче-
стве адсорбента и носителя катализаторов дегидрирования. Платиновый катализатор, полученный
на основе полученного оксидного носителя, сравним по своим свойствам в дегидрировании пропана с
модельными системами на основе алюминиевого сплава А0.
Ключевые слова: Ga-In эвтектика; активированный сплав алюминия; оксид алюминия; платиновый
катализатор; дегидрирование пропана
DOI: 10.31857/S0044461822020086, EDN: DEGIQF
При использовании реакции взаимодействия воды
миния по отношению к воде готовят специальные
с металлами для получения водорода в водородных
многокомпонентные алюминиевые сплавы с высоким
картриджах возникает задача утилизации побочных
содержанием Ga, In, Bi, Zn, Sn, Mg, что существенно
продуктов. Выбор Al для использования в качестве
удорожает полученный материал. Применение меха-
реагента в реакции с водой для получения газо-
нохимической обработки алюминия также приводит
образного H2 оптимален [1-3]. Известно [4-6], что
к увеличению его реакционной способности [7, 8].
высокодисперсные порошки алюминия интенсивно
Особенностью развиваемого авторами метода при-
взаимодействуют с водой либо в сильнощелочной
готовления активированного материала для получе-
среде, либо при высоких температурах и давлении.
ния водорода из воды является обработка массивных
Для повышения реакционной способности алюминия
алюминиевых конструкционных сплавов Ga-In эв-
при нейтральном pH необходима предварительная
тектикой без дополнительного механохимического
его активация. С целью повышения активности алю-
воздействия [9].
Продукт взаимодействия активированных промышленных алюминиевых сплавов с водой...
265
Ранее нами проводились исследования возможно-
В качестве способа разделения полученных про-
сти использования продуктов взаимодействия активи-
дуктов была выбрана методика гравитационной се-
рованного алюминия с водой для получения матери-
диментации. В прозрачную пластиковую емкость
алов с высокой добавочной стоимостью, а именно в
цилиндрической формы помещали десятикратно раз-
качестве исходного сырья для производства носите-
бавленную взвесь продуктов реакции взаимодействия
лей металлических нанесенных катализаторов. Были
активированных алюминиевых сплавов с водой. По
проведены исследования носителей и катализаторов,
мере оседания осадка излишки воды удаляли. После
полученных на основе алюминиевого сплава А0, ак-
прекращения седиментации визуально взвесь пред-
тивированного чистым Ga или Ga-In эвтектикой [10,
ставляла собой слоистую систему, слои которой раз-
11]. Также была показана возможность проведения
личались по цвету. Из средней части каждого слоя
реакции Al с водой при использовании активирован-
отбирали образцы, которые затем раздельно сушили.
ных материалов не только на основе сплава А0, но
Образцы обозначены как N1, N2, N3, N4 (N1 — верх-
и промышленных конструкционных алюминиевых
ний слой, N4 — нижний слой, N2, N3 — промежуточ-
сплавов, содержащих существенное количество ле-
ные слои). На дне емкости собирался осадок непро-
гирующих компонентов [10].
реагировавших частиц и остатки эвтектики. Размер
Цель работы — получение носителей для нанесен-
частиц оценивали методом лазерной дифракции на
ных металлических Pt-катализаторов при использова-
лазерном анализаторе SALD-2101 (Shimadzu) с ди-
нии продуктов реакции активированных промышлен-
апазоном измерений 0.03-1000 мкм. Определение
ных конструкционных алюминиевых сплавов типа
проводили в водных суспензиях.
Д16Т и Д1Т с водой.
Концентрацию металлов в образцах продуктов
взаимодействия алюминиевого сплава с водой опре-
деляли методом атомно-эмиссионной спектрометрии
Экспериментальная часть
с индуктивно-связанной плазмой (ОРТIMA 4300 DV,
Метод активации алюминия заключался в обра-
Perkin Elmer).*
ботке поверхности массивных образцов из конструк-
Для получения оксидных форм Al2O3-N(1-4) про-
ционных алюминиевых сплавов Д1Т, Д16Т (ОАО
дукты взаимодействия активированных алюмини-
«КУМЗ») Ga-In эвтектикой, содержащей 76 мас% Ga
евых сплавов с водой прокаливали в токе воздуха
и 24 мас% In (Tпл = 15.9°C), полученной путем сплав-
при Т = 550°С. При приготовлении катализаторов
ления Ga (Гл0, ОАО «Новосибирский завод редких
в качестве соединения — прекурсора платины ис-
металлов») и In (Ин00, ОАО «Челябинский цинковый
пользовали H2PtCl6·6H2O (массовая доля платины
завод»), в сушильном шкафу (ШС-80-01-СПУ, OАО
не менее 37.5%, ОАО «АУРАТ»). Ее сорбцию на
«Смоленское СКТБ СПУ») при Т = 180°C в тече-
Al2O3-N1 выполняли из водного раствора при отно-
ние 10 ч и последующим охлаждением до Т = 20°C.
шении объема раствора к объему носителя, равном
Активацию проводили путем смачивания эвтекти-
10. Данное отношение было принято из расчета на-
кой поверхности среза при Т = 150°C в герметичной
несения 1 мас% металла на носитель. В течение 1 ч
емкости с силикагелем (силикагель индикаторный,
происходило полное извлечение металлокомплекса из
ООО «АКВАХИМ») в течение 300 ч по методике [9].
пропиточного раствора. После стадий сушки при 25
После охлаждения избыток эвтектики удаляли с
и 120°С и прокалки при 550°С проводили восстанов-
поверхности образцов механическим способом.
ление платины в токе водорода (сорт 2, 99.994 об%,
Реакцию активированного продукта с водой прово-
ООО «НИИ КМ») при 550°С.
дили при атмосферном давлении в 100 см3 реакторе
Фазовый состав полученных образцов оксидов
из нержавеющей стали, внешняя поверхность кото-
был охарактеризован с использованием порошкового
рого была покрыта теплоизоляционным материалом.
рентгеновского дифрактометра D8 Advance (Bruker)
Количество дистиллированной воды (аквадистил-
в CuKα-излучении (длина волны 0.15406 нм, позици-
лятор медицинский электрический АЭ-5, ООО ПФ
онно-чувствительный детектор Lynxeye). Режимы
«ЛИВАМ») для проведения реакции было взято с
измерения: шаг сканирования 0.1 2θ°, время нако-
пятикратным избытком относительно стехиометрии
пления сигнала 3 с, напряжение и ток эмиссии 40 кB
реакции. Реактор с водой предварительно термоста-
тировали при Т = 20°C, затем происходил контакт с
* Томпсон M., Уолш Д. Н. Руководство по спектро-
активированным материалом. Наблюдалось интенсив-
метрическому анализу с индуктивно-связанной плаз-
ное выделение водорода практически без индукцион-
мой / Пер. с англ. под ред. В. Б. Беленко. М.: Недра,
ного периода, которое завершалось в течение 5 мин.
1988. С. 153-160.
266
Бельская О. Б. и др.
и 40 мA соответственно, область углов сканирования
графически (газовый хроматограф «Цвет 500», ЗАО
5-80 2θ°. Расшифровка полученных дифрактограмм
СКБ «ХРОМАТЭК», колонка Rt-Alumina PLOT, 50 м,
проведена с использованием базы данных по по-
пламенно-ионизационный детектор) в режиме online.
рошковой дифракции ICDD PDF-2.
При проведении всех экспериментов в работе ис-
Спектры ЯМР 27Al образцов γ-Al2O3 (Condea
пользовались газы: аргон газообразный (ос.ч., АО
Chemia GmbH), Al2O3-N1 и Al2O3-N3 были получены
«Сибтехгаз» им. Кима Ф. И.), водород газообраз-
на ЯМР-спектрометре Аvance-400 (Bruker) c много-
ный (ос.ч., АО «Сибтехгаз» им. Кима Ф. И.). В каче-
ядерным датчиком SB4 в условиях простого одноим-
стве растворителя в работе использовался этиловый
пульсного эксперимента при вращении образцов под
магическим углом в роторах из ZrO2. Параметры экс-
перимента: резонансная частота 104 МГц, длитель-
«Мариинский ЛВЗ»).
ность импульсов 2.5 мкс, интервал повторения им-
пульсов 0.5 с, ширина окна 20 800 Гц, число точек на
Обсуждение результатов
спектр 4096, внешний стандарт — 1 М раствор AlCl3.
Текстурные характеристики исследуемых образ-
Продукты, полученные при взаимодействии ак-
цов были определены из анализа изотерм адсорбции-
тивированных материалов с водой и разделенные
десорбции азота при 77.4 K, полученных на объем-
с использованием методики гравитационной седи-
ной вакуумной статической установке ASAP-2020M
ментации, были исследованы методами лазерной
(Micromeritics). Перед проведением адсорбционных
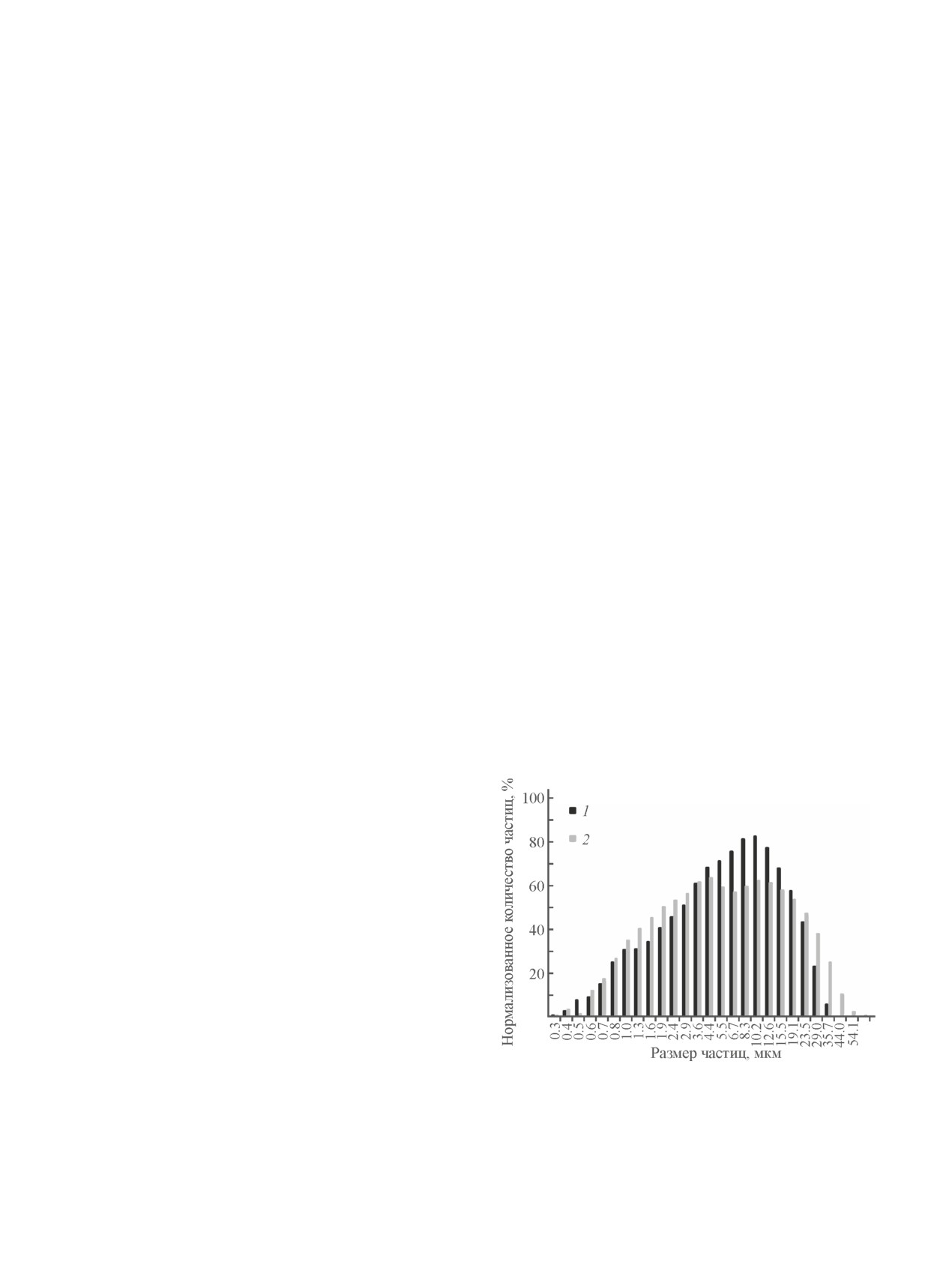
дифракции и элементного анализа. Из данных рас-
измерений образцы, прокаленные при 550°С, ваку-
пределения частиц по размерам (рис. 1) следует, что
умировали при 300°С в течение 6 ч. Расчеты удель-
материал, находящийся в нижнем слое полученного
ной поверхности выполняли в интервале равновес-
осадка, характеризуется более широким распределе-
ных относительных значений давления паров азота
нием частиц по размерам и присутствием большей
Р/Р0 = 0.05-0.25 по изотерме адсорбции с учетом ве-
доли крупных частиц 20-60 мкм. В то же время про-
личины молекулярной площадки азота в заполненном
дукт однороден по химическому составу независимо
монослое 0.162 нм2. Адсорбционный объем пор опре-
от размера частиц. Основным примесным металлом
деляли по величине адсорбции азота при Р/Р0 = 0.990,
является Ga, его содержание составляет ~5 мас%, и
принимая плотность адсорбата равной плотности
~1 мас% приходится на In и Cu (табл. 1). Также были
нормальной жидкости для азота. Для получения кри-
обнаружены Fe, Zn, Ca, Mg, Mn в количествах, не
вых распределения пор по размерам применяли метод
превышающих 0.1 мас%.
Баррета-Джойнера-Халенды.
Исследование процесса поглощения водорода при
температурно-программируемом восстановлении Pt
проводили на прецизионном хемосорбционном ана-
лизаторе AutoChem-2920 (Micromeritics) с детектором
по теплопроводности с использованием смеси 10%
Н2-Ar. Для определения дисперсности нанесенного
металла D(Н2) хемосорбцию водорода проводили по-
сле температурно-программируемого восстановления
и охлаждения катализатора в потоке Ar до комнатной
температуры. Дисперсность металла рассчитывали с
учетом стехиометрии сорбции Н:Pt = 1:1.
Реакцию дегидрирования пропана (UN 1978,
«PBM GAS») проводили в проточном реакторе с не-
подвижным слоем катализатора (загрузка 0.5 г) при
550°C, атмосферном давлении, мольном отношении
Н2:С3Н8 = 0.25 и массовой скорости подачи сырья
Рис. 1. Распределение частиц по размерам продуктов
8 г·ч-1. Длительность каждого эксперимента состав-
взаимодействия активированных алюминиевых сплавов
ляла 5 ч. Перед испытанием катализаторы были про-
с водой, полученных в процессе гравитационной седи-
калены при 550°C и восстановлены в токе водорода
ментации, в зависимости от точки отбора образцов по
непосредственно в каталитической установке при
слоям: образец N2 — второй слой от поверхности (1),
550°C. Состав продуктов анализировали хромато-
образец N4 — нижний слой (2).
Продукт взаимодействия активированных промышленных алюминиевых сплавов с водой...
267
Таблица 1
Содержание примесных катионов в образцах гидроксидов алюминия — продуктов взаимодействия
активированного алюминиевого сплава с водой в зависимости от точки отбора образцов
(N1 — верхний слой, N4 — нижний слой).
Содержание элемента, мас%
Элемент
N1
N2
N3
N4
Cu
0.74
0.74
0.68
0.56
Ga
4.89
5.15
4.72
4.46
In
0.75
0.62
0.70
0.59
Оксидная фаза была получена из образцов смеси
гидроксидов алюминия, отобранных из продуктов
взаимодействия активированных алюминиевых спла-
вов с водой, при прокаливании при 550°С в течение
3 ч со ступенчатым подъемом температуры. Для ис-
следования были выбраны образцы Al2O3-N1 (1) и
Al2O3-N3 (2) из материала, отобранного в верхнем и
среднем слоях продуктов, полученных в результате
гравитационной седиментации (рис. 2).
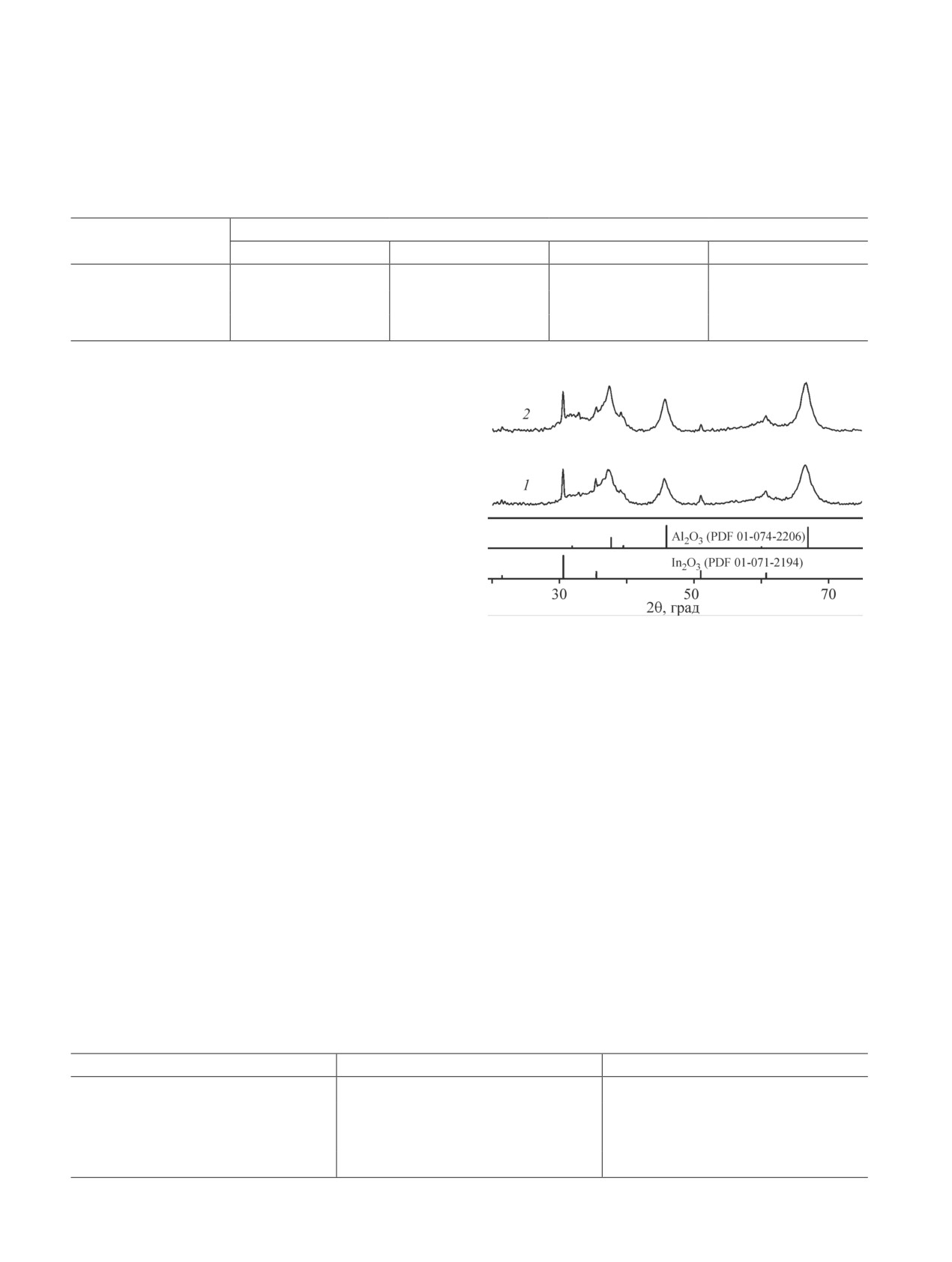
Образцы имеют одинаковый фазовый состав,
представленный γ-Al2O3 и In2O3 (рис. 2, табл. 2).
Рефлексы, относящиеся к Ga2O3, не наблюдаются.
Вероятно, Ga2O3 присутствует в составе твердого
Рис. 2. Дифрактограммы образцов, полученных в про-
раствора с γ-Al2O3 и находится в кубической модифи-
цессе гравитационной седиментации продуктов реак-
кации. Это подтверждается некоторым увеличением
ции.
параметра решетки а 7.941 и 7.943 Å по сравнению
Al2O3-N1 (1) — верхний слой, Al2O3-N3 (2) — третий из
со значением а решетки γ-Al2O3 (7.903 Å).
четырех от поверхности слой продуктов седиментации.
Обнаруженные структурные изменения, связан-
ные с образованием твердого раствора Ga2O3-Al2O3,
результате которого Ga включается в структуру Al2O3,
хорошо согласуются с данными, полученными
вытесняя Al из тетраэдрического положения [13].
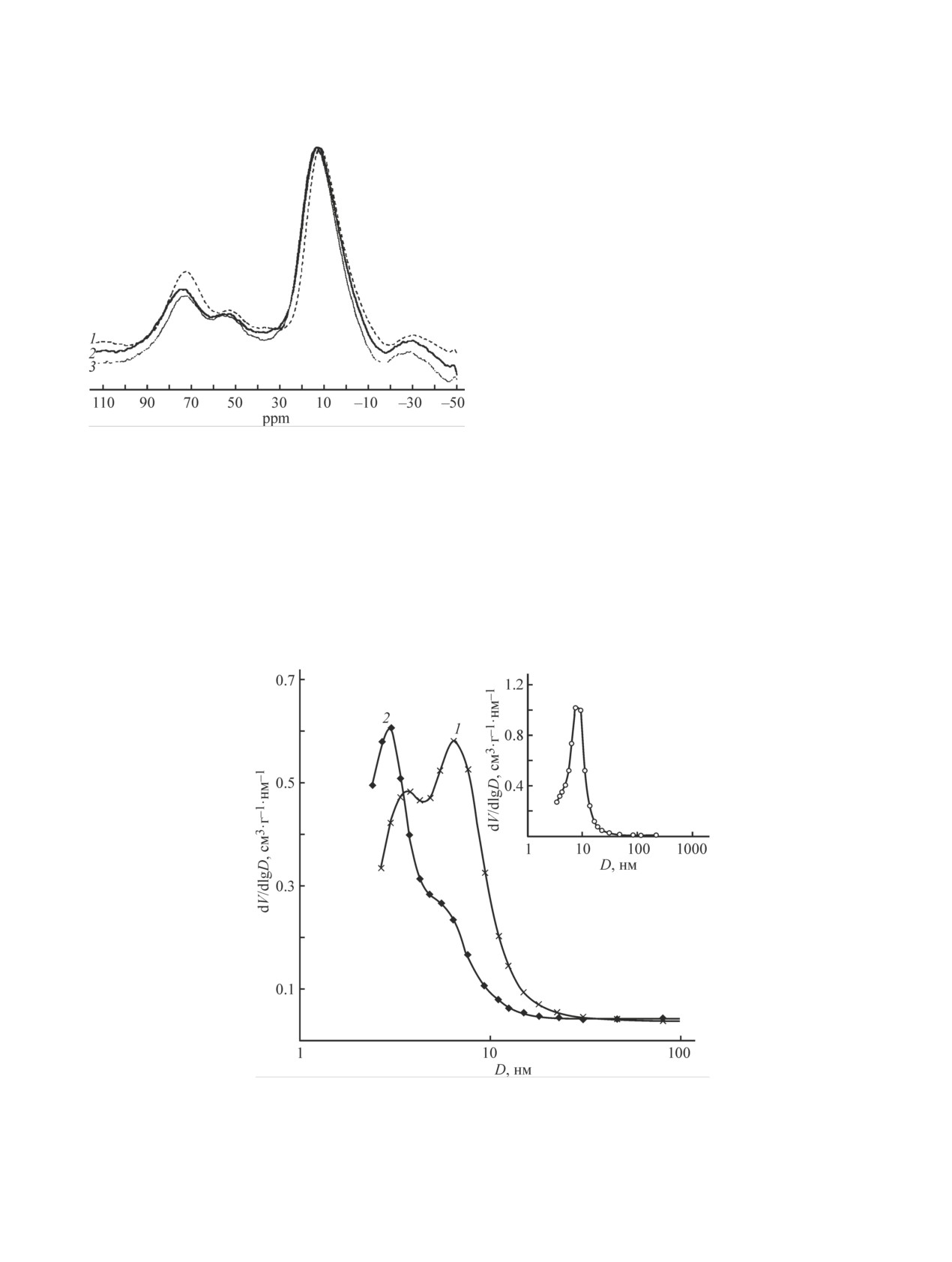
методом ЯМР (рис. 3). В спектре ЯМР γ-Al2O3 на-
Несмотря на близкое массовое содержание In и
блюдаются два пика в области 10 и 75 ppm, харак-
Cu, фаз, относящихся к соединениям Cu, обнаружено
теризующие состояние атомов Al в октаэдрическом
не было. Вероятно, оксидные формы Cu присутству-
и тетраэдрическом окружении атомов кислорода
ют в исследованных образцах в высокодисперсном
соответственно [12, 13]. В присутствии Ga при об-
состоянии.
разовании Ga2O3-Al2O3 наблюдается уменьшение
Полученные образцы оксидов имеют разви-
интенсивности пика, соответствующего тетраэдри-
тую текстуру с величиной удельной поверхности
ческому окружению при взаимодействии оксидов, в
~300 м2·г-1. По сравнению с образцом Al2O3(Ga-2),
Таблица 2
Фазовый состав образцов оксидов, полученных в процессе гравитационной седиментации из слоев осадков N1 и
N3 после прокаливания при 550°С
Образец
Фазовый состав
Параметр ячейки а, Å
Al2O3-N1
Al2O3 (PDF 01-074-2206)
7.941
In2O3 (PDF 01-071-2194)
10.129
Al2O3-N3
Al2O3 (PDF 01-074-2206)
7.943
In2O3 (PDF 01-071-2194)
10.125
268
Бельская О. Б. и др.
пор по размерам менее однородно (табл. 3, рис. 4).
Заметно увеличивается доля пор меньшего диаметра,
и на кривой распределения фиксируются пики, мак-
симумы которых соответствуют размерам пор 3.8 и
3.0 нм. Кроме того, большой вклад вносят крупные
мезопоры диаметром >20 нм. Вероятно, наблюдае-
мые различия связаны с химическим составом по-
лученных оксидных фаз. Ранее было показано [11,
12], что присутствие более узких пор может быть
результатом формирования агломератов частиц твер-
дого раствора Ga2O3-Al2O3. Увеличение содержания
Ga в образце способствует образованию твердого
раствора. Наличие в составе образцов Al2O3-N1 (N3)
оксидов In и Cu также может влиять на морфологию
оксидов.
Рис. 3. Спектры ЯМР 27Al образцов γ-Al2O3 (1),
При получении платинового катализатора с ис-
Al2O3-N1 (2) и Al2O3-N3 (3).
пользованием в качестве носителя прокаленного про-
дукта взаимодействия активированного технического
полученным из активированного сплава А0 [11],
алюминиевого сплава с водой нанесение Pt проводи-
образцы Al2O3-N1 (N3) характеризуются несколько
ли из раствора H2PtCl6·6H2O. После высушивания и
меньшим объемом порового пространства при мень-
прокаливания при 550°С процесс восстановления Pt
шем среднем значении диаметра пор (табл. 3). Хотя
на примере образца Al2O3-N1 был исследован мето-
основное поровое пространство всех исследованных
дом температурно-программируемого восстановле-
образцов формируется за счет мезопор размером до
ния. На профиле температурно-программируемого
10 нм, в случае Al2O3-N1 и Al2O3-N3 распределение
восстановления наблюдается четкий максимум погло-
Рис. 4. Кривые распределения объема пор по размерам для образцов, полученных из осадков в процессе гравита-
ционной седиментации продуктов реакции.
Al2O3-N1 (1) — верхний слой и Al2O3-N3 (2) — третий из четырех от поверхности слой продуктов седиментации.
На вставке — данные для образца Al2O3(Ga-2), полученного из активированного сплава А0 с содержанием Ga 2.2 мас%
и In 0.17 мас% [12].
Продукт взаимодействия активированных промышленных алюминиевых сплавов с водой...
269
Таблица 3
Основные текстурные характеристики оксидов алюминия
Объем пор,* см3·г-1 (%)
Удельная поверхность,
Адсорбционный
Средний диаметр
Образец
м2·г-1
объем пор, см3·г-1
пор, нм
3-10 нм
10-20 нм
> 20 нм
Al2O3(Ga-2) [22]
249
0.435
7.0
0.321 (77)
0.074 (18)
0.022 (5)
Al2O3-N1
280
0.381
5.4
0.279 (79)
0.030 (9)
0.044 (12)
Al2O3-N3
312
0.312
4.0
0.211 (76)
0.016 (6)
0.050 (18)
* Оценен из данных расчета кривых распределения пор по размерам (методом Баррета-Джойнера-Халенды).
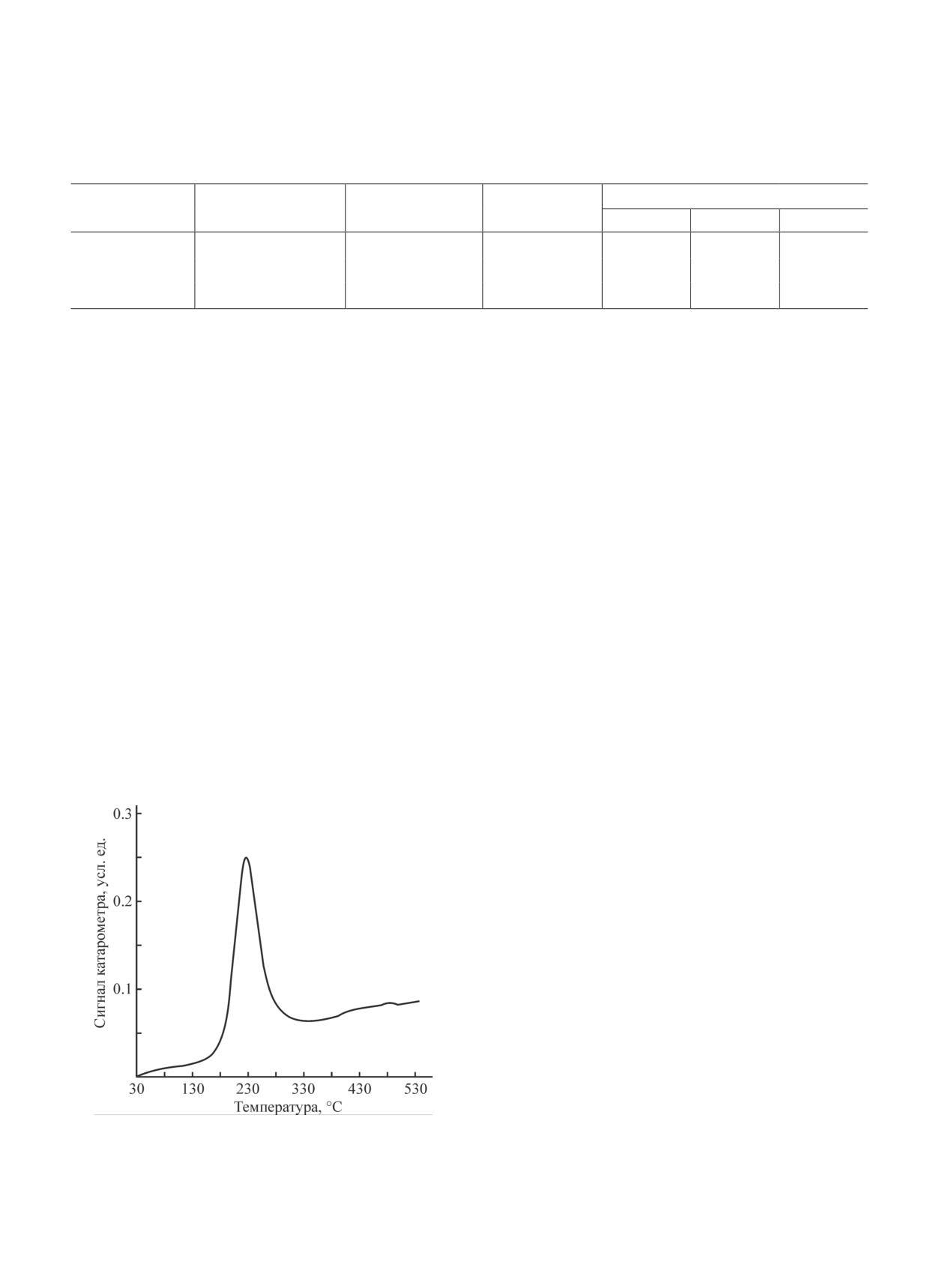
щения H2 при 230°С, характерный для восстановле-
что близко к значению, определенному ранее для
ния оксидных форм Pt на поверхности Al2O3 (рис. 5).
Al2O3(Ga-2) (56%) [11]. Следовательно, присутствие
Однако положение данного максимума смещено в
заметного количества примесных металлов (Ga, In,
область более высоких температур по сравнению с
Cu) не оказывает влияния на доступность частиц Pt.
ранее опубликованными данными для Pt, нанесенной
Перед тестированием полученного катализатора
на γ-Al2O3 и оксиды на основе сплава А0 [10, 11].
в модельной реакции дегидрирования пропана про-
Это может быть результатом взаимодействия Pt с
водили восстановление Pt в токе H2 при температуре
Al2O3 и (или) присутствующими в составе носителя
550°С, соответствующей температуре проведения
металлами. При проведении температурно-програм-
реакции дегидрирования пропана. Несколько более
мируемого восстановления наблюдается поглощение
высокая начальная конверсия при пониженной селек-
H2 во всей высокотемпературной области (до 550°С).
тивности образования пропилена (рис. 6, а), вероятно,
Заметное превышение количества поглощенного H2
связана с протеканием побочных реакций (рис. 6, б).
(460 мкмоль·г-1) относительно стехиометрии реак-
Однако после проведения тестовой реакции в течение
ции восстановления Pt (100 мкмоль·г-1) является
1 ч селективность образования пропилена состав-
подтверждением того, что помимо восстановления Pt
ляет 90-94% и соответствует данному параметру
происходит восстановление катионов других метал-
реакции дегидрирования пропана с использованием
лов, присутствующих в составе носителя.
катализатора 1%Pt/Al2O3(Ga-2) с меньшим содер-
Дисперсность нанесенной Pt в образце 1%Pt/
жанием Ga и In [10]. При этом выходы продуктов
Al2O3-N1, определенная методом хемосорбции H2 по-
С3+ и гидрогенолиза С—С-связей для катализатора
сле обработки образца в режиме температурно-про-
1% Pt/Al2O3-N1 ниже и составляют 1.2-0.5 и 0.2-
граммируемого восстановления, составляла 50%,
0.15 мас% соответственно.
Селективность образования пропилена на моно-
металлических платиновых катализаторах в данных
условиях реакции не превышает 60 мас% вследствие
интенсивного протекания гидрогенолиза С—С-связей
[10, 14]. Модифицирование Pt компонентами носи-
теля приводит к увеличению селективности. Важно
подчеркнуть, что все основные примесные катио-
ны — Ga, In и Cu, присутствующие в продукте взаи-
модействия активированного технического сплава с
водой, модифицируют платиновые центры в реакциях
дегидрирования алканов [15-18]. Данные модифи-
каторы вводятся либо при формировании носителя,
либо совместно с предшественником Pt. В условиях
восстановительной предобработки (550-650°С) со-
единения металлов частично или полностью вос-
станавливаются с образованием с Pt либо твердых
растворов (в случае Cu), либо сплавов (в случае Ga и
In). При этом лишь интерметаллиды определенного
Рис. 5. Профиль температурно-программируемого вос-
становления образца PtОх/Al2O3-N1, прокаленного при
состава обладают высокой дегидрирующей активно-
550°С.
стью [15, 16].
270
Бельская О. Б. и др.
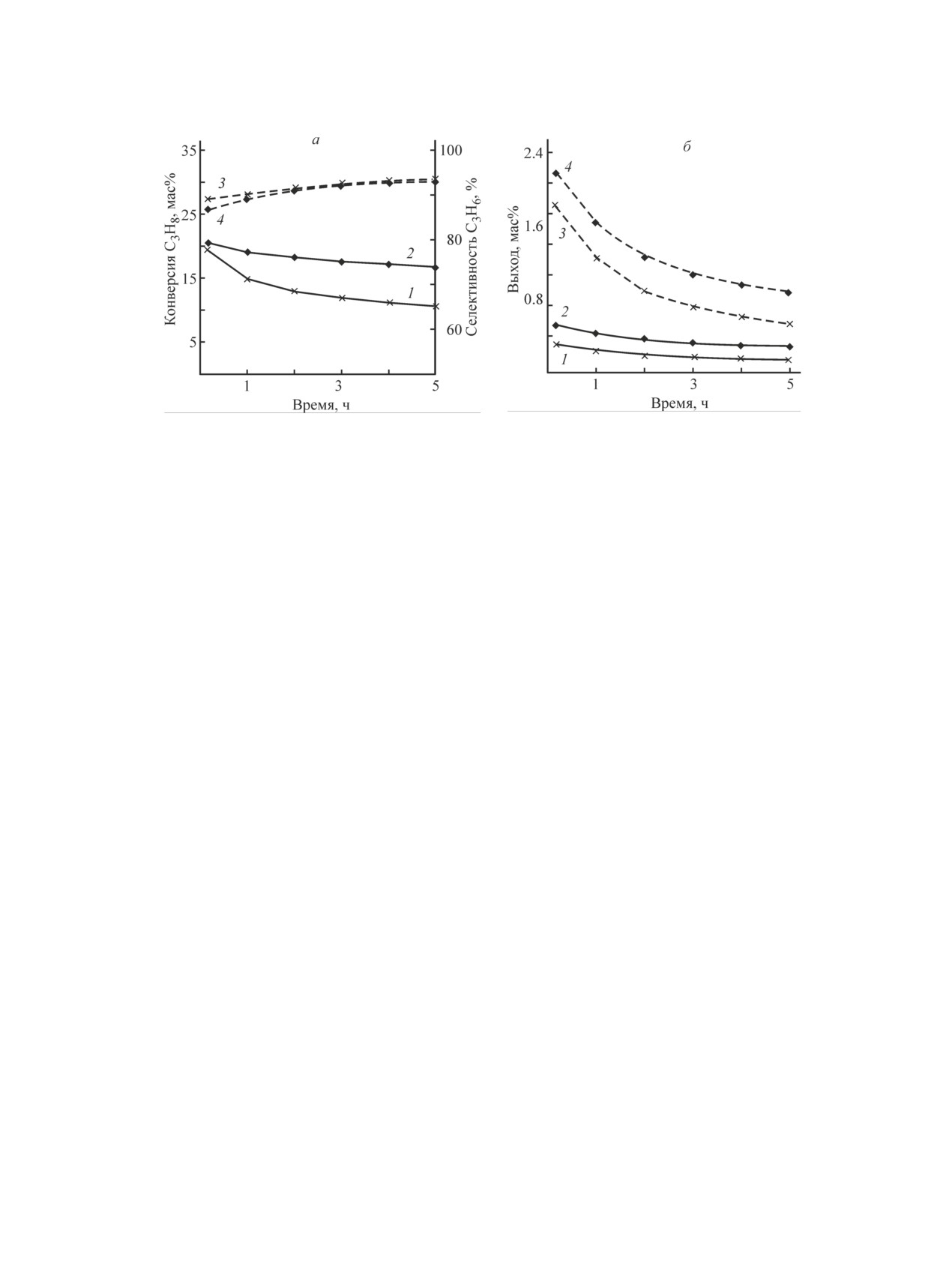
Рис. 6. Каталитические характеристики образцов 1% Pt/Al2O3(Ga-2) (2, 4) и 1% Pt/Al2O3-N1 (1, 3) в реакции деги-
дрирования пропана.
Т = 550°C, атмосферное давление, Н2:С3Н8 = 0.25, массовая скорость подачи сырья 8 г·ч-1.
Катализатор, полученный с использованием тех-
доочистке при 60°C в стеклянной емкости дистил-
нического алюминиевого сплава, является менее
лированной водой при постоянном перемешивании.
активным и менее стабильным в выбранных реак-
Критерием завершения очистки эвтектики от при-
ционных условиях по сравнению катализатором на
месей, затрудняющих ее дальнейшее использование
основе сплава А0, также модифицированного Ga-In
для активирования, было прекращение выделения
эвтектикой (рис. 6). Как было показано выше, алю-
газовых пузырьков. Затем полученную эвтектику
мооксидный носитель катализатора 1%Pt/Al2O3-N1
отделяли от осадка и многократно промывали ди-
содержит большее количество модифицирующих
стиллированной водой и этиловым спиртом, после
металлов, и, возможно, в данном случае соотношение
чего высушивали при Т = 25°С. Регенерированная
модификатор/платина и (или) условия предобработки
таким методом Ga-In эвтектика имела характерный
являются неоптимальными. Для уточнения данных
зеркальный блеск, сохранявшийся в течение продол-
о максимально допустимом содержании компонен-
жительного времени.
тов-модификаторов при их совместном присутствии
необходимо выяснение индивидуального влияния
Выводы
каждого из них на характеристики носителя и нане-
сенной Pt.
Побочный продукт, образующийся при взаимодей-
Важной задачей при создании водородных кар-
ствии активированных технических сплавов алюми-
триджей является регенерация загрязненной в про-
ния с водой в реакции получения H2, может быть ис-
цессе активирования алюминиевых сплавов Ga-In эв-
пользован (наряду с чистым алюминиевым сплавом)
тектики, являющейся активирующим агентом. После
в качестве предшественника носителя катализаторов,
проведения реакции активированных материалов с
поскольку обеспечивает формирование необходимых
водой остатки эвтектики, загрязненные непрореаги-
структурных и текстурных свойств оксидной фазы.
ровавшими частицами, собираются на дне емкости.
Свойства платинового катализатора данной серии
Для регенерации эвтектики образовавшийся осадок
(на основе образца N1) близки к описанным в пре-
непрореагировавших частиц алюминия с эвтектикой
дыдущих работах авторов. Основными примесями в
объединяли с эвтектикой, которую удаляли с поверх-
составе алюмооксидного носителя, полученного на
ности образцов после их активации как избыточную.
основе активированных технических алюминиевых
Затем полученную смесь заливали дистиллированной
сплавов, являются металлы (Ga, In, Cu), способные
водой при Т = 50-70°C. После выдержки в стеклян-
взаимодействовать с Pt и изменять ее каталитиче-
ной емкости в течение нескольких суток происходило
ские свойства в реакции дегидрирования пропана,
расслоение системы, а на поверхности формиро-
обеспечивая высокую селективность образования
вался пористый слой смеси гидроксидов алюминия.
пропилена. В то же время обнаруженный эффект
Эвтектику отделяли и подвергали дополнительной
дезактивации катализатора в данной реакции тре-
Продукт взаимодействия активированных промышленных алюминиевых сплавов с водой...
271
бует проведения дополнительных исследований для
Бухтияров Валерий Иванович, д.х.н., академик
выяснения его причины и установления диапазона
РАН,
концентраций примесных металлов, при котором не
происходит ухудшения текстурных и каталитических
свойств катализатора.
Список литературы
[1]
Deng Z-Y., Ferreira J. M. F., Sakka Y. Hydrogen
Благодарности
generation materials for portable applications // J. Am.
Ceram. Soc. 2008. V. 91. N 12. P. 3825-3834.
Авторы выражают благодарность Е. Н. Кудре за
определение размера частиц методом лазерной диф-
[2]
Ouyang L., Jiang J., Chen Zhu K. M., Liu Z. Hydrogen
ракции, О. В. Маевской за участие в синтезе катали-
production via hydrolysis and alcoholysis of light
заторов, к.х.н. Л. Н. Степановой за их тестирование
metal-based materials: A Review // Nano-Micro Lett.
в каталитической реакции.
2021. V. 13. P. 134-164.
[3]
Wang H. Z., Leung D. Y. C., Leung M. K. H., Ni M.
A review on hydrogen production using aluminum and
Финансирование работы
aluminum alloys // Renew. Sust. Energ. Rev. 2009.
Работа выполнена при финансовой поддержке
V. 13. N 4. P. 845-853.
Министерства науки и высшего образования РФ в рам-
ках государственного задания Института катализа им.
[4]
Parmuzina A. V., Kravchenko O. V. Activation of
Г. К. Борескова СО РАН (проекты AAAA-A21-12101139
aluminium metal to evolve hydrogen from water // Int.
0009-1, AAAA-A21-12101149 0008-3).
J. Hydrogen Energy. 2008. V. 33. P. 3073-3076.
[5]
Razavi-Tousi S. S., Szpunar J. A. Effect of addition
Конфликт интересов
of water-soluble salts on the hydrogen generation of
aluminum in reaction with hot water // J. Alloys Compd.
Авторы заявляют об отсутствии конфликта инте-
2016. V. 679. P. 364-374.
ресов, требующего раскрытия в данной статье.
[6]
Шейндлин А. Е., Жук А. З. Концепция алюмоводо-
родной энергетики // Рос. хим. журн. 2006. Т. L.
Информация о вкладе авторов
№ 6. С. 105-108 [Sheindlin A. E., Zhuk A. Z. Concept
of aluminum hydrogen energy industry // Russ. J. Gen.
О. Б. Бельская — обобщение результатов экспе-
Chem. 2007. V. 77. P. 778-782.
риментальных исследований; А. И. Низовский —
приготовление активированного алюминия, по-
[7]
Trowell K. A., Goroshin S., Frost D. L.,
лучение продукта его взаимодействия с водой;
Bergthorson J. M. The use of supercritical water for the
Т. И. Гуляева — выполнение экспериментов по низ-
catalyst-free oxidation of coarse aluminum for hydrogen
котемпературной адсорбции азота, температурно-про-
production // Sust. Energy Fuels. 2020. V. 4. N 11.
граммируемого восстановления, хемосорбции водо-
P. 5628-5635.
рода; И. В. Муромцев — выполнение экспериментов
по рентгенофазовому анализу; В. И. Бухтияров —
[8]
Macanás J., Soler L., Candela A. M., Muñoz M.,
концепция работы.
Casado J. Hydrogen generation by aluminum corrosion
in aqueous alkaline solutions of inorganic promoters:
The AlHidrox process // Energy. 2011. V. 36. N 5.
Информация об авторах
P. 2493-2501.
Бельская Ольга Борисовна, к.х.н.,
[9]
Тренихин М. В., Бубнов А. В., Низовский А. И.,
Дуплякин В. К. Взаимодействие эвтектики системы
Низовский Александр Иванович, к.х.н., доцент,
In-Ga c алюминием и его сплавами // Неорган. мате-
риалы. 2006. Т. 42. № 3. С. 298-303 [Trenikhin M. V.,
Гуляева Татьяна Ивановна,
Bubnov A. V., Nizovskii A. I., Duplyakin V. K. Chemical
interaction of the In-Ga eutectic with Al and Al-base
Муромцев Иван Владимирович,
alloys // Inorg. Mater. 2006. V. 42. N 3. P. 256-260.
272
Бельская О. Б. и др.
[10]
Бельская О.Б., Низовский А.И., Гуляева Т.И.,
[13]
Kwak J. H., Hu J. Z., Kim D. H. Szanyi J.,
Бухтияров В.И. Оксид алюминия, полученный с
Peden C. H. F. Penta-coordinated Al3+ ions as
использованием активированного алюминия, как
preferential nucleation sites for BaO on γ-Al2O3: An
носитель платиновых катализаторов // ЖПХ. 2018.
ultra-high-magnetic field 27Al MAS NMR study // J.
Т. 91. № 11. С. 1602-1609.
Catal. 2007. V. 251. P. 189-194.
[Belskaya O. B., Nizovskii A. I., Gulyaeva T. I.,
[14]
Ma Z., Wu Z., Miller J. T. Effect of Cu content
Bukhtiyarov V. I. Aluminum oxide produced with the
on the bimetallic Pt-Cu catalysts for propane
use of activated aluminum as support for platinum
dehydrogenation. Catalysis // Structure & Reactivity.
catalysts // Russ. J. Appl. Chem. 2018. V. 91. N 11.
2017. V. 3. N 1-2. P. 43-53.
P. 1814-1820.
[15]
Filez M., Redekop E. A., Poelman H., Galvita V. V.,
[11]
Бельская О. Б., Низовский А. И., Гуляева Т. И.,
Meledina M., Turner S., Van Tendeloo G.,
Леонтьева Н. Н., Бухтияров В. И. Катализаторы
Detavernierc C., Marina G. B. One-pot synthesis of
Pt/(Ga)Al2O3, полученные с использованием метал-
Pt catalysts based on layered double hydroxides: An
лического алюминия, активированного галлием //
application in propane dehydrogenation // Catal. Sci.
ЖПХ. 2020. Т. 93. № 1. С. 132-141.
Technol. 2016. V. 6. P. 1863-1869.
[Belskaya O. B., Nizovskii A. I., Gulyaeva T. I., Leontʹeva
[16]
Wegener E. C., Wu Z., Tseng H-T., Gallagher J. R.,
N. N., Bukhtiyarov V. I. Сatalysts Pt/(Ga)Al2O3
Ren Y., Diaz R. E., Ribeiro F. H., Miller J. T.
obtained using aluminum metal activated with gallium
Structure and reactivity of Pt-In intermetallic alloy
// Russ. J. Appl. Chem. 2020. V. 93. N 1. P. 118-126.
nanoparticles: Highly selective catalysts for ethane
dehydrogenation // Catal. Today. 2018. V. 299. P. 146-
[12]
Афонасенко Т. Н., Леонтьева Н. Н., Талзи В. П.,
Смирнова Н. С., Савельева Г. Г., Шилова А. В.,
[17]
Tolek W., Suriye K., Praserthdam P., Panpranot J.
Цырульников П. Г. Синтез и свойства твердого рас-
Effect of preparation method on the Pt-In modified
твора γ-Ga2O3-Al2O3 // ЖФХ. 2017. Т. 91. № 10.
Mg(Al)O catalysts over dehydrogenation of propane
С. 1712-1718.
// Catal. Today. 2020. V. 358. P. 100-108.
[Afonasenko T. N., Leont′eva N. N., Talzi V. P.,
[18]
Passos F. B., Lopes I. S., Silva P. R. J., Saitovitch H.
Savel′eva G. G., Shilova A. V., Tsyrul′nikov P. G.,
Hyperfine interactions studies on Pt-In/Nb2O5
Smirnova N. S. Synthesis and properties of γ-Ga2O3-
catalysts // Catal. Today. 2003. V. 78. P. 411-417.
Al2O3 solid solution // Russ. J. Phys. Chem. A. 2017.
V. 91. N 10. P. 1939-1945.