444
Драчук А. О. и др.
Журнал прикладной химии. 2022. Т. 95. Вып. 4
УДК 536.421.4:548.562
ПОЛУЧЕНИЕ ГИДРАТОВ ДИОКСИДА УГЛЕРОДА
С ИСПОЛЬЗОВАНИЕМ ЗАМОРОЖЕННЫХ ВОДНЫХ РАСТВОРОВ
ПОЛИВИНИЛОВОГО СПИРТА
© А. О. Драчук1,2, Н. С. Молокитина1,3, А. А. Кибкало1,2, Л. С. Поденко1
1 Институт криосферы Земли Тюменского научного центра СО РАН,
625026, г. Тюмень, ул. Малыгина, д. 86
2 Тюменский государственный университет,
625003, г. Тюмень, ул. Володарского, д. 6
3 Казанский Приволжский федеральный университет,
625003, г. Казань, ул. Кремлевская, д. 18
Поступила в Редакцию 13 мая 2022 г.
После доработки 22 июня 2022 г.
Принята к публикации 5 июля 2022 г.
Изучена кинетика образования гидратов диоксида углерода в замороженных водных растворах по-
ливинилового спирта. Установлено превышение степени перехода воды в гидрат диоксида углерода в
замороженных водных растворах поливинилового спирта по сравнению с дисперсным льдом. Показано,
что значения скорости и степени перехода воды в гидрат в статических условиях гидратообразования
(без перемешивания) в замороженных водных растворах поливинилового спирта могут быть больше
по сравнению с водными растворами поверхностно-активных веществ, порошковыми криогелями
поливинилового спирта, микрокапельными дисперсными системами («сухой водой») при сравнимых
условиях гидратообразования.
Ключевые слова: газовые гидраты; кинетика гидратообразования; улавливание диоксида углерода;
поливиниловый спирт; замороженные растворы; дисперсный лед
DOI: 10.31857/S0044461822040041, EDN: DGUOLL
Одним из экономически перспективных направле-
может протекать быстрее и с большей степенью пере-
ний развития технологий улавливания и захоронения
хода воды в гидрат по сравнению с перспективными
СО2, образующегося в результате промышленной
для применения в газогидратных технологиях хра-
деятельности, является применение процессов гидра-
нения и транспортировки газа системами (например,
тообразования [1-4]. Однако низкая скорость и сте-
водные растворы поверхностно-активных веществ,
пень перехода воды в гидрат и наличие значительной
микрокапельная дисперсная система «сухая вода»
задержки начала гидратообразования в статических
[10] и порошковые криогели поливинилового спирта).
условиях в жидкой воде [5] препятствуют масштаб-
Можно ожидать, что в случае образования гидратов
ному применению газовых гидратов для улавлива-
СО2 скорость и степень перехода воды в гидрат также
ния СО2. Образование газовых гидратов в условиях
возрастут в результате замены льда на замороженный
плавления льда протекает без заметной задержки
водный раствор поливинилового спирта.
[6, 7]. В наших работах [8, 9] было показано, что
Цель работы — установление характера влияния
образование гидратов метана в замороженном вод-
добавки поливинилового спирта на скорость и сте-
ном растворе поливинилового спирта в статических
пень перехода воды в гидрат СО2 в замороженных
условиях гидратообразования (без перемешивания)
водных растворах поливинилового спирта.
Получение гидратов диоксида углерода с использованием замороженных водных растворов поливинилового спирта
445
Экспериментальная часть
получения после его размораживания порошкового
криогеля [12].
Дистиллированная вода (аквадистиллятор элек-
Микрокапельная дисперсная система «сухая вода»
трический, ООО ПФ «Ливам»), поливиниловый
была получена методом, описанным Wang W. et al.
спирт (средняя молекулярная масса 86 000 Да, класс
[13], с использованием дистиллированной воды и
16/1, ОАО «Невинномысский Азот»), гидрофоби-
аэросила R202 в количестве 95 и 5 г соответственно.
зированные пирогенные наночастицы кремнезема
Образование гидратов СО2 происходило в реакто-
(аэросил R202 Evonik Industries AG, удельная по-
ре из нержавеющей стали объемом 60 см3. Подробное
верхность 80-120 м2·г-1, средний размер частиц
описание экспериментальной установки для получе-
14 нм), додецилсульфат натрия чистотой 99.9 мас%
ния газовых гидратов и изучения кинетики их роста
(АО «ЛенРеактив») и газообразный СО2 (99.9 об%,
было описано ранее [9].
ОАО «Завод Уралтехгаз») были использованы для
Получение гидратов СО2 выполняли следующим
получения гидратов СО2.
образом. 7 г дистиллированной воды, водного раство-
Для приготовления дисперсного льда, дисперсно-
ра додецилсульфата натрия (0.1 мас%), порошкового
го замороженного водного раствора поливинилово-
криогеля или «сухой воды» загружали в реактор при
го спирта и порошкового криогеля поливинилового
комнатной температуре, реактор помещали в тер-
спирта дистиллированную воду и свежеприготовлен-
морегулируемую ванну с заданной температурой
ные на паровой бане при 343 K растворы поливини-
293.2 K и затем в реактор подавали СО2 до давле-
лового спирта замораживали при температуре 253 K.
ния ~2.2 МПа. После того как температура образца
В наших работах было показано, что при концентра-
и давление в реакторе стабилизировались, реактор
ции поливинилового спирта 3 мас% скорость роста
изохорно охлаждали со скоростью 0.3 град·мин-1 до
гидратов метана в замороженных водных растворах
273.2 K и выдерживали при этой температуре необхо-
поливинилового спирта оказалась выше, чем при кон-
димое для начала гидратообразования время и затем
центрации 1 и 2 мас% [8]. Предполагая наличие кон-
дополнительно не менее 150 мин либо до момента
центрационной зависимости скорости роста гидратов
стабилизации давления.
СО2, замороженный водный раствор поливинилового
7 г молотого замороженного водного раствора
спирта готовили из раствора концентрацией 3.0 мас%.
поливинилового спирта или дисперсного льда загру-
Порошковый криогель готовили из раствора концен-
жали в реактор при 263.2 K в термостатированной
трацией 7 мас%. Растворы концентрацией 7 мас%
камере (TELEDOOR Melle Isoliertechnik GmbH), за-
поливинилового спирта могут образовывать крио-
тем реактор помещали в терморегулируемую ванну
генно-структурированный полимерный материал,
с заданной температурой 263.2 K. Выбор начальной
так называемые криогели, если проводится процесс
температуры реактора обусловлен тем, что скорость
криотропного гелеобразования [11]. Методика полу-
перехода льда в гидрат СО2 при температуре ≤260 K
чения криогеля состоит в замораживании исходного
низкая [14], и это позволяет минимизировать гидрато-
раствора, его выдержке в течение определенного вре-
образование на этапе напуска газа в реактор. Затем в
мени и оттаивании. Растворы поливинилового спирта
реактор подавали СО2 до давления ~2.2 МПа, превы-
замораживали и выдерживали при температуре 258 K
шающего равновесное давление образования гидра-
не менее 10 ч. Затем при этой же температуре лед
тов СО2 во льду при температуре 263.2 K (0.75 МПа)
и замороженные водные растворы поливинилового
(в наших работах на примере гидратов метана показа-
спирта измельчали в бытовом блендере Braun VX2050
но, что наличие поливинилового спирта в воде суще-
со скоростью 18700 об·мин-1 в течение 30 с. В случае
ственно не влияет на термодинамические параметры
приготовления порошкового криогеля измельчение
гидратообразования [9]). После этого реактор нагре-
осуществлялось с добавлением частиц стабилизатора
вали со скоростью 0.25 град·мин-1 до температуры
(5 мас%). Для получения гидратов и изучения кине-
269.5, 271.2 или 272.2 K и выдерживали при конечной
тики их роста использовалась фракция с размером
температуре в течение 150 мин либо до момента ста-
частиц замороженных водных растворов поливини-
билизации давления.
лового спирта или льда 80-140 мкм, выделенная на
Количество молей метана (ΔH), поглощенных за
электродинамическом вибростенде ПЭ-6700 (ООО
счет гидратообразования, рассчитывали по умень-
«ЭКРОСХИМ») с частотой 20 Гц при температуре
шению давления метана в газовой фазе в реакто-
258 K. Фракционированные образцы, содержащие
ре с использованием уравнения состояния Пенга-
7 мас% поливинилового спирта, нагревали до комнат-
Робинсона [15]. Предполагая, что состав гидратов
ной температуры со скоростью 0.03 град·мин-1 для
СО2 определялся стехиометрическим соотношением
446
Драчук А. О. и др.
CО2·7.3·Н2О, коэффициент превращения воды в ги-
степень перехода воды в гидрат была наибольшей в
драт (Δh) был рассчитан по формуле
образцах «сухой воды» (рис. 2).
, полученного в «сухой во-
Образцы гидрата СО2
Δh = (7.3·ΔН·Мw)/mw,
(1)
де», представляли собой смесь монолитного твердого
тела и сыпучего порошка (рис. 3, а), так же как и в
где Мw — молярная масса воды, mw — исходная мас-
случае гидратов метана, полученных в «сухой воде»,
са воды в образце.
содержащей 5 мас% R202 [16]. Образцы, полученные
Время индукции гидратообразования принимали
в порошковом криогеле, после извлечения из реак-
за интервал времени с момента перехода системы в
тора распадались на отдельные части, которые при
зону стабильности (давление-температура) гидрата
незначительном механическом воздействии рассы-
и до тех пор, пока Δh не превысил 0.01.
пались в порошок (рис. 3, б).
В экспериментах по получению гидратов в образ-
цах дисперсного льда и замороженного водного рас-
Обсуждение результатов
твора поливинилового спирта наблюдали выраженное
В образцах дистиллированной воды, водного рас-
снижение давления в реакторе сразу после напуска
твора додецилсульфата натрия (0.1 мас%), порошко-
газа (рис. 4). Дальнейший нагрев реактора и выдер-
вого криогеля или «сухой воды» наблюдали линейное
живание его при постоянной температуре (269.2 или
уменьшение давления в реакторе при его охлаждении
271.2 K) также сопровождались снижением давления
от 293.2 до 273.2 K со скоростью 0.3 град·мин-1, об-
во всех экспериментах, свидетельствующим о проте-
условленное понижением температуры газа. После
кании процесса гидратообразования.
установления постоянной температуры 273.2 K
В случае образцов, нагретых до 269.2 K, скорость
давление в реакторе стабилизировалось выше рав-
перехода воды в гидрат монотонно уменьшалась как
новесной температуры образования гидратов СО2
в образцах дисперсного льда, так и в образцах замо-
(1230 кПа). Затем давление резко снижалось в резуль-
роженного водного раствора поливинилового спирта
тате гидратообразования (рис. 1). Величина времени
(рис. 5, кривые 1 и 3). Такое поведение характерно
индукции гидратообразования после установления
для перехода льда в газовый гидрат [14]. Температура
температуры 273.2 K имела случайный характер и
образцов льда и замороженного водного раствора
изменялась от 50 до 900 мин в дистиллированной во-
поливинилового спирта на протяжении всего про-
де, растворе додецилсульфата натрия и «сухой воде»,
цесса гидратообразования не превышала 269.5 K, при
а в порошковом криогеле не превышала нескольких
этом давление в реакторе оставалось ниже 2.2 МПа.
минут.
Согласно фазовой диаграмме плавления льда в ат-
На протяжении всего времени гидратообразования
мосфере СО2 [17], при гидратообразовании не возни-
степень перехода воды в гидрат в образцах «сухой во-
кало условий для плавления льда. Степень перехода
ды» и порошкового геля, рассчитанная на основании
данных изменения давления и температуры газа в ре-
акторе, была в разы больше, чем в дистиллированной
воде и растворе додецилсульфата натрия, при этом
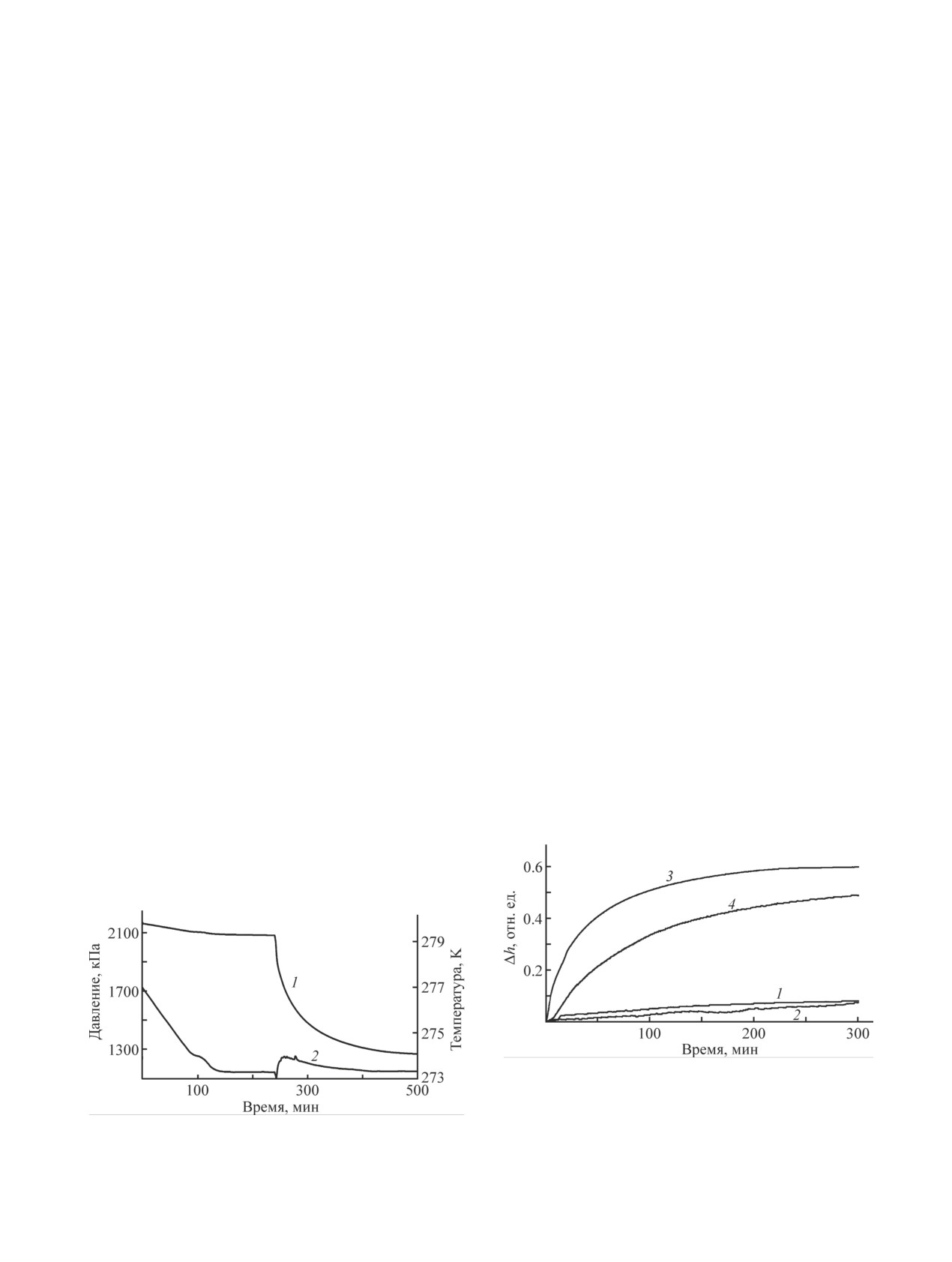
Рис. 2. Характерные кривые изменения степени пере-
хода воды в гидрат в образцах дистиллированной воды
(1), раствора додецилсульфата натрия (2), «сухой воды»
(5.0 мас% R202) (3), порошкового криогеля (4) сразу
Рис. 1. Характерные кривые изменения давления СО2
(1) и температуры образца (2) в образце «сухой воды»
после начала гидратообразования.
(5.0 мас% R202), изохорные условия.
Температура 273.2 K, начальное давление 2.1-2.2 МПа.
Получение гидратов диоксида углерода с использованием замороженных водных растворов поливинилового спирта
447
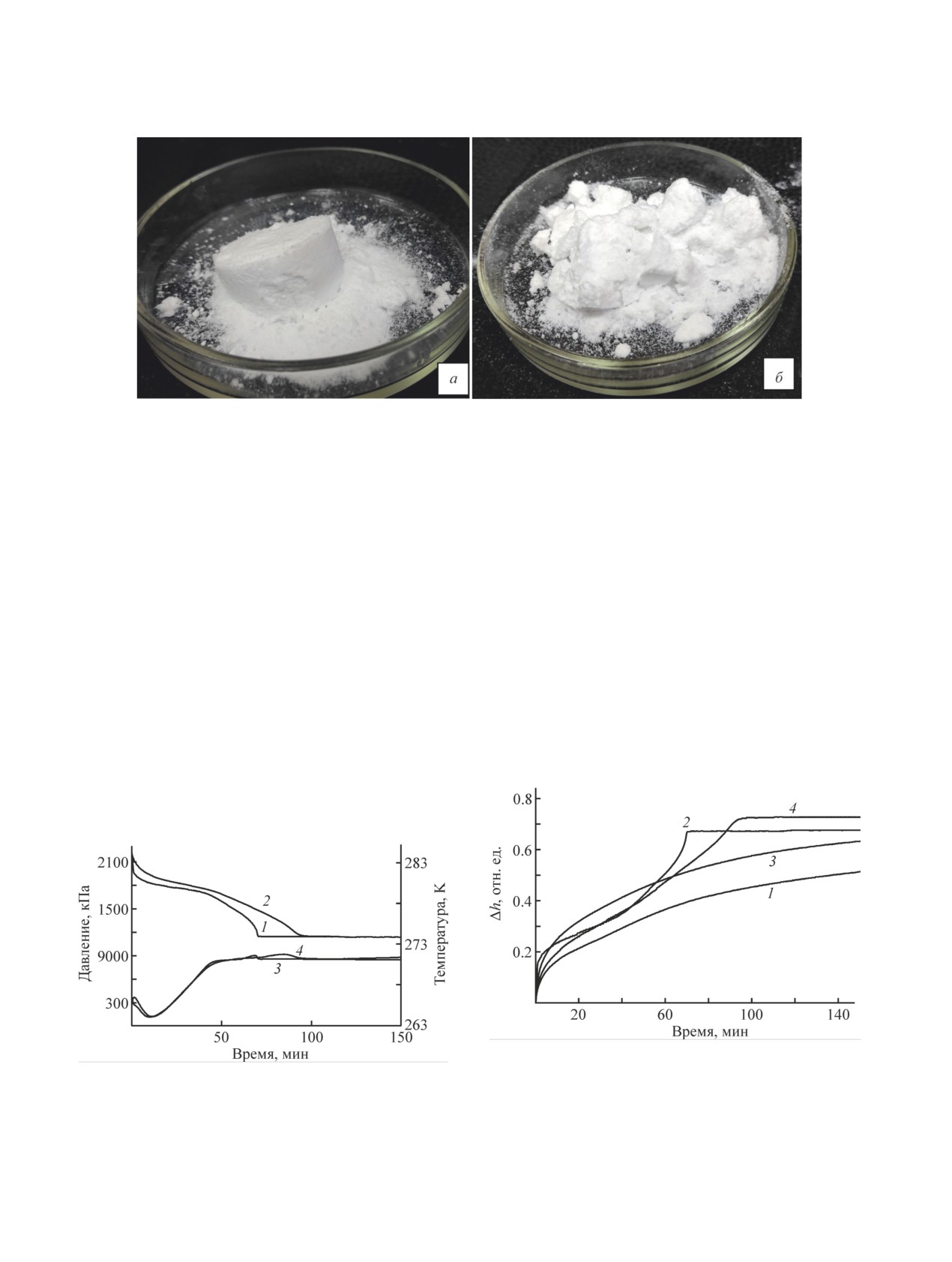
Рис. 3. Изображения образцов «сухой воды» (5.0 мас% R202) (а), порошкового криогеля поливинилового спирта
(б), извлеченных из реактора сразу после завершения гидратообразования.
Извлечение происходило при комнатной температуре.
воды в гидрат в образцах замороженного водного
условиям плавления льда в образцах замороженно-
раствора поливинилового спирта была выше, чем
го водного раствора поливинилового спирта и льда
в образцах дисперсного льда, на протяжении всего
спустя 50 мин после напуска газа [17]. Известно, что
процесса гидратообразования (рис. 5, кривые 1 и 3).
в условиях плавления льда скорость перехода воды в
По-видимому, поливиниловый спирт препятствует
гидрат значительно возрастает [6, 7]. Следовательно,
формированию сплошной непроницаемой для газа и
наблюдаемый рост скорости гидратообразования обу-
воды гидратной корки на поверхности частиц льда.
словлен плавлением льда, содержащегося в образцах.
В случае нагрева образцов льда и замороженного
Значения степени перехода воды в гидрат в ста-
водного раствора поливинилового спирта до 271.2 K
тических условиях гидратообразования (без переме-
наблюдали значительное увеличение скорости пере-
шивания) в замороженных водных растворах поли-
хода воды в гидрат спустя ~50 мин после напуска газа
винилового спирта (0.73) были больше по сравнению
(рис. 5). В этот момент времени температура образ-
с объемной водой (0.06), водными растворами по-
цов составляла 271.2 K, давление — 1600 и 1690 кПа
верхностно-активных веществ (0.04), порошковыми
в дисперсном льду и замороженном водном раство-
ре поливинилового спирта соответственно (рис. 4).
Эти термодинамические параметры соответствуют
Рис. 5. Изменение степени перехода воды в гидрат СО2
в образцах дисперсного льда (1, 2), замороженного вод-
Рис. 4. Характерные кривые изменения давления СО2 (1,
ного раствора поливинилового спирта (3, 4) при их
2) и температуры (3, 4) образцов дисперсного льда (1,
нагреве от 263.2 до 269.2 (1, 3) и 271.2 K (2, 4) со скоро-
3) и замороженного водного раствора поливинилового
стью 0.25 град·мин-1 и дальнейшем выдерживании при
спирта (2, 4) при их нагреве от 263.2 до 271.2 K со ско-
постоянной температуре.
ростью 0.25 град·мин-1 и дальнейшем выдерживании
при постоянной температуре, изохорные условия.
Изохорные условия, начальное давление 2.2 МПа.
448
Драчук А. О. и др.
Степень перехода воды в гидрат СО2 Δh0 спустя 150 мин после начала гидратообразования
Начальное давление около 2.2 МПа, изохорный режим
Материал
Температурный режим
Δh0, отн. ед.
Дистиллированная вода
273.2 K
0.06
Водный раствор додецилсульфата натрия (0.1 мас%)
273.2 K
0.04
«Сухая вода» (5.0 мас% R202)
273.2 K
0.55
Порошковый криогель поливинилового спирта (5.0 мас% R202,
273.2 K
0.40
7.0 мас% поливинилового спирта)
Дисперсный лед
269.2 K (нагрев от 263.2 K)
0.50
271.2 K (нагрев от 263.2 K)
0.68
Замороженный водный раствор поливинилового спирта (3.0 мас%)
269.2 K (нагрев от 263.2 K)
0.63
271.2 K (нагрев от 263.2 K)
0.73
криогелями поливинилового спирта (0.40), «сухой
Информация об авторах
водой» (0.55), дисперсным льдом (0.68) при сравни-
Драчук Андрей Олегович, к.ф.-м.н.
мых условиях гидратообразования (см. таблицу). По-
видимому, причина ускорения образования гидратов
Молокитина Надежда Сергеевна, к.т.н.
СО2 в замороженных водных растворах поливини-
лового спирта по сравнению с замороженной чистой
Кибкало Александр Андреевич
водой такая же, как и в случае образования гидратов
пропана в замороженных водных растворах поли-
Поденко Лев Степанович, к.ф.-м.н.
винилового спирта, а именно формирование более
мелких кристаллов гидратов [18].
Список литературы
Выводы
[1] DʹAlessandro D. M., Smit B., Long J. R. Carbon dioxide
Использование замороженных водных растворов
capture: Prospects for new materials // Angew. Chem.
поливинилового спирта для получения гидратов СО2
Int. Ed. 2010. V. 49. P. 6058-6082.
позволяет увеличить скорость и степень перехода
воды в гидрат в статических условиях гидратообра-
[2] Nguyen N. N., La V. T., Huynh C. D., Nguyen A. V.
зования (без перемешивания) по сравнению с во-
Technical and economic perspectives of hydrate-based
дными растворами поверхностно-активных веществ,
carbon dioxide capture // Appl. Energy. 2022. V. 307.
ID 118237.
порошковыми криогелями поливинилового спирта,
«сухой водой» при сравнимых условиях гидратообра-
[3] Li A., Wang J., Bao B. High-efficiency CO2 capture and
зования. Полученные результаты свидетельствуют
separation based on hydrate technology: A review //
о возможности и перспективности использования
Greenhouse Gas: Sci. Technol. 2019. V. 9. P. 175-193.
дисперсных замороженных водных растворов по-
ливинилового спирта в технологиях улавливания и
[4] Wang X., Zhang F., Lipiʹnski W. Research progress and
захоронения СО2 в форме газовых гидратов.
challenges in hydrate-based carbon dioxide capture
applications // Appl. Energy. 2020. V. 269. ID 114928.
Финансирование работы
[5] Zhang J., Lee J. W. Enhanced kinetics of CO2 hydrate
formation under static conditions // Ind. Eng. Chem.
Работа выполнена при поддержке госзадания
Res. 2009. V. 48. P. 5934-5942.
№ 121041600040-3.
[6] Hwang M. J., Wright D. A., Kapur A., Holder G. D.
An experimental-study of crystallization and crystal
Конфликт интересов
growth of methane hydrates from melting // J. Inclusion
Авторы заявляют об отсутствии конфликта инте-
Phenom. Mol. Recognit. Chem. 1990. V. 8. P. 103-116.
ресов, требующего раскрытия в данной статье.
Получение гидратов диоксида углерода с использованием замороженных водных растворов поливинилового спирта
449
[7]
Stern L. A., Kirby S. H., Durham W. B. Peculiarities of
summary and modeling extended to low temperatures
methane clathrate hydrate formation and solid-state
// J. Phys. Chem. C. 2013. V. 117. N 16. P. 8443-8457.
deformation, including possible superheating of water
ice // Science. 1996. V. 273. N 5283. P. 1843-1848.
[15]
Peng D., Robinson D. B. A new two-constant equation
of state // Ind. Eng. Chem. Fundam. 1976. V. 15.
[8]
Мельников В. П., Поденко Л. С., Драчук А. О.,
Молокитина Н. С. Получение гидратов метана в
[16]
Мельников В. П., Поденко Л. С., Нестеров А. Н.,
дисперсных замороженных водных растворах по-
Драчук А. О., Молокитина Н. С., Решетников А. М.
ливинилового спирта // ДАН. 2019. Т. 487. № 2.
Эффект самоконсервации гидратов метана, полу-
С. 164-168.
ченных в «сухой воде» // ДАН. 2016. Т. 466. № 5.
С. 554-558.
[Melʹnikov V. P., Podenko L. S., Drachuk A. O.,
Molokitina N. S. Production of methane hydrates
[Melʹnikov V. P., Podenko L. S., Nesterov A. N.,
in dispersed frozen aqueous solutions of polyvinyl
Drachuk A. O., Molokitina N. S., Reshetnikov A. M.
alcohol // Doklady Chem. 2019. V. 487. Part 1. P. 198-
Self-preservation of methane hydrates produced in
«dry water» // Doklady Chem. 2016. V. 466. N 2.
[9]
Molokitina N. S., Drachuk A. O. Effect of PVA
P. 53-56.
contained in ice on methane hydrate formation and
gas storage // J. Nat. Gas. Sci. Eng. 2022. V. 97.
[17]
Мельников В. П., Нестеров А. Н., Поденко Л. С.,
ID 104339.
Решетников А. М. Влияние диоксида углерода на
плавление подземного льда // ДАН. 2014. Т. 459.
[10]
Binks B., Murakami R. Phase inversion of particle-
№ 3. С. 337-339.
stabilized materials from foams to dry water // Nat.
Mater. 2006. V. 5. P. 865-869.
[Melʹnikov V. P., Nesterov A. N., Podenko L. S.,
Reshetnikov A. M. Influence of carbon dioxide on
[11]
Лозинский В. И. Криотропное гелеобразование
melting of underground ice // Doklady Earth Sci.
растворов поливинилового спирта // Успехи хи-
2014. V. 459. N 1. P. 1353-1355.
мии. 1998. Т. 67. № 7. С. 641-655 [Lozinsky V. I.
Cryotropic gelation of poly(vinyl alcohol) solutions //
[18]
Поденко Л. С., Драчук А. О., Молокитина Н. С.
Russ. Chem. Rev. 1998. V. 67. N 7. P. 641-655. http://
Кинетика образования гидратов пропана при плав-
лении льда в замороженных водных растворах
[12]
Пат. РФ 2574403 (опубл. 2016). Способ получения
поливинилового спирта // ЖПХ. 2021. Т. 94. № 1.
стабильной дисперсии геля поливинилового спир-
С. 47-54.
та в виде порошка.
[13]
Wang W., Bray C. L., Adams D. J., Cooper A. I.
[Podenko L. S., Drachuk A. O., Molokitina N. S.
Methane storage in dry water gas hydrates // J. Am.
Kinetics of propane hydrate formation from melting
Chem. Soc. 2008. V. 130. P. 11608-11609.
ice in frozen aqueous poly(vinyl alcohol) solutions
// Russ. J. Appl. Chem. 2021. V. 94. N 1. P. 43-50.
[14]
Falenty A., Salamatin A. N., Kuhs W. F. Kinetics
of CO2-hydrate formation from ice powders: Data