Журнал прикладной химии. 2022. Т. 95. Вып. 4
ПРИКЛАДНАЯ ЭЛЕКТРОХИМИЯ И ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
УДК 620.193.013:544.65
ИССЛЕДОВАНИЕ АНОДНОГО ПОВЕДЕНИЯ СПЛАВА Zn55Al,
ЛЕГИРОВАННОГО ХРОМОМ, В КОРРОЗИОННО-АКТИВНЫХ СРЕДАХ
© Ш. Г. Раджабова, Р. Н. Амини, И. Н. Ганиев, З. Р. Обидов*
Институт химии им. В. И. Никитина НАН Таджикистана,
734063, г. Душанбе, ул. Айни, д. 299/2
* E-mail: obidovzr@gmail.com
Поступила в Редакцию 10 мая 2022 г.
После доработки 14 июня 2022 г.
Принята к публикации 26 июня 2022 г.
Приведены результаты исследования анодного поведения сплава Zn55Al, легированного хромом, в
средах электролитов HCl, NaCl и NaOH при различных значениях pH среды. Показано, что для всех
образцов легированных хромом сплавов по сравнению с исходным сплавом Zn55Al наблюдается сме-
щение электрохимических потенциалов коррозии, питтингообразования и репассивации в область
положительных значений. Сплавы, содержащие по 0.01-1.0 мас% хрома, в диапазоне pH среды 3-10
наиболее устойчивы к питтинговой коррозии. Установлено, что скорость коррозии легированных
(0.01-0.1%) хромом сплавов в 1.5-2 раза меньше, чем сплава Zn55Al. Продукты коррозии сплавов
состоят из смеси оксидов Al2O3, ZnO, ZnAl2O4, Al2O3·Cr2O3.
Ключевые слова: сплав Zn55Al с хромом; скорость коррозии; анодное поведение
DOI: 10.31857/S0044461822040144, EDN: DHXGBH
Одним из путей повышения анодной устойчи-
Экспериментальная часть
вости цинк-алюминиевого сплава (используемого
в качестве антикоррозионных покрытий) является
В качестве исходных материалов использовали
легирование подходящим металлом [1, 2]. Наиболее
гранулированный цинк (ч.д.а., ООО «Таджикско-
изучены свойства сплавов Zn5Al и Zn55Al, леги-
Китайская горнопромышленная компания»), алюми-
рованных элементами подгруппы скандия и церия.
ний марки А7 (тех.ч., ГУП «Таджикская алюминиевая
Добавление редкоземельного металла к сплаву изме-
компания») и его лигатуру с металлическим хромом
няет его структуру, полученный трехфазный сплав
(2% Cr) (ч.д.а., ООО «Новотроицкий завод хромовых
отличается от двойного наличием интерметаллида
соединений»), которую синтезировали в вакуумной
(например, Al3Sc) и характеризуется мелкозернистой
печи СНВЭ-1.3.1/16ИЗ (ООО «Московский завод
структурой [3]. Установлено положительное влияние
вакуумных электропечей») под избыточным давле-
добавок хрома на анодную стойкость сплава Zn0.5Al
нием гелия.
к окислению [4].
Из указанных металлов были получены сплавы в
Цель работы — исследование анодного поведения
тиглях из оксида алюминия в шахтной печи сопро-
сплава Zn55Al, легированного хромом, в коррозион-
тивления типа СШОЛ (ООО «Завод электротехно-
но-активных средах.
логия»). Взвешивание шихты производили на анали-
524
Исследование анодного поведения сплава Zn55Al, легированного хромом, в коррозионно-активных средах
525
тических весах типа АРВ-200 (ООО «Сартогосм») с
Потенциодинамическое исследование анодного
точностью 0.1·10-4 кг.
поведения сплава Zn55Al, легированного хромом,
После разогрева печи до 850°С расплавляли цинк
проводили в кислых (0.1, 0.01, 0.001 М; рН 1, 2, 3
и алюминий, затем вводили лигатуру. После выдерж-
соответственно), нейтральных (0.03, 0.3, 3%; рН
ки (до 30 мин) при температуре 750-850°С расплав
6.7-7.4) и щелочных (0.001, 0.01, 0.1 М; рН 10, 11,
тщательно перемешивали и отливали образцы. Их
12) средах электролитов HCl, NaCl и NaOH (х.ч.,
химический состав оценивали методом микрорент-
АО «ЭКОС-1») с помощью потенциостата ПИ-50.1
геноспектрального анализа с помощью сканирую-
(РУП «Гомельский завод измерительных приборов»),
щего электронного микроскопа AIS2100 (S-Factory)
скорость развертки потенциала 2 мВ·с-1. Методика
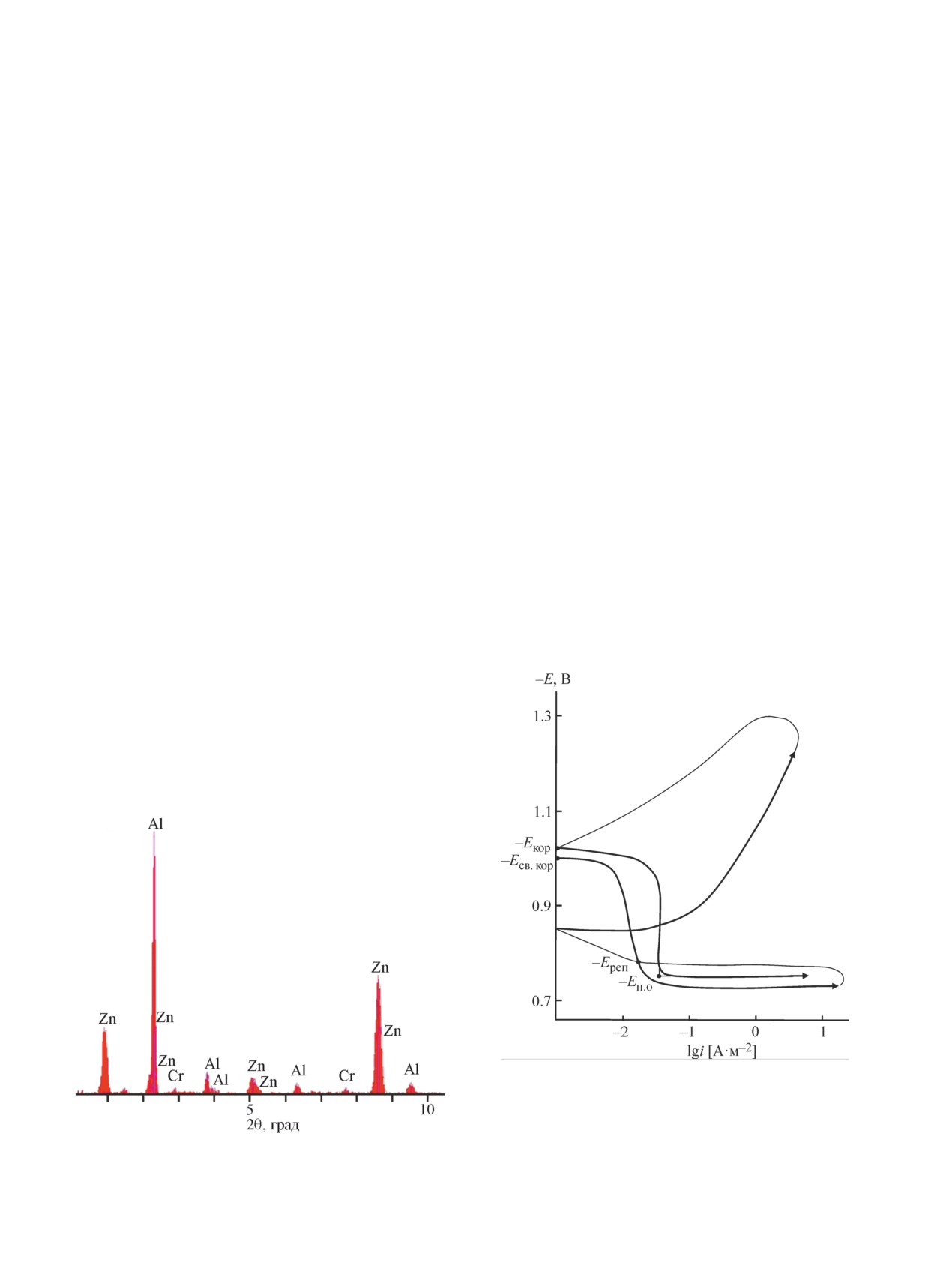
(пример спектра — на рис. 1). Точность определения
исследования сплавов описана в работе [5].
содержания легирующего компонента сплава состав-
При коррозионно-электрохимических исследова-
ляла ±10-3%.
ниях образцы поляризовали потенциодинамически в
Из каждой плавки в графитовую изложницу от-
положительном направлении от стационарного по-
ливали стержни диаметром 8 мм и длиной 140 мм.
тенциала Есв.кор, который устанавливался при погру-
Боковые части образцов изолировали смолой
жении, до резкого увеличения тока при достижении
из смеси сосновой канифоли марки А (х.ч., ООО
потенциала питтингообразования Еп.о. Далее образцы
«СПЕЦТЕХНОХИМ») и твердого парафина марки
поляризовали до потенциала 1300 мВ в обратном
Т-3 (х.ч., ОАО «Завод горного воска») в соотношении
направлении, в результате чего отмечали потенциалы
1:1. Рабочей поверхностью служил торец электрода.
коррозии Екор и репассивации Ереп. Затем поляризовали
Перед погружением образца в рабочий раствор его
образцы в положительном направлении (рис. 2).
торцевую часть зачищали наждачной бумагой, поли-
Фазовый анализ продуктов коррозии исследуе-
ровали и обезжиривали в течение 10-15 с в 10%-ном
мых сплавов проводили на дифрактометре ДРОН-2.0
растворе NaOH (х.ч., АО «ЭКОС-1»). Температуру
(НПП «Буревестник») с медным (CuKα) излучением,
раствора в ячейке поддерживали постоянной (25°С)
их изображения микроструктуры получали на микро-
с помощью термостата МЛШ-8 (ЗАО «Лабораторное
скопе LEITS ERGOLUX AMC (Leits).
оборудование и приборы»). В качестве электро-
да-сравнения был выбран хлорсеребряный электрод
(ЭСО-01, РУП «Гомельский завод измерительных
приборов»), вспомогательным электродом служил
высокотемпературный платиновый электрод (ЭПВ-1,
РУП «Гомельский завод измерительных приборов»).
Погрешность установки потенциала рабочего элект-
рода составляла ±0.001 мВ.
Рис. 2. Потенциодинамические анодные и катодные
поляризационные кривые сплава Zn55Al, содержащего
1.0 мас% Cr, в среде 0.001 М HCl.
Есв.кор, Екор, Еп.о, Ереп — потенциалы свободной коррозии,
Рис. 1. Интенсивность рентгеноспектральных линий коррозии, питтингообразования, репассивации соответ-
компонентов сплава Zn55Al, содержащего 0.5 мас% Cr.
ственно.
526
Раджабова Ш. Г. и др.
Обсуждение результатов
Зависимость потенциала свободной коррозии
сплавов от времени играет важную роль в пассивации
поверхности. Для всех исследованных групп сплавов
отмечено незначительное смещение потенциала в
положительную область значений со временем. Сдвиг
потенциала завершается к 30 (NaCl), 35 (NaOH) и
40 мин (HCl) от начала процесса и остается неизмен-
ным до окончания наблюдений (табл. 1). Пассивация
исследованных сплавов связана с образованием на их
поверхности защитной покровной пленки.
Отмечается увеличение коррозионной устойчиво-
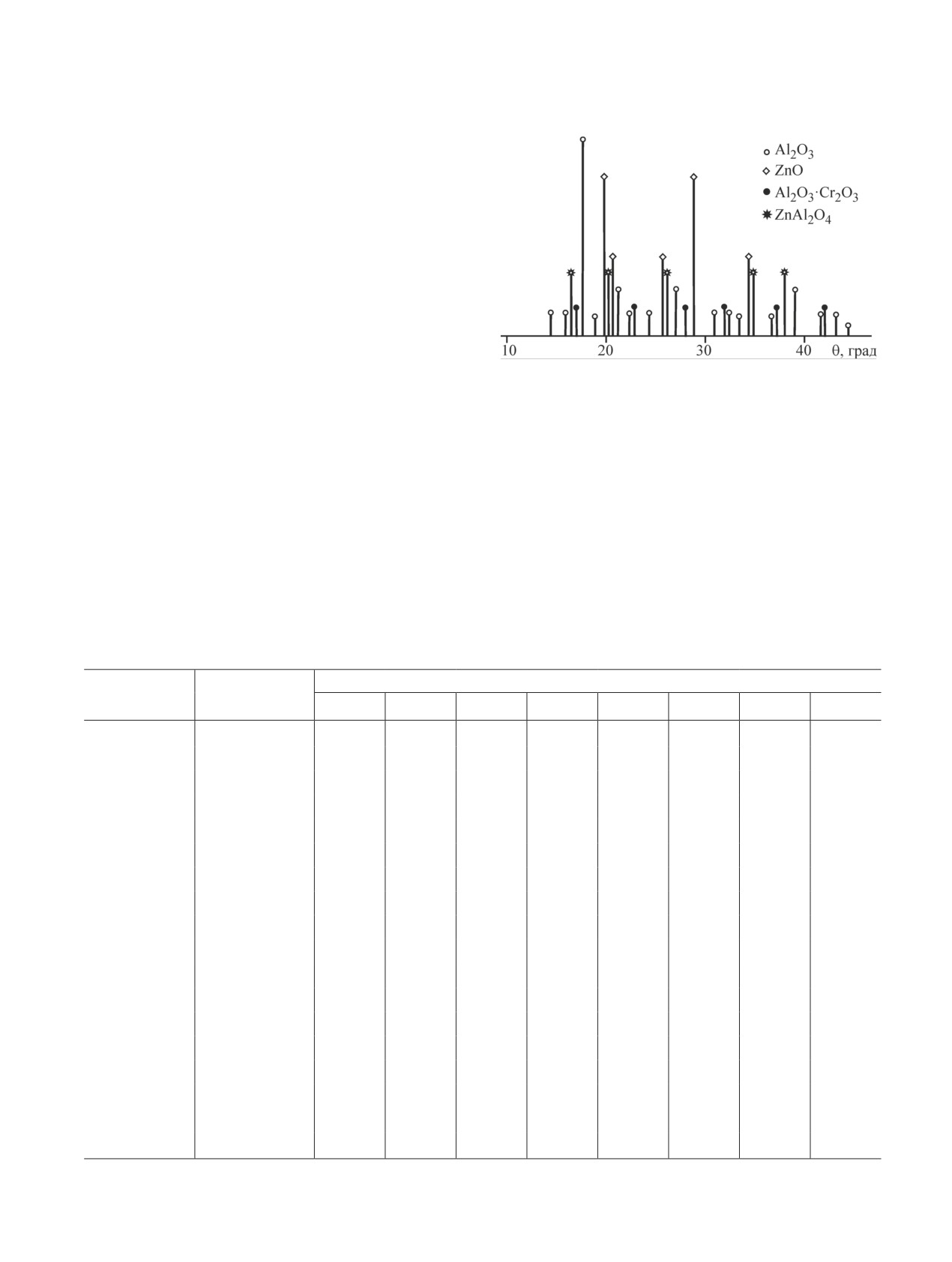
Рис. 3. Штрих-дифрактограммы продуктов коррозии
сти сплавов при легировании хромом. Введение 0.5
сплава Zn55Al, содержащего 0.1 мас% Cr.
и 1.0% хрома в исходный сплав Zn55Al несколько
смещает потенциал свободной коррозии в отрица-
тельном направлении, но по абсолютной величине
присутствуют кристаллические фазы исходных ком-
последнее не превышает Есв.кор исходного сплава
понентов (рис. 3).
(табл. 1). Вследствие усиления коррозии и неравно-
Согласно диаграмме состояния системы Zn-Al
мерного растворения увеличивается и площадь по-
структура исходного Zn55Al состоит из твердых
верхности образцов сплава. На поверхности сплавов
растворов цинка в алюминии и алюминия в цин-
образуются защитные оксидные пленки Al2O3, ZnO,
ке, находящихся в эвтектоидном равновесии друг
ZnAl2O4, Al2O3·Cr2O3, шпинели сложного состава и
с другом [3]. Легирующие добавки хрома, раство-
Таблица 1
Изменения потенциала свободной коррозии сплава Zn55Al, легированного хромом, во времени
-Есв.кор, В, при времени выдержки сплава, мин
Добавка Cr
Среда
в сплаве, мас%
1/3
2/3
1
5
15
30-40
50
60
0.01 М HCl
—
1.082
1.080
1.077
1.074
1.070
1.055
1.055
1.055
0.01
0.943
0.942
0.940
0.935
0.922
0.907
0.907
0.907
0.05
0.949
0.949
0.948
0.943
0.931
0.900
0.900
0.900
0.1
0.963
0.961
0.960
0.956
0.945
0.914
0.914
0.914
0.5
0.981
0.979
0.979
0.974
0.968
0.954
0.954
0.954
1.0
1.009
1.008
1.006
0.997
0.988
0.973
0.973
0.973
0.3% NaCl
—
1.022
1.022
1.020
1.016
1.009
1.000
1.000
1.000
0.01
0.918
0.915
0.914
0.908
0.900
0.894
0.894
0.894
0.05
0.933
0.933
0.930
0.928
0.916
0.900
0.900
0.900
0.1
0.963
0.961
0.958
0.947
0.934
0.908
0.908
0.908
0.5
0.981
0.980
0.978
0.965
0.948
0.920
0.920
0.920
1.0
1.002
1.000
0.988
0.976
0.966
0.943
0.943
0.943
0.01 М NaOH
—
1.114
1.114
1.109
1.108
1.101
1.100
1.100
1.100
0.01
0.953
0.953
0.950
0.942
0.933
0.922
0.922
0.922
0.05
0.976
0.975
0.974
0.967
0.951
0.918
0.918
0.918
0.1
1.000
0.998
0.996
0.989
0.978
0.930
0.930
0.930
0.5
1.015
1.014
1.011
0.995
0.985
0.969
0.969
0.969
1.0
1.037
1.037
1.036
1.024
1.004
0.985
0.985
0.985
Примечание. «—» — сплав Zn55Al без содержания хрома.
Исследование анодного поведения сплава Zn55Al, легированного хромом, в коррозионно-активных средах
527
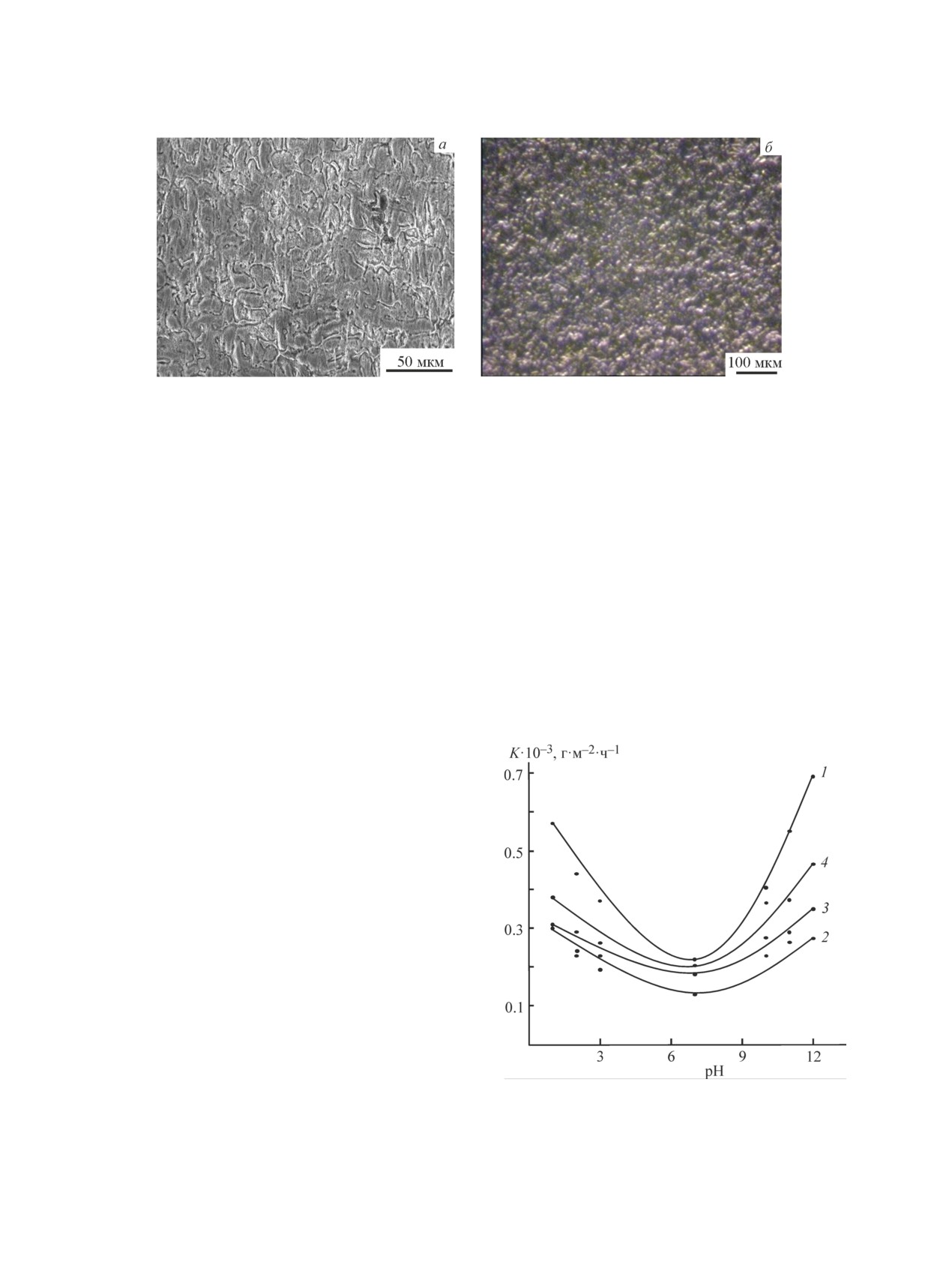
Рис. 4. Изображения микроструктуры: а — сплав Zn55Al, б — сплав Zn55Al с 0.05 мас% Cr.
ряясь в твердых растворах α-Al + γ-Zn, не образу-
кристаллизации и обеспечивают высокий уровень ан-
ют новые фазы, но значительно уменьшают размер
тикоррозионных свойств. Добавки хрома в пределах
зерна сплава Zn55Al. При этом игольчатые структу-
0.01-0.1% снижают скорость коррозии исходного
ры Zn55Al превращаются в мелкую шарообразную
сплава Zn55Al в 1.5-2 раза. Более того, указанные
форму (рис. 4).
сплавы наиболее устойчивы к питтинговой коррозии,
Изменение потенциалов коррозии, питтингооб-
особенно в кислой (0.001 М HCl), нейтральной (0.03,
разования и репассивации показывает повышение
0.3, 3% NaCl) и щелочной (0.001 М NaOH) среде.
анодной устойчивости сплава Zn55Al с хромом в
Наименьшее значение скорости коррозии исходного
кислых и щелочных средах. Добавки хрома (0.01-
сплава Zn55Al с хромом зафиксировано в диапазоне
1.0%) способствуют смещению указанных потенци-
pH 3-10. Повышение содержания хрома до 1.0%, а
алов в область положительных значений. Увеличение
также увеличение концентрации Cl- и OH- в среде в
анодной устойчивости легированного хромом сплава
100 раз приводит к увеличению скорости коррозии
зависит от времени нахождения в агрессивной сре-
исследуемых сплавов (рис. 5).
де. При увеличении времени наблюдения в период
коррозионного процесса падает скорость анодного
растворения сплава. Это обусловлено образованием
малорастворимых продуктов коррозии, препятству-
ющих взаимодействию агрессивной среды с участ-
ками сплава, подвергнутого коррозии. В результате
снижается плотность тока коррозии исходного сплава
Zn55Al в 1.5-2 раза (табл. 2).
Электрохимические потенциалы коррозии, пит-
тингообразования и репассивации сплавов, легиро-
ванных хромом, повышаются с ростом концентра-
ции Cl-, что свидетельствует о снижении анодной
устойчивости сплавов в присутствии Cl- (табл. 3).
При этом механизм коррозии определяется типом
агрессивной среды. Однако картина коррозионного
разрушения далеко не всегда так проста, так как при
достижении потенциала питтингообразования может
происходить местное нарушение сплошности пасси-
вирующего слоя. С увеличением скорости коррозии
на поверхности сплавов появляются очаги коррозии
и снижается коррозионная стойкость образцов.
Рис. 5. Зависимость скорости коррозии сплава Zn55Al
Малые добавки легирующего компонента способ-
(1), содержащего по 0.01 (2), 0.1 (3) и 1.0% (4) хрома,
ствуют уменьшению размера зерна сплава Zn55Al при
от pH среды.
528
Раджабова Ш. Г. и др.
Исследование анодного поведения сплава Zn55Al, легированного хромом, в коррозионно-активных средах
529
Таблица 3
Анодные характеристики сплава Zn55Al, легированного хромом, в нейтральной среде
Потенциал
Потенциал
Потенциал
Потенциал
Ток
Скорость
Добавка Cr
свободной
питтинго-
Среда NaCl,
коррозии
репассивации
коррозии
коррозии
в сплаве,
коррозии
образования
мас%
-Eкор, В
-Eреп, В
iкор∙10-2,
K∙10-3,
мас%
-Eсв.кор, В
-Еп.o
А∙м-2
г∙м-2∙ч-1
Ag/AgCl, KCl
нас
—
0.970
0.990
0.850
0.870
0.026
0.190
0.01
0.874
0.880
0.780
0.793
0.015
0.109
0.05
0.833
0.864
0.772
0.785
0.013
0.095
0.03
0.1
0.840
0.875
0.786
0.806
0.016
0.117
0.5
0.856
0.880
0.795
0.816
0.018
0.132
1.0
0.885
0.994
0.810
0.820
0.021
0.154
—
1.000
1.018
0.935
0.948
0.030
0.219
0.01
0.894
0.994
0.856
0.875
0.017
0.124
0.05
0.900
0.903
0.867
0.874
0.022
0.161
0.3
0.1
0.908
0.914
0.874
0.883
0.025
0.183
0.5
0.920
0.954
0.885
0.897
0.027
0.198
1.0
0.943
0.972
0.908
0.915
0.029
0.212
—
1.043
1.055
0.988
0.994
0.035
0.256
0.01
0.933
0.940
0.900
0.914
0.019
0.139
0.05
0.924
0.934
0.895
0.901
0.023
0.168
3.0
0.1
0.940
0.950
0.908
0.922
0.026
0.190
0.5
0.962
0.965
0.916
0.931
0.030
0.219
1.0
0.975
0.985
0.930
0.938
0.031
0.227
Примечание. Электрохимические потенциалы приведены по отношению к хлорсеребряному насыщенному элек-
троду сравнения.
Выводы
Ганиев Изатулло Наврузович
Введение легирующих добавок (0.01-1.0 мас%)
Обидов Зиёдулло Рахматович
хрома в состав сплава Zn55Al способствует смеще-
нию потенциалов коррозии, питтингообразования
и репассивации сплавов в область положительных
значений. Скорость коррозии сплавов, легированных
Список литературы
хромом, в 1.5-2 раза ниже, чем исходного сплава
[1] Ahmad K., Mohsen S., Mohammad R. S. Anodic
Zn55Al.
behavior of Al-Zn-In sacrificial anodes at different
concentration of zinc and indium // Int. J. Mater. Res.
Конфликт интересов
2012. V. 103. N 12. P. 1533-1538.
Авторы заявляют об отсутствии конфликта инте-
[2] Mazilkin A. A., Straumal B. B., Borodachenkova M. V.,
ресов, требующего раскрытия в данной статье.
Valiev R. Z., Kogtenkova O. A. Gradual softening of Al-
Zn alloys during high-pressure torsion // Mater. Lett.
2012. V. 84. P. 63-65.
Информация об авторах
Раджабова Шафоат Гафуровна
[3] Обидов З. Р., Ганиев И. Н. Физикохимия цинк-алю-
миниевых сплавов с редкоземельными металла-
Амини Реза Наджафабади
ми. Душанбе: ООО «Андалеб-Р», 2015. С. 160-164,
308-311.
530
Раджабова Ш. Г. и др.
[4] Обидов З. Р., Иброхимов П. Р., Рахимов Ф. А., Гани-
[5] Обидов З. Р., Ганиев И. Н., Алиев Дж. Н., Гание-
ев И. Н. Кинетика окисления сплава Zn0.5Al, леги-
ва Н. И. Анодное поведение сплавов Zn5Al,
рованного хромом, в твердом состоянии // ЖФХ.
Zn55Al, легированных кальцием, в растворах NaCl
2021. Т. 95. № 1. С. 152-154.
// ЖПХ. 2010. Т. 83. № 6. С. 962-965 [Obidov Z. R.,
Ganiev I. N., Aliev Dzh. N., Ganieva N. I. Anodic
[Obidov Z. R., Ibrokhimov P. R., Rakhimov F. A.,
behavior of Zn5Al and Zn55Al alloys alloyed with
Ganiev I. N. Kinetics of the oxidation of chromium-
calcium in NaCl solutions // Russ. J. Appl. Chem. 2010.
doped Zn0.5Al alloy in the solid state // Russ. J. Phys.
V. 83. N 6. P. 1015-1018.
Chem. A. 2021. V. 95. N 1. P. 221-223.