Журнал прикладной химии. 2022. Т. 95. Вып. 5
УДК 66.092.088:66.092.097:661.97
ПЛАЗМЕННО-КАТАЛИТИЧЕСКОЕ РАЗЛОЖЕНИЕ УГЛЕКИСЛОГО ГАЗА
(обзор)
© О. В. Голубев, А. Л. Максимов
Институт нефтехимического синтеза им. А. В. Топчиева РАН,
119991, ГСП-1, г. Москва, Ленинский пр., д. 29
Поступила в Редакцию 15 апреля 2022 г.
После доработки 27 мая 2022 г.
Принята к публикации 20 июня 2022 г.
Проанализированы данные литературы по разложению CO2 в условиях плазменного катализа. При-
менение катализатора позволяет значительно увеличить конверсию CO2 и энергетическую эффек-
тивность процесса. В большинстве работ описывается разложение CO2 в реакторе с барьерным
разрядом, что связано с простотой конструкции такого типа реактора. Определены ключевые
характеристики катализаторов, влияющие на эффективность разложения CO2 в газовом разряде:
наличие кислородных вакансий в структуре катализатора, а также оснóвных центров в образце.
Ключевые слова: плазма; утилизация углекислого газа; плазменный катализ; плазмохимия
DOI: 10.31857/S0044461822050012, EDN: DIARUT
Введение
тепловой энергии для разрыва связей в исходных мо-
лекулах и смещения термодинамического равновесия.
Интенсивное сжигание углеводородов для нужд
Для ускорения реакции и обеспечения селективности
промышленности приводит к значительному уве-
процесса используют катализаторы, которые при вы-
личению выбросов парниковых газов, в частности
сокой температуре в присутствии одноуглеродных
CO2, что является причиной существенных измене-
молекул могут дезактивироваться или подвергаться
ний в атмосфере Земли, приводящих к глобально-
зауглероживанию. Снизить степень дезактивации
му потеплению на планете. С уверенностью можно
катализатора можно при переходе к низкотемператур-
заявить, что устранение негативного воздействия
ным способам активации молекул CO2, в том числе
парниковых газов является одной из важнейших за-
электрохимической, фотохимической, биохимической
дач современной науки, в связи с этим превращение
активацией, а также активацией солнечной энерги-
CO2 в синтез-газ и ценные продукты нефтехимии с
ей [1-3]. Перспективным направлением в решении
высокой добавленной стоимостью представляется
поставленных задач являются плазмохимические
одним из решений данной проблемы. Так, например,
процессы, а именно проведение реакций в условиях
проводят превращение CO2 в синтез-газ по реакции
низкотемпературной плазмы различных типов раз-
углекислотного риформинга метана. Еще одним на-
ряда.
правлением утилизации CO2 является гидрирование
Плазма является квазинейтральной системой, со-
с получением метана или метанола.
держащей заряженные и нейтральные частицы: элек-
Для превращения молекул CO2 в нефтехимическое
троны, ионы, электронно- и колебательные возбуж-
сырье требуется подвод значительного количества денные частицы, радикалы и атомы. Применительно
547
548
Голубев О. В., Максимов А. Л.
к плазмохимическим процессам рассматривают
CO2 [23], синтез NH3 [24-26], пиролиз метана [27] и
низкотемпературную плазму с температурой ме-
др. [28]. В данной работе основное внимание будет
нее 105 K. Различают два типа плазмы — терми-
сфокусировано на плазменно-каталитическом воздей-
ческую и нетермическую (неравновесную) плазму.
ствии в процессе превращения CO2 без использова-
Термическая плазма находится в термодинамиче-
ния дополнительных реагентов, а именно процессе
ском равновесии: температура электронов совпадает
разложения CO2 в среде плазмы, генерируемой в
с температурой тяжелых частиц (температура газа),
различных электрических разрядах.
при этом температура газа достигает 3000-5000 K.
Цель работы — систематизация данных литерату-
Неравновесная плазма характеризуется низкой эн-
ры по теме плазменно-каталитического разложения
тальпией, что позволяет проводить реакции при
CO2 в различных типах разряда и определение клю-
комнатной температуре и атмосферном давлении:
чевых характеристик катализаторов, которые влияют
средняя энергия электронов в плазме может дости-
на активность в процессе разложения CO2.
гать 15 эВ, что достаточно для разрыва межатомных
связей в молекулах [4].
Способы превращения CO2 в продукты
Проведение каталитических процессов в среде
с добавленной стоимостью
низкотемпературной плазмы носит название плаз-
менного катализа. В последнее десятилетие интерес
Пионерской реакцией по превращению углекисло-
к теме плазменно-каталитических технологий мно-
го газа в ценные продукты можно считать каталити-
гократно возрос в связи с тенденцией к переходу на
ческую реакцию гидрирования CO2 в метан (реакция
альтернативные источники энергии для проведения
Сабатье), открытую в конце XIX в. французским хи-
химических процессов и углерод-нейтральную энер-
миком P. Sabatier [29]. С этого времени ведутся ра-
гетику в целом. Плазменный катализ — перспектив-
боты по переработке CO2 с применением различных
ная область исследований в энергетической и эколо-
процессов, которые можно разделить на две большие
гической сферах, в таких процессах, как, например,
группы [30]: процессы получения продуктов нефтехи-
разложение летучих органических веществ [5-7],
мической промышленности и полимеров и процессы
очистка воды [8-10], удаление NOx [11-13], а также в
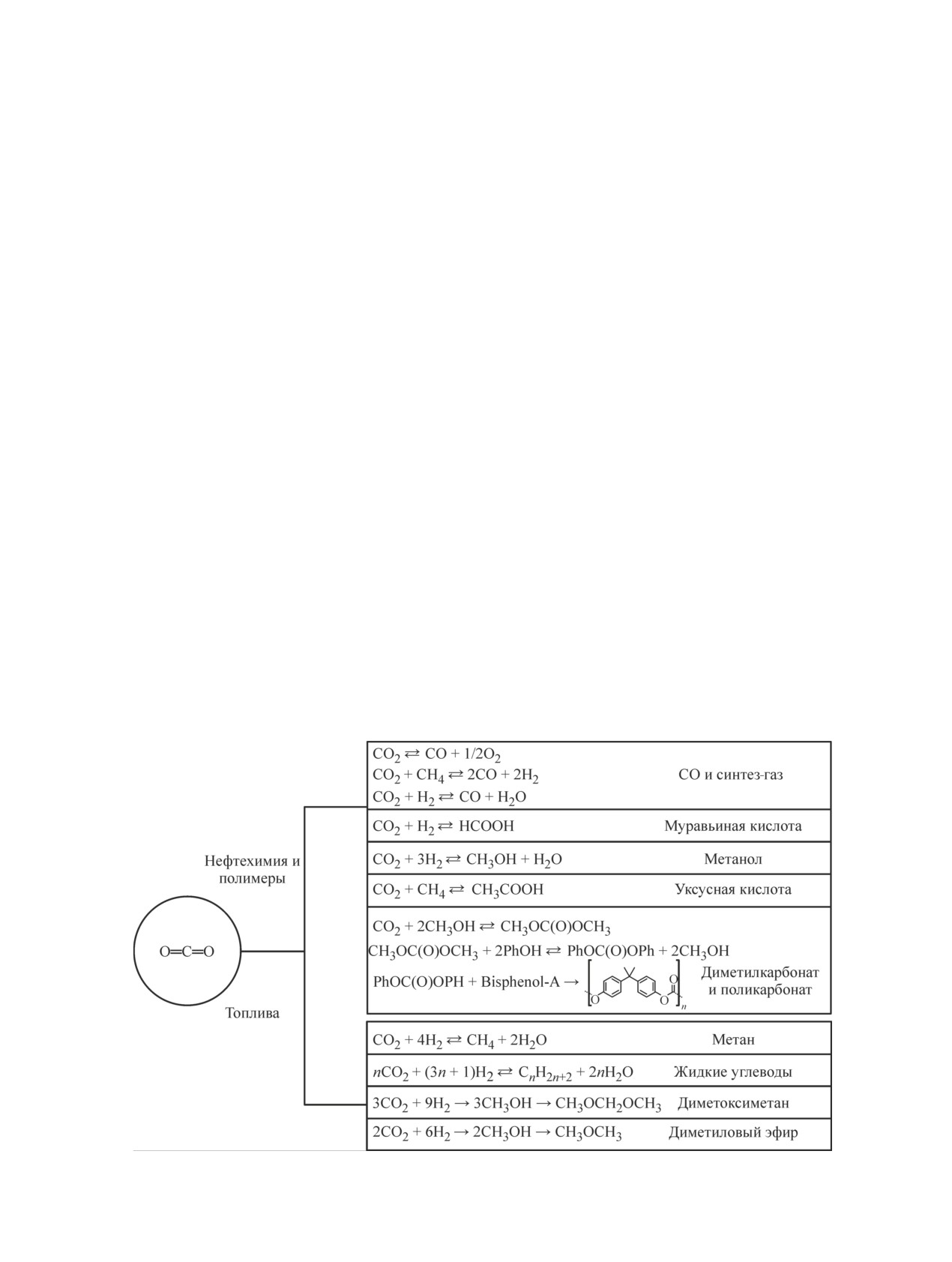
получения синтетических топлив (рис. 1). Процессы
нефтехимических, газохимических или смежных про-
получения продуктов нефтехимии подразделяют на
цессах: углекислотный риформинг метана [14-18],
два типа: продукты переработки CO2 могут быть
паровой риформинг метана [19-22], гидрирование
внедрены в действующие цепочки производства (по-
Рис. 1. Схема переработки углекислого газа по нефтехимическому и топливному вариантам.
Плазменно-каталитическое разложение углекислого газа (обзор)
549
лучение СО, метанола и их дальнейшая переработка)
и конверсию CO2. Комбинация плазмы с катализа-
или CO2 может выступать в качестве одноуглеродного
тором — еще один путь к увеличению ключевых
фрагмента более сложных молекул — карбоновых
показателей процесса.
кислот и органических карбонатов и поликарбонатов.
Топливный вариант переработки углекислого газа
Взаимодействие плазма-катализатор
предполагает получение таких продуктов, как метан,
жидкие углеводороды и оксигенаты [31].
В настоящее время в русскоязычной литературе
Процессы переработки CO2 в ценные продукты
не существует устоявшегося понятия, относящего-
с использованием плазмохимических и плазменно--
ся к катализу в плазме. Так, в монографии [44] под
каталитических процессов схожи с описанными вы-
эффектом плазменного катализа подразумевается
ше процессами получения продуктов нефтехимии и
ускорение химической реакции под воздействием
топлив. Так, в среде плазмы проводят процессы ги-
плазмы. В этом контексте плазма выступает не в ка-
дрирования CO2 [23, 32, 33] с образованием CO, CH4
честве источника энергии, а в качестве катализатора,
и оксигенатов; углекислотный риформинг метана с
хотя и разделить эти два воздействия представляет-
получением синтез-газа, оксигенатов и олефинов [34,
ся довольно сложной задачей. В настоящем обзоре
35]; разложение CO2 с выделением CO и О2.
к плазменно-каталитическим процессам мы будем
Прямое разложение CO2 до CO и O2 затруднено
относить реакции в газовых разрядах в присутствии
при температуре ниже 2000°С. При высокой темпе-
гетерогенных наполнителей, схожих с традиционны-
ратуре преодолеваются термодинамические ограни-
ми каталитическими системами.
чения, однако возрастает скорость обратной реакции.
Преимуществом плазменно-каталитического ме-
Образование CO2 из CO и O2 ограничивает степень
тода (в сравнении с термокаталитическим) является
разложения CO2.
проведение процесса при более низкой температуре,
что способствует более высокой степени адсорбции
CO2 CO + 1/2O2 (ΔH298 K = 283 кДж·моль-1).
(1)
реагирующих веществ на поверхности катализатора.
При этом плазма является источником высокоэнер-
Для разложения CO2 до CO в отсутствие катали-
гетических электронов, радикалов, а также тепло-
затора используют различные источники плазмы.
вой энергии [45]. Низкотемпературная плазма может
Наиболее часто разложение проводят в реакторах с
приводить к изменению свойств катализатора, на-
барьерным разрядом [36-38], сверхвысокочастотным
пример, изменять его кислотно-основные свойства,
разрядом [39-41] и дуговым разрядом [42, 43]. При
увеличивать дисперсность нанесенных металлов,
плазмохимическом разложении углекислого газа ча-
варьировать структуру наночастиц металлов и вза-
сто достигается компромисс между конверсией СО2
имодействие металл-носитель [46, 47]. Кроме того,
и энергетической эффективностью процесса. Под
физико-химические свойства поверхности катализа-
конверсией подразумевается следующее соотноше-
тора могут изменяться вследствие непрерывной бом-
ние:
бардировки высокоэнергетическими электронами и
реагирующими частицами, образующимися в плазме
α(%) =
·100%,
(2)
(радикалы, ионы). Это приводит к модифицированию
катализатора: окислению [48], восстановлению [49],
перераспределению активных компонентов по по-
где ν(CO2) — количество газа на входе и выходе из
верхности катализатора [50], образованию дефектов
реактора.
в кристаллической решетке.
Энергетическая эффективность определяется со-
В то же время присутствие катализатора в зо-
отношением
не разряда может влиять и на физические свойства
плазмы. Сообщается, что в закрепленном слое ка-
η(%) =
·100%,
(3)
тализатора или инертного сегнетоэлектрического
(ферроэлектрического) материала на границах гра-
где α(CO2) — конверсия углекислого газа; G(CO2) —
нул или сферических частиц возникает локальное
скорость подачи газа (моль·с-1); ΔH°298 K — энергия
увеличение напряженности электрического поля [4].
разрыва связи С O, составляющая 283 кДж·моль-1;
Это приводит к изменению типа разряда — от стри-
P — мощность разряда (кВт).
меров внутри плазмы к стримерам на поверхности
Разработка новых конструкций реакторов позво-
катализатора. Примечателен эффект образования
ляет одновременно повысить энергоэффективность
микроразрядов в порах каталитического материала.
550
Голубев О. В., Максимов А. Л.
В работе [51] выявлены закономерности возникно-
Плазменно-каталитическое разложение CO2
вения таких микроразрядов в порах диаметром боль-
в барьерном разряде
ше дебаевского радиуса. Стримеры плазмы могут
Барьерный разряд — это электрический разряд
проникать в поры диаметром порядка нескольких
между двумя электродами (плоскими или цилиндри-
сотен нм. В порах меньшего диаметра (единицы нм)
ческими), разделенными материалом, выполняю-
также может проникать разряд вследствие диффузии
щим роль изолятора (диэлектрический барьер). Для
активных частиц плазмы. Материалы с низкой ди-
генерации этого типа разряда требуется переменное
электрической проницаемостью более подвержены
напряжение. Плазма, генерируемая с помощью ба-
прониканию плазмы в поры меньшего диаметра по
рьерного разряда, используется при конверсии CO2
сравнению с материалами с высокой проницаемо-
в ценные продукты при атмосферном давлении.
стью. Описанные закономерности напрямую влияют
Масштабируемость и простота поддержания низко-
на взаимодействие катализатора с плазмой, а также
температурной плазмы — основные преимущества
определяют его активность.
этого типа плазмохимического реактора [54].
Если сравнивать концепцию катализа в плазме с
Наиболее часто используют концентрические ци-
термокатализом, выявляются следующие различия.
линдрические электроды: центральный высоковольт-
В традиционном каталитическом процессе тепло-
ный электрод и внешний электрод из металлической
вая энергия равномерно воздействует на все степе-
сетки или фольги вокруг диэлектрического барьера
ни свободы интермедиатов на всех промежуточных
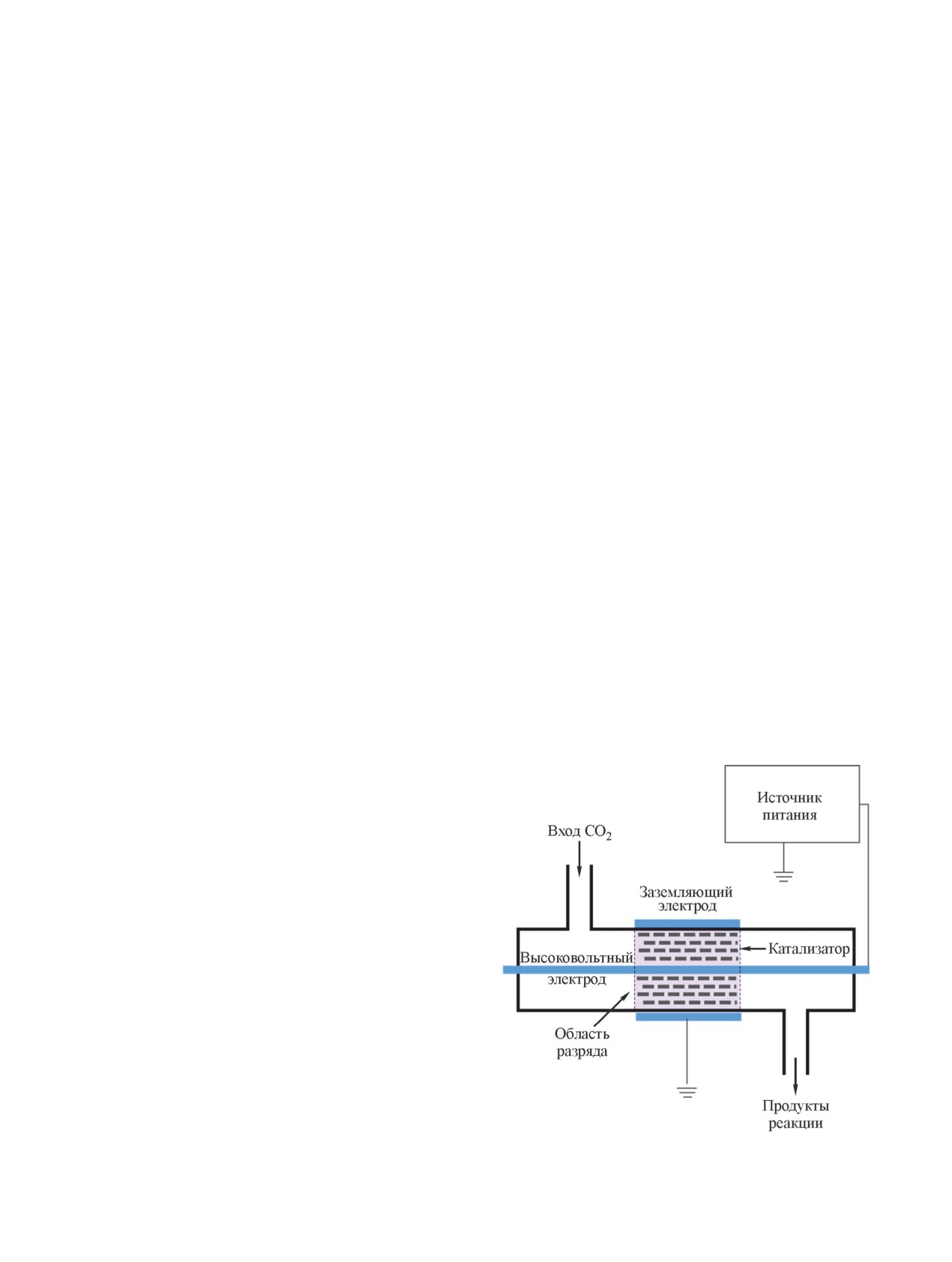
(стенок реактора) (рис. 2). Расстояние между электро-
стадиях реакции. В отличие от этого в присутствии
дами (разрядный промежуток) обычно не превышает
низкотемпературной плазмы существует возможность
нескольких миллиметров. В плазменно-каталитиче-
направлять энергию на возбуждение внутренних сте-
ском режиме проведения реакций катализатор распо-
пеней свободы молекул. Иными словами, плазменный
лагается между электродами. Высоковольтное напря-
катализ отличается от традиционного катализа раз-
жение подается на центральный электрод, внешний
личной концепцией «температуры». Температура
электрод заземляется. Напряжение варьируется от 1
газа в низкотемпературной плазме варьируется от
до 100 кВ, частота приложенного напряжения — от
300 до 3000 K, температура электронов — 104-105 K.
единиц Гц до МГц. Реакции в барьерном разряде
Представляет интерес колебательная температура
проводятся при атмосферном давлении или при не-
(несколько тысяч Кельвинов): плазма способствует
большом разрежении. При подаче напряжения между
селективной активации колебательного состояния
электродами возникает электрический разряд (поток
молекулы. Возбужденное колебательное состояние
молекулы приводит к наиболее энергоэффективной
конверсии CO2 [52, 53], а также большей реакцион-
ной способности на поверхности катализатора.
Роль плазменного катализа заключается в увели-
чении конверсии продукта с одновременным увели-
чением энергетической эффективности без допол-
нительного расхода энергии. Описываемый эффект
может возникать при помещении катализатора в
область разряда или вне зоны разряда, чаще всего
после области возбуждения (область послесвечения
разряда). В первом случае плазма и катализатор взаи-
модействуют с реагентом одновременно, во втором —
реагирующая молекула подвергается бомбардировке
электронами в области плазмы, а затем активные
частицы (радикалы, ионы) претерпевают превра-
щения на поверхности катализатора. Может быть
воплощен мультистадийный вариант плазменно-ка-
талитического режима, когда последовательно распо-
ложены несколько ячеек с разными катализаторами в
области плазмы. Данная конфигурация способствует
различным каталитическим превращениям в одном
реакторе.
Рис. 2. Схема реактора барьерного разряда.
Плазменно-каталитическое разложение углекислого газа (обзор)
551
высокоэнергетических электронов), что приводит
обеспечивается наибольшая конверсия (25%) и энер-
к образованию в газовой среде между электродами
гоэффективность (4.5%). При сравнении результатов
возбужденных частиц: ионов, радикалов, электро-
эксперимента в зависимости от используемых ди-
нов — и возникновению множества микроразрядов
электрических материалов (стекловолокно, кварце-
[55, 56]. Для реакции разложения CO2 барьерный
вое волокно, а также гранулы ZrO2, SiO2 и Al2O3) и
разряд используется наиболее часто, что обусловле-
размера гранул в разрядном промежутке установлены
но простотой конструкции и условиями проведения
следующие закономерности. Заполнение гранулами
эксперимента [57]. Масштабирование таких систем
диэлектрического материала повышает плотность
осуществляется путем конструирования множества
электрического поля в точках контакта гранул, что по-
реакторов в параллельном режиме [55].
ложительно влияет на энергоэффективность и конвер-
При помещении катализатора в область барьерно-
сию CO2. В то же время в присутствии гранул матери-
го разряда протекание химических реакций в плазме
ала снижается время их контакта с CO2, что является
обусловливается как газофазными взаимодействиями,
скорее негативным эффектом. В зависимости от типа
так и гетерогенными процессами на поверхности
материала, а также размера гранул или сферических
катализатора. Таким образом, присутствие катализа-
частиц влиять на эффективность процесса могут и
тора оказывает значительное влияние на плазмохи-
пустоты между частицами. Таким образом, важную
мический процесс. Взаимодействие между барьер-
роль играет не только диэлектрическая проницае-
ным разрядом и катализатором может приводить к
мость материала, но также взаимное расположение
изменениям характеристик плазмы, так же как и к
гранул в реакторе. Повышение конверсии и энер-
изменениям свойств катализатора [58].
гоэффективности процесса разложения CO2 авторы
Природа катализатора или инертного материа-
связывают с большим количеством точек контакта,
ла с диэлектрическими свойствами, используемого
объемом пустот между гранулами и высоким отно-
для заполнения реактора, существенно влияет на
шением размера гранул к разрядному промежутку.
эффективность процесса разложения CO2. В лите-
В работе [61] показано, что в присутствии гра-
ратуре, относящейся к плазменно-каталитическим
нул диэлектрического материала CaTiO3 повышает-
процессам, катализатором часто называют материал,
ся средняя энергия электронов плазмы, тем самым
обладающий свойствами диэлектрика, далее эти два
способствуя диссоциации СО2 в барьерном разряде.
понятия (катализатор и диэлектрик) будут разделены.
Отмечено, однако, что в присутствии слоя диэлек-
Диэлектрические материалы используют в плазмохи-
трических гранул может также повышаться скорость
мическом реакторе для повышения напряженности
рекомбинации радикалов CO• и О•, что снижает кон-
электрического поля, что приводит к увеличению
версию CO2.
концентрации активных частиц плазмы и увеличе-
Сочетание диэлектрического материала BaTiO3 и
нию числа актов их взаимодействия с молекулами
катализатора Ni/Al2O3 в барьерном разряде исследо-
CO2. Это приводит к повышению конверсии молекул
вано в работе [62]. Введение катализатора 10 мас%
углекислого газа.
Ni/γ-Al2O3 или носителя катализатора γ-Al2O3 в
В работе [59] изучали разложение CO2 в барьер-
реактор, заполненный BaTiO3, повышает как кон-
ном разряде в присутствии слоя BaTiO3. BaTiO3 явля-
версию CO2, так и энергоэффективность процесса
ется сегнетоэлектриком с высоким значением диэлек-
разложения CO2. Загрузка катализатора перед слоем
трической проницаемости (~10 000). В присутствии
BaTiO3 ведет к более высокой конверсии CO2 и энер-
BaTiO3 обеспечивалась более высокая конверсия CO2
гоэффективности по сравнению с расположением в
и энергоэффективность в сравнении с процессом без
слое BaTiO3 или ниже по слою, поскольку обратная
введенного материала. В работе также изучали влия-
реакция — рекомбинация CO• и O• в CO2 — чаще
ние разбавления CO2 различными инертными газами
происходит ниже по слою. По сравнению с носителем
на конверсию CO2. В реакторе со слоем диэлектрика
γ-Al2O3 использование Ni-катализатора ведет к более
конверсия СО2 увеличилась с 19 в чистом СО2 до
высокой конверсии СО2, что может быть объяснено
36% в смеси СО2-Ar (20/80%) и до 35% в СО2-N2
присутствием активных частиц никеля на поверх-
(20/80%).
ности катализатора. Утверждается при этом, что в
В работе [60] исследовано влияние материала ре-
присутствии катализатора вклад в диссоциацию CO2
актора, а также конфигурации реактора/гранул на
вносят как газофазные реакции, так и поверхност-
конверсию и энергетическую эффективность про-
ные реакции с участием плазмы. В дополнение к
цесса разложения СО2 в реакторе с барьерным раз-
диссоциации CO2 под действием электронного удара
рядом. В присутствии инертного материала BaTiO3
в газовой фазе плазмы (4) молекулы CO2 как в основ-
552
Голубев О. В., Максимов А. Л.
ном, так и в возбужденном состоянии могут адсорби-
жет быть повышена вследствие увеличения плотно-
роваться на поверхности Ni с образованием CO2(адс),
сти электрического поля путем введения материалов с
которые способны диссоциировать на COадс и Oадс
высокой диэлектрической проницаемостью, таких как
под воздействием высокоэнергетических электро-
BaTiO3, оптимизированной конфигурации реактора,
нов (5). Частица COадс десорбируется, частица Oадс
введения подходящего катализатора и рекуперации/
рекомбинирует с образованием O2(адс) (6) с последу-
удаления тепловой энергии из реактора.
ющей десорбцией и выделением O2. Частицы COадс
В работе [64] сообщается о влиянии различных
и Oадс также могут образовываться при адсорбции
катализаторов на основе Fe2O3, промотированных
радикалов CO• и O• из газовой фазы на поверхности
CeO2, на разложение CO2 при низкой температуре и
катализатора. Не исключено протекание обратной ре-
атмосферном давлении. Указывается, что сочетание
акции рекомбинации CO• (или COадс) и O• (или Oадс)
оксидов Ce и Fe выбрано с целью снижения стои-
с образованием CO2 (7)-(10). Однако сообщалось,
мости таких катализаторов. В присутствии образца
что рекомбинация радикалов О• с образованием О2
5 мас% Fe-5 мас% Ce/γ-Al2O3 энергоэффективность
преобладает над рекомбинацией СО• с радикалами
составляла 13.6%, а конверсия CO2 — 24.5%, что поч-
О• на поверхности катализатора при низких темпе-
ти вдвое превышало значение конверсии, достигну-
ратурах [58].
тое при использовании 10 мас% Fe/γ-Al2O3 (13.3%).
Обнаружено, что эффективность реакции линейно
e + CO2 → CO• + O• + e,
(4)
зависит от степени образования твердого раствора
e + CO2(адс) → COадс + Oадс + e,
(5)
в биметаллических оксидных катализаторах Fe/Ce.
Это объясняют тем, что в твердом растворе легче
Oадс + Oадс → O2(адс),
(6)
происходит образование кислородных вакансий в
COадс + Oадс → CO2,
(7)
сравнении с катализатором, в котором оксиды Fe и
COадс + O• → CO2,
(8)
Ce находятся в отдельных фазах. Образование боль-
шего количества кислородных вакансий увеличивает
COадс + Oадс → CO2,
(9)
конверсию СО2, поскольку кислородные вакансии
CO• + O• + M → CO2 + M.
(10)
являются активными центрами диссоциации СО2.
Максимальная конверсия и энергоэффективность бы-
Для достижения более высокой конверсии СО2
ли достигнуты в присутствии катализатора 10 мас%
в барьерном разряде в работе [63] использовали
Сe/γ-Al2O3, что, однако, не связывают с образованием
ZrO2-CeO2-содержащий сферический катализатор.
кислородных вакансий.
В присутствии данного материала достигается макси-
Использование CeO2 в качестве катализатора раз-
мальная конверсия CO2 64% и энергоэффективность
ложения CO2 описано в работе [65]. Исследовано
8.76%. Сообщается, что в отличие от монооксидных
плазменно-каталитическое разложение CO2 в при-
материалов (Al2O3, ZrO2) катализатор с двумя окси-
сутствии CeO2-катализаторов, модифицированных
дами в составе (ZrO2-CeO2) может приводить к более
различными металлами: Fe, Co, Ni, Cu, Cr, V, Mn,
высокой эффективности процесса. Превосходящую
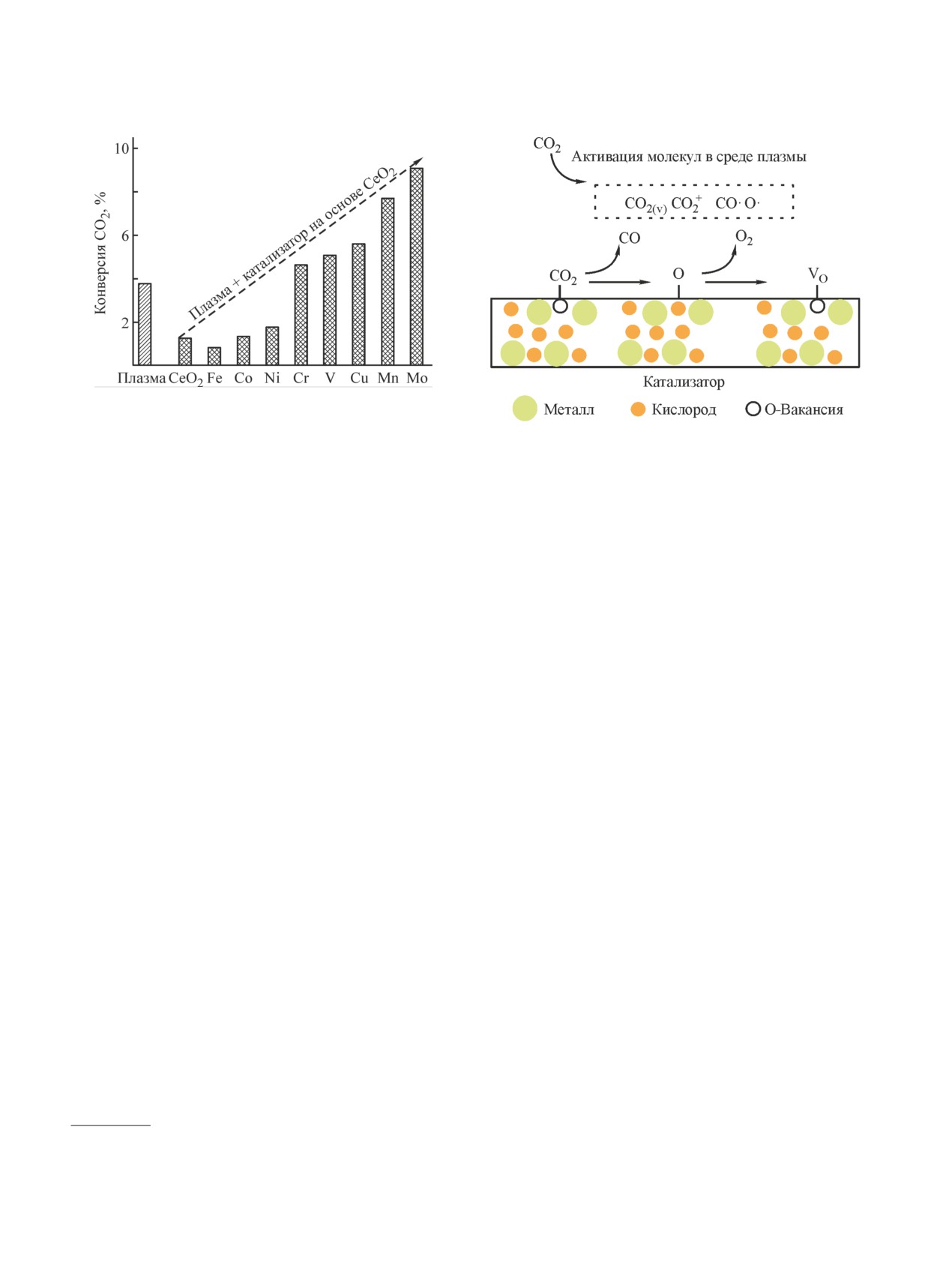
Mo. Наибольшую активность проявлял катализатор
активность смесевого катализатора связывают с кис-
Mo/CeO2 (рис. 3), что связывают с увеличением ко-
лородными вакансиями CeO2, которые стабилизиру-
личества кислородных вакансий вследствие сильного
ют атомарный кислород, образующийся в реакции,
взаимодействия металл-носитель между Mo и CeO2.
и тем самым способствуют повышению конверсии
Помимо увеличенного количества вакансий взаимо-
СО2.
действие металл-носитель приводило к повышению
Введение катализатора Ni/SiO2 в плазмохимиче-
стабильности вакансий. Это объясняется взаимодей-
ский реактор с BaTiO3 повышает конверсию CO2.
ствием между активным O•, образующимся в газовой
Утверждается [58], что молекула CO2 может акти-
фазе, и адсорбированным O на месте кислородной
вироваться на поверхности катализатора, что при-
вакансии, что приводит к десорбции кислорода в
водит к более высокой степени разложения CO2.
виде молекул O2 и восстановлению кислородных
Катализатор, однако, может способствовать протека-
вакансий.
нию обратной реакции (CO + O2 → CO2) при более
Предложен вероятный механизм диссоциации
высокой температуре стенок реактора (>115°C), что
молекулы CO2 в присутствии Ce-катализатора. На
приводит к снижению конверсии CO2 и снижению
первой стадии молекула СО2 активируется с образо-
энергоэффективности. Отмечено также, что энерго-
ванием возбужденных частиц СО2+, СО2(v) (колеба-
эффективность разложения CO2 в среде плазмы мо-
тельное возбужденное состояние молекулы), радика-
Плазменно-каталитическое разложение углекислого газа (обзор)
553
Рис. 3. Конверсия CO2 в присутствии модифицирован-
ных CeO2-катализаторов.*
Рис. 4. Механизм диссоциации CO2 в присутствии ката-
лизатора с кислородными вакансиями.
лов СО• и О• (рис. 4). Затем возбужденные частицы
CO2 адсорбируются на кислородных вакансиях VO
со снижением их внутренней энергии. Далее проис-
[68] сообщают об использовании пенометаллов Cu и
ходит разрыв связи C O и образуются частицы CO
Ni, в присутствии которых достигается увеличение
конверсии CO2 до 49%. Утверждается, что пеноме-
и Oадс. Эти частицы десорбируются с поверхности
таллы помимо генерации микроразрядов в плазме
катализатора в виде молекул CO и O2 (вследствие
способствуют адсорбции радикалов O• на поверхно-
реакции Oадс с активными радикалами О• в газовой
сти, вследствие чего равновесие смещается в сторону
фазе). Кислородные вакансии восстанавливаются, что
образования CO.
завершает каталитический цикл.
В присутствии гранул ZrO2 конверсия углекислого
В работе [66] исследовали процесс разложения
CO2 в барьерном разряде в присутствии катализато-
газа составляет 49-52% в зависимости от размера
ров TiO2, Al2O3, CeO2. Конверсия углекислого газа в
частиц катализатора [69]. Авторы работы отмечают,
присутствии CeO2 была максимальной и составляла
что увеличение конверсии CO2 в присутствии ZrO2
10.6%. В присутствии инертного материала — стек-
может быть связано как с диэлектрическими свой-
ствами катализатора, так и с морфологией частиц.
лянных шаров конверсия составляла 7.9%, в отсут-
Немаловажным фактором также является присут-
ствие какого-либо загруженного материала данная
ствие основных центров в катализаторе, что может
характеристика снижалась до 6.3%.
способствовать лучшей хемосорбции CO2 на по-
Использование пористых металлических катали-
верхности катализатора и приводит к увеличенной
заторов — пенометаллов Fe, Al, Ti описано в работе
конверсии CO2 [70]. Влияние кислотно-основных
[67]. Загрузка реактора таким материалом способ-
свойств катализаторов CaO, MgO, Al2O3, SiO2 на
ствовала изменению характера разряда: от нитевид-
ного к поверхностному разряду. Конверсия CO2 со-
конверсию CO2 также отмечено в работе [71]. В ре-
ставляла 45, 44 и 47%, а энергоэффективность — 6.9,
акторе с катализатором СаО конверсия была наивыс-
6.2, и 8.9% при использовании Fe, Al и Ti соответ-
шей и достигала 42%. Утверждается, что конверсия
CO2 коррелировала с основностью катализаторов.
ственно. Для сравнения конверсия CO2 в реакторе
В работе также утверждается, что высокая удельная
без пенометаллических материалов составляла 21%,
площадь поверхности катализатора Al2O3 не влия-
а энергоэффективность — 3.9%. Данные результаты
ет на конверсию CO2. Более существенное влияние
были подтверждены расчетами методом функционала
оказывает характер взаимодействия молекул CO2 с
плотности. Указывается, что адсорбция молекулы
катализатором. Подчеркивается, что CO2 легче разла-
CO2 на поверхности пенометалла Ti характеризуется
наименьшим активационным барьером среди ис-
гается в случае хемосорбции на поверхности MgO и
следованных катализаторов. Те же авторы в работе
CaO, чем при физической адсорбции на поверхности
Al2O3.
Оснóвные оксиды (MgO, CaO, Mg-Al-гидроксиды)
* Адаптировано из источника [65] с разрешения Royal
также были исследованы в качестве катализаторов раз-
ложения CO2 в работе [72]. Наибольшую активность в
554
Голубев О. В., Максимов А. Л.
разложении CO2 в барьерном разряде проявил образец
сит не только от состава катализатора, но также и от
MgO. Указывается, что при увеличении подводимой
размера и формы частиц. Важную роль в процессе
мощности с 30 до 60 Вт конверсия CO2 увеличилась
играет расстояние между электродами — разрядный
с 14.9 до 23.6%, при этом энергоэффективность сни-
промежуток. Уменьшение разрядного промежутка в
зилась с 8.9 до 6.1%. Активность MgO связывают с
реакторе со стационарным слоем катализатора мо-
характеристиками пористой структуры и наличием
жет значительно увеличить конверсию СО2, однако
основных центров в образце, что способствует хемо-
приводит к снижению энергоэффективности [78].
сорбции CO2 на поверхности катализатора.
Сравнительные характеристики процесса разложения
В работе [73] исследовали каталитический эффект
СО2 в барьерном разряде с использованием описанных
TiO2 и Al2O3 в смеси CO2 и Ar в различных соот-
катализаторов и диэлектриков приведены в таблице.
ношениях. Наилучший результат достигался с ис-
пользованием газовой смеси, содержащей 20% CO2,
Плазменно-каталитическое разложение CO2
в присутствии катализатора TiO2 (конверсия 30%,
в сверхвысокочастотном разряде
энергетическая эффективность 2.9%). При сравнении
кинетики реакции в присутствии Al2O3 и TiO2 выяв-
Сверхвысокочастотный разряд (СВЧ-разряд, также
лено, что скорость образования CO в обоих случаях
используется термин микроволновой разряд) широко
примерно одинакова, однако скорость обратной ре-
используется для разложения CO2 [39]. СВЧ-разряд
акции в ~2-3 раза ниже в случае TiO2. Авторы отме-
генерируется электромагнитным излучением в ди-
чают, что более высокие скорости обратной реакции
апазоне частот 915 МГц-2.45 ГГц [79, 80]. Важно
с использованием γ-Al2O3 и, как следствие, более
отметить, что в отличие от генерации других типов
низкие характеристики конверсии CO2 по сравнению
плазмы для генерации СВЧ-разряда не требуется
с TiO2 можно объяснить значительно более высокой
использование электродов. Отсутствие электродов
удельной площадью поверхности, что способствует
является преимуществом, поскольку электроды при
протеканию побочной реакции между CO и О на по-
длительной работе подвергаются эрозии. Наиболее
верхности катализатора.
часто для диссоциации CO2 используется плазма в
В исследовании [74] в качестве катализаторов
генераторах с поверхностными волнами. Указанный
разложения CO2 синтезировали нанесенные окси-
разряд возникает при пропускании газа через кварце-
ды NiO/Al2O3 и CuO/Al2O3 с содержанием оксида
вую трубку, которая пересекает устройство, генери-
металла 15 мас%. В присутствии NiO/Al2O3 кон-
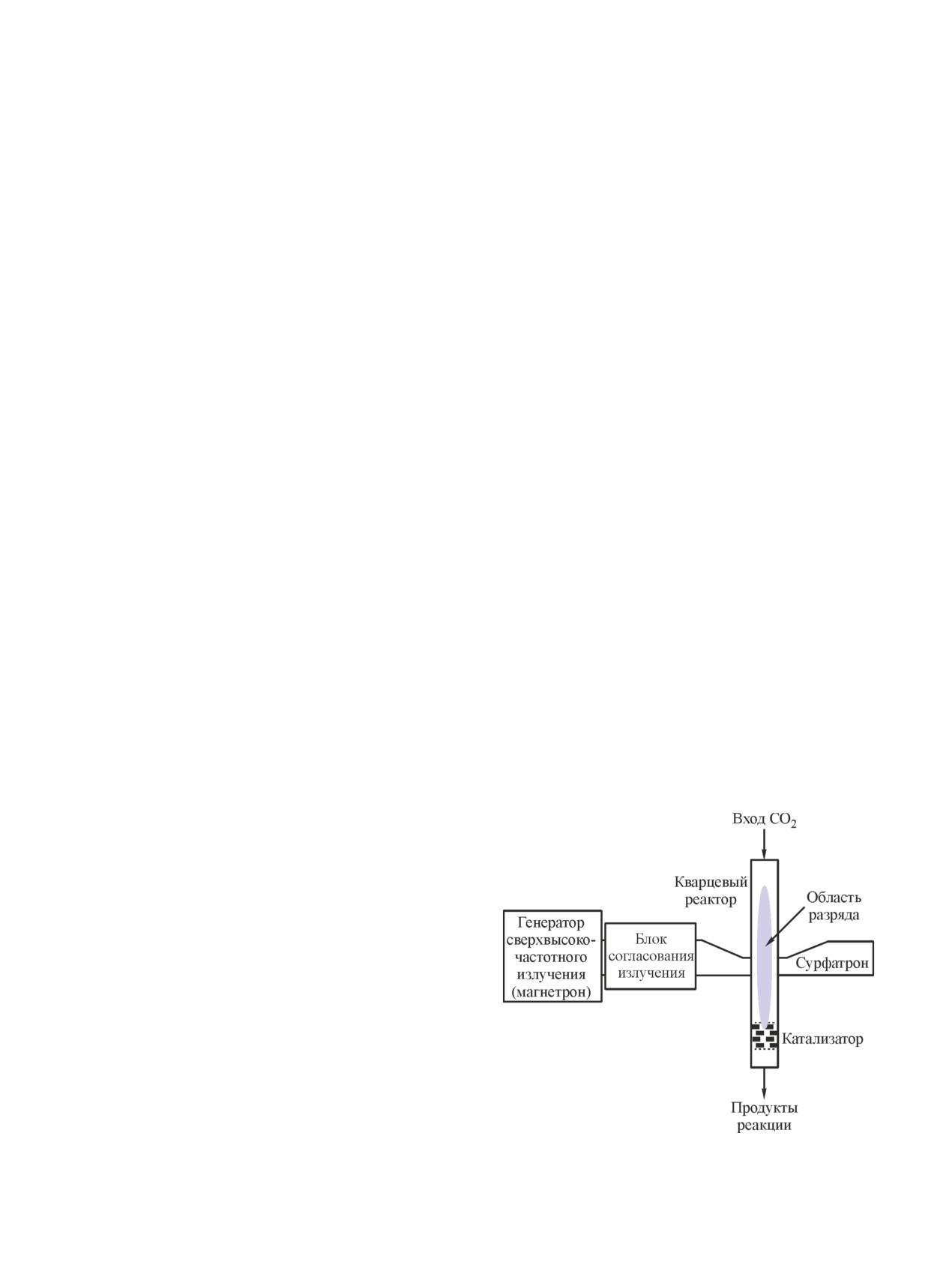
рующее поверхностные волны (сурфатрон) (рис. 5).
версия CO2 увеличилась с 7.4 (при проведении про-
Энергия поглощается плазмой при распространении
цесса без катализатора) до 10.5%. Использование
электромагнитных волн вдоль границы между кварце-
катализатора CuO/Al2O3 привело к увеличению кон-
вой трубкой и плазменным столбом. Эффективность
версии CO2 в сравнении с образцом NiO/Al2O3, что
объясняется более основными свойствами образца
CuO/Al2O3.
Помимо традиционных катализаторов на основе
оксидов металлов для плазменно-каталитического
разложения CO2 используют соединение g-C3N4 (гра-
фитоподобный нитрид углерода), который может
выступать в качестве носителя для катализаторов,
а также используется в фотокатализе [75]. В рабо-
те [76] конверсия CO2 в присутствии катализатора
g-C3N4 увеличилась вдвое в сравнении с плазмохими-
ческим процессом без катализатора (17% в условиях
охлаждаемого реактора). В работе [77] исследовано
разложение CO2 в присутствии смешанных ката-
лизаторов TiO2/g-C3N4 и ZnO/g-C3N4. Отмечается,
что наилучшие показатели конверсии достигаются в
присутствии ZnO/g-C3N4 вследствие более основных
свойств ZnO.
Эффективность плазменно-каталитического раз-
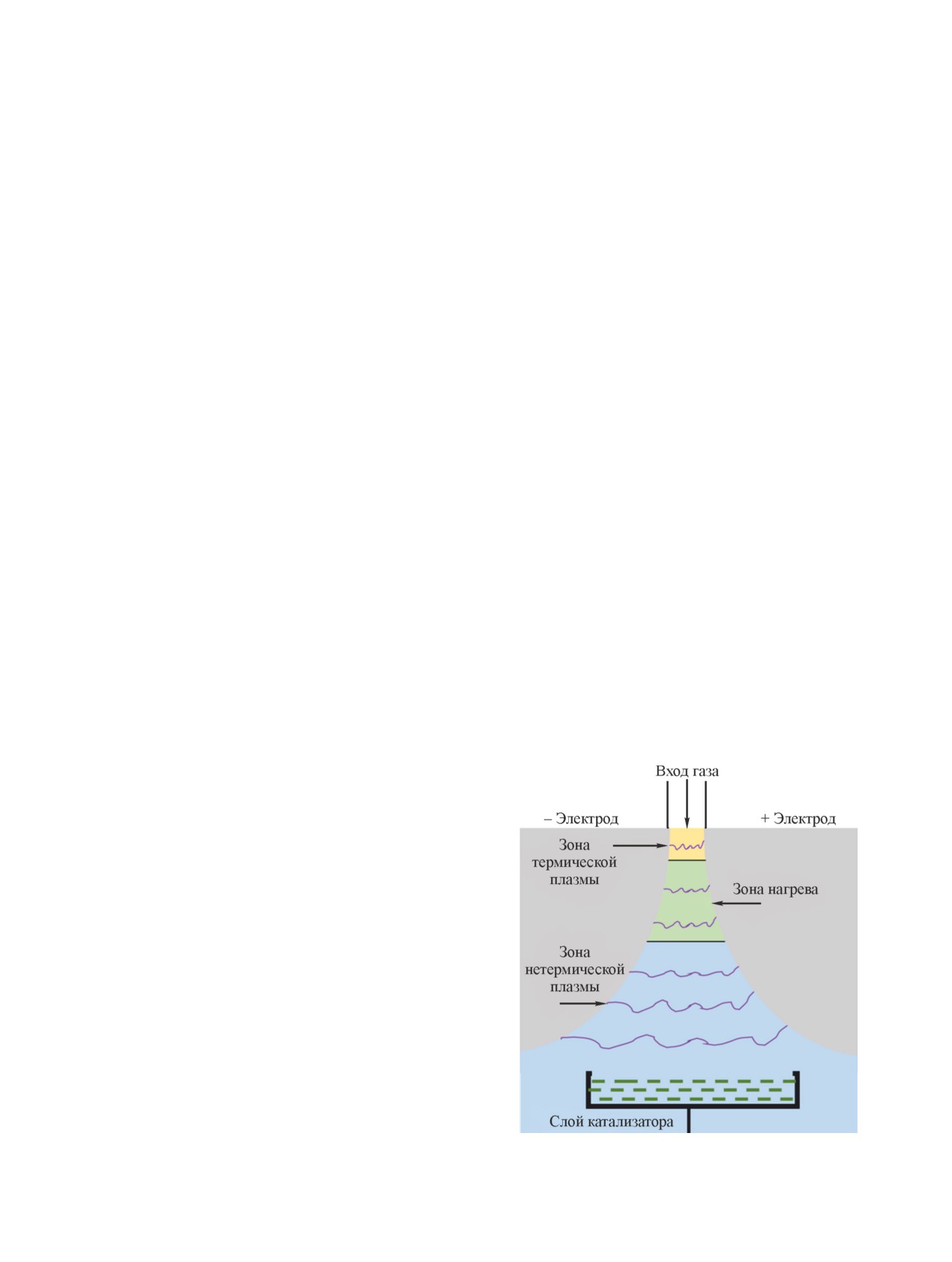
Рис. 5. Блок-схема плазменно-каталитической установки
ложения CO2 в реакторе с барьерным разрядом зави-
со сверхвысокочастотным разрядом.
Плазменно-каталитическое разложение углекислого газа (обзор)
555
Сравнение эффективности различных катализаторов и диэлектрических материалов
в процессе разложения CO2 в барьерном разряде
Расход CO2,
Энергетическая
Конверсия CO2,
Литературный
Катализатор/диэлектрик
Мощность, Вт
мл·мин-1
эффективность, %
%
источник
Ni/SiO2 + BaTiO3
50
105
—
23
[58]
BaTiO3
—
—
4.5
25
[60]
Al2O3
40
35
—
16.5
[61]
CaTiO3
40
35
—
20.5
[61]
BaTiO3 + Ni/Al2O3
30
40
4.1
26.3
[62]
BaTiO3 + Al2O3
30
40
3.9
24.7
[62]
BaTiO3
30
40
3.5
22.6
[62]
ZrO2-CeO2
20
50
2.4
64
[63]
γ-Al2O3
40
15
10.2
18.3
[64]
5 мас%Fe-5 мас%Ce/γ-Al2O3
40
15
13.6
24.5
[64]
10 мас%Fe/γ-Al2O3
40
15
7.4
13.3
[64]
7 мас%Fe-3 мас%Ce/γ-Al2O3
40
15
6.7
12.1
[64]
3 мас%Fe-7 мас%Ce/γ-Al2O3
40
15
5.3
9.5
[64]
10 мас%Ce/γ-Al2O3
40
15
15.7
28.2
[64]
Mo/CeO2
40
13.5
14.3
23.2
[65]
CeO2
20
1.6
—
10.6
[66]
TiO2
20
2.2
—
8.2
[66]
γ-Al2O3
20
1.9
—
9.1
[66]
Пенометалл Ti
20
110
8.9
47
[67]
Пенометалл Fe
20
110
6.9
45
[67]
Пенометалл Al
20
110
6.2
44
[67]
Пенометалл Cu
20
55
3.4
49.2
[68]
Пенометалл Ni
20
55
3.2
48.6
[68]
ZrO2
20
55
4
52.1
[69]
CaO
19.8
25
5.7
41.9
[71]
TiO2
43.7
60
4
16
[72]
MgO
43.7
60
6.1
24
[72]
Mg-Al-LDH
43.7
60
5.8
20
[72]
CaO
43.7
60
4.8
19
[72]
TiO2
—
—
2.9
30
[73]
NiO/Al2O3
30
2.2
—
10.5
[74]
CuO/Al2O3
30
2.2
—
15.7
[74]
CuO/CeAl
30
2.2
—
13.5
[74]
g-C3N4
—
40
—
17
[76]
5мас% ZnO/g-C3N4
30
2.4
—
12
[77]
П р и мечан и е. «—» — нет данных.
СВЧ-разряда в процессе диссоциации CO2 значи-
ется до 90% [81]. Утверждается, что при плазмохими-
тельно зависит от давления: при низком давлении
ческом разложении CO2 СВЧ-разряд характеризуется
(10 мТорр), энергоэффективность процесса повыша-
наибольшей энергетической эффективностью [33, 82].
556
Голубев О. В., Максимов А. Л.
Введение катализатора может повышать эффектив-
ка при возбуждении разряда может варьироваться
ность разложения CO2 в СВЧ-разряде. Катализатор в
от нескольких ампер до нескольких сотен ампер.
реакторе СВЧ-разряда предпочтительно располагать
Установка состоит из двух наклонных или полуба-
в области послесвечения разряда (в отличие от кон-
рабанных электродов, расходящихся вертикально.
струкции реактора с барьерным разрядом), поскольку
В основании электродов дуга является термической,
высокая температура в зоне плазмы может негатив-
затем, по мере перемещения дуги, приобретает не-
но влиять на структуру катализатора: приводить к
равновесные характеристики (рис. 6). Ввод газа осу-
дезактивации активных центров, а также повышать
ществляется в месте, где разрядный промежуток ми-
степень образования углерода [83].
нимален. В скользящем дуговом разряде различают
В исследовании [84] разложение CO2 в СВЧ-
три фазы существования дуги: фаза газового пробоя
разряде проводили в присутствии катализатора NiO/
(высокое напряжение создает разряд), фаза равно-
TiO2. Показано, что предварительная обработка
весного нагрева (разряд достигает более высокой
Ar-плазмой приводит к образованию кислородных
температуры) и нетермическая плазменная стадия,
вакансий в TiO2. При использовании NiO/TiO2(Ar)
образующаяся при движении дуги вверх на больших
значительно повышаются как конверсия CO2 (с 23 до
расстояниях между электродами.
42%), так и энергоэффективность процесса (с 9.6 до
Сообщается, что реактор со скользящим дуговым
17.2%). Это объясняется образованием кислородных
разрядом позволяет осуществлять разложение CO2
вакансий на поверхности катализатора. Молекулы
с высокой энергоэффективностью [87] вследствие
CO2 адсорбируются на кислородных вакансиях CeO2
большой разницы температур между дугой и вхо-
с последующим разрывом связи С O и отщеплением
дящим газом. В работе [88] исследовано влияние
молекулы CO. Те же авторы в работе [85] исследовали
образца TiO2, размещенного вне зоны разряда, на
влияние способов предобработки катализатора NiO/
конверсию CO2 и энергоэффективность. Сообщается,
TiO2 на конверсию СО2 и энергоэффективность в
что конверсия CO2 в присутствии катализатора повы-
непрерывном СВЧ-разряде. Отмечается, что по срав-
шается с 4.8 до 10.8%, а энергоэффективность — с
нению с традиционным прокаливанием на воздухе
5.4 до 12.6%. Авторы объясняют каталитический
или в аргоне плазменная обработка в атмосфере Ar
эффект TiO2 наличием кислородных вакансий на
приводит к более высокой плотности кислородных
поверхности катализатора (аналогичный эффект в
вакансий и равномерному распределению NiO на
СВЧ-разряде описывается в работах [81, 82]). В ду-
поверхности TiO2. Кислородные вакансии стабили-
говом разряде конверсия CO2 снижается при более
зируются ионами Ni2+ в решетке анатаза.
высоких скоростях потока вследствие уменьшения
Пример негативного эффекта при введении напол-
нителя в плазмохимический реактор в реакции раз-
ложения CO2 проиллюстрирован в [86]. В реактор с
СВЧ-разрядом помещали монолитные материалы Rh/
TiO2, в присутствии которых эффективность диссо-
циации CO2 снижается. Указывается, что монолитная
структура материалов сужает выходящий газовый
поток, что приводит к повышению давления и сни-
жает эффективность процесса. Отмечается также,
что композиция Rh/TiO2 ускоряет обратную реакцию
(образование CO2 из CO и O2), что приводит к уве-
личению количества СО2, выходящего из реактора.
Плазменно-каталитическое разложение CO2
в дуговом разряде
Скользящий дуговой разряд образуется при про-
текании электрического тока в сильном электриче-
ском поле в малом разрядном промежутке между
двумя электродами [4]. Название этого типа разряда
объясняется движением электрической дуги вдоль
Рис. 6. Схема реактора со скользящим дуговым разря-
электрода под воздействием потока газа. Сила то-
дом.
Плазменно-каталитическое разложение углекислого газа (обзор)
557
времени контакта газа с катализатором. Указывается,
разложения CO2 в различных конфигурациях разря-
что размещение катализатора на большом расстоянии
дов: барьерном разряде, СВЧ-разряде и скользящем
от разряда (15-20 мм) нецелесообразно. Поскольку
дуговом разряде. Большинство опубликованных ра-
катализаторы обычно размещают ниже по потоку,
бот, касающихся данной тематики, описывают раз-
что соответствует нетермической области дугового
ложение CO2 в реакторе с барьерным разрядом, что
разряда, предполагают, что каталитический эффект
обусловлено относительной простотой конструкции
является в основном результатом взаимодействия
реактора. Для повышения конверсии CO2 в барьерном
катализатора с высокоэнергетическими электронами
разряде пространство между электродами заполняют
плазмы.
диэлектрическими материалами и катализаторами.
Роль диэлектрического материала заключается в уве-
личении плотности электрического поля и создании
Факторы, обусловливающие каталитическую
микроразрядов в точках контакта гранул или сфер диэ-
активность в процессе разложения CO2
лектрика. Повышение плотности электрического поля
Проанализированные источники позволяют вы-
способствует увеличению конверсии CO2 в результа-
делить ключевые факторы, способствующие по-
те бомбардировки молекул высокоэнергетическими
вышению конверсии углекислого газа в условиях
электронами. В качестве диэлектриков используют
плазменного катализа. Одним из важных факторов
вещества с высокой диэлектрической проницаемо-
является наличие в кристаллической решетке ок-
стью (ε ~ 100-10 000): ZrO2, CaTiO3, BaTiO3. При
сида металла дефектов, обусловливающих появле-
помещении каталитического материала (CeO2, TiO2,
ние кислородных вакансий (CeO2, TiO2, ZnO и др.).
Al2O3, CaO, MgO и др.) в область разряда происходит
Кислородные вакансии способствуют адсорбции мо-
как изменение физических характеристик плазмы,
лекул СО2. Высокоэнергетические электроны плазмы,
обусловленное возникновением микроразрядов в ме-
взаимодействуя с молекулами CO2, способствуют
стах контакта гранул, так и каталитические эффекты,
диссоциации последних на CO и O. Впоследствии
обусловленные адсорбцией CO2 на поверхности ка-
молекула CO десорбируется с поверхности катали-
тализатора. Одними из важных свойств катализатора,
затора. Регенерация кислородной вакансии осущест-
обеспечивающих высокую конверсию CO2, являются
вляется за счет рекомбинации мостикового атома
кислотно-основные свойства образца. Наличие основ-
кислорода на поверхности катализатора с атомом
ных центров в катализаторе приводит к эффективной
кислорода в газовой фазе. Таким образом поддержи-
хемосорбции CO2 и последующему его разложению.
вается равновесие активных центров катализатора
Еще одним фактором, способствующим адсорбции
[89]. Существенными являются и иные свойства ката-
CO2 на поверхности катализатора и повышению кон-
лизатора, определяющие эффективность разложения
версии CO2 в плазменно-каталитической системе,
CO2: структурные, кислотно-основные свойства и
является наличие кислородных вакансий в структу-
иные физико-химические характеристики катализа-
ре катализатора (CeO2, TiO2 и другие соединения).
тора. Удельная площадь поверхности катализатора
Плазменно-каталитическое разложение CO2 в
незначительно влияет на эффективность разложения
СВЧ-разряде и дуговом разряде описано в работах не
CO2 в разряде: более важными факторами, опреде-
столь подробно по сравнению с реакцией в барьерном
ляющими конверсию CO2, являются кислотно-ос-
разряде. Причинами этому могут быть сложность кон-
новные свойства катализатора. В случае носителя
струкции таких систем, а также высокая температура
катализатора, обладающего кислотными свойствами,
в области разряда (~3000 K), что приводит к необхо-
CO2 физически адсорбируется на активных центрах
димости располагать катализатор вне зоны плазмы.
катализатора, в то время как при использовании ма-
Сочетание плазменных и каталитических техноло-
териала с основными свойствами молекула диоксида
гий в процессе разложения CO2 перспективно с точки
углерода хемосорбируется с образованием карбонат-
зрения увеличения конверсии CO2 и энергоэффектив-
ных частиц. Отмечается, что к наиболее высокой кон-
ности процесса, поэтому актуальным остается разра-
версии приводит хемосорбция CO2 на поверхности
ботка новых каталитических систем и исследование
катализаторов с основными свойствами.
их активности.
Заключение
Благодарности
В работе проанализированы закономерности плаз-
Авторы выражают благодарность д.ф.-м.н.
менно-каталитического взаимодействия в процессе
Ю. А. Лебедеву за помощь при подготовке публикации.
558
Голубев О. В., Максимов А. Л.
Финансирование работы
[8]
Бубнов А. Г., Бурова Е. Ю. (Квиткова Е. Ю.),
Гриневич В. И., Кувыкин Н. А. Плазменно-каталити-
Работа выполнена в рамках государственного
ческая деструкция фенолов // ЖПХ. 2005. Т. 78.
задания Института нефтехимического синтеза им.
№ 7. С. 1127-1129 [Bubnov A. G., Burova E. Yu.,
А. В. Топчиева РАН.
Grinevich V. I., Kuvykin N. A. Combined plasma-
induced and catalytic decomposition of phenols //
Russ. J. Appl. Chem. 2005. V. 78. P. 1106-1109.
Конфликт интересов
[9]
Bubnov A. G., Burova E. Yu., Grinevich V. I.,
А. Л. Максимов является главным редактором
Rybkin V. V., Kim J.-K., Choi H.-S. Plasma-catalytic
Журнала прикладной химии. О. В. Голубев заявляет
decomposition of phenols in atmospheric pressure
об отсутствии конфликта интересов, требующего
dielectric barrier discharge // Plasma Chem. Plasma
раскрытия в данной статье.
Process. 2006. V. 26. P. 19-30.
[10]
Bobkova E. S., Grinevich V. I., Ivantsova N. A.
Информация об авторах
Influence of various solid catalysts on the destruction
Голубев Олег Владимирович, к.х.н.
kinetics of sodium lauryl sulfate in aqueous solutions
by DBD // Plasma Chem. Plasma Process. 2012. V 32.
Максимов Антон Львович, д.х.н., чл-корр. РАН
N 4. P. 703-714.
[11]
Kim H. H., Takashima K., Katsura S., Mizuno A. Low-
temperature NOx reduction processes using combined
systems of pulsed corona discharge and catalysts // J.
Список литературы
Phys. D: Appl. Phys. 2001. V. 34. N 4. P. 604-613.
[1] Yaashikaa P. R., Senthil Kumar P., Varjanic S. J.,
Saravanan A. A review on photochemical, biochemical
[12]
Bröer S., Hammer T. Selective catalytic reduction of
and electrochemical transformation of CO2 into value-
nitrogen oxides by combining a non-thermal plasma
added products // J. CO2 Util. 2019. V. 33. P. 131-147.
and a V2O5-WO3/TiO2 catalyst // Appl. Catal. B.
2000. V. 28. N 2. P. 101-111.
[2] Roy S. C., Varghese O. K., Paulose M., Grimes C. A.
Toward solar fuels: Photocatalytic conversion of carbon
[13]
Wang Z., Kuang H., Zhang J., Chu L., Ji Y. Nitrogen
dioxide to hydrocarbons // ACS Nano. 2010. V. 4.
oxide removal by non-thermal plasma for marine
diesel engines // RSC Adv. 2019. V. 9. P. 5402-5416.
[3] Erdogan A., Orhan O. Y. CO2 utilization: Developments
in conversion processes // Petroleum. 2017. V. 3.
[14]
Гущин П. А., Иванов Е. В., Винокуров В. А. Плаз-
N 1. P. 109-126.
менно-каталитическая углекислотная конверсия
метана в синтез-газ // Технологии нефти и газа.
[4] Carreon M. L. Plasma catalysis: A brief tutorial //
2008. Т. 59. № 6. С. 16-20.
Plasma Res. Express. 2019. V. 1. ID 043001.
[15]
Tu X., Whitehead J. C. Plasma dry reforming of
methane in an atmospheric pressure AC gliding
[5] Holzer F., Roland U., Kopinke F.-D. Combination
arc discharge: Co-generation of syngas and carbon
of non-thermal plasma and heterogeneous catalysis
nanomaterials // Int. J. Hydrogen Energy. 2014. V. 39.
for oxidation of volatile organic compounds: Part 1.
N 18. P. 9658-9669.
Accessibility of the intra-particle volume // Appl. Catal.
B. 2002. V. 38. N 3. P. 163-181.
[16]
Tu X., Whitehead J. C. Plasma-catalytic dry reforming
of methane in an atmospheric dielectric barrier
[6] Hossain Md. M., Mok Y. S., Nguyen V. T., Sosiawati T.,
discharge: Understanding the synergistic effect at low
Lee B., Kim Y. J., Lee J. H., Heo I. Plasma-catalytic
temperature // Appl. Catal. B. 2012. V. 125. P. 439-448.
oxidation of volatile organic compounds with
honeycomb catalyst for industrial application // Chem.
[17]
Diao Y., Zhang X., Liu Y., Chen B., Wu G., Shi C.
Eng. Res. Des. 2022. V. 177. P. 406-417.
Plasma-assisted dry reforming of methane over Mo2C-
Ni/Al2O3 catalysts: Effects of β-Mo2C promoter //
[7] Liu S., Zhou J., Liu W., Zhang T. Removal of toluene
Appl. Catal. B. 2022. V. 301. ID 120779.
in air by a non-thermal plasma-catalytic reactor using
MnOx/ZSM-5 // Catal. Lett. 2022. V. 152. N 1. P. 239-
[18]
Lin S.-S., Li P.-R., Jiang H.-B., Diao J.-F., Xu Z.-N.,
Guo G.-C. Plasma promotes dry reforming reaction
Плазменно-каталитическое разложение углекислого газа (обзор)
559
of CH4 and CO2 at room temperature with highly
[Chistyakov A. V., Konstantinov G. I., Tsodikov M. V.,
dispersed NiO/γ-Al2O3 catalyst // Catalysts. 2021.
Maximov A. L. Rapid conversion of methane to
V. 11. N 12. ID 1433.
hydrogen stimulated by microwave irradiation on the
surface of a carbon adsorbent // Dokl. Phys. Chem.
[19]
Kim S. S., Jorat M., Voecks G., Kuthi A., Surampudi S.,
2021. V. 498. N 1. P. 49-53.
Kent R. L. Hydrogen from steam methane reforming
by catalytic nonthermal plasma using a dielectric
[28]
Цодиков М. В., Чистяков А. В., Константинов Г. И.,
barrier discharge reactor // AIChE J. 2020. V. 66.
Николаев С. А., Борисов Р. С., Левин И. С.,
Максимов Ю. В., Гехман А. Е. Cтимулированное
[20]
King B., Patel D., Chen J. Z., Drapanauskaite D.,
микроволновым излучением превращение сме-
Handler R., Nozaki T., Baltrusaitis J. Comprehensive
си гудрона и лигнина в углеводороды в плазмен-
process and environmental impact analysis of
но-каталитическом режиме // ЖПХ. 2021. Т. 94.
integrated DBD plasma steam methane reforming //
№ 10-11. С. 1336-1348.
Fuel. 2021. V. 304. ID 121328.
[Tsodikov M. V., Chistyakov A. V., Konstantinov G. I.,
[21]
Zhu X., Liu X., Lian H.-Y., Liu J.-L., Li X.-S. Plasma
Nikolaev S. A., Borisov R. S., Levin I. C.,
catalytic steam methane reforming for distributed
Maksimov Yu. V., Gekhman A. E. Microwave-
hydrogen production // Catal. Today. 2019. V. 337.
stimulated conversion of a tar/lignin blend into
hydrocarbons in a plasma-catalytic mode // Russ. J.
[22]
Nozaki T., Hiroyuki T., Fukui W., Okazaki K. Kinetic
Appl. Chem. 2021. V. 94. P. 1513-1524.
analysis of the catalyst and nonthermal plasma hybrid
reaction for methane steam reforming // Energy Fuels.
[29]
Rönsch S., Schneider J., Matthischke S., Schlüter M.,
2007. V. 21. P. 2525-2530.
Götz M., Lefebvre J., Prabhakaran P., Bajohr S.
Review on methanation — From fundamentals to
[23]
Gao X., Liang J., Wu L., Wu L., Kawi S. Dielectric
current projects // Fuel. 2016. V. 166. P. 276-296.
barrier discharge plasma-assisted catalytic CO2
hydrogenation: Synergy of catalyst and plasma //
[30]
Artz J., Muller T. E., Thenert K. Sustainable conversion of
Catalysts. 2022. V. 12. N 1. ID 66.
carbon dioxide: An integrated review of catalysis and life
cycle assessment // Chem. Rev. 2018. V. 118. P. 434-504.
[24]
Iwamoto M., Akiyama M., Aihara K., Deguchi T.
Ammonia synthesis on wool-like Au, Pt, Pd, Ag, or Cu
[31]
Godin J., Liu W., Ren S., Xu C. C. Advances in recovery
electrode catalysts in nonthermal atmospheric-pressure
and utilization of carbon dioxide: A brief review // J.
plasma of N2 and H2 // ACS Catal. 2017. V. 7. N 10.
Environ. Chem. Eng. 2021. V. 9. ID 105644.
P. 6924-6929.
[32]
Ronda-Lloret M., Wang Y., Oulego P., Rothenberg G.,
[25]
Gorky F., Lucero J. M., Crawford J. M., Blake B.,
Tu X., Shiju N. R. CO2 hydrogenation at atmospheric
Carreon M. A., Carreon M. L. Plasma-induced
pressure and low temperature using plasma-enhanced
catalytic conversion of nitrogen and hydrogen to
catalysis over supported cobalt oxide catalysts // ACS
ammonia over zeolitic imidazolate frameworks ZIF-8
Sustainable Chem. Eng. 2020. V. 8. N 47. P. 17397-
and ZIF-67 // ACS Appl. Mater. & Interfaces. 2021.
17407.
V. 13. N 18. P. 21338-21348.
[33]
George A., Shen B., Craven M., Wang Y., Kang D.,
[26]
Liu T.-W., Gorky F., Carreon M. L., Gómez-
Wu C., Tu X. A Review of non-thermal plasma
Gualdrón D. A. Energetics of reaction pathways
technology: A novel solution for CO2 conversion
enabled by N and H radicals during catalytic, plasma-
and utilization // Renewable Sustainable Energy Rev.
assisted NH3 synthesis // ACS Sustainable Chem. Eng.
2021. V. 135. ID 109702.
2022. V. 10. N 6. P. 2034-2051.
[34]
Mehta P., Barboun P., Go D. B., Hicks J. C.,
[27]
Чистяков А. В., Константинов Г. И., Цодиков М. В.,
Schneider W. F. Catalysis enabled by plasma activation
Максимов А. Л. Скоростное превращение метана в
of strong chemical bonds: A review // ACS Energy
водород на поверхности углеродного адсорбен-
Lett. 2019. V. 4. P. 1115-1133.
та, стимулированное микроволновым излучением
// Докл. РАН. Химия, науки о материалах. 2021.
[35]
Wang L., Yi Y., Wu C., Guo H., Tu X. One-step
T. 498. № 1. С. 64-68.
reforming of CO2 and CH4 into high-value liquid
chemicals and fuels at room temperature by plasma-
560
Голубев О. В., Максимов А. Л.
driven catalysis // Angew. Chem. Int. Ed. 2017. V. 56.
[46]
Chen H. L., Lee H. M., Chen S. H., Chao Y.,
N 44. P. 13679-13683.
Chang M. B. Review of plasma catalysis on
hydrocarbon reforming for hydrogen production —
[36]
Mei D., Tu X. Conversion of CO2 in a cylindrical
Interaction, integration, and prospects // Appl. Catal.
dielectric barrier discharge reactor: Effects of plasma
B. 2008. V. 85. N 1-2. P. 1-9.
processing parameters and reactor design // J. CO2
Util. 2017. V. 19. P. 68-78.
[47]
Chung W.-C., Chang M.-B. Review of catalysis and
plasma performance on dry reforming of CH4 and
[37]
Paulussen S., Verheyde B., Tu X., De Bie C.,
possible synergistic effects // Renewable Sustainable
Martens T., Petrovic D., Bogaerts A., Sels B.
Energy Rev. 2016. V. 62. P. 13-31.
Conversion of carbon dioxide to value-added
chemicals in atmospheric pressure dielectric barrier
[48]
Kim H. H., Teramoto Y., Sano T., Negishi N., Ogata A.
discharges // Plasma Sources Sci. Technol. 2010.
Effects of Si/Al ratio on the interaction of nonthermal
V. 19. ID 034015.
plasma and Ag/HY catalysts // Appl. Catal. B. 2015.
V. 166-167. P. 9-17.
[38]
Matsumoto H., Tanabe S., Okitsu K., Hayashi Y.,
Suib S. L. Profiles of carbon dioxide decomposition in
[49]
Tu X., Gallon H. J., Whitehead J. C. Plasma-assisted
a dielectric-barrier discharge-plasma system // Bull.
reduction of a NiO/Al2O3 catalyst in atmospheric
Chem. Soc. Jpn. 1999. V. 72. N 11. P. 2567-2571.
pressure H2/Ar dielectric barrier discharge // Catal.
Today. 2013. V. 211. P. 120-125.
[39]
Лебедев Ю. А., Шахатов В. А. Разложение углекис-
лого газа в СВЧ-разрядах // ЖПХ. 2022. Т. 95. № 1.
[50]
Wu Y.-W., Chung W.-C., Chang M.-B. Modification of
С. 39-59.
Ni/γ-Al2O3 catalyst with plasma for steam reforming
of ethanol to generate hydrogen // Int. J. Hydrogen
[Lebedev Y. A., Shakhatov V. A. Decomposition of
Energy. 2015. V. 40. N 25. P. 8071-8080.
carbon dioxide in microwave discharges (an analytical
review) // Russ. J. Appl. Chem. 2022. V. 95. N 1.
[51]
Bogaerts A., Zhang Q.-Z., Zhang Y.-R., Van Laer K.,
Wang W. Burning questions of plasma catalysis:
[40]
Mitsingas C., Rajasegar R., Hammack S., Do H.
Answers by modeling // Catal. Today. 2019. V. 337.
High energy efficiency plasma conversion of CO2
at atmospheric pressure using a direct-coupled
[52]
Fridman A. Plasma Chemistry. Cambridge: Cambridge
microwave plasma system // IEEE Trans. Plasma Sci.
University Press, 2008. P. 268.
2016. V. 44. N 4. P. 651-656.
[53]
Snoeckx R., Bogaerts A. Plasma technology — a novel
solution for CO2 conversion? // Chem. Soc. Rev. 2017.
[41]
Berthelot A., Bogaerts A. Modeling of CO2 splitting in
V. 46. P. 5805-5863.
a microwave plasma: How to improve the conversion
and energy efficiency // J. Phys. Chem. C. 2017.
[54]
Scapinello M., Delikonstantis E., Stefanidis G. D. The
V. 121. N 15. 8236-8251.
panorama of plasma-assisted non-oxidative methane
reforming // Chem. Eng. Process.: Process Intensif.
[42]
Li L., Zhang H., Li X., Kong X., Xu R., Tay K., Tu X.
2017. V. 117. P. 120-140.
Plasma-assisted CO2 conversion in a gliding arc
discharge: Improving performance by optimizing the
[55]
Kogelschatz U. Dielectric-barrier discharges: Their
reactor design // J. CO2 Util. 2019. V. 29. P. 296-303.
history, discharge physics, and industrial applications
// Plasma Chem. Plasma Process. 2003. V. 23. N 1.
[43]
Zhang H., Li L., Li X., Wang W., Yan J., Tu X. Warm
plasma activation of CO2 in a rotating gliding arc
[56]
Fridman A., Chirokov A., Gutsol A. Non-thermal
discharge reactor // J. CO2 Util. 2018. V. 27. P. 472-
atmospheric pressure discharges // J. Phys. D: Appl.
Phys. 2005. V. 38. N 2. R1.
[44]
Фортов В. Е. Энциклопедия низкотемпературной
плазмы. Тематический том VIII-1. Химия низко-
[57]
Лебедев Ю. А., Шахатов В. А. Разложение СО2 в
температурной плазмы. М: Янус-К, 2005. С. 4-35.
барьерном разряде атмосферного давления (ана-
[45]
Kim H. H., Teramoto Y., Ogata A., Takagi H., Nanba T.
литический обзор) // Успехи прикл. физики. 2022.
Plasma catalysis for environmental treatment and
energy applications // Plasma Chem. Plasma Process.
2016. V. 36. P. 45-72.
[58]
Zhang K., Zhang G., Liu X., Phan A.N., Luo K.
A Study on CO2 decomposition to CO and O2 by
Плазменно-каталитическое разложение углекислого газа (обзор)
561
the combination of catalysis and dielectric-barrier
[69]
Zhou A., Chen D., Ma C., Yu F., Dai B. DBD
discharges at low temperatures and ambient pressure //
Plasma-ZrO2 catalytic decomposition of CO2 at low
Ind. Eng. Chem. Res. 2017. V. 56. N 12. P. 3204-3216.
temperatures // Catalysts. 2018. V. 8. ID 256.
[59]
Xu S., Whitehead C. J., Martin P. A. CO2 conversion
[70]
Mei D., He Y., Liu S., Yan J., Tu X. Optimization of
in a non-thermal, barium titanate packed bed plasma
CO2 conversion in a cylindrical dielectric barrier
reactor: The effect of dilution by Ar and N2 // Chem.
discharge reactor using design of experiments //
Eng. J. 2017. V. 327. P. 764-773.
Plasma Process. Polym. 2016. V. 13. P. 544-556.
[60]
Michielsen I., Uytdenhouwen Y., Pype J.,
[71]
Duan X., Hu Z., Li Y., Wang B. Effect of dielectric
Michielsen B., Mertens J., Reniers F., Meynen V.,
packing materials on the decomposition of carbon
Bogaerts A. CO2 dissociation in a packed bed DBD
dioxide using DBD microplasma reactor // AlChE J.
reactor: First steps towards a better understanding
2015. V. 61. N 3. P. 898-903.
of plasma catalysis // Chem. Eng. J. 2017. V. 326.
[72]
Wang B., Li X., Wang X., Zhang B. Effect of filling
[61]
Yu Q., Kong M., Liu T., Fei J., Zheng X. Characteristics
materials on CO2 conversion with a dielectric barrier
of the decomposition of CO2 in a dielectric packed-
discharge reactor // J. Environ. Chem. Eng. 2021. V. 9.
bed plasma reactor // Plasma Chem. Plasma Process.
2012. V. 32. P. 153-163.
[73]
Banerjee A. M., Billinger J., Nordheden K. J., Peeters
F. J. J. Conversion of CO2 in a packed-bed dielectric
[62]
Mei D., Tu X. Atmospheric pressure non-thermal
barrier discharge reactor // J. Vac. Sci. Technol. A.
plasma activation of CO2 in a packed-bed dielectric
2018. V. 36. ID 04F403.
barrier discharge reactor // ChemPhysChem. 2017.
V. 18. P. 3253-3259.
[74]
Ray D., Chawdhury P., Bhargavi K. V. S. S.,
Thatikonda S., Lingaiah N., Subrahmanyam Ch. Ni
[63]
Li J., Zhu S., Lu K., Ma C., Yang D., Yu F. CO2
and Cu oxide supported γ-Al2O3 packed DBD plasma
conversion in a coaxial dielectric barrier discharge
reactor for CO2 activation // J. CO2 Util. 2021. V. 44.
plasma reactor in the presence of mixed ZrO2-CeO2
// J. Environ. Chem. Eng. 2021. V. 9. ID 104654.
[75]
Inagaki M., Tsumura T., Kinumoto T., Toyoda M.
Graphitic carbon nitrides (g-C3N4) with comparative
[64]
Ashford B., Wang Y., Poh C.-K., Chen L., Tu X. Plasma-
discussion to carbon materials // Carbon. 2019. V. 141.
catalytic conversion of CO2 to CO over binary metal
P. 580-607.
oxide catalysts at low temperatures // Appl. Catal. B.
2020. V. 276. ID 119110.
[76]
Lu N., Sun D., Zhang C., Jiang N., Shang K., Bao X.,
Li J., Wu Y. CO2 conversion in non-thermal plasma
[65]
Wang L., Du X., Yi Y., Wang H., Gul M., Zhu Y., Tu X.
and plasma/g-C3N4 catalyst hybrid processes // J.
Plasma-enhanced direct conversion of CO2 to CO over
Phys. D: Appl. Phys. 2018. V. 51. ID 094001.
oxygen-deficient Mo-doped CeO2 // Chem. Commun.
2020. V. 56. P. 14801-14804.
[77]
Ray D., Chawdhury P., Subrahmanyam Ch. A facile
method to decompose CO2 using a g-C3N4-assisted
[66]
Ray D., Subrahmanyam Ch. CO2 decomposition in
DBD plasma reactor // Environ. Res. 2020. V. 183.
a packed DBD plasma reactor: Influence of packing
N 8. ID 109286.
materials // RSC Adv. 2016. V. 6. P. 39492-37499.
[78]
Uytdenhouwen Y., Van Alphen S., Michielsen I.,
[67]
Li J., Zhai X., Ma C., Zhu S., Yu F., Dai B., Ge G.,
Meynen V., Cool P., Bogaerts A. A packed-bed DBD
Yang D. DBD plasma combined with different
micro plasma reactor for CO2 dissociation: Does size
foam metal electrodes for CO2 decomposition:
matter? // Chem. Eng. J. 2018. V. 348. P. 557-568.
Experimental results and DFT validations //
Nanomaterials. 2019. V. 9. ID 1595.
[79]
Lebedev Yu. A. Microwave discharges at low
pressures and peculiarities of the processes in strongly
[68]
Zhu S., Zhou A., Yu F., Dai B., Ma C. Enhanced CO2
nonuniform plasma // Plasma Sources Sci. Technol.
decomposition via metallic foamed electrode packed
2015. V. 24. N 5. ID 053001.
in self-cooling DBD plasma device // Plasma Sci.
Technol. 2019. V. 21. ID 085504.
[80]
Bogaerts A., Neyts E., Gijbels R., Van der Mullen J.
Gas discharge plasmas and their applications (review)
562
Голубев О. В., Максимов А. Л.
// Spectrochim. Acta. Part B. 2002. V. 57. P. 609-658.
of plasma-catalysis // J. Phys. D: Appl. Phys. 2017.
V. 50. ID 084001.
[81]
Shah Y. T., Verma J., Katti S. S. Plasma activated
catalysis for carbon dioxide dissociation: A review //
[86] Spencer L. F., Gallimore A. D. CO2 dissociation in an
J. Indian Chem. Soc. 2021. V. 98. ID 100152.
atmospheric pressure plasma/catalyst system: A study
of efficiency // Plasma Sources Sci. Technol. 2013.
[82]
Kozʹak T., Bogaerts A. Evaluation of the energy
V. 22. ID 015019.
efficiency of CO2 conversion in microwave discharges
using a reaction kinetics model // Plasma Sources Sci.
[87] Nunnally T., Gutsol K., Rabinovich A., Fridman A.,
Technol. 2015. V. 24. ID 015024.
Gutsol A., Kemoun A. Dissociation of CO2 in a low
current gliding arc plasmatron // J. Phys. D: Appl.
[83]
Ong M. Y., Nomanbhay S., Kusumo F., Show P. L.
Phys. 2011. V. 44. ID 274009.
Application of microwave plasma technology to
convert carbon dioxide (CO2) into high value products:
[88] Zhang H., Li L., Xu R., Huang J., Wang N., Li X.,
A review // J. Cleaner Prod. 2022. V. 336. ID 130447.
Tu X. Plasma-enhanced catalytic activation of CO2 in
a modified gliding arc reactor // Waste Dispos. Sustain.
[84]
Chen G., Georgieva V., Godfroid T., Snyders R.,
Energy. 2020. V. 2. P. 139-150.
Delplancke-Ogletree M.-P. Plasma assisted catalytic
decomposition of CO2 // Appl. Catal. B. 2016. V. 190.
[89] Chen G., Wang L., Godfroid T., Snyders R. Progress in
P. 115-124.
plasma-assisted catalysis for carbon dioxide reduction
in plasma chemistry and gas conversion. London:
[85]
Chen G., Britun N., Godfroid T., Georgieva V.,
IntechOpen, 2018. 17 p.
Snyders R., Delplancke-Ogletree M.-P. An overview
on CO2 conversion in a microwave discharge: The role