Журнал прикладной химии. 2022. Т. 95. Вып. 8
НЕОРГАНИЧЕСКИЙ СИНТЕЗ И ТЕХНОЛОГИЯ НЕОРГАНИЧЕСКИХ ПРОИЗВОДСТВ
УДК 546.98:546.924:66.061.352
ЭКСТРАКЦИОННОЕ ВЫДЕЛЕНИЕ И РАЗДЕЛЕНИЕ ПАЛЛАДИЯ(II)
И ПЛАТИНЫ(IV) ИЗ ХЛОРИДНЫХ РАСТВОРОВ
© О. Н. Катасонова1,2, О. Б. Моходоева1,2, К. Б. Осипов1, Т. А. Марютина1,2
1 ООО «Страта Солюшенс»,
141700, Московская обл., г. Долгопрудный, Научный переулок, д. 4
2 Институт геохимии и аналитической химии им. В. И. Вернадского РАН,
119991, г. Москва, ул. Косыгина, д. 19
E-mail: katasonova_ol@mail.ru
Поступила в Редакцию 5 июля 2022 г.
После доработки 18 октября 2022 г.
Принята к публикации 31 октября 2022 г.
Исследованы особенности выделения и разделения Pd(II) и Pt(IV) из модельных растворов с высоким
содержанием Cl- (~300 г·л-1). Изучено поведение Pd(II), Pt(IV) и матричных компонентов в зависи-
мости от величины кислотности модельного раствора, концентрации Cl-, природы экстрагентов и
реэкстрагентов. Описаны механизмы экстракционного извлечения платиновых металлов различными
экстрагентами (триоктиламин, метилтриалкиламмоний хлорид, три-н-октилфосфиноксид, дибу-
тилсульфоксид, трибутилфосфат) из хлоридных растворов. Для одновременного количественного
выделения Pd(II) и Pt(IV) из растворов с широким диапазоном кислотности и высоким содержанием
Cl- предложено использовать реагент класса четвертичных аммониевых оснований — метилтри-
алкиламмоний хлорид. Последующее селективное разделение платиновых металлов из органической
фазы осуществляется в процессе реэкстракции раствором 0.3 М NH4OH + 0.1 M NH4Cl. Подобран
состав промывных растворов, позволяющих отделять матричные компоненты, такие как Fe(III),
Te(IV), Cu(II), Pb(II) и частично Se(IV), от Pd(II) и Pt(IV), а также регенерировать экстрагент после
процессов экстракции и реэкстракции. Показано, что эффективность выделения Pd(II) и Pt(IV), коли-
чество ступеней реэкстракции, чистота и выход индивидуальных фракций зависят главным образом
от кислотности раствора и концентрации Cl-.
Ключевые слова: жидкостная экстракция; реэкстракция; палладий(II); платина(IV); высокосолевые
модельные растворы; метилтриалкиламмоний хлорид
DOI: 10.31857/S0044461822080023; EDN: NWQWUC
Повышенный спрос на платину и палладий из-
применяют метод гидрохлорирования, включающий
менил подход к сырьевой базе: помимо минераль-
растворение соединений платиновых металлов под
ного (медно-никелевых сульфидных руд, хромитов)
воздействием горячей соляной кислоты и газообраз-
перерабатывается вторичное сырье (отработанные
ного хлора, при этом Pd(II) и Pt(IV) переходят в рас-
катализаторы, химическая посуда, ювелирный, элек-
твор в виде стабильных хлорокомплексов [PdCl4]2- и
тронный и медицинский лом и т. д.) [1]. Для пере-
[PtCl6]2- [2]. При выборе схем по извлечению и раз-
работки металлсодержащего сырья наиболее часто
делению платиновых металлов из сложных растворов
971
972
Катасонова О. Н. и др.
должен учитываться ряд критериев, таких как кис-
концентрации HCl и Cl- сопоставимы с характеристи-
лотность, высокое содержание Cl-, наличие окисли-
ками технологических растворов.
телей и сопутствующих компонентов, концентрация
Цель работы — выбор экстракционных систем
металлов.
и условий одновременного экстракционного выде-
Для извлечения палладия и платины из их кон-
ления Pd(II) и Pt(IV) из модельных высокосолевых
центратов перспективно использование экстракци-
растворов с содержанием Cl- до 300 г·л-1 и концен-
онного метода, который имеет ряд достоинств, та-
трацией HCl в интервале 1-5 М с последующим их
ких как высокая селективность, обеспечивающая
разделением на стадии реэкстракции, а также оценка
полноту разделения и получение чистых фракций
возможности отделения целевых металлов от сопут-
целевых металлов, эффективность концентрирования
ствующих компонентов, традиционно присутствую-
из растворов с низкими содержаниями выделяемых
щих в технологических растворах.
компонентов, возможность регенерации используе-
мых экстрагентов [3]. Экстракционные методы вы-
Экспериментальная часть
деления и разделения платиновых металлов были
внедрены в промышленность в середине 1970-х го-
В качестве экстрагентов использовали следующие
дов и используются до настоящего времени [Vale
коммерчески доступные реагенты: триоктиламин
S. A. (Бразилия), Johnson Matthey (Великобритания)
(98%, Sigma-Aldrich, MERCK, кат. номер T81000);
и Anglo American Platinum (ЮАР)] [4]. Извлечение
метилтриалкиламмоний хлорид (Adogen 464, 98%,
палладия из технологических растворов на вышеука-
Sigma-Aldrich, MERCK, кат. номер 856576); три-н-ок-
занных предприятиях проводят экстрагентами класса
тилфосфиноксид (99%, Acros Organics, кат. номер
оксимов [β-гидроксиоксим (LIX 84А)], сульфидов
207600250); дибутилсульфоксид (>96%, TCI, кат. но-
(ди-н-октилсульфид) и нефтяных сульфоксидов (АО
мер D1173); трибутилфосфат (99%, Acros Organics,
«Приокский завод цветных металлов»*), платины —
кат. номер 169930100). Концентрация реагентов в
трибутилфосфатом или аминами [3, 5]. Сообщается
растворах составляла 0.5 М. В качестве растворите-
о медленной кинетике экстракции палладия окси-
ля использовали Solvesso-150 (100%, Exxon Mobil)
мами и сульфидами, нестабильности экстрагентов в
с температурой вспышки 65°С, характеризующий-
высококислых растворах, содержащих окислитель,
ся высокой растворяющей способностью наряду с
соэкстракции матричных компонентов в растворах,
низкой летучестью, что способствует его широкому
характеризующихся высокими концентрациями кис-
применению в технологических процессах. Для ре-
лоты и Cl- [3]. Недостаток применения первичных-
экстракции платиновых металлов применяли вод-
третичных аминов при переработке технологиче-
ные растворы 0.1 и 5 М HCl (х.ч.), 2 М HClO4 (х.ч.),
ских растворов платиновых металлов заключается
4 М HNO3 (ос.ч.), 0.1-0.5 М NH4OH (х.ч.), 0.1-0.5 М
в неполной реэкстракции платины из органической
NH4OH + 0.1 M NH4Cl (х.ч.), 2 М NaOH (х.ч.), 0.01 и
фазы вследствие образования кинетически инерт-
1 М CS(NH2)2 (х.ч.) в 0.5 М HCl и аммиачный буфер-
ных к реакциям замещения комплексов внедрения,
ный раствор (pH 10). Все перечисленные реагенты
реэкстракция которых практически невозможна [6].
производства ООО «Компонент-Реактив».
Разделение палладия и платины в промышленных
Модельные растворы, содержащие Pd(II), Pt(IV),
объемах основано на применении селективных экс-
Сu(II), Ni(II), Pb(II), Se(IV), Te(IV), Fe(III), готовили
трагентов для каждого металла, о коммерческом спо-
из их солей: PdCl2 (99%, Sigma-Aldrich, MERCK, кат.
собе совместного извлечения палладия и платины
номер 205885), PtCl4 (96%, Sigma-Aldrich, MERCK,
одним экстрагентом с дальнейшим их разделением
кат. номер 206113), CuCl2 (98%, Clearsynth, рег. но-
на стадии реэкстракции данных нет [1]. Несмотря
мер СS-CE-00941), NiCl2 (98%, Clearsynth, рег. номер
на большое количество опубликованных работ, по-
священных синтезу новых экстрагентов или приме-
нению хорошо изученных реагентов для экстракции
мер CP10026-07-0-BULK), SeCl4 (99%, Sigma-Aldrich,
платиновых металлов, весьма ограниченное число
MERCK, кат. номер 323527), PbCl2 (98%, Sigma-
статей посвящено извлечению и разделению платины
Aldrich, MERCK, кат. номер 268690) — в 1-5 М
и палладия из высокосолевых растворов, в которых
HCl c последующим добавлением NaCl (ос.ч., ООО
«Компонент-Реактив») до достижения общей концен-
трации Сl-, равной 300 г·л-1. Соотношение палладия
и платины в модельном растворе было рассчитано с
* ИТС 14-2016. Производство драгоценных металлов.
М.: Бюро НДТ, 2016. С. 35.
учетом их содержания в медно-никелевых рудах —
Экстракционное выделение и разделение палладия(II) и платины(IV) из хлоридных растворов
973
3:1.* Концентрации ионов платиновых металлов и
Обсуждение результатов
основных матричных компонентов в растворе со-
ставляли: Pd — 9 г·л-1; Pt — 3 г·л-1; Cu, Ni, Pb, Se,
Известно, что серосодержащие экстрагенты
Te, Fe — 200 мг·л-1для каждого элемента. Для пред-
(сульфоксиды) характеризуются большей химиче-
варительного выбора экстрагентов и реэкстрагентов
ской устойчивостью, чем сульфиды [1]. Кривая экс-
также использовали модельный раствор, содержащий
тракционного выделения палладия раствором 0.5 М
Pd(II) и Pt(IV) без матричных компонентов.
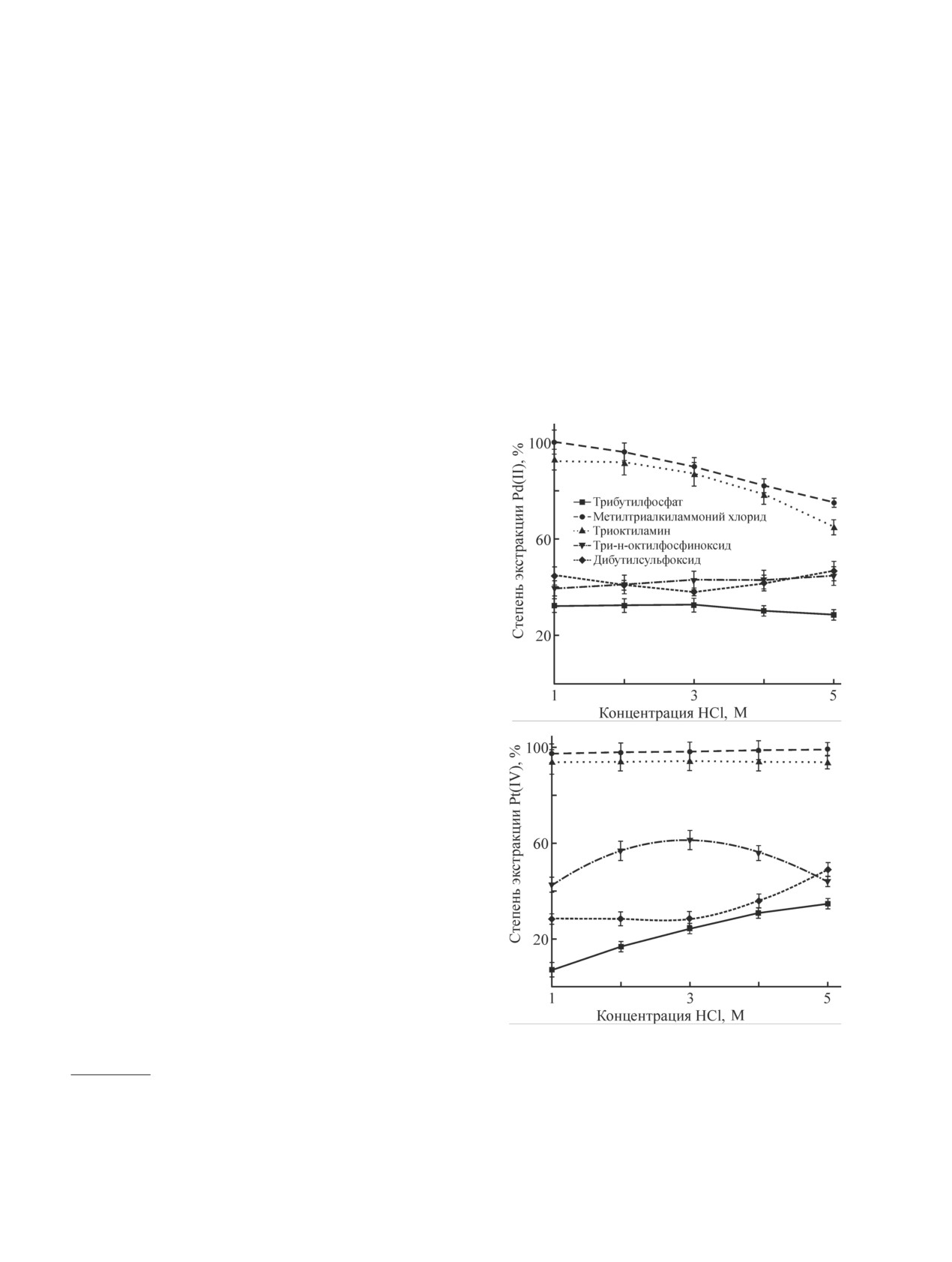
дибутилсульфоксида (рис. 1) имеет параболический
Для выполнения экспериментов использовали
характер, аналогичное распределение степени из-
лабораторный механический шейкер Stuart SSL2
влечения металла сульфоксидами описано в работах
(Stuart) и центрифугу CM-6МТ (ELMI). Экстракцию
[4, 7, 8] и основано на предположении о двух разных
и реэкстракцию проводили в статическом режиме
механизмах извлечения палладия в зависимости от
при комнатной температуре в полипропиленовых
кислотности раствора. Так, при экстракции палладия
пробирках объемом 50 мл при соотношении водной
сульфоксидами (L) в растворах с низкой концентра-
и органической фаз Vв:Vо = 1:1 в течение 15 мин при
механическом перемешивании. Общий объем экс-
тракционной системы не превышал 20 мл. Пробирки
в шейкере устанавливали в горизонтальном поло-
жении для увеличения площади поверхности кон-
такта модельного раствора с экстрагентом. Полное
разделение фаз двухфазной системы после экстрак-
ции осуществляли в течение 10 мин в центрифуге
при скорости вращения 1000 об·мин-1. Водную фазу
анализировали на содержание металлов. Для полно-
го выделения платиновых металлов из экстрагента
требуется несколько ступеней реэкстракции, каждая
последующая из которых проводилась с добавлением
свежей порции реагента к органической фазе экстра-
гента при соотношении Vо:Vв = 1:1. Коэффициенты
разделения (αPd/Pt) и распределения (Dp) платины и
палладия при их реэкстракции рассчитывались по
формулам
αPd/Pt = DрPd/DрPt,
(1)
Dp = св/со,
(2)
где св и со — концентрация металла в водной и орга-
нической фазе соответственно.
Анализ растворов осуществляли методом масс--
спектрометрии с индуктивно связанной плаз-
мой на масс-спектрометре Agilent 7900 (Agilent
Technologies), снабженном двухходовой стеклянной
распылительной камерой, стеклянным распылителем
MicroMist и кварцевой горелкой.
Рис. 1. Результаты экстракционного выделения Pd(II) и
Pt(IV) из высокохлоридных модельных растворов раз-
личными экстрагентами в зависимости от концентрации
* Платина и палладий России. Государственный доклад
соляной кислоты.
«О состоянии и использовании минерально-сырьевых
ресурсов Российской Федерации в 2016 и 2017 годах» //
Vо:Vв = 1:1, [Cl-общ] = 300 г·л-1, совместное присутствие
платиновых металлов в растворе: Pd = 9 г·л-1, Pt = 3 г·л-1,
концентрация для каждого экстрагента 0.5 М (n = 3,
(дата обращения 11.06.2022).
P = 0.95).
974
Катасонова О. Н. и др.
цией HCl происходит внутрисферное замещение двух
Pd(II) и Pt(IV) извлекаются фосфорорганически-
ацидолигандов по схеме
ми экстрагентами в виде комплексных кислот, при
этом их формы нахождения зависят от кислотности
2L + [PdCl4]2- = [PdCl2L2] + 2Cl-.
(3)
раствора [9]:
Однако содержание комплекса [PdCl2L2] в фазе
[MCln]2- + 2H+ H[MCln]- + H+ H2[MCln].
(6)
экстрагента снижается с ростом кислотности рас-
Для платины в виде комплекса H[MCln]- по срав-
твора, при этом главным фактором, ограничиваю-
нению с другими ее формами энергетически более
щим эффективность экстракции, является увеличение
выгодно образование ассоциата с гидратосольватом
концентрации Cl- в соответствии с уравнением реак-
протона по схеме
ции (3), а не концентрации H+ [4]. При достижении
кислотности раствора свыше 2-3 М механизм экс-
[H+·H2Om·Ln] + H[PtCl6]-
тракции меняется на гидратно-сольватный с предва-
(7)
{[H+·H2Om·Ln]·H[PtCl6]-}.
рительным образованием сложного катиона, вклю-
чающего ион гидроксония Н3О+ и сольватирующие
При изменении кислотности раствора равновесие
молекулы экстрагента с последующим образованием
сдвигается в сторону образования менее экстрагируе-
ионных ассоциатов по схеме (4), что способствует
мых форм [MCln]2- и H2[MCln]. Уменьшение степени
повторному увеличению степени извлечения Pd(II)
экстракции металлов с увеличением кислотности
из солянокислых растворов [7].
раствора также объясняют связыванием свободных
[L2·H3O+] + L + [PdCl4]2- =
молекул экстрагента HCl.
(4)
= {[L2·H3O+][PdCl3L]-} + Cl-.
Приоритет в извлечении Pd(II) и Pt(IV) может
быть связан с величинами заряда и эффективно-
го радиуса их комплексов. Плотность заряда иона
Следует отметить, что высокое содержание Cl- в
увеличивается при переходе от [PtCl6]2- к [PdCl4]2-.
модельном растворе подавляет экстракционную эф-
Комплекс с меньшей плотностью заряда притягива-
фективность сульфоксида в отношении Pd(II), смещая
ет меньше молекул воды и соответственно образу-
равновесие реакции (4) в левую сторону.
ет меньшую гидратную оболочку [10]. Поскольку
Извлечение Pt(IV) сульфоксидами растет при уве-
выделение металла с помощью трибутилфосфата и
личении кислотности модельного раствора (>3 М)
три-н-октилфосфиноксида может происходить путем
(рис. 1). В соответствии с исследованием [8] Pt(IV)
экстрагируется при высоких концентрациях HCl по
вытеснения сольватированных молекул и замены их
ионно-обменному механизму с образованием со-
на молекулы экстрагента, экстракционное выделение
Pd(II) будет затруднено по сравнению с Pt(IV). Другое
единений {[L3·H3O+][L2·H3O+] [PtCl6]2-}или их сме-
предположение строится на большей кинетической
си {[L3·H3O+]2[PtCl6]2-} или {[L2·H3O+]2[PtCl6]2-}:
лабильности комплекса Pd(II) относительно Pt(IV)
2[Ln·H3O+] + [PtCln]2- =
и существенной зависимости его экстракции от кон-
(5)
центрации Cl- в растворе, который подавляет извле-
= {[Ln·H3O+]2[PtCln]2-}.
чение Pd(II), протекающего по анионообменному
При экстракции Pd(II) равновесие, как правило,
механизму:
устанавливается в течение первых пяти минут, в то
2[H3O+LCl-] + [PdCl4]2-
время как для Pt(IV) требуется более длительное
(8)
{[H3O+L]2·[PdCl4]2-}+ 2Cl-.
время [8].
Для трибутилфосфата и три-н-октилфосфинокси-
Среди азотсодержащих экстрагентов для выделе-
да в кислых средах характерен сходный с сульфок-
ния платиновых металлов широко применяют четвер-
сидами гидратно-сольватный механизм экстракции
тичные аммониевые основания и третичные амины.
платиновых металлов [9]. Экстракционные свойства
Азотсодержащие основания обладают постоянным
фосфорорганических экстрагентов усиливаются при
положительным зарядом, легче образуя комплексы с
увеличении числа алкильных радикалов, связанных
металлами в более широком диапазоне кислотности,
с фосфором углеродными атомами, — при переходе
чем третичные амины [11]. Последние необходимо
от трибутилфосфата к три-н-октилфосфиноксиду
протонировать перед стадией экстракции:
степень извлечения платиновых металлов из соляно-
кислых растворов должна увеличиваться [10].
[R3N] + HCl
[R3NH+Cl-]о.
(9)
Экстракционное выделение и разделение палладия(II) и платины(IV) из хлоридных растворов
975
В сильнокислых средах возможно протекание сле-
извлечения Pt(IV), но при этом существенно снижал
дующей реакции [12]:
процент выделения Pd(II).
Несмотря на вышесказанное, метилтриалкилам-
[R3NHCl] + HCl
[R3NH2Cl2]o.
(10)
моний хлорид является более приемлемым реагентом
для одновременного извлечения Pd(II) и Pt(IV) в ши-
После протонирования третичных амминов хло-
роком диапазоне концентраций HCl при содержании
рокомплексы Pd(II) и Pt(IV) извлекаются по ионо-
Cl- ~ 300 г·л-1 в сравнении с другими классами пред-
обменному механизму:
ставленных экстрагентов. Триоктиламин уступает
метилтриалкиламмоний хлориду по эффективно-
[MClnn-] + n[R3NH+Cl-]
сти экстракции, реэкстракции (с учетом комплек-
(11)
{[R3NH]n[MCln]} + nCl-.
сов внедрения), а также по стоимости. Совместная
экстракция Pt(IV) и Pd(II) при использовании 0.5 М
[MClnn-] + n[R3NH2Cl2]
(12)
дибутилсульфоксида возможна только из сильно-
{[R3NH]n[MCln]} + HCl + nCl-.
кислых растворов, степень экстракции из 5 М HCl
не превышает 50% для каждого металла. Три-н-
Наряду с экстракцией ионных ассоциатов для тре-
октилфосфиноксид является более эффективным
тичных аминов возможно образование комплексов
фосфорорганическим экстрагентом по сравнению
внедрения, в которых металл прочно связан с моле-
с трибутилфосфатом при концентрации 0.5 М для
кулой азота экстрагента. Такие соединения инертны к
обоих реагентов. При использовании три-н-октил-
реакциям замещения, что в свою очередь значитель-
фосфиноксида экстракционный максимум для Pt(IV)
но усложняет реэкстракцию металлов платиновой
при концентрации HCl 3 М превышает 60%, при этом
группы.
степень экстракции Pd(II) в данных условиях состав-
ляет не более 43%. Дальнейшие исследования прово-
[MClnn-] + n[R3N]
[M(R3N)nCln],
(13)
дили с метилтриалкиламмоний хлоридом.
[MClnn-] + n[R3NHCl]
[M(R3N)nCln] + [HCl].
(14)
Варьирование концентрации Cl- и кислотности
модельного раствора также влияет на поведение ма-
Для четвертичных аммониевых оснований ком-
тричных компонентов Cu(II), Ni(II), Pb(II), Se(IV),
плексы внедрения не характерны.
Te(IV) и Fe(III). Повышение кислотности раствора
Pt(IV) количественно извлекается в 0.5 М три-
способствует их экстракционному извлечению [за
октиламин и метилтриалкиламмоний хлорид во
исключением Pb(II)] в органическую фазу вследствие
всем диапазоне кислотности модельного раствора
формирования в данных условиях хорошо экстраги-
(1-5 М HCl), несмотря на высокую концентрацию
руемых комплексов [TeCl6]2-, [СuCl3]-, [СuCl4]2- и
Cl-. Однако извлечение Pd(II) снижается с ростом
[FeCl4]- (рис. 2) [14]. Добавление к раствору Cl- в
концентрации HCl. С одной стороны, в сильнокис-
виде NaCl способствует формированию хлороком-
лых растворах (>3 M) возникает конкуренция между
плексов металлов и их переходу в фазу экстрагента.
молекулой кислоты и хлорокомплексом металла за
Se(IV) извлекается в метилтриалкиламмоний хлорид
молекулу экстрагента, что объясняет снижение экс-
при более высокой кислотности, когда возможно об-
тракции Pd(II) при увеличении концентрации HCl.
разование соединений HSeCl5 или HSeCl6 [15]. Ni(II)
С другой, значительное содержание Cl- может спо-
относится к металлам, которые могут экстрагиро-
собствовать образованию кинетически инертного
ваться четвертичными аммониевыми основаниями
комплекса Pd(IV):
только при относительно высоких концентрациях
экстрагента [16]. Pb(II) практически количественно
[PdCl4]2- + 2Сl-
[PdCl6]2-,
(15)
выделяется аминами и четвертичными аммониевыми
основаниями из слабокислых сред, при повышении
2[PdCl6]2- + 2[R3NH+Cl-]
концентрации HCl его степень извлечения значитель-
(16)
{[R3NH]2[PdCl5]2} + 4Cl-.
но снижается, поскольку хорошо экстрагируемый
комплекс [PbCl3]-, образуемый главным образом за
Данный вид соединения авторы исследования [13]
счет увеличения концентрации Cl-, трансформирует-
наблюдали в процессе экстракции палладия аминами
ся в другие формы [PbCl4]2-, [PbCl6]4-, отличающиеся
из модельного раствора (pH 1.5) при изменении кон-
низкой экстракционной активностью [17].
центрации NaCl от 0.05 до 6.14 М. Было показано,
Одна из задач исследования заключалась в пред-
что солевой фон практически не влиял на степень
варительном выделении из фазы экстрагента ма-
976
Катасонова О. Н. и др.
твор 0.1 М HCl может быть использован как про-
мывной после стадии экстракции металлов в 0.5 М
метилтриалкиламмоний хлорид для удаления ряда
матричных компонентов, при этом Pd(II), Pt(IV) и
Pb(II) остаются в фазе экстрагента. Для удаления
Pb(II) из фазы экстрагента после стадии реэкстрак-
ции целесообразно использовать более концентри-
рованный раствор HCl (≥5 М), который также может
использоваться для регенерации экстрагента (пере-
вода метилтриалкиламмоний хлорида в исходную
хлоридную форму).
В качестве реэкстрагентов Pd(II) и Pt(IV) были
изучены водные растворы различного состава [10-13,
18-23]. Согласно литературным данным, для селек-
Рис. 2. Степень извлечения матричных компонентов тивного извлечения Pd(II) и Pt(IV) из фазы экстраген-
(200 мг·л-1 для каждого металла при их совместном
та наиболее часто применяются минеральные кисло-
присутствии с платиновыми металлами) из модель-
ты, NaOH, NH4OH, тиомочевина. На первом этапе
ных растворов (0.1 и 1 М HCl и 1-5 M HCl + Cl-, где
исследования эксперименты по реэкстракции про-
[Cl-общ] = 300 г·л-1) на примере использования в каче-
стве экстрагента 0.5 М метилтриалкиламмоний хлорида
водили из органической фазы 0.5 М метилтриалкил-
в Solvesso-150 (Vо/Vв
= 1:1) (n = 3, P = 0.95).
аммоний хлорида в отсутствие матричных компо-
нентов.
Растворы HClO4 и HNO3 не позволяют селектив-
тричных компонентов в промывной раствор до ре-
но разделить палладий и платину — оба металла
экстракции платиновых металлов для минимизации
вымываются из органической фазы одновременно.
загрязнения их индивидуальных фракций. Согласно
В случае использования растворов NH4OH и NaOH
экспериментальным данным (рис. 2, табл. 1), рас-
высокой концентрации (>4 M) происходит образова-
Таблица 1
Степень реэкстракции элементов из фазы 0.5 М метилтриалкиламмоний хлорид в Solvesso-150 (Vо:Vв = 1:1)
(n = 3, P = 0.95)
Степень реэкстракции, %
Реагент
Коэффициент разделения αPd/Pt
Pd
Pt
0.1 М HCl
0.006 ± 0.002
0.003 ± 0.001
2
5 М HCl
5.6 ± 1.1
0.3 ± 0.09
0.14
2 M HClO4*
59.3 ± 3.2
68.2 ± 3.1
0.66
4 M HNO3
48.5 ± 2.6
56.8 ± 3.2
0.73
2 M NaOH**
26.9 ± 1.8
3.4 ± 0.8
11.56
1 M NH4OH**
82.4 ± 3.7
3.1 ± 0.9
146.25
0.5 М NH4OH**
74.7 ± 3.2
2.3 ± 0.7
125
0.3 М NH4OH**
59.1 ± 2.7
0.8 ± 0.2
180
0.1 М NH4OH**
26.4 ± 1.9
0.4 ± 0.2
90
0.5 М NH4OH + 0.1 M NH4Cl
72.8 ± 3.6
1.2 ± 0.4
223
0.3 М NH4OH + 0.1 M NH4Cl
56.2 ± 2.8
0.31 ± 0.09
426.6
0.1 М NH4OH + 0.1 M NH4Cl
24.2 ± 1.5
0.14 ± 0.06
227.8
0.01 М CS(NH2)2 + 0.5 М HCl
36.5 ± 2.3
2.1 ± 0.8
26.6
1 М CS(NH2)2 + 0.5 М HCl
56.3 ± 2.6
80.9 ± 3.5
0.3
* Образуется эмульсия в органической фазе, отстаиваемая в течение 1 сут.
** Образуется эмульсия в водной фазе, отстаиваемая в течение 1-3 сут.
Экстракционное выделение и разделение палладия(II) и платины(IV) из хлоридных растворов
977
ние трудно- или нерастворимых соединений плати-
новых металлов.
Несмотря на то что тиомочевина является одним
из наиболее часто используемых реэкстрагентов, из-
влечение чистых платиновых металлов из ее солей
представляет весьма энергозатратный процесс (тре-
буется термическое разложение свыше 1000°С). Было
отмечено, что при использовании растворов NH4OH в
качестве реэкстрагента металлов после их экстракции
раствором 0.5 М метилтриалкиламмоний хлорида в
Solvesso-150 в водной фазе образуется стойкая эмуль-
сия, которая не разрушается в процессе центрифуги-
рования и отстаивается в течение 1-3 сут. Добавление
0.1 M NH4Cl в растворы NH4OH позволяет получать
на выходе четкое разделение экстракционной си-
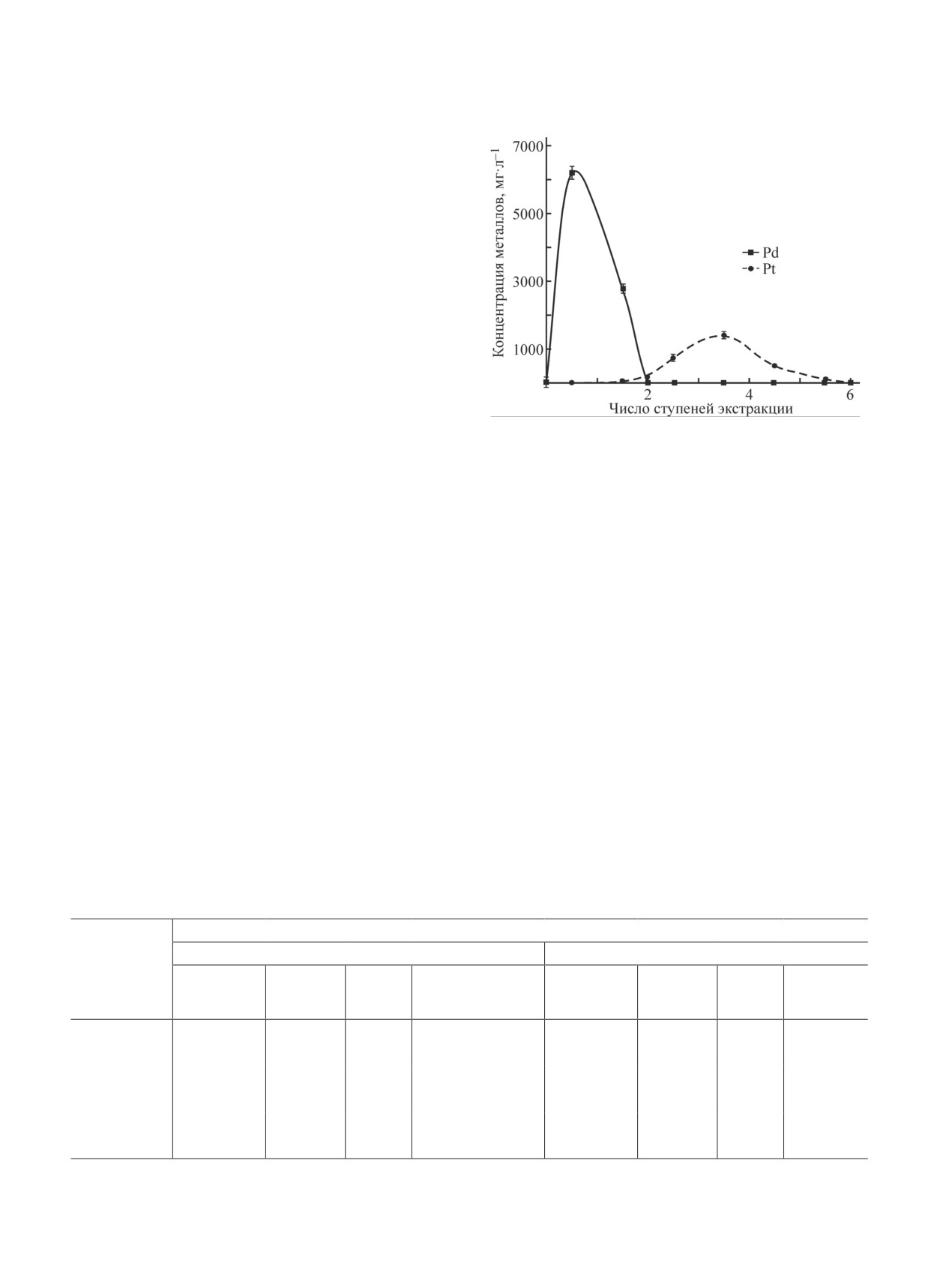
Рис. 3. Разделение Pd(II) и Pt(IV) раствором 0.3 М
стемы на две фазы, а также повышает коэффициент
NH4OH в присутствии 0.1 M NH4Cl на стадии реэкс-
разделения металлов в процессе реэкстракции.
тракции из 0.5 М метилтриалкиламмоний хлорида в
Применение раствора 0.3 М NH4OH в присутствии
Solvesso-150 (Vо:Vв = 1:1 для каждой ступени реэкстрак-
0.1 M NH4Cl для извлечения Pd(II) и Pt(IV) из 0.5 М
ции) (n = 3, P = 0.95).
метилтриалкиламмоний хлорида в Solvesso-150 обе-
спечивает максимальное значение αPd/Pt. В результате
алкиламмоний хлорида количественно выделяются в
процесса реэкстракции хлорокомплексы палладия и
отдельные фракции Pd(II) и Pt(IV) с чистотой 99.7 и
платины переходят в аквахлоро- и аквагидроксох-
100% соответственно.
лорокомплексы, хлорокомплексы платины более
Как было показано (рис. 1), степень экстракции
инертны в процессах замещения хлора на молекулу
Pd(II) в 0.5 М метилтриалкиламмоний хлорид из
воды или OH- по сравнению с палладием, поэтому на
модельного раствора снижается с ростом его кис-
первых стадиях реэкстракции из органической фазы
лотности, поэтому для количественного извлечения
извлекается Pd(II), на последующих — Pt(IV) (рис. 3).
металла в кислых средах необходимо увеличить от-
Для второй ступени реэкстракции характерна неболь-
ношение объема экстрагента к водной фазе как (1.2-
шая зона частичного перекрытия кривых палладия и
1.6):1 для 3 и 5 М HCl соответственно. Раствор 0.1 М
платины, что приводит к незначительному извлече-
HCl, который применяется в качестве промывного
нию Pt(IV) (не более 1%) во фракцию Pd(II). В ходе
раствора, позволил выделить из фазы экстрагента
реэкстракции из органической фазы 0.5 М метилтри-
полностью Fe(III), Cu(II), Te(IV) и частично Se(IV).
Таблица 2
Характеристика фракций Pd(II) и Pt(IV), полученных при реэкстракции раствором 0.3 М NH4OH в присутствии
0.1 M NH4Cl, после экстракции из хлоридных растворов 1, 3, 5 М HCl + Cl- ([Cl-общ] = 300 г·л-1)
0.5 М метилтриалкиламмоний хлоридом в Solvesso-150 (n = 3, P = 0.95)
Реэкстракция
реэкстракт Pd
реэкстракт Pt
Модельный
раствор
число
степень
степень
число
степень
степень
ступеней
извлечения
чистоты
примеси, %
ступеней
извлечения
чистоты
примеси, %
реэкстракции
Pd, %
Pd, %
реэкстракции
Pt, %
Pt, %
1 М HCl + Сl-
2
100 ± 3.2
99.66
0.325 (Е* = 1%) Pt,
4
98.9 ± 4.1
99.6
0.4 (Se, Pb)
0.015 (Se, Pb).
3 M HCl + Сl-
3
100 ± 4.3
99.4
0.4 (Е = 1.3%) Pt,
5
98.65 ± 4.7
98.4
1.6 (Se, Pb)
0.18 (Se, Pb).
5 M HCl + Сl-
3
100 ± 4.8
98.5
1.4 (Е = 4.2%) Pt,
7
95.8 ± 5.2
97.2
2.8 (Se, Pb)
0.22 (Se, Pb)
* E — степень извлечения платины от ее общего содержания в модельном растворе во фракцию палладия.
978
Катасонова О. Н. и др.
В ходе реэкстракции раствором 0.3 М NH4OH + 0.1 M
Полученные результаты исследования могут быть по-
NH4Cl последовательно извлекаются из органической
ложены в основу разработки нового экстракционного
фазы фракции Pd(II) и Pt(IV). В обе фракции плати-
способа переработки технологических растворов
новых металлов выделяются от 0.015 до 2.8% Se(IV)
концентратов благородных металлов, содержащих
и Pb(II), при этом значительная их часть реэкстра-
высокую концентрацию Сl-.
гируется в фазу Pt(IV). Второй промывной раствор
5 М HCl при соотношении Vо:Vв = 1:2 удаляет коли-
Благодарности
чественно Pb(II) из фазы экстрагента. В результате
всех стадий экстракции, реэкстракции и промывок в
Работа выполнена при поддержке инновационного
экстрагенте содержится 3-18% Se(IV) от его концен-
центра «Сколково» (проект «136C»).
трации в исходном модельном растворе 200 мг·л-1,
который достаточно сложно извлекается из аминов
Конфликт интересов
и четвертичных аммониевых оснований и требует
проведения дополнительных исследований.
Авторы заявляют об отсутствии конфликта инте-
От концентрации HCl зависит не только степень
ресов, требующего раскрытия в данной статье.
извлечения целевых компонентов и сопутствующих
элементов в органическую фазу, но также и полнота
реэкстракции Pd(II) и Pt(IV). С увеличением кис-
Информация о вкладе авторов
лотности модельного раствора и содержания в нем
О. Н. Катасонова и О. Б. Моходоева — постановка
хлоридсодержащих солей требуется больший объем
задач и плана исследования, анализ литературных
как экстрагента, так и реэкстрагента для полного
данных, разработка экстракционной схемы выделе-
их извлечения, увеличивается соэкстракция Cu(II),
ния и разделения платины и палладия из хлоридных
Fe(III), Te(IV) в органическую фазу, а также Se(IV),
растворов, концепция статьи; К. Б. Осипов — опре-
Pb(II) и взаимных примесей в фазы платиновых ме-
деление концентрации металлов в растворах методом
таллов при реэкстракции (табл. 2). Несмотря на это,
масс-спектрометрии с индуктивно связанной плаз-
предложенный способ экстракционного выделения и
мой; Т. А. Марютина — формирование направления
разделения платиновых металлов позволяет количе-
исследования и постановка задач, участие в обсужде-
ственно извлекать отдельные фракции Pd(II) и Pt(IV)
нии результатов и написании текста статьи.
с чистотой свыше 98.5 и 97.2% соответственно из
высокосолевых модельных растворов, содержащих
матричные компоненты.
Информация об авторах
Катасонова Олеся Николаевна, к.х.н.
Выводы
Моходоева Ольга Борисовна, к.х.н.
Соль четвертичного аммониевого основания —
Осипов Константин Борисович, к.х.н.
метилтриалкиламмоний хлорид позволяет коли-
чественно извлекать Pd(II) и Pt(IV) из модельных
Марютина Татьяна Анатольевна, д.х.н.
технологических растворов, характеризующихся
высоким содержанием Сl- (до 300 г·л-1), концен-
трацией HCl в диапазоне 1-5 М и наличием матрич-
ных компонентов, таких как Cu(II), Fe(III), Ni(II),
Список литературы
Te(IV), Se(IV) и Pb(II). Реэкстрагент 0.3 М NH4OH
[1] Wang J., Xu W., Liu H., Yu F., Wang H. Extractant
в присутствии модификатора 0.1 М NH4Cl, добав-
structures and their performance for palladium
ляемого во избежание образования третьей фазы и
extraction and separation from chloride media:
стойкой эмульсии, обеспечивает последовательное
A Review // Miner. Eng. 2021. V. 163. ID 106798.
количественное извлечение Pd(II) и Pt(IV) из фазы
метилтриалкиламмоний хлорида в отдельные фрак-
[2] Mpinga C. N., Eksteen J. J., Aldrich C., Dyer L. Direct
ции с чистотой не ниже 99.6% для обоих металлов.
leach approaches to platinum group metal (PGM) ores
Частично соизвлекаемые ионы Cu(II), Fe(III), Te(IV)
and concentrates: A Review // Miner. Eng. 2015. V. 78.
и Pb(II) могут быть удалены из фазы экстрагента на
P. 93-113.
стадии промывки после экстракции и реэкстракции.
Экстракционное выделение и разделение палладия(II) и платины(IV) из хлоридных растворов
979
[3]
Cole P. M., Sole K. C., Feather A. M. Solvent extraction
by solvent extraction using Alamine 300 //
developments in Southern Africa // Tsinghua Sci.
Hydrometallurgy. 2010. V. 104. P. 1-7.
Technol. 2006. V. 11. N 2. P. 153-159.
[14]
Aprahamian V. H., Demopoulos G. P. The Solution
[4]
Extractive metallurgy of nickel, cobalt and platinum
chemistry and solvent extraction behaviour of Cu,
group metals / Eds F. K. Crundwell, M. S. Moats,
Fe, Ni, Zn, Pb, Sn, Ag, As, Sb, Bi, Se and Te in acid
V. Ramachandran, T. G. Robinson, W. G. Davenport.
chloride solutions reviewed from the standpoint of
Elsevier, Oxford, 2011. P. 489-534.
PGM refining // Miner. Process. Extr. Metall. Rev.
1995. V. 14. N 3-4. P. 143-167.
[5]
Аналитическая химия металлов платиновой груп-
пы / Под ред. Ю. А. Золотова, Г. М. Варшал, В. М.
[15]
Назаренко И. И., Ермаков А. Н. Аналитическая хи-
Иванова. М.: КомКнига, 2005. С.162-165.
мия селена и теллура Сер.: Аналитическая химия
[6]
Huang Y., Tong Y., Wang C., Tang K., Yang Y.
элементов. М.: Наука, 1971. С. 149-159.
Solvent extraction of palladium (II) with newly
[16]
Шмидт В. С. Экстракция аминами. М.: Атомиздат,
synthesized asymmetric branched alkyl sulfoxides
1970. С. 172-173.
from hydrochloric acid // RSC Adv. 2015. V. 5. N 81.
[17]
Rodrıguez de San Miguel E., Aguilar J. C.,
P. 66376-66383.
Rodrıguez M. T. J., de Gyves J. Solvent extraction of
Ga(III), Cd(II), Fe(III), Zn(II), Cu(II), and Pb(II) with
[7]
Preston J. S., du Preez A. C. Solvent extraction of
ADOGEN 364 dissolved in kerosene from 1-4 mol
platinum group metals from hydrochloric acid solution
dm-3 HCl media // Hydrometallurgy. 2000. V. 57. N 2.
by dialkyl sulphoxides // Solvent Extr. Ion Exch. 2002.
P. 151-165.
V. 20. N 3. P. 359-374.
[18]
Rajua B., Kumarb J. R., Leeb J. Y., Kwoncc H. S.,
[8]
Pan L., Zhang Z. Solvent extraction and separation of
Kantama M. L., Reddya B. R. Separation of platinum
palladium(II) and platinum(IV) from hydrochloric acid
and rhodium from chloride solutions containing
medium with dibutyl sulfoxide // Miner. Eng. 2009.
aluminum, magnesium and iron using solvent
V. 22. N 15. P. 1271-1276.
extraction and precipitation methods // J. Hazard.
Mater. 2012. V. 227-228. P. 142-147.
[9]
Москвин Л. Н., Симанова С. А., Якимова Н. М.
Новые возможности экстракции платиновых ме-
[19]
Peng C. Yu., Teh-Hua Tsai T. H
. Solvent extraction
таллов кислородсодержащими экстрагентами
of palladium(II) from acidic chloride solutions using
в форме хлорокомплексов // ЖОХ. 2012. Т. 82.
tri-octyl/decyl ammonium chloride (Aliquat 336) //
№ 1. С. 11-19 [Moskvin L. N., Simanova S. A.,
Desalination Water Treat. 2013. V. 52. P. 1101-1108.
Yakimova N. M. New capabilities in extraction of
platinum metal chloride complexes with oxygen-
[20]
Nguyen T. N., Sonu C. H., Lee M. S. Separation of
containing extractants // Russ. J. Gen. Chem. 2012.
platinum (IV) and palladium (II) from concentrated
V. 82. N 1. P. 9-16.
hydrochloric acid solution by mixtures of amines with
neutral extractants // J. Ind. Eng. Chem. 2015. V. 32.
[10]
Sun P. P., Lee J. Y., Lee M. S. Separation of Pt(IV) and
Rh(III) from chloride solution by solvent extraction
[21]
Pasdar H., Saghavaz B. H., Fallah Z., Shahi M.,
with amine and neutral extractants // Mater. Trans.
Davallo M. Liquid-liquid extraction of palladium (II)
2011. V. 52. N 11. P. 2071-2076.
in acids chloride solution using tri-n-octylamine //
ASRJETS. 2017. V. 38. N 1. P. 258-264.
[11]
Lee J.-Y., J. Kumar R., Kim J.-S., Kim D.-J., Yoon H.-S.
[22]
Jaree A., Khunphakdee N. Separation of concentrated
Extraction and separation of Pt(IV)/Rh(III) from acidic
platinum(IV) and rhodium(III) in acidic chloride
chloride solutions using Aliquat 336 // J. Ind. Eng.
solution via liquid-liquid extraction using tri-
Chem. 2009. V. 15. P. 359-364.
octylamine // J. Ind. Eng. Chem. 2011. V. 17. P. 243-
[12]
Jha M. K., Gupta D., Lee J., Kumar V., Jeong J.
[23]
Lee J.-Y., Kumar J. R., Kim J.-S., Park H.-K.,
Solvent extraction of platinum using amine based
Yoon H.-S. Liquid-liquid extraction/separation of
extractants in different solutions: A Review //
platinum(IV) and rhodium(III) from acidic chloride
Hydrometallurgy. 2014. V. 142. P. 60-69.
solutions using tri-iso-octylamine // J. Hazard. Mater.
2009. V. 168. P. 424-429.
[13]
Swain B., Jeong J., Kim S. K., Lee J. C. Separation
of platinum and palladium from chloride solution