Получение, структура и свойства микротрубок хитозана
69
Журнал прикладной химии. 2023. Т. 96. Вып. 1
УДК 547.458:[544.412.3+66.021.3+620.17]
ПОЛУЧЕНИЕ, СТРУКТУРА И СВОЙСТВА МИКРОТРУБОК ХИТОЗАНА
© А. Б. Шиповская, Н. О. Гегель*, Т. С. Бабичева, А. А. Голядкина
Саратовский национальный исследовательский государственный университет
им. Н. Г. Чернышевского,
410012, г. Саратов, ул. Астраханская, д. 83
* E-mail: GegelNO@yandex.ru
Поступила в Редакцию 21 ноября 2022 г.
После доработки 10 марта 2023 г.
Принята к публикации 5 июля 2023 г.
Разработаны способы формирования полых цилиндрических структур с толщиной стенки в микроме-
тровом диапазоне (микротрубок) из растворов хитозана в лимонной, молочной и гликолевой кислотах.
В основе способов лежит межфазная реакция нейтрализации, индуцированная транспортом ионов
(далее, ионно-индуцированная реакция), протекающая на границе раздела жидкость-жидкость
или твердое тело-жидкость: реакция полимераналогичного превращения солевой формы полимера
в основную в среде NaOH или триэтаноламина либо реакция формирования водонерастворимого
полиэлектролитного комплекса с додецилбензосульфонатом натрия. Проведен сравнительный
анализ зависимости морфологических, структурных, упруго-пластических, физико-механических и
биологических свойств структур от условий проведения химической реакции, природы органической
кислоты и нейтрализующего реагента. Установлено, что микротрубки, полученные из раствора
хитозана в гликолевой кислоте способом ионно-индуцированной нейтрализации на границе раздела
твердое тело-жидкость в среде NaOH и триэтаноламина, обладают оптимальными показателями
прочности и эластичности, сопоставимыми с аналогичными характеристиками фрагмента сонной
артерии человека и ксеноперикардиальной пластины. Гемо-, биосовместимость и контролируемая
биодеградация данных образцов показывают перспективность применения полученных материалов
в качестве аналогов биодеградируемых имплантов кровеносных сосудов.
Ключевые слова: хитозан; микротрубки; межфазная реакция нейтрализации; биодеградируемые
протезы кровеносных сосудов
DOI: 10.31857/S0044461823010097; EDN: HUYTKR
К настоящему времени разработан и детально
вращающемся стержневом электроде методом элек-
исследован широкий спектр хитозансодержащих
троформования растворов хитозана в муравьиной,
материалов разного функционального назначения,
концентрированной уксусной или трифторуксусной
прежде всего для фармацевтических и медико-биоло-
кислотах [6, 7].
гических приложений [1-3]. Одно из новых направ-
Более экологичный способ формирования микро-
лений — получение из хитозана материалов в форме
трубчатых конструкций предусматривает выщела-
полых цилиндрических структур с толщиной стенки
чивание нанесенной на вращающуюся пластиковую
в микрометровом диапазоне (микротрубок). Такие
трубку глицериновой эмульсии хитозан-желатино-
материалы перспективны для использования в каче-
вых микросфер [8] либо адсорбированного на капил-
стве имплантатов (протезов) кровеносных сосудов,
лярном шаблоне уксуснокислого раствора хитозана
мочеточников и нервных волокон [4, 5]. Основной
(в том числе армированного сеткой хитозановых во-
подход к их получению заключается в формировании
локон) с последующим сшиванием генипином [9, 10].
полой полимерной структуры на металлическом или
Еще один вариант создания трубчатых каркасов —
пластиковом темплате с круглым поперечным сече-
экструзия многокомпонентных гелей на основе кар-
нием. Например, известно получение микротрубок на
боксиметилхитозана и альгиновой кислоты в коагу-
70
Шиповская А. Б. и др.
ляционную ванну с солями кальция с последующим
прочность материала. Авторы [17] обнаружили, что
образованием мостиковых сшивок Ca2+ с полиани-
пленки, сформированные из растворов хитозана в
онами для придания материалу формоустойчиво-
лимонной и молочной кислотах, менее прочные, чем
сти [11].
из раствора в уксусной кислоте. При этом образцы,
Интересен также подход к получению твердо-
полученные из растворов лактата хитозана, проявля-
фазной трубчатой формы (прекурсора углеродных
ют высокую эластичность.
микротрубок) путем самопроизвольного скручивания
Для перевода водорастворимой солевой формы
тонкой пленки ацетата хитозана в водной среде при
хитозана в водонерастворимую основную форму про-
150°С [12].
водят нейтрализацию протонированных аминогрупп,
Описанные в данных работах способы и подходы
выдерживая образец в среде NaOH (другие щелочные
зачастую многостадийны, энергозатратны, а в ряде
реагенты практически не используются). Изменяя
случаев предполагают использование дорогостоящего
условия реакции нейтрализации, индуцированной
оборудования и агрессивных растворяющих сред.
ионами ОН-, можно получать хитозансодержащие
Сказанное предопределяет разработку более эколо-
материалы разной морфоструктуры, в том числе пе-
гически безопасной и экономически целесообразной
риодической (типа осадков Лизеганга). В частности,
технологии формирования микротрубок хитозана,
гидрогели со слоисто-ориентированным упорядо-
предусматривающей применение сравнительно про-
чением получают выдерживанием раствора ацетата
стых методических подходов и биологически актив-
хитозана, помещенного в пресс-форму, в среде NaOH
ных реагентов.
[18]. Ориентация слоев наблюдается вдоль направ-
Традиционно для растворения хитозана (форми-
ления диффузии ионов ОН-, а их количественные
рования его солевой формы) используют водные рас-
характеристики согласуются с феноменом Лизеганга.
творы уксусной или соляной кислот. Поскольку ос-
В работе [19] формируют гидрогели хитозана анало-
новное прикладное применение хитозансодержащих
гичной структуры многократным чередованием де-
материалов — фармацевтика и медицина, а природа
протонирования ацетата хитозана в щелочной среде
кислотного остатка оказывает существенное влияние
с промывкой в воде вплоть до полной нейтрализации
на структуру и свойства конечного продукта, инте-
протонированных аминогрупп, что приводит к обра-
ресным как с научной, так и с практической точки
зованию периодических слоев.
зрения является использование для растворения хи-
Нейтрализованную водонерастворимую форму
тозана биологически активных органических кислот:
хитозана получают и посредством формирования
лимонной, молочной, гликолевой, аскорбиновой, ас-
поликомплексов с противоположно заряженными
парагиновой и др. [13-16]. Это позволяет не только
полиэлектролитами или поверхностно-активными
варьировать физико-химические свойства получа-
веществами [2, 20, 21]. Не исключено, что реакции
емых материалов, но и объединить биохимические
полимер-аналогичного превращения соль→осно-
активности полимера и кислоты.
вание хитозана и комплексообразования с поверх-
Процесс солеобразования и структурно-морфоло-
ностно-активными веществами могут быть весьма
гические характеристики материала определяются не
результативными и при получении полых цилиндри-
только кислотными свойствами, значением рН и ион-
ческих структур. Кроме того, представляется целесо-
ной силы растворяющей среды, но и молекулярной
образным варьирование природы кислоты-раствори-
структурой и объемом кислотного остатка, опреде-
теля хитозана и нейтрализующего реагента в данном
ляющими силу ионного взаимодействия полимер-
процессе.
кислота и количество формирующихся между сво-
Цель работы — получение полых цилиндриче-
бодными функциональными группами Н-связей [16,
ских структур из растворов хитозана в органических
17]. Так, хитозан в пленках, полученных из растворов
кислотах с использованием межфазной реакции ион-
уксусной и соляной кислот, характеризуется аморф-
но-индуцированной нейтрализации солевой формы
но-кристаллическим упорядочением, а полученных
полимера.
из растворов в лимонной и молочной кислотах —
практически полностью аморфным надмолекуляр-
Экспериментальная часть
ным упорядочением [16]. Наиболее низкое значение
температуры стеклования имеет цитрат хитозана, что
В работе использовали хитозан со средневяз-
свидетельствует о более сильном взаимодействии ци-
костной молекулярной массой 700 кДа и степенью
трат-ионов с NH3+-группами макроцепей. С увеличе-
деацетилирования 80 мол% (ЗАО «Биопрогресс»);
нием объема противоиона уменьшается и разрывная
биологически активные карбоновые гидроксикисло-
Получение, структура и свойства микротрубок хитозана
71
ты, показавшие большой потенциал при получении
Полученный образец снимали со стержня, про-
хитозансодержащих материалов биомедицинского
мывали дистиллированной водой до нейтрального
назначения [15-17]: лимонную (≥99.8%, АО «База
значения рН и хранили в дистиллированной воде, по
№ 1 Химреактивов»); молочную (80%, АО «Вектон»)
постоянству рН и показателя преломления которой
и гликолевую (70%, Sigma-Aldrich, кат. № 8.14662);
контролировали полноту протекания реакции ней-
нейтрализующие реагенты: NaOH (АО «База № 1
трализации.
Химреактивов»), триэтаноламин (АО «База № 1
Некоторые образцы микротрубок хранили в эти-
Химреактивов») и додецилбензосульфонат натрия
ловом спирте в течение 3 лет.
(≥99%, Sigma-Aldrich, кат. № 436143); соли NaCl,
В отдельных экспериментах применяли пленки
Na2HPO4, KH2PO4 (АО «База № 1 Химреактивов»);
хитозана основной формы, полученные как класси-
лизоцим (ООО «Медиген»); нингидрин (ООО
ческим методом полива водно-кислотного раствора
«Диаэм»); кармуазин (краситель пищевой Е122,
полимера с последующим высушиванием на возду-
ООО «Ялога-НТ»); дистиллированную воду, полу-
хе и обработкой в среде NaOH, так и способом 2.
ченную на аквадистилляторе ДЭ-10М (ООО «Завод
Использовали также ксеноперикардиальную пласти-
«Электромедоборудование»); этиловый спирт (96.3%,
ну (марка «Кардиоплант», ООО «Кардиоплант») и
«Экстра», ООО «Абсолют»); хлоргексидин биглю-
биоматериал (фрагмент сонной артерии человека),
конат (0.05%, ООО «Петрофарм»). Все химические
предоставленный Саратовским городским бюро су-
вещества квалификации х.ч.
дебно-медицинской экспертизы.
Растворы хитозана концентрации 2.0-4.0 мас%
Внешний вид микротрубок оценивали визуаль-
готовили растворением воздушно-сухой навески
но по следующим параметрам: цвет, прозрачность,
порошка полимера в водном растворе 5%-ной ли-
однородность внутренней и внешней поверхности.
монной, 1.5%-ной молочной и 1.5%-ной гликолевой
Фотографии получены с использованием цифрового
кислот при перемешивании на магнитной мешалке
фотоаппарата Sony SX 37, для контрастности микро-
в течение 5-7 ч при комнатной температуре. Выбор
трубки окрашивали кармуазином. Толщину стенок
концентрации кислот обусловлен их растворяющей
измеряли микрометром CT200-521 (ЗАО «ЧИП и
способностью в отношении хитозана и соблюдением
ДИП»). Измерения проводили не менее 10 раз на
максимального мольного соотношения кислота:по-
различных участках образца и рассчитывали среднее
лимер, не превышающего 2.0-2.2 моль:осново-моль,
значение.
с целью минимизирования присутствия в системе
Деформационно-прочностные характеристики
несвязанной кислоты.
определяли на одноколонной испытательной маши-
Микротрубки хитозана получали межфазной реак-
не Instron 5944 (Instron) с нагрузочной ячейкой 500 Н
цией ионно-индуцированной нейтрализации (реакция
в условиях одноосного растяжения со скоростью
полимераналогичного превращения солевой формы
10 мм·мин-1. Испытания проводили в воздушно-су-
полимера в основную в среде 5%-ного NaOH или
хой атмосфере при 22 ± 2°С и в жидкой среде (0.15 М
50%-ного триэтаноламина) либо реакцией форми-
NaCl — модель физиологического раствора) ванны
рования водонерастворимого полиэлектролитного
BioBath (Instron) при 37°С. При испытании в воз-
комплекса с 0.1 М додецилбензосульфонатом Na,
душной среде образцы микротрубок разрезали вдоль,
протекающей на границе раздела жидкость-жид-
распрямляли и закрепляли в стандартных зажимах
кость (способ 1) или твердое тело-жидкость (спо-
разрывной машины в виде пластин; в жидкой сре-
соб 2) [22].
де — образец фиксировали в специальных зажимах
Способ 1. Раствор полимера адсорбировали на
с сохранением исходной геометрии полого цилин-
стеклянном стержне диаметром d = 5-10 мм либо
дра. По полученным данным строили зависимость
металлической проволоке с d = 0.3 мм, погружали
нагрузка-удлинение σ = f(ε). Разрывное напряжение
вертикально в раствор нейтрализующего реагента и
(σр, МПа), модуль Юнга (E, МПа) и относительное
выдерживали 12 ч до полной нейтрализации солевой
удлинение при разрыве (εр, %) рассчитывали с уче-
формы хитозана.
том площади поперечного сечения и первоначальной
Способ 2. Стержень с адсорбированным раствором
длины исходного образца.
солевого хитозана выдерживали 1 мин в нейтрали-
Рентгеновские дифрактограммы получали на диф-
зующей среде, сушили 1 ч в термошкафу ШСУ-М
рактометре ДРОН-3 (АО «НПП Буревестник») с из-
(ОАО «Электроприбор») при 50°С до формирования
лучением CuKα при U = 22 кВ и Iа = 20 мА. Степень
воздушно-сухого материала и вновь выдерживали
кристалличности (χ, %) рассчитывали как отношение
3-12 ч в среде нейтрализующего реагента.
интегральной интенсивности суммарного рассеяния
72
Шиповская А. Б. и др.
кристаллитов к полному рассеянию от аморфных и
37°С, 90%-ной влажности и 5% СО2 в течение 7 сут.
кристаллических областей графическим интегриро-
Проводили по три опытных посева. Наблюдение за
ванием (программа IpSquare v.5.0).
адгезией и пролиферацией клеток осуществляли на
Морфологию поверхности и внутренней структу-
инвертируемом микроскопе Биолам П (АО «ЛОМО»)
ры стенки микротрубок оценивали методом скани-
с цифровой ССD-камерой DMS 300 Scopotek (объек-
рующей электронной микроскопии на микроскопе
тив 10Х, разрешение 3 Mрх). В принятых условиях
MIRA\\LMU (Tescan) при напряжении 15 кВ и прово-
проведения опытов воспроизводимость культивиро-
дящем токе 400 пА. Пробоподготовку проводили сле-
вания клеток составила 98 ± 2%.
дующим образом: микротрубку надевали на стержень
Биодеградацию оценивали in vitro в процессе
соответствующего диаметра, отрезали кольцо высо-
выдерживания микротрубок в 2 мг·мл-1 раство-
той 3 мм, выдерживали при -90°С в течение 12 ч,
ре фермента лизоцим или фосфатном буферном
помещали в 96.3%-ный этиловый спирт на 30 мин и
растворе (контроль, 66.7 ммоль·л-1 Na2HPO4 +
сушили при комнатной атмосфере 24 ч. Перед про-
+ 66.7 ммоль·л-1 KH2PO4, рН 7.4) при 37°C в тече-
ведением исследований на образцы напыляли слой
ние 180 сут. Оптимальную концентрацию фермента
золота толщиной 5 нм на установке K450X Carbon
и время его биокаталитической активности опреде-
Coater (Quorum Technologies Ltd).
ляли в предварительных опытах методом диффузии
Гемосовместимость изучали in vitro на модели
в мясопептонный агар (ООО «Агат-Мед») в отно-
эритроцитов человека в условиях детекции окислен-
шении штамма Esherichia coli 113-13 (Саратовский
ных форм гемоглобина [13]. Образцы микротрубок
национальный исследовательский государственный
стерилизовали в 70%-ном растворе этилового спирта
университет им. Н. Г. Чернышевского) по стандарт-
в течение 20 мин, помещали в стерильные чашки
ной методике. Пробы отбирали через каждые 30 сут
Петри (FalconBD), вносили суспензию эритроцитов
кондиционирования, выдерживали в хлоргексидине
здоровых доноров и инкубировали на термошейкере
биглюконате 10 мин, промывали дистиллированной
BioSan PST 60HL (ООО «BioSan») в режиме встряхи-
водой и сушили до воздушно-сухого состояния при
вания при 350 об·мин-1 и 37°С в течение 1 ч. Далее
комнатной температуре 24 ч. Убыль массы контро-
пробы центрифугировали на центрифуге-встряхи-
лировали гравиметрически на аналитических весах
вателе СМ-70М-07 SIA (ELMI) при скорости вра-
Ohaus Discovery (OHAUS Corporation, точность взве-
щения 1000 об·мин-1 в течение 10 мин и измеряли
шивания ±0.01 мг), морфологию поверхности — ме-
оптическую плотность супернатанта на фотометре
тодом сканирующей электронной микроскопии, как
Stat Fax 4200 (Awareness Technology) при λ = 545 нм.
описано выше.
Проводили три параллельных опыта. Степень гемо-
лиза (%) рассчитывали по разнице оптической плот-
Обсуждение результатов
ности супернатанта тестируемой системы и суспен-
зии эритроцитов в физиологическом растворе (0.15 М
Были разработаны два способа получения полых
NaCl, положительный контроль, 0%-ный гемолиз) с
цилиндрических структур.
учетом оптической плотности суспензии эритроцитов
Согласно первому способу, межфазная химическая
в дистиллированной воде (отрицательный контроль,
реакция ионно-индуцированной нейтрализации про-
100%-ный гемолиз). Тестируемый образец считали
текает на границе раздела двух жидких фаз (раствор
гемосовместимым при степени гемолиза менее 5%.
солевой формы хитозана-раствор нейтрализующего
Статистическую обработку данных проводили с при-
реагента), согласно второму — преимущественно на
менением пакета программ Statistica 6.0.
границе твердое тело-жидкость (твердообразный со-
Цитотоксическое действие исследовали in vitro на
левой хитозан-раствор нейтрализующего реагента).
модели клеточной линии эпителиоцитов эмбриональ-
При использовании NaOH и триэтаноламина водоне-
ной почки макаки резус MA-104 (Институт цитологии
растворимая форма полимера в виде полого цилиндра
РАН). Образцы стерильных микротрубок (см. выше)
формировалась по механизму полимераналогичного
помещали в стерильные чашки Петри, заливали ро-
превращения соль → основание хитозана, додецил-
стовой средой DMEM (ООО «БиолоТ») с добавле-
бензосульфоната Na — по механизму нейтрализован-
нием 10% фетальной бычьей сыворотки (Hyсlone)
ного полиэлектролитного комплекса с поверхност-
и 1% смеси пенициллина со стрептомицином (РУП
но-активным веществом. Поскольку различия данных
«Белмедпрепараты»), вносили суспензию клеточной
способов формирования микротрубок значимо отра-
культуры в концентрации 1·104 кл/см3 и культиви-
жаются на морфологии, структуре и свойствах полу-
ровали в СО2-инкубаторе MCO-18AIC (Sanyo) при
чаемых образцов, уместно их раздельное обсуждение.
Получение, структура и свойства микротрубок хитозана
73
Образцы, сформированные из раствора хитозана
молочной кислоте показывают деформационно-проч-
в лимонной кислоте способом 1, являются хрупкими,
ностное поведение хрупких полимерных материалов
имеют поверхностные дефекты, а толщина их стенок
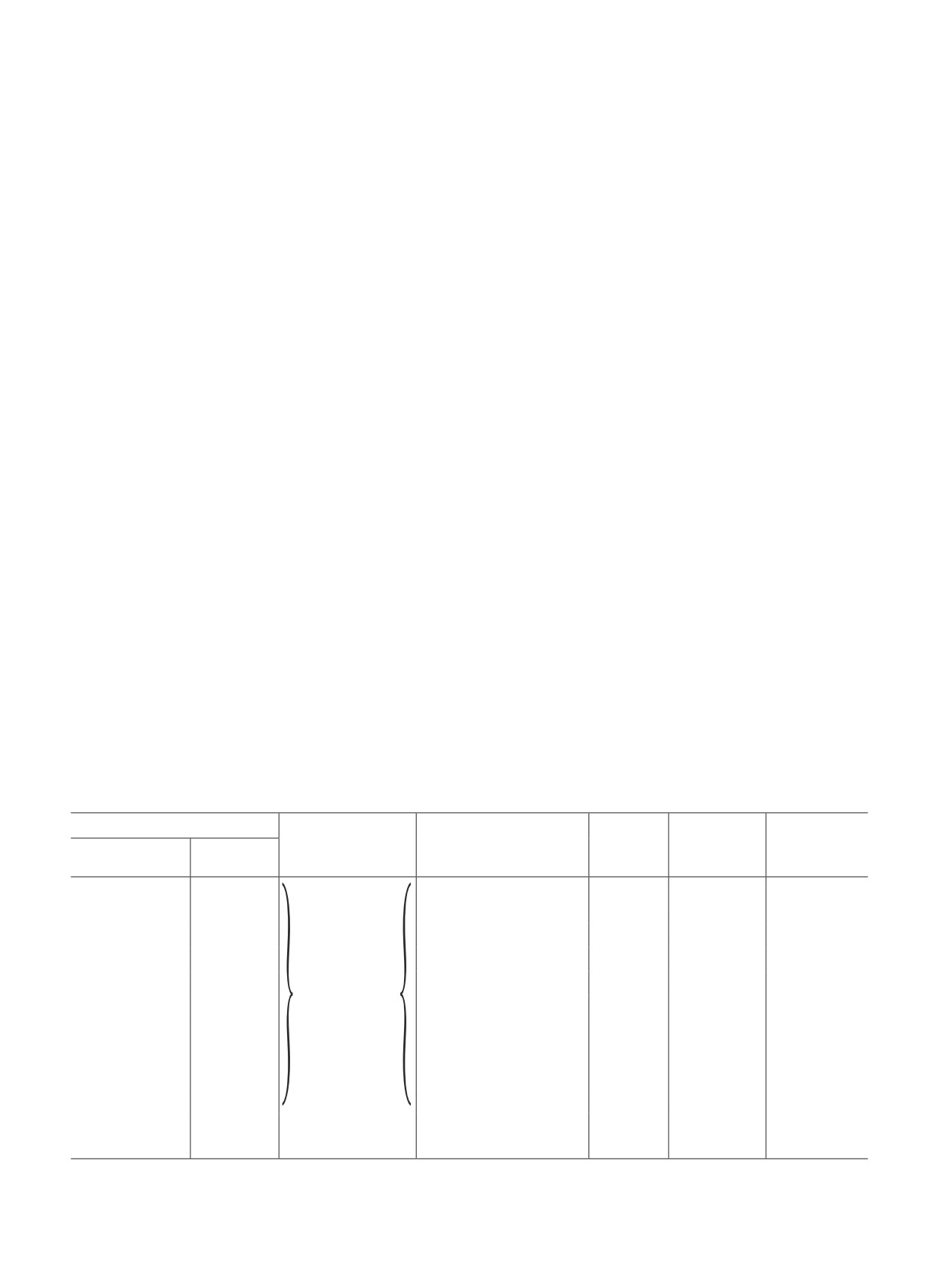
(рис. 3, кривые 1 и 2). Зависимости σ = f(ε) образцов,
и морфология образцов практически не зависят от
полученных из растворов хитозана в гликолевой кис-
мольного соотношения кислота:полимер (моль:ос-
лоте в том же нейтрализующем реагенте, являются
ново-моль) в исходном растворе, в молочной и глико-
типичными для вязкопластичных систем (рис. 3, кри-
левой кислотах — формоустойчивы, эластичны и без
вые 3 и 4). Однако после достижения предела те-
видимых дефектов (табл. 1; рис. 1, а-в). Наилучшие
кучести наблюдается плато, свидетельствующее о
образцы микротрубок получены из растворов хитоза-
частичном разрушении материала.
на в гликолевой кислоте. Они характеризуются разви-
Деформационные кривые нагрузка-удлинение ми-
той поверхностью (рис. 2, а), толщина стенок соста-
кротрубок, полученных из тех же растворов гликолята
вила 350-700 мкм, длина — 30-70 мм. По-видимому,
хитозана, но с использованием додецилбензосульфо-
бόльшие по размерам цитрат- и лактат-анионы созда-
ната Na, аналогичны таковым для образцов, получен-
ют стерические затруднения для надмолекулярного
ных нейтрализацией в щелочной среде: имеют участок
упорядочения полимерного вещества по сравнению с
упругой деформации, значение которой не превышает
меньшим по объему гликолят-анионом. Это приводит
2-3%, и «пластическую ветвь» (рис. 3, кривые 5 и
к различиям в морфоструктуре материала и согласу-
6). Особенностью являются более высокие значе-
ется с концепцией авторов [16] о влиянии объема про-
ния σр и εр. Во всех случаях наиболее оптимальное
тивоиона на структуру и свойства пленок хитозана.
мольное соотношение гликолевая кислота:хитозан,
Вместе с тем нельзя исключить влияние заряда ма-
обеспечивающее удовлетворительные упруго-пла-
кроцепи и гидрофобных взаимодействий реагентов.
стические характеристики микротрбок, составило
Высказанное предположение подтверждается ис-
0.9-1.1 моль:осново-моль. Тем не менее прочность
следованием упруго-пластических характеристик
материалов, полученных способом ионно-индуциро-
образцов (рис. 3, а; табл. 1). Микротрубки, получен-
ванной нейтрализации солевой формы полимера на
ные из растворов хитозана в лимонной кислоте в
границе жидкость-жидкость, невысокая. Кроме того,
среде NaOH, практически мгновенно разрушаются
отмечается неравномерность толщины стенки по дли-
при приложении растягивающей силы, а сформи-
не образца вследствие стекания раствора полимера по
рованные в аналогичных условиях из растворов в
стержню в процессе формирования полой структуры.
Таблица 1
Морфология, размерные и физико-механические характеристики микротрубок,
полученных ионно-индуцированной нейтрализацией солевой формы хитозана на границе жидкость-жидкость,
в зависимости от концентрации полимера в растворе, природы кислоты и нейтрализующего реагента
Состав формовочного раствора
Толщина
Разрывное
Удлинение
Нейтрализующий
Морфология
стенки,
напряжение
при разрыве
концентрация
реагент
образца микротрубки
кислота
мкм
σр, МПа
εр, %
хитозана, мас%
2-4
Лимонная
Непрозрачный, очень
440 ± 80
—
—
хрупкий
2.0
Молочная
Прозрачный, хрупкий
500 ± 70
—
—
3.0
Прозрачный, эластич-
520 ± 50
0.70 ± 0.15
34.0 ± 2.0
3.5
ный
540 ± 50
0.25 ± 0.04
23.0 ± 5.0
NaOH
4.0
Не формуется
—
—
—
2.5
Гликолевая
Непрозрачный, хрупкий
400 ± 55
0.24 ± 0.07
14.0 ± 3.4
3.0
400 ± 40
0.40 ± 0.17
14.0 ± 5.4
3.5
Непрозрачный, эластич-
420 ± 40
0.83 ± 0.27
20.0 ± 7.5
4.0
ный
700 ± 45
0.70 ± 0.20
24.0 ± 4.2
3.5
Додецилбензо-
Прозрачный, высокоэла-
480 ± 50
1.25 ± 0.2
28.0 ± 5.2
4.0
сульфонат Na
стичный
350 ± 35
2.42 ± 0.4
30.0 ± 1.1
Примечание. «—» — не определяли.
74
Шиповская А. Б. и др.
Рис. 1. Фотографии микротрубок, полученных из раствора хитозана в лимонной (а), молочной (б) и гликолевой
кислотах (в, г) ионно-индуцированной нейтрализацией солевой формы полимера на границе жидкость-жидкость
(а-в) и твердое тело-жидкость (г) с использованием в качестве нейтрализующего реагента NaOH (а-в) и пары
додецилбензосульфонат Na-додецилбензосульфонат Na (г).
г — фотографии сделаны через 3 года хранения образцов в этиловом спирте.
Указанные недостатки устранены во втором способе
жидкость-жидкость, характеризуются формоустой-
получения микротрубок. Для предотвращения эффек-
чивостью, эластичностью и отсутствием дефектов
та стекания полимерной системы на поверхностности
(рис. 1, г; табл. 2). Толщина стенки (160-275 мкм) и
раствора хитозана формировали водонерастворимую
отклонения в значениях толщины по длине образца
оболочку путем кратковременного выдерживания
существенно меньше, а сочетание нейтрализующих
стержневого темплата с адсорбированным полимером
реагентов разной химической природы существенно
в нейтрализующем реагенте. Поскольку одним из
влияет на поверхностную морфоструктуру и пори-
способов упрочнения хитозансодержащих продуктов
стость образцов. Так, использование органического и
является термообработка [24], введен этап сушки об-
неорганического оснований на первом и втором эта-
разца. Далее темплат с твердофазным солевым хитоза-
пах нейтрализации сопровождается формированием
ном повторно подвергали ионно-индуцированной ней-
пористой структуры с размером пор 0.90-1.47 мкм.
трализации. Вследствие двухэтапного формирования
Замена NaOH на втором этапе на додецилбензосуль-
водонерастворимой формы полимера использовали
фонат Na также приводит к получению развитой
как одинаковые, так и разные сочетания нейтрали-
структуры, но с меньшим размером пор 0.80-0.95 мкм.
зующих реагентов (NaOH-NaOH, триэтаноламин-
Применение NaOH и додецилбензосульфоната Na на
NaOH, триэтаноламин-додецилбензосульфонат Na и
обоих этапах нейтрализации приводит к формиро-
додецилбензосульфонат Na-додецилбензосульфонат
ванию практически гладкой поверхности (рис. 2, в).
Na). Для дальнейших исследований выбраны рас-
Микротрубки, сформированные способом 2 с ис-
творы хитозана в гликолевой кислоте, из которых
пользованием в качестве нейтрализующей среды па-
способом 1 был получен бездефектный материал с
ры триэтаноламин-NaOH или NaOH-NaOH, являют-
удовлетворительными механическими свойствами.
ся вязкопластичными материалами с более высокой
Микротрубки, сформированные двухэтапной
долей упругой (~4-5%) и высокоэластической дефор-
ионно-индуцированной нейтрализацией гликолята
мации (рис. 3, б, кривые 1 и 2), чем полученные спо-
хитозана на границе твердое тело-жидкость, как и
собом 1. Образцы, нейтрализованные в среде триэта-
полученные из растворов того же состава на границе
ноламин-додецилбензосульфонат Na (кривая 3) или
Получение, структура и свойства микротрубок хитозана
75
Рис. 2. Изображения, полученные методом сканирующей электронной микроскопии, поверхности (а, в, д, е) и
структуры стенки (б, г) микротрубок, полученных из 4.0 мас%-ного раствора хитозана в гликолевой кислоте ион-
но-индуцированной нейтрализацией солевой формы полимера на границе жидкость-жидкость в среде NaOH (а, б)
и на границе твердое тело-жидкость с использованием NaOH-NaOH (в-е).
Образцы: а-г — исходные, д, е — после 120 и 180 сут биорезорбции в ферментативной среде лизоцима.
додецилбензосульфонат Na-додецилбензосульфонат
образованием шейки вследствие ориентационного
Na (кривая 4), проявляют вынужденно-эластическое
упорядочения материала. Как и в первом способе,
деформирование вязкоупругих полимерных систем.
наибольшую прочность и эластичность демонстриру-
Данные образцы деформируются при растяжении с
ют образцы микротрубок, полученные из растворов
76
Шиповская А. Б. и др.
Рис. 3. Зависимость нагрузка-удлинение в воздушной атмосфере при 22 ± 2°C (а, б) и физиологическом растворе
при 37°C (в) образцов микротрубок, полученных ионно-индуцированной нейтрализацией солевой формы полимера
на границе жидкость-жидкость (а) и твердое тело-жидкость (б, в).
Образцы: а — микротрубки, полученные из 3.0 (1), 3.5 (2, 3, 5) и 4.0 мас%-ных (4, 6) растворов хитозана в молочной (1, 2)
и гликолевой кислотах (3-6) в среде NaOH (1-4) и додецилбензосульфоната Na (5, 6); б, в — микротрубки, полученные из
4.0 мас%-ного раствора хитозана в гликолевой кислоте с использованием двухэтапной нейтрализации в среде триэтанола-
мин-NaOH (1), NaOH-NaOH (2), триэтаноламин-додецилбензосульфанат Na (3) и додецилбензосульфонат Na-додецил-
бензосульфонат Na (4); пластина ксеноперикардиальная (5); биоматериал (фрагмент сонной артерии человека) (6) [23].*
при мольном соотношении кислота:полимер = 0.9-
поверхностно-активного вещества понижает модуль
1.1 моль:осново-моль.
Юнга по сравнению с триэтаноламином и NaOH.
Значения σр всех образцов, сформованных спосо-
Представляется, что такой характер изменения физи-
бом 2, значимо выше по сравнению с полученными
ко-механических свойств в зависимости от природы
способом 1, а εр — в большинстве случаев сопоста-
нейтрализующей среды обусловлен структурными
вимы (табл. 2). Как и морфоструктура поверхности,
особенностями конденсированной полимерной фазы.
прочностные показатели зависят от природы нейтра-
Вследствие депротонизации макроклубков в процессе
лизующего реагента. Существенно более прочные
получения материала в среде NaOH и триэтаноламина
образцы получены с использованием додецилбензо-
образуется уплотненная надмолекулярная структу-
сульфоната Na. Вместе с тем нейтрализация в среде
ра, стабилизированная развитой системой меж- и
внутримолекулярных контактов. При использовании
мицеллярного раствора поверхностно-активного
* Разрешение на повторную публикацию материалов от
вещества (с концентрацией додецилбензосульфоната
авторов Голядкина А. А., Иванова Д. В., Кириллова И. В.,
Na существенно выше критической концентрации
Коссович Л. Ю., Павлова О. Е., Полиенко А. В., Сафонова
Р. А. получено 24.07.2023.
мицеллообразования) формируется более рыхлая
Получение, структура и свойства микротрубок хитозана
77
Таблица 2
Морфология, размерные и физико-механические параметры микротрубок, полученных из 4.0 мас%-ного
раствора хитозана в гликолевой кислоте двухэтапной ионно-индуцированной нейтрализацией солевой формы
полимера на границе твердое тело-жидкость
Сочетание нейтрализующих реагентов на эта-
Толщина
Разрывное
Модуль
Удлинение
Морфология образца
пах формирования водонерастворимой формы
стенки,
напряжение
Юнга E,
при разрыве
микротрубки
полимера
мкм
σр, МПа
МПа
εр, %
Испытания в воздушной среде
Триэтаноламин-NaOH
Непрозрачный, эла-
160 ± 25
1.8 ± 0.7
1.60 ± 0.46
20.5 ± 7.2
стичный
NaOH-NaOH
180 ± 25
4.8 ± 2.2
0.93 ± 0.31
26.1 ± 6.4
Триэтаноламин-додецилбензосульфонат Na
255 ± 30
5.9 ± 2.1
0.25 ± 0.16
27.7 ± 8.6
Додецилбензосульфонат Na-додецилбензо-
Прозрачный, эла-
275 ± 40
6.6 ± 1.7
0.65 ± 0.23
29.5 ± 5.1
сульфонат Na
стичный
Ксеноперикард*
Непрозрачный, эла-
280 ± 15
3.7 ± 0.9
29.8 ± 6.2
30.0 ± 2.0
стичный
И с п ыт а ни я в м оде л ьн о й водно й с р еде (0.15 М NaCl)
Триэтаноламин-NaOH
Непрозрачный, эла-
160 ± 25
0.55 ± 0.21
33.0 ± 2.4
20.7 ± 1.2
стичный
NaOH-NaOH
180 ± 25
0.62 ± 0.34
38.0 ± 3.2
30.6 ± 3.4
Внутренняя сонная артерия (биоматериал)
Непрозрачный, эла-
125 ± 15
0.73 ± 0.13
35.2 ± 2.1
24.8 ± 2.5
[23]*
стичный
надмолекулярная структура из мицеллоподобных
кластеров полиэлектролитных комплексов, характе-
ристические размеры которых определяются средним
расстоянием между мицеллоподобными агрегата-
ми [2]. Так, например, размер таких полостей при
ионотропном гелеобразовании хитозана в присутствии
додецилсульфата Na может достигать 3.5-7.5 нм [20].
Деформационно-прочностное поведение микро-
трубок в условиях, максимально приближенных к
нативным, оказалось аналогичным деформированию
сонной артерии (рис. 3, в; табл. 2). При одноосном
растяжении в имитирующей плазму крови модельной
водной среде (0.15 М NaCl) после начального прямо-
линейного участка (ε < 5-7%) реализуется участок
пластической деформации без выраженной площадки
текучести. Значения разрывной прочности, модуля
Юнга и удлинения при разрыве микротрубок и труб-
чатого биооргана практически совпадают. Значения
σр и εр данных образцов микротрубок, сопоставимые
с коммерческим образцом ксеноперекардиальной
пластины, зафиксированы и при растяжении в воз-
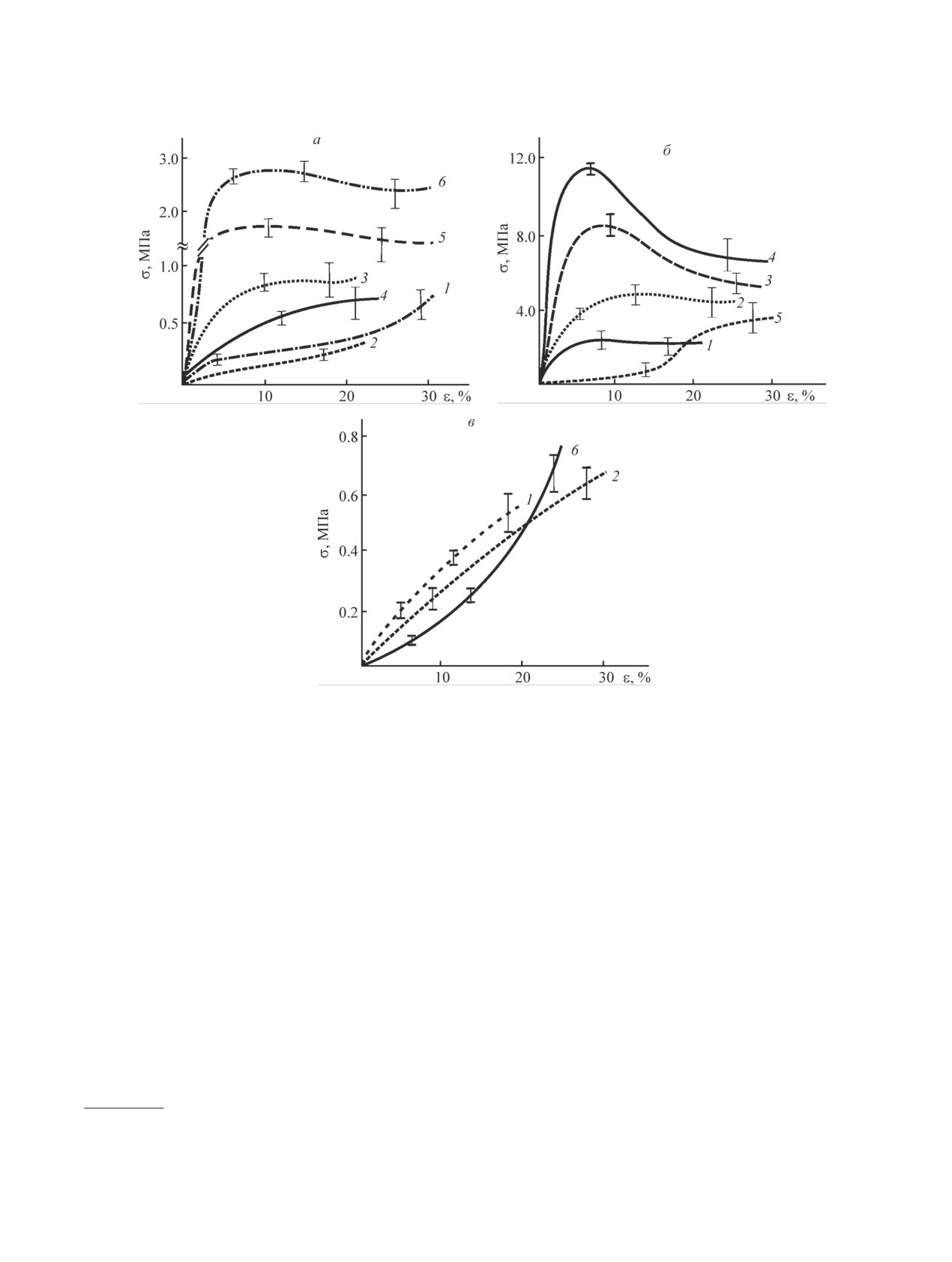
Рис. 4. Рентгеновские дифрактограммы исходного по-
рошка хитозана (1), микротрубки (2) и основных пленок
душной атмосфере (рис. 3, б, кривая 5; табл. 2).
хитозана (3, 4), полученных из 4.0 мас%-ного раствора
полимера в гликолевой кислоте ионно-индуцированной
нейтрализацией солевой формы полимера на границе
* Разрешение на повторную публикацию материалов от
твердое тело-жидкость с использованием NaOH-NaOH
авторов Голядкина А. А., Иванова Д. В., Кириллова И. В.,
(2, 3) и методом полива на горизонтальную подлож-
Коссович Л. Ю., Павлова О. Е., Полиенко А. В., Сафонова
ку с последующей сушкой и нейтрализацией в среде
Р. А. получено 24.07.2023.
NaOH (4).
78
Шиповская А. Б. и др.
Таблица 3
Межплоскостные расстояния в кристаллитах и степень кристалличности образцов хитозана разной
морфологической формы
Угол
Степень
Образец
Межплоскостное
Способ получения
дифракции
кристалличности
хитозана
расстояние d, Å
2θ, град
χ, %
Порошок
Деацетилирование хитина в гетерогенных условиях
11.80
7.500
40.0
в среде NaOH
20.50
4.332
29.50
3.280
Микротрубка
Двухэтапная нейтрализация гликолята хитозана на
10.70
8.270
61.9
искривленной поверхности на границе раздела
20.30
4.375
твердое тело-жидкость в среде NaOH-NaOH (спо-
29.40
3.038
соб 2)
Пленка основ-
Двухэтапная нейтрализация гликолята хитозана на
11.00
8.043
59.6
ной формы
плоской поверхности на границе раздела твердое
15.00
5.906
тело-жидкость в среде NaOH-NaOH (способ 2)
20.80
4.270
22.20
4.004
23.50
3.789
26.50
3.243
Одноэтапная нейтрализация гликолята хитозана на
10.70
8.270
55.8
плоской поверхности на границе раздела твердое
20.40
4.353
тело-жидкость в среде NaOH (традиционный спо-
22.80
3.900
соб получения пленок хитозана основной формы)
26.75
3.331
28.40
3.143
29.50
3.028
Следует также отметить, что микротрубки, по-
пленки основной формы, полученной методом по-
лученные способом 2, устойчивы при длительном
лива, а значения d в кристаллитах всех морфологи-
хранении. Выдерживание в этиловом спирте в течение
ческих форм хитозана различаются незначительно.
трех лет практически не изменяет морфоструктуру
Степень кристалличности микротрубки (61.9%) и
(рис. 1, г) и физико-механические показатели образцов.
пленок (55.8-59.6%) значимо выше по сравнению с
Рентгеновские дифрактограммы микротрубок, ис-
исходным порошком (40.0%). Это свидетельствует о
ходного порошка и пленок хитозана основной формы,
формировании более ориентированной структуры по-
для сравнения полученных способом 2 и традици-
лимера в данных образцах и является типичным при
онным способом высушивания раствора на плоской
перекристаллизации хитозана в щелочной среде [24,
поверхности в воздушной атмосфере, практически
25]. Наибольшее значение χ наблюдается для микро-
идентичны: на фоне аморфного гало проявляются
трубки. Следовательно, микротрубчатые субстраты
перекрывающиеся рефлексы при 2θ ~ 10.7°-11.8°
отличаются более упорядоченной надмолекулярной
и 20.3°-20.8°, характерные для кристаллической
структурой с более развитой системой Н-связей.
структуры полиморфных модификаций полимера
Еще одна особенность — внутренняя структура
(рис. 4; табл. 3). Тем не менее наблюдаются разли-
стенки микротрубок представлена слоисто-ориенти-
чия в интенсивности рефлексов, значениях межпло-
рованным упорядочением. Наиболее ярко выражен-
скостных расстояний и степени кристалличности
ная слоистая структура наблюдается для образцов,
образцов. Так, при малых 2θ интенсивность рефлекса
полученных способом 1 с использованием NaOH
для материала микротрубки и порошка сопоставима,
(рис. 2, б) или триэтаноламина. Толщина слоев со-
но существенно больше, чем для пленок. При этом
ставляет 0.5-4.5 мкм, расстояние между слоями ва-
межплоскостные расстояния в полимерной фазе ми-
рьируется в диапазоне 1.5-8 мкм. Введение дополни-
кротрубки и пленок соизмеримы и больше, чем в
тельного этапа сушки (способ 2) не изменяет характер
полимерной фазе порошка. При больших 2θ наиболее
слоисто-периодического упорядочения, но приводит
интенсивные рефлексы наблюдаются для порошка и
к формированию более уплотненной структуры об-
Получение, структура и свойства микротрубок хитозана
79
разцов (рис. 2, г). Тем не менее разделенность слоев
реакций, а соотношение положений периодических
сохраняется, что говорит о самостоятельном форми-
слоев и кинетика их образования описываются за-
ровании каждого слоя. В экспериментах по изуче-
коном времени и пространства, характерным для
нию диффузии гидроксид-ионов в растворе гликолята
явления Лизеганга [18].
хитозана в отсутствие конвекции и перемешивания
На основании полученных результатов механизм
установлено, что межфазная реакция соль → основа-
массопереноса в процессе нейтрализации солевой
ние, лежащая в основе получения полых цилиндри-
формы хитозана при получении микротрубок пред-
ческих структур, протекает по механизму поэтапного
ставляется следующим. Рассмотрим его на при-
депротонирования поликатиона, что и приводит к
мере реакции полимераналогичного превращения
формированию многослойной структуры полимер-
соль → основание хитозана в щелочной среде на
ного материала [15]. Данный процесс описывается
границе жидкость-жидкость. Вследствие значимого
классическими закономерностями ионно-обменных
различия вязкости растворов реагирующих веществ
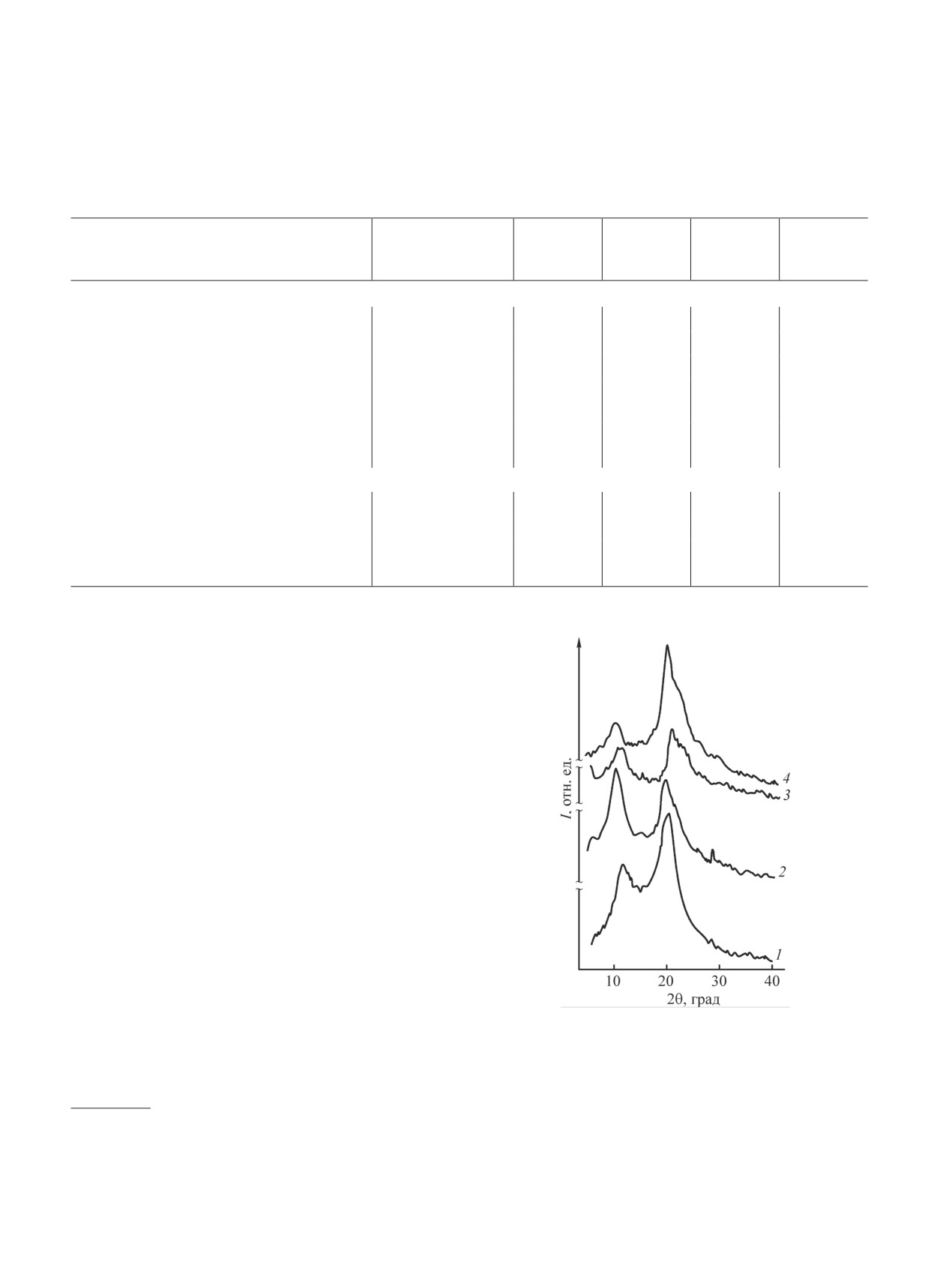
Рис. 5. Схематическое представление начального (а), промежуточных (б, в) и конечного этапов (г) ионно-индуци-
рованной нейтрализации солевой формы хитозана на границе жидкость-жидкость в среде NaOH, протекающей
при получении микротрубок.
Черным кругом изображено поперечное сечение стержневого темплата; стрелками показано направление диффузии
гидроксид-ионов; h1, h2, h3 — ширина пространственно-разделенных слоев основания хитозана [22].*
* Journal of Soft Matter, Creative Commons Attribution License.
80
Шиповская А. Б. и др.
контакт адсорбированного на темплате солевого хи-
тозана с NaOH приводит к образованию на границе
раздела двух жидких фаз диффузионного барьера,
препятствующего хаотическому перемешиванию
жидкостей и соответственно встречной диффузии ре-
агентов (рис. 5, а). Однонаправленная диффузия ио-
нов ОН- и депротонирование NH3+-групп сегментов
макроцепей сопровождается формированием первич-
ного водонерастворимого слоя в виде полупроницае-
мой полимерной мембраны (рис. 5, б, кольцевой слой
шириной h1). По мере протекания реакции граница
мембрана-раствор полимера перемещается вдоль
направления диффузии ионов ОН- с образованием
пространственно-разделенных слоев основания хи-
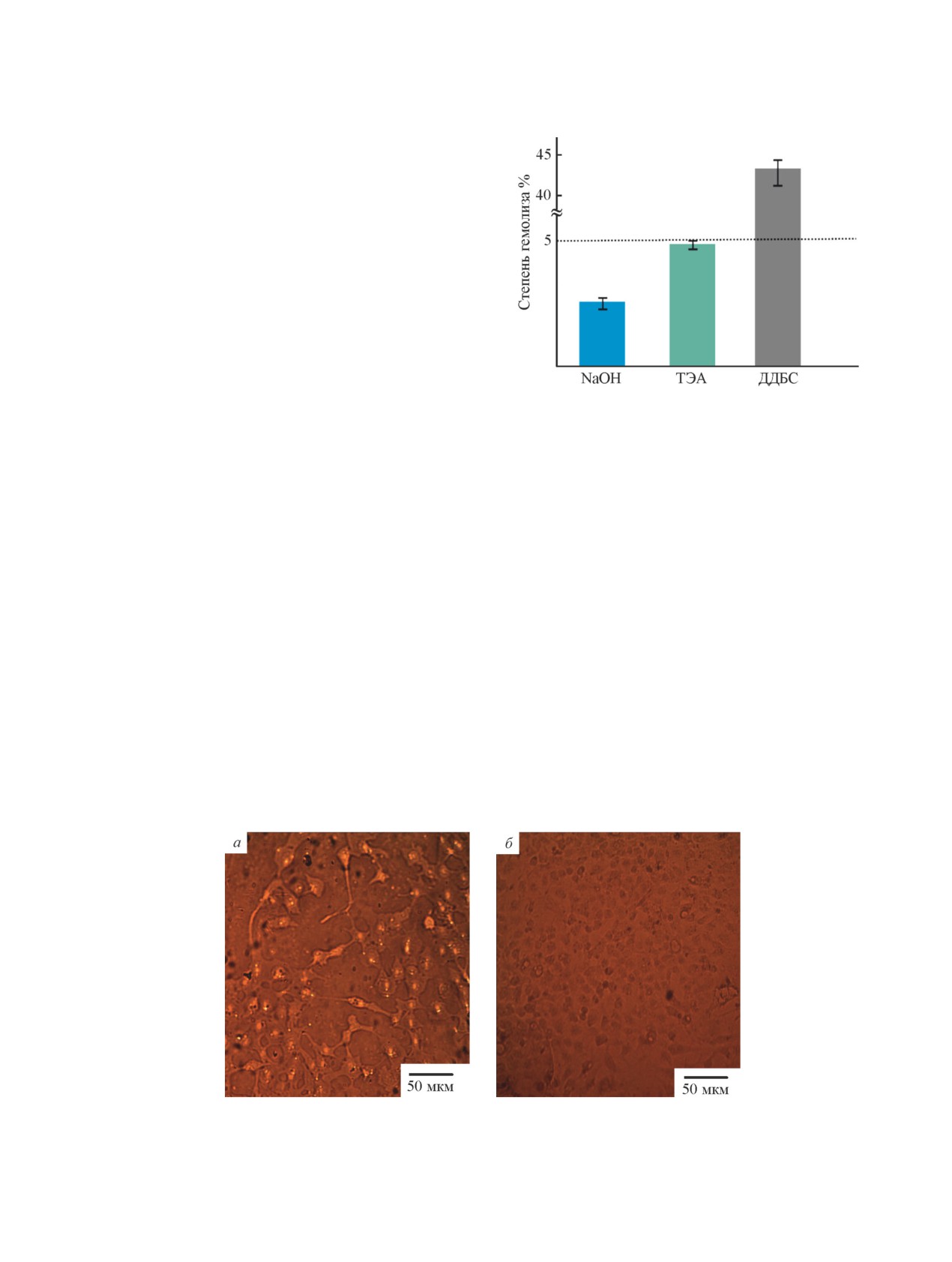
Рис. 6. Степень гемолиза эритроцитов в присутствии
тозана (рис. 5, в, г, кольцевые слои шириной h2 и h3).
микротрубок хитозана, полученных из 4.0 мас%-ного
При протекании реакции полимераналогичного
раствора хитозана в гликолевой кислоте ионно-индуци-
рованной нейтрализацией солевой формы полимера на
превращения на границе раздела твердое тело-жид-
границе жидкость-жидкость с использованием NaOH,
кость массоперенос в процессе однонаправленной
триэтаноламина (ТЭА) и додецилбензосульфоната Na
диффузии ОН--ионов в солевой форме хитозана про-
(ДДБСН).
исходит аналогично реакции на границе жидкость-
Пунктиром показано максимально допустимое значение
жидкость, но ввиду нейтрализации твердой фазы
степени гемолиза, характерное для гемосовместимых ма-
поликатиона сопровождается уменьшением ширины
териалов.
гидрогелевых слоев и межслоевого пространства и
соответственно формированием уплотненной сло-
образцами, полученными способом 1 с использова-
исто-упорядоченной организации материала.
нием NaOH и триэтаноламина, составил 1.6 ± 0.8 и
Поскольку одним из направлений практического
4.0 ± 1.0% соответственно, что не превышает макси-
использования микротрубок хитозана является меди-
мально допустимые значения данной величины для
цина, выполнены оценки их биологических свойств.
гемосовместимых материалов. Значительно более
Исследование гемосовместимости показало, что
высокая степень гемолиза, 42.0 ± 4.0%, наблюдает-
степень гемолиза эритроцитов при контакте с ми-
ся для образцов, сформованных тем же способом в
кротрубчатыми субстратами зависит от химической
среде додецилбензосульфоната Na, что может быть
природы используемого нейтрализующего реагента
обусловлено разрушением целостности клеточной
(рис. 6). Так, гемолиз эритроцитов при контакте с
мембраны вследствие взаимодействия липидных
Рис. 7. Эпителиоциты почки эмбриона макаки (МА-104) через 4 (а) и 7 сут (б) культивирования на поверхности
микротрубки, полученной из 4.0 мас%-ного раствора хитозана в гликолевой кислоте двухэтапной ионно-индуци-
рованной нейтрализацией солевой формы полимера на границе твердое тело-жидкость с использованием три-
этаноламин-NaOH.
Получение, структура и свойства микротрубок хитозана
81
участков эритроцитов и гидрофобных хвостовых
ния соль → основание хитозана или формирования
групп анионного поверхностно-активного вещества
полиэлектролитного комплекса) на границе твер-
[26]. Показатели гемосовместимости в зависимости
дое тело-жидкость, отличаются от полученных в
от природы нейтрализующей среды для полученных
условиях протекания химической реакции на грани-
способом 2 микротрубок аналогичные.
це жидкость-жидкость равномерностью толщины
Оценена цитотоксичность гемосовместимых
стенки по длине образца и высокими механически-
микротрубок на примере культуры эпителиопо-
ми характеристиками. Микротрубчатые субстраты,
добных клеток МА-104 (рис. 7). Для всех образцов
сформированные в среде NaOH и триэтаноламина,
наблюдается адгезия и пролиферация эпителиоци-
характеризуются слоисто-упорядоченной структу-
тов на поверхности микротрубчатых субстратов.
рой, демонстрируют деформационно-прочностное
Формирование полного монослоя клеточной куль-
поведение вязкопластичных полимерных материалов,
туры МА-104 наблюдается в среднем на 7-е сутки
нецитотоксичны, гемо- и биосовместимы.
культивирования, что свидетельствует об отсутствии
Результаты исследования морфологии, структуры,
токсичности и биосовместимости образцов.
физико-механических и биохимических свойств ми-
При исследовании биодеградации установлено,
кротрубок хитозана показывают перспективы их ис-
что выдерживание микротрубок в среде лизоцима
пользования в медико-биологических приложениях, в
сопровождается изменением их микрорельефа от
частности, в качестве биодеградируемых сосудистых
изначально гладкой (рис. 2, в) до ярко выраженной
трансплантатов для замены поврежденных участков
рыхлой поверхности (рис. 2, д, е), а также умень-
кровеносных сосудов, мочеточников и других труб-
шением массы полимерного вещества. Например,
чатых образований живого организма. Такие мате-
убыль массы микротрубки, полученной способом 2 с
риалы предполагают кратковременное нахождение в
использованием пары триэтаноламин-NaOH, соста-
организме вследствие биодеградации естественным
вила ~8 и ~20-25% за 30 и 180 сут инкубации соот-
метаболическим путем и максимально возможное
ветственно, с использованием двухэтапной нейтрали-
восстановление клеточного состава поврежденной
зации в среде NaOH-NaOH - ~12 и ~30-35%. В среде
ткани или даже части органа.
фосфатного буферного раствора (контрольный экс-
Предложенные способы получения микротрубок
перимент) значимого изменения морфоструктуры
хитозана на цилиндрическом темплате выгодно отли-
поверхности образцов не наблюдается, а убыль мас-
чаются от представленных в литературе сравнительно
сы за весь срок эксперимента не превышает ~5-7%.
простыми методологическими приемами и возможно-
Результаты качественной реакции Руэманна с нин-
стью создавать полые цилиндрические структуры с
гидрином показали наличие в составе ферментатив-
заранее заданными толщиной и физико-химическими
ного гидролизата низкомолекулярных продуктов со
характеристиками.
свободными аминогрупами и их отсутствие в составе
буферного гидролизата. Следовательно, деградация
Благодарности
микротрубчатых субстратов в ферментативной среде
протекает по механизму разрыва β-(1, 4)-гликозидной
Авторы выражают благодарность центру коллек-
связи, что согласуется с результатами работ [27, 28],
тивного пользования «Физико-химические мето-
а в буферном растворе — лишь за счет растворения
ды исследования и анализа веществ и материалов»
низкомолекулярных фракций. Исходя из экспери-
Саратовского национального исследовательского
ментальных количественных показателей, а также
государственного университета им. Н. Г. Черны-
учитывая биокаталитическую активность лизоцима
шевского за анализ образцов микротрубок методами
и других гидролаз, можно предположить, что полная
сканирующей микроскопии и рентгеновской дифрак-
биорезорбция микротрубок в естественной метабо-
тометрии.
лической среде наступит в среднем через 8-12 мес.
Этого времени вполне достаточно для восстановле-
Финансирование работы
ния живой ткани протезированного органа.
Финансовая поддержка работы осуществлялась
в рамках госзадания Минобрнауки России в сфе-
Выводы
ре научной деятельности № 4.1212.2014/К, грантов
Микротрубки хитозана, полученные с использо-
Фонда содействия инновациям № 4276ГУ1/2014 и
ванием межфазных реакций ионно-индуцированной
Российского фонда фундаментальных исследований
нейтрализации (полимераналогичного превраще-
№ 16-33-00953.
82
Шиповская А. Б. и др.
Конфликт интересов
[4]
Li X., Tang J., Bao L., Chen L., Hong F. F. Performance
improvements of the BNC tubes from unique double-
Авторы заявляют об отсутствии конфликта инте-
silicone-tube bioreactors by introducing chitosan and
ресов, требующего раскрытия в данной статье.
heparin for application as small-diameter artificial
blood vessels // Carbohydr. Polym. 2017. V. 178.
Информация о вкладе авторов
P. 394-405.
А. Б. Шиповская сформулировала цель и обо-
[5]
Yin K., Divakar P., Wegst U. G. K. Freeze-casting
сновала задачи исследования; А. Б. Шиповская,
porous chitosan ureteral stents for improved drainage
Н. О. Гегель и Т. С. Бабичева разработали план экс-
// Acta Biomater. 2019. V. 84. P. 231-241.
перимента; Н. О. Гегель и Т. С. Бабичева получили
микротрубки хитозана; Н. О. Гегель, Т. С. Бабичева
[6]
Al Rez M. F., BinObaid A., Alghosen A., Mirza E.,
и А. А. Голядкина провели исследование физико-ме-
Alam J., Hashem M., Alsalman H., Almalak H. M.,
ханических свойств микротрубок; А. А. Голядкина
Mahmood A., Moussa I., Al-Jassir F. F. Tubular poly(ε-
оценила физико-механические свойства ксенопери-
caprolactone)/chitosan nanofibrous scaffold prepared
кардиальной пластины и фрагмента сонной артерии
by electrospinning for vascular tissue engineering
человека; Т. С. Бабичева изучила гемосовместимость
applications // J. Biomater. Tissue Eng. 2017. V. 7.
микротрубчатых субстратов; Н. О. Гегель провела
[7]
Попрядухин П. В., Юкина Г. Ю., Суслов Д. Н.,
исследование цитотоксичности и биосовместимости
Добровольская И. П., Иванькова Е. Н., Юдин В. Е.
микротрубок; А. Б. Шиповская и Н. О. Гегель уча-
Биорезорбция пористых 3D-материалов на основе
ствовали в написании статьи.
хитозана // Цитология. 2016. Т. 58. № 10. P. 771-
777. EDN: XWRWWD
Информация об авторах
[8]
Badhe R. V., Bijukumar D., Chejara D. R.,
Mabrouk M., Choonara Y. E., Kumar P., du Toit L. C.,
Шиповская Анна Борисовна, д.х.н, проф.
Kondiah P. P. D., Pillay V. A composite chitosan-
gelatin bi-layered, biomimetic macroporous scaffold
Гегель Наталья Олеговна, к.х.н.
for blood vessel tissue engineering // Carbohydr.
Polym. 2017. V. 157. P. 1215-1225.
Бабичева Татьяна Сергеевна, к.х.н.
[9]
Zhao X., Liu S., Han Y., Wang Y., Lin Q. Preparation
of 5-fluorouracil loaded chitosan microtube via in situ
Голядкина Анастасия Александровна, к.ф.-м.н.
precipitation for glaucoma drainage device application:
in vitro and in vivo investigation // J. Biomater.
Sci. Polym. Ed. 2021. V. 32. N 14. P. 1849-1864.
Список литературы
[10]
Macêdo M. D. M., de Lucena B. M., de
[1] Wang J., Zhuang S. Chitosan-based materials:
Cerqueira G. R. C., de Sousa W. J. B., Pedrosa T. C.,
Preparation, modification and application // J. Clean.
Barbosa R. C., de Azevedo A. C. S., de Souza M. F.,
Prod. 2022. V. 355. ID 31825.
de Oliveira D. K. M., Fook M. V. L. Tubular chitosan
device for use as prosthesis coating in vascular
[2] Rinaudo M. Chitin and chitosan: Properties and
surgery // Res. Soc. Develop. [S. l.]. 2021. V. 10. N 4.
applications // Progress Polym. Sci. 2006. V. 31.
P. e25610414031.
[11]
Neufurth M., Wang X., Tolba E., Dorweiler B.,
[3] Мударисова Р. Х., Кулиш Е. И., Зинатуллин P. M.,
Schröder H. C., Link T., Diehl-Seifert B.,
Таминдарова Н. Э., Колесов С. В., Хунафин С. Н.,
Muller W. E. G. Modular small diameter vascular
Монаков Ю. Б. Пленки комплексов на основе хи-
grafts with bioactive functionalities // PLoS ONE.
тозана с контролируемым высвобождением лево-
2015. V. 10. N 7. P. e0133632.
мицетина // ЖПХ. 2006. Т. 79. № 10. С. 1737-1739.
EDN: HVKFJH [Mudarisova R. K., Kulish E. I.,
[12]
Beda A., Yamada H., Egunov A., Ghimbeu C. M.,
Zinatullin R. M., Tamindarova N. E., Kolesov S. V.,
Malval J. P., Saito Y., Luchnikov V. Carbon microtubes
Khunafin S. N., Monakov Y. B. Films of chitosan-based
derived from self-rolled chitosan acetate films and
complexes with controlled release of levomycetin //
graphitized by joule heating // J. Mater. Sci. 2019.
Russ. J. Appl. Chem. 2006. V. 79. N 10. P. 1718-1720.
V. 54. N 16. P. 11345-11356.
Получение, структура и свойства микротрубок хитозана
83
[13]
Lugovitskaya T. N., Shipovskaya A. B., Shmakov S. L.,
[21]
Базунова М. В., Мустакимов Р. А., Бакирова Э. Р.
Shipenok X. M. Formation, structure, properties of
О формировании устойчивых полиэлектролитных
chitosan aspartate and metastable state of its solutions
комплексов на основе N-сукцинила хитозана и по-
for obtaining nanoparticles // Carbohydr. Polym. 2022.
ли-N,N-диаллил-N,N-диметиламмоний хлорида //
V. 277. ID 118773.
ЖПХ. 2022. Т. 95. № 1. С. 42-48.
[14]
Шиповская А. Б., Малинкина О. Н., Гегель Н. О.,
[Bazunova M. V., Mustakimov R. A., Bakirova E. R.
Зудина И. В., Луговицкая Т. Н. Структура и свой-
Conditions of formation of stable polyelectrolyte
ства солевых комплексов хитозана с диастерео-
complexes based on N-succinyl chitosan and poly-
мерами аскорбиновой кислоты // Изв. АН. Сер.
N,N-diallyl-N,N-dimethylammonium chloride // Russ.
хим. 2021. № 9. С. 1765-1774. EDN: TVLXSM
J. Appl. Chem. 2022. V. 95. N 1. P. 46-52.
[Shipovskaya A. B., Malinkina O. N., Gegel N. O.,
Zudina I. V., Lugovitskaya T. N. Structure and
[22]
Gegel N. O., Shipovskaya A. B., Vdovykh L. S.,
properties of chitosan salt complexes with ascorbic
Babicheva T. S. Preparation and properties of 3D
acid diastereomers // Russ. Chem. Bull. 2021. V. 70.
chitosan microtubes // J. Soft Matter. 2014. V. 2014.
N 9. P. 1765-1774.
[23]
Голядкина А. А, Иванов Д. В., Кириллова И. В.,
[15]
Babicheva T. S., Konduktorova A. A., Shmakov S. L.,
Коссович Е. Л., Павлова О. Е., Полиенко А. В.,
Shipovskaya A. B. Formation of Liesegang structures
Сафонов Р. А. Биомеханика сонной артерии.
under the сonditions of the spatiotemporal reaction
Саратов: Саратовский источник, 2015. С. 70. EDN:
of polymer-analogous transformation (salt→base)
VIKEJR
of chitosan // J. Phys. Chem. B. 2020. V. 124. N 41.
[24]
Агеев Е. П., Вихорева Г. А., Зоткин М. А., Ма-
P. 9255-9266.
тушкина Н. Н., Герасимов В. И., Зезин С. Б., Обо-
лонкова Е. С. Структура и транспортные свой-
[16]
Qiao C., Ma X., Wang X., Liu L. Structure and
ства хитозановых пленок, модифицированных
properties of chitosan films: Effect of the type of
термообработкой // Высокомолекуляр. соеди-
solvent acid // LWT. 2021. V. 135. ID 109984.
нения. 2004. Т. 46А. № 12. С. 2035-2041. EDN:
NEMWOV [Ageev E. P., Vikhoreva G. A., Zotkin M. A.,
[17]
Melro E., Antunes F. E., da Silva G. J., Cruz I.,
Matushkina N. N., Gerasimov V. I., Zezin S. B.,
Ramos P. E., Carvalho F., Alves L. Chitosan films in
Obolonkova E.S. Structure and transport behavior of
food applications. Tuning film properties by changing
heat-treated chitosan films // Polym. Sci. Ser. A. 2004.
acidic dissolution conditions // Polymers. 2021. V. 13.
V. 46. N 12. P. 1245-1250].
[25]
Shipovskaya A. B., Shmakov S. L., Gegel N. O.
[18]
Nie J., Lu W., Ma J., Yang L., Wang Z., Qin A.,
Optical activity anisotropy of chitosan-based films //
Hu Q. Orientation in multi-layer chitosan hydrogel:
Carbohydr. Polym. 2019. V. 206. Р. 476-486.
Morphology, mechanism and design principle // Sci.
Reports. 2015. V. 5. N 1. P. 1-7.
[26]
Жанкалова З. М. Показатели перекисного окисле-
ния липидов у больных с алкогольной болезнью
[19]
Li B., Gao Y., Feng Y., Ma B., Zhu R., Zhou Y.
печени // Медицина и экология. 2008. Т. 48. № 3.
Formation of concentric multilayers in a chitosan
P. 31-33.
hydrogel inspired by Liesegang ring phenomena // J.
Biomater. Sci. Polym. Ed. 2011. V. 22. N 17. P. 2295-
[27]
Zhang L., Dou S., Li Y., Yuan Y., Ji Y., Wang Y., Yang Y.
Degradation and compatibility behaviors of poly
[20]
Babak V. G., Merkovich E. A., Galbraikh L. S.,
(glycolic acid) grafted chitosan // Mater. Sci. Eng.
Shtykova E. V., Rinaudo M. Kinetics of diffusionally
Part C. 2013. V. 33. N 5. P. 2626-2631.
induced gelation and ordered nanostructure formation
in surfactant-polyelectrolyte complexes formed at
[28]
Кулиш Е. И. Чернова В. В., Володина В. П., Коле-
water/water emulsion type interfaces // Mendeleev
сов С. В. Биодеградация пленочных полимерных
покрытий на основе хитозана // Вестн. Башкир.
ун-та. 2008. Т. 13. № 1. С. 23-26. EDN: IPVEKV
Научное редактирование проведено научным редактором журнала «Нефтехимия» к.х.н. Н. В. Шелеминой.