Журнал прикладной химии. 2023. Т. 96. Вып. 11
НЕОРГАНИЧЕСКИЙ СИНТЕЗ И ТЕХНОЛОГИЯ НЕОРГАНИЧЕСКИХ ПРОИЗВОДСТВ
УДК 546.05+546.06:546-328
ПРИМЕНЕНИЕ ПЕРОКСИДНОГО МЕТОДА АКТИВАЦИИ ВАНАДИЯ
ДЛЯ ПОЛУЧЕНИЯ СМЕШАННЫХ ГЕТЕРОПОЛИСОЕДИНЕНИЙ
СО СТРУКТУРОЙ КЕГГИНА
© Ю. А. Родикова, Т. Ю. Кардаш, Е. Г. Жижина
Институт катализа им. Г. К. Борескова СО РАН,
630090, г. Новосибирск, пр. Академика Лаврентьева, д. 5
Поступила в Редакцию 18 октября 2023 г.
После доработки 29 декабря 2023 г.
Принята к публикации 29 декабря 2023 г.
Показана возможность получения смешанных гетерополисоединений со структурой Кеггина путем
введения в каркас Mo- и W-содержащих гетерополианионов каталитически активных атомов ва-
надия(V), активированных пероксидным методом. Установлено, что предварительная обработка
требуемого количества ванадия(V) в виде V2O5 концентрированным раствором H2O2 обеспечивает
значительное снижение посторонних ионов в растворах гетерополисоединений и солях на их основе.
На примере кислых солей составов Cs3.5H0.5PMo11VO40, Cs3.5H0.5PW11VO40 и Cs4.5H0.5SiW11VO40 доказа-
но внедрение атомов ванадия(V) в каркас гетерополианионов при сохранении целостности структуры.
Выполнено исследование текстурных характеристик целевых соединений, получены термограммы,
установлен фазовый состав. Продемонстрированы высокая стабильность и низкая растворимость
Cs-содержащих солей в трех циклах гидротермальной обработки.
Ключевые слова: активация ванадия; гетерополисоединение; структурная стабильность; цезиевые
соли; экологичный синтез; структура Кеггина
DOI: 10.31857/S0044461823110014; EDN: BLTNET
Смешанные гетерополисоединения структуры
свойства и используются для получения функцио-
Кеггина состава K8-a+хХМ12-хVxO40 (K — катион,
нальных материалов [1, 2].
Х — гетероатом, М — структурообразующий атом,
Синтез K8-a+хХМ12-хVxO40 в общем виде осно-
а — степень окисления Х) — востребованный и пер-
вывается на процедуре конденсации простых анио-
спективный тип полиоксометаллатов, обладающий
нов структурообразующих элементов в присутствии
окислительной активностью благодаря способности
H+-ионов. При этом от выбора используемых пред-
приобретать электроны. Подобные ванадийсодержа-
шественников в значительной степени зависит как
щие гетерополисоединения находят широкое приме-
продолжительность процесса и достигаемый состав,
нение в качестве катализаторов в различных областях
так и чистота итоговых соединений [3]. Методы по-
химии, среди которых сероочистка природного газа
лучения K8-a+хХМ12-хVxO40 можно разделить на ги-
и нефтепродуктов, получение физиологически актив-
дротермальные с применением оксидов элементов М
ных веществ и фармацевтических субстанций, транс-
(для соединений с х < 2) (см., например [4, 5]), синтез
формация растительного сырья в ценные молекулы
c использованием соответствующих солей (напри-
и др. Они также демонстрируют противовирусные
мер, [6, 7]), а также комбинированные способы [8].
842
Применение пероксидного метода активации ванадия для получения смешанных гетерополисоединений...
843
Общим этапом последних двух подходов является
охлаждении до полного растворения взвеси и измене-
применение NaVO3 в качестве источника ванадия в
ния его окраски на темно-красную, затем перемеши-
присутствии избытка сильной минеральной кислоты
вание продолжали при комнатной температуре (Тк) до
(HCl, H2SO4). Недостатком подобных методов явля-
полного выделения О2. Необходимые загрузки Н2О и
ется загрязнение целевых соединений катионами Na+
Н2О2 рассчитывали исходя из образования 0.0175 М
и анионами вводимой кислоты, приводящее к образо-
раствора декаванадиевой кислоты H6V10O28 [уравне-
ванию промывных вод в больших объемах.
ние (I)] и установленного нами ранее оптимального
Забота об окружающей среде стимулирует модер-
отношения [H2O2]/[V2O5], равного 15 [10].*
низацию технологий с учетом тенденций «зеленой»
5V2O5 + 2H2O2 + H2O → H6V10O28 + O2. (I)
химии, переход на использование гетерогенных ката-
литических систем, преимуществом которых являют-
Получение 0.2 М раствора незамещенной гете-
ся безэкстракционные методы отделения. Ключевым
рополикислоты состава H4PMo11VO40 выполняли
усовершенствованием применяемых сегодня подходов
смешением раствора H3PMo12O40, полученного рас-
к получению K8-a+хХМ12-хVxO40 может стать переход
творением МоО3 (х.ч., ООО «АО РЕАХИМ») в H2O/
на безотходный метод активации VV, основанный на
H3PO4 (ос.ч., ≥85%, АО «ВЕКТОН»), с раствором
предварительной обработке V2O5 концентрированным
H9PV14O40, приготовленным взаимодействием пред-
раствором H2O2 (пероксидный метод активации).
варительно образованной по уравнению (I) кислоты
В кристаллическом состоянии K8-a+хХМ12-хVxO40
H6V10O28 с H3PO4 (подробная методика описана в
с K = Н+, Li+ и Na+ растворимы в воде и некоторых
работе [10]). Концентрирование образующейся смеси
полярных органических растворителях. Потенциал их
обеспечивало полное растворение исходных реаген-
применения в качестве гетерогенных катализаторов
тов с образованием чистого раствора без посторонних
окисления может быть расширен путем замещения
ионов.
Н+-ионов крупными катионами из серии K+, Cs+,
0.1 М водный раствор гетерополикислоты состава
NH4+ или Bu4N+, введение которых приводит к по-
H4PW11VO40 со сниженным содержанием примесных
лучению гетерополисоединений с низкой раствори-
ионов получали допированием лакунарного аниона
мостью [9]. При этом использование Cs+ в качестве
состава [PW11O39]7- каталитически активными ато-
противоиона обеспечивает получение соединений с
мами VV в виде H6V10O28. Одновакантный анион
наиболее высокими величинами площади поверхно-
готовили щелочным гидролизом H3PW12O40 (ч.д.а.,
сти, что делает синтез цезиевых солей ванадийсодер-
АО «ВЕКТОН») по методике [11], для чего кислоту
жащих гетерополисоединений актуальным направле-
(0.02 моль) помещали в колбу емкостью 200 мл, ос-
нием для исследования.
нащенную магнитной мешалкой с нагревом, и рас-
Цель работы
— синтез ряда гетероген-
творяли в 50 мл дистиллированной Н2О при Тк и не-
ных ванадийсодержащих соединений состава
прерывном перемешивании. Взвесь перемешивали в
Cs8.5-аH0.5ХМ11VO40 (Х — PV, SiIV; М — MoVI, WVI) с
течение 10 мин, после чего рН полученного раствора
использованием пероксидного метода активации VV.
доводили до значения 4.8 добавлением по каплям на-
сыщенного водного раствора NaOH (ч.д.а., ООО «АО
Экспериментальная часть
РЕАХИМ»). Контроль за величиной рН осуществляли
на pH-метре InoLab pH 730 (WTW) с использованием
Для активации ванадия пероксидным методом
электрода SenTix 41 (WTW). Синтез 0.0175 М водно-
точную навеску V2O5 (х.ч., ООО «АО РЕАХИМ»)
го раствора H6V10O28 проводили по вышеописанной
помещали в стеклянный стакан требуемого объ-
общей методике с использованием 0.15 моль 30%-но-
ема, оснащенный магнитной мешалкой и тер-
го раствора H2O2 и 0.01 моль V2O5, растворенного
мометром, и растворяли в заданном количестве
в 114 мл дистиллированной Н2О. На заключитель-
охлажденной до 4-6°С дистиллированной Н2О (ак-
ном этапе раствор H6V10O28 порционно добавляли
вадистиллятор ДЭ-4М, АО «ЛОиП»). К полученной
к раствору лакунарного аниона при Тк. Полученную
суспензии при непрерывном перемешивании порци-
смесь перемешивали 10 мин, после чего ее рН дово-
онно добавляли 30%-ный раствор H2O2 (ос.ч., 8-4,
дили до значения ~2 прикапыванием по каплям 6 М
ООО «СПЕКТР-ХИМ») аналогичной температуры.
Введение H2O2 проводили при поддержании тем-
пературы суспензии ниже 10-12°С, для чего стакан
* При данной концентрации раствор H6V10O28 обладает
опускали в емкость со льдом. После объединения
наилучшей устойчивостью к осаждению гелеобразного
реагентов полученный раствор перемешивали при
V2O5·хН2О в случае необходимости его хранения.
844
Родикова Ю. А. и др.
раствора HCl (ос.ч., 20-4, ООО «АО РЕАХИМ»).
и дальнейшее старение осадка проводили при Тк в
После достижения целевого рН раствор нагревали
течение 20 ч. По истечении заданного времени ма-
до 60°С в течение ~20 мин, затем быстро охлажда-
точный раствор отделяли на роторном испарителе,
ли до Тк и снова подкисляли. Процедуру повторя-
осадок перетирали и сушили в сушильном шкафу при
ли несколько раз до стабилизации рН на значении
150°С в течение 2.5 ч.
2.0 ± 0.1, затем раствор разбавляли до объема 200 мл.
H9-aXM11VO40 +
Cs2CO3 →
Получение 0.1 М водного раствора гетерополикис-
лоты состава H5SiW11VO40 проводили по методике
(II)
[12]. Одновакантный анион состава [SiW11O39]8- по-
→ Cs8.5-aH0.5XM11VO40 + CO2 +
H2O.
лучали подщелачиванием 0.04 моль незамещенной
кислоты H4SiW12O40 (ч.д.а., ООО «АО РЕАХИМ»),
Инфракрасные спектры нарушенного полного вну-
растворенной в 100 мл дистиллированной Н2О, до
треннего отражения (ИК-НПВО) регистрировали
значения рН 5.5-6.0 в колбе емкостью 400 мл, осна-
в диапазоне 4000-350 см-1 с разрешением 4 см-1 и
щенной магнитной мешалкой с нагревом. Для ста-
накоплением 40 сканов на Фурье-ИК-спектрометре
билизации рН раствор нагревали до 40°С, переме-
Cary 660 FTIR (Agilent Technologies), оснащенном
шивали в течение 5-10 мин, затем охлаждали до Тк
приставкой НПВО GladiATR (PIKE Technologies).
и повторно доводили рН до требуемого значения с
Рентгенограммы образцов получали при комнат-
использованием насыщенного раствора NaOH. Затем
ной температуре с применением CuKα1,2-излуче-
приготовленный отдельно 0.0175 М раствор H6V10O28
ния в фокусирующей геометрии Брэгга-Брентано
объемом 228 мл, полученный активацией 0.02 моль
на дифрактометре TD-3700 (Tongda) в диапазо-
V2O5 с использованием 0.3 моль 30%-ного раствора
не углов 2θ = 5°-60°, шаг 0.02°, время накопле-
H2O2, прибавляли к раствору лакунарного аниона при
ния — 3 с. Для записи сигнала использовали по-
Тк. После введения H6V10O28 смесь перемешивали
зиционно-чувствительный детектор MYTHEN2
15 мин, затем нагревали до 60°С и термостатировали
(Dectris). Фазовый анализ выполняли с привлече-
в течение 10-15 мин. По истечении указанного вре-
нием баз данных ICDD PDF-2 (International Center
мени раствор охлаждали до Тк, доводили его рН до
of Diffraction Data, Powder Diffraction File) и ICSD
значения 2.0-2.5 добавлением по каплям 6 М раство-
(Inorganic Crystal Structure Database). Расчет модель-
ра HCl и разбавляли до объема 200 мл.
ной рентгенограммы Cs4PMo11VO40·хH2O (ICDD
Кислые соли составов Cs3.5H0.5PW11VO40 и
PDF-2 #00-046-0481) выполнялся с использованием
Cs4.5H0.5SiW11VO40 готовили путем частичного за-
структуры K2.7(H3O)0.3PMo12O40 [13] путем замены
мещения Н+-ионов в полученных гетерополикислотах
ионов калия на катионы цезия по аналогии с рабо-
катионами Сs+ с использованием стехиометрического
той [14]. Модельные рентгенограммы Cs4SiW12O40
количества Cs2CO3 (безв., 99.995%, Acros Organics) в
и Cs3PW12O40 рассчитывали на базе структуры
виде 0.1 М водного раствора при температуре 40°С
K2.7(H3O)0.3PMo12O40 путем замены ионов калия
[уравнение (II)]. Cs2CO3 вводили при помощи ка-
на катионы цезия, атомов Mo на W и атомов Р на
пельной воронки со скоростью 0.75 мл·мин-1, после
Si (для Cs4SiW12O40). Определение текстурных ха-
чего взвесь перемешивали при 40°С в течение 15 ч.
рактеристик осуществляли на приборе ASAP-2400
По истечении заданного времени осадок отделяли ва-
(Micromeritics) при температуре -196°C. Перед ана-
куумным фильтрованием через стеклофильтр ПОР16
лизом образцы дегазировали до остаточного давле-
(пористость 10-16 мкм), промывали несколько раз
ния ~10 Па при 150°С в течение 12 ч. Термический
дистиллированной Н2О и сушили в сушильном шка-
анализ проводили на синхронном термоанализаторе
фу при температуре 150°С в течение 2.5 ч. Синтез
STA 449 C Jupiter (NETZSCH) в интервале темпера-
Cs3.5H0.5PMo11VO40 выполняли из 0.2 М раствора
тур 30-600°С при скорости нагрева 10 град·мин-1 в
H4PMo11VO40 двумя методами. По первому мето-
потоке гелия 30 мл·мин-1. Элементный анализ вы-
ду соль получали прикапыванием 0.125 М раствора
полняли методом атомно-эмиссионной спектроме-
Cs2CO3 при температуре 40°С, по второму водные
трии с индуктивно связанной плазмой (АЭС-ИСП)
растворы гетерополикислоты и Cs2CO3 тех же кон-
на оптико-эмиссионном спектрометре Perkin Elmer
центраций перед смешением разбавляли в 2 раза с
Optima 4300 DV.
использованием этилового спирта (х.ч., 96 об%, ООО
Растворимость образцов исследовали в стеклян-
ТД «ХИММЕД», кат. номер ET00042500). В обоих
ном реакторе с рубашкой на 150 мл, оснащенном маг-
случаях после полного введения Cs2CO3 взвесь пере-
нитной мешалкой и термостатом. Гидротермальную
мешивали в течение 10 мин, затем нагрев отключали
обработку проводили при 80°С в течение 3 ч, после
Применение пероксидного метода активации ванадия для получения смешанных гетерополисоединений...
845
чего осадки отделяли фильтрованием, промывали
дистиллированной водой и сушили в сушильном
шкафу 3 ч при 150°С. Структурную стабильность
соединений после обработки контролировали мето-
дами ИК-НПВО и рентгенофазового анализа, тогда
как их растворимость оценивали методом АЭС-ИСП
по содержанию структурообразующих элементов в
маточных растворах.
Обсуждение результатов
Рассмотрение лакунарных молибден- и вольфрам-
содержащих гетерополисоединений как неорганиче-
ских лигандов для активного переходного металла, в
качестве которого выбран VV благодаря его окисли-
тельным свойствам, с введением последнего в виде
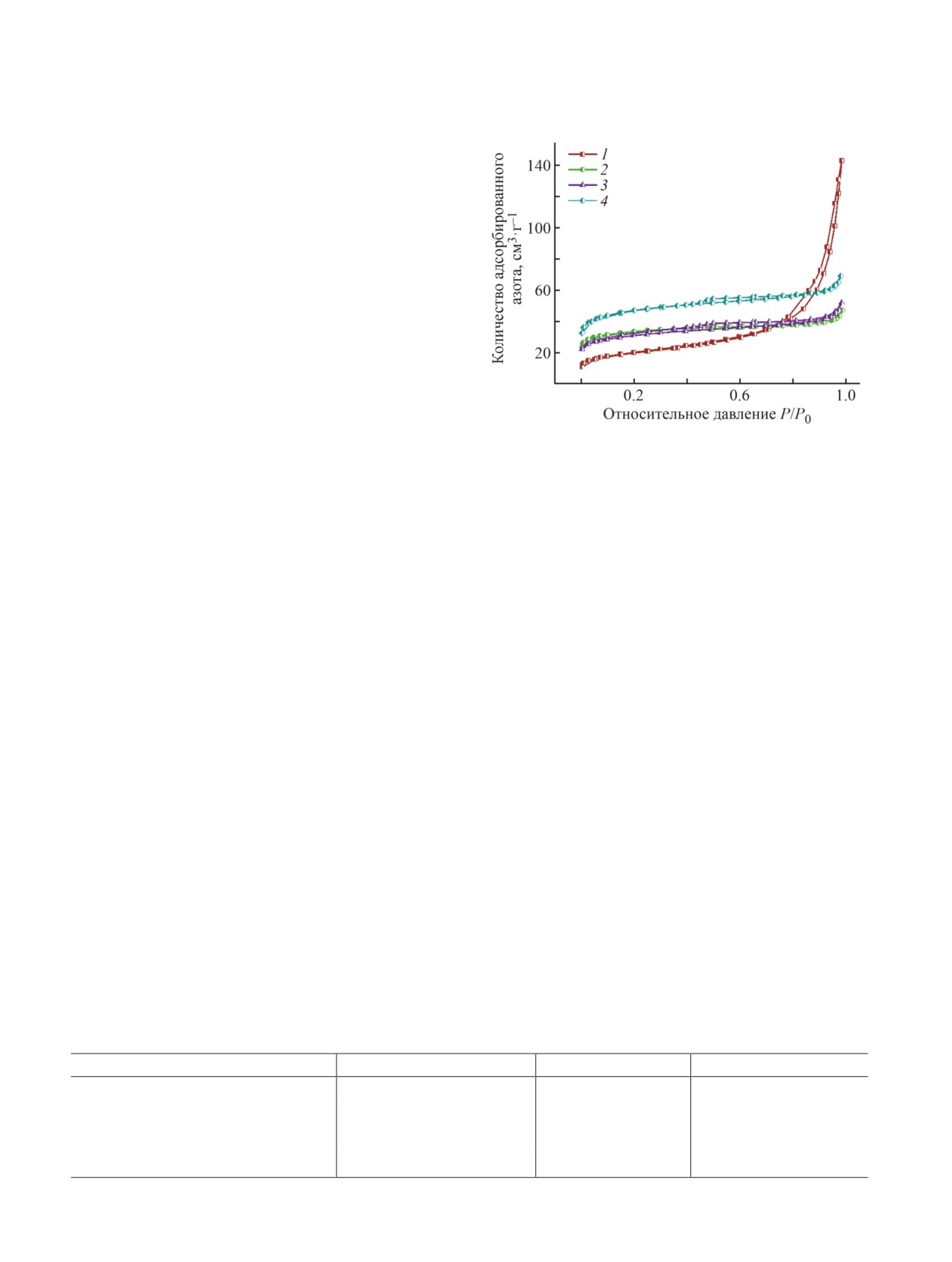
Рис. 1. Изотермы адсорбции-десорбции азота ва-
чистого раствора H6V10O28 позволило получить три
надийсодержащих гетерополисоединений: 1 —
Cs3.5H0.5PMo11VO40 (Н2О), 2 — Cs3.5H0.5PMo11VO40
раствора ванадийсодержащих гетерополисоедине-
(этиловый спирт), 3 — Cs4.5H0.5SiW11VO40, 4 —
ний, различающихся составом структурообразую-
Cs3.5H0.5PW11VO40.
щих атомов. Последующее введение Cs2CO3 в рас-
творы привело к осаждению кислых солей состава
Cs8.5-аH0.5ХМ11VO40, стехиометрия которых была
нагревании от комнатной температуры до ~150°С, по-
подтверждена с использованием элементного анали-
сле чего их масса остается практически неизменной
за. Для каждого состава получение H6V10O28 задан-
(рис. 2). Наблюдаемое на термогравиметрических
ного объема осуществлялось отдельно, что дало воз-
кривых снижение массы образцов отражается выра-
можность отработать пероксидный метод активации
женным отрицательным пиком на дифференциаль-
VV на различных количествах V2O5.
но-термогравиметрических кривых. Полное разложе-
Синтезированные соли ванадийсодержащих ге-
ние анионов синтезированных солей происходит при
терополисоединений были исследованы методом
температурах выше 500°С. Замена структурообразу-
азотной порометрии с целью определения их тек-
ющих атомов с МоVI на WVI, а также центрального
стурных характеристик (см. таблицу). Изотермы
атома Х с SiIV на РV способствует росту термостой-
адсорбции N2 на полученных соединениях (рис. 1)
кости: Cs3.5H0.5PW11VO40 > Cs4.5H0.5SiW11VO40 >
имеют вид, характерный для макропористых ма-
> Cs3.5H0.5PMo11VO40.
териалов, и относятся к типу II по классификации
Сопоставление ИК-профилей синтезированных
IUPAC [15]. Дополнительно наблюдается слабовы-
солей в области «отпечатков пальцев» аниона Кеггина
раженный капиллярно-конденсационный гистере-
с имеющимися в литературе спектрами соединений
зис, что позволяет предположить наличие мезопор
схожего состава [4, 6] и их недопированных предше-
в образцах. Использование водно-этанольного рас-
ственников — H3PMo12O40, H3PW12O40 и H4SiW12O40
твора приводит к увеличению площади поверхности
[7, 16, 17] — позволило установить, что зарегистри-
Cs3.5H0.5PMo11VO40 почти в 2 раза по сравнению с
рованные нами кривые содержат четыре выраженных
образцом, осажденным из воды.
пика поглощения, соответствующие асимметрич-
В массивном состоянии образцы претерпевают
ным валентным колебаниям P(Si)—Oa, Mo(W)—Od,
непрерывную потерю массы в интервале 2-4.5% при
Mo(W)—Ob—Mo(W) и Mo(W)—Oc—Mo(W) в анионе
Текстурные характеристики ванадийсодержащих гетерополисоединений
Образец
Площадь поверхности, м2·г-1
Объем пор, см3·г-1
Средний диаметр пор, Å
Cs3.5H0.5PMo11VO40 (Н2О)
71
0.221
124
Cs3.5H0.5PMo11VO40 (этиловый спирт)
125
0.073
23
Cs4.5H0.5SiW11VO40
113
0.08
28
Cs3.5H0.5PW11VO40
174
0.107
25
846
Родикова Ю. А. и др.
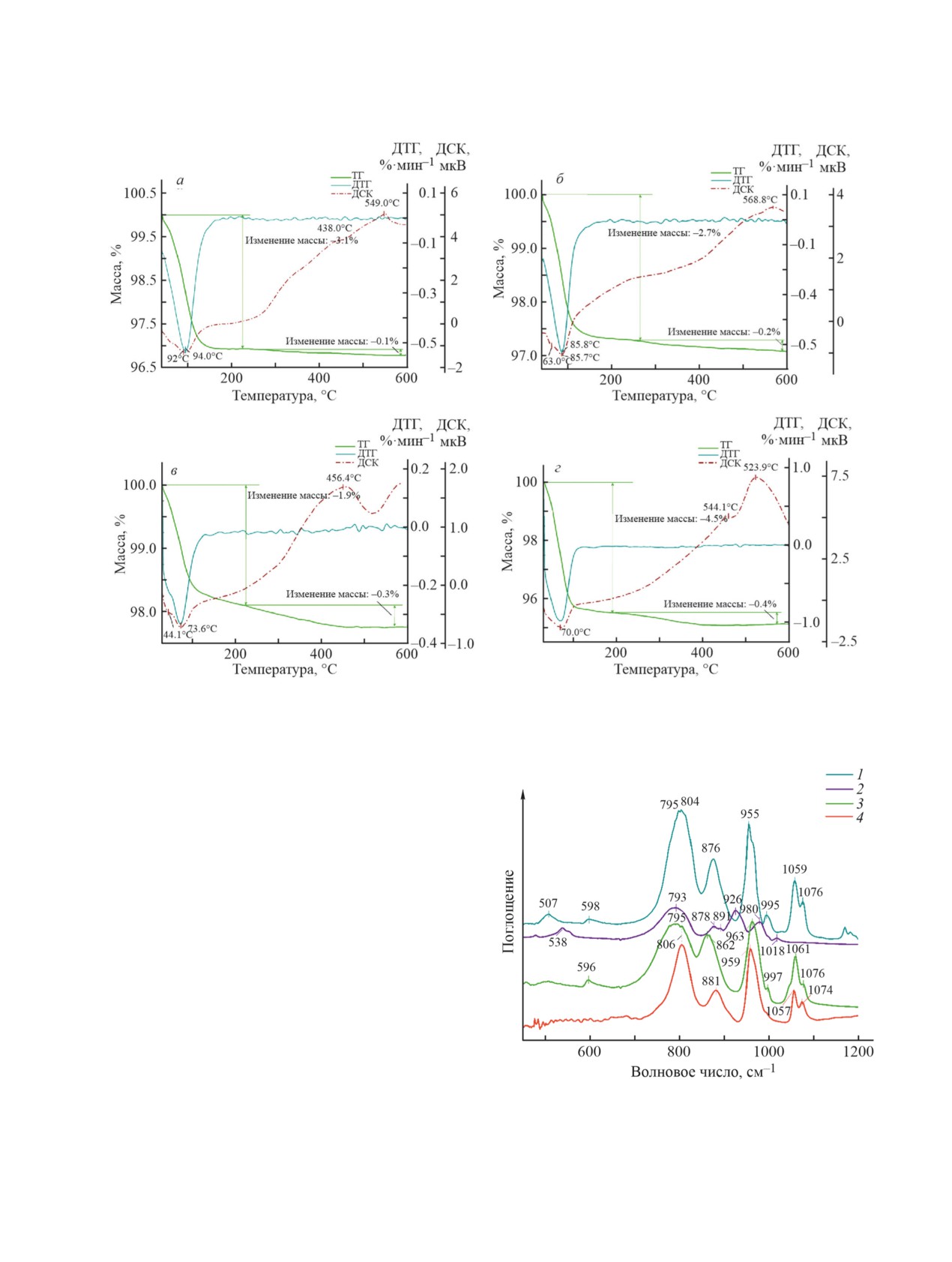
Рис. 2. Термогравиметрические (ТГ), дифференциально-термогравиметрические (ДТГ) кривые и кривые дифферен-
циальной сканирующей калориметрии (ДСК) ванадийсодержащих гетерополисоединений: а — Cs4.5H0.5SiW11VO40,
б — Cs3.5H0.5PW11VO40, в — Cs3.5H0.5PMo11VO40 (Н2О), г — Cs3.5H0.5PMo11VO40 (этиловый спирт).
структуры Кеггина (рис. 3). Сходство полученных
спектров со спектрами недопированных гетерополи-
соединений в указанной области убедительно под-
тверждает сохранение структурной целостности ани-
онов Кеггина в процессе допирования атомами VV, а
также в ходе их осаждения в виде солей. Замещение
части атомов Мо(W) атомами ванадия приводит к рас-
щеплению (образованию плеча) полосы, приписывае-
мой колебанию X—Oa—M3, в результате образования
связей M—O—V. Внедрение ванадия также отражает-
ся на спектрах изменением положения валентных ко-
лебаний νas(M—Od) по сравнению с безванадиевыми
кислотами. Наблюдаемые пики хорошо согласуются
с описанными в литературе полосами поглощения
ванадийсодержащих гетерополисоединений.
Варьирование условий синтеза солей состава
Cs3.5H0.5PMo11VO40 не оказывает влияния на фа-
Рис. 3. Инфракрасные спектры синтезированных вана-
зовый состав (рис. 4, а) (в отличие от текстурных
дийсодержащих гетерополисоединений в области «отпе-
характеристик). Оба использованных метода при-
чатков пальцев» аниона Кеггина: 1 — Cs3.5H0.5PW11VO40,
водят к однофазным изоструктурным образцам,
2 — Cs4.5H0.5SiW11VO40, 3 — Cs3.5H0.5PMo11VO40 (эти-
все линии на рентгенограммах которых соответ-
ловый спирт), 4 — H4PMo11VO40.
Применение пероксидного метода активации ванадия для получения смешанных гетерополисоединений...
847
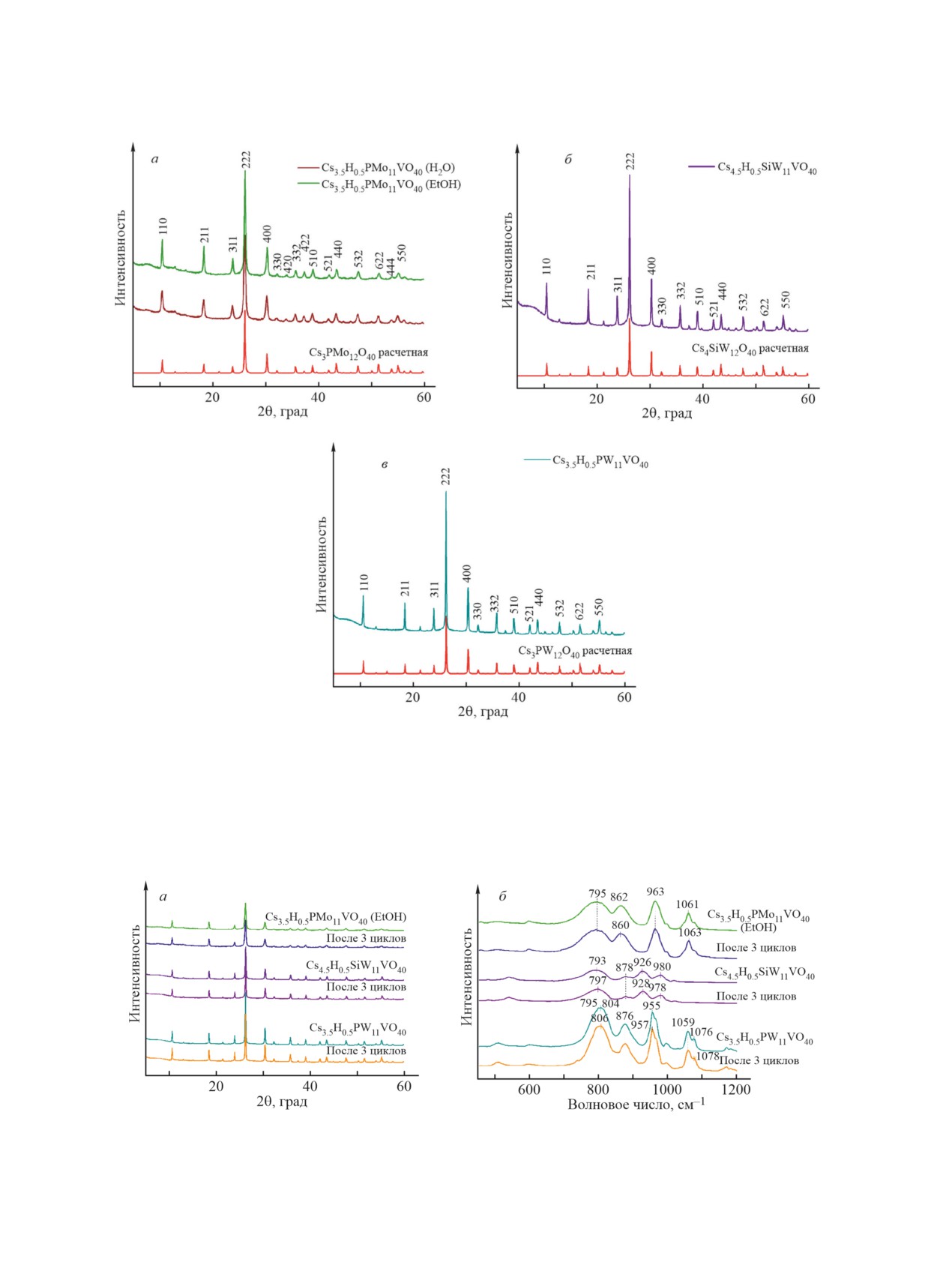
Рис. 4. Рентгенограммы образцов ванадийсодержащих гетерополисоединений: а — Cs3.5H0.5PMo11VO40, б —
Cs4.5H0.5SiW11VO40, в — Cs3.5H0.5PW11VO40.
Для основных линий приведены индексы Миллера, характеризующие расположение атомных плоскостей в кристаллах.
Рис. 5. Сопоставление рентгенограмм (а) и инфракрасных спектров (б) в области «отпечатков пальцев» аниона
Кеггина исходных солей ванадийсодержащих гетерополисоединений и образцов после трехкратной гидротермаль-
ной обработки.
848
Родикова Ю. А. и др.
ствуют фазе Cs4PMo11VO40·хH2O. Соли составов
Финансирование работы
Cs4.5H0.5SiW11VO40 (рис. 4, б) и Cs3.5H0.5PW11VO40
Работа выполнена при финансовой поддерж-
(рис. 4, в) также представляют собой однофазные
ке Российского научного фонда в рамках проекта
образцы, дифракционные картины которых соответ-
ствуют структурам Cs4SiW12O40 и Cs3PW12O40.
Сохранение структурной стабильности исследу-
емых материалов после пребывания в реакционных
Конфликт интересов
условиях является важным критерием их пригодно-
Авторы заявляют об отсутствии конфликта инте-
сти к повторному (многоцикловому) использованию в
ресов, требующего раскрытия в данной статье.
качестве катализаторов. Трехцикловая гидротермаль-
ная обработка полученных гетерополисоединений с
анализом после каждого цикла наблюдаемых измене-
Информация об авторах
ний на рентгенограммах и ИК-спектрах (рис. 5) по-
Родикова Юлия Анатольевна, к.х.н.
казала их значительную структурную устойчивость.
Растворимость соединений после каждой обработки
Кардаш Татьяна Юрьевна, к.х.н.
не превышала 0.6%.
Жижина Елена Георгиевна, д.х.н.
Выводы
С использованием метода допирования лакунар-
ных анионов синтезированы три ванадийсодержащих
Список литературы
гетерополисоединения, различающиеся составом
[1]
Woźniak Budych M. J., Staszak K., Bajek A., Pniewski F.,
металлатного каркаса. Предварительная обработка
Jastrząb R., Staszak M., Tylkowski B., Wieszczycka K.
V2O5 с использованием Н2О2 позволяет полностью
The future of polyoxymetalates for biological and
переводить предшественник в активную форму без
chemical apllications // Coord. Chem. Rev. 2023.
использования минеральных кислот, а допирование
V. 493. ID 215306.
гетерополианионов образующимся раствором обе-
спечивает снижение содержания примесных ионов
[2]
Heravi M. M., Bamoharram F. F. Heteropolyacids as
highly efficient and green catalysts applied in organic
при формировании смешанных гетерополисоеди-
transformations. Elsevier, 2022. P. 141-264.
нений. Замещение протонов в растворах катионами
Cs+ при соотношении 7/1 для Р-содержащих и 9/1
[3]
Odyakov V. F., Zhizhina E. G., Rodikova Y. A.,
для Si-содержащих монованадиевых гетерополи-
Gogin L. L. Mo-V-Phosphoric heteropoly acids and their
кислот приводит к осаждению их кислых солей без
salts: Aqueous solution preparation - challenges and
выпадения индивидуальных фаз структурообразу-
perspectives // Eur. J. Inorg. Chem. 2015. V. 2015. N 22.
ющих элементов. Анализ рентгенограмм и инфра-
красных спектров полученных в работе соединений
[4]
Liao X., Wu D., Geng B., Lu S., Yao Y. Deep oxidative
подтверждает образование анионов со структурой
desulfurization catalyzed by (NH4)xH4-xPMo11VO40
Кеггина и внедрение в них VV при проведении синте-
(x = 1, 2, 3, 4) using O2 as an oxidant // RSC Adv. 2017.
за с использованием пероксидного подхода. Переход
V. 7. P. 48454-48460.
от незамещенных монованадиевых гетерополикислот
к их Сs+-содержащим солям вызывает увеличение
[5]
Zhou L., Wang L., Zhang S., Yan R., Diao Y. Effect of
vanadyl species in Keggin-type heteropoly catalysts in
термической стабильности последних, в то время как
selective oxidation of methacrolein to methacrylic acid
внедрение VV в каркас оказывает противоположный
// J. Catal. 2015. V. 329. P. 431-440.
эффект по сравнению с безванадиевыми гетерополи-
соединениями из-за снижения симметрии анионов
[6]
Huang T., Tian N., Wu Q., Yan Y., Yan W. Synthesis,
Кеггина. Замена структурообразующих атомов с Мо
crystal structure and conductive mechanism of solid
на W, а также центрального атома с Si на Р способ-
high-proton conductor tungstovanadosilicic heteropoly
ствует росту термостойкости и увеличению площади
acid // Mater. Chem. Phys. 2015. V. 165. P. 34-38.
поверхности Сs+ солей. В ходе трехкратной гидротер-
мальной обработки доказаны низкая растворимость в
[7]
Vilanculo C. B., da Silva M. J., Rodrigues A. A.,
воде и высокая структурная стабильность приготов-
Ferreira S. O., da Silva R. C. Vanadium-doped sodium
ленных ванадийсодержащих гетерополисоединений.
phosphomolybdate salts as catalysts in the terpene
Применение пероксидного метода активации ванадия для получения смешанных гетерополисоединений...
849
alcohols oxidation with hydrogen peroxide // RSC
[13]
Boeyens J. C. A., McDougal G. J., Smit J. van R.
Adv. 2021. V. 11. P. 24072-24085.
Crystallographic study of the ammonium/potassium
12-molybdophosphate ion-exchange system // J. Solid
[8]
Zhang J., Tang Y., Li G., Hu C. Room temperature
State Chem. 1976. V. 18. N 2. P. 191-199. ICSD #210.
direct oxidation of benzene to phenol using hydrogen
peroxide in the presence of vanadium-substituted
[14]
Berndt S., Herein D., Zemlin F., Beckmann E.,
heteropolymolybdates // Appl. Catal. A: General.
Weinberg G., Schütze J., Mestl G., Schlögl R. A new
2005. V. 278. P. 251-261.
unifying structural model of heteropolymolybdate
salts: Microstructure and thermal stability of a series
[9]
Kozhevnikov I. V. Catalysts for fine chemical synthesis.
of molecular oxides // Ber. Bunsen. Phys. Chem. 1998.
V. 2. Catalysis by polyoxometalates. Chichester: John
V. 102. N 5. P. 763-774.
Wiley & Sons Ltd, 2002. P. 64.
[10]
Одяков В. Ф., Жижина Е. Г. Новый способ синтеза
[15]
Thommes M., Kaneko K., Neimark A. V., Oliver J. P.,
водных растворов Mo-V-фосфорных гетерополи-
Rodriquez-Reinoso F., Rouquerol J., Sing K. S. W.
кислот // ЖНХ. 2009. Т. 54. № 3. С. 409-414.
Physisorption of gases, with special reference to the
https://www.elibrary.ru/JWITUB
evaluation of surface area and pore size distribution
[Odyakov V. F., Zhizhina E. G. New process for
(IUPAC Technical Report) // Pure Appl. Chem. 2015.
preparing aqueous solutions of Mo-V-phosphoric
V. 87. N 9-10. P. 1051-1069.
heteropoly acids // Russ. J. Inorg. Chem. 2009. V. 54.
N 3. P. 361-367.
[16]
da Silva M. J., Rodrigues A. A., Gonçalves
Lopes N. P. Cesium heteropolyacid salts: Synthesis,
[11]
Domaille P. J., Hervéa G., Téazéa A. Vanadium(V)
characterization and activity of the solid and versatile
substituted dodecatungstophosphates // Inorg. Synth.
heterogeneous catalysts // Chemistry. 2023. V. 5. N 1.
1990. V. 27. P. 96-104.
[17]
Biela´nski A., Datka J., Gil B., Małecka-Luba´nska A.,
[12]
Téazéa A., Hervéa G., Finke R. G., Lyon D. K. α-,
Micek-Ilnicka A. FTIR study of hydration of
β-, and γ-Dodecatungstosilicic acids: Isomers and
dodecatungstosilicic acid // Catal. Lett. 1999. V. 57.
related lacunary compounds // Inorg. Synth. 1990. V.
P. 61-64.
27. P. 85-96.