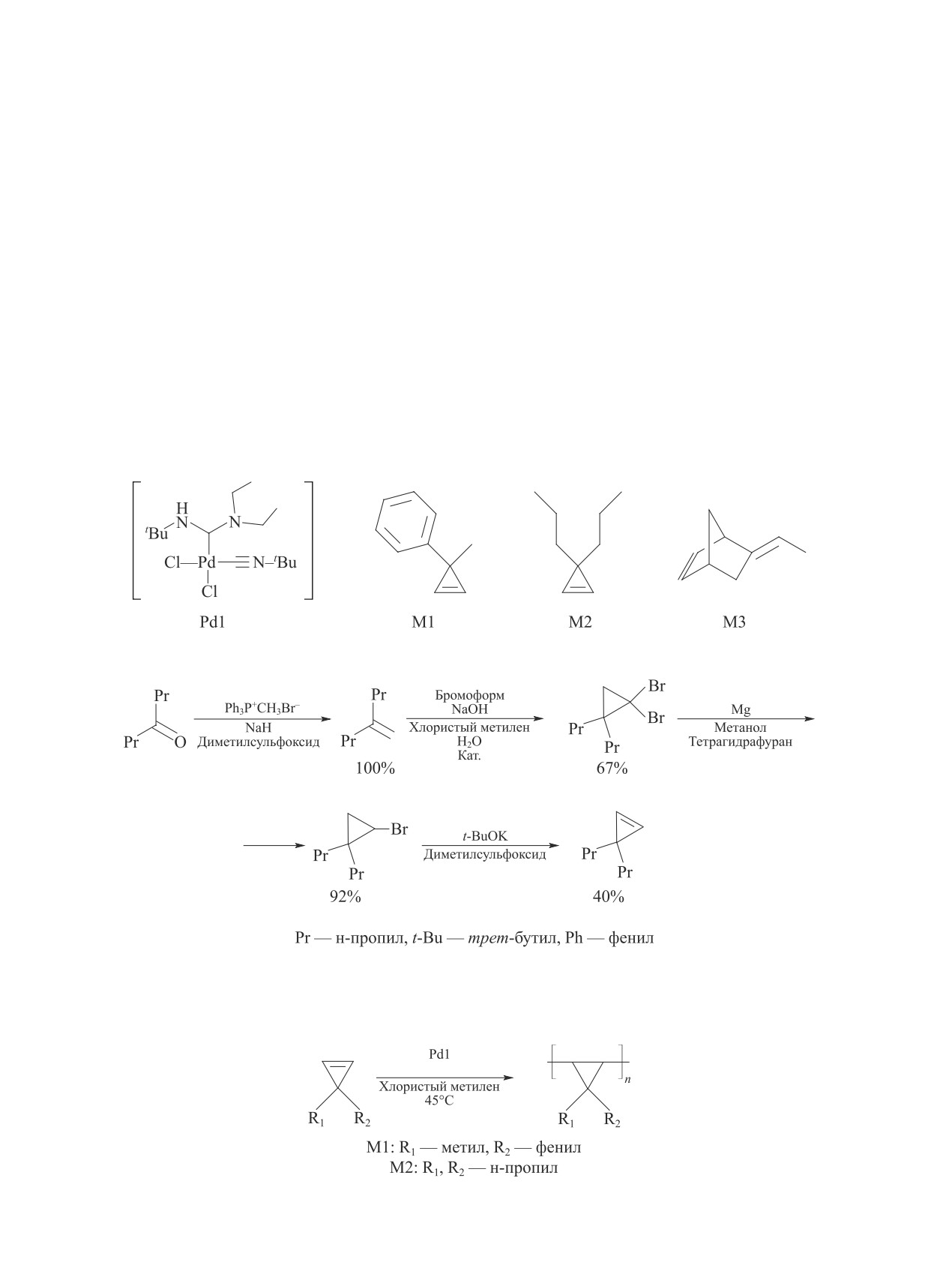
Аддитивная полимеризация 3,3-дизамещенных циклопропенов в присутствии палладиевого комплекса...
965
Журнал прикладной химии. 2023. Т. 96. Вып. 12
УДК 547.514.72
АДДИТИВНАЯ ПОЛИМЕРИЗАЦИЯ 3,3-ДИЗАМЕЩЕННЫХ ЦИКЛОПРОПЕНОВ
В ПРИСУТСТВИИ ПАЛЛАДИЕВОГО КОМПЛЕКСА, СОДЕРЖАЩЕГО
АЦИКЛИЧЕСКИЙ ДИАМИНОКАРБЕНОВЫЙ ЛИГАНД
© Е. И. Меденцева1, А. П. Хрычикова1, Е. В. Бермешева1,
К. В. Потапов2, М. В. Бермешев1,*
1 Институт нефтехимического синтеза им. А. В. Топчиева РАН (ИНХС РАН),
19991, ГСП-1, г. Москва, Ленинский пр., д. 29, стр. 2
2 Институт органической химии им. Н. Д. Зелинского РАН (ИОХ РАН),
119991, г. Москва, Ленинский пр., д. 47
Поступила в Редакцию 27 июня 2023 г.
После доработки 29 декабря 2023 г.
Принята к публикации 29 декабря 2023 г.
Исследована аддитивная полимеризация 3-метил-3-фенилциклопропена-1 и 3,3-ди(н-пропил)цикло-
пропена-1 в присутствии палладиевого комплекса, содержащего ациклический диаминокарбеновый
лиганд. Показано, что такие комплексы при активации органоборатом (Na+[B(3,5-(CF3)2C6H3)4]-)
катализируют аддитивную полимеризацию замещенных циклопропенов. Полимеризация протекает
селективно, без разрушения циклопропанового кольца. На основании результатов исследования про-
цесса сополимеризации 3,3-ди(н-пропил)циклопропена с мономером норборненового ряда (5-этили-
ден-2-норборненом), протекание которого отслеживали методом спектроскопии ядерно-магнитного
резонанса (ЯМР) по уменьшению характеристических сигналов соответствующих мономеров в спек-
тре 1H ЯМР, установлено, что замещенные циклопропены являются более активными мономерами в
аддитивной полимеризации, чем норборнены. Синтезированные аддитивные гомополимеры на основе
3-метил-3-фенилциклопропена-1 и 3,3-ди(н-пропил)циклопропена-1 охарактеризованы методами диф-
ференциальной сканирующей калориметрии, термогравиметрического и рентгенофазового анализа.
Ключевые слова: аддитивная полимеризация; циклопропен; 5-этилиден-2-норборнен; комплексы пал-
ладия; диаминокарбеновый лиганд
DOI: 10.31857/S0044461823120046; EDN: KTMDJE
Аддитивные полимеры на основе напряженных
ции ограничено норборненовыми структурами (см.,
циклоолефинов, как правило, обладают высокими
например, [2-4]), тогда как существуют и другие
температурой стеклования, термо- и хемостабиль-
коммерчески доступные мономеры с напряженным
ностью, а также жесткими основными цепями [1],
циклом. Одним из примеров таких циклоолефинов
что делает их перспективными материалами для
является циклопропен. В настоящее время аддитив-
применения в качестве мембранных материалов
ная полимеризация циклопропенов изучена весьма
для газоразделения и первапорации, сорбентов для
незначительно [5-7]. Кроме того, в данных работах
транспортировки и хранения газов и материалов для
не удалось подобрать эффективные каталитические
микро- и оптоэлектроники. Ключевыми факторами,
системы, при использовании которых можно было
определяющими выбор производного циклоолефина
бы получить полимерные продукты с молекулярными
в качестве мономера, являются коммерческая до-
массами, достаточными для дальнейшего изучения
ступность и полимеризационная активность, завися-
механических и газотранспортных свойств поли-
щая от напряженности цикла. На сегодняшний день
циклопропенов. При этом с учетом высокой реак-
большинство примеров по аддитивной полимериза-
ционной способности циклопропенового кольца в
966
Меденцева Е. И. и др.
полимеризации ввиду большой напряженности цикла
2-451-11), метилтрифенилфосфоний бромид (98%,
требуется поиск каталитических систем, которые по-
Merck, кат. номер 130079), 4-гептанон (98%, Merck,
зволяли бы не просто вовлекать данные мономеры в
кат. номер 101745), тетрагидрофуран [чистота ВЭЖХ
полимеризацию с получением высокомолекулярных
(>99.9%), Panreac, кат. номер 361736], HgCl2 (98%,
продуктов, но катализировали бы именно селектив-
Merck, кат. номер 413445), NH4Cl (ч.д.а., ООО «АО
ную реакцию по кратным связям с сохранением ци-
РЕАХИМ», кат. номер 010316), цетилтриметиламмо-
клопропанового кольца.
ний бромид (гексадецилтриметиламмоний бромид,
Ранее было показано, что в аддитивной полиме-
>99%, Acros Organics, кат. номер 22716-0100), бромо-
ризации циклоолефинов каталитические системы на
форм (ч., АО «ЛенРеактив», кат. номер 181245), NaCl
основе палладиевых комплексов с N-гетероцикли-
(ч., ООО «Компонент-Реактив», кат. номер 2-245-10),
ческими карбеновыми лигандами проявляют высо-
MgSO4·7H2O (х.ч., ООО «АО РЕАХИМ», кат. номер
кую активность, катализируют полимеризацию мо-
120054), Mg (х.ч., ООО «Компонент-Реактив», кат.
номеров с различными функциональными группами
номер 3-303-10), трет-бутилат калия (≥98.0%, Merck,
селективно лишь по эндоциклической двойной связи
кат. номер 804918), изо-пропанол [чистота ВЭЖХ
и не чувствительны к кислороду воздуха и следам во-
(>99.9%), Panreac, кат. номер 361090], трет-бутанол
ды [3, 8-10], а активность этих систем определяется
(≥99.5%, Merck, кат. номер 471712), Na2SO4 (х.ч., АО
структурой карбенового лиганда. В работе [11] обна-
«ЛенРеактив», кат. номер 130246), н-пентан (ч.д.а.,
ружен новый тип каталитических систем, содержа-
ООО «Компонент-Реактив», кат. номер 1-711-15),
щих родственные, ациклические диаминокарбеновые
трициклогексилфосфин (>98%, ABCR GmbH, кат.
лиганды, для аддитивной полимеризации норборне-
номер 264139), 4-гептанон (98%, Acros Organics, кат.
нов. Данные комплексы Pd при активации борорга-
номер 14655-5000), н-гексан (х.ч., ООО «Компонент-
ническими соединениями катализируют аддитивную
Реактив», кат. номер 2-008-06) использовали без до-
полимеризацию алкилзамещенных норборненов с
полнительной очистки. Палладиевый комплекс, со-
образованием высокомолекулярных растворимых
держащий ациклический диаминокарбеновый лиганд
продуктов. В связи с вышесказанным представляется
[Pd1 (I)], синтезирован по ранее описанной методике
актуальным, с одной стороны, дальнейшая оценка
[13]. трет-Бутил изоцианид (97%, Acros Organics,
возможностей в качестве катализаторов нового ти-
кат. номер 403600010), PdCl2 (59% Pd, Acros Organics,
па систем на основе Pd-комплексов, содержащих
кат. номер 195200050). Трет-бутил изоцианид (97%,
ациклические диаминокарбеновые лиганды, и, с дру-
Acros Organics, кат. номер 403600010), PdCl2 (59% Pd,
гой — синтез и исследование свойств аддитивных
Acros Organics, кат. номер 195200050) использовали
полимеров замещенных циклопропенов.
без дополнительной очистки, диэтиламин (≥99.0%,
Цель работы — установить возможность прове-
Alfa Aesar, кат. номер A11716.AE, Ткип = 56-57°С)
дения аддитивной полимеризации замещенных ци-
кипятили над CaH2 в токе аргона 5 ч и перегоня-
клопропенов в присутствии каталитической систе-
ли, ацетонитрил (чистота ВЭЖХ (>99.9%), ООО
мы на основе палладиевого комплекса, содержащего
ТД «Химмед») абсолютизировали на установке для
ациклический диаминокарбеновый лиганд, а также
очистки растворителей SPS-7 (MBraun).
оценить активность используемой каталитической
Конверсия мономеров в аддитивной полиме-
системы в данной реакции и охарактеризовать полу-
ризации контролировалась с помощью 1Н ЯМР-
ченные полимерные продукты.
спектроскопии.
Для регистрации спектров ЯМР использо-
вали CDCl3 (99.96%, Sigma-Aldrich, кат. номер
Экспериментальная часть
212-742-4). Спектры ЯМР мономеров и промежу-
3-Метил-3-фенилциклопропен-1 (М1) син-
точных соединений в их синтезе регистрирова-
тезировали по ранее описанной методике [12].
ли на ЯМР-спектрометре Fourier 300 HD, Bruker
Хлористый метилен [чистота ВЭЖХ (>99.9%), ООО
Corporation (300 МГц) при частоте 300.1 МГц для 1H
ТД «Химмед», Ткип = 40-41°С] кипятили над CaH2
ЯМР-спектров и 75.5 МГц для 13С ЯМР-спектров.
(96%, кат. номер UN 1404) в токе аргона (99.998%,
Спектры ЯМР полимеров регистрировали на ЯМР-
ООО «Аргон») 5 ч и перегоняли. Хлороформ (х.ч.,
спектрометре Bruker AVANCE III HD (400 МГц) с
ООО ТД «Химмед», Ткип = 61-62°С) кипятили над
рабочей частотой 400.1 и 100.6 МГц для спектров
CaH2 в токе аргона 5 ч и перегоняли. NaH (95%, ООО
1Н и 13С ЯМР соответственно. Химический сдвиг
ТД «Химмед», кат. номер 22344-1), диметилсульф-
определяли относительно сигнала остаточного про-
оксид (х.ч., ООО «Компонент-Реактив», кат. номер
тона хлороформа (7.24 м. д. для спектров 1Н ЯМР) и
Аддитивная полимеризация 3,3-дизамещенных циклопропенов в присутствии палладиевого комплекса...
967
атома углерода хлороформа (77.00 м. д. для спектров
дисперсии NaH (60% в минеральном масле) и 86 г
13С ЯМР).
метилтрифенилфосфоний бромида. Суспензию на-
Хроматомасс-спектрометрический анализ прово-
грели до 60°С и выдержали при перемешивании до
дили на газохроматомасс-спектрометре MAT 95 XL
прекращения выделения газа (~2 ч). Смесь охладили
(Finnigan) с хроматографом HP 6890+ (Agilent).
до комнатной температуры и добавили по каплям 25 г
Режим и характеристики масс-спектрометра: элек-
4-гептанона (экзотермическая реакция). Через 10 мин
тронная ионизация (энергия ионизации 70 эВ), ди-
реакционную массу снова нагрели до 60°С и переме-
апазон масс 20-800 а. е. м., разрешение 1000, тем-
шивали 3 ч. Не убирая нагрев, отогнали полученный
пература источника 200°С, скорость сканирования
продукт в вакууме (14 мм рт. ст.) в ловушку, охлаждае-
1 с/декада масс. Режим и характеристики хроматогра-
мую жидким азотом. Продукт получен в виде бесцвет-
фа: капиллярная колонка 30 м × 0.25 мм с фазой DB-5
ной жидкости, 25 г, выход 100% (примесь ~12 мол%
(полидиметилсилоксан, содержащий 5% фениль-
бензола из коммерческого фосфоний бромида).
ных групп); газ-носитель — He (чистота 99.995%,
1H ЯМР (CDCl3, δ, м. д.): 4.70 с (2H), 2.05-1.98 м
ООО «НИИ КМ»), деление потока 1:30; скорость
(4H), 1.53-1.34 м (4H), 0.90 т (3J = 7.3 Гц, 6H). 13C
подъема температуры 5 град·мин-1 от 30 до 120°С,
ЯМР (CDCl3, δ, м. д.): 150.0, 108.8, 38.4, 21.1, 14.0.
10 град·мин-1 от 120 до 270°С, далее выдержка при
Синтез 1,1-дибром-2,2-дипропилциклопропана.
270°С в течение 10 мин.
К 66.8 мл водного 10 М раствора NaOH при комнат-
ИК-спектры регистрировали с помощью IFS-66-v/s
ной температуре добавили раствор 18.7 г 4-метилен-
Фурье-спектрометра (Bruker) методом нарушенного
гептана в 7.5 мл хлористого метилена и 7.3 г цетил-
полного внутреннего отражения. Регистрацию про-
триметиламмоний бромида. К полученной системе
водили на кристалле из ZnSe в диапазоне от 4000
при сильном перемешивании по каплям добавили
до 600 см-1, разрешение 2 см-1, количество сканов
раствор 84.5 г бромоформа в 35 мл хлористого мети-
поглощения 15.
лена. Смесь активно перемешивали 8 ч при комнат-
Калориметрические исследования выполняли
ной температуре, после чего слои разделили. Водный
на дифференциальном сканирующем калориметре
слой экстрагировали хлористым метиленом. Все ор-
ТА-4000 (Mettler) с ячейкой DSC-30 при скорости
ганические слои объединили, промыли насыщен-
повышения температуры 20 град·мин-1 в атмосфере
ным (~26%) раствором NaCl, высушили над MgSO4
аргона. Термогравиметрический анализ производили
и упарили на роторном испарителе. Полученную
с помощью прибора Perkin-Elmer TGA-7 при скоро-
полукристаллическую смесь растворили в хлори-
сти повышения температуры 10 град·мин-1.
стом метилене и упарили с добавлением силикаге-
Рентгенографические измерения осуществляли на
ля. Силикагель с нанесенным веществом поместили
дифрактометре ДРОН-3М (АО «ИЦ «Буревестник») в
в экстрактор Сокслета и промывали гексаном 3 ч.
режиме регистрации пропускаемого излучения (асим-
Раствор охладили до комнатной температуры и упа-
метричный, фокусирующий на детектор, кварцевый
рили на роторном испарителе. Продукт перегнали в
монохроматор на первичном пучке). Использовали
вакууме (65-70°С/6 мм рт. ст.). Продукт получен в
CuKα-излучение. Сканирование дифракционной кар-
виде бесцветной жидкости, 31.8 г, выход 67%.
тины проводили в «пошаговом режиме» с шагом
1H ЯМР (CDCl3, δ, м. д.): 1.72-1.30 м (8H), 1.37 с
∆2θ = 0.04° и временем накопления τ = 10 с. Длина
(2H), 0.94 т (3J = 7.1 Гц, 6H). 13C ЯМР (CDCl3, δ,
волны 0.154 нм.
м. д.): 40.0, 37.0, 34.2, 32.9, 19.5, 14.1.
Молекулярные массы определяли методом гель--
Синтез 2-бром-1,1-ди(н-пропил)циклопропана.
проникающей хроматографии на хроматографе вы-
В четырехгорлую колбу, снабженную механиче-
сокого давления Waters, оснащенном рефрактоме-
ской мешалкой, двумя обратными холодильниками
трическим детектором (Chromatopack Microgel-5;
и капельной воронкой, поместили 19 г магниевой
элюент — хлороформ; скорость потока 1 мл·мин-1,
стружки и 30 мг 0.1%-ного водного раствора HgCl2.
объем пробы 200 мкл, концентрация образцов
К смеси добавили 160 мл сухого тетрагидрофурана,
1 мг·мл-1) по рефрактометрическому детектору.
смесь нагрели до кипения и выдержали при переме-
Молекулярные массы рассчитывали по стандарт-
шивании 5 мин для активации магния. В кипящий
ной методике относительно стандартных образцов
тетрагидрофуран добавили в одну порцию раствора
монодисперсного полистирола (Agilent, кат. номер
31.8 г 1,1-дибром-2,2-дипропилциклопропана в 21 мл
PL2010-0105).
метанола, после чего смесь кипятили еще 30 мин.
Синтез 4-метиленгептана. К 250 мл сухого диме-
Затем систему охладили до комнатной температуры
тилсульфоксида в атмосфере аргона добавили 10.5 г
и нейтрализовали водой (35 мл). Перемешивали полу-
968
Меденцева Е. И. и др.
ченную систему 10 мин. Жидкую часть перенесли в
ской системе. Готовили раствор комплекса Pd1 (I)
делительную воронку, промыли насыщенным (~28%)
концентрацией 0.05 М путем растворения 10.0 мг
водным раствором NH4Cl. Водный слой экстрагиро-
Pd1 (I) в 0.48 мл хлористого метилена и отдельно
вали диэтиловым эфиром. Все органические фракции
раствор сокатализатора концентрацией 0.04 М путем
объединили, промыли насыщенным (~26%) водным
растворения 20 мг тетракис[3,5-бис(трифторметил)-
раствором NaCl, сушили над MgSO4 и упарили на
фенил]бората натрия (NaBARF) в 0.56 мл хлористого
роторном испарителе. Продукт перегнали в вакууме
метилена. Все компоненты смешивали в количествах,
(68-70°С/14 мм рт. ст.). Продукт получен в виде бес-
соответствующих мольным соотношениям компо-
цветной жидкости, 21.1 г, выход 92%.
нентов в каталитической системе Pd1/NaBARF = 1:3,
1H ЯМР (CDCl3, δ, м. д.): 2.83 д.д (J = 7.7, 4.3 Гц,
т. е. 0.15 мл 0.05 М раствора Pd1 смешивали с 0.56 мл
1H), 1.60-1.10 м (8H), 1.02-0.83 м (7H), 0.65-0.55 м
0.04 М раствора NaBARF. Полученную смесь выдер-
(1H). 13C ЯМР (CDCl3, δ, м. д.): 37.5, 35.3, 30.1, 24.6,
живали в ультразвуковой бане в течение 20 мин, затем
21.9, 19.4, 19.2, 14.3, 14.2.
фильтровали через тефлоновый фильтр с размером
Синтез 3,3-ди(н-пропил)циклопроп-1-ена. В трех-
пор 0.2 мкм. В стеклянную виалу последовательно
горлую колбу с капельной воронкой и длинным деф-
загружали 0.1 г 3-метил-3-фенилциклопропена-1.
легматором (~35 см) с отводом на ловушку, охла-
Мономер нагревали до 45°С. Затем к мономеру до-
ждаемую в системе сухой лед (ООО «Технологии
бавляли 0.37 мл раствора каталитической смеси в
Холодовой Цепи»)/изо-пропанол (сухой лед добавлял-
хлористом метилене, мольные соотношения ком-
ся с течением времени в количестве, необходимом для
понентов в реакционной массе M1/Pd1/NaBARF =
поддержания температуры изо-пропанола -78.5°С,
= 200/1/3. Реакционную массу интенсивно переме-
которую контролировали по термометру), в атмо-
шивали 10 с и оставляли при 45°С в течение 45 ч.
сфере аргона поместили 17.4 г трет-бутилата калия
Реакционную массу выливали в стакан, наполненный
и 90 мл свежеперегнанного сухого диметилсульфок-
метанолом, полимер отделяли и сушили в вакууме в
сида. Суспензию нагрели до 50°С и выдержали до
течение 3 ч до постоянной массы. Полимер переоса-
полного растворения осадка (5 мин). Систему дега-
ждали из раствора в хлороформе метанолом и снова
зировали при давлении 15-18 мм рт. ст., после чего
сушили в вакууме, процедуру повторяли дважды.
через капельную воронку в колбу медленно добавили
Выделенный полимер [поли(M1)] представлял собой
раствор 21.1 г 2-бром-1,1-дипропилциклопропана
белый твердый порошок. Выход 6%.
в 20 мл диметилсульфоксида. Продукт образуется
Аддитивная полимеризация 3-метил-3-фенилци-
немедленно и отгоняется в приемник (температура
клопроп-1-ена на трехкомпонентной каталитической
кипения продукта ~15°С). После добавления всего
системе. Готовили раствор палладиевого комплекса
исходного вещества и прекращения отгонки продукта
концентрацией 0.05 М путем растворения 20 мг Pd1
реакционную массу нагрели до 65°С и выдержали до
в 0.96 мл хлористого метилена и отдельно раствор
прекращения кипения системы. После этого нагрев
сокатализатора NaBARF концентрацией 0.04 М пу-
убрали, реакционную массу охладили до комнатной
тем растворения 80 мг NaBARF в 2.26 мл хлористого
температуры и систему заполнили аргоном. Смесь
метилена, а также раствор фосфина концентрацией
из ловушки, содержащую кроме продукта трет-бу-
0.05 М путем растворения 25 мг трициклогексил-
танол и диметилсульфоксид, перелили в делитель-
фосфина (PCy3) в 1.79 мл хлористого метилена. Все
ную воронку, разбавили пентаном и промыли водой.
компоненты смешивали в количествах, соответству-
Водный слой экстрагировали пентаном, после чего
ющих мольным соотношениям компонентов в ката-
все органические фракции объединили и высушили
литической системе Pd1/NaBARF/PCy3 = 1/3/2, т. е.
над Na2SO4 в холодильной камере. Пентан отогнали
0.60 мл 0.05 М раствора Pd1 смешивали с 2.26 мл
при атмосферном давлении. Далее продукт перегнали
0.04 М раствора NaBARF и 1.20 мл 0.05 М раствора
в вакууме (61-65°С/73 мм рт. ст.). Продукт получен в
трициклогексилфосфина. Полученную смесь выдер-
виде бесцветной жидкости, 5.1 г, выход 40%.
живали в ультразвуковой бане в течение 20 мин, затем
1H ЯМР (CDCl3, δ, м. д.): 7.28 с (2H), 1.47-1.35 м
фильтровали через тефлоновый фильтр с размером
(4H), 1.18-1.00 м (4H), 0.83 т (3J = 7.2 Гц, 6H). 13C
пор 0.2 мкм. В стеклянную виалу последовательно
ЯМР (CDCl3, δ, м. д.): 120.0, 41.1, 24.6, 20.3, 14.3.
загружали 0.6 г 3-метил-3-фенилциклопропена-1.
Масс-спектр (электронная ионизация): 124 (0.2%,
Мономер нагревали до 45°С. Затем к мономеру до-
M+•), 136 (100%, С6Н9).
бавляли 3.11 мл раствора каталитической смеси в
Аддитивная полимеризация 3-метил-3-фенилци-
хлористом метилене, мольные соотношения ком-
клопроп-1-ена на двухкомпонентной каталитиче-
понентов в реакционной массе M1/Pd1/NaBARF/
Аддитивная полимеризация 3,3-дизамещенных циклопропенов в присутствии палладиевого комплекса...
969
PCy3 = 200/1/3/2. Реакционную массу интенсивно пе-
Обсуждение результатов
ремешивали 10 с и оставляли при 45°С в течение 45 ч.
Реакционную массу выливали в стакан, наполненный
Данная работа является пилотным исследованием
метанолом, полимер отделяли и сушили в вакууме в
полимеризации замещенных циклопропенов в при-
течение 3 ч до постоянной массы. Полимер переоса-
сутствии Pd-комплексов, содержащих ациклические
ждали из раствора в хлороформе метанолом и снова
диаминокарбеновые лиганды, поэтому на этом этапе
сушили в вакууме, процедуру повторяли дважды.
исследований в качестве мономеров были выбра-
Выделенный полимер [поли(M1)] представлял собой
ны циклопропены с инертными углеводородными
белый твердый порошок. Выход 34%, Mn = 3.5·103,
группами: 3-метил-3-фенилциклопропен-1 (М1)
Mw/Mn = 1.6. 1H ЯМР (CDCl3, δ, м. д.): 7.80-6.30 м
и 3,3-ди(н-пропил)циклопропен-1 (М2). Мономер
(5H), 2.25-0.50 м (5H). 13C ЯМР (CDCl3, δ, м. д.):
М2 синтезирован на основе ди(н-пропил)кетона с
146.2-140.0 м, 137.5-122.5 м, 37.5-22.0 м, 18.5-
выходом 40% (II). Строение и чистота полученных
15.0 м. ИК (ATR, см-1): 3054, 3022, 2951, 1027, 762.
мономеров были подтверждены методами 1Н и 13С
Аддитивный полимер 3,3-ди(н-пропил)цикло-
ЯМР-спектроскопии, а также газожидкостной хро-
проп-1-ена. 1H ЯМР (CDCl3, δ, м. д.): 2.45-1.65 м
матографии.
(2H), 1.60-0.60 м (14H).
(I)
(II)
Аддитивная полимеризация синтезированных ци- Pd-комплекса Pd1 (I), содержащего ациклический
клопропенов М1 и М2 была проведена в присутствии диаминокарбеновый лиганд (III).
(III)
970
Меденцева Е. И. и др.
Комплекс Pd1 без введения сокатализатора —
аддитивных гомополимеров М1 и М2 подтверждены
органобората (NaBARF) не катализировал полиме-
с помощью спектроскопии ЯМР 1H и 13С, а также
ризацию М1 и М2. Активация данного комплекса
ИК-спектроскопии. На основании данных спектро-
NaBARF в количестве трех эквивалентов по отноше-
скопии ЯМР 1H и 13С удалось показать, что полиме-
нию к Pd привела к развитию активности: исследо-
ризация исследованных циклопропенов протекает
ванные мономеры были вовлечены в полимеризацию
селективно, и напряженный трехчленный цикл не
на каталитической системе Pd1/NaBARF. Однако
разрушается в процессе полимеризации.
выходы соответствующих полимеров были низкими
Судить о реакционной способности циклопропена
(табл. 1), что скорее всего связано с низкой устой-
и родственных циклоолефиновых мономеров — про-
чивостью каталитической системы, поскольку спу-
изводных норборнена на основании результатов адди-
стя 1 ч в реакционной смеси наблюдались частицы
тивной гомополимеризации не всегда корректно из-за
обнуленного палладия. Введение в данную систему
возможного влияния на протекание полимеризации
дополнительно лиганда, трициклогексилфосфина,
микропримесей, содержащихся в мономерах. Ввиду
существенно увеличило ее каталитическую актив-
данного обстоятельства была исследована сополиме-
ность и выходы образующихся полимеров (табл. 1).
ризация производного циклопропена (мономера М2)
Синтезированные аддитивные гомополимеры на ос-
с модельным мономером норборненового ряда —
нове М1 и М2 хорошо растворимы в хлороформе,
5-этилиден-2-норборненом (М3).
тетрагидрофуране и хлористом метилене. Анализ
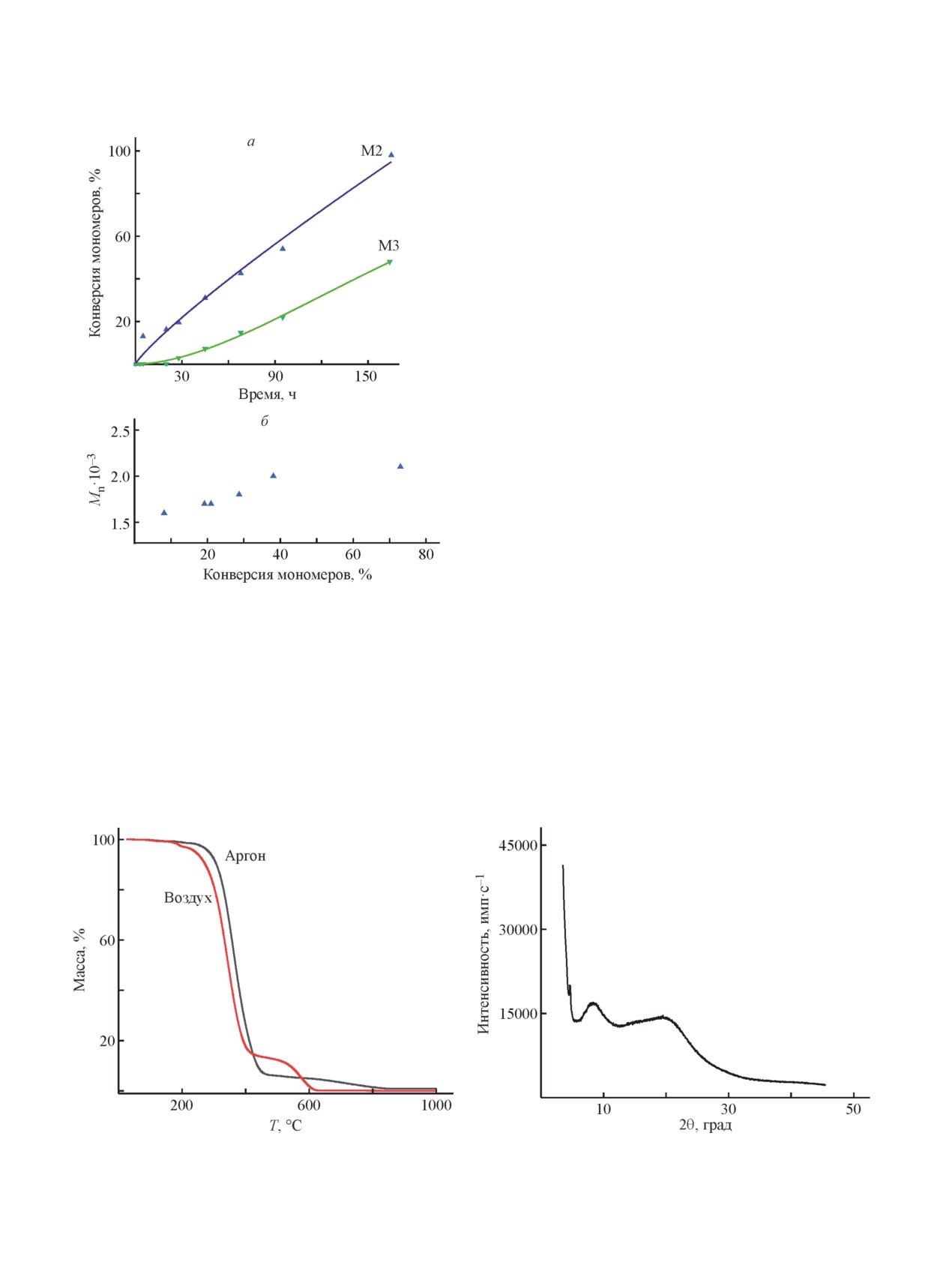
На основании результатов кинетики сополимери-
молекулярно-массовых характеристик продуктов
зации (рис. 1, а) можно сделать вывод о более высо-
реакции полимеризации показал, что, используя ка-
кой полимеризационной активности производного
талитическую систему Pd1/NaBARF/PCy3, можно
циклопропена: конверсия мономера М2 в полиме-
получать полимеры производных циклопропена с
ризации была существенно выше, чем конверсия
молекулярными массами несколько ниже теорети-
5-этилиден-2-норборнена. С увеличением времени
ческих и унимодальными молекулярно-массовыми
реакции достигалась практически количественная
распределениями (табл. 1). Это свидетельствует о
конверсия производного циклопропена, в то время
протекании аддитивной полимеризации исследуемых
как конверсия 5-этилиден-2-норборнена на момент
мономеров на каталитических центрах одного типа и
израсходования М2 оказалась ниже 50%. Таким об-
реализации обрыва цепи с образованием активных ка-
разом, активность производного циклопропена выше
талитических частиц, инициирующих формирование
активности производного норборнена в аддитивной
новых полимерных цепей. Более широкое молекуляр-
полимеризации. Учитывая наличие в М2 более объ-
но-массовое распределение для полимера на основе
емных заместителей и их близкое расположение к
М2 скорее всего связано с ограничением диффузии
полимеризуемой двойной связи, наблюдаемая более
молекул мономера к активным каталитическим цен-
высокая полимеризационная активность производных
трам, что вызвано проведением полимеризации в
циклопропена по сравнению с активностью 5-этили-
условиях более высокой концентрации мономера в
ден-2-норборнена скорее всего объясняется большей
реакционной смеси. Строение и чистота полученных
энергией напряжения цикла. С увеличением конвер-
Таблица 1
Условия и результаты полимеризации 3-метил-3-фенилциклопропена-1 и 3,3-ди(н-пропил)циклопропена-1
в присутствии Pd-комплекса с ациклическим диаминокарбеновым лигандом
Мольное
Мольное
Мономер (М)
с(М), М
Выход, %
Mn
Mw/Mn
соотношение PCy3/Pd1
соотношение M/Pd1
3-Метил-3-фенилциклопропен-1
0/1
200
1.65
6
—
—
3-Метил-3-фенилциклопропен-1
2/1
200
1.24
34
3500
1.6
3-Метил-3-фенилциклопропен-1
2/1
100
1.0
39
3300
1.7
3,3-Ди(н-пропил)циклопропен-1
2/1
100
1.5
20*
8600
2.7
Примечание. Условия проведения: прекатализатор — Pd-комплекс с ациклическим диаминокарбеновым лигандом
Pd1 (I), сокатализатор — тетракис[3,5-бис(трифторметил)фенил]борат натрия (NaBARF), PCy3 — трициклогексилфосфин,
мольное соотношение [Pd]/[NaBARF] = 1/3, растворитель — хлористый метилен, время полимеризации 45 ч, температура
45°С; «—» — не определяли.
* Время полимеризации 22 ч, температура 60°С.
Аддитивная полимеризация 3,3-дизамещенных циклопропенов в присутствии палладиевого комплекса...
971
сии мономеров наблюдался плавный рост молеку-
лярных масс образующихся сополимеров (рис. 1, б).
Температура разложения полимеров (потеря 5%
массы) для данных полимеров составляла более
200°С (рис. 2), т. е. полимеры обладают достаточно
хорошей термической устойчивостью, несмотря на
наличие напряженных циклопропановых колец в
структуре основных цепей полимеров.
На основании результатов дифференциальной
сканирующей калориметрии установлено, что син-
тезированные полимеры являются стеклообразны-
ми. Температуры стеклования поли(М1) и поли(М2)
выше, чем их температуры разложения. На кривых
дифференциальной сканирующей калориметрии от-
сутствуют пики, соответствующие плавлению, что
свидетельствует об аморфной природе изучаемых
полимеров.
Результаты исследования синтезированного го-
мополимера на основе М1 методом рентгенофазо-
вого анализа подтверждают его аморфный характер
(рис. 3). На дифрактограмме поли(М1) наблюдаются
четыре широких пика (рис. 3). Это сильно контрасти-
рует с дифрактограммами аддитивных полимеров на
Рис. 1. Зависимость конверсии мономеров от времени
основе 5-этилиден-2-норборнена и незамещенного
) сополи-
полимеризации (а) и молекулярной массы (Mn
норборнена (табл. 2), на которых наблюдаются толь-
мера от конверсии мономеров (б).
ко два широких пика. Пики на дифрактограмме по-
М2 — 3,3-ди(н-пропил)циклопропен-1, М3 — 5-этили-
ли(М1) при 2θ от 8° до 12° характеризуют расстояния
ден-2-норборнен, прекатализатор — Pd-комплекс с ацикли-
между цепями и сегментами основной цепи, пики при
ческим диаминокарбеновым лигандом Pd1 (I), сокатализа-
2θ от 15° до 23° — расстояния между структурными
тор — тетракис[3,5-бис(трифторметил)фенил]борат натрия
(NaBARF), мольное соотношение [Pd]/[NaBARF]/[PCy3] =
фрагментами в пределах одной цепи, а также свиде-
= 1/3/2 (PCy3 — трициклогексилфосфин), исходное моль-
тельствуют о наличии агломерации боковых замести-
ное соотношение мономеров 50/50, [M2] = [М3] = 0.75 М,
телей с вероятным формированием соответствующих
[М3]/[Pd] = [М2]/[Pd] =100/1, дихлорметан, 45°С.
наноразмерных фаз.
Рис. 2. Кривые термогравиметрического анализа адди- Рис. 3. Дифрактограмма аддитивного поли(3-метил-3-фе-
тивного поли(3-метил-3-фенилциклопропена-1).
нилциклопропена-1).
972
Меденцева Е. И. и др.
Таблица 2
Структурные характеристики аддитивных полимеров
(2θ)1,
(2θ)2,
(2θ)3,
(2θ)4,
Литературный
Полимер
d1, Å
d2, Å
d3, Å
d4, Å
град
град
град
град
источник
Поли(3-метил-3-фенилциклопро-
8.07
10.9
9.7
9.1
15.0
5.9
20.2
4.4
Данная
пен-1)
работа
Поли(5-этилиден-2-норборнен)
8.5
10.4
17.4
5.1
—
—
—
—
[14]
Полинорборнен
10.0
8.8
18.5
4.7
—
—
—
—
[15]
Примечание. Расстояния рассчитаны по уравнению Вульфа-Брэгга: d = λ/2sinθ, где d — межплоскостное рассто-
яние, θ — угол скольжения, λ = 1.54 Å; «—» — соответствующие пики на дифрактограмме отсутствуют.
Выводы
тез полимеров, обработка данных, написание статьи,
описание физико-химических свойств полимеров;
Исследована аддитивная полимеризация двух ци-
К. В. Потапов — синтез 3-метил-3-фенилциклопро-
клопропенов с углеводородными заместителями в
пена-1 и 3,3-ди(н-пропил)циклопропена-1; М. В. Бер-
присутствии Pd-комплекса, содержащего ацикли-
мешев — написание статьи, интерпретация результа-
ческий диаминокарбеновый лиганд. Показано, что
тов исследования.
двухкомпонентная каталитическая система на ос-
нове данного комплекса, активированного борорга-
Информация об авторах
ническим сокатализатором, позволяет вовлечь за-
мещенные циклопропены в полимеризацию, однако
Хрычикова Анна Петровна
выход полимерных продуктов в таком процессе ни-
зок. Введение фосфина в данную каталитическую
Меденцева Екатерина Игоревна
систему существенно увеличило ее активность и
позволило получить целевые полимеры со значи-
Бермешева Евгения Владимировна, к.х.н., доцент
тельно более высокими выходами. Установлено, что
циклопропены являются значительно более актив-
Потапов Константин Владиславович
ными мономерами по сравнению с производными
норборнена. Синтезированные полимеры на основе
Бермешев Максим Владимирович, д.х.н., доцент
изученных циклопропенов являются аморфными,
стеклообразными и обладают необходимой терми-
ческой стабильностью, что открывает возможности
Список литературы
создания на их основе новых функциональных поли-
[1] Blank F., Janiak C. Metal catalysts for the vinyl/addition
мерных материалов и делает актуальными дальней-
polymerization of norbornene // Coord. Chem. Rev.
шие исследования с целью установления взаимосвязи
2009. V. 253. P. 827-861.
строение полимера-его свойство.
[2] Wang X., Wilson T. J., Alentiev D., Gringolts M.,
Finkelshtein E., Bermeshev M., Long B. K. Substituted
Финансирование работы
polynorbornene membranes: A modular template for
Работа выполнена при поддержке гранта
targeted gas separations // Polym. Chem. 2021. V. 12.
Президента РФ МД-497.2022.1.3 (Соглашение
№ 075-15-2022-359 от 05.05.22).
[3] Суслов Д. С., Быков М. В., Кравченко О. В.
Аддитивная полимеризация норборнена с катализа-
торами на основе соединений переходных металлов:
Конфликт интересов
2008-2018 // Высокомолекуляр. соединения. Сер. С.
Авторы заявляют об отсутствии конфликта инте-
2019. Т. 61. № 1. С. 122-151.
ресов, требующего раскрытия в данной статье.
[Suslov D. S., Bykov M. V., Kravchenko O. V.
Norbornene addition polymerization with catalysts
Информация о вкладе авторов
based on transition metal compounds: 2008-2018 //
Е. И. Меденцева — синтез полимеров; А. П. Хры-
Polym. Sci. Ser. C. 2019. V. 61. P. 145-173.
чикова — синтез полимеров; Е. В. Бермешева — син-
Аддитивная полимеризация 3,3-дизамещенных циклопропенов в присутствии палладиевого комплекса...
973
[4]
Bermeshev M. V., Chapala P. P. Addition
[Khrychikova A. P., Medentseva E. I., Bermesheva E. V.,
polymerization of functionalized norbornenes as a
Woznyak A. I., Kashina M. V., Kinzhalov M. A.,
powerful tool for assembling molecular moieties of
Bermeshev M. V. Synthesis of addition poly(5-methyl-
new polymers with versatile properties // Prog. Polym.
2-norbornene) in the presence of palladium complexes
Sci. 2018. V. 84. P. 1-46.
containing acyclic diaminocarbene ligands // Russ. J.
Appl. Chem. 2022. V. 95. P. 1603-1610.
[5]
Zhang Z., Gao Y., Chen S., Wang J. Palladium-
catalyzed living/controlled vinyl addition
[12]
Li C., Yu R., Cai S.-Z., Fang X. Highly
polymerization of cyclopropenes // J. Am. Chem. Soc.
diastereoselective synthesis of polysubstituted
2021. V. 143. P. 17806-17815.
cyclopropanecarbonitriles via palladium-catalyzed
cyanoesterification of cyclopropenes // Org. Lett.
[6]
Elling B. R., Su J. K., Xia Y. Polymerization of
2023. V. 25. P. 5128-5133.
cyclopropenes: Taming the strain for the synthesis of
controlled and sequence-regulated polymers // Acc.
[13]
Hashmi A. S. K., Lothschütz C., Böhling C.,
Chem. Res. 2021. V. 54. P. 356-365.
Rominger F. From isonitriles to carbenes: Synthesis
of new NAC- and NHC-palladium(I) compounds and
[7]
Xiaohua Hou Z. W. Living/controlled vinyl addition
their catalytic activity // Organometallics. 2011. V. 30.
polymerization of cyclopropenes catalyzed by
palladium complex // Chin. J. Org. Chem. 2021. V. 41.
[14]
Бермешева Е. В., Возняк А. И., Борисов И. Л.,
P. 4830-4831.
Евлампиева Н. П., Везо О. С., Карпов Г. О.,
Бермешев М. В., Асаченко А. Ф., Топчий М. А.,
[8]
Bermesheva E. V., Bermeshev M. Single-component
Грибанов П. С., Нечаев М. С., Волков В. В.,
catalysts for vinyl-addition polymerization of
Финкельштейн Е. Ш. Синтез, молекулярные и га-
norbornene and its derivatives // ChemCatChem.
зотранспортные свойства гомополимеров на ос-
2023. P. 15076-15090.
нове 5-этилиден-2-норборнена и 5-винил-2-нор-
борнена // Высокомолекуляр. соединения. Сер. С.
[9]
Jung I. G., Seo J., Chung Y. K., Shin D. M.,
2019. Т. 61. № 1. С. 61-76.
Chun S.-H., Son S. U. Polymerization of carboxylic
ester functionalized norbornenes catalyzed by (η3-
[Bermesheva E. V., Wozniak A. I., Borisov I. L.,
allyl)-palladium complexes bearing N-heterocyclic
Yevlampieva N. P., Vezo O. S., Karpov G. O.,
carbene ligands // J. Polym. Sci. Part A: Polym. Chem.
Bermeshev M. V., Asachenko A. F., Topchiy M. A.,
2007. V. 45. P. 3042-3052.
Gribanov P. S., Nechaev M. S., Volkov V. V.,
Finkelshtein E. S. Synthesis, molecular, and gas-
[10]
Lee D. J., Choi W. H., Kim M., Kim C. K., Lee I. M.
transport properties of homopolymers based on
Copolymerization of functional norbornenes catalyzed
5-ethylidene-2-norbornene and 5-vinyl-2-norbornene
by pd complexes: Is it living? // Bull. Korean Chem.
// Polym. Sci. Ser. C. 2019. V. 61. P. 86-101.
Soc. 2020. V. 41. P. 697-701.
[15]
Zhao C.-T., do Rosário Ribeiro M., de Pinho M. N.,
[11]
Хрычикова А. П., Меденцева Е. И., Бермешева Е. В.,
Subrahmanyam V. S., Gil C. L., de Lima A. P. Structural
Возняк А. И., Кашина М. В., Кинжалов М. А.,
characteristics and gas permeation properties of
Бермешев М. В. Синтез аддитивного поли(5-ме-
polynorbornenes with retained bicyclic structure //
тил-2-норборнена) в присутствии палладиевых
Polymer. 2001. V. 42. P. 2455-2462.
комплексов, содержащих ациклические диамино-
карбеновые лиганды // ЖПХ. 2022. Т. 95. № 10.
С. 1312-1319.