Журнал прикладной химии. 2023. Т. 96. Вып. 12
ОРГАНИЧЕСКИЙ СИНТЕЗ И ТЕХНОЛОГИЯ ОРГАНИЧЕСКИХ ПРОИЗВОДСТВ
УДК 547.792+547.793
ДИЗАЙН, СИНТЕЗ И ФУНГИЦИДНАЯ АКТИВНОСТЬ
2-АЛКИЛТИО-5-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-1,3,4-ОКСАДИАЗОЛОВ
© Г. В. Цаплин1, С. А. Казаков1, М. И. Семчукова1, Е. А. Алексеева1,
А. Л. Алексеенко1,2, И. М. Чернега3, С. В. Попков1,4
1 Российский химико-технологический университет им. Д. И. Менделеева,
125047, г. Москва, Миусская пл., д. 9
2 Институт органической химии им. Н. Д. Зелинского РАН,
119991, г. Москва, Ленинский пр., д. 47
3 Ведущий научно-исследовательский институт химической технологии госкорпорации «Росатом»,
111524, г. Москва, ул. Электродная, д. 2, стр. 1
4 Всероссийский научно-исследовательский институт фитопатологии,
143050, Московская обл., Одинцовский р-н, р.п. Большие Вяземы, ул. Институт, владение 5
Поступила в Редакцию 27 ноября 2023 г.
После доработки 29 декабря 2023 г.
Принята к публикации 29 декабря 2023 г.
Разработан метод синтеза 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов путем
алкилирования 5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазол-2-тиона β-бромфенетолами в при-
сутствии триэтиламина в ацетоне с выходом до 90%. В результате испытаний целевых соединений
на фунгицидную активность in vitro по отношению к шести видам фитопатогенных грибов разных
таксономических классов выявлено, что S-галогенфеноксиэтилзамещенные производные превосходят
эталон триадимефон по действию на Venturia inaequalis, Rhizoctonia solani и Bipolaris sorokiniana.
Ключевые слова: алкилирование; 1,3,4-оксадиазол-2-тион; 1,2,4-триазол; фунгицидная активность
DOI: 10.31857/S0044461823120071; EDN: SBBHBT
Применение фунгицидных препаратов позволяет
ми нормами расхода, низкой токсичностью и пер-
решать вопросы сохранения, качества и урожайности
систентностью. В последние годы вышли на рынок
сельскохозяйственных культур, предотвращать за-
новые эффективные агрохимические и лекарственные
грязнение продукции микотоксинами [1]. Заражение
препараты, такие как протиоконазол, эфиноконазол,
сельскохозяйственной продукции микотоксинами
изавуконазол и др. [3].
приводит к серьезным последствиям для человека
При разработке современных препаратов выяв-
и животных: к отравлениям, возникновению аллер-
лена общая тенденция сочетания в структуре дей-
гических реакций, образованию злокачественных
ствующего вещества нескольких гетероциклов [3].
опухолей и снижению иммунитета [2]. Одним из наи-
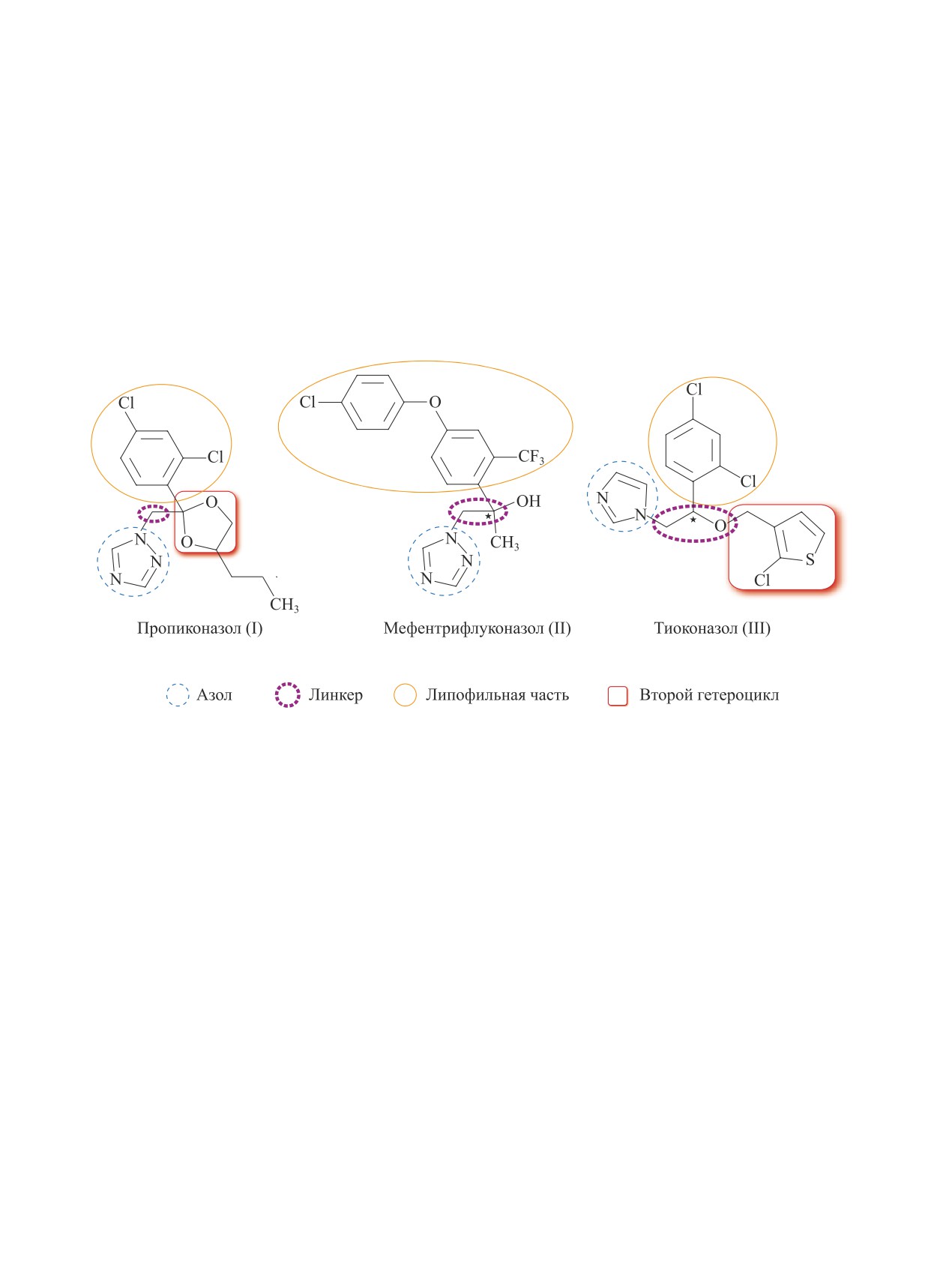
1,2,4-Триазольный фрагмент выступает в качестве
более важных классов фунгицидов являются азолы,
фармакофорной группы, а второй гетероцикл, сое-
высокоэффективные системные препараты с низки-
диненный через линкер (элемент, связывающий ча-
994
Дизайн, синтез и фунгицидная активность 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
995
сти молекулы и не оказывающий непосредственного
Классический подход к дизайну азольных пре-
влияния на биологическую активность вещества), за
паратов применяется в настоящее время, типичным
счет образования дополнительных связей в активном
примером может служить выпущенный компани-
сайте фермента обеспечивает эффективное действие
ей BASF препарат мефентрифлуконазол, который
препарата. Липофильная часть молекулы действую-
отсутствует на рынке химических средств защиты
щего вещества представлена арилсодержащим фраг-
растений в Российской Федерации. Он не содер-
ментом, отвечающим за моделирование ланостерина.
жит в своей структуре фрагмент второго гетеро-
Этот подход использовался при разработке таких
цикла, однако включает удлиненный липофильный
фунгицидов, как пропиконазол (I), мефентрифлуко-
фрагмент с дополнительным ароматическим коль-
назол (II), тиоконазол (III) [4, 5].
цом [6].
Молекулярная модель азольных препаратов, осно-
Наша молекулярная модель азолов уже показала
ванная на введении дополнительных гетероциклов,
свою эффективность при разработке новых фунгици-
таких как 1,2,4-триазол, пиримидин, тиазол, вместо
дов в ряду полученных нами 3-алкилтио-5-(1,2,4-три-
неароматических гетероциклов, показала свою эф-
азол-1-илметил)-1,2,4-триазолов [10]. Важным свой-
фективность, так как такие производные нашли ши-
ством является низкая токсичность соединений
рокое применение в медицинской химии в качестве
подобного строения [11, 12].
лекарственных препаратов для лечения микозов [7, 8].
Цель исследования — разработка дизайна и синтез
Дизайн азольных препаратов, основанный на
новых фунгицидов на основе замещенных фенетолов,
введении дополнительных гетероциклов, таких как
содержащих в структуре 1,2,4-триазол, 1,3,4-оксади-
1,2,4-триазол, пиримидин, тиазол, вместо неарома-
азол-2-тион и липофильный стерин-моделирующий
тических гетероциклов, привел к разработке целого
фрагмент.
нового поколения препаратов для лечения микозов
человека и животных, однако на данный момент не
Экспериментальная часть
привел к разработке новых химических средств за-
щиты растений.
Спектры ЯМР 1Н и 13С записаны на спектрометре
Исходя из современных тенденций разработки
магнитного резонанса Bruker 300 МГц.
азольных фунгицидов, мы предложили новую моле-
Масс-спектры получены на жидкостном хрома-
кулярную модель азолов — соединений-ингибиторов
тографе с масс-спектрометром высокого разрешения
CYP51, основанную на протяженных соединениях,
QExactive (ThermoScientific) в режиме электрорас-
содержащих в своем составе 1,2,4-триазол, соединен-
пылительной ионизации при атмосферном давле-
ный линкером со вторым азотсодержащим гетероци-
нии. Колонка HYPERSILGoldaQ (ThermoScientific)
клом и липофильной частью [9].
длиной 150 мм, внутренним диаметром 2.1 мм, под-
996
Цаплин Г. В. и др.
вижная фаза — ацетонитрил-вода-муравьиная кис-
ли на роторно-пленочном испарителе в вакууме во-
лота (99:1:0.1), напряжение на капилляре — 4000 В,
доструйного насоса. Остаток разделяли фракционной
в режиме полного ионного тока при регистрации
перегонкой в вакууме масляного насоса. Получили
положительных ионов в диапазоне 80-750 Да с раз-
29.25 г (63%) этил(1Н-1,2,4-триазол-1-ил)ацетата с
решением 35 000.
Ткип = 115-125°С (0.15 Торр), по литературным дан-
В работе использовали триазол (99.5%, Acros
ным Ткип = 94-110°С (0.13 Торр) [13]. Спектр ЯМР
Organics, кат. № 139285000), этилхлорацетат (99%,
1Н, δ, м. д.: 1.22 т (3Н, СН3, 3J = 7.4 Гц), 4.18 кв (1H,
Acros Organics, кат. № 118220010), гидразин гидрат
CH2CH3, 3J = 7.4 Гц), 5.21 c [2H, CH2C(O)], 8.02 c
(98%, Alfa Aesar, кат. № А14005.36), сероуглерод
(1H, C5HTrz), 8.54 c (1H, C3HTrz).
(99.5%, Panreac, кат. № 161244.1611), триэтиламин
2-(1Н-1,2,4-Триазол-1-ил)ацетгидразид (1).
(99%, Acros Organics, кат. № 157910010), метилиодид
К раствору 0.065 моль этил(1Н-1,2,4-триазол-1-
(99%, Acros Organics, кат. № 122375000), бензилбро-
ил)ацетата в 25 мл этанола добавляли 0.1625 моль
мид (98%, Acros Organics, кат. № 105871000), п-хлор-
98%-ного гидразин гидрата и кипятили в течение
бензилхлорид (Acros Organics, кат. № 150242500),
6 ч. Растворитель удаляли на роторно-пленоч-
1-(2-бромэтокси)-2-фторбензол (97%, BDLpharm,
ном испарителе в вакууме водоструйного насоса.
кат. № BD49860), 1-(2-бромэтокси)-4-хлорбензол
Образовавшийся осадок перекристаллизовывали из
(98%, BDLpharm, кат. № BD49870), 4-(2-бромэтокси)-
изопропанола. Получили 6.03 г (66%) 2-(1Н-1,2,4-
1-бромбензол (98%, BDLpharm, кат. № BD49876),
триазол-1-ил)ацетгидразида (1) с Тпл = 118-119°С, по
1-(2-бромэтокси)-4-нитробензол (100%, Sigma-
литературным данным Тпл = 119-120°С [14]. Спектр
Aldrich, кат. № РН010955), 4-(2-бромэтокси)-1,2-
ЯМР 1Н, δ, м. д.: 4.85 c (2H, CH2), 7.97 c (1H, C5HTrz),
дихлорбензол (95%, BDLpharm, кат. № BD01111988),
8.51 c (1H, C3HTrz), 9.46 с (1Н, NH).
2-(2-бромэтокси)-1,3,5-трихлорбензол (95%,
Калиевая соль 2-(1H-1,2,4-триазол-1-илацетил)-
BDLpharm, кат. № BD60944), 1-(2-бромэтокси)-4-ме-
гидразинкарбодитионовой кислоты (2). К раствору
тилбензол (Sigma-Aldrich, кат. № PH000131),
0.028 моль 2-(1Н-1,2,4-триазол-1-ил)ацетгидразида и
1-(2-бромэтокси)-4-хлор-2-метилбензол (98%,
0.056 моль 85% гидроксида калия в 100 мл этанола по
BDLpharm, кат. № BD01792642), 2-(2-бромэток-
каплям добавляли раствор 0.056 моль сероуглерода
си)-1-хлор-4-метилбензол (95%, BDLpharm, кат.
в 8 мл этанола. Реакционную массу перемешивали
№ BD275066), 1-(2-бромэтокси)-2-метоксибензол
в течение 2 ч при комнатной температуре, осадок
(97%, BDLpharm, кат. № BD61130), 1-(2-бромэтокси)-
отфильтровывали и сушили в пистолете Фишера над
4-метоксибензол (Sigma-Aldrich, кат. № PH009793),
пятиокисью фосфора. Получили 9.58 г (98%) калие-
соляную кислоту (х.ч., OOO «Компонент-Реактив»,
вой соли 2-(1Н-1,2,4-триазол-1-илацетил)гидразин-
ГОСТ 3118-77), KOH (х.ч., АО «ЭКОС-1»), P2O5
карбодитионовой кислоты (2) с Тпл = 189-191°С.
(ч., OOO «Компонент-Реактив»), K2CO3 (х.ч., OOO
Спектр ЯМР 13С, δ, м. д.: 43.48 (СН2), 151.50 (С3Trz),
«Компонент-Реактив»), MgSO4 безводный (96%,
151.62 (С5Trz), 159.81 (C S), 161.91 (C—S).
Panreac, кат № 212486.1211).
5-(1Н-1,2,4-Триазол-1-илметил)-1,3,4-оксадиазол-
В качестве растворителей были использованы аце-
2-тион (3). Раствор 4 ммоль калиевой соли
тонитрил (х.ч., OOO «Компонент-Реактив»), изопро-
2-(1H-1,2,4-триазол-1-илацетил)гидразинкарбодитио-
пиловый спирт (х.ч., OOO «Компонент-Реактив»),
новой кислоты (2) в 65 мл этанола кипятили в течение
ацетон (х.ч., OOO «Компонент-Реактив»,), хлороформ
9 ч, реакционную массу подкисляли 4.9 мл 3%-ного
(х.ч., OOO «Компонент-Реактив»), диэтиловый эфир
раствора хлороводорода в изопропиловом спирте.
(99.7%, Panreac, кат. № 132770.0311), этиловый спирт
Полученный осадок отфильтровывали и перекри-
(ООО ТД «Химмед», СР10288-08-1-BULK).
сталлизовывали из этанола. Получили 0.44 г (61%)
При проведении фунгицидных испытаний
5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазол-2-
был использован Агар-Агар 900 (Е406) (Zhenpai
тиона (3) с Тпл = 190-191°С, по литературным дан-
Hydrocolloids Co. Ltd, кат. № ZP202108152).
ным Тпл = 194-195°С [15]. Спектр ЯМР 1Н, δ, м. д.:
Этил 1Н-(1,2,4-триазол-1-ил)ацетат. К раствору
3.28 уш.с (1Н, NH), 5.68 c (2H, CH2), 8.09 c (1H,
0.3 моль 1,2,4-триазола в 180 мл ацетонитрила добав-
C5HTrz), 8.70 c (1H, C3HTrz). Спектр ЯМР 13С, δ, м. д.:
ляли 0.309 моль карбоната калия и кипятили в тече-
43.9 (C-6), 145.42 (C-2), 152.39 (С-3), 158.32 (С-10,
ние 30 мин, затем прикапывали 0.295 моль этилхлор-
С-7). Масс-спектрометрия высокого разрешения,
ацетата так, чтобы температура реакционной массы
ионизация электрораспылением (ИЭР): рассчита-
не превышала 60°С. Далее массу кипятили в течение
но m/z [M+] = 183.0215, найдено m/z [C5H5N5OS+] =
5 ч, осадок отфильтровывали, а растворитель отгоня-
= 183.0222.
Дизайн, синтез и фунгицидная активность 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
997
Общая методика получения 2-алкилтио-5-
7.1 м (4H, 4CHAr), 8.04 c (1H, C5HTrz), 8.72 c (1H,
(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов (4).
C3HTrz). Спектр ЯМР 13C, δ, м. д.: 31.80 (С-1), 40.10
Смесь 0.546 ммоль алкилгалогенида, 0.546 ммоль
(С-7), 67.26 (C-14), 116.51 (С-18), 116.67 (C-21),
5-(1H-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-
122.13 (С-19), 125.35 (С-20), 145.61 (С-3), 151.13
тиона (3) и 0.546 ммоль триэтиламина в 3 мл ацетона
(С-16, С-17), 153.2 (С-4), 163.13 (С-12), 164.98 (С-8).
кипятили с обратным холодильником 4-24 ч (табл. 1).
Масс-спектрометрия высокого разрешения, ИЭР:
Реакционную массу охлаждали, растворитель уда-
рассчитано m/z [M + H+] = 322.0774, найдено m/z
ляли на РПИ в вакууме водоструйного насоса, а к
[C13H11FN5O2S + H+] = 322.0783.
остатку добавляли 4 мл воды и 4 мл хлороформа.
2-{[2-(4-Хлорфенокси)этил]тио}-5-[(1H-1,2,4-
Отделяли органическую фазу, водный слой промы-
триазол-1-ил)метил]-1,3,4-оксадиазол (4е), вы-
вали хлороформом (2 × 4 мл). Органические фазы
ход 0.17 г (90%), Тпл = 80-83°С. Спектр ЯМР 1Н,
объединяли и сушили над сульфатом магния, затем
δ, м. д.: 3.64 т (2H, SCH2CH2O J3 = 5.86 Гц), 4.3 т
осушитель отфильтровывали, хлороформ удаляли на
(2H, SCH2CH2O, J3 = 5.13 Гц), 5.83 с (1Н, СH2NTrz),
роторно-пленочном испарителе. К остатку добавляли
6.95 д (2H, 2CHAr, J3 = 8.85 Гц), 7.32 д (2Н, 2CHAr,
3 мл диэтилового эфира. Образовавшиеся кристаллы
J3 = 8.85 Гц), 8.05 c (1H, С5НTrz), 8.73 с (1Н, С3НTrz).
отфильтровывали и промывали диэтиловым эфиром.
Спектр ЯМР 13C, δ, м. д.: 31.85 (С-1), 43.51 (C-7),
2-Метилтио-5-[(1H-1,2,4-триазол-1-ил)ме-
66.60 (С-14), 116.76 (C-21, С-17), 125.22 (C-19), 129.76
тил]-1,3,4-оксадиазол (4a), выход 0.06 г (57%),
(C-18, C-20), 145.64 (С-3), 152.60 (С-4), 157.17 (С-16),
Тпл = 129-132°С. Спектр ЯМР 1Н, δ, м. д.: 2.51 с (3H,
163.14 (С-12), 164.99 (С-8). Масс-спектрометрия вы-
(CH3S), 5.82 c (2H, CH2N), 8.06 с (1H, C5HTrz), 8.73 с
сокого разрешения, ИЭР: рассчитано m/z [M + H+] =
(1Н, С3НTrz). Спектр ЯМР 13C, δ, м. д.: 14.76 (С-13),
= 338.0478, найдено m/z [C13H12ClN5O2S + H+] =
43.50 (C-6), 145.68 (С-2), 152.63 (C-3), 162.95 (C-10),
= 338.0476.
166.15 (C-7). Масс-спектрометрия высокого разре-
2-{[2-(4-Бромфенокси)этил]тио}-5-[(1H-1,2,4-
шения, ИЭР: рассчитано m/z [M + H+] = 198.0449,
триазол-1-ил)метил]-1,3,4-оксадиазол (4f), вы-
найдено m/z [C6H7N5OS + H+] = 198.0455.
ход 0.11 г (52%), Тпл = 84-87°С. Спектр ЯМР 1Н,
2-Бензилтио-5-[(1H-1,2,4-триазол-1-ил)ме-
δ, м. д.: 3.62 д (2Н, SCH2CH2O J3 = 5.86 Гц), 4.30 д
тил]-1,3,4-оксадиазол (4b), выход 0.09 г (64%),
(2Н, SCH2CH2O, J3 = 5.86 Гц), 5.83 с (2Н, СH2NTrz),
Тпл = 87-90°С. Спектр ЯМР 1Н, δ, м. д.: 4.48 с (2H,
6.89 д (2H, 2CHAr, J3 = 8.8 Гц), 6.95 д (2Н, 2CHAr,
SCH2C6H5), 5.83 с (2H, СH2NTrz), 7.31 м (3H, CHAr),
J3 = 8.79 Гц), 8.06 c (1Н, С5НTrz), 8.73 с (1Н, С3НTrz).
7.38 м (2H, CHAr), 8.08 c (1H, CH5Trz), 8.73 с (1Н,
Спектр ЯМР 13C, δ, м. д.: 31.84 (С-1), 43.51 (C-7),
CH3Trz). Спектр ЯМР 13C, δ, м. д.: 36.29 (С-13), 43.50
66.53 (С-14), 117.29 (C-19), 117.45 (C-17, C-21),
(C-6), 128.23 (С-15, С-19), 129.01 (С-16, С-18), 129.44
132.66 (C-18, C-20), 152.66 (С-3, С-4), 157.62 (С-16),
(С-17), 136.82 (C-14), 145.62 (C-2), 152.61 (C-3),
163.13 (С-12), 164.99 (С-8). Масс-спектрометрия вы-
163.16 (С-7, С-10). Масс-спектрометрия высокого
сокого разрешения, ИЭР: рассчитано m/z [M + H+] =
разрешения, ИЭР: рассчитано m/z [M + H+] = 274.076,
= 381.9973, найдено m/z [C13H12BrN5O2S + H+] =
найдено m/z [C12H11N5OS + H+] = 274.078.
= 381.9975.
2-{[(4-Хлорфенил)метил]тио}-5-[(1H-1,2,4-три-
2-{[2-(4-Нитрофенокси)этил]тио}-5-[(1H-
азол-1-ил)метил]-1,3,4-оксадиазол (4с), выход 0.07 г
1,2,4-триазол-1-ил)метил]-1,3,4-оксадиазол (4g),
(42%), Тпл = 97-100°С. Спектр ЯМР 1Н, δ, м. д.:
выход 0.15 г (79%), Тпл = 97-100°С. Спектр ЯМР
4.47 c (2H, SCH2С6H4), 5.82 с (2H, CH2N), 7.39 м
1Н, δ, м. д.: 3.68 т (2H, SCH2CH2O, J3 = 5.9 Гц),
(2Н, 4СHAr), 8.07 c (1H, C5HTrz), 8.72 с (1Н, С3НTrz).
4.47 т (3H, SCH2CH2O, J3 = 5.9 Гц), 5.84 с (2H,
Спектр ЯМР 13C, δ, м. д.: 31.83 (С-13), 43.50 (C-6),
CH2N), 7.15 д (2Н, 2СНAr, J3 = 9.5 Гц), 8.07 с (1Н,
117.64 (С-16, С-18), 125.51 (С-15, С-19), 130.00 (С-17),
С5НTrz), 8.21 д (2Н, 2СНAr, J3 = 9.5 Гц), 8,74 с (1Н,
137.10 (C-14), 145.64 (C-2), 152.63 (C-3), 163.16
С3НTrz). Спектр ЯМР 13C, δ, м. д.: 31.65 (С-1), 43.50
(С-10), 165.04 (С-7). Масс-спектрометрия высокого
(C-7), 67.20 (С-14), 115.55 (C-17, С-21), 126.34
разрешения, ИЭР: расчитано m/z [M + H+] = 308.0373,
(C-18, С-20), 141.64 (C-19), 145.61 (С-3), 152.61
найдено m/z [C12H10ClN5OS + H+] = 308.0380.
(С-4), 163.19 (С-12), 163.55 (С-16), 164.87 (С-8).
2-{[2-(2-Фторфенокси)этил]тио}-5-[(1H-1,2,4-
Масс-спектрометрия высокого разрешения, ИЭР:
триазол-1-ил)метил]-1,3,4-оксадиазол (4d), вы-
рассчитано m/z [M + H+] = 349.0719, найдено m/z
ход 0.15 г (85%), Тпл = 79-82°С. Спектр ЯМР 1Н,
[C13H11N6O4S + H+] = 349.0722.
δ, м. д.: 3.69 т (2H, SCH2CH2O, J3 = 6.2 Гц), 4.31 т
2-{[2-(3,4-Дихлорфенокси)этил]тио}-5-[(1H-1,2,4-
(2H, SCH2CH2O, J3 = 6.23 Гц), 5.83 c (2H, CH2NTrz),
триазол-1-ил)метил]-1,3,4-оксадиазол (4h), выход
998
Цаплин Г. В. и др.
0.13 г (64%), Тпл = 68-71°С. Спектр ЯМР 1Н, δ,
2-{[2-(1-Хлор-4-метилбензол)этил]тио}-5-[(1H-
м. д.: 3.71 т (2H, SCH2CH2O, J3 = 5.86 Гц), 4.4 т (2H,
1,2,4-триазол-1-ил)метил]-1,3,4-оксадиазол (4l), вы-
SCH2CH2O, J3 = 5.86 Гц), 5.83 с (2H, CH2NTrz), 7.22 м
ход 0.12 г (60%), Тпл = 74-77°С. Спектр ЯМР 1Н,
(2H, 2CHAr), 7.36 c (1H, 1CHAr), 8.06 с (1H, C5HTrz),
δ, м. д.: 2.29 с (3H, CH3), 3.61 т (2H, SCH2CH2O,
8.73 (1H, C3HTrz). Спектр ЯМР 13C, δ, м. д.: 31.66
J3 = 5.9 Гц), 4.27 т (2H, SCH2CH2O, J3 = 5.9 Гц),
(С-1), 43.51 (C-7), 67.66 (С-14), 115.77 (C-21), 116.03
5.83 с (2Н, СН2NTrz), 6.74 д (1Н, СНAr, J3 = 8.8 Гц),
(C-17), 125.45 (C-19), 129.82 (С-18), 145.59 (С-3),
6.93 м (1Н, 1СНAr), 7.27 д (1Н, 1СНAr, J3 = 8.8 Гц),
152.52 (С-4), 152.85 (С-16), 163.07 (С-12), 164.95
8.06 c (1H, C5HTrz), 8.73 c (1H, C3HTrz). Спектр ЯМР
(С-8). Масс-спектрометрия высокого разрешения,
13C, δ, м. д.: 20.19 (С-23), 31.84 (C-1), 43.53 (С-7),
ИЭР: рассчитано m/z [M + H+] = 372.0089, найдено
68.46 (C-14), 117.66 (C-21), 117.88 (C-17), 125.51
m/z [C13H10Cl2N5O2S + H+] = 372.0095.
(С-19), 129.98 (С-18), 137.07 (С-20), 145.61 (С-3),
2-[(1H-1,2,4-Триазол-1-ил)метил]-5-{[2-(2,4,6-
152.52 (С-4), 157.07 (С-16), 163.13 (С-12), 165.01 (С-
трихлорфенокси)этил]тио}-1,3,4-оксадиазол (4i),
8). Масс-спектрометрия высокого разрешения, ИЭР:
выход 0.12 г (55%), Тпл = 101-104°С. Спектр ЯМР
рассчитано m/z [M + H+] = 352.0635, найдено m/z
1Н, δ, м. д.: 3.66 т (2Н, SCH2CH2O, J3 = 5.86 Гц),
[C14H13ClN5O2S + H+] = 352.0641.
4.38 т (2H, SCH2CH2O, J3 = 5.86 Гц), 5.83 c (2Н,
2-{[2-(2-Метоксифенокси)этил]тио}-5-[(1H-
CH2NTrz), 7.71 с (2H, 2CHAr), 8.05 с (1Н, С5НTrz),
1,2,4-триазол-1-ил)метил]-1,3,4-оксадиазол (4m),
8.72 c (1H, C3HTrz). Спектр ЯМР 13C, δ, м. д.: 32.34
выход 0.13 г (71%), Тпл = 87-90°С. Спектр ЯМР 1Н,
(С-1), 43.50 (С-7), 71.58 (C-14), 129.42 (С-19),
δ, м. д.: 3.62 т (2H, SCH2CH2O, J3 = 5.86 Гц), 3.75 c
129.71 (C-17, С-18, С-20, С-21), 145.58 (С-3),
(3H, CH3OC6H4), 4.27 т (2H, SCH2CH2O, J3 = 5.86 Гц),
149.93 (С-16), 152.58 (С-4), 163.10 (С-12), 164.90
5.83 с (2Н, СН2NTrz), 6.69 м (3Н, 3СНAr), 6.96 м (1Н,
(С-8). Масс-спектрометрия высокого разрешения,
СНAr), 8.06 с (1Н, C5HTrz), 8.73 c (1H, C3HTrz). Спектр
ИЭР: рассчитано m/z [M + H+] = 405.9699, найдено
ЯМР 13C, δ, м. д.: 25.43 (С-23), 31.80 (С-1), 40.15
m/z[C13H9Cl3N5O2S + H+] = 405.9698.
(С-7), 67.56 (C-14), 116.59 (С-18), 116.67 (C-21),
2-{[2-(4-Метилфенокси)этил]тио}-5-[(1H-1,2,4-
122.14 (С-19), 125.39 (С-20), 145.54 (С-3), 151.11
триазол-1-ил)метил]-1,3,4-оксадиазол (4j), выход
(С-16, С-17), 153.22 (С-4), 163.39 (С-12), 164.99 (С-8).
0.11 г (64%), Тпл = 96-99°С. Спектр ЯМР 1Н, δ, м. д.:
Масс-спектрометрия высокого разрешения, ИЭР:
2.23 c (3H, CH3C6H4O, J3 = 5.86 Гц), 3.61 т (2H,
рассчитано m/z [M + H+] = 322.0774, найдено m/z
SCH2CH2O, J3 = 5.86 Гц), 4.26 т (3H, SCH2CH2O,
[C14H14N5O3S + H+] = 322.0776.
J3 = 5.86 Гц), 5.82 с (2Н, СН2NTrz), 6.81 м (2H, 2CHAr),
2-{[2-(4-Метоксифенокси)этил]тио}-5-[(1H-1,2,4-
7.08 м (2Н, 2СНAr), 8.06 c (1H, C5HTrz), 8,72 c (1H,
триазол-1-ил)метил]-1,3,4-оксадиазол (4n), выход
C3HTrz). Спектр ЯМР 13C, δ, м. д.: 20.53 (С-22),
0.12 г (66%), Тпл = 56-59°С. Спектр ЯМР 1Н, δ, м. д.:
32.00 (С-1), 43.50 (C-7), 66.19 (С-14), 115.01 (C-17,
3.70 c (3H, CH3OC6H4), 3.77 т (2H, SCH2CH2O,
С-21), 130.33 (С-18, С-20), 145.59 (С-3), 152.60
J3 = 5.13 Гц), 4.25 т (2H, SCH2CH2O, J3 = 5.13 Гц),
(С-4), 156.20 (С-16), 163.12 (С-8), 165.82 (C-8).
5.83 с (2Н, СН2NTrz), 6.88 м (4Н, 4СНAr), 8.06 с (1Н,
Масс-спектрометрия высокого разрешения, ИЭР:
C5HTrz), 8.73 c (1H, C3HTrz). Спектр ЯМР 13C, δ, м. д.:
рассчитано m/z [M + H+] = 318.1025, найдено m/z
25.23 (С-23), 31.12 (С-1), 43.45 (C-7), 67.00 (С-14),
[C14H15N5O2S + H+] = 318.1032.
115.04 (C-17, С-21), 126.50 (C-18, С-20), 142.64 (C-19),
2-[(1H-1,2,4-Триазол-1-ил)метил]-5-{[2-(4-хлор-
145.99 (С-3), 152.60 (С-4), 163.11 (С-12), 163.22 (С-16),
2-метилбензол)этил]тио}-1,3,4-оксадиазол (4k), вы-
164.49 (С-8). Масс-спектрометрия высокого разреше-
ход 0.06 г (32%), Тпл = 83-86°С. Спектр ЯМР 1Н,
ния, ИЭР: рассчитано m/z [M + H+] = 334.0974, най-
δ, м. д.: 2.04 c (3H, CH3С6H3), 3.66 т (2H, SCH2CH2O,
дено m/z [C14H14N5O3S + H+] = 334.0977.
J3 = 5.86 Гц), 4.31 т (2Н, SCH2CH2O, J3 = 5.86 Гц),
Синтезированные 1,2,4-триазол-1-илметилазо-
5.82 с (2H, 2CH2NTrz), 6.97 д (1Н, СНAr, J3 = 8.06),
лы были испытаны на фунгицидную активность
7.2 м (2H, 2СНAr), 8.06 с (1Н, С5HTrz), 8.72 c (1H,
in vitro по общеизвестной методике [16] на шести
C3HTrz). Спектр ЯМР 13C, δ, м. д.: 15.93 (С-23), 32.04
фитопатогенных грибах: Sclerotinia sclerotiorum —
(С-1), 43.47 (C-7), 66.69 (С-14), 113.58 (C-21), 124.73
возбудителе белых гнилей, Fuzarium oxysporum,
(С-20), 126.90 (С-19), 128.83 (С-17), 130.43 (С-18),
Fuzarium moniliforme — возбудителях фузариозов,
145.62 (С-3), 152.50 (С-4, С-16), 155.29 (С-12), 163.09
Rhizoctonia solani — возбудителе ризоктониоза,
(С-8). Масс-спектрометрия высокого разрешения,
Bipolaris sorociniana — возбудителе корневых гнилей
ИЭР: рассчитано m/z [M + H+] = 352.0635, найдено
и Venturia inaequalis — возбудителе парши яблонь,
m/z [C14H13ClN5O2S + H+] = 352.0641.
полученных в центре коллективного пользования
Дизайн, синтез и фунгицидная активность 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
999
«Государственная коллекция фитопатогенных микро-
Расчет липофильности целевых соединений (lgP)
организмов и сортов-идентификаторов (дифферен-
проводили в пакете программ ACD Labs [ACD/
циаторов) патогенных штаммов микроорганизмов»
ChemSketch (Freeware) 2022.2.3, ACD/ Labs 2022.2.3
Федерального государственного бюджетного науч-
(File version C45E41, Build 130928, 16 Dec 2022)] в
ного учреждения «Всероссийский научно-исследо-
автоматическом режиме.
вательский институт фитопатологии». В качестве
питательной среды использовался картофеле-саха-
Обсуждение результатов
розный агар (Агар-Агар 900, Е406). Действие пре-
паратов на радиальный рост мицелия определяли
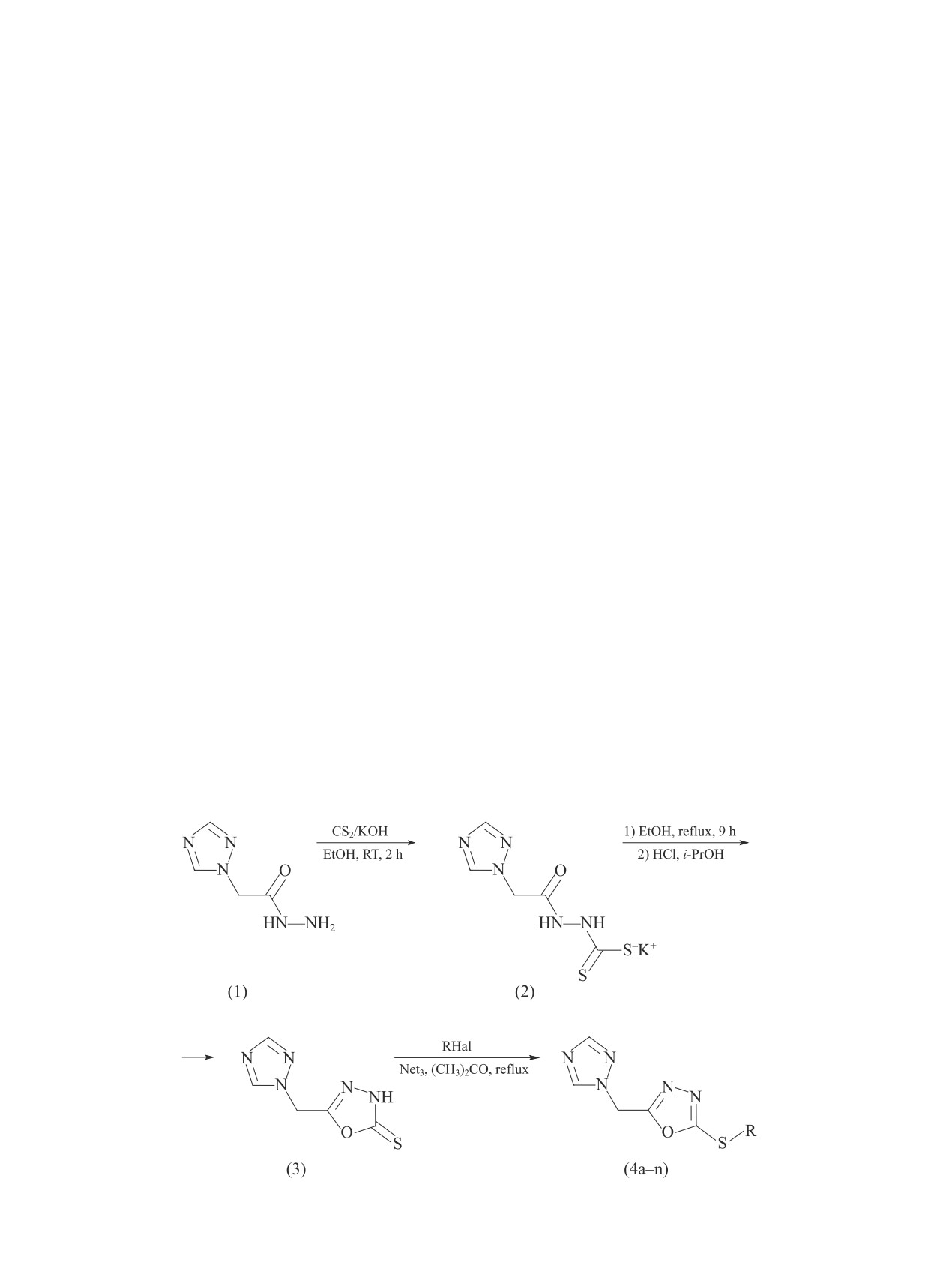
Для получения целевых 2-алкилтио-5-(1,2,4-три-
растворением соединения в ацетоне и внесением
азол-1-илметил)-1,3,4-оксадиазолов (4a-n) разрабо-
аликвоты в стерильный картофеле-сахарозный агар
тана трехстадийная схема синтеза (схема I), основан-
в асептических условиях при 50°С до концентрации
ная на использовании полученного по литературной
30 мг·л-1 по действующему веществу. Полученные
методике 2-(1,2,4-триазол-1-ил)ацетгидразида (1)
при этом среды разливали в чашки Петри. Конечная
[13, 14].
концентрация ацетона в контрольных растворах с
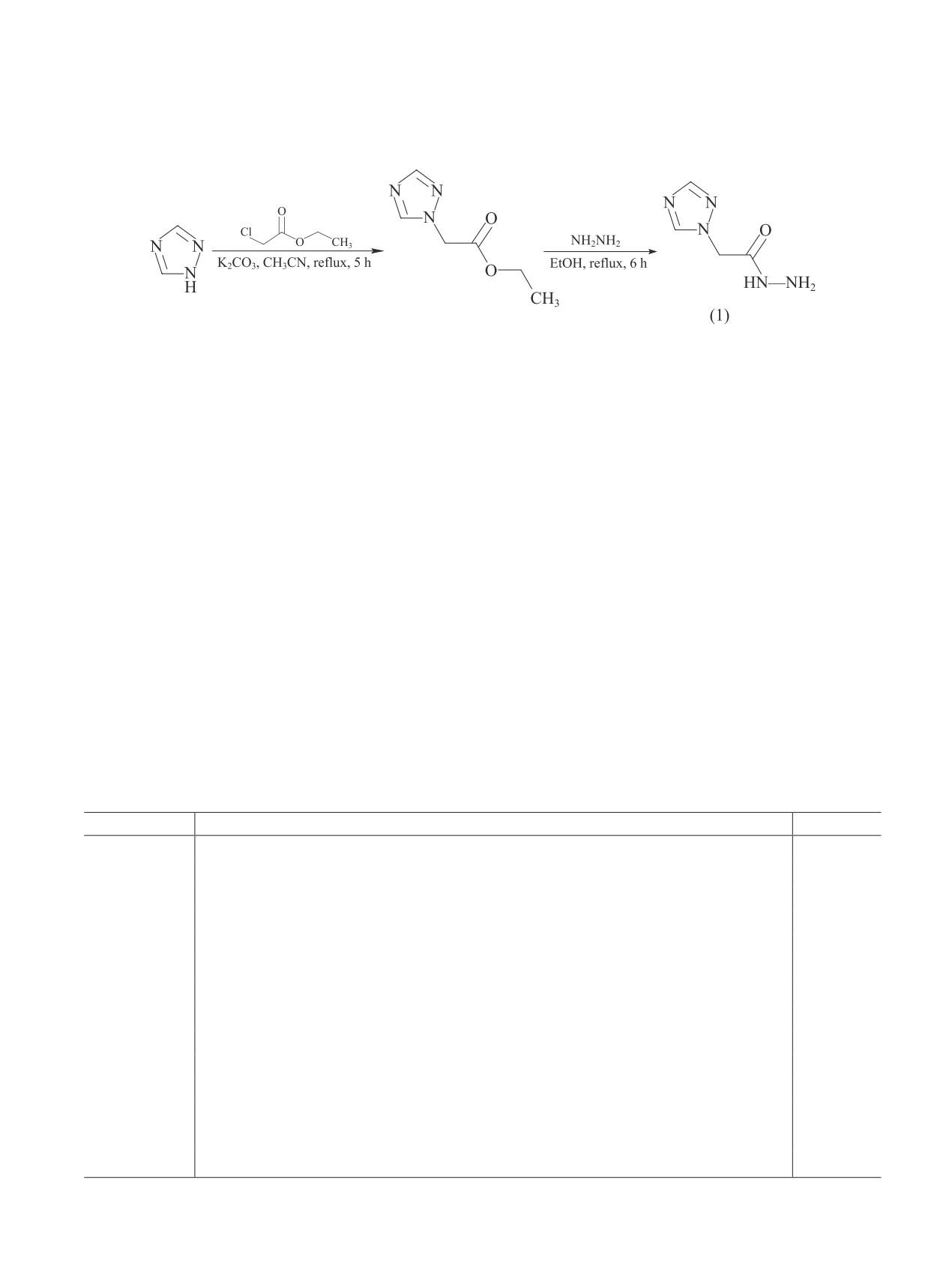
Исходный ацетгидразид (1) можно получить в две
действующими веществами составила 1%. В чашки
стадии с суммарным выходом 41% последовательным
Петри, содержащие 15 мл агаровой среды, наносили
алкилированием 1,2,4-триазола этилхлорацетатом в
иглой культуры грибов на агаровую поверхность.
присутствии основания с последующим введением
Образцы выдерживали в инкубаторе при 25°С и изме-
промежуточного этил(1Н-1,2,4-триазол-1-ил)ацета-
ряли радиальный рост мицелия через 3 сут. Изучали
та в реакцию с гидразин гидратом с образованием
действие препаратов на радиальный рост мицелия в
гидразида (1) (схема II).
сравнении с широко применяемым фунгицидом три-
При взаимодействии 2-(1,2,4-триазол-1-ил)-
адимефоном. Процент ингибирования роста мицелия
ацетгидразида (1) с сероуглеродом в присутствии
(%инг) рассчитывали по Эбботу:
гидроксида калия в абсолютном этаноле образует-
ся калиевая соль 2-(1H-1,2,4-триазол-1-илацетил)
%инг = [(Дк - До)/Дк]·100%,
гидразинкарбодитионовой кислоты (2) с выходом
98%. Далее калиевую соль (2) кипятят в этано-
где Дк — диаметр колоний гриба в контрольной сре-
ле в течение 20 ч до прекращения выделения се-
де, До — диаметр колоний гриба в среде с исследуе-
роводорода. Последующее подкисление 3%-ным
мым веществом (4a-n).
раствором хлороводорода в изопропиловом спир-
Схема I
1000
Цаплин Г. В. и др.
Схема II
те приводит к получению ключевого 5-(1Н-1,2,4-
так и липофильность 2-алкилтио-5-(1Н-1,2,4-три-
триазол-1-илметил)-1,3,4-оксадиазол-2-тиона (3) с
азол-1-илметил)-1,3,4-оксадиазолов (4a-n). К сожа-
выходом 61%.
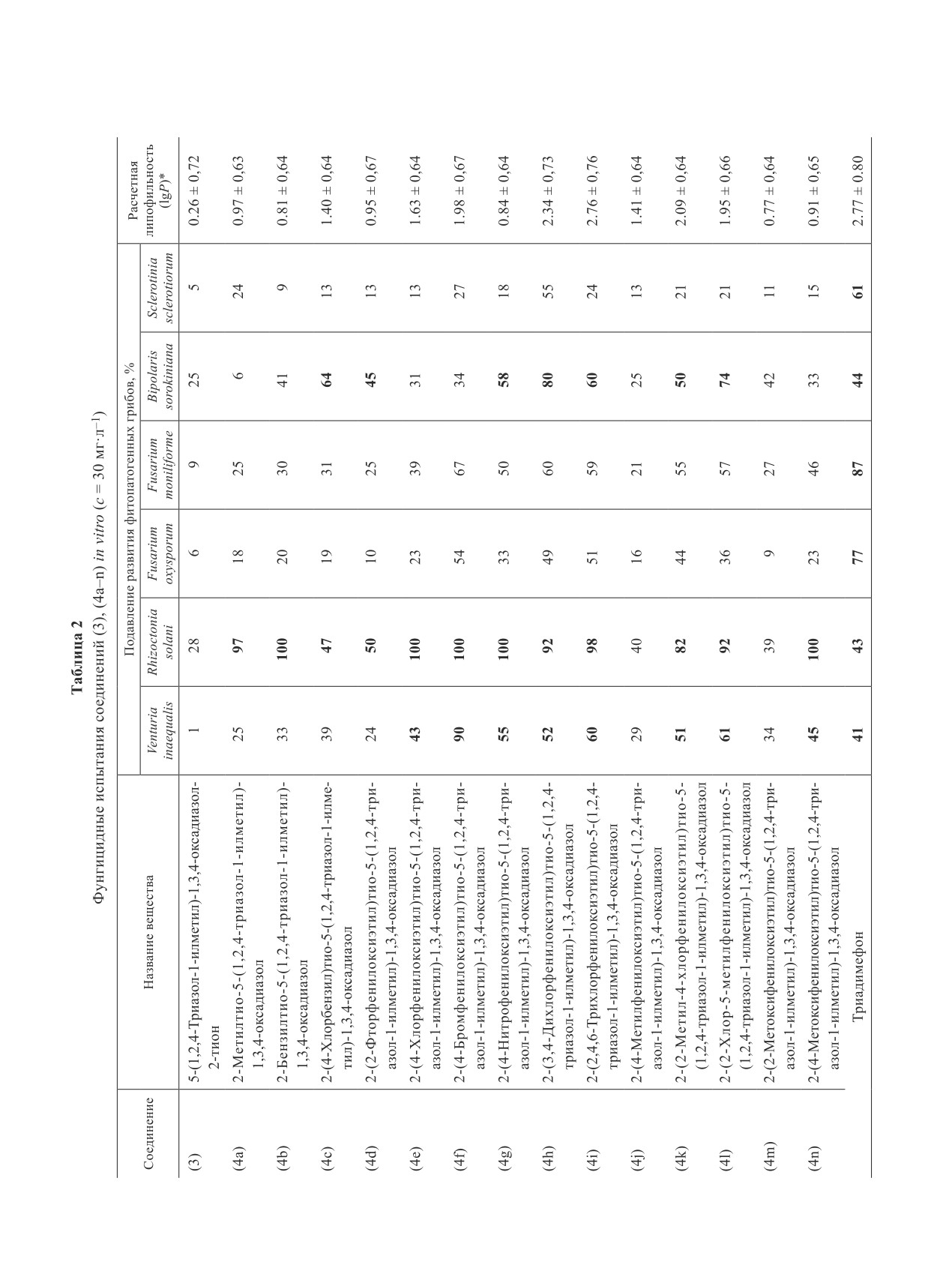
лению, выявить зависимость фунгитоксичности от
Дальнейшее алкилирование соединения (3) пер-
липофильности (изменяется от 0.84 до 2.7) в ряду
вичными алкилгалогенидами в системе триэтил-
соединений (4a-n) не удалось. Наибольшую фунги-
амин-ацетон приводит к получению ряда 2-алкилтио-
токсичность соединения этого ряда проявляют по
5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
отношению к фитопатогену Rhizoctonia solani, в ря-
(4a-n) с выходом до 90%. Алкилирование бензил-
де случаев подавляя рост его мицелия полностью
галогенидами протекает несколько медленнее, чем
(4b), (4e-g), (4n). Также по фунгицидной активности
β-бромфенетолами. Реакция бензилирования ослож-
некоторые соединения превосходят эталон триади-
няется образованием низкомолекулярных продук-
мефон по отношению к возбудителям парши яблони
тов, но позволяет получить целевые соединения с
(Venturia inaequalis) и пятнистости листьев ячменя
выходом до 90% (табл. 1). Использование в данной
(Bipolaris sorokiniana) [соединения (4c), (4g-i), (4l)].
реакции сильных оснований, таких как алкоголя-
Стоит отметить, что наибольшую активность ко всем
ты щелочных металлов, в протонных и апротонных
трем вышеупомянутым фитопатогенам проявляют
растворителях приводит к осмолению исходного
S-галогенфеноксиэтилзамещенные производные (4e),
1,3,4-оксадиазол-2-тиона (3).
(4f), (4h), (4i) (табл. 2). Арилоксиэтильный фрагмент
Введение заместителей к экзоциклическому ато-
присутствует в молекуле фунгицидного препарата
му серы значительно увеличивает как активность, прохлораз, феноксиэтилтриазолов и др., значитель-
Таблица 1
Выход 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов (4a-n)
Cоединение
Название вещества
Выход, %
(4a)
2-Метилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
57
(4b)
2-Бензилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
64
(4c)
2-(4-Хлорбензил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
42
(4d)
2-(2-Фторфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
85
(4e)
2-(4-Хлорфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
90
(4f)
2-(4-Бромфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
52
(4g)
2-(4-Нитрофенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
79
(4h)
2-(3,4-Дихлорфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
64
(4i)
2-(2,4,6-Трихлорфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
55
(4g)
2-(4-Метилфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
64
(4k)
2-(2-Метил-4-хлорфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
32
(4l)
2-(2-Хлор-5-метилфенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
60
(4m)
2-(2-Метоксифенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
71
(4n)
2-(4-Метоксифенилоксиэтил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол
66
Дизайн, синтез и фунгицидная активность 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
1001
1002
Цаплин Г. В. и др.
но увеличивая их фунгитоксичность [17]. Можно
(4e-g); М. И. Семчукова — синтез целевых 2-алкил-
ожидать, что тестирование на фунгицидное действие
тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
по отношению к другим патогенным грибам позво-
(4h-j); Е. А. Алексеева — синтез целевых 2-алкил-
лит более полно охарактеризовать синтезированные
тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4--
(4k-n); А. Л. Алексеенко — проведение фунгицидных
оксадиазолы, и наиболее активные из них смогут най-
испытаний; И. М. Чернега — получение исходных
ти применение в качестве химических средств защиты
соединений (1)-(3); С. В. Попков — разработка кон-
растений. Мы предполагаем, что полученные соеди-
цепции статьи, формулирование целей и задач.
нения действуют аналогично другим фунгицидам азо-
льного типа, селективно ингибируя фермент CYP51.
Информация об авторах
Цаплин Григорий Валерьевич, ассистент, каф. хи-
Выводы
мии и технологии органического синтеза РХТУ им.
Выявлено, что 2-алкилтио-5-(1Н-1,2,4-триазол-
Д. И. Менделеева
1-илметил)-1,3,4-оксадиазолы могут быть получены
взаимодействием 5-(1Н-1,2,4-триазол-1-илметил)-
Казаков Семён Алексеевич, бакалавр, каф. хи-
1,3,4-оксадиазол-2-тиона с алкилгалогенидами в при-
мии и технологии органического синтеза РХТУ им.
сутствии тритиламина в ацетоне при кипячении с
Д. И. Менделеева
выходом от 32 до 90%. Изучена их фунгицидная актив-
ность in vitro на шести видах фитопатогенных грибов
Семчукова Марина Игоревна, вед. инж., каф. хи-
и выявлено, что 2-алкилтио-5-(1Н-1,2,4-триазол-1-ил-
мии и технологии органического синтеза РХТУ им.
метил)-1,3,4-оксадиазолы превосходят по активности
Д. И. Менделеева
препарат сравнения триадимефон в отношении таких
фитопатогенов, как Venturia inaequalis, Rhizoctonia
Алексеева Екатерина Александровна, ассистент,
solani, Bipolaris sorokiniana. Обнаружено, что значи-
каф. химии и технологии органического синтеза
мую роль играет наличие у целевых веществ в стро-
РХТУ им. Д. И. Менделеева
ении арилоксиалкильного заместителя, значительно
повышающего фунгицидную активность 2-алкилти-
Алексеенко Анна Леонидовна, к.х.н., вед. инж., каф.
о-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов.
химии и технологии органического синтеза РХТУ им.
Синтезированный ряд соединений является важ-
Д. И. Менделеева, н. с., лаборатория № 33, Институт
ным примером предложенного нами дизайна азо-
органической химии им. Н. Д. Зелинского РАН
лов с фунгицидной активностью и показывает эф-
фективность данного химотипа, основанного на
Чернега Иван Михайлович, вед. инж., Ведущий
последовательном соединении фармакофорной груп-
научно-исследовательский институт химической тех-
пы, линкера, второго гетероцикла и липофильной части.
нологии госкорпорации «Росатом»
Попков Сергей Владимирович, к.х.н., доцент, зав.
Финансирование работы
кафедрой химии и технологии органического синте-
Работа выполнена при финансовой поддержке
за РХТУ им. Д. И. Менделеева, н.с., Всероссийский
Российского научного фонда (грант 19-73-20190).
научно-исследовательский институт фитопатологии
Конфликт интересов
Авторы заявляют об отсутствии конфликта инте-
Список литературы
ресов, требующего раскрытия в данной статье.
[1] Beckerman J., Palmer C., Tedford E., Ypema H. Fifty
years of fungicide development, deployment, and future
Информация о вкладе авторов
use // Phytopathology. 2023. V. 113. N 4. P. 694-706.
Г. В. Цаплин — синтез целевых 2-алкилтио-
[2] Roe K. How major fungal infections can initiate severe
5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
autoimmune diseases // Microb. Pathog. 2021. V. 161.
(4а-d); С. А. Казаков — синтез целевых 2-алкил-
P. 160. ID 105200.
тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
Дизайн, синтез и фунгицидная активность 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов
1003
[3]
Shafiei M., Peyton L., Hashemzadeh M., Foroumadi A.
тил)-1,2,4-триазолы, способ их получения, фун-
History of the development of antifungal azoles: A
гицидные и рострегуляторные композиции на их
review on structures, SAR, and mechanism of action
основе.
// Bioorg. Chem. 2020. V. 104. P. 1-21. ID 104240.
[11]
Zykova S. S., Tsaplin G. V., Talismanov V. S.,
Bulatov I. P., Popkov S. V., Karmanova О. Antioxidant
[4]
Bielská L., Hale S. E., Škulcová L. A review on the
activity and acute toxicity of new N4-substituted
stereospecific fate and effects of chiral conazole
5-(1,2,4-triazole-1-ylmethyl)-1,2,4-triazole-3-thiones
fungicides // Sci. Total Environ. 2021. V. 750. P. 1-13.
and S-derivatives // Int. J. Pharm. Res. 2021. V. 13.
ID 141600.
N 1. P. 309-313. ID 2021.13.01.056.
[5]
Ahmadi A., Mohammadnejadi E., Karami P.,
[12]
Zykova S. S., Talismanov V. S., Tsaplin G. V.,
Razzaghi-Asl N. Current status and structure activity
Bulatov I. P., Popkov S. V., Karmanova O. G.,
relationship of privileged azoles as antifungal agents
Savinkov A. V. Study of acute toxicity and antihypoxic
(2016-2020) // Int. J. Antimicrob. Agents. 2022. V. 59.
activity of N4-substituted 5-(1,2,4-triazole-1-
N 3. ID 106518.
ylmethyl)-1,2,4-triazole-3-thiones // Int. J. Pharm. Res.
2019. V. 11. N 3. P. 1189-1192. ID 2019.11.03.097.
[6]
Tesh S. A., Tesh J. M., Fegert I., Buesen R., Schneider S.,
Mentzel T. Innovative selection approach for a new
[13]
Ainsworth C., Jones R. G. Isomeric and nuclear-
antifungal agent mefentrifluconazole (Revysol®)
substituted β-aminoethyl-1,2,4-triazoles // J.
and the impact upon its toxicity profile // Regul.
Am. Chem. Soc. 1955. V. 77. N 3. P. 621-624.
Toxicol. Pharm. 2019. V. 106. P. 152-168. ID 141600.
ID ja01608a028.
[7]
Kazeminejad Z., Marzi M., Shiroudi A.,
[14]
Попков C. В., Алексеенко А. Л., Тихомиров Д. С.
Kouhpayeh S. A., Farjam M., Zarenezhad E. Novel
Синтез, строение и фунгицидная активность заме-
1,2,4-triazoles as antifungal agents // Biomed. Res.
щенных N2-фенилалкилиден-2-(азол-1-ил)ацетги-
Int. 2022. V. 2022. ID 4584846.
дразидов // Изв. вузов. Химия и хим. технология.
2007. Т. 50. № 6. С. 98-101.
[8]
Teixeira M. M., Carvalho D. T., Sousa E., Pinto E.
New antifungal agents with azole moieties //
[15]
Xu L., Bi W., Shang Y., Zhai Z., Yi X. Structure
Pharmaceuticals (Basel). 2022. V. 15. N 11. P. 1427.
and biological activities of novel triazole
compounds containing 1,3,4-oxadiazole ring //
[9]
Цаплин Г. В., Золотухина А. С., Алексеева Е. А.,
Chem. Res. Chin. 2008. V. 24. N 3. P. 299-302.
Алексеенко А. Л., Попков С. В. Дизайн и синтез
ID 1005-9040(08)60064-1.
2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-
тиадиазолов и их фунгицидная активность // Изв.
[16]
Методические рекомендации по определению
АН. Сер. Хим. 2023. Т. 72. N 9. С. 2125-2132
фунгицидной активности новых соединений.
[Tsaplin G. V., Zolotukhina A. S., Alekseeva E. A.,
Черкассы: НИИТЭХИМ, 1984. 34 с.
Alekseenko A. L., Popkov S. V. Design and synthesis
[17]
Popkov S. V., Kovalenko L. V., Bobylev M. M.,
of 2-alkylthio-5-(1,2,4-triazol-1-ylmethyl)-1,3,4-
Molchanov O. Y., Krimer M. Z., Tashchi V. P.,
thiadiazoles and their fungicidal activity // Russ. Chem.
Putsykin Y. G. The synthesis and fungicidal
Bull. V. 72. P. 2125-2132. ID 11172-023-4007-7.
activity of 2-substituted 1-azol-1-ylmethyl-6-
arylidenecyclohexanols // Pest. Sci. 1997. V. 49.
[10]
Пат. РФ 2668212 (опубл. 2017). N4-Замещенные
3-алкилсульфанил-5-(1,2,4-триазол-1-илме-