580
Горбунова М. Н. и др.
Журнал прикладной химии. 2023. Т. 96. Вып. 6
УДК 541.64+546.57
КОМПОЗИТЫ НА ОСНОВЕ ГУАНИДИНИЕВЫХ ПОЛИАМФОЛИТОВ
И НАНОЧАСТИЦ СЕРЕБРА
© М. Н. Горбунова1, А. В. Овчарук2, Д. М. Кисельков1, Л. М. Лемкина3
1 Институт технической химии УрО РАН — филиал ПФИЦ УрО РАН,
614013, г. Пермь, ул. Королева, д. 3
2 ПГНИУ,
614090 г. Пермь, ул. Букирева, д. 15
3 Институт экологии и генетики микроорганизмов УрО РАН — филиал ПФИЦ УрО РАН,
614081, г. Пермь, ул. Голева, д. 13
Поступила в Pедакцию 9 октября 2023 г.
После доработки 8 декабря 2023 г.
Принята к публикации 21 декабря 2023 г.
Cополимеры 2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида с акриловой, метакриловой, крото-
новой и винилуксусной кислотами были синтезированы методом радикальной сополимеризации в
присутствии радикального инициатора азобисизобутиронитрила. Боргидридным методом получены
композиционные материалы, содержащие наночастицы серебра размером от 7 до 43.5 нм в зависи-
мости от природы полимерной матрицы. Структура нанокомпозитов исследована с использованием
УФ-, ИК-, ЯМР-спектроскопии, сканирующей электронной микроскопии и рентгенофазового анализа.
Синтезированные нанокомпозиты обладают антимикробной активностью и являются перспектив-
ными для разработки новых лекарственных средств.
Ключевые слова: 2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорид; непредельные кислоты; полиам-
фолиты; наночастицы; серебро; композиты; антимикробная активность
DOI: 10.31857/S004446182306004X; EDN: SVRZRH
Создание полимерных композиционных матери-
рбционными свойствами [5]. Полигексаметилен-
алов, включающих в состав наночастицы металлов,
бигуанидин гидрохлорид представляет собой по-
является перспективным направлением материалове-
ликатионный полимер, содержащий в своей цепи
дения [1]. Для их получения в качестве второй фазы
иминный азот, поэтому он может эффективно ста-
часто используют наночастицы металлов, при этом
билизировать наночастицы серебра за счет образо-
возникает необходимость достичь равномерного рас-
вания прочной координационной связи Ag—N [6,
пределения наночастиц в объеме полимерной матри-
7]. Агрегативно устойчивые золи серебра были по-
цы и устойчивости полученных нанокомпозиционных
лучены также при использовании поли-(4,9-диокса-
материалов. Для предотвращения агрегации нано-
додекана-1,12-гуанидин)хлорида в качестве стаби-
частиц металла широко применяют стабилизаторы.
лизирующей матрицы [8]. Наличие карбоксильных,
В качестве стабилизирующей матрицы перспективно
карбонильных, азотсодержащих функциональных
использование полимеров (полистирол, полиимид,
групп в гуанидинсодержащих сополимерах способ-
полиамид, полибутадиен, полиметилметакрилат и
ствует эффективной стабилизации наночастиц ме-
др.), причем природа полимера оказывает значи-
таллов, поэтому сополимеры гуанидиниевой соли —
тельное влияние на стабильность металлических
2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида
частиц [2-4].
(АГХ) — могут выступать в качестве стабилизирую-
Известно, что полимеры на основе гуанидина
щих высокомолекулярных матриц для металлических
обладают высокими комплексообразующими и со- частиц.
Композиты на основе гуанидиниевых полиамфолитов и наночастиц серебра
581
Наночастицы серебра — наиболее изученные на-
Растворители (х.ч., ООО ПКФ «УралРеаХим»),
ночастицы для биомедицинских применений [9]. Они
используемые в работе, после очистки общеприняты-
обладают выраженными антибактериальными свой-
ми методами* имели характеристики, соответствую-
ствами, что позволяет использовать их для усиления
щие литературным данным: метанол — температура
или придания антибактериальных свойств различным
кипения 64-65°С, ацетон — температура кипения
материалам [10].
55-56°С, диэтиловый эфир — температура кипения
Цель работы — получение композитных мате-
34-35°С, тетрагидрофуран — температура кипения
риалов, матрицей в которых являются сополимеры
65-66°С, диметилсульфоксид — температура кипе-
2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида
ния 189°С.
с непредельными карбоновыми кислотами (акрило-
Сополимеризацию АГХ с непредельными кис-
вой, метакриловой, кротоновой и винилуксусной)
лотами проводили в массе и растворе органических
с включением наночастиц серебра, и исследование
растворителей при суммарной концентрации мономе-
биологической активности материалов.
ров 1 моль·л-1 в присутствии динитрила азобисизо-
масляной кислоты (3 мас%) [12]. Кинетику процесса
изучали гравиметрическим методом. При достиже-
Экспериментальная часть
нии нужной степени конверсии полимеризацию пре-
2,2-Диаллил-1,1,3,3-тетраэтилгуанидиний хлорид
рывали охлаждением и последующим осаждением
синтезировали по методике [11]. Тетраэтилмочевину
сополимеров АГХ с акриловой кислотой ацетоном,
(Alfa Aesar, кат. номер 1187-03-07), диаллиламин
сополимеров АГХ с метакриловой кислотой и с кро-
(Alfa Aesar, кат. номер 124-02-07) использовали без
тоновой кислотой диэтиловым эфиром, сополимеров
дополнительной очистки, NaOH (х.ч., ООО ПКФ
АГХ с винилуксусной кислотой тетрагидрофураном.
«УралРеаХим») использовали в виде 50%-ного вод-
Систему растворитель-осадитель подбирали для
ного раствора. Чистоту АГХ контролировали эле-
каждого сополимера индивидуально: для сополиме-
ментным анализом и методом ЯМР-спектроскопии.
ров АГХ с акриловой кислотой — метанол-ацетон;
По данным элементного анализа содержание С
АГХ с метакриловой кислотой и АГХ с кротоновой
62.42% (теор. 62.61%), Н — 10.67% (теор. 10.43%),
кислотой — метанол-эфир; АГХ с винилуксусной
N — 14.58% (теор. 14.61%) и Cl — 12.32% (теор.
кислотой — метанол-тетрагидрофуран. Очистку со-
12.35%). 1H ЯМР (ДМСО-d6), δ: 0.97-1.10 м (12Н),
полимеров проводили трехкратным переосаждением
3.03 м (8H), 3.73 т (4H), 5.26-3.34 м (4H), 5.89-6.04 м
из растворителя в осадитель. Очищенные сополи-
(2H). 13C ЯМР (ДМСО-d6), δ: 12.86, 43.59, 52.25,
меры сушили в вакууме при температуре 50°С до
120.54, 132.44, 162.64.
постоянной массы. Состав сополимеров определяли
Акриловую (98%, Alfa Aesar, кат. номер 79-10-7),
по результатам элементного анализа.
метакриловую (99%, Alfa Aesar, кат. номер 79-41-4) и
Синтез нанокомпозитов серебра и полиамфолитов
винилуксусную (96%, Alfa Aesar, кат. номер 625-38-7)
проводили следующим образом. Для получения нано-
кислоты очищали перегонкой. В работе использовали
композитов использовали сополимеры с содержанием
фракцию акриловой кислоты с температурой кипения
АГХ 40, 38, 65 и 70 мол% для АГХ-акриловая кис-
138°С и nD20 1.4202, метакриловой кислоты с темпе-
лота, АГХ-метакриловая кислота, АГХ-кротоновая
ратурой кипения 163°С, nD20 1.4309 и винилуксусной
кислота и АГХ-винилуксусная кислота соответствен-
кислоты с температурой кипения 162°С, nD20 1.4249.
но. Сополимер (1.58 г АГХ-акриловая кислота, 1.63 г
Кротоновую кислоту (транс-2-бутеновую кислоту)
АГХ-метакриловая кислота, 2.17 г АГХ-кротоновая
(Sigma-Aldrich, кат. номер 107-93-7) использовали
кислота, 2.27 г АГХ-винилуксусная кислота) рас-
без дополнительной очистки, температура плавления
творяли в 20 мл дистиллированной воды, к получен-
70-72°С.
ному раствору добавляли 1%-ный раствор AgNO3
Инициатор динитрил азобисизомасляной кислоты
(0.17 г) и перемешивали смесь в течение 1 ч при
(ч., OOO «НПФ «Кристалл») трижды перекристалли-
комнатной температуре. Затем порциями добавляли
зовывали из метанола и сушили в вакууме, темпера-
NaBH4 (0.0418 г) в течение 10 мин при постоянном
тура плавления 103°С.
перемешивании. При добавлении NaBH4 наблюда-
AgNO3 (х.ч., ООО «ПЗЦМ-Втормет») использо-
лась смена окраски от светлой до темно-коричневой.
вали в виде свежеприготовленного 1%-ного водного
раствора, NaBH4 (х.ч., ОАО «Авиабор») использовали
* Гордон А., Форд Р. Спутник химика. М.: Мир, 1976.
без дополнительной очистки.
С. 440-444.
582
Горбунова М. Н. и др.
Полученный темный раствор перемешивали в тече-
aerogenes, АТСС 13048, полученные из коллекции
ние 10 ч при комнатной температуре. Композиты вы-
ФГБУ «Научный центр экспертизы лекарственных
деляли путем диализа и сушили в вакуумном шкафу
средств» Минздрава России.
при 50°С в течение 24 ч.
Водные растворы сополимеров и нанокомпозитов
Диализ выполняли следующим образом. В мешо-
(1 мг·мл-1) стерилизовали ультрафильтрацией через
чек из регенерированной целлюлозы (2000 MWCO,
фильтры Millex-GS 0.22 мкм (Merck). Бактериальную
Sigma-Aldrich, кат. номер D2272) помещали водный
культуру помещали в 96-луночный полистироловый
раствор композита, мешочек погружали в стакан с
планшет для иммунологических реакций (AO «Фирма
бидистиллированной водой и выдерживали 24 ч.
Медполимер»). После раститровывания изучаемых
Бидистиллированная вода получена путем двойной
образцов в каждую лунку вносили по 10 мкл инокулу-
перегонки на лабораторном бидистилляторе БЭ-12
ма бактериальной культуры, содержащей 106 КОЕ/мл.
(ПФ «Ливам»).
Планшет помещали в термостат с оптималь-
ИК-спектры соединений в вазелиновом масле
ной для каждой тест-культуры температурой (для
регистрировали на спектрометре IFS 66/S Bruker.
Lactococcus lactic и Micrococcus luteus — 30°С,
Спектры ЯМР 1H и 13С регистрировали на спектро-
для остальных культур — 37°С) на 16-18 ч.
метре Bruker Avance II. Спектры записаны в режимах
Концентрацию планктонных клеток оценивали пу-
с широкополосной развязкой по протонам и в режиме
тем измерения оптической плотности при 570 нм
JMOD. В качестве растворителя использовали D2O и
(OD570) на микропланшетном ридере Benchmark Plus
ДМСО-d6 (оба — аналитической степени чистоты,
(Bio Rad Laboratories). Минимальную ингибирующую
ООО «Инновационные химические технологии»), вну-
концентрацию каждого образца определяли как наи-
тренний стандарт — тетраметилсилан (аналитический
меньшую концентрацию препарата, подавляющую
стандарт для ЯМР, Sigma-Aldrich, кат. номер 75-76-3).
видимый невооруженным глазом рост микрофлоры.
Элементный анализ выполнен на элементном анализа-
Эксперимент проводили в трехкратной повторности,
торе CHNS-9321P (Leco), навеска образца составляла
каждый раз готовили дубликаты наборов планшетов
2 мг, коэффициент вариации значений находится в
для получения точных результатов.
интервале 0.05-0.29%. Спектры поглощения реги-
стрировали на спектрофотометре UV-2600 (Shimadzu).
Обсуждение результатов
Содержание Ag в водных растворах определяли
на атомно-абсорбционном спектрометре iCE 3500
Было установлено, что при сополимеризации не-
(Thermo Fisher Scientific). Структура полученных
зависимо от среды образующиеся продукты имеют
нанокомпозитов исследована методом рентгенофазо-
статистическое распределение сомономерных зве-
вого анализа на дифрактометре XRD-7000 (Shimadzu)
ньев в макромолекуле. При сополимеризации акри-
с использованием CuKα-излучения (k = 1.54062 Å) в
ловая и метакриловая кислоты значительно активнее
интервале углов 2θ = 10°-80°. Средний размер на-
2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида,
нокристаллитов металлического серебра был рас-
поэтому при всех исходных соотношениях мономе-
считан с использованием формулы Дебая-Шеррера.
ров образующиеся сополимеры обогащены звенья-
Микрофотографии получены на сканирующем
ми акрилового мономера; в случае винилуксусной и
электронном микроскопе QUANTA FEG 650 (FEI).
кротоновой кислот сополимеры обогащены звеньями
Оценка антибактериальной активности проводи-
гуанидиниевой соли.
лась микрометодом серийных двукратных разведе-
Установлено, что в результате внутримолеку-
ний в бульоне.* Использовали тестовые культуры:
лярной циклизации сополимеризация АГХ с не-
Staphylococcus aureus, ATCC 25923; Staphylococcus
предельными карбоновыми кислотами протекает с
epidermidis, ATCC 12228; Staphylococcus cohnii, BKM
образованием симметричных стереоизомерных пир-
B-165; Streptococcus pyogenes, ATCC 8668; Bacillus
ролидиниевых циклов в полимерной цепи.
subtilis, АТСС 6633; Lactococcus lactis, NCDO 763;
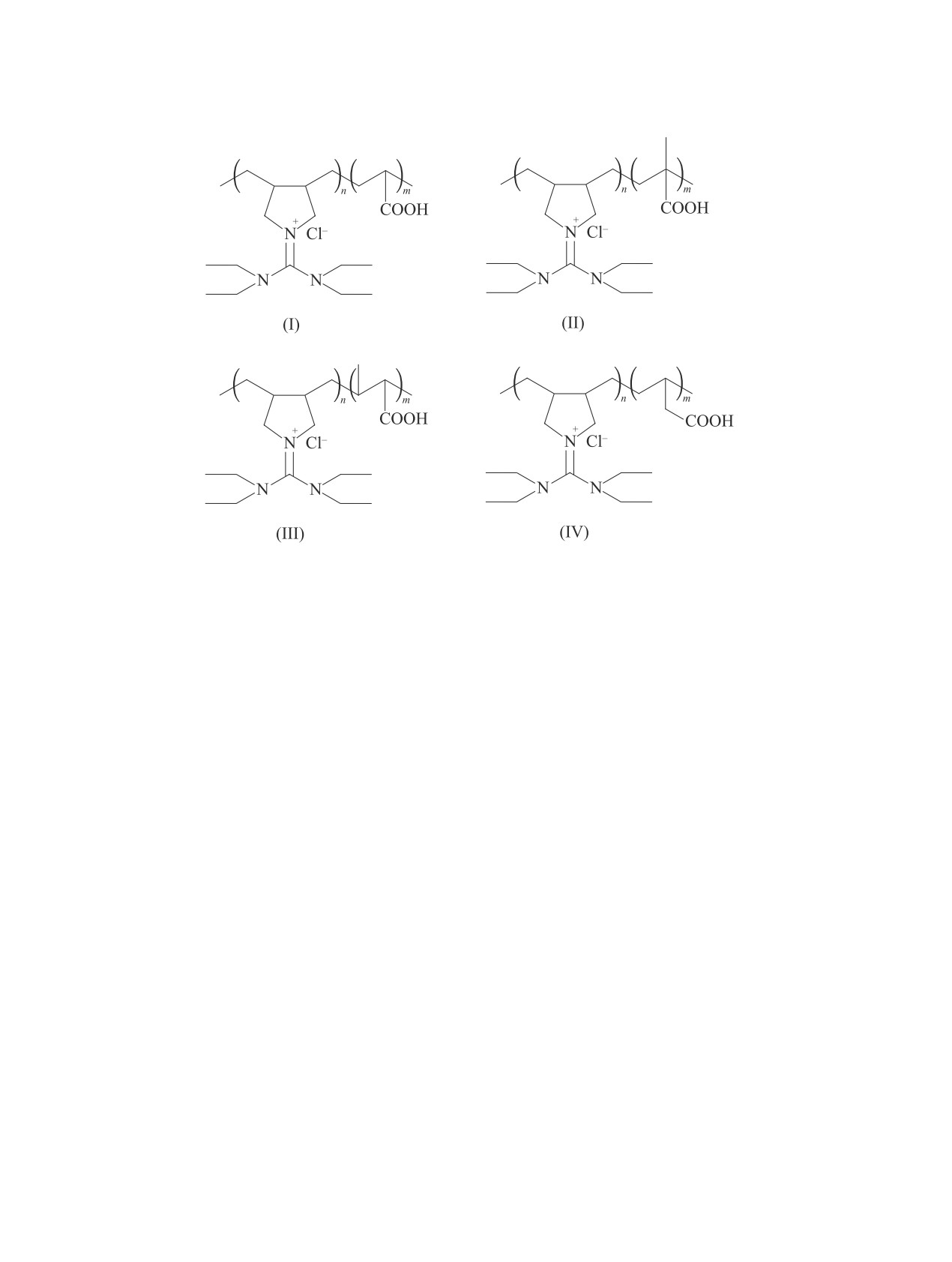
Cополимеры 2,2-диаллил-1,1,3,3-тетраэтилгуа-
Enterococcus faecalis, АТСС 29212; Micrococcus
нидиний хлорида с акриловой (I), метакриловой (II),
luteus, NCIMB 196; Escherichia coli, АТСС 25922;
кротоновой (III) и винилуксусной (IV) кислотами
Pseudomonas aeruginosa, ATCC 27853; Enterobacter
представляют собой светлые порошки. Все сополиме-
ры растворимы в воде, спирте и диметилсульфоксиде
и не растворяются в ацетоне и диэтиловом эфире, со-
* Методические указания МУК 4.2.1890-04. Опреде-
полимеры АГХ с акриловой кислотой растворяются
ление чувствительности микроорганизмов к антибактери-
альным препаратам.
также в тетрагидрофуране.
Композиты на основе гуанидиниевых полиамфолитов и наночастиц серебра
583
Добавление NaBH4 приводит к восстановлению
тоновая кислота) и 1384 см-1 (АГХ-винилуксусная
ионной формы серебра, находящегося в координа-
кислота), соответствующие валентным симметрич-
ционном взаимодействии с макромолекулами со-
ным и антисимметричным колебаниям карбокси-
полимеров, до металлического состояния, при этом
лат-аниона. Подобные изменения подтверждают вза-
постепенно цвет раствора изменяется от прозрачного
имодействие полимерной матрицы с поверхностью
до темно-коричневого.
наночастиц серебра, обеспечивающее стабилизацию
Обнаружено, что полученные нанокомпозиты рас-
последних. Взаимодействие ионов серебра возможно
творимы в воде при содержании серебра менее 12%.
с атомами азота в звеньях АГХ и кислорода в звеньях
При высоком содержании серебра (более 20%) наблю-
кислоты. Поэтому если при взаимодействии серебра
дается полная потеря растворимости, что обусловле-
с сополимерами N,N-диаллил-Nʹ-ацилгидразинов с
но усилением межмолекулярного взаимодействия за
акриловой кислотой атом азота не способен коорди-
счет связывания полимерных макромолекул с наноча-
нироваться с ионом металла и взаимодействие иона
стицами серебра под действием кооперативных сил.
серебра возможно только с двумя атомами кислорода
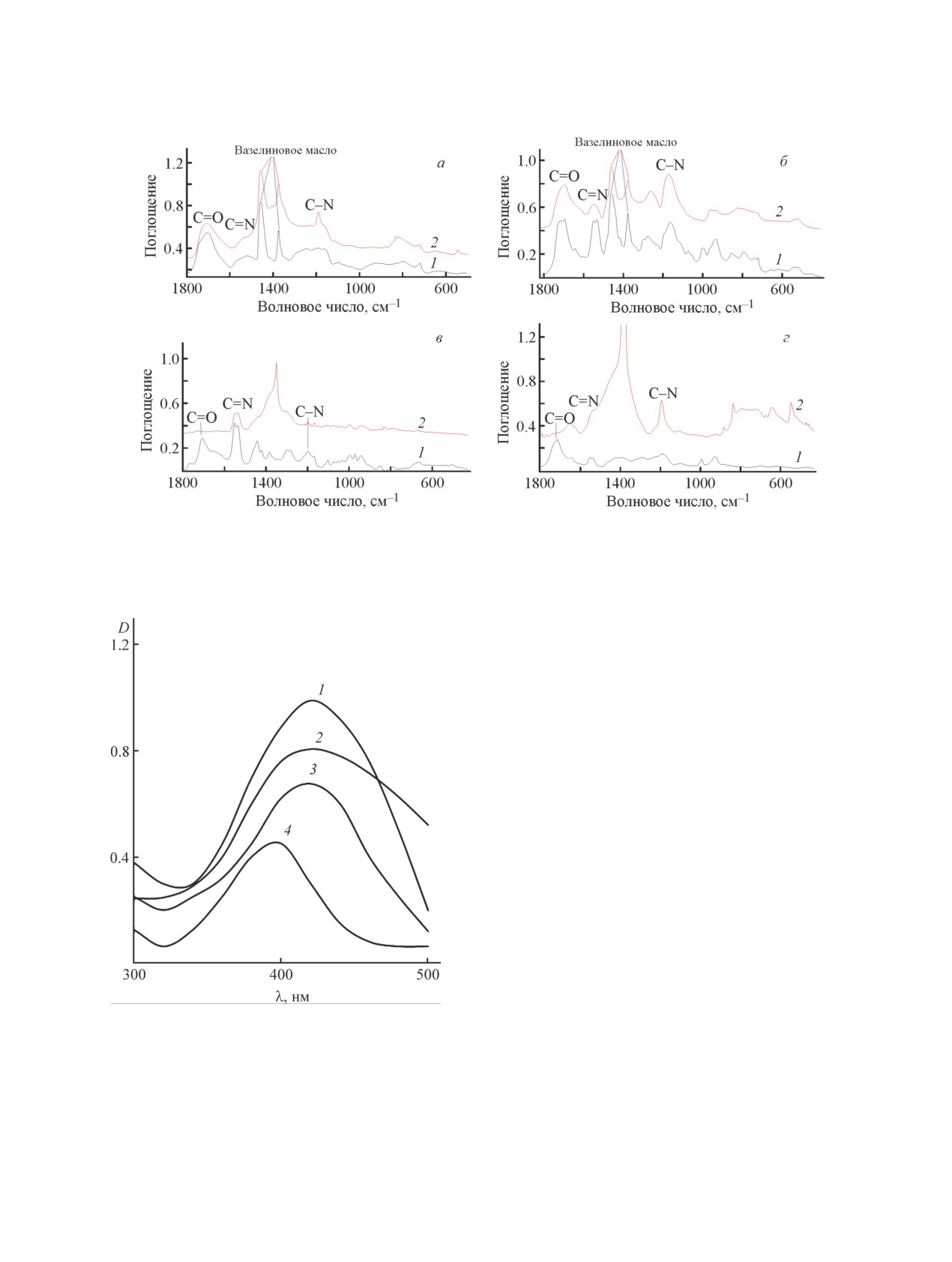
В ИК-спектрах полученных нанокомпозитов кро-
карбоксилат-аниона [13], то в случае исследуемых
ме сигналов исходных сополимеров других сигна-
полиамфолитов в стабилизации частиц участвуют и
лов не обнаружено, что в целом свидетельствует о
карбоксильная группа, и гуанидиниевая группа АГХ.
неизменности химической структуры полимерной
В электронных спектрах водных растворов на-
матрицы (рис. 1).
нокомпозитов на основе сополимеров АГХ с непре-
В ИК-спектрах нанокомпозитов на основе сополи-
дельными кислотами появляется характерная полоса
меров АГХ-метакриловая кислота и АГХ-акриловая
плазмонного поглощения, свидетельствующая об
кислота наблюдается уменьшение интенсивности
образовании серебра с размерами в нанометровом ди-
полосы поглощения валентных колебаний карбок-
апазоне. Максимум полосы плазмонного поглощения
сильной группы кислоты при 1700-1710 см-1 и поло-
растворов нанокомпозитов на основе сополимеров
сы поглощения валентных колебаний С N-группы
АГХ с акриловой, метакриловой и винилуксусной
АГХ при 1554 см-1. В ИК-спектрах нанокомпозитов
кислотами наблюдается в области 420 нм, а в случае
на основе сополимеров АГХ-кротоновая кислота и
сополимеров АГХ с кротоновой кислотой пик — в
АГХ-винилуксусная кислота практически отсутству-
области 400 нм (рис. 2).
ют полосы, соответствующие валентным колебаниям
Вид спектров поглощения свидетельствует об об-
С О-связи в области 1700 см-1, однако появляются
разовании золей изолированных наночастиц серебра
интенсивные полосы поглощения при 1350 (АГХ-кро-
[14]. При использовании сополимера АГХ-метакри-
584
Горбунова М. Н. и др.
Рис. 1. ИК-спектры сополимеров 2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида с непредельными кислотами (1)
и соответствующие им композиты серебра (2).
а — акриловая кислота, вазелиновое масло; б — метакриловая кислота, вазелиновое масло; в — кротоновая кислота,
пленка из хлороформа; г — винилуксусная кислота, пленка из хлороформа.
ловая кислота наблюдается появление длинновол-
нового крыла, что свидетельствует о присутствии
небольшой фракции агрегатов, состоящих из несколь-
ких частиц [15, 16].
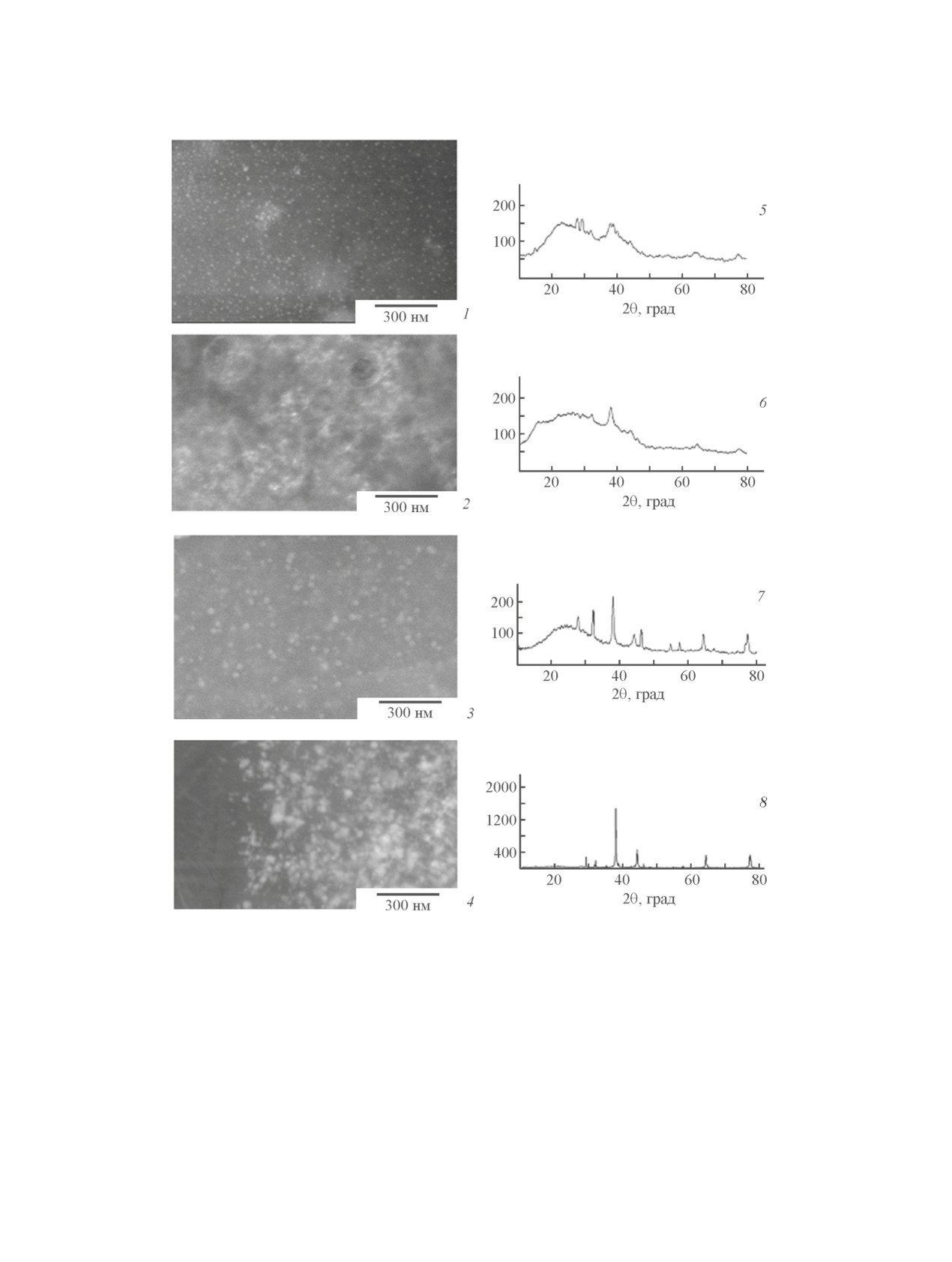
Результаты сканирующей электронной микроско-
пии подтверждают получение нанокомпозитов с уз-
кодисперсным распределением наночастиц серебра
в полимерной матрице (рис. 3). Установлено, что в
результате синтеза образуются наночастицы сфери-
ческой формы со средним диаметром 12.8, 10.0, 20.1
и 42.8 нм в присутствии сополимеров АГХ-акри-
ловая кислота, АГХ-метакриловая кислота, АГХ-
винилуксусная кислота и АГХ-кротоновая кислота
соответственно. В случае АГХ-кротоновая кислота
наблюдаются широкое распределение частиц по раз-
мерам, в нанокомпозите имеются частицы размерами
12-75 нм. При стабилизации наночастиц сополимера-
ми АГХ-винилуксусная кислота и АГХ-кротоновая
кислота наблюдается образование более крупных
Рис. 2. Спектры поглощения водных растворов нано-
композитов сополимеров с серебром: 1 — 2,2-диал- частиц, что может быть связано с низкой активностью
лил-1,1,3,3-тетраэтилгуанидиний хлорид-акриловая
винилуксусной и кротоновой кислот в реакции ради-
кислота, с = 10-3 моль·л-1; 2 — 2,2-диаллил-1,1,3,3--
кальной сополимеризации и образованием полимеров
тетраэтилгуанидиний хлорид-метакриловая кис-
с невысокой молекулярной массой [12]. Уменьшение
лота, с = 10-3 моль·л-1; 3 — 2,2-диаллил-1,1,3,3-
размеров образующихся частиц при увеличении мо-
тетраэтилгуанидиний хлорид-винилуксусная
лекулярной массы используемых сополимеров было
кислота, с = 8·10-3 моль·л-1; 4 — 2,2-диаллил-1,1,3,3--
тетраэтилгуанидиний хлорид-кротоновая кислота,
показано при применении в качестве стабилизаторов
с = 5·10-3 моль·л-1.
поли-N-винилпирролидона [16, 17], поливинилаце-
Композиты на основе гуанидиниевых полиамфолитов и наночастиц серебра
585
Рис. 3. Микрофотографии, полученные методом сканирующей электронной микроскопии (1-4), и дифрактограммы
(5-8) композитов на основе наночастиц серебра и сополимеров: АГХ-акриловая кислота (1, 5), АГХ-метакриловая
кислота (2, 6), АГХ-винилуксусная кислота (3, 7), АГХ-кротоновая кислота (4, 8).
тата [18] и при использовании сополимеров АГХ с
танные по данным рентгенофазового анализа, нахо-
винилацетатом и N-винилпирролидоном [19].
дятся в соответствии с данными, полученными по
Наличие в композитах частиц серебра наноме-
результатам сканирующей электронной микроскопии
трового размера подтверждено результатами рент-
(табл. 1).
генофазового анализа (рис. 3). На дифрактограммах
Установлено, что с увеличением содержания в
нанокомпозитов имеются интенсивные рефлексы,
составе сополимера непредельной кислоты уменьша-
характерные для плоскостей кристаллической фазы
ется размер наночастиц серебра (табл. 2). Ранее такое
металлического серебра. Значения среднего размера
влияние состава сополимера на размеры наночастиц
нанокристаллитов металлического серебра, рассчи-
серебра наблюдалось при получении композитов на
586
Горбунова М. Н. и др.
Таблица 1
Характеристики нанокомпозитов серебра на основе полиамфолитов 2,2-диаллил-1,1,3,3-тетраэтилгуанидиний
хлорида
АГХ-акриловая
АГХ-метакриловая
АГХ-винилуксусная
АГХ-кротоновая
Характеристика
кислота
кислота
кислота
кислота
Содержание кислоты в сополиме-
60
62
30
35
ре, мол%
Содержание Ag, мас%
8.8
11.7
7.4
11.3
Средний размер частиц,* нм
12.8
10.0
20.1
42.8
Средний размер частиц,** нм
8.8
7.1
17.1
43.5
* Определен методом сканирующей электронной микроскопии.
** Определен методом рентгенофазового анализа.
основе серебра и сополимеров 1-винил-1,2,4-триазо-
для наночастиц серебра. В этом случае происходит
ла и кротоновой кислоты [20]. Данный факт авторы
депротонирование карбоксильных групп и образо-
объясняют тем, что с увеличением количества кар-
вание органических ионов, ориентирующихся свои-
боксильных групп в молекуле полиамфолита изме-
ми длинными осями перпендикулярно поверхности
няется суммарный заряд макромолекулы. Высокая
металла, что приводит к увеличению содержания
концентрация отрицательно заряженных групп будет
акриловых звеньев в сополимере, сопровождающе-
приводить к их иммобилизации на положительно
муся линейным уменьшением диаметра наночастиц
заряженной поверхности серебряных наночастиц
серебра.
и, следовательно, к повышению стабилизирующей
Гуанидин и его производные обладают широким
способности полимерной матрицы за счет образова-
спектром бактерицидного действия [22], поэтому
ния защитных полимерных слоев и формированию
присутствие в исходных мономерах и в элементарных
наночастиц с меньшими размерами.
звеньях синтезированных на их основе (со)полимеров
Следует также учитывать возможность адсорбции
достаточно лабильных ионогенных гуанидинсодер-
макромолекул на наночастицах по диполь-дипольно-
жащих фрагментов должно придавать соединениям
му механизму, что было показано авторами [21] при
высокую биоцидную активность.* Ранее нами было
применении сополимеров акриловой кислоты и циа-
установлено, что сополимеры на основе 2,2-диал-
нобифенилоксиалкилакрилатов в качестве матрицы
лил-1,1,3,3-тетраэтилгуанидиний хлорида обладают
антибактериальной активностью [11, 12], в частно-
сти, показана высокая антибактериальная активность
Таблица 2
полиамфолитов АГХ в отношении грамположи-
Влияние состава сополимеров
тельных микроорганизмов [12]. Наночастицы се-
2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида
ребра также обладают антимикробной активностью
с непредельными кислотами на размер наночастиц
[10]. Мы ожидали, что введение в материал двух
серебра
биоцидных фрагментов будет усиливать антими-
Содержание
Средний размер
Кислота
кробную активность. Данное предположение было
кислоты, мол%
частиц,* нм
подтверждено. Действительно, антибактериальная
Акриловая
60
8.8
активность материалов, содержащих наночастицы
72
7.2
серебра, выше, чем в случае исходных полиамфоли-
84
6.5
тов (табл. 3).
Метакриловая
62
22.2
70
16.7
79
14.1
Кротоновая
28
57.2
35
43.5
* Encyclopedia of biomedical polymers and polymeric
Винилуксусная
19
33.5
biomaterials / Ed. by M. Mishra. New York: Taylor & Francis
Group, 2015. P. 3672-3680.
30
17.1
* Определен методом рентгенофазового анализа.
Композиты на основе гуанидиниевых полиамфолитов и наночастиц серебра
587
Таблица 3
Антибактериальная активность полиамфолитов 2,2-диаллил-1,1,3,3-тетраэтилгуанидиний хлорида
с непредельными кислотами и их композитов с наночастицами серебра
Mинимальная ингибирующая концентрация, мкг·мл-1
акриловая кислота
метакриловая кислота
винилуксусная кислота
кротоновая кислота
Тестовая культура
композит
композит
композит
композит
сополимер*
сополимер*
сополимер*
сополимер*
с серебром
с серебром
с серебром
с серебром**
Staphylococcus
31.2
15.6
250
7.8
250
62.5
125
62.5
aureus
Staphylococcus
7.8
3.9
3.9
2.9
7.8
7.8
3.9
31.2
epidermidis
Staphylococcus
125
7.8
3.9
1.9
3.9
7.8
2.9
62.5
cohnii
Streptococcus
250
62.5
125
31.2
250
62.5
125
125
pyogenes
Bacillus subtilis
31.2
15.6
125
15.6
250
62.5
125
125
Micrococcus luteus
125
7.8
31.2
7.8
125
62.5
31.2
31.2
Escherichia coli
250
31.2
250
31.2
250
125
125
125
Pseudomonas
250
125
188
125
250
125
125
125
aeriginosa
* Данные работы [12].
** В необходимой концентрации образец полностью не растворился, для исследования взята надосадочная жидкость.
Выводы
Финансирование работы
Полиамфолиты на основе 2,2-диаллил-1,1,3,3-те-
Работа выполнена при финансовой поддержке
траэтилгуанидиний хлорида и акриловой, метакри-
Российского научного фонда (грант № 23-23-00073).
ловой, кротоновой и винилуксусной кислот, полу-
ченные методом радикальной сополимеризации,
являются стабилизаторами наночастиц серебра.
Конфликт интересов
Методами сканирующей электронной микроскопии
Авторы заявляют об отсутствии конфликта инте-
и рентгенофазового анализа подтверждено образо-
ресов, требующего раскрытия в данной статье.
вание композиционных материалов с равномерным
распределением сферических наночастиц серебра в
гуанидинсодержащей полимерной матрице, облада-
Информация об авторах
ющих выраженным противомикробным действием в
отношении грамположительных и грамотрицатель-
Горбунова Марина Николаевна, д.х.н., с.н.с. ИТХ
ных микроорганизмов. Доклинические исследова-
УрО РАН
ния подобных материалов могут быть продолжены с
целью разработки новых антибактериальных лекар-
Овчарук Андрей Васильевич
ственных средств.
Кисельков Дмитрий Михайлович, к.т.н., с.н.с. ИТХ
УрО РАН
Благодарности
Авторы благодарят Центр коллективного пользо-
Лемкина Лариса Марковна, к.м.н., с.н.с. ИЭГМ
вания ПФИЦ УрО РАН «Исследование материалов и
УрО РАН
вещества» за спектральные, аналитические и биоло-
гические исследования.
588
Горбунова М. Н. и др.
Список литературы
A review // Mater. Sci. Eng. C. Mater. Biol. Appl.
2019. V. 97. P. 954-965.
[1]
Nanomaterials and polymer nanocomposites.
Raw materials to applications / Ed. by N. Karak.
[11]
Gorbunova M. N., Vorobʹeva A. I., Tolstikov A. G.,
Amsterdam: Elsevier, 2019. P. 1-121.
Monakov Yu. B. New N-allylated monomers in the
synthesis of practical valuable high-molecular-weight
[2]
Hazra Chowdhury A., Debnath R., Islam S. M., Saha T.
compounds // Polym. Adv. Tech. 2009. V. 20. N 3.
Impact of nanoparticle shape, size, and properties
of silver nanocomposites and their applications //
[12]
Gorbunova M. N., Zagumennova D. D., Lemkina L. M.
Sustainable polymer composites and nanocomposites
Novel biocidal polyampholytes with guanidinium and
/ Eds S. Inamuddin, R. Thomas, Mishra Kumar,
carboxy groups for drug delivery // Polym. Adv. Tech.
A. M. Asiri. Cham: Springer, 2019. P. 1067-1091.
2023. V. 34. N 9. P. 2961-2973.
[3]
Chumachenko V., Kutsevol N., Rawiso M., Schmutz M.,
[13]
Гoрбунова М. Н., Батуева Т. Д., Ерошенко Д. В.,
Blanck C. In situ formation of silver nanoparticles in
Кисельков Д. М. Нанокомпозиты серебра на основе
linear and branched polyelectrolyte matrices using
сополимеров N,N-диаллил-Nʹ-ацилгидразинов с
various reducing agents // Nanoscale Res. Lett. 2014.
акриловыми мономерами // ЖПХ. 2021. Т. 94. № 2.
С. 206-214.
[4]
Kang H., Buchman J. T., Rodriguez R. S., Ring H. L.,
He J., Bantz K. C., Haynes C. L. Stabilization of silver
[Gorbunova M. N., Batueva T. D., Eroshenko D. V.,
and gold nanoparticles: Preservation and improvement
Kiselkov D. M. Silver nanocomposites based on
of plasmonic functionalities // Chem. Rev. 2019.
copolymers of N,N-diallyl-Nʹ-acylhydrazines with
V. 119. P. 664-699.
acrylic monomers // Russ. J. Appl. Chem. 2021. V. 94.
N 2. P. 192-201.
[5]
Zhao P., Zhou X., Huang Y., Xu Y., Chen S., Zheng C.,
Jin Y., Xia C. Cationic covalent organic polymers
[14]
Карпов С. В., Слабко В. В. Оптические и фотофи-
based on guanidine with higher positive potential
зические свойства фрактально-структурированных
for selective sorption of ReO4-: Synthesis and DFT
золей металлов. Новосибирск: Изд-во СО РАН,
calculation // Surfaces and Interfaces. 2022. V. 29.
2003. C. 89-122.
ID 101788.
[15]
Heard S. M., Greiser F., Barraclough C. G.,
Sanders J. V. The characterization of Ag sols by electron
[6]
Guanidines as reagents and catalysts II. Topics in
microscopy, optical absorption, and electrophoresis
heterocyclic chemistry / Ed. by P. Selig. Amsterdam:
// Colloid. Interface Sci. 1983. V. 93. P. 545-555.
Springer, 2015. V. 51. P. 95-164.
[7]
Krutyakov Yu. A., Kudrinskiy A. A., Gusev A. A.,
[16]
Du B. D., Phu D. V., Duy N. N., Lan N. T. K.,
Zakharova O. V., Klimov A. I., Yaprintsev A. D.,
Lang V. T. K., Thanh N. V. K., Phong N. T. P., Hien N. Q.
Zherebin P. M., Shapoval O. A., Lisichkin G. V.
Preparation of colloidal silver nanoparticles in
Synthesis of positively charged hybrid PHMB-
poly(N-vinylpyrrolidone) by γ-irradiation // J. Expert.
stabilized silver nanoparticles: The search for a new
Nanosci. 2008. V. 3. P. 207-213.
type of active substances used in plant protection
products // Mater. Res. Express. 2017. V. 4. ID 075018.
[17]
Yin B., Ma H., Wang Sh., Chen Sh. Electrochemical
synthesis of silver nanoparticles under protection of
[8]
Кузнецов В. В., Смагина В. В., Кривощепов А. Ф.,
poly(N-vinylpyrrolidone) // J. Phys. Chem. B. 2003.
Авраменко Г. В., Катулева С. П. Синтез наночастиц
V. 107. P. 8898-8904.
серебра боргидридным методом и определение их
размеров фотон-корреляционной спектроскопией
[18]
Temgire M. K., Joshi S. S. Optical and structural studies
// Бутлеровские сообщ. 2015. Т. 44. № 11. С. 60-64.
of silver nanoparticles // Radiat. Phys. Chem. 2004.
https://www.elibrary.ru/vbfzzr
V. 71. P. 1039-1044.
[9]
types of nanoparticles, and regulatory aspects / Eds
[19]
Gorbunova M. N., Lemkina L. M. New biocide
P. Kesharwani and K. K. Singh. London: Acad. Press,
guanidine-containing nanocomposites // J. Nanopart.
2021. Ch. 10. P. 359-375.
Res. 2014. V. 16. ID 2566.
[10]
Deshmukh S. P., Patil S. M., Mullani S. B., Deleka S. D.
[20]
Поздняков А. С., Емельянов А. И. Ермакова Т. Г.,
Silver nanoparticles as an effective disinfectant:
Прозорова Г. Ф. Функциональные нанокомпози-
Композиты на основе гуанидиниевых полиамфолитов и наночастиц серебра
589
ты, содержащие триазольные и карбоксильные
ными группами // Высокомолекуляр. соединения.
группы // Высокомолекуляр. соединения. Б. 2014.
A. 2006. Т. 48. C. 1045-1057.
Т. 56. С. 226-235. https://www.elibrary.ru/tjejan
https://www.elibrary.ru/hulwsb
[Pozdnyakov A. S., Emelʹyanov A. I., Ermakova T. G.,
[Barmatov E. B., Medvedev A. S., Pebalk D. A.,
Prozorova G. F. Functional polymer nanocomposites
Barmatova M. V., Nikanorova N. A., Zezin S. B.,
containing triazole and carboxyl groups // Polym. Sci.
Shibaev V. P. The effect of silver nanoparticles on the
B. 2014. V. 56. P. 238-246.
phase state of comb-shaped liquid crystalline polymers
with cyanobiphenyl mesogenic groups. Polym. Sci. A.
[21] Барматов Е. Б, Медведев А. С., Пебалк Д. А.,
2006. V. 48. P. 665-675.
Барматова М. В., Никонорова Н. А., Зезин С. Б.,
Шибаев В. П. Влияние наночастиц серебра на фа-
[22] Sivov N. A. Biocide guanidine containing polymers.
зовое состояние гребнеобразных жидкокристалли-
Synthesis, structure and properties. London: CRC
ческих полимеров с цианобифенильными мезоген-
Press, 2006. Ch. 5. P. 140-152.