РАДИОХИМИЯ, 2020, том 62, № 2, с. 169-174
УДК 546.110.23
ВЛИЯНИЕ ОКСИДА ГРАФЕНА И УГЛЕРОДНЫХ
НАНОТРУБОК НА РЕАКЦИЮ АТОМОВ ТРИТИЯ
С ДАЛАРГИНОМ
© 2020 г. М. Г. Чернышева*, В. А. Буняев, Г. А. Бадун**
Московский государственный университет имени М.В.Ломоносова, химический факультет, кафедра радиохимии,
119991, Москва, Ленинские горы, дом 1, строение 10.
e-mail: *chernysheva@radio.chem.msu.ru; **badunga@yandex.ru
Получено 27.03.2019, после доработки 18.04.2019, принята к публикации 25.04.2019
В работе проведено изучение влияния углеродных подложек (оксид графена, восстановленный оксид
графена, одностенные углеродные нанотрубки) на результат введения трития в пептид даларгин с помо-
щью метода термической активации. Показано, что при нанесении даларгина на углеродные подложки
существенно меняется распределение трития по аминокислотным остаткам по сравнению с толстой
мишенью, нанесенной непосредственно на стеклянные стенки сосуда. Показано, что при нанесении
монослоя даларгина на изученные углеродные материалы происходит существенное увеличение со-
держание трития в фенилаланине, что свидетельствует о протекании реакции изотопного обмена по
электрофильному механизму. Также было обнаружено значительное изменение содержания трития в
других аминокислотных остатках, что связано с различием структур адсорбционных слоев пептида,
образующихся на рассматриваемых углеродных материалах.
Ключевые слова: Изотопный обмен, тритий, метод термической активации трития, даларгин
DOI: 10.31857/S0033831120020112
Использование радиоактивной метки позволяет
дить радиоактивную метку в различные вещества
изучать метаболизм различных веществ в живых
и материалы, включая аминокислоты, пептиды,
организмах [1]. Среди радионуклидов биогенных
полимеры, вирусы и углеродные наноматериалы
[17-19]. Ниже приведена схема (схема 1) протека-
элементов, применяемых для in vitro и in vivo ис-
ющих в системе реакций:
следований белков и пепетидов, тритий имеет ряд
несомненных преимуществ: период полураспада
Только реакции (1.2) и (1.4) приводят к полу-
чению меченого материнского соединения, в то
(12,3 лет) обуславливает высокую удельную ра-
диоактивность однократно-меченных соединений
Схема 1. Радикальные реакции, протекающие при тер-
1 ПБк/моль и позволяет проводить достаточно
мической активации трития.
длительные исследования; а низкая энергия β-ча-
стиц (Emax = 18.6 кэВ) и отсутствие γ-квантов не
(1.1)
требует использования защиты от внешнего облу-
(1.2)
чения. Существует множество способов введения
(1.3)
трития в органические молекулы, которые можно
разделить на химические, которые описаны в об-
(1.4)
зорах [2-4] и исследовательских статьях [5-12], и
(1.5)
физико-химические методы, включающие обра-
ботку вещества тритием в условиях высокочастот-
(1.6)
ного разряда [13], плазмы [14], ионного пучка [15]
(1.7)
и метод термической активации трития [16].
(1.8)
Метод термической активации трития, основы
которого изложены в работе [17], позволяет вво-
169
170
ЧЕРНЫШЕВА и др.
время как результатом остальных реакций являет-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
ся образование побочных продуктов или рекомби-
Материалы. В работе использовали олиго-
нация атомов трития [реакция (1.8)]. Вероятность
пептид
тирозил-D-аланил-глицил-фенилала-
протекания реакций зависит от условий проведе-
нил-лейцил-аргинина диацетат (ООО «Эллара»,
ния эксперимента, таких как температура воль-
Россия) коммерчески известный как даларгин
фрамового катализатора, давление газа, время
(PubChem CID 6917894). Использовали одностен-
экспонирования, температура мишени-вещества.
ные углеродные нанотрубки и монослойный оксид
Распределение трития в молекулах определяется
графена компании CheapTubes. Удельная поверх-
как химической природой групп, так и их стери-
ность материалов, определенная по сорбции азо-
ческой доступностью, что позволило использовать
та и рассчитанная по теории Брюнера-Эммета-
взаимодействие атомов трития с белками для ис-
Теллера, составила 570 и 60 м2/г для нанотрубок и
следования их пространственной организации -
оксида графена соответственно. Восстановленный
метод тритиевой планиграфии [20-22].
оксид графена получали по методике, описанной
Для получения высокой радиоактивности мече-
ниже. Для приготовления суспензий и растворов
ного соединения требуется полное покрытие сте-
использовали воду, очищенную с помощью систе-
клянных стенок реакционного сосуда веществом,
мы Milipore.
но часто это удается осуществить при использова-
Получение восстановленного оксида графе-
нии количества вещества много больше, чем тре-
на. Восстановление оксида графена проводили по
буется для равномерного монослойного покрытия.
модифицированной методике, описанной в работе
Как следствие не все молекулы вещества доступ-
ны для реакции с атомарным тритием, и не удает-
[27]. 30 мг оксида графена суспендировали в 15 мл
воды, добавляли 300 мг аспарагиновой кислоты,
ся получить предельно высокую удельную ради-
нагревали суспензию до 90°С и выдерживали при
оактивность меченого материнского соединения.
этой температуре 3 ч. По окончании реакции цвет
Решением проблемы может быть предварительное
нанесение вещества на подложки с развитой по-
суспензии менялся от исходно коричневого до чер-
верхностью.
ного. В качестве контроля проводили нагревание
суспензии оксида графена без добавки аспараги-
Влияние подложки на выход меченого продук-
новой кислоты. В этом случае суспензия остава-
та ранее подробно не изучалось, однако в работе
лась коричневой. Суспензию с восстановленным
[23] проведено сравнение распределения трития
оксидом графена центрифугировали в течение
в олигопептиде даларгин при активации реакции
30 мин при 21000 об./мин. Осадок декантировали,
на вольфрамовой проволоке, а также палладии и
промывали водой и высушивали.
платине, нанесенных на активированный уголь и
малослойный графит. Было показано увеличение
Введение трития в даларгин. 1 мг даларгина
содержания трития в ароматических аминокислот-
растворяли в 6.7 мл метанола. К 1 мл раствора до-
ных остатках при монослойном нанесении пепти-
бавляли 5 мг углеродного материала и подвергали
да на активированный уголь для двух способов
ультразвуковой обработке. Затем суспензию рав-
активации реакции.
номерно распределяли по стенкам реакционного
сосуда и удаляли метанол током газа.
Для дальнейшего выявления влияния подложки
на взаимодействие атомов трития с даларгином в
Сосуд с готовой мишенью присоединяли к
данной работе использовали углеродные нанома-
специальной вакуумной установке для работы с
териалы с разным содержанием функциональных
газообразным тритием и заполняли протий-трити-
групп и отличающихся структурой (оксид графе-
евой смесью, содержащей 60% трития до давления
на, восстановленный оксид графена, однослойные
0.5 Па. Вольфрамовую проволоку, расположенную
углеродные нанотрубки). Выбор даларгина обу-
в центре реакционного сосуда, нагревали электри-
словлен его строением - наличием ароматических
ческим током до 1850 K в течение 10 с. Затем отка-
и алифатических аминокислотных остатков, а так-
чивали остаточный газ с помощью форвакуумного
же его важностью в биохимических процессах в
насоса, заполняли сосуд новой порцией газовой
организме [24-26].
смеси и повторяли нагрев катализатора.
РАДИОХИМИЯ том 62 № 2 2020
ВЛИЯНИЕ ОКСИДА ГР
АФЕНА И УГЛЕРОДНЫХ НАНОТРУБОК
171
Схема 2. Получение дериватов аминокислот.
S
N
HN
R2
O
R2
H2N
S
NEt3
O
+
R1
OH
R1
C2H
OH, H2O
5
O-
Материал диспергировали в воде, удаляли три-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
тий из лабильных положений молекул двукратным
В результате обработки даларгина, нанесенно-
упариванием с помощью роторного испарителя и
го на углеродные наноматериалы, атомами трития
повторного суспендирования в воде.
в течение 10 с при температуре атомизатора 1850 К
Анализ распределения трития в аминокис-
была достигнута удельная радиоактивность от
лотных остатках даларгина. Проводили гидро-
0.57 Ки/ммоль (оксид графена) до 0.84 Ки/ммоль
лиз даларгина без удаления с углеродных нанома-
(восстановленный оксид графена и нанотрубки).
териалов [28]. Высушенный углеродный материал
Значение удельной радиоактивности хотя и выше
с нанесенным пептидом суспендировали в смеси
полученного для даларгина, нанесенного на ак-
соляной и трифторуксусной кислот (2:1 по объему)
тивированный уголь (0.47 Ки/ммоль [30]), оно
с добавкой 0.001% β-меркаптоэтанола. Гидролиз
сильно уступает величинам, достигнутым при на-
проводили в запаянных стеклянных ампулах при
несении даларгина на стеклянные стенки реакци-
155°С в течение 1 ч. Отделяли гидролизат от угле-
онного сосуда (8.4 и 31 Ки/ммоль для температуры
родного материала и удаляли компоненты гидро-
стенок 77 и 295 К [23]).
лизной смеси двукратной лиофилизацией.
Наиболее высокая удельная радиоактивность
Предколоночную дериватизацию аминокислот
даларгина была получена в работе [31] при ис-
проводили по модифицированной методике [29].
пользовании высокотемпературного твердофаз-
Лиофильно высушенную смесь аминокислот рас-
ного каталитического изотопного обмена, когда
творяли в смеси этанол-триэтиламин 2:1 по объе-
пептид наносили на Al2O3, а в качестве актива-
му и высушивали с помощью роторного испарите-
ции реакции использовали нагрев системы до
ля. Затем растворяли аминокислоты в 100 мкл сме-
140-190°С в течение 10-60 мин в присутствии 5%
си этанол-триэтиламин-вода-фенилизотиоцианат
Rh/Al2O3. При моделировании реакции на смеси
7:1:1:1 по объему и выдерживали при комнатной
водорода и трития в соотношении 1000:1 при тем-
температуре в темноте в течение ночи. Реакция де-
пературе 190°С указана удельная радиоактивность
риватизации показана на схеме 2.
323 Ки/ммоль, хотя это значение кажется завышен-
Жидкие компоненты реакционной смеси уда-
ным, так как молярная радиоактивность глицина
ляли с помощью роторного испарителя при 40°C.
70 Ки/ммоль в составе пептида превышает теоре-
Осадок растворяли в 0.5 мл воды и проводили
тически достижимую. Эксперимент с тритием при
экстракцию побочных продуктов реакции сме-
150°С позволил получить пептид с удельной ради-
сью гексан-этилацетат 7:1 по объему. При этом
оактивностью 52 Ки/ммоль.
дериваты аминокислот оставались в водной фазе.
Помимо величины удельной радиоактивности
Органическую фазу отбрасывали и экстракцию
важно знать внутримолекулярное распределение
повторяли до тех пор, пока водная фаза не станови-
трития, так как оно определяется механизмом изо-
лась прозрачной. Затем водный раствор упаривали
с помощью роторного испарителя, осадок раство-
топного обмена и зависит от химической природы
ряли в 50 мкл воды и проводили анализ с помощью
вступающего в реакцию трития. Рассмотрим изме-
высокоэффективной жидкостной хроматографии с
нение этого параметра для различных подложек,
контролем радиоактивности выходящих фракций.
на которые был нанесен пептид. Для удобства со-
Анализ проводили на колонке C18 (NovaPark), в
поставления результатов распределения трития по
качестве подвижной фазы использовали градиент
аминокислотным остаткам пептида используем
буфера AccQ Tag Eluent (Waters) и 60% ацетони-
нормирование удельной радиоактивности каждо-
трила в воде.
го остатка на удельную радиоактивность пептида,
РАДИОХИМИЯ том 62 № 2 2020
172
ЧЕРНЫШЕВА и др.
(а)
16
(б)
40
3
2
14
35
1
3
12
4
30
2
10
25
8
20
6
15
4
4
1
10
2
5
0
0
Tyr Ala Gly Phe Leu Arg
Tyr Ala Gly Phe Leu Arg
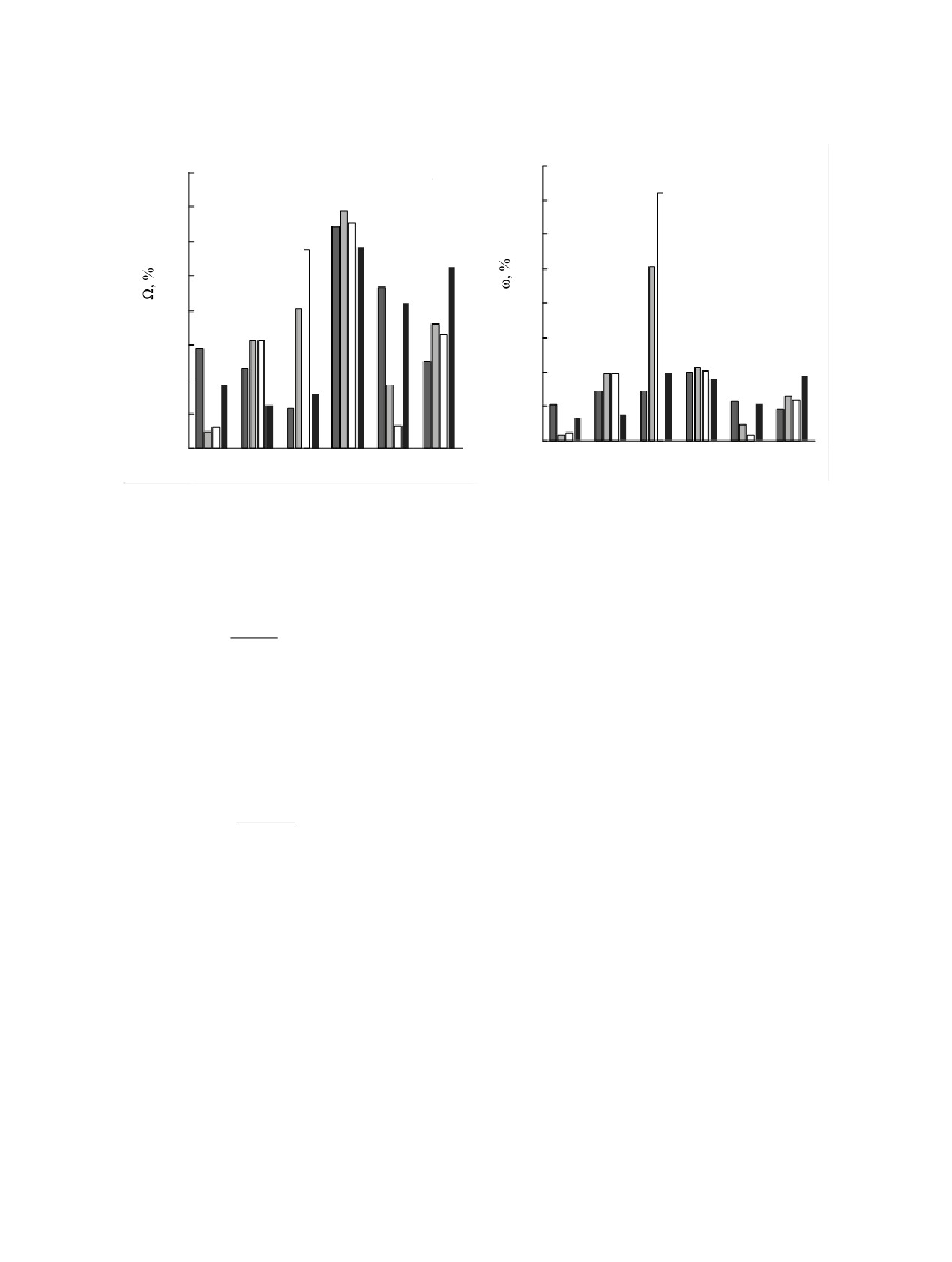
Рис. 1. Распределение трития в аминокислотных остатках даларгина на углеродных поверхностях: (1) активированный уголь
по данным работы [23], (2) оксид графена, (3) восстановленный оксид графена, (4) одностенные углеродные нанотрубки:
(а) нормирование удельной радиоактивности остатка на удельную радиоактивность пептида; (б) нормирование на число
необменных атомов водорода (С-Н) в аминокислотном остатке.
определенную как сумму удельных радиоактивно-
рованного угля - 32%. В эксперименте, описанном
стей всех остатков:
в работе [31], в фенилаланине содержалось около
30% радиоактивности. Этим самым подтвержда-
a
моль
i
Ω
=
×100%,
(2)
ется, что при нанесении пептида разреженным
∑
a
мольi
i
монослоем на углеродные материалы реализуется
удельная радиоактивность i-го аминокис-
где aмоль
электрофильный механизм реакции изотопного
лотного остатка.
обмена, что связано с взаимодействием поступа-
Для учета способности атомов водорода к изо-
ющих на мишень атомов с материалом подложки.
топному обмену в составе различных остатков ис-
В работе [23] высказано предположение, что при-
пользуем также нормировку на число необменных
сутствие значительного количества кислорода на
атомов водорода (С-Н) в аминокислотном остатке
поверхности активированного угля приводит или
a
к поляризации атома трития, либо к образованию
моль
i
ω
=
×100%,
(3)
протона на поверхности активированного угля, за
ni
∑
a
мольi
i
счет чего возрастает вероятность протекания ре-
где ni
- число необменных атомов водорода в i-ом
акции замещения по электрофильному механизму.
аминокислотном остатке.
То же самое можно сказать о поверхности оксида
На рис. 1а и 1б приведено распределение три-
графена и восстановленного оксида графена. При
тия по аминокислотным остаткам даларгина в рас-
попадании атома трития на углеродную поверх-
сматриваемых единицах.
ность происходит реакция с кислородными груп-
Важно отметить, что для всех использованных
пами поверхности с образованием кислотных цен-
углеродных наноматериалов наблюдается высо-
тров Бренстеда (-О3Н) [32], на которых возможен
кое (от 29 до 34%) содержание трития в остатке
изотопный обмен по электрофильному замеще-
фенилаланина. Ранее было показано, что при на-
нию в ароматических аминокислотных остатках
несении даларгина на стеклянные стенки в ана-
пептида. Таким образом, углеродная подложка,
логичных условиях проведения эксперимента в
адсорбируя активированный тритий, влияет на
фенилаланине содержится только 4% трития, а
механизм изотопного обмена. При образовании
при использовании в качестве подложки активи-
плотного слоя пептида на стекле реакция протека-
РАДИОХИМИЯ том 62 № 2 2020
ВЛИЯНИЕ ОКСИДА ГР
АФЕНА И УГЛЕРОДНЫХ НАНОТРУБОК
173
(а)
(б)
(в)
Рис. 2. Структура даларгина (а), и даларгина на углеродной поверхности: (б) оксид графена; (в) углеродные нанотрубки.
ет по радикальному механизму. Если стекло при
Для оценки расположения даларгина на по-
температуре жидкого азота адсорбирует водород
верхности углеродных материалов провели мо-
посредством образования химических или Ван-
делирование методом молекулярной механики с
дер-Ваальсовых связей [33], то углеродная поверх-
помощью программы HyperChem 8.0 [38] в сило-
ность способствует перемещению активных форм
вом поле AMBER. Результаты расчета приведены
водорода [34-37].
на рис. 2. Структура молекулы даларгина без уча-
Важно отметить, что доля трития в остатке фе-
стия подложки удерживается за счет образования
нилаланина мало меняется для всех рассмотрен-
внутримолекулярных водородных связей между
ных углеродных материалов. Вместе с тем обна-
остатками аргинина и глицина, а также остатками
ружено большое различие по включению трития
аргинина и фенилаланина. На поверхности оксида
в остатки глицина, лейцина и тирозина. При обра-
графена внутримолекулярные водородные связи
ботке атомами трития даларгина, нанесенного на
заменяются водородные связи между кислородом
оксид графена и восстановленный оксид графена,
поверхности и NH-группами аргинина, лейцина и
резко снижалась радиоактивность остатков лейци-
тирозина. за счет этого молекула даларгина плоско
на и тирозина, но возрастала радиоактивность гли-
«лежит» на поверхности оксида графена. Так как в
цина. Такое синхронное снижение радиоактивно-
остатке глицина расстояние между атомами азота
сти для алифатического и ароматического остатков
и углерода карбонильной группы увеличивается
нельзя объяснить только изменением механизма
от 2.49 Å (свободная молекула) до 2.68 Å (на ок-
реакции из-за изменения химического состояния
сиде графена), атомы водорода в остатке глицина
вступающего в реакцию трития. Вероятно, здесь
становятся более доступны для взаимодействия
может сказываться структурная организация моле-
с атомами трития, как поступающим из газовой
кул в адсорбционном слое.
фазы, так и диффундирующим по поверхности
Принимая во внимание площадь поверхно-
оксида графена. Также при адсорбции даларгина
сти, занимаемую даларгином, равную 2.93 нм2
на поверхности оксида графена остатки фенилала-
(PubChem CID 6917894) и удельную поверхность
нина и лейцина испытывают достаточное сильное
углеродных материалов, можно оценить плотность
взаимодействие с атомами подложки, что способ-
покрытия: оксид графена покрывается монослоем
ствует изменению механизма реакции на элек-
даларгина, а в случае нанотрубок образуется не-
трофильный. Кроме того, из-за уменьшения угла
насыщенный слой. Если молекулам даларгина до-
между ароматическим кольцом фенилаланина и
ступно только 100 м2/г поверхности нанотрубок,
алкильным радикалом лейцина от 107° (свободная
то толщина образующегося слоя близка к монос-
молекула) до 93° (на оксиде графена) возможно
лою, что видится более реалистичным для моле-
некоторое экранирование атомов водорода в остат-
кул с молекулярной массой 725.8 г/моль.
ках лейцина.
РАДИОХИМИЯ том 62 № 2 2020
174
ЧЕРНЫШЕВА и др.
При контакте даларгина с углеродной нано-
11.
Egan J.A., Filer C.N. // J. Radioanal. Nucl. Chem.
Springer Netherlands, 2016. Vol. 307, № 1. P. 549.
трубкой молекула «обворачивается» вокруг труб-
12.
Pająk M. et al. // J. Radioanal. Nucl. Chem., 2018.
ки (рис. 2в). На поверхности нанотрубок образу-
Vol. 317, № 2. P. 643.
ются внутримолекулярные водородные связи меж-
13.
Нейман Л.А., Смоляков В.С., Шишков А.В. // Итоги
ду остатками аргинина и фенилаланина, аргинина
науки и техники. Москва. Москва: Москва, 1985.
и глицина, а также тирозина и аланина. В резуль-
P. 193.
14.
Girard H.A. et al.T // Chem. Commun., 2014. Vol. 50.
тате все аминокислотные остатки не испытывают
№ 22. P. 2916.
стерических и других затруднений для реакции с
15.
Bush G.A. et al. // J. Biol. Chem., 1981. Vol. 256,
тритием и распределение трития по остаткам ста-
№ 23. P. 12213.
новится гораздо более равномерным.
16.
Филатов Э.С., Симонов Е.Ф. Физико-химические
и ядерно-химические способы получения меченых
Представленные данные показывают слож-
соединений и их идентификация. Москва: Энергоа-
ность процессов изотопного обмена трития при
томиздат, 1987. 348 p.
нанесении соединений мономолекулярным слоем
17.
Badun G.A., Chernysheva M.G., Ksenofontov A.L. //
на подложки. В результате взаимодействия атомов
Radiochim. Acta., 2012. Vol. 100. № 6. P. 401.
трития с углеродной подложкой они приобрета-
18.
Badun G.A. et al. // Radiochim. Acta., 2016. Vol. 104,
№ 8, P. 593.
ют свойства протонов, которые могут вступать в
19.
Badun G.A. et al. // Radiochim. Acta., 2014. Vol. 102,
реакцию изотопного обмена по механизму элек-
№ 10. P. 941.
трофильного замещения. Во фрагментах молеку-
20.
Tsetlin V.I. et al. T // Eur. J. Biochem., 1988. Vol. 178,
лы, не контактирующих с подложкой, возможен
№ 1. P. 123.
изотопный обмен по радикальному механизму.
21.
Agafonov D.E., Kolb V.A., Spirin A.S. // Proc. Natl.
Acad. Sci. U. S. A. National Academy of Sciences,
Поэтому для объяснения результатов необходимо
1997. Vol. 94, № 24. P. 12892.
учитывать межмолекулярные взаимодействия и
22.
Bogacheva E.N. et al. // Proc. Natl. Acad. Sci. National
структурную организацию адсорбционного слоя.
Acad. Sci., 1998. Vol. 95, № 6. P. 2790.
23.
Разживина И.А. et al. // Радиохимия., 2019. Vol. 61,
ФОНДОВАЯ ПОДДЕРЖКА
№ 1. P. 56.
Работа выполнена при поддержке Российского
24.
Plotnikov E.Y. et al. // Toxicol. Lett. Elsevier Ireland
фонда фундаментальных исследований (грант
Ltd, 2013. Vol. 220. № 3. P. 303.
№ 18-33-20147-мол-а-вед).
25.
Schroeder U., Sommerfeld P., Sabel B.A. // Peptides.,
1998. Vol. 19, № 4. P. 777.
КОНФЛИКТ ИНТЕРЕСОВ
26.
Tadzhibova L.T. et al. // Bull. Exp. Biol. Med., 2011.
Авторы заявляют об отсутствии конфликта
Vol. 150. № 3. P. 304.
27.
Tran D.N.H., Kabiri S., Losic D. // Carbon N. Y. Elsevier
интересов.
Ltd, 2014. Vol. 76. P. 193.
СПИСОК ЛИТЕРАТУРЫ
28.
Chernysheva M.G. et al. // Colloids Surfaces A
1. Lee A.J. et al. // Amino Acids., 2015. Vol. 47, № 5. P. 91.
Physicochem. Eng. Asp., 2017. Vol. 520. P. 1.
2. Saljoughian M., Williams P. // Curr. Pharm. Des., 2000.
29.
Степанов К.В. et al. // Вест. Моск. унив., Серия 2.
Vol. 6, № 10. P. 1029.
Химия, 2005. Vol. 46, № 6. P. 395.
3. Myasoedov N.F. // J. Label. Compd. Radiopharm., 1993.
30.
Разживина И.А. // Дисс. кан. хим. наук, Москва,
Vol. 33, № 5. P. 391.
2019.
4. Lockley W.J.S. // J. Label. Compd. Radiopharm., 2007.
31.
Zolotarev Y.A. et al. // Amino Acids., 2003. Vol. 24,
Vol. 50. № 5-6. P. 256.
№ 3. P. 325.
5. Shevchenko V.P., Nagaev I.Y., Myasoedov N.F. // J.
32.
Шевченко В.П., Нагаев И.Ю., Мясоедов Н.Ф. //
Label. Compd. Radiopharm., 2010. Vol. 53, № 11-12.
Радиохим., 2018. Vol. 60. № 2. P. 97.
P. 693.
33.
Филатов Э.С., Симонов Е.Ф., Орлова М.А. // Усп.
6. Kopylov A.T. et al. // Rapid Commun. Mass Spectrom.,
химии., 1981. Vol. 50. № 12. P. 1134.
2016. Vol. 30. № 11. P. 128.
34.
Prins R. // Chem. Rev., 2012. Vol. 112, № 5. P. 2714.
7. Hickey M.J. et al. // J. Label. Compd. Radiopharm.,
35.
Lipson A.G. et al. // Int. J. Hydrogen Energy. Elsevier
2007. Vol. 50. № 5-6. P. 286.
Ltd, 2012. Vol. 37, № 7. P. 5676.
8. Шевченко В.П., Нагаев И.Ю., Мясоедов Н.Ф. // Ра-
36.
Pham V.H. et al. // J. Mater. Chem. A., 2013. Vol. 1,
диохим., 2012. Vol. 54, № 1. P. 75.
№ 4. P. 1070.
9. Kozlowska M., Kanski R., Kanska M. // J. Label. Compd.
37.
Silambarasan D. et al. // ACS Appl. Mater. Interfaces.,
Radiopharm., 2005. Vol. 48, № 3. P. 23.
2013. Vol. 5, № 21. P. 11419-11426.
10. Zhang Y. // J. Label. Compd. Radiopharm., 2017. Vol.
38.
Pazun J.L. // J. Chem. Inf. Model., 1993. Vol. 33,
60. № 13. P. 608.
№ 6. P. 931.
РАДИОХИМИЯ том 62 № 2 2020