РАДИОХИМИЯ, 2020, том 62, № 4, с. 312-317
УДК 546.799.3
ФОТОЛИЗ ИОНОВ НЕПТУНИЯ В РАСТВОРАХ
HCOOH
© 2020 г. А. В. Гоголев*, В. П. Шилов, В. П. Перминов, А. М. Федосеев
Институт физической химии и электрохимии им. А. Н. Фрумкина РАН, 119071, Москва, Ленинский пр., д. 31, корп. 4.
*e-mail: gogolev@ipc.rssi.ru
Получена 13.05.2019, после доработки 16.10.2019, принята к публикации 16.10.2019
Спектрофотометрическим методом изучены валентные превращения ионов нептуния в муравьинокис-
лых водных растворах под действием излучения ртутной лампы. Показано, что ионы Np(VI) за ~ 10 мин
восстанавливаются до Np(IV), содержащего небольшое количество Np(V). Ионы Np(V) в растворах и
взвесях также эффективно восстанавливаются до Np(IV). При фотолизе растворов Np(IV) появляется
Np(III). В 99.7%-ной HCOOH превращение Np(IV) → Np(III) происходит почти полностью. Ионы Np(III)
неустойчивы и переходят в Np(IV) при хранении. Гидролиз и полимеризация Np(IV) препятствуют вос-
становлению Np(IV) в 1 моль/л HCOOH.
Ключевые слова: нептуний(VI, V, IV, III), муравьиная кислота, фотолиз
DOI: 10.31857/S0033831120040048
Окислительно-восстановительные
(редокс)
кислот [1, 2]. Известны также работы по фотолизу
реакции имеют важное значение в химии трансу-
карбонатных растворов нептуния [3]. Еще одной
рановых элементов. Они являются основой про-
перспективной средой для проведения фотохи-
цессов выделения и очистки целевых продуктов в
мических процессов являются водные растворы
технологических и лабораторных процессах. Од-
муравьиной кислоты, так как продукт окисления
ним из способов инициирования редокс-процес-
HCOOH - углекислый газ - удаляется из реакци-
сов является фотолиз. Фотохимические превраще-
онного объема. В настоящей работе изучены фото-
ния ионов 5f-элементов, в том числе нептуния, в
химические превращения ионов нептуния в сме-
водных растворах обсуждались в обзоре [1]. При-
сях HCOOH-H2O под действием света ртутных
менительно к топливному циклу фотохимические
ламп ДРК-120.
превращения ионов нептуния обсуждаются в ра-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
боте [2]. Имеющий устойчивые степени окисления
состояния от 3+ до 6+ нептуний является удобным
В работе использовали HClO4 и LiHCOO квали-
и информативным объектом для изучения фотохи-
фикации х.ч. и 99.7%-ную HCOOH (HCOOHконц)
мических превращений комплексных соединений
квалификации ч.д.а. 237Np очищали анионообмен-
5f-элементов в различных средах. Высокая устой-
ным методом и осаждением оксалата. Водные рас-
чивость оксокатионов Np(V) в воде и водно-орга-
творы перхлоратов шести- и пятивалентного 237Np
нических средах и, напротив, резкое снижение его
готовили по использованным ранее методикам
устойчивости при небольшом содержании Н2O в
[4, 5]. Для УФ облучения растворов применяли
органических растворителях затрудняют прогно-
установку ВИО-1 с двумя лампами ДРК-120. Облу-
зирование фотохимических превращений и стаби-
чение и регистрацию спектров растворов проводи-
лизации различных валентных состояний в таких
ли в кварцевых спектрофотометрических кюветах
средах.
с тефлоновыми пробками с длиной оптического
До настоящего времени различные авторы из-
пути 1 см. Контроль присутствия валентных форм
учали фотохимические превращения ионов неп-
нептуния в облучаемых растворах осуществляли
туния преимущественно в растворах сильных
на спектрофотометре Shimadzu-UV 3100. Перед
312
ФОТОЛИЗ ИОНОВ НЕПТУНИЯ В Р
АСТВОРАХ HCOOH
313
регистрацией спектров в нептунийсодержащие
свидетельствует положение максимума полосы
муравьинокислые растворы добавляли HClO4 до
поглощения при λmax ~ 1237 нм. При уменьшении
концентрации ~1 моль/л для устранения нало-
концентрации HCOOH до 10 моль/л (и соответ-
жения полос поглощения Np(V) (λmax ~ 980 нм)
ствующем увеличении концентрации H2O) λmax
и гидролизованного Np(IV) (λmax ~ 974-976 нм).
смещается до 1225 нм, т.е. приближается к по-
Для расчета концентрации Np(V) в запасном рас-
ложению, характерному для аква-иона NpO22+. В
1 моль/л HCOOH λmax ~ 1223 нм, т.е. соответствует
творе использовали коэффициент погашения в
положению аква-иона Np(VI) [6].
максимуме около 980 нм, равный 395 л/(моль·см) [6].
Наличие интенсивной полосы поглощения в
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
УФ части спектра способствует эффективной фо-
Известно, что муравьиная кислота и формиат-
тоактивации ионов Np(VI) под действием УФ из-
ионы проявляют восстановительные свойства в
лучения ртутной лампы. Относительно устойчи-
реакциях со многими ионами металлов. Однако
вый при комнатном освещении Np(VI) (1 ммоль/л)
ионы Np(VI) в кислых водных растворах, содер-
под действием УФ излучения был полностью вос-
жащих муравьиную кислоту, относительно устой-
становлен до Np(IV) с небольшой примесью Np(V)
чивы, и для проведения реакций (1) и (2) в 0.1-
за 10 мин в 99.7%-ной и 10 моль/л HCOOH. В
4.0 моль/л HClO4, содержащей 0.001-1.0 моль/л
1 моль/л HCOOH, содержащей 1 ммоль/л Np(VI),
HCOOH, применяют катализаторы [7]
для завершения реакций (1) и (2) потребовалось
~25 мин. Следовательно, нептунил-ионы эффек-
2NpO22+ + HCOOH → 2NpO2+ + CO2 + 2H+,
(1)
тивно активируются УФ излучением и окисляют
NpO22+ + 3HCOOH → Np4a+q + CO2 + 2H2O + 2HCOO-. (2)
HCOOH (HCOO-). По аналогии с фотохимически-
Поэтому первоначально была проверена устой-
ми реакциями уранил-ионов можно представить
чивость Np(VI) в 99.7%-ной HCOOH при темпера-
механизм превращения возникающих в процессе
туре 22-29°С и рассеянном комнатном освещении.
поглощения УФ излучения NpO22+ + hν → *NpO22+
В растворе, содержащем 1.5 ммоль/л Np(VI), за
фотовозбужденных нептунил-ионов *NpO22+ в виде
время хранения 170 мин оптическая плотность в
двух реакций
полосе поглощения Np(V) (D980) возросла от 0.03
*NpO22+ + HCOO- (HCOOH) → NpO2+ + COOH (+ H+), (3)
до 0.04. В 10 моль/л HCOOH D980 возросла от 0.025
NpO22+ + COOH → NpO2+ + CO2 + H+ (k3).
(4)
до 0.028 за 94 мин. В 1 моль/л HCOOH растворе,
Нептунил-ионы в отличие от уранил-ионов не
содержащем первоначально Np(VI) (D1223 = 0.04)
имеют долгоживущего возбужденного состояния,
и Np(V) (D980 = 0.034) за время хранения 122 ч
однако присутствие молекул муравьиной кислоты
в темноте при температуре 5°С D980 увеличилась
либо формиат-ионов в их координационной сфере
до 0.045. Рост D980 свидетельствует о протекании
обеспечивает эффективный внутрисферный пе-
в растворах HCOOH реакции (1) даже в темновых
ренос электрона от лиганда к металлу. Скорость
условиях, однако этот процесс достаточно медлен-
реакции (4) контролируется диффузией [8]. Если
ный. Так как в неводных и смешанных растворите-
реакция (3) протекает внутрисферно, то можно
лях усиливается тенденция ионов NpO2+ к диспро-
предположить, что часть возникших ион-ради-
порционированию, была проверена устойчивость
кальных пар претерпевает последующее превра-
Np(V) в 99.7% HCOOH и в 10 моль/л HCOOH.
щение согласно реакции (5)
Обнаружено, что диспропорционирование Np(V)
NpO2+(COOH) +3HCOOH
происходит чрезвычайно медленно даже в присут-
→ Np4+ + CO2 + 2H2O + 3HCOO-.
(5)
ствии 0.9 моль/л HClO4. Предварительные опыты
показали, что за время проведения фотохимиче-
Появившийся Np(IV) в начальной стадии фото-
ских экспериментов темновые реакции с участием
лиза реагирует с Np(VI)
ионов NpO22+ и NpO2+ не вносят заметный вклад в
NpO22+ + Np4+ → 2NpO2+ + 4H+.
(6)
наблюдаемые процессы.
Снижение концентрации Np(VI) замедляет ре-
Ионы Np(VI) в HCOOHконц, по-видимому,
акцию (6), и в муравьинокислом растворе в про-
сольватированы молекулами муравьиной кисло-
цессе фотолиза накапливается смесь ионов Np(V)
ты или образуют формиатные комплексы. Об этом
и Np(IV).
РАДИОХИМИЯ том 62 № 4 2020
314
ГОГОЛЕВ и др.
Рис. 2. Деполимеризация Np(IV)p в растворе, содер-
жащем 0.91 моль/л HClO4, 0.91 моль/л HCOOH и
1.4 ммоль/л [Np(IV)]. 1 - cпектр исходного раствора с
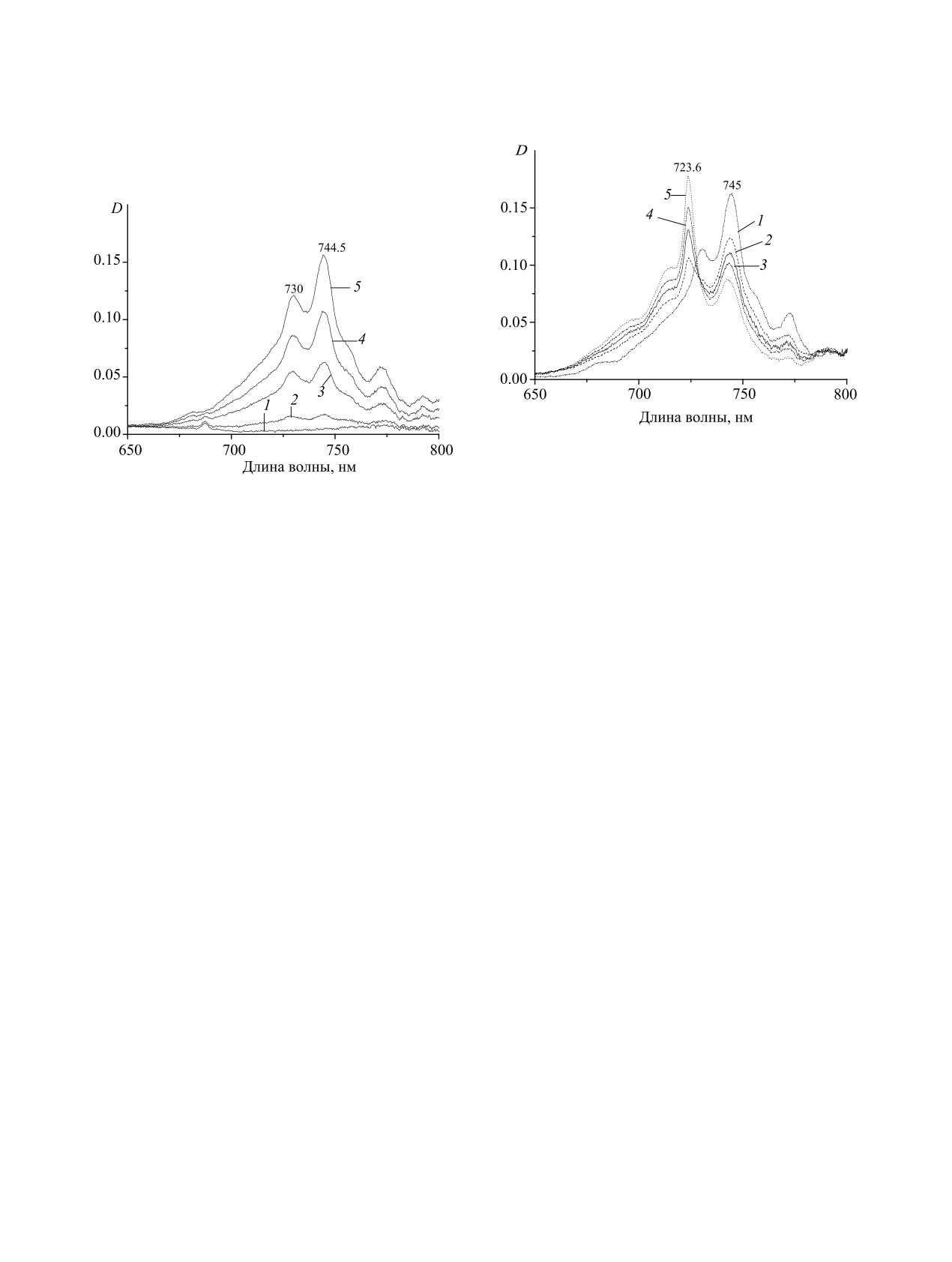
Рис. 1. Накопление Np(IV)p при УФ облучении рас-
[HCOOH] = 1 моль/л и [Np(V)] = 1.6 ммоль/л/ Время,
творов, содержащих 1 моль/л HCOOH и 1.6 ммоль/л
прошедшее после добавления 10 моль/л HClO4 τ (мин):
Np(V). Στобл (мин): 1 - 0, 2 - 5, 3 - 10, 4 - 15, 5 - 120.
2 - 5, 3 - 10, 4 - 22, 5 - 44.
Небольшая растворимость нептуния(V) в
ния ионами Np(IV), форма существования кото-
HCOOHконц затрудняет изучение фотолиза таких
рых изменяется в процессе фотолиза. В 99.7%-ной
растворов. После добавления раствора NpO2ClO4
и 10 моль/л HCOOH эти изменения протекают и
к HCOOHконц из расчета 0.8 ммоль/л Np(V) была
после завершения УФ облучения.
получена тонкодисперсная взвесь, содержащая в
УФ облучение муравьинокислых растворов, со-
спектре характерную для нептуноил-иона полосу
держащих Np(VI) или Np(V), приводит к их пол-
поглощения с λmax ~ 980 нм и добавочные полосы
ному превращению в Np(IV). Однако форма полос
с λmax ~ 1004 и 1116 нм. Также в спектре присут-
и положение λmax в спектре таких растворов свиде-
ствовала очень небольшая полоса с λmax ~ 731-
тельствуют об отсутствии в них после завершения
732 нм, характерная для Np(IV). За первые 5 мин
фотолиза аква-ионов Np(IV). Аналогичные спек-
УФ облучения характерное для Np(IV) погло-
тральные характеристики муравьинокислых рас-
щение исчезло и появилось за последующие
творов Np(IV), представленные в статье [9], сви-
5 мин. Затем накопление Np(IV) резко ускорилось.
детельствуют, по мнению авторов, о нахождении
Взвесь и осадок за время фотолиза растворились и
Np(IV) в растворах с pH > 2.3 в виде гексаядерных
при суммарном времени облучения Στобл = 30 мин
комплексов Np6(μ-HCOO)12(μ3-O)4(μ3-OH)4, содер-
раствор содержал только Np(IV).
жащих формиат-ионы и гидроксильные мостики.
В
1 и
10 моль/л HCOOH, содержащей
Эта структура подтверждена результатами EXAFS
1.6 ммоль/л Np(V), его полное превращение в
спектроскопии. В более кислой области гексамер
Np(IV) завершалось за 25-30 мин. В растворах, со-
находится в равновесии с гидроксоформиатным и
держащих первоначально Np(V), после появления
гидроксокомплексами Np(HCOO)(OH)2+, Np(OH)22+
в растворе четырехвалентного нептуния отчетливо
и Np(OH)3+. Работа [9] была выполнена в рас-
наблюдается ускорение процесса (7).
творах с суммарной концентрацией [HCOOH] +
2NpO2+ + 7HCOOH → 2Np4+ + CO2 + 6HCOO- + 4H2O. (7)
[HCOO-] = 1 моль/л. В более концентрирован-
Этот факт объясняется наличием у ионов
ных растворах HCOOH возрастает вероятность
Np(IV) более интенсивных полос поглощения
нахождения большего числа формиат-ионов и
в УФ области по сравнению с Np(V) и HCOOH.
меньшего числа гидроксильных ионов в коорди-
Последующие фотохимические превращения осу-
национной сфере Np(IV). Однако форма спектров
ществляются вследствие поглощения УФ излуче-
и положение λmax свидетельствуют о присутствии
РАДИОХИМИЯ том 62 № 4 2020
ФОТОЛИЗ ИОНОВ НЕПТУНИЯ В Р
АСТВОРАХ HCOOH
315
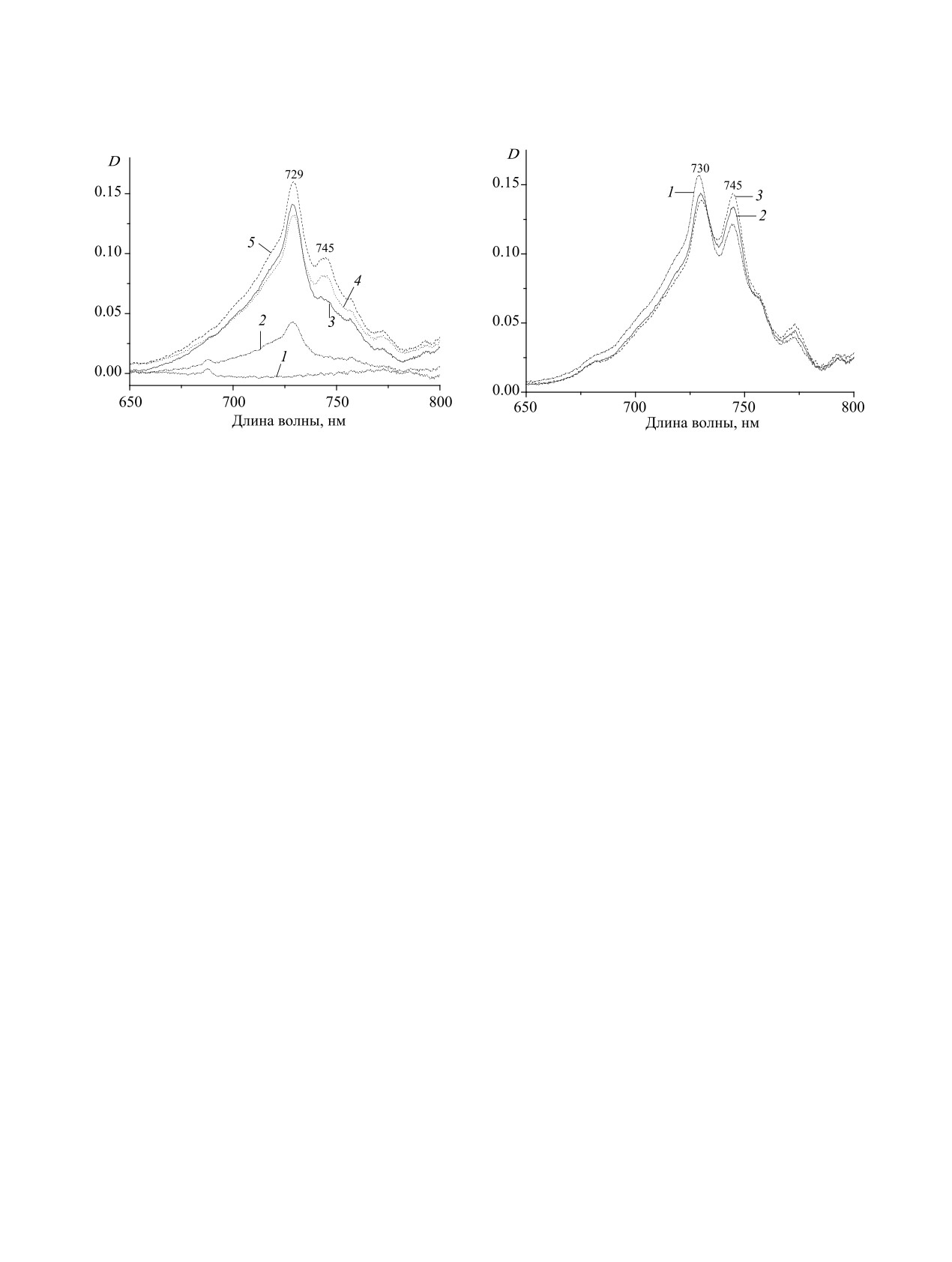
Рис. 3. Накопление Np(IV)p при УФ облучении рас-
Рис. 4. Спектры растворов, содержащих 10 моль/л
творов, содержащих 10 моль/л HCOOH и 1.6 ммоль/л
HCOOH и 1.6 ммоль/л Np(IV) (1) и 0.1 моль/л LiHCOO.
Np(V). Στобл (мин): 1 - 0, 2 - 5, 3 - 10, 4 - 10 (+55 мин
Время прошедшее после добавления LiHCOO τ (мин):
без УФ облучения), 5 - 15.
2 - 45 мин, 3 - 4 ч 15 мин.
в растворах полимерных частиц даже в 99.7%-ной
ностей D744/D723.6. Полоса поглощения приобре-
HCOOH. Относительно медленное образование
тает вид с одним явно выраженным максимумом.
и диссоциация гексамерных комплексов Np(IV)
В содержащих 1.6 ммоль/л Np(V) растворах в
были зарегистрированы нами во время и после
10 моль/л HCOOH УФ облучение также приводит
прекращения фотолиза и после подкисления УФ
к накоплению Np(IV), однако спектральные изме-
облученных растворов соответственно.
нения в таких растворах (рис. 3) отличаются от по-
В процессе фотолиза растворов Np(V), в
казанных выше для растворов 1 моль/л HCOOH.
1 моль/л HCOOH, возникающий Np(IV)p имеет
Наличие в спектре полосы одного максимума с
спектр, характерный для гексамерного комплекса
λmax = 729 нм позволяет предполагать, что Np(IV)
Np6(μ-HCOO)12(μ3-O)4(μ3-OH)4 (рис. 1).
возникает в виде моноядерного иона, содержаще-
го в координационной сфере несколько формиат-
Соотношение D744/D730 для спектра 5 составля-
ионов или молекул недиссоциированной муравьи-
ет 1.29, что меньше аналогичной величины ~ 1.38
ной кислоты.
(pH 2.47), оцененной по Fig. S1 в дополнительной
информации к статье [9], и подтверждает непол-
Скорость полимеризации возникающего в ре-
ную полимеризацию Np(IV) за время фотолиза.
акции (7) Np(IV) заметно меньше, чем в растворах
Через 20.5 ч хранения при комнатной температуре
1 моль/л HCOOH. Величина D744/D730 не достигает
D744/D730 составляет 1.43, т.е. Np(IV) полностью
полученного в 1 моль/л HCOOH значения даже че-
перешел в полимерную форму Np(IV)p (рис. 2,
рез 18.5 ч (рис. 4, спектр 1).
спектр 1).
Внесение в раствор формиата лития вызывает
Прибавление к содержащим гидролизован-
дальнейшие изменения спектра, однако даже через
ный Np(IV)p растворам HClO4 до концентрации
19.5 ч (рис. 5, спектр 1) D744/D730 = 1.05, т.е. Np(IV)
0.9 моль/л HClO4 вызывает трансформацию спек-
не переходит полностью в полимерную фор-
тра, показанную на рис. 2. За 44 мин форма поло-
му в растворе, содержащем 10 моль/л HCOOH +
сы поглощения в области 650-800 нм приобретает
0.1 моль/л LiHCOO.
вид, характерный для Np(IV)aq, возможно находя-
В HCOOHконц, содержащей Np(VI) или Np(V),
щегося в равновесии с моноформиатным комплексом.
возникающий при УФ облучение спектр растворов
Из рис. 2 видно, что максимум с λmax = 730 нм за
имеет один явно выраженный максимум и может
время смешивания смещается до 723.6 нм и имеет
быть отнесен к смеси моноядерных формиатных
место изменение соотношения оптических плот-
комплексов Np(IV). Подтверждением этому явля-
РАДИОХИМИЯ том 62 № 4 2020
316
ГОГОЛЕВ и др.
Рис. 5. Деполимеризация Np(IV)p в растворе, со-
держащем 0.91 моль/л HClO4, 9.1 моль/л HCOOH и
1.4 ммоль/л [Np(IV)]. 1 - спектр исходного раствора,
Рис. 6. Спектры HCOOHконц, содержащей 0.85 ммоль/л
содержащего 10 моль/л HCOOH и 1.6 ммоль/л Np(IV).
Np(IV) до (1) и после (2) УФ облучения в течение
Время, прошедшее после добавления 10 моль/л HClO4,
120 мин. Полосы Np(III) имеют λmax 556, 607, 663 и
τ (мин): 2 - 5, 3 - 15, 4 - 21, 5 - 3 ч 50 мин.
786 нм.
ется смещение λmax до ~ 725 нм. Вследствие не-
УФ облучение 10 моль/л HCOOH, содержащей
достатка H2O возможна также пересольватация
1.6 ммоль/л Np(IV), также вызывает появление в
ионов Np(IV) молекулами недиссоциированной
растворе Np(III). После 85 мин хранения в темно-
муравьиной кислоты. Однако уже в процессе фо-
те при комнатной температуре Np(III) в спектро-
толиза спектр Np(IV) изменяет вид. Наблюдается
фотометрической кювете отсутствовал, вероятно,
рост максимума с λmax =745.8 нм. Максимум с λmax
вследствие окисления проникающим в кювету
725 нм смещается до 732.5 нм и интенсивность
кислородом.
его заметно снижается. Такое изменение спектра
В отличие от растворов с высокой концентра-
продолжается и после завершения УФ облучения.
цией HCOOH накопление Np(III) при фотолизе
Величина D745.8/D732.6 = 0.95, полученная через
растворов Np(IV)p в 1 моль/л HCOOH не проис-
20 ч хранения раствора при комнатной температу-
ходит в течение 120 мин. Полученный после УФ
ре, значительно меньше D744/D730 = 1.43 в 1 моль/л
облучения раствор имеет полосу поглощения с
HCOOH и D744.5/D729 = 1.29 в 10 моль/л HCOOH.
По-видимому, процесс полимеризации Np(IV) →
λmax = 974 нм и группу полос c наиболее интен-
Np(IV)p затрудняет большая концентрация
сивными максимумами при 744 и 730 нм. Затем к
HCOOH и соответственно недостаточная концен-
муравьинокислому раствору Np(IV) была добав-
трация H2O. Внесение HClO4 до концентрации
лена 10 моль/л HClO4 в количестве, необходимом
0.9 моль/л в 10 моль/л HCOOH, содержащую
для подавления диссоциации HCOOH и гидро-
Np(IV)p вызывает спектральные изменения, пока-
лиза Np(IV). Общий вид спектра в области 600-
занные на рис. 5. В спектре Np(IV) после заверше-
800 нм приобретает вид, характерный для аква-ио-
ния деполимеризации λmax = 726 нм.
нов Np(IV). В длинноволновой части спектра исче-
УФ облучение растворов Np(IV) в HCOOHконц
зает полоса поглощения с λmax = 974 нм и появля-
вызывает изменение спектра раствора вследствие
ется принадлежащая Np(IV)aq полоса поглощения
превращения Np(IV) в Np(III) (рис. 6).
с λmax = 960 нм. После хранения этого раствора в
За первые 50 мин УФ облучения спектр 1
спектрофотометрической кювете в течение ~20 ч
на рис. 6 не изменился, за последующие 70 мин
в спектре появилась полоса с λmax = 980 нм, при-
Np(IV) восстановился до Np(III). При дальнейшем
надлежащая Np(V). Последующее УФ облуче-
УФ облучении до Στобл = 180 мин из раствора вы-
ние раствора, содержащего 0.91 моль/л HClO4,
пал осадок, вероятно формиат нептуния(III).
0.91 моль/л HCOOH,
~0.52 ммоль/л Np(IV) и
РАДИОХИМИЯ том 62 № 4 2020
ФОТОЛИЗ ИОНОВ НЕПТУНИЯ В Р
АСТВОРАХ HCOOH
317
~0.39 ммоль/л Np(V), приводит к появлению в
Полученные результаты показывают, что под
спектре полос поглощения, характерных для
действием УФ излучения в муравьинокислых
Np(III). После 90 мин фотолиза концентрация
растворах стабилизируется Np(IV). Соотношение
Np(III) составляла ~0.39 ммоль/л. Из полученных
концентраций полимерных (возможно гексамер-
результатов следует, что полимерный Np(IV)p не
ных) и мономерных комплексных ионов нептуния
восстанавливается фотохимически в растворах
зависит от концентрации муравьиной кислоты.
1 моль/л HCOOH до Np(III). Напротив, моноядер-
КОНФЛИКТ ИНТЕРЕСОВ
ные аква- или акваформиатокомплексы Np(IV)
в растворах, содержащих HClO4 и 0.9 моль/л
Авторы заявляют об отсутствии конфликта
HCOOH, под действием УФ излучения частич-
интересов.
но восстанавливаются до Np(III). В 99.7%-ной и
СПИСОК ЛИТЕРАТУРЫ
10 моль/л HCOOH Np(IV) находится частично в
виде моноядерных акваформиатокомплексов, и
1. Юсов А.Б., Шилов В.П. // Изв. АН. Сер. хим. 2000.
фотохимическое восстановление до Np(III) проис-
№ 12. С. 1957.
ходит без добавки HClO4. Ионы Np(III) при хра-
2. Kessinger G.F., Kyser E.A., Almond P.M. Literature
нении раствора в спектрофотометрической кювете
Review: Reduction of Np(V) to Np(IV)—Alternatives
полностью окисляются до Np(IV).
to Ferrous Sulfamate. SRNL-STI-2009-00610. P. 4.
Полимерные и моноядерные комплексы непту-
3. Шилов В.П. Юсов А.Б. // Радиохимия. 2001. Т. 43,
ния(IV) имеют в УФ области коффициенты пога-
№ 4. С. 326.
шения, значительно превышающие аналогичные
4. Шилов В.П., Федосеев А.М. // Радиохимия. 2015.
величины для Np(V) и HCOOH. Поэтому в раство-
Т. 57, № 3. C 218.
рах происходит фотоактивация ионов Np(IV). По-
5. Шилов В.П., Федосеев А.М. // Радиохимия. 2015.
следующий процесс
Т. 57, № 4. C 348.
2Np(IV) + HCOOH → 2Np(III) + CO2 + 2H+
(8)
6. Hagan P.G., Cleveland J.M. // J. Inorg. Nucl. Chem.
имеет важное значение в механизме фотолиза рас-
1966. Vol. 28, N 12. P. 2905.
творов Np(IV) и Np(V). Возникающие в реакции
7. Ананьев А.В., Шилов В.П. // Радиохимия. 2001.
(8) ионы Np(III) восстанавливают Np(V) до Np(IV),
Т. 43, № 1. С. 41.
Np(III) + Np(V) → 2Np(IV),
(9)
8. Гоголев А.В., Шилов В.П., Пикаев А.К. // ХВЭ. 1996.
т.е. процесс фотохимического восстановления
Т. 30, № 5. С. 388.
Np(V) в муравьиной кислоте является фотокатали-
9. Takao K., Takao Sh., Scheinost A.C., Bernhard G.,
тическим.
Hennig Ch. // Inorg. Chem. 2012. Vol. 51, N 3. P. 1336.
РАДИОХИМИЯ том 62 № 4 2020