РАДИОХИМИЯ, 2020, том 62, № 5, с. 425-429
УДК 621.039.73
ИСПОЛЬЗОВАНИЕ НИТРАТА КАРБАМИДА
В ГИДРОМЕТАЛЛУРГИИ УРАНА
© 2020 г. Ю. В. Островскийa,b,*, Г. М. Заборцевa, Д. Ю. Островскийa
a НПЦ «ЭЙДОС», 630075, Новосибирск, ул. Богдана Хмельницкого, 2
b Новосибирский государственный технический университет, 630073, Новосибирск, пр. Карла Маркса, 20
*e-mail: ostrovsky@sibmail.com
Получена 18.02.2020, после доработки 03.06.2020, принята к публикации 04.06.2020
Исследовано влияние добавки нитрата карбамида в экстракционном аффинаже урана на емкость экстра-
гента (23%-ный ТБФ в органическом разбавителе), полноту реэкстракции урана из насыщенного экстра-
гента, а также остаточную концентрацию урана в азотнокислом рафинате. В экспериментах использовали
нитратно-карбамидный и азотнокислый растворы, содержащие нитрат уранила [UO2(NO3)2], получен-
ный при растворении закиси-окиси урана (U3O8). Реэкстракцию урана проводили подкисленной водой
при рН 3. Установлено, что емкость экстрагента по урану для нитратно-карбамидного и азотнокислого
растворов сопоставима, что позволяет использовать нитрат карбамида в качестве высаливателя уранил-
нитрата. Остаточная концентрация урана в рафинате после карбамидной денитрации не превышает 13.6-
14.1 мг/л. Раствор аммонийнокарбонатных солей также обеспечивает полноту твердофазной реэкс-
тракции урана из экстрагента, насыщенного в нитратно-карбамидном растворе. Накопление нитрата
карбамида в технологическом цикле отсутствует при кислотности исходного раствора 0.4-0.6 моль/л.
Рассчитана температура устойчивости исследуемой системы. Предложен процесс гидролиза нитрата
карбамида до нитрата аммония при повышенном давлении. Полученный раствор после коррекции
кислотности может быть использован в качестве десорбирующего реагента в процессе сорбционного
аффинажа урана технологии подземного выщелачивания урана.
Ключевые слова: аффинаж урана, карбамидная денитрация рафинатов, нитрат карбамида, экстракция
урана, гидролиз нитрата карбамида, нитрат аммония, подземное выщелачивание урана
DOI: 10.31857/S0033831120050093
ВВЕДЕНИЕ
ной азотной кислоты, находящейся в рафинате,
что может быть осуществлено методом карбамид-
Одной из важных экологических задач на пред-
ной денитрации [1-5]. При добавке карбамида в
приятиях фабрикации ядерного топлива, исполь-
азотнокислый рафинат образуется малораствори-
зующих в своем технологическом цикле АДУ-про-
мый моносольват карбамида с азотной кислотой
цесс (аммоний диуранат), является денитрация
(нитрата карбамида) по реакции:
рафинатов азотнокислого аффинажа урана.
(1)
Содержание азотной кислоты в экстракцион-
ных рафинатах может достигать 4 моль/л, поэто-
Нитрат карбамида представляет собой кристал-
му перед сбросом стоков в хвостохранилище из-
лическое соединение (комплекс включения или
быточную кислотность рафинатов нейтрализуют
аддукт) [6], поэтому он практически не загрязня-
щелочным агентом, как правило, гидроксидом
ется примесями, содержащимися в рафинате [3], и
кальция. Однако этот прием не приводит к сни-
легко отделяется от водной фазы.
жению поступления в хвостохранилище жидких
радиоактивных отходов нитрат-ионов, которые ак-
Поскольку другие методы денитрации азотно-
тивно способствуют миграции тяжелых и радиоак-
кислых растворов отличаются высокой энерго-
тивных металлов в прилегающем почвенном слое.
емкостью
[7,
8], низкой производительностью
Для того чтобы снизить поступление нитрат-
процесса [9] или образованием трудноутилизируе-
ионов, необходимо снизить концентрацию свобод-
мых полупродуктов [10], технология карбамидной
425
426
ОСТРОВСКИЙ и др.
Таблица 1. Состав исходных урансодержащих раство-
Таблица 2. Условия экстракции урана из нитрат-
ров
но-карбамидного и азотнокислого растворов
Растворы,
Параметр
Значение
г/л
Экстрагент
23%-ный ТБФ в
органическом
разбавителе
Вещество
Соотношение фаз на
О : В = 1 : 1
экстракции
Время контакта фаз на
5 мин
экстракции
UO2(NO3)2 (по U)
70.0
70.0
Число ступеней экстракции
4 ступени
HNO3
30.0
30.0
Температура экстракции
20°С
CO(NH2)2·HNO3
75.0
-
Частота вращения мешалки
1000 мин-1
денитрации рафинатов азотнокислого аффинажа
урана определяли фотоколориметрическим мето-
урана представляет определенный практический
дом по стандартным методикам с иcпользованием
интерес. При карбамидной денитрации экстрак-
Арсеназо III. Концентрацию уранилнитрата рас-
ционных рафинатов происходит образование и
считывали по содержанию урана(VI). Содержание
накопление осадка нитрата карбамида, количество
нитрата карбамида рассчитывали по общему азоту.
которого зависит от исходной кислотности рафи-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
натов. Нитрат мочевины можно использовать в
процессах растворения урановых концентратов
В экспериментах использовали экстрагент
(U3O8) в качестве высаливателя в экстракционном
(23% ТБФ в органическом разбавителе), нитрат
аффинаже урана [11, 12] или для синтеза нитрата
карбамида [CO(NH2)2·HNO3] получали по мето-
аммония, используемого при десорбции урана из
дике, изложенной в работе [3], при этом исполь-
смол при подземной добыче урана [13].
зовали карбамид и азотную кислоту марки ХЧ.
Концентрацию урана определяли фотокалориме-
В данной статье авторы публикуют результаты
трическим методом по стандартным методикам с
исследований по использованию нитрата карбами-
иcпользованием реагента Арсеназо III. Концен-
да в данных процессах.
трацию уранилнитрата рассчитывали по содер-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
жанию урана(VI). Содержание нитрата карбамида
рассчитывали по общему азоту.
В качестве экстрагента использовали 23%-ный
ТБФ в органическом разбавителе. Нитрат карбами-
Использование нитрата карбамида в аффи-
да [CO(NH2)2·HNO3] получали по методике, изло-
наже урана. При использовании нитрата карба-
женной в работе [3], при этом использовали карба-
мида в экстракционном аффинаже урана важно
мид и азотную кислоту марки х.ч. Концентрацию
знать влияние карбамида на изменение емкости
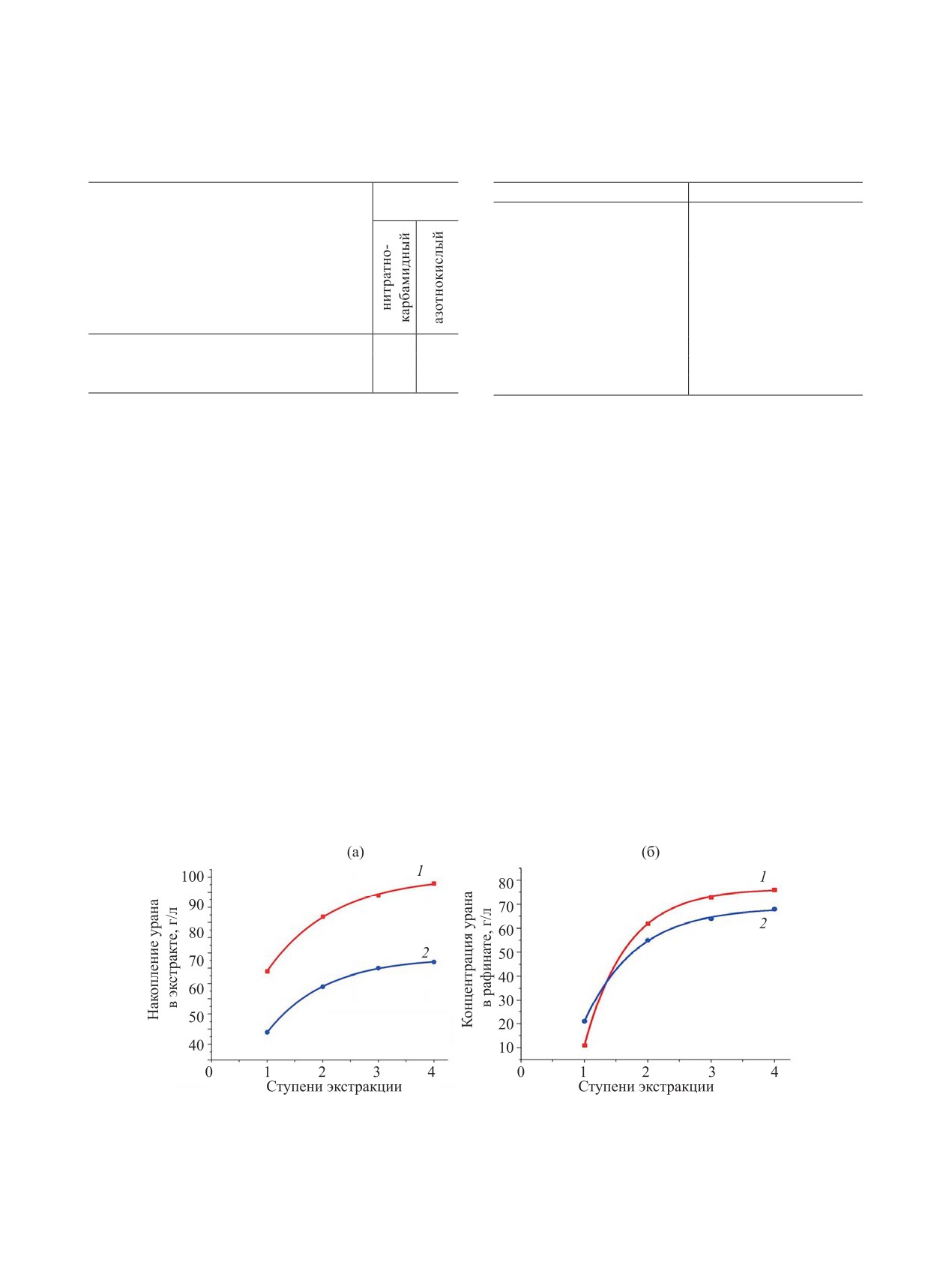
Рис. 1. Экстракция урана из (1) нитратно-карбамидного и (2) азотнокислого растворов. а - накопление урана в экстракте,
б - остаточная концентрация урана в рафинате.
РАДИОХИМИЯ том 62 № 5 2020
ИСПОЛЬЗОВАНИЕ НИТР
АТА КАРБАМИДА
427
Таблица 3. Параметры экстракционной обработки ни-
Таблица 4. Условия твердофазной реэкстракции урана
тратно-карбамидного и азотнокислого урансодержа-
Параметр
Значение
щих растворов
Экстрагент
23%-ный ТБФ в органическом
Номер
Время
разбавителе
Раствор
ступени
расслаивания
Реэкстрагент
Раствор 17.5 мас% аммоний-
экстракции
фаз, с
нокарбонатных солей + 5 мас%
Нитратно-карбамидный
1
124
NH4OH
2
120
Соотношение фаз
О : В = 1 : 1
3
120
на реэкстракции
4
60
Время контакта фаз
30 мин
Азотнокислый
1
184
при реэкстракции
2
180
Число ступеней
2 ступени
3
150
реэкстракции
4
175
Температура
20°С
реэкстракции
экстрагента по урану, полноту реэкстракции урана
Частота вращения
1000 мин-1
из насыщенного экстрагента при использовании
мешалки
карбамида, а также на остаточную концентрацию
[14]. Условия экспериментов по реэкстракции ура-
урана в рафинате.
на представлены в табл. 4.
Влияние карбамида на емкость экстраген-
При твердофазной реэкстракции урана из на-
та по урану. В экспериментах по экстракции экс-
сыщенного экстракта на первой ступени извле-
трагент приводили в контакт последовательно с
несколькими порциями свежего нитратно-карба-
кается не менее 95.5% урана, а на второй ступе-
мидного
[система UO2(NO3)2-CO(NH2)2·HNO3-
ни - до 4.5% урана. Эти результаты позволяют
HNO3] или азотнокислого [система UO2(NO3)2-
утверждать, что присутствие нитрата карбамида в
HNO3-H2O] растворов, содержащих UO2(NO3)2,
исходном растворе не препятствует количествен-
полученный при растворении закиси-окиси урана
ному извлечению урана из экстракта.
(U3O8). Составы исходных растворов представле-
Остаточная концентрация урана в рафи-
ны в табл. 1.
нате при использовании нитрата карбамида.
Условия экспериментов по экстракции урана из
Для установления влияния карбамида на оста-
нитратно-карбамидного и азотнокислого раство-
точную концентрацию урана в рафинате были
ров представлены в табл. 2.
проведены эксперименты по экстракции урана
из нитратно-карбамидного
[система UO2(NO3)2-
Параметры экстракционной обработки раство-
CO(NH2)2·HNO3-H2O] и азотнокислого [система
ров представлены в табл. 3, а результаты экспери-
UO2(NO3)2-HNO3-H2O] растворов, содержащих
ментов - на рис 1. Из данных табл. 3 следует, что по
70 г/л урана в виде нитрата уранила, полученного
мере насыщения экстрагента ураном в нитратно-
при растворении закиси-окиси урана (U3O8).
карбамидом растворе расслаивание фаз ускоряет-
ся до 60 с.
В ходе экспериментов использовали один и тот
При экстракции урана из нитратно-карбамид-
же раствор, который приводили в контакт с пор-
ного раствора емкость экстрагента по урану дости-
цией свежего экстрагента, содержащего 27.7 г/л
гает 98.0 г/л, а из азотнокислого раствора - 72 г/л,
HNO3. Составы исходных водных растворов пред-
что объясняется большей кислотностью исходного
ставлены в табл. 1, а условия экспериментов - в
нитратно-карбамидного раствора.
табл. 2.
Полнота реэкстракции урана. Насыще-
В результате 4 ступеней экстракции остаточная
ние экстрагента по урану [система UO2(NO3)2-
концентрация рафинатов по урану снижается со-
CO(NH2)2·HNO3-H2O] приводили в соответствие
ответственно до 13.6 и 14.1 мг/л.
с условиями, указанными в табл. 2. Состав исход-
При охлаждении рафината, полученного после
ных растворов представлен в табл. 1
4-й ступени экстракции из нитратно-карбамид-
Твердофазную реэкстракцию урана проводили
ного раствора, до 0°С, выпадает плотный осадок
в 2 ступени с использованием на каждой ступени
нитрата карбамида (25-30% от объема раствора),
свежего раствора аммонийнокарбонатных солей
который можно утилизировать или повторно ис-
РАДИОХИМИЯ том 62 № 5 2020
428
ОСТРОВСКИЙ и др.
Таблица 5. Составы экстракционных рафинатов
Таблица 6. Показатели карбамидной денитрации рафи-
натов
Рафинат
Рафинат
Вещество
Размерность
№ 1
№ 2
Рафинат
Рафинат
Характеристика
HNO3
моль/л
2.0
2.0
№ 1
№ 2
Степень извлечения HNO3 в
70
80
Al3+
г/л
-
25-35
виде CO(NH2)2·HNO3, %
F-
г/л
-
25-40
Остаточное содержание
0.6
0.4
Uобщ
мг/л
50
50
HNO3, моль/л
пользовать в процессах экстракционного аффина-
растворения урановых концентратов и коррекции
жа урана или растворения урановых концентратов.
кислотности исходного раствора перед экстраги-
Граница температурной устойчивости системы
рованием урана трибутилфосфатом в органиче-
для данного рафината, рассчитанная по методике,
ском разбавителе.
представленной в работе [15], составляет 3.8°С.
Использование продукта гидролиза нитрата
Анализ накопления нитрата карбамида при
карбамида в технологии подземного выщелачи-
экстракционном аффинаже урана. Схема экс-
вания урана. При кислотности исходного раство-
тракционного аффинажа урана с использованием
ра более 2.0 моль/л накопление нитрата карбамида
нитрата карбамида предусматривает растворение
неизбежно, что создаст определенные сложности с
урановых концентратов в азотной кислоте, под-
его хранением и дальнейшим использованием. Ра-
кисление полученного раствора нитратом карба-
дикальным решением этой проблемы может быть
мида, экстракцию урана, а затем карбамидную де-
его поставка в твердом виде на площадки подзем-
нитрацию рафината с получением осадка нитрата
ного выщелачивания урана с последующим гидро-
карбамида и его возврата в голову технологическо-
лизом нитрата карбамида до нитрата аммония при
го процесса [12]. Оптимальными для проведения
атмосферном или повышенном давлении [16].
предложенного процесса являются условия, когда
Нитрат карбамида гидролизуется в нитрат ам-
весь нитрат карбамида, образующийся в процессе
мония по реакции
карбамидной денитрации экстракционных рафи-
(2)
натов, возвращается в технологический цикл.
Оценку накопления избытка нитрата карбамида
Термодинамические расчеты, подтверждающие
при экстракционном аффинаже урана проводили
возможность и эффективность проведения реак-
в условиях, когда растворение урановых концен-
ции (2) при повышенной температуре и давлении,
тратов происходит при избытке азотной кислоты в
представлены авторами в работе [16]. Поскольку
интервале 0.0-2.0 моль/л, а доводка концентрация
бикарбонат аммония термически неустойчив и
азотной кислоты в рафинате до 2.0 моль/л обеспе-
при небольшом нагревании распадается на амми-
чивается добавкой нитрата карбамида.
ак, воду и углекислый газ, то для связывания выде-
ляющегося аммиака в раствор добавляют азотную
Составы использованных экстракционных ра-
кислоту:
финатов (№ 1 и № 2) приведены в табл. 5. Высокое
содержание алюминия и фтора в составе рафината
(3)
№ 2 обусловлено проведением АДУ-процесса.
Полученный раствор нитрата аммония после
Степени извлечения азотной кислоты в виде
коррекции рН можно использовать в качестве десор-
CO(NH2)2·HNO3 и остаточное содержание HNO3
бирующего реагента для процесса сорбционного
при карбамидной денитрации рафинатов пред-
аффинажа урана на предприятиях подземного вы-
ставлены в табл. 6.
щелачивания урана [13], например, АО «ДАЛУР»
(Курганская обл.) [17]. В этом случае уранодо-
Установлено, что при кислотности исходного
бывающим предприятиям можно отказаться от
раствора, образующегося при растворении ура-
закупки значительной части дорогостоящего то-
новых концентратов, 0.4-0.6 моль/л, доведении
варного нитрата аммония при сохранении каче-
его по кислотности до 2.0 моль/л и последую-
ства получаемой закиси-окиси урана. Процесс ги-
щей денитрации рафинатов карбамидом накопле-
дролиза нитрата карбамида может быть наиболее
ние нитрата карбамида в технологическом цикле
эффективно реализован при повышенном давлении.
практически отсутствует. В этих условиях весь
образующийся нитрат карбамида может быть ис-
В ходе экспериментальных работ использовали
пользован как донор азотной кислоты в процессах
растворы, составы которых представлены в табл. 7.
РАДИОХИМИЯ том 62 № 5 2020
ИСПОЛЬЗОВАНИЕ НИТР
АТА КАРБАМИДА
429
Таблица 7. Состав используемых растворов (г/л)
СПИСОК ЛИТЕРАТУРЫ
Вещество
Раствор № 1
Раствор № 2
1. Молодкин А.К., Эллерт Г.В., Иванова О.М., Скотни-
CO(NH2)2·HNO3
200
200
кова Г.А. // ЖНХ. 1967. Т. 12, № 4. С. 947.
HNO3
–
100
2. Narayanan Kutty T.R., Vasudeva Murthy A.R. // Indian
J. Chem. 1973. Vol. 11, N 3. P. 253.
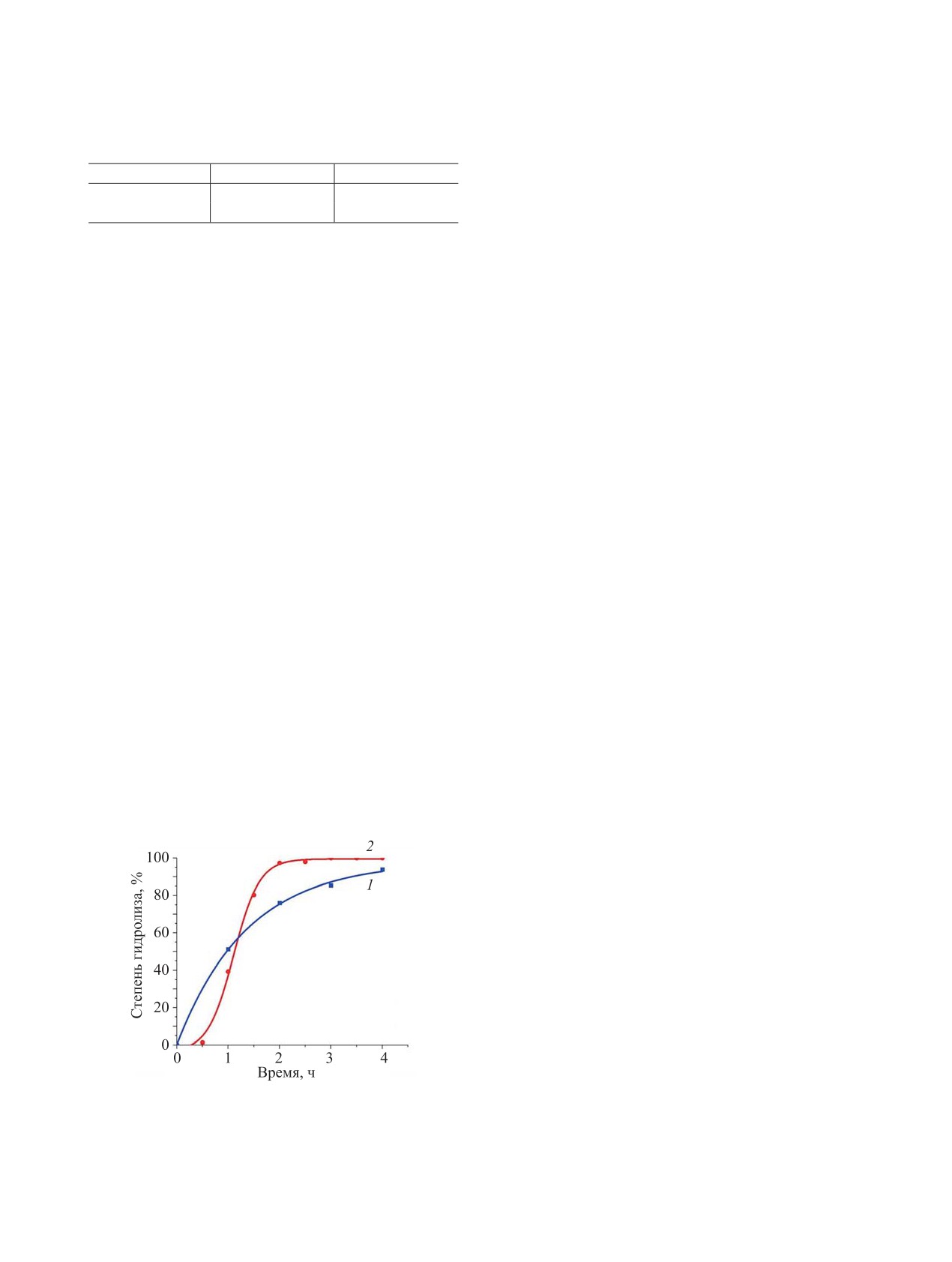
Процесс гидролиза нитрата карбамида при по-
3. Островский Ю.В., Заборцев Г.М., Шпак А.А., Якоб-
вышенной давлении проводили в течение 4 ч в
чук С.П., Александров А.Б., Хлытин А.Л., Гусев А.А. //
лабораторном автоклаве объемом 70 мл (матери-
Радиохимия. 2004. Т. 46, № 3. С. 232.
ал - сталь 12Х18Н10Т) при температуре 150°С. В
4. Островский Ю.В., Заборцев Г.М. // Вестник
процессе гидролиза давление в автоклаве возрас-
УГТУ-УПИ. Радиохимия. Тр. II Уральской конф.
тало до 20-25 атм. Результаты исследования пред-
Екатеринбург, 2004. С. 134.
ставлены на рис. 2.
5. Островский Ю.В., Заборцев Г.М., Шпак А.А., Алек-
Как видно из данных рис. 2, процесс автоклав-
сандров А.Б., Сайфутдинов С.Ю., Дробяз А.И., Хлы-
ного гидролиза протекает количественно, а добав-
тин А.И. Патент RU 2253161. Опубл. 27.05.2005. //
ка азотной кислоты с целью увеличения выхода
Б.И. 2005. № 15.
нитрата аммония до теоретического ускоряет про-
6. Нурахметов Н.Н. // Итоги науки и техники. Сер.:
цесс в 2 раза.
Физ. химия. 1989. № 4. С. 64.
7. Жильбер Ш., Антуан Ф., Сильви Д. Патент RU
ВЫВОДЫ
2179761. Опубл. 20.02.2002 // Б.И. 2002. № 5.
Использование нитрата карбамида в качестве
8. Квэкенбуш А.Б. Патент RU 2061671. Опубл.
донора азотной кислоты не ухудшает показателей
10.06.1996 // Б.И. 1996. № 16.
экстракционного аффинажа урана по сравнению с
9. Васильев Ю.Б., Эвентов В.Л., Громыко В.А., Гада-
традиционной схемой, однако экологические ха-
дымов В.Б. // Итоги науки и техники. Сер.: Электро-
рактеристики предлагаемой схемы значительно
химия. 1990. Т. 31. С. 55.
лучше. Образующийся в процессе денитрации экс-
10. Химическая энциклопедия: в 5 Т. Т. 3: Меди сульфи-
тракционных рафинатов нитрат карбамида может
ды-Полимерные красители / Под ред. Кнунянц И.Л.,
быть возвращен в голову технологического цикла
Зефиров Н.С., Кулов Н.Н., Золотов Ю.А., Каба-
или выведен из него и гидролизован в автоклаве
нов В.А., Калечиц И.В., Колотыркин Я.М., Коп-
до нитрата аммония, используемого в процессах
тюг В.А., Кутепов А.М., Малюсов В.А., Нефе-
сорбционного аффинажа урана.
дов О.М., Тальрозе В.Л., Спирин А.С., Степанов Н.Ф.,
Шолле В.Д., Ягодин Г.А. М.: Сов. энциклопедия,
КОНФЛИКТ ИНТЕРЕСОВ
1992. С. 639.
Авторы заявляют об отсутствии конфликта
11. Островский Ю.В., Заборцев Г.М., Александров А.Б.,
интересов.
Дробяз А.И., Сайфутдинов С.Ю., Хлытин А.Л.
Патент RU 2295168. Опубл. 10.03.2007 // Б.И. 2007.
№ 7.
12. Островский Ю.В., Заборцев Г.М., Чапаев И.Г., Алек-
сандров А.Б., Сайфутдинов С.Ю., Хлытин А.Л. //
Радиохимия. 2009. Т. 51, № 1. С. 30.
13. Емельянов В.С., Евстюхин А.И. Металлургия ядер-
ного горючего. М.: Атомиздат, 1968. 2-е изд. С. 207.
14. Шевченко В.Б., Судариков Б.Н. Технология урана.
М.: Гос. изд-во литературы в области атомной науки
и техники, 1961. С. 234.
15. Голощапов Р.Г., Дедов Н.В., Дорда Ф.Л., Скотно-
ва В.Н. //Тез. докл. Второй Рос. конф. по радиохи-
мии. Димитровград: НИИАР, 1997. С. 214.
16. Островский Ю.В., Заборцев Г.М., Жерин И.И.,
Островский Д.Ю., Егоров Н.Б. // Альтернативная
энергетика и экология. 2017. № 13-15 (225-227).
C. 101.
Рис. 2. Зависимость степени гидролиза нитрата кар-
бамида от времени при T = 150°С: (1) раствор № 1,
17. Санников В.Н., Луценко Н.И. // Горный журн. 2017.
(2) раствор № 2.
№ 8. С. 23.
РАДИОХИМИЯ том 62 № 5 2020