РАДИОХИМИЯ, 2021, том 63, № 3, с. 250-258
УДК 621.039.3
ИССЛЕДОВАНИЕ ВЗАИМОДЕЙСТВИЯ
СОЛЕЙ РАДИЯ С КОНСТРУКЦИОННЫМИ
МАТЕРИАЛАМИ
© 2021 г. П. С. Буткалюк, И. Л. Буткалюк*, С. В. Томилин,
А. С. Куприянов, Р. Г. Абдуллов, А. А. Колобова, К. В. Ротманов
Научно-исследовательский институт атомных реакторов,
433510, Димитровград Ульяновской обл., Западное шоссе, д. 9
*e-mail: butkaluk-il@yandex.ru
Получена 27.12.2019, после доработки 27.12.2019, принята к публикации 12.02.2020
Исследовано взаимодействие Ra(NO3)2 и RaCO3 с металлическими Fe, Ni, Cr, Ti. Экспериментальные
образцы изготавливали путем нанесения водно-спиртовых суспензий солей радия на подложки из соот-
ветствующих металлов с последующим упариванием и прокаливанием в течение 7-14 ч при темпера-
туре 800°С. Согласно результатам рентгенофазового анализа, при совместном прокаливании Ra(NO3)2
и RaCO3 с металлическими Fe, Ni, Cr, Ti происходит образование смешанных оксидов состава RaMOx,
где M = Fe, Cr, Ti, Ni.
Ключевые слова: радий, реакторное получение изотопов, смешанные оксиды.
DOI: 10.31857/S0033831121030072
ВВЕДЕНИЕ
логичной BaCrO4, а также факт образования фазы,
аналогичной фазе BaPtO2.38, при прокаливании
RaСO3/PbCO3 в платиновом тигле [2]. Между тем,
В настоящее время в НИИАР ведется разработка
эксперименты по прокаливанию Ra(NO3)2 с нержа-
технологии получения медицинских альфа-излуча-
веющей сталью не позволили однозначно опреде-
телей путем облучения 226Ra в исследовательском
лить фазовый состав полученной смеси [3].
реакторе СМ [1]. Для облучения радия использу-
Исходя из этих данных, можно предположить,
ют смесь метаплюмбата радия (RaPbO3 со структу-
что соли радия при высокой температуре взаимо-
рой кубического перовскита [2]) с оксидом свинца
PbO, упакованную в оболочку из нержавеющей
действуют с отдельными компонентами нержаве-
ющей стали с образованием смешанных оксидов.
стали. После растворения облученного материала
Целью работы был поиск новых соединений радия,
в HCOOH отмечается присутствие в растворе вы-
относящихся к классу смешанных оксидов, которые
соких концентраций солей железа, никеля и хрома,
в том числе изотопов 60Co, 59Fe и 51Cr, которые за-
могут образовываться на поверхности компактных
образцов переходных металлов Fe, Ni, Ti, Cr (как ос-
трудняют выделение и очистку полезных продуктов
новных компонентов нержавеющей стали).
активации радия. Было выдвинуто предположение,
что возможной причиной этого является взаимодей-
ствие солей радия с компонентами нержавеющей
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
стали с образованием соединений общей формулой
RaxMyOz, которые затем растворяются в муравьи-
Материалы и методы. В данной работе исполь-
ной кислоте. Ранее нами был установлен факт взаи-
зовали азотную кислоту квалификации ос.ч., ни-
модействия смеси RaСO3/PbCO3 с материалом тигля
трат бария и карбонат аммония х.ч., квалификация
из нержавеющей стали с образованием фазы, ана-
остальных реактивов была не ниже ч.д.а.
250
ИССЛЕДОВАНИЕ ВЗАИМОДЕЙСТВИЯ СОЛЕЙ Р
АДИЯ
251
Взвешивание аликвот и навесок проводили при
нержавеющей стали с последующим упариванием
помощи аналитических весов Ohaus PA64C, по-
и прокалкой на электроплитке с открытой спиралью
грешность взвешивания составляла ± 0.2 мг.
для отгонки 222Rn. Перед измерением альфа-спек-
тра подготовленный образец выдерживали в тече-
Подложки для прокаливания солей бария и радия
ние 1.5 ч, что необходимо для снижения активно-
изготавливали из стали Ст3 (Fe ≥ 97, C 0.14-0.22,
сти короткоживущих дочерних продуктов распада
Si 0.15-0.3, Mn 0.4-0.65%), металлического нике-
ля НП3 (Ni > 99.3, Fe ≤ 0.15, Si ≤ 0.15, Mg ≤ 0.1,
222Rn. Для градуировки спектрометров использова-
ли образцовые спектрометрические альфа-источни-
Mn ≤ 0.2, Cu ≤ 0.15, S ≤ 0.015, C ≤ 0.15%), металли-
ки (ОСАИ).
ческого титана ВТ1-0 (Ti ≥ 98.61, Fe ≤ 0.18, C ≤ 0.07,
Si ≤ 0.1, N ≤ 0.4, O ≤ 0.12, H ≤ 0.01%). Они представ-
Содержание нерадиоактивных примесей в пре-
ляли собой диски диаметром от 9 мм с зеркально
паратах 226Ra(NO3)2 определяли методом атом-
отполированной поверхностью.
но-эмиссионного анализа с использованием уста-
новки, представляющей собой искровой источник
Подложку из металлического хрома получали
возбуждения спектров ИВС-28, смонтированный
электролитическим осаждением хрома из раствора,
внутри радиационно-защитного бокса, и спектро-
полученного растворением 7.5 г CrO3 в 30 мл 2.5 г/л
граф ИСП-1, соединенный с этим источником при
H2SO4, на металлическую медную пластину толщи-
помощи оптического выхода.
ной 2 мм из электротехнической меди (Cu ≥ 99.93,
Bi ≤ 0.002, Se ≤ 0.002, Te ≤ 0.002, Sb ≤ 0.0004,
Рентгенограммы образцов снимали на дифрак-
Fe ≤ 0.001, S ≤ 0.0015, Ag ≤ 0.0025, O ≤ 0.04%). На-
тометре ДРОН-7-Mythen (медное излучение с Ni-
несение осуществляли в течение 30 ч до толщины
фильтром, алмазный стандарт) и интерпретировали
слоя хрома в 1.5 мм.
с использованием базы дифракционных данных
PDF-2 и комплекса программ PDWin.
Измерение pH растворов проводили при помо-
щи рН-метра HANNA-HI 2210 со стеклянными
Исследование взаимодействия солей бария
электродами Hi 1131B (Hanna Instruments). Кали-
с конструкционными материалами. Предва-
бровку рН-метра осуществляли при помощи стан-
рительные эксперименты проводили с использо-
дартных буферных растворов c pH 9.18, 6.86 и 4.01
ванием бария в качестве имитатора радия. Изна-
(ООО «Химтитры»).
чальная методика эксперимента предполагала на-
несение солей радия и бария в виде растворимых
Содержание бария в растворе определяли c ис-
солей и медленного упаривания. В случае карбо-
пользованием радиоактивного изотопа 131Ва (про-
натов это должны были быть растворы гидрокси-
изводства НИИАР) c известной удельной актив-
дов соответствующих элементов, которые должны
ностью. Объемную активность 131Ва определяли
были бы на воздухе превратиться в карбонаты:
методом гамма-спектрометрического анализа при
M(OH)2 + CO2 = MCO3 + H2O.
помощи полупроводникового гамма-спектрометра
с коаксиальным Ge-Li детектором типа ДГДК-В150
Первые же эксперименты показали непригод-
(энергетическое разрешение
3.0 кэВ по линии
ность данного подхода к решению поставленной
1.3 МэВ). Для градуировки спектрометра исполь-
задачи. Вследствие краевых эффектов испарение
зовали образцовые радиоактивные растворы. Рас-
капель на подложках с высокой теплопроводностью
шифровку гамма-спектров проводили в полуавто-
происходит с краев более интенсивно [4]. Следстви-
матическом режиме при помощи стандартного про-
ем этого является образование областей с локаль-
граммного обеспечения фирмы «ГринСтар».
ным пресыщением и образование там зародышей,
Содержание 226Ra определяли с помощью альфа-
рост которых приводит к крайне неравномерному
спектрометра на основе кремниевых PIPS-
распределению солей в образующемся пятне. На
детекторов ПДПА-1К (ОАО «ИФТП», Дубна, Рос-
рис. 1, а показан результат испарения капли, содер-
сия) и амплитудного анализатора импульсов АЦП-
жащей 4 мг бария в виде нитрата в 200 мкл воды,
8К-И2. Образцы (источники) для измерения актив-
на металлической подложке диаметром 16 мм. Как
ности альфа-излучения 226Ra готовили нанесением
видно из рисунка, соли бария образуют кольцо
10-25 мкл анализируемого раствора на подложку из
на краях подложки, при этом в центре кристаллы
РАДИОХИМИЯ том 63 № 3 2021
252
БУТКАЛЮК и др.
раствора нитрата радия (~10 мг) в 7 моль/л HNO3
(а)
(б)
добавляли (в качестве носителя) 500 мг Pb(NO3)2,
затем добавляли 50 мл 15.6 моль/л HNO3. Получен-
ный раствор упаривали до объема 75 мл, охлаждали
в течение 4 ч. Затем добавляли 25 мл 15.6 моль/л
HNO3. Операции упаривания, охлаждения и добав-
ления кислоты повторяли еще 4 раза. Полученный
осадок, содержащий нитраты радия и свинца, отде-
ляли от раствора декантацией и промывали тремя
порциями 15.6 моль/л HNO3. Полученный осадок
Рис. 1. Нанесение Ba(NO3)2 на металлические подлож-
ки: (а) из водного раствора, (б) из суспензии в 80%-ном
Ra(NO3)2/Pb(NO3)2 растворяли в 50 мл бидистил-
этаноле.
лированной воды и проводили осаждение хлорида
свинца добавлением 5 мл 10 моль/л HCl. Маточный
практически отсутствуют. Такое неравномерное
раствор декантировали, упаривали досуха.
распределение нежелательно для проведения рент-
Второй этап включал хроматографическую
геновской дифрактометрии образцов, поэтому были
очистку радия от свинца и щелочноземельных эле-
проведены работы по выяснению условий создания
ментов на двух колонках с катионообменной смо-
равномерного слоя солей на подложке. Наилучшие
лой BioRad AG 50×8. Соли радия растворили в
результаты были получены при осаждении нитрата
40 мл ацетатно-аммиачного буферного раствора с
бария из водно-спиртового раствора, промывке по-
концентрацией 1 моль/л и рН 4.5 и концентрацией
лученных кристаллов 95%-ным этанолом и нанесе-
ЭДТА 0.025 моль/л. Для контроля очистки радия
нии спиртовой суспензии на подложку (рис. 1, б).
к препарату перед подачей на колонку добавляли
BaCO3 получали смешиванием 1 мл раствора ни-
раствор, содержащий 131Ba(NO3)2 с ~4 × 106 Бк. Че-
трата бария с концентрацией 3.8 мг Ba/мл и 3 мл
рез хроматографическую колонку объемом 2 см3
раствора (NH4)2CO3 с концентрацией 4 моль/л. Вы-
с сорбентом BioRad AG 50 × 8 пропускали 40 мл
павший осадок промывали тремя порциями биди-
полученного раствора. Далее колонку промывали
стиллированной воды объемом по 3 мл каждая и на-
40 мл ацетатно-аммиачного буферного раствора с
носили на подложку из 200 мкл водной суспензии.
концентрацией 1 моль/л и рН 4.5 и концентрацией
Ba(NO3)2 получали добавлением к 0.5 мл раство-
ЭДТА 0.02 моль/л. Барий и радий элюировали аце-
татно-аммиачным буферным раствором с рН 8.0 и
ра нитрата бария с концентрацией 3.8 мг/мл 2 мл
концентрацией ЭДТА 0.01 моль/л. Элюент соби-
95%-ного этанола. Жидкость над осадком декан-
рали фракциями. Контрольное элюирование ра-
тировали, и на подложку наносили получившуюся
дия проводили раствором ЭДТА с концентрацией
суспензию осадка нитрата бария.
0.02 моль/л и рН 9.5. Затем фракции, содержащие
Полученные образцы высушивали на воздухе и
226Ra и не содержащие 131Ва объединяли, подкис-
прокаливали в шахтной печи в следующем режиме:
ляли 1 моль/л ацетатно-аммиачным буферным рас-
150°C - 1 ч, 400°С - 1 ч, 800°С - 7-12 ч.
твором с рН 4.5 из расчета 4 мл буферного раствора
Очистка радия. Для экспериментов с радием
на каждые 10 мл раствора 226Ra. Пропускали по-
использовали аликвоты от фракций 226Ra, выде-
лученный раствор через хроматографическую ко-
ленных ранее из облученных радиевых мишеней
лонку объемом 2 см3 с сорбентом BioRad AG 50×8.
[1]. Изначально образцы радия были загрязнены
Промывали колонку 30 мл ацетатно-аммиачного
примесями Ba, Ca, Na, Si, Cr, Ni, Fe и содержали
буферного раствора с концентрацией 1 моль/л и
макроколичества нитрата свинца. Было проведено
рН 4.5 и концентрацией ЭДТА 0.02 моль/л. Затем
три эксперимента с использованием 226Ra, при этом
промывали 10 мл ацетатно-аммиачного буферного
очистку проводили во всех случаях по одной схеме.
раствора с концентрацией 1 моль/л и рН 4.5, 10 мл
Очистку проводили в несколько этапов. На первом
бидистиллированной воды, 80 мл 0.5 моль/л HNO3.
этапе проводили совместное осаждение нитрата ра-
Радий элюировали 40 мл 8 моль/л HNO3. Полу-
дия с нитратом свинца из 15.6 моль/л HNO3 по мето-
ченный раствор упаривали досуха и растворяли в
дике, аналогичной описанной в работе [5]. K 50 мл
0.01 моль/л HNO3.
РАДИОХИМИЯ том 63 № 3 2021
ИССЛЕДОВАНИЕ ВЗАИМОДЕЙСТВИЯ СОЛЕЙ Р
АДИЯ
253
Таблица 1. Исследование взаимодействия BaCO3, Ba(NO3)2 с металлическими Fe, Ni, Cr, Ti
Наносимая
Материал
Фазовый состав
соль
подложки
Ba(NO3)2
Железо
Набор слабых рефлексов орторомбической фазы BaFe2O4. Имеется набор сильных
рефлексов, часть которых близка к моноклинной фазе Ba2Fe2O5
BaCO3
Железо
BaCO3 орторомбический, Fe2O3 гексагональный; следовые количества гексагональных
фаз BaFe2O4 и BaFeO3-x
Ba(NO3)2
Никель
Ni кубический, NiO кубический; часть слабых рефлексов орторомбической и
гексагональной модификаций BaCO3
BaСO3
Никель
BaCO3 орторомбический, Ni кубический, NiO кубический
Ba(NO3)2
Хром
BaCrO4 орторомбический; возможно, присутствуют BaCr2O4, BaCO3 орторомбический
(следы), Вa3CuO4 ромбоэдрический
BaСO3
Хром
BaCO3 орторомбический, ВaCrO4 орторомбический; возможно, присутствует BaCr2O4
Ba(NO3)2
Титан
TiO2 тетрагональный, BaTiO3 тетрагональный либо орторомбический, BaCO3
орторомбический в следовых количествах
BaСO3
Титан
TiO2 тетрагональный, BaTiO3 тетрагональный, BaCO3 орторомбический
Исследование взаимодействия солей радия с
риевые образцы анализировали методом рентгенов-
конструкционными материалами. Ra(NO3)2 на
ской дифрактометрии с использованием дифракто-
подложки наносили из водно-спиртовой суспен-
метра ДРОН-7. Результаты представлены в табл. 1.
зии Ra(NO3)2, которую получали добавлением 1 мл
Из полученных данных видно, что при прокали-
95%-ного этанола к 200 мкл раствора Ra(NO3)2
вании солей бария со сталью Ст3 помимо рефлек-
(~2 мг 226Ra) с последующим высушиванием на воз-
сов, характерных для стали Ст3 и оксидов железа,
духе и прокаливанием в шахтной печи при темпера-
на дифрактограммах наблюдаются рефлексы сме-
туре 800°С в течение 7-14 ч.
шанных оксидов, содержащих барий: BaFeO3 и
RaCO3 получали добавлением к 200 мкл раство-
BaFe2O4. Дополнительно для образца, полученно-
ра Ra(NO3)2, содержащего ~2 мг 226Ra, 1 мл раство-
го нанесением Ba(NO3)2 из спиртовой суспензии,
ра 4 моль/л (NH4)2CO3 с последующей промывкой
имеется набор сильных рефлексов, часть которых
осадка тремя порциями 95%-ного этанола по 1 мл.
близка рефлексам моноклинной фазы Ba2Fe2O5.
Затем полученную спиртовую суспензию RaCO3
Прокаливание как нитрата, так и карбоната бария
наносили на металлические подложки с последу-
с металлическими хромом и титаном приводит к
ющим высушиванием и прокаливанием осадка в
образованию хромата BaCrO4 и титаната бария Ba-
шахтной печи при температуре 800°С в течение
TiO3 соответственно. В то же время реакция с ме-
7-14 ч.
таллическими никелем в данных условиях не про-
текает, и барий присутствует только в форме карбо-
Все операции проводили в радиационно-
ната BaCO3.
защитном печаточном боксе, препараты перед
снятием дифрактограммы покрывали двумя слоями
Очистка радия. Эксперименты с радием прово-
цапон-лака для предотвращения распыления.
дили в разное время, было получено и охарактери-
зовано три порции очищенного радия, характери-
стики которых, согласно результатам атомно-эмис-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
сионного анализа, представлены в табл. 2.
Исследование взаимодействия бария с кон-
Общее содержание металлических примесей в
струкционными материалами. Полученные ба- образцах радия не превышало 5.7, 0.8 и 2.25% от
РАДИОХИМИЯ том 63 № 3 2021
254
БУТКАЛЮК и др.
Таблица 2. Характеристики препаратов очищенного
При прокаливании солей радия на подложках
226Ra(NO3)2
из металлического никеля присутствует группа
рефлексов, по положению близких к таковым для
Номер препарата
Компонент
BaNiO3; их можно интерпретировать как RaNiO3.
1
2
3
Так же были обнаружены отдельные рефлексы,
Масса, мг
226Ra
8.2
14.45
12.43
относящиеся к фазе, аналогичной BaO2 (вероятно
Масса примесей, мкг
RaO2), которая может играть роль промежуточно-
го соединения в механизме окисления поверхно-
Ba
52
5.5
12
Ca
148
44
260
сти металлов. Увеличение устойчивости пероксида
Cr
<4
<5.5
<4
при переходе от бария к радию является возможной
Fe
28
<16.5
8
причиной более высокой химической активности
Ni
<4
<5.5
<4
солей радия в реакциях с металлическим никелем.
Pb
20
<16.5
<12
Анализ дифракционных картин обоих образцов
Pt
5.6
<16.5
<4
радия с хромом позволил установить, что они оди-
Si
200
-
-
наковы в отношении присутствия основной фазы,
которую, очевидно, можно трактовать как фазу
радия с хромом. Дополнительные, не основные
массы радия для первого, второго и третьего образ-
фазы - это хром и его оксиды. В базе дифракцион-
цов радия соответственно, при этом примесь бария
ных данных PDF-2 имеется один набор с данными
как ближайшего аналога радия составила 0.6, 0.04 и
для RaCrO4 (№ 00-027-0488); тем не менее, при
0.1% соответственно.
близком наборе линий экспериментальные данные
Первая порция была использована для экспери-
и данные для RaCrO4 заметно различались по угло-
мента по прокаливанию Ra(NO3)2 с железом, вто-
вому положению рефлексов. Заметно лучшее со-
рая - для прокаливания RaCO3 с железом и RaCO3 и
впадение полученных данных было с орторомбиче-
Ra(NO3)2 с никелем, третья - для исследования вза-
ской фазой BaCrO4 (№ 00-015-0376). По угловому
имодействия RaCO3 и Ra(NO3)2 с хромом и титаном.
положению полученные рефлексы занимали проме-
Результаты рентгенофазового анализа радиевых
жуточное положение между литературными данны-
образцов представлены в табл. 3 и на рис. 2-8.
ми для RaCrO4 и BaCrO4. После отделения рефлек-
Таблица 3. Исследование взаимодействия RaCO3, Ra(NO3)2 с металлическими Fe, Ni, Cr, Ti
Наносимая
Материал подложки
Фазовый состав
соль 226Ra
Ra(NO3)2
Металлическое железо
Fe2O3 гематит; набор рефлексов, которые можно отнести к фазам-аналогам
BaFeO3-x (тетрагональная и гексагональная)
RaCO3
Металлическое железо
Fe2O3 тригональный, Fe кубический, RaCO3; фаза-аналог кубического
BaFeO3-x
Ra(NO3)2
Металлический никель
Ni кубический, NiO кубический; фаза-аналог BaO2 тетрагональная;
фаза-аналог BaNiOx орторомбическая
RaCO3
Металлический никель
Фаза-аналог BaCO3 орторомбическая; Ni кубический, NiO кубический;
фаза-аналог BaNiOx орторомбическая
Ra(NO3)2
Металлический хром
RaCrO4 орторомбический; возможно присутствие Cr2O3; Cr кубический
RaСO3
Металлический хром
RaCrO4; возможно присутствие Cr2O3
Ra(NO3)2
Металлический титан
Фаза, близкая к кубическому BaTiO3; возможно присутствие Ra(NO3)2
кубического, а также оксидов титана
RaСO3
Металлический титан
TiO2 тетрагональный, RaCO3 орторомбический; неизвестная фаза состава
ABO3, близкая по параметрам к CeAlO3
РАДИОХИМИЯ том 63 № 3 2021
ИССЛЕДОВАНИЕ ВЗАИМОДЕЙСТВИЯ СОЛЕЙ Р
АДИЯ
255
Fe2O2
BaFeO3 - тетрагон
RaCO3
BaFeO3-х
1200
Fൾ
O3
углерод
BaFeO3 - гексагон
1200
2
Fe
неизв.фаза
(Fe,C)
1000
Fe2C
800
800
600
400
400
200
0
20
30
40
50
60
70
80
20
30
40
50
60
70
80
2θ, град
2θ, град
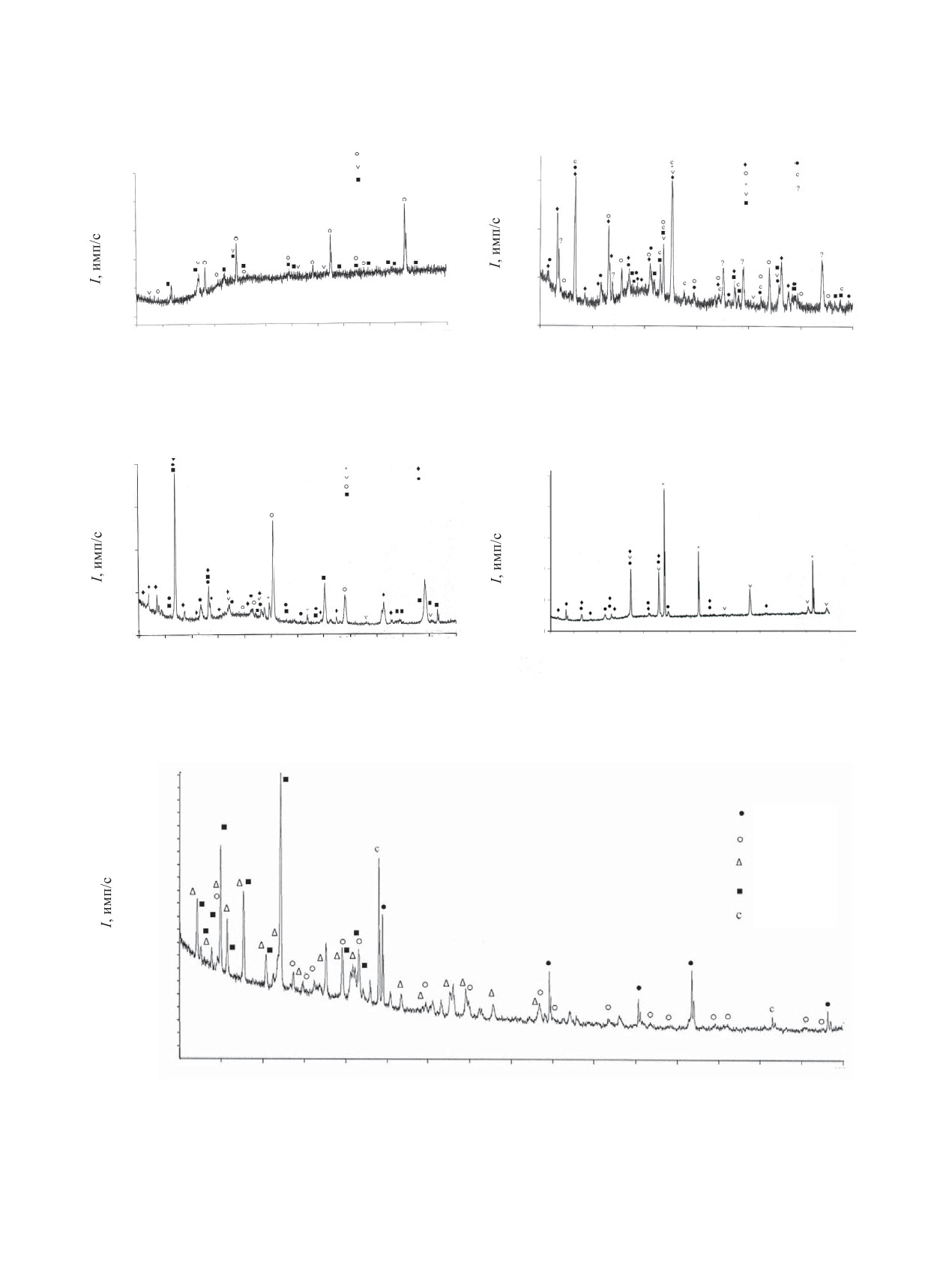
Рис.2. Дифрактограмма препарата, полученного про-
Рис. 3. Дифрактограмма препарата, полученного про-
каливанием Ra(NO3)2 на подложке из металлического
каливанием RaCO3 на подложке из металлического
железа.
железа.
1600
Ni
RaCo3
NiO
BaNiOx
5000
°
Ni
Ni (thin fiems)
˅ NiO
BaO
2
♦ RaCo3
1200
4000
● BaNiOx
3000
800
2000
400
1000
0
0
20
30
40
50
60
70
80
20
30
40
50
60
70
80
2θ, град
2θ, град
Рис. 4. Дифрактограмма препарата, полученного про-
Рис. 5. Дифрактограмма препарата, полученного про-
каливанием Ra(NO3)2 на подложке из металлического
каливанием RaCO3 на подложке из металлического
никеля.
никеля.
9900
Cr
8100
Cr2O3
RaCrO4
6300
BaCrO4
алмаз
4500
2700
900
30
40
50
60
70
80
90
100
2θ, град
Рис. 6. Дифрактограмма препарата, полученного прокаливанием Ra(NO3)2 на подложке из металлического хрома.
РАДИОХИМИЯ том 63 № 3 2021
256
БУТКАЛЮК и др.
15000
13000
▲ RaTiO3
● Ti4O7
11000
♦ Ra(NO3)2
9000
7000
5000
3000
1000
10
30
40
50
60
70
80
90
2θ, град
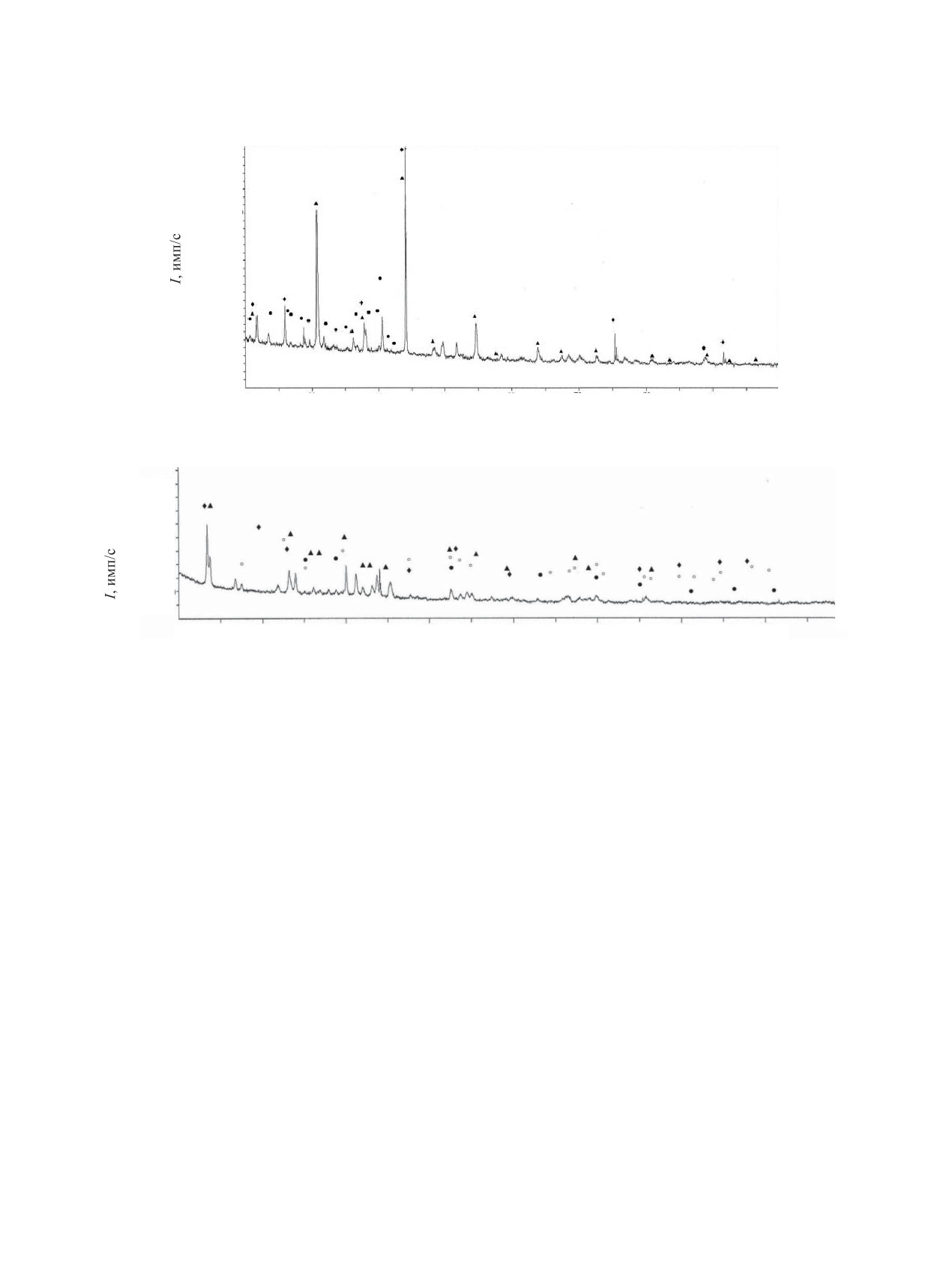
Рис. 7. Дифрактограмма препарата, полученного прокаливанием Ra(NO3)2 на подложке из металлического титана.
▲ RaCO3
10000
♦ CeAlO3
8000
° TiO2
● TiO1.76
6000
4000
2000
10
30
40
50
60
70
80
90
2θ, град
Рис. 8. Дифрактограмма препарата, полученного прокаливанием RaСO3 на подложке из металлического титана.
сов металлического Сr и его оксидов был выделен
рост для RaCrO4 (00-027-0488), по данным PDF-2,
оставшийся набор рефлексов, предположительно
составляет 24.6 Å3, что выглядит несколько завы-
основной фазы. Рефлексы были идентифицирова-
шенным. Завышенные значения параметров кри-
ны по аналогии с литературными данными BaCrO4,
сталлической решетки в данном случае могли быть
и методом наименьших квадратов были уточнены
следствием экспериментальных погрешностей при
параметры кристаллической решетки в орторомби-
рентгенографировании фотометодом в камере диа-
ческой сингонии, пространственная группа Pnma
метром 57.3 мм.
(табл. 4 и 5). Совпадение экспериментальных и
На рентгенограмме, полученной при прокалива-
вычисленных межплоскостных расстояний вполне
нии нитрата радия на титановой подложке, выделя-
удовлетворительное.
ется набор из 14 отражений, хорошо совпадающих с
Структура орторомбического BaCrO4 относит-
набором для кубической фазы, близкой к составу Ra-
ся к структурному типу орторомбического BaSO4
TiO3, с параметром кубической решетки а = 8.236 ±
(минерал барит), где Ba имеет координационное
0.002 Å и пространственной группой F3m3m.
число 12. Исходя из ионных радиусов Ba2+ и Ra2+,
равных соответственно 1.61 и 1.70 Å, и числа фор-
ЗАКЛЮЧЕНИЕ
мульных единиц в ячейке, можно ориентировочно
оценить прирост объема элементарной ячейки при
Установлено, что соли радия при температуре
переходе от бариевого к радиевому соединению.
800°С на воздухе реагируют с отдельными компо-
Вычисленный прирост составляет 12.5 Å3. Экс-
нентами нержавеющей стали с образованием сме-
периментальный прирост для полученной нами
шанных оксидов состава RaCrO4, RaFeO3-x, RaTiO3
фазы составляет 15.7 Å3. В то же время этот при-
и RaNiOx. Таким образом, образование данных сое-
РАДИОХИМИЯ том 63 № 3 2021
ИССЛЕДОВАНИЕ ВЗАИМОДЕЙСТВИЯ СОЛЕЙ Р
АДИЯ
257
Таблица 4. Расчет межплоскостных расстояний и индицирование рефлексов фазы RaCrO4.
Номер линии
Интенсивность, %
2θэксп, град
dэксп, Å
dрасч, Å
hkl
1
25
22.03
4.021
4.026
111
2
6
22.47
3.942
3.933
201
3
9
23.78
3.729
3.728
002
4
56
24.87
3.569
3.565
210
5
26
25.66
3.461
3.459
102
6
42
27.62
3.220
3.216
211
7
14
30.31
2.940
2.940
112
8
4
31.11
2.867
2.852
301
9
100
32.04
2.786
2.793
020
10
4
34.71
2.578
2.577
212
11
22
37.53
2.390
2.400
103
12
24
39.49
2.276
2.278
221
13
10
40.51
2.222
2.235
022
14
13
40.79
2.207
2.205
113
15
12
41.08
2.193
2.190
203
16
4
42.02
2.145
2.139
410
17
8
45.31
1.997
1.996
321
18
8
46.72
1.940
1.936
303
19
3
49.29
1.845
1.855
412
20
5
49.78
1.828
1.829
313
21
6
51.51
1.770
1.773
131
22
12
52.58
1.737
1.737
114
23
15
52.94
1.726
1.733
421
24
13
54.47
1.681
1.694
403
25
5
56.09
1.637
1.640
132
26
5
56.39
1.629
1.621
413
27
6
57.77
1.593
1.591
323
28
2
60.48
1.528
1.529
124
29
3
62.14
1.491
1.490
033
30
3
63.13
1.470
1.470
224
31
4
64.01
1.452
1.452
404
32
3
66.21
1.409
1.405
414
33
6
67.02
1.394
1.392
040
34
4
67.85
1.379
1.376
215
35
2
69.35
1.353
1.352
432
36
3
71.69
1.314
1.314
504
37
3
75.80
1.253
1.253
433
38
5
81.38
1.181
1.181
441
РАДИОХИМИЯ том 63 № 3 2021
258
БУТКАЛЮК и др.
Таблица 5. Параметры кристаллической решетки изоструктурных фаз BaCrO4 и RaCrO4
Соединение
Номер набора PDF-2
a, Å
b, Å
c, Å
V, Å3
BaCrO4
00-015-0376
9.105
5.541
7.343
370.5
00-035-0642
9.112
5.541
7.343
370.8
RaCrO4
00-027-0488
9.300
5.620
7.560
395.1
RaCrO4,
9.260 ± 0.001
5.5870 ± 0.0003
7.4644 ± 0.0007
386.2
экспериментальные
данные
динений возможно также при реакции солей радия
СПИСОК ЛИТЕРАТУРЫ
с оболочками мишеней, выполненными из нержа-
веющей стали. Этот факт хорошо согласуются с
1.
Kuznetsov R.A., Butkalyuk P.S., Tarasov V.A.,
ранее полученными данными о высокой скорости
Baranov A.Yu., Butkalyuk I.L. // Radiochemistry. 2012.
Vol. 54, N 4. P. 383-387.
выщелачивания компонентов из стальных оболо-
2.
Butkalyuk P.S., Butkalyuk I.L., Kuznetsov R.A.,
чек облученных радиевых мишеней. Появление в
Tomilin S.V. // Radiochemistry. 2013. Vol. 55, N 1.
облученном радии значимых количеств продуктов
P. 41-45.
его взаимодействия с материалом оболочки необхо-
3.
Буткалюк И.Л., Буткалюк П.С., Томилин С.В. //
димо учитывать при разработке технологии перера-
Изв. Самарск. науч. центра РАН. 2013. Т. 15, № 4-5.
ботки облученных радиевых мишеней.
C. 1053-1057.
4.
Бараш Л.Ю. Испарение и динамика лежащей на под-
ложке капли: Дис. … к.ф.-м.н. М.: Ин-т теор. физики
КОНФЛИКТ ИНТЕРЕСОВ
им. Л.Д. Ландау, 2009. 74 с.
5.
Кузнецов Р.А., Тарасов В.А., Романов Е.Г. и др. //
Авторы заявляют об отсутствии конфликта
Изв. Самарск. науч. центра РАН. 2014. Т. 16, № 6.
интересов.
С. 136-141.
РАДИОХИМИЯ том 63 № 3 2021