РАДИОХИМИЯ, 2021, том 63, № 3, с. 281-295
УДК 546.831.4
ПОЛУЧЕНИЕ РАСТВОРОВ 89Zr ДЛЯ СИНТЕЗА
РАДИОФАРМПРЕПАРАТОВ
© 2021 г. В. Б. Бубенщиковa,*, А. А. Ларенковa,б, Г. Е. Кодинаa
a Федеральный медицинский биофизический центр им. А. И. Бурназяна ФМБА России,
123182, Москва, Живописная ул., д.46;
б Московский государственный университет им. М. В. Ломоносова, 119991,Москва, Ленинские горы, д. 1
*e-mail: bubenschikov2011@yandex.ru
Получена 20.02.2020, после доработки 16.04.2020, принята к публикации 23.04.2020
Цирконий-89 является перспективным радионуклидом для применения в ядерной медицине и имеет
оптимальные ядерно-физические характеристики для исследования процессов, характеризующихся
медленной кинетикой. Возрастающая популярность таргетной визуализации привела к сопутствующему
развитию радиофармацевтической химии 89Zr. В настоящее время проведен огромный объем научных
работ по всем направлениям: начиная от получения 89Zr на ускорителях до клинических исследований
целого ряда радиофармпрепаратов. В обзоре содержится описание и сравнение различных методов
получения, выделения и очистки 89Zr, обсуждаются наиболее распространенные химические формы,
используемые при синтезе комплексов.
Ключевые слова: цирконий-89, получение, выделение, очистка, хлорид, оксалат, цитрат, радиофарма-
цевтические препараты, позитронно-эмиссионная томография.
DOI: 10.31857/S0033831121030114
ВВЕДЕНИЕ
ния биомолекулы, наиболее подходящими радиону-
клидами для исследования биологических процес-
сов с медленной кинетикой методом ПЭТ являются
Разработка новых радиофармацевтических ле-
124I (Т1/2 = 4.17 сут), 64Cu(Т1/2 = 12.7 ч), 86Y(Т1/2 = 14.7 ч),
карственных препаратов (РФЛП или упрощенно
89Zr (Т1/2 = 78.42 ч) [1, 2].
РФП) для позитронно-эмиссионной томографии
(ПЭТ) в аспекте персонализированной медицины
В последнее время особый интерес представля-
характеризуется невероятным прогрессом в течение
ет радионуклид 89Zr, поскольку он обладает рядом
последних двух десятилетий [1-3]. Большое внима-
преимуществ по сравнению с другими радионукли-
ние сосредоточенно на разработке и внедрении в
дами для ПЭТ с близкими периодами полураспада.
клиническую практику визуализирующих агентов
89Zr может быть легко получен на низкоэнергетиче-
на основе моноклональных антител (mAb), глав-
ских циклотронах, при этом не требуется изотопное
ным образом для диагностики и мониторинга те-
обогащение мишени, поскольку исходным матери-
рапии онкологических заболеваний. Моноклональ-
алом является моноизотопный природный иттрий.
ные антитела имеют относительно медленную фар-
89Zr имеет более подходящий период полураспада,
макокинетику, в результате чего оптимальное био-
чем 64Cu и 86Y; он также более безопасен в обра-
распределение соответствующих РФП достигается
щении и более стабилен in vivo, чем 124I, который,
в течение нескольких часов или суток. Поскольку
помимо высокой энергии испускаемых позитро-
одним из фундаментальных принципов разработки
нов (табл. 1), имеет γ-линию с энергией, близкой
РФП является соответствие периода полураспада
к 511 кэВ (602.7 кэВ, Gγ = 62.9%), что ухудшает
радионуклида эффективному периоду полувыведе-
качество получаемых изображений [2, 3]. Еще од-
281
282
БУБЕНЩИКОВ и др.
Таблица 1. Некоторые радионуклиды, применяемые в клинической практике ПЭТ
Eβ+, МэВ
Выход позитронов,
Потери пространственного
Радионуклид
Т1/2
Ссылка
(макс.)
%
разрешения, мм
11С
20.36 мин
0.960
99.7
0.92
[6, 7]
13N
9.96 мин
1.198
99.8
1.49
[6, 7]
15O
2.04 мин
1.735
99.8
2.48
[6, 7]
18F
110 мин
0.633
96.8
0.54
[6, 7]
44Sc
3.97 ч
1.474
94.3
2.3
[8, 7]
64Cu
12.7 ч
0.653
17.5
0.7
[4, 7]
68Ga
67.8 мин
1.899
87.7
2.83
[6, 7]
82Rb
1.26 мин
3.381
81.8
6.14
[6, 7]
86Y
14.7 ч
3.14
31.9
1.8
[9, 10]
89Zr
78.4 ч
0.902
22.8
1.3
[4, 7]
124I
4.176 сут
2.14
22.7
2.3
[9, 11]
ним преимуществом 89Zr является тот факт, что 89Zr
обзорах, посвященных радиофармацевтической
имеет одну из самых низких максимальных энергий
химии 89Zr [40-45], в них практически не затра-
испускаемых позитронов (после 18F, 64Cu и 11С), что
гивается вопрос получения исходных растворов
позволяет получать ПЭТ-изображения с высоким
циркония-89. Настоящий обзор посвящен методам
разрешением (табл. 1) [3-5].
получения, выделения и очистки циркония-89, ко-
В настоящее время ряд РФП на основе 89Zr уже
торый должен быть получен в фармацевтически
применяется в клинических исследованиях имму-
приемлемой для изготовления РФП форме раствора
ноПЭТ: для визуализации применяют монокло-
с высокой химической, радионуклидной и радиохи-
нальные антитела, меченные 89Zr, после чего про-
мической чистотой.
водят «холодную» терапию. Первое клиническое
Ядерно-физические характеристики изото-
исследование с препаратом 89Zr было посвящено
пов циркония. На сегодняшний день известно 39
визуализации CD44v6-позитивных опухолей го-
изотопов Zr, пять из которых содержатся в природ-
ловы и шеи химерным антителом 89Zr-cmAb U36
ной смеси (90Zr, 91Zr, 92Zr, 94Zr и 96Zr), 96Zr слабо
[12, 13]. Позже был проведен ряд исследований с
радиоактивен (Т1/2 = 2.35×1019 лет) [46]. Наиболее
использованием различных 89Zr-mAb для диагно-
изученные радиоактивные изотопы циркония
-
стики колоректального рака [14], рака предста-
93Zr (Т1/2
= 64 сут) и
тельной железы [15, 16], глиомы [17], карцином
97Zr (Т1/2 = 16.7 ч) - являются продуктами деле-
поджелудочной железы и яичников [18]. Была по-
ния
235U. Радиоактивные изотопы 86Zr (Т1/2 =
казана возможность визуализации HER2-положи-
17 ч, Gγ = 100%, Eγ = 241 кэВ), 88Zr (Т1/2 = 85 сут,
тельного метастатического рака молочной желе-
Gγ = 100%, Eγ = 390 кэВ) и 89Zr могут быть по-
зы 89Zr-трастузумабом [19-21], CD20-позитивной
лучены на циклотроне с использованием различ-
В-клеточной лимфомы 89Zr-ритуксимабом [22] и
ных ядерных реакций [47, 48]. 89Zr (Т1/2 = 78.42 ч)
89Zr-ибритумомабом [23], рака молочной желе-
распадается путем электронного захвата (77.2%)
зы [24], рака легких [25], карциномы почек [26] и
и испускания позитронов (22.8%, Еβ+ = 902 кэВ)
нейроэндокринных опухолей [27] 89Zr-бевацизу-
в метастабильный 89mY (T1/2 = 15.84 c), который
мабом. Кроме того, опубликованы результаты не-
распадается в стабильный 89Y (ИП, Еγ = 909 кэВ,
скольких перспективных доклинических исследо-
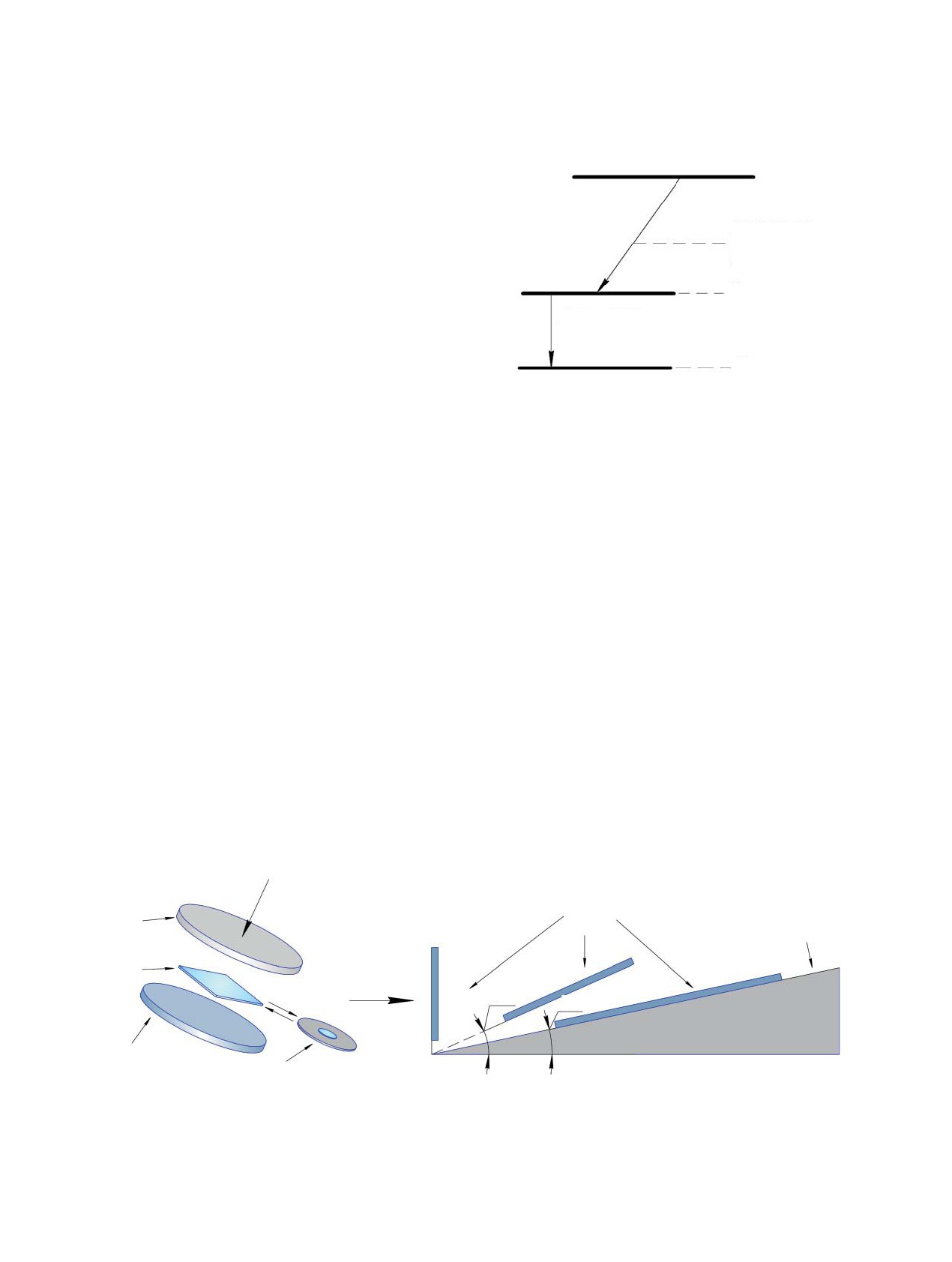
Gγ = 99.0%) (рис. 1) [7]. Дополнительно для 89Zr
ваний, связанных с применением фрагментов анти-
необходимо отметить наличие γ-линии высокой
тел [28-31], пептидов [32], меченых клеток [33-35]
энергии (909 кэВ, Gγ = 99%), которая, согласно
и наночастиц [36-39].
проведенным исследованиям, вносит значитель-
Несмотря на значительный прогресс в синтезе
ный вклад в поглощенную дозу при введении РФП
89Zr-РФП, что отражено в нескольких подробных
89Zr-mAb (0.4-0.7 мЗв/МБк [13, 23, 49], для иссле-
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
283
дования вводится примерно 37 МБк РФП [17, 20,
89Zr (T1/2 = 78.42 ч)
21, 24-26]).
Методы получения 89Zr. На данный момент
существует несколько способов получения 89Zr: об-
ЕЭ 77.2%
лучение 89Y протонами 89Y(p,n)89Zr или дейтрона-
β+ 22.8%
ми 89Y(d,2n)89Zr; облучение природного стронция
(смесь изотопов 84Sr, 86Sr, 87Sr, 88Sr) альфа-частица-
89Y (T1/2 = 15.84 c)
ми natSr(α,xn)89Zr [48]; облучение изотопно-обога-
ИП-100%
щенных мишеней 91Zr(p,pxn)89Zr [30], 90Zr(n,2n)89Zr
[50, 51]. Несмотря на многообразие представленных
908.97 кэВ
методов, наиболее практичной ядерной реакцией
89Y (стаб.)
для получения 89Zr является реакция 89Y(p,n)89Zr
[52-61], реализовать которую можно в том числе
Рис. 1. Схема распада 89Zr.
и на низкоэнергетических медицинских циклотро-
нах. Для получения 89Zr разработаны различные ва-
рианты мишеней, наиболее распространенными из
50 мкА, в результате чего выход 89Zr увеличился бо-
которых являются иттриевая фольга, прессованные
лее чем в три раза и составил 48 ± 4 МБк/(мкA·ч).
гранулы и напылённый иттрий.
Линк и соавт. [62] проводили облучение иттриевой
Иттриевая фольга (рис. 2, а). Данный метод явля-
фольги протонами (11 МэВ, 25-41 мкA) под разны-
ется наиболее популярным и простым с точки зре-
ми углами (12°, 24°, 90°) на низкоэнергетическом
ния подготовки мишени к облучению. Иттриевую
циклотроне (Siemens Eclipse Cyclotron) (рис 2, б).
фольгу закрепляют на медной или алюминиевой
Расположение мишени под углом 12° приводит к
подложке [54, 56, 58, 60, 62-67]. Полученную ми-
увеличению площади облучения и эффективно-
шень облучают протонами с энергией 12-14 МэВ в
го теплообмена, что позволяет увеличить выход
течение 1-2 ч. Интенсивность пучка, как правило,
89Zr до 23 ± 10 МБк/(мкA·ч) по сравнению с 20.5 ±
не превышает 20 мкА, поскольку использование бо-
1.1 МБк/(мкA·ч) при 90°.
лее высоких токов может привести к деформации
Гранулы иттрия. В ряде публикаций авто-
и разрушению мишени. Для повышения устойчи-
ры изготавливали прессованные иттриевые гра-
вости мишени к протонному облучению Эллисон
нулы диаметром ~10 мм из порошкообразного Y
и соавт. [68] предложили использовать точечную
и Y2O3. Звейт и соавт. [69], Кандил и соавт. [70]
сварку иттриевой фольги с танталовой подлож-
покрывали полученные прессованные гранулы
кой. Данное решение позволило увеличить ток до
алюминиевой фольгой, после чего полученные
(а)
(б)
1
6
2
7
1
24°
12°
5
4
Рис. 2. (а) Kонструкция мишени; (б) схема размещения мишени. 1 - ионный пучок, 2 - алюминиевый деградер, 3 - иттри-
евая фольга или 4 - монета с иттриевым напылением, 5 - медная подложка, 6 - мишень, 7 - корпус мишенного устройства.
РАДИОХИМИЯ том 63 № 3 2021
284
БУБЕНЩИКОВ и др.
Таблица 2. Ядерные реакции, которые могут происходить при наработке циркония-89
Радионуклид
Реакция получения
Т1/2
Eγ (Gγ)а [7]
89Zr
89Y(p,n)89Zr
78.4 ч
511 (45.6%)
909 (99.0%)
88Zr
89Y(p,2n)88Zr
83.4 сут
392.9
(97.3%)
88Y
89Y(p,pn)88Y
106 сут
898 (93.7%)
89Y(p,d)88Y
1836 (99.3%)
88Zr → 88Y
65Zn
65Cu(p,n)65Zn
244 сут
511 (2.8%)
1115.5
(50.2%)
63Zn
63Cu(p,n)63Zn
38.3 мин
511 (185.6%)
669.9
(8.19%)
962.0
(6.5%)
56Coб
56Fe(p,n)56Co
77.3 сут
511 (39.2%)
771.3
(15.4%)
846.7
(99.9%)
1037.8
(14.0%)
1238.3
(66.4%)
2598.4
(16.9%)
48V
48Ti(p,n)48V
16 сут
511 (100.6%)
944.1
(7.7%)
983.5
(99.8%)
1312.1
(97.5%)
2240.4
(2.4%)
a Указаны γ-линии с Gγ > 1%; б Gγ > 10%.
мишени облучали дейтронами [16 МэВ, 3-5 мкА,
слой иттрия толщиной ~25 мкм [55, 57, 59, 72]. По-
τ = 12-20 мин, выход 67 МБк/(мкA·ч)] и протонами
лученная мишень обеспечивает более эффективное
[12 МэВ, 2 мкА, τ = 3-5 ч, выход 28 МБк/(мкA·ч)]
теплорассеяние, что позволяет повысить ток до
соответственно. Необходимо отметить, что изго-
40 мкА [57]. Данный способ является самым эко-
товленная таким образом мишень из Y2O3 обладает
номичным, поскольку для изготовления мишени
низкой теплоотдачей, вследствие чего облучение
требуется меньше иттрия, что также уменьшает
проводится с низкой интенсивностью [70]. Ал-
количество потенциальных примесей в конечном
нахви и соавт. [71] проводили протонное облуче-
растворе. Кроме того, использование иттриевого
ние иттриевых фольг (11.3-13.3 МэВ, 10-40 мкА,
напыления позволяет ускорить процедуру выделе-
τ = 3-5 ч, выход 24-54 МБк/(мкA·ч)) и прессован-
ния 89Zr, а также получать продукт с более высокой
ных иттриевых гранул [11-15 МэВ, 10-42 мкА,
объемной активностью [57]. Необходимо отметить,
τ = 1.5-5 ч, выход 20-50 МБк/(мкA·ч)]. Авторы
что в результате облучения помимо 89Zr могут обра-
отмечают, что прессованные иттриевые гранулы,
зоваться радионуклидные примеси (табл. 2).
как и иттриевая фольга, позволяют получать 89Zr
Незначительные количества 65Zn и 63Zn могут
с высокой эффективной молярной активностью
образоваться в результате реакций 65Cu(p,n)65Zn и
(162 ± 30 и 379 ± 23 ГБк/мкмоль для иттриевых
63Cu(p,n)63Zn при использовании медной подложки
гранул и иттриевой фольги соответственно). Кро-
во время облучения. В энергетическом диапазоне
ме того, изготовление гранул является коммерчески
10-15 МэВ реакция 65Cu(p,n)65Zn имеет высокое
более выгодным, однако требует наличия специаль-
сечение захвата, близкое к 1 барн [73]. Образо-
ного пресс-устройства.
вание изотопов 56Co и 48V возможно по реакциям
Напыленный иттрий. Для изготовления мише-
56Fe(p,n)56Co и 48Ti(p,n)48V из металлических при-
ни на медную или ниобиевую подложку напыляют
месей, находящихся в составе иттриевой мишени
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
285
Рис. 4. Зависимость сечения захвата от энергии дейтро-
Рис. 3. Зависимость сечения захвата от энергии протонов
нов (построено авторами по данным работы [82]).
(построено авторами по данным работы [74]).
[72]. При облучении также образуется 89mZr (Т1/2 =
акции 89Y(d,2n)89Zr составляет 7-16 МэВ, при этом
4.2 мин), который не является радионуклидной
выход 89Zr достигает 67 МБк/(мкA·ч) [59, 69].
примесью, поскольку в течение часа полностью
Состояние циркония в водных растворах.
распадается в 89Zr. Основными радионуклидными
Цирконий имеет сложную химию в водных рас-
примесями являются 88Zr и 88Y, образование кото-
творах, связанную с многообразием образующихся
рых происходит в результате побочных ядерных ре-
форм и их составом. Цирконий может существовать
акций 89Y(p,2n)88Zr, 89Y(p,pn)88Y и 89Y(p,d)88Y. Од-
в нескольких степенях окисления: Zr(II), Zr(III),
нако данные реакции имеют относительно высокий
однако наиболее устойчивой является Zr(IV). Эф-
энергетический порог - 13.07, 11.60 и 9.35 МэВ для
фективный ионный радиус катиона Zr4+ составляет
89Y(p,2n)88Zr, 89Y(p,pn)88Zr и 89Y(p,d)88Y соответ-
0.84 Å, и в отличие от Ga(III), Y(III) и Cu(II) Zr(IV)
ственно [74] (рис. 3).
предпочтительно образует комплексы с координа-
В настоящее время реакция 89Y(p,n)89Zr доско-
ционным числом 8 [84].
нально изучена различными группами исследовате-
В водных растворах Zr(IV) имеет высокую
лей
[52, 64, 70, 75-79]. Энергетический диапазон
склонность к гидролизу и существует в виде мно-
9-14 МэВ является оптимальным для получения
жественных моно- и полиядерных соединений с
89Zr. Облучение проводится в течение 2-3 ч, при
окси- и гидрокси-мостиками в растворах с низ-
этом образуется менее 0.2% примесного 88Zr [10].
ким значением pH. В области микроконцентраций
Для уменьшения количества радионуклидых при-
(10-9-10-11 M 95Zr) при концентрации [H+] < 2 М
месей при энергии пучка более 14 МэВ целесоо-
наблюдается значительный гидролиз, который про-
бразно применение алюминиевых или ниобиевых
текает поэтапно с образованием гидроксокатионов
деградеров [58, 66, 71, 80]. Выход 89Zr в данной
[Zr(OH)x]4-x (x < 3), мономолекулярного гидроксида
реакции варьируется, по разным данным, от 8 до
Zr(OH)4, а также смешанных комплексных катио-
50 МБк/(мкA·ч) в зависимости от метода подготов-
нов и нейтральных молекул [85]. В растворах, со-
ки мишени.
держащих макроколичества Zr(IV), химическое по-
Альтернативным методом получения 89Zr из 89Y
ведение осложняется протеканием реакций оляции
является реакция 89Y(d,2n)89Zr [59, 69, 81-83]. Ис-
и оксоляции: при определенных условиях аква- и
пользование данного метода позволяет исключить
гидроксокомплексы полимеризуются с образова-
образование радионуклидных примесей 88Zr, 88Y.
нием соединений следующего состава Zr3(OH)48+,
Данная особенность связанна с различием энер-
Zr3(OH)57+, Zr4(OH)8+ [86]. Гидролиз циркония пода-
гетических порогов для реакций 89Y(d,2n)89Zr и
вляется только в сильнокислых средах (CHCl, HNO3 >
89Y(d,3n)88Zr (рис. 4), которые составляют 5.97 и
1.5 M) или в присутствии сильных комплексообра-
15.5 МэВ соответственно [82]. Образование незна-
зователей [87, 88]. Неорганические лиганды по спо-
чительных количеств 88Y возможно по реакциям
собности комплексообразования с Zr можно распо-
(d,t), (d,dn) и (d,p2n). Оптимальная энергия для ре-
ложить в следующем порядке: OH- > F- > PO3- >
РАДИОХИМИЯ том 63 № 3 2021
286
БУБЕНЩИКОВ и др.
Таблица 3. Методы ионообменной хроматографии для выделения 89Zr
Ионообменная
Исходный
смола, размер
Промывка после сорбции
Раствор десорбции
Выход
Ссылка
раствор
колонки
12 M HCl
Dowex 1×8 (Cl-)
150 мл 12 M HCl, 1.5 мл/мин
15 мл 2 М HCl,
63%
[69]
+H2O2
11 × 1 см
12 мл /мин
Dowex 2×8 (Cl-)
80%
11 × 1 см
3 М HCl
Dowex 1×8 (Cl-)
40 мл 12 М HCl
40 мл 2 M HCl
80%
[55]
11 × 1 см
1 М HCl
Dowex 50W×8
1 M HCl 2 мл/мин, 200 мл
200 мл смеси 0.5%
75%
[70]
(H+)
0.5 мл/мин 1 М СH3COOH, 200 мл
(COOH)2 и
22 × 1.5 см
0.1 М H3Citr, 2.2 мл/мин
0.1 М H3Citr (1 : 1),
12 М HCl
Dowex 21K (Сl-)
200 мл 12 М HCl 0.5 мл/мин,
1 мл/мин
21.7%
22 × 1.5 см
200 мл 1 М СH3COOH 0.5 мл/мин,
200 мл 0.1 М H3Citr 2.2 мл/мин
1 М HCl
Dowex 1×8 (Cl-)
180 мл
120 мл 2 М HCl
85%
[59]
22 × 1 см
12 M HCl
HClконц
Dowex 1×8 (Cl-)
20 мл HClконц
40 мл 2 М HCl
98%
[98]
+ H2O2
15 × 1 см
1 М HCl
Dowex 50×8 (H+)
10 мл 1 М HCl, 10 мл 2 М HCl
30 мл 1% (COOH)2 +
70%
15 × 1 см
0.1 М Na3Citr (1 : 1)
12 M HCl
Dowex 1×8 (Cl-)
25 мл 12 М HCl
30 мл 1 М HCl +
>80%
[61]
0.01 M (COOH)2
4 М HF
Dowex 1×8 (Cl-)
50 мл 4 М HF
8 мл 0.2 М HCl
100%
[64]
HClконц
1 стадия:
50 мл 12 M HCl
20 мл 6 M HCl; сушка
90%
[99]
Dowex-1×8 (Cl-)
и растворение в 5 мл
16.5 × 1 см
3 М HF
3 М HF
2-я стадия:
2 мл 3 М HF
1 M HNO3
90%
Dowex-1×8 (F-)
(общий
10 × 0.4 см
80%)
C2O2- > SO4
2- > CO2- > NO– > Cl- > СlО– [89, 90].
Zr(C2O4)4- возможно даже в сильнокислых средах
Томасом и Оуэне [91] был представлен следующий
(CHCl > 2 М). В нейтральных средах (pH 6.8-7.2)
ряд: цитрат > оксалат > малеат > тартрат > глико-
при избытке оксалат-иона Zr(IV) образует ком-
лят > сукцинат = малонат = малеинат = пропионат =
плекс Zr(C2O4)6-. Авторы отмечают, что уменьше-
ацетат = фумарат > формиат > сульфат > хлорид =
ние числа метиленовых фрагментов в гомологи-
нитрат. Однако данный ряд не в полной мере согла-
ческом ряду, как и введение группы -OH в состав
суется с данными, представленными Рябчиковым
молекулы карбоновой кислоты, способствует обра-
и соавт. [90]. Согласно опубликованным данным,
зованию более прочных комплексов. Данная тен-
наиболее стабильные комплексы с Zr(IV) образу-
денция хорошо согласуется с результатами опреде-
ет щавелевая кислота (оксалат > триоксиглутарат
ления констант устойчивости для комплексов Zr с
> цитрат > тартрат = лактат > сукцинат), что хоро-
щавелевой и малоновой кислотой. Так, Кобаяси и
шо согласуется с экспериментальными данными
соавт. [93] сообщают о более высоких константах
[92]. По сравнению с комплексами уксусной, ма-
устойчивости оксалатных комплексов (11.5, 20.8,
лоновой, малеиновой, янтарной и глутаровой кис-
27.2 и
29.7 для
[Zr(C2O4)]2+, [Zr(C2O4)2(H2O)]0,
лотой образование оксалатов циркония Zr(C2O4)2-,
[Zr(C2O4)3]2-,
[Zr(C2O4)4]4- соответственно), чем
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
287
для малонатных (10.4, 17.9, 22.0 для [Zr(C3Н2O4)]2+,
[Zr(C3Н2O4)2(Н2О)]0, [Zr(C3Н2O4)3]2- соответствен-
но).
Очистка 89Zr. Важной задачей на этапе произ-
водства 89Zr является выбор оптимальной техноло-
гии его выделения из облученной мишени, посколь-
ку Y, Fe и другие металлы могут конкурировать с
89Zr при формировании комплексов [55].
Первоначально для выделения 89Zr использова-
лиь различные ионообменные смолы (например,
Dowex 50WX8, Dowex 1×8), а в качестве растворов
для сорбции и десорбции - минеральные кислоты.
Наиболее популярными стали методы, основанные
на использовании анионообменных смол (главным
образом Dowex 1×8). Оптимальными растворами
для сорбции в данном случае являются разбавлен-
ные H2SO4, HF и смесь HCl-HF, а также концен-
трированные растворы HCl (CHCl > 8 M) [94-96].
Отмечено слабое сродство Zr(IV) к катионобмен-
ным смолам, при этом наиболее высокие коэффи-
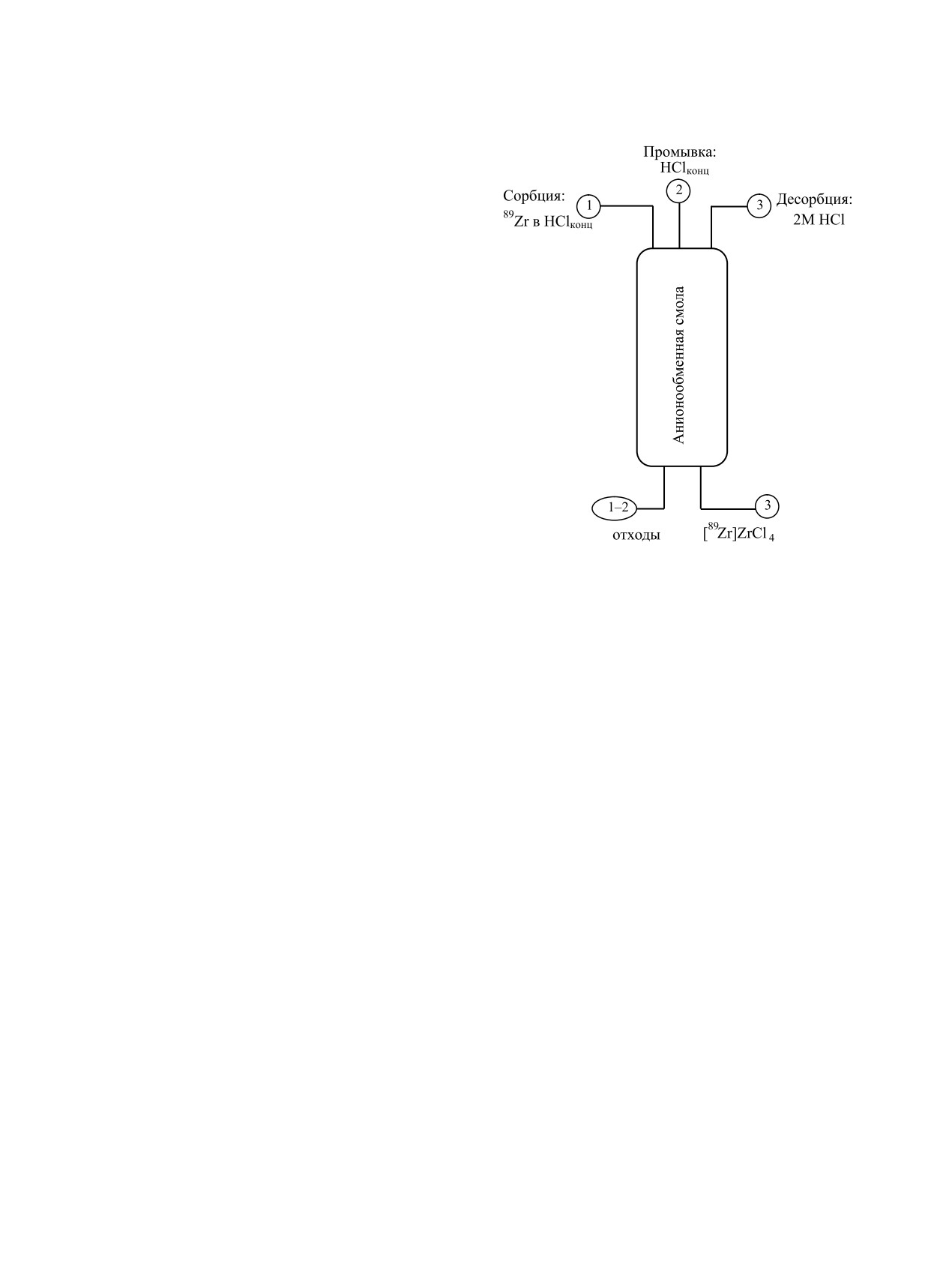
Рис. 5. Схема получения [89Zr]ZrCl4 на анионообменной
циенты распределения достигаются в концентриро-
смоле.
ванных растворах HClO4 (>6 M) [97].
Типичную схему переработки мишени с ис-
Помимо методов хроматографии для выделения
пользованием анионообменных смол можно пред-
89Zr были разработаны различные экстракционные
ставить следующим образом (рис. 5): облученную
схемы, как в комбинации с хроматографией, так
мишень растворяют в концентрированной соля-
и отдельно (табл. 4). Однако экстракционные ме-
ной кислоте, далее полученный раствор пропу-
тоды не получили широкого распространения по
скают через колонку с ионообменной смолой. Для
сравнению с хроматографией несмотря на высо-
эффективного удаления Y и других примесных
кую эффективность выделения 89Zr, как правило,
металлов через колонку пропускают несколько
при меньших затратах времени и в меньшем объ-
колоночных объемов HClконц. Десорбцию 89Zr осу-
еме конечного раствора. Неселективная очистка
ществляют 2 М HCl или комбинированными рас-
от примесных металлов и содержание органиче-
творами, содержащими, как правило, щавелевую
ских растворителей приводят к непригодности ко-
кислоту. Выход 89Zr при использовании данного
нечного продукта для применения в синтезе РФП
метода очистки колеблется от 70 до 98% в зависи-
[70, 100, 101].
мости от объема и состава элюента (табл. 3). При
этом полученные растворы могут значительно раз-
Большим прорывом в очистке 89Zr стали резуль-
личаться по составу химических и радионуклид-
таты, полученные Барончелли и Гросси. В 1965 г.
ных примесей. Например, Мейсом и соавт. [55]
они обнаружили, что гидроксаматные группы об-
было показанно, что [59Fe]Fe ведет себя аналогич-
ладают высокой аффинностью к цирконию и обра-
но 89Zr и ~65% [59Fe]Fe элюируется совместно с
зуют с ним стабильные комплексы [104]. Согласно
[89Zr]Zr-хлоридом.
данным рентгеноструктурного анализа, образуемые
комплексы имеют стехиометрическое соотношение
Главным недостатком данного метода являет-
1 : 4 (рис. 6) [105].
ся большой объем используемых растворов. При
низкой скорости потока это приводило к тому, что
Первое выделение 89Zr из облученной мише-
разделение занимало более 10 ч, а конечный про-
ни с использованием гидроксаматных смол было
дукт требовал концентрирования для дальнейшего
описано Мейсом и соавт. в 1994 г. [55]. В качестве
синтеза РФП.
элюента авторы использовали растворы щавелевой,
РАДИОХИМИЯ том 63 № 3 2021
288
БУБЕНЩИКОВ и др.
Таблица 4. Экстракционные методы выделения 89Zr
Процесс разделения,
Исходный
Конечный
Экстрагент
объемное отношение
Выход
Примечание
раствор
раствор
фаз
4 М HCl
0.5 М 4,4,4-трифтор-1-
Экстракция: 2 × 10 мл;
0.5 М HNO3 +
100%
Общий 25%
[61]
(2-тиенил)-1,3-
реэкстракция 1 : 1
0.5 М HF, сушка
бутандион в ксилоле
0.5 М HNO3 + 0.5 М
и растворение в
HF
12 М HCl
12 M HCl
Хроматография: смола
30 мл 1 М HCl +
>80%
Dowex 1 × 8 (Cl-), про-
0.01 M (COOH)2
мывка 25 мл 12 М HCl
1 М HCl
0.03 M дибутилфосфат
Экстракция 1 : 1, 4
4 М HF
94%
Общий
[64]
или
в дибутиловом эфире
промывки 1 М H2SO4
84.4%
H2SO4
1 : 1; реэкстракция
4 М HF
4 М HF
Хроматография: смола
8 мл 0.2 М HCl
100%
Dowex 1 × 8 (Cl-), про-
мывка 50 мл 4 M HF
5 × 10-4 M
10% Д2ЭГФК в цикло-
Экстракция 1 : 1
5 × 10-4 M
80%
89Zr
[100]
H2SO4
гексане
(10 мин)
H2SO4
остается в
10-3 М
10% Д2ЭГФК в цикло-
Экстракция 1 : 1
10-3 М H2SO4
~90%
исходном
[102]
H2SO4
гексане
растворе
1 Н H2SO4
0.1 М триэтиламин
Экстракция 1 : 1
0.1 М TOA в
~90%
[103]
(TOA) в циклогексане
циклогексане
9 М HCl
10% Д2ЭГФК в
Экстракция 1 : 1
Д2ЭГФК +
91%
[70]
н-гептане
H2SO4
9 М HCl
3% трифенилфосфи-
Экстракция 1 : 1
15 мл 0.5%
98%
ноксид в хлороформе
(3 мин), промывка
(COOH)2
10 мл 9 М HCl,
реэкстракция 15 мл
0.5% (COOH)2 (3 мин)
лимонной и уксусной кислот различной концентра-
шени в раствор HCl дополнительно вводили H2O2
ции. Наиболее высокая эффективность десорбции
[69, 98, 106, 107]. В настоящее время существует
со смолы была достигнута с использованием щаве-
неопределенность относительно влияния H2O2 на
левой кислоты, при этом увеличение концентрации
полноту последующей сорбции 89Zr. Голланд и со-
с 0.01 до 1.0 М повысило эффективность элюиро-
авт. [54] сообщают об отсутствии связи между до-
вания с ~20 до 98% в 2 мл раствора. Позже Голлан-
бавкой H2O2 и эффективностью сорбции, в то время
дом и соавт. [54] было показано, что [89Zr]Zr-окса-
как группа Мэтью Дж. О’Хары [108] сообщает об
лат, полученный с использованием гидроксамат-
улучшении эффективности сорбции с 76 до 95% при
ной смолы, обладает высокой химической и ради-
растворении мишени в присутствии H2O2. Авторы
онуклидной чистотой и подходит для получения
предполагают, что H2O2 способствует разрушению
комплексов с дефероксамином с высокой молярной
оксида циркония и/или цирконильных частиц, кото-
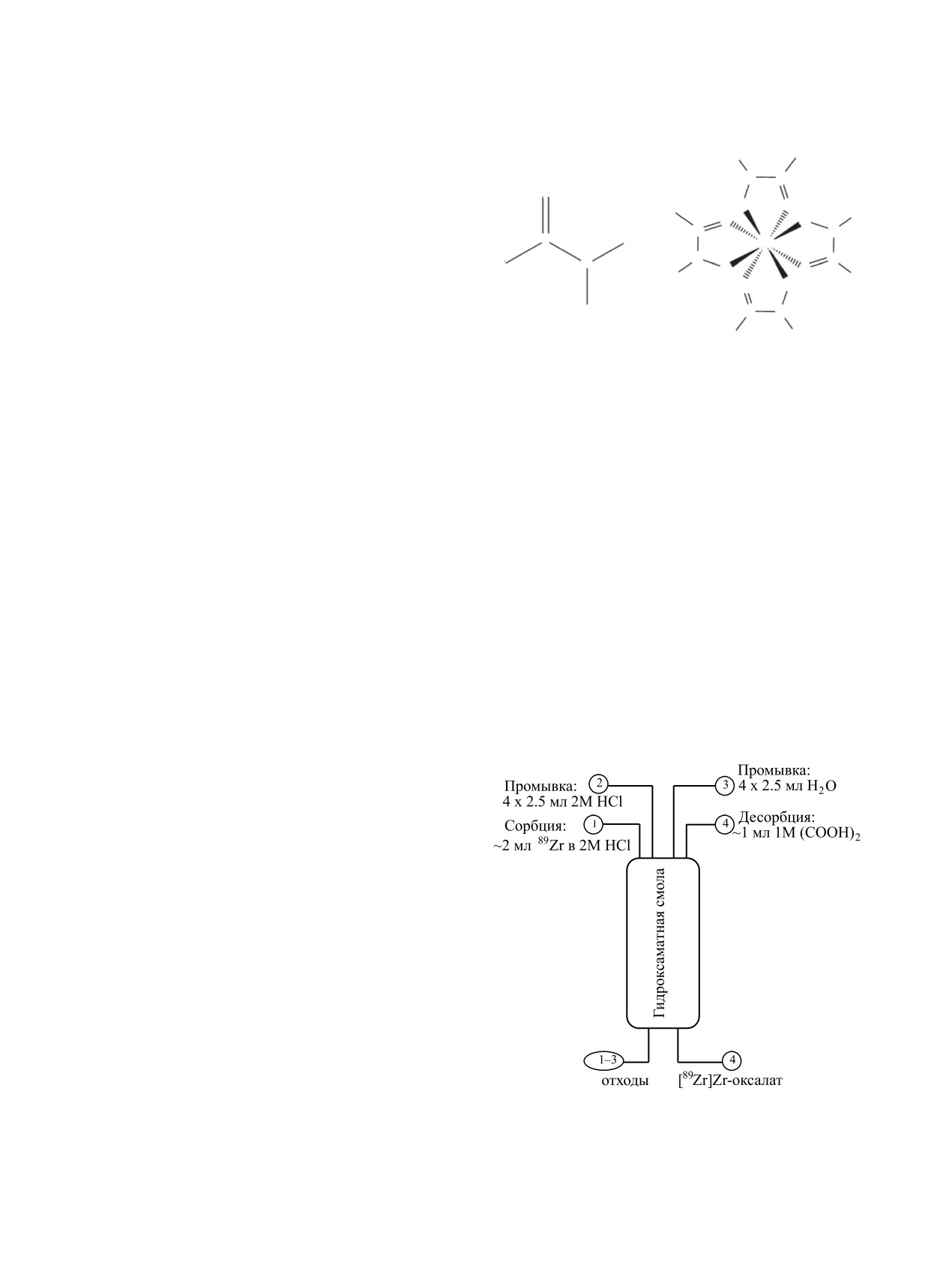
активностью. В настоящее время данный способ
рые могут образовываться во время облучения или
(рис. 7) широко используется для лабораторного
растворения мишени.
выделения 89Zr из облученных мишеней [54, 55, 57,
Важно отметить, что гидроксаматные смолы,
66, 72], а также реализован на различных модулях
упомянутые в подавляющем большинстве публика-
синтеза [56, 60, 106].
ций, изготовлены согласно способу, предложенно-
В ряде работ для обеспечения полного окисле-
му Верелем и соавт [72]. Смола ZR Resin (TrisKem
ния Zr до Zr (IV) при растворении облученной ми- International), вероятно, является единственной на
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
289
сегодняшний день коммерчески доступной гидрок-
R
R′
саматной смолой [109]. Согласно данным произ-
N
C
O
водителя, эта смола обладает высокой селектив-
R′
O
O
R
ностью к ионам Zr(IV) в широком диапазоне кон-
O
O
центраций HCl (0.01-10 М) и в растворах HNO3
с
C
N
C
OH
Zr
концентрациями до 5 М [110]. В то же время смола
N
C
N
R′
O
O
имеет низкую аффинность к Y, а также к Fe(III) в
R
R′
O
O
растворах 1-6 М HCl и, следовательно, может быть
R
C
N
эффективно использована для выделения 89Zr из об-
лученной мишени.
R′
R
Основной проблемой применения гидроксамат-
(а)
(б)
ных смол является использование щавелевой кис-
Рис. 6. (а) гидроксамовая кислота, (б) гидроксаматный
лоты с высокой концентрацией (~1 М). Щавелевая
комплекс Zr(IV). R, R′ - углеводородные радикалы.
кислота является токсичной, поскольку может вы-
зывать острую почечную недостаточность из-за об-
ческой и радионуклидной чистоте. Согласно дан-
струкции почечных канальцев оксалатом кальция.
ным ICP-MS-анализа, в полученных растворах
Дополнительно Пандя и соавт. [111] сообщают, что
[89Zr]Zr-оксалата и [89Zr]Zr-фосфата было обна-
высокая стабильность оксалата циркония влияет
ружено 0.4-5.38 мг/л Al, 0.6-1.2 мг/л Fe, 0.15-
на эффективность комплексообразования 89Zr с
макроциклическими лигандами. Так, при синтезе
0.5 мг/л Y.
комплексов 89Zr с DOTA, DOTAM и DOTP авто-
Для удаления избытка щавелевой кислоты из
ры считают более предпочтительным использова-
конечного раствора Мейсом и соавт. [55] были
ние растворов [89Zr]ZrCl4, чем [89Zr]Zr-оксалата.
описаны способы декарбоксилирования (добав-
Выход реакции комплексообразования 89Zr c ли-
ление H2O2 в 6 М HCl при 80°C, сушка реакцион-
гандом DOTA (инкубирование 120 мин, 99°С, рН
ной смеси при комнатной температуре в вакууме)
7.0) составил 65% и 100% для [89Zr]Zr-оксалата и
и вакуумной сублимации (комнатная температура,
[89Zr]ZrCl4 соответственно. Несмотря на очевид-
26.7 мПа). Однако следует отметить, что раство-
ные минусы, в настоящее время [89Zr]Zr-оксалат
ры 89Zr после декарбоксилирования и сублимации
используется практически во всех опубликован-
показали различную эффективность комплексо-
ных процедурах синтеза 89Zr-РФП, а для удаления
щавелевой кислоты проводится очистка методом
эксклюзионной хроматографии [72]. Тем не менее,
в настоящее время действительно не существует
однозначного мнения о влиянии щавелевой кис-
лоты на комплексообразование 89Zr с лигандами,
обеспечивающими функциональную пригодность
РФП.
Альтернативный вариант очистки 89Zr с исполь-
зованием гидроксаматной смолы был предложен
Пандей и соавт. [112]. Для десорбции 89Zr с ги-
дроксаматной смолы авторы использовали фос-
фатный буфер (1.2 М K2HPO4/KH2PO4, рН 3.5).
Колонку предварительно заполняли фосфат-
ным буфером ~0.25 мл и выдерживали в течение
30 мин, после чего 89Zr элюировали 2 мл буфер-
ного раствора с выходом 91.7 ± 3.7%. По мнению
авторов, данный способ не уступает классическо-
Рис. 7. Схема получения [89Zr]Zr-оксалата на гидрокса-
му методу получения [89Zr]Zr-оксалата по хими-
матной смоле.
РАДИОХИМИЯ том 63 № 3 2021
290
БУБЕНЩИКОВ и др.
Таблица 5. Методы получения [89Zr]ZrCl4
Коэффициент очистки
Анионит
Элюент
Выход
Ссылка
по Y
AG MP-1M (Cl-)
7.5 мл 6 М HCl
84 ± 4%
3.1 × 105
[108]
5 мл 6 M HCl + 0.33 мМ NaF
96.2 ± 1.9%
TBP Resin
1 мл 0.1 М HCl
89 ± 3%
1.5 × 105
[63]
образования с дефероксамином:
89Zr, получен-
Гравес и соавт. [63] исследовали возможность
ный сублимационным методом, образовывал ком-
получения [89Zr]ZrCl4 на смолах UTEVA и TBP.
плексы с дефероксамином даже при очень низких
Авторы отмечают, что, несмотря на высокие ко-
концентрациях (выход > 90% при 10 мкМ дефе-
эффициенты распределения при СHCl > 9 M на
роксамина), тогда как 89Zr, полученный методом
обеих смолах, смола UTEVA характеризуется бо-
декарбоксилирования, образовывал комплексы
лее медленной кинетикой сорбции. Наиболее вы-
с низким выходом даже при высокой концентра-
сокая эффективность разделения была достигнута
ции дефероксамина (выход < 60% при 10 мМ).
на смоле TBP Resin (выход 89 ± 3% в 1 мл 0.1 М
Позже Голландом и соавт. [54] был предложен
HCl). Однако, согласно данным MP-AES-анали-
более простой метод с использованием анионо-
за, метод, основанный на смоле TBP Resin, по-
обменного картриджа Sep-pak QMA. 89Zr коли-
казал более низкую эффективность очистки от
чественно улавливается на картридже Sep-pak
примесных металлов, таких как Ni, Fe, Cr, Mn,
QMA, после чего картридж промывают большим
Cu, по сравнению с двухстадийным методом, ос-
объемом воды (~40 мл). 89Zr полностью элюируют
нованным на гидроксаматной смоле и картридже
300-500 мкл 1.0 М HCl. Данный способ позволяет
Sep-pak QMA. Важно отметить, что для работы с
удалить более 99.8% (COOH)2 и широко использу-
[89Zr]ZrCl4 при pH > 5 необходимо введение в рас-
ется для получения [89Zr]ZrCl4 из [89Zr]Zr-оксалата
твор комплексонов для предотвращения гидролиза
[54, 60, 63, 113, 114]. Стоит отметить, что элюи-
89Zr [54, 63, 114].
рование картриджа Sep-pak QMA также возможно
Поскольку оксалат циркония является потенци-
изотоническим раствором NaCl, но с низким выхо-
ально токсичным, а хлорид циркония склонен к ги-
дом (22-38% в 500 мкл 0.9% NaCl) [54]. Позже не-
дролизу, авторами настоящего обзора была предло-
сколькими группами были описаны альтернатив-
жена технология получения растворов 89Zr в форме
ные способы получения растворов 89Zr высокой
[89Zr]Zr-цитрата [92]. Данный метод основан на ис-
химической и радионуклидной чистоты в форме
пользовании комбинации гидроксаматной смолы ZR
[89Zr]ZrCl4 (табл. 5).
Resin с хелатной смолой Chelex-100, которая при раз-
О’Хара и соавт. [108] использовали для по-
личных значениях pH способна выступать в качестве
лучения [89Zr]ZrCl4 анионообменную смолу AG
анионита, катионита или хелатора [115]. Результаты,
MP-1M (Cl-). Авторы рассмотрели возможность
полученные при изучении распределения U, Zr-Nb,
элюирования 89Zr растворами HCl различной кон-
Th, Mo, Te, Tc на смоле Chelex-100 (NH4+-форма),
центрации (0.1-9 М), при этом оптимальная кон-
свидетельствуют о том, что Zr имеет сравнительно
центрация HCl составила 6 М. Однако часть 89Zr
низкие коэффициенты распределения (<30) при со-
оставалась на колонке (14
± 5%). Для повыше-
рбции из разбавленных растворов серной, соляной,
ния эффективности элюирования был использо-
лимонной и винной кислот и высокий (>100) коэф-
ван комбинированный раствор 6 M HCl + 0.33 мМ
фициент распределения в случае 0.1 М щавелевой
NaF. Необходимо отметить, что присутствие ионов
кислоты при pH < 1. При повышении значения pH
F- в конечном растворе неприемлемо для РФП,
коэффициенты распределения уменьшаются и до-
поэтому авторы дополнили данный метод вто-
стигают нуля при pH > 4, что позволяет проводить
рой колонкой, заполненной гидроксаматной смо-
высокоэффективную десорбцию растворами солей
лой, для получения 89Zr в форме [89Zr]Zr-оксалата
различных карбоновых кислот [116, 117]. Данное
(выход >90% в 0.3 мл 0.8 М (COOH)2 [107]).
свойство было использовано для разработки метода
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
291
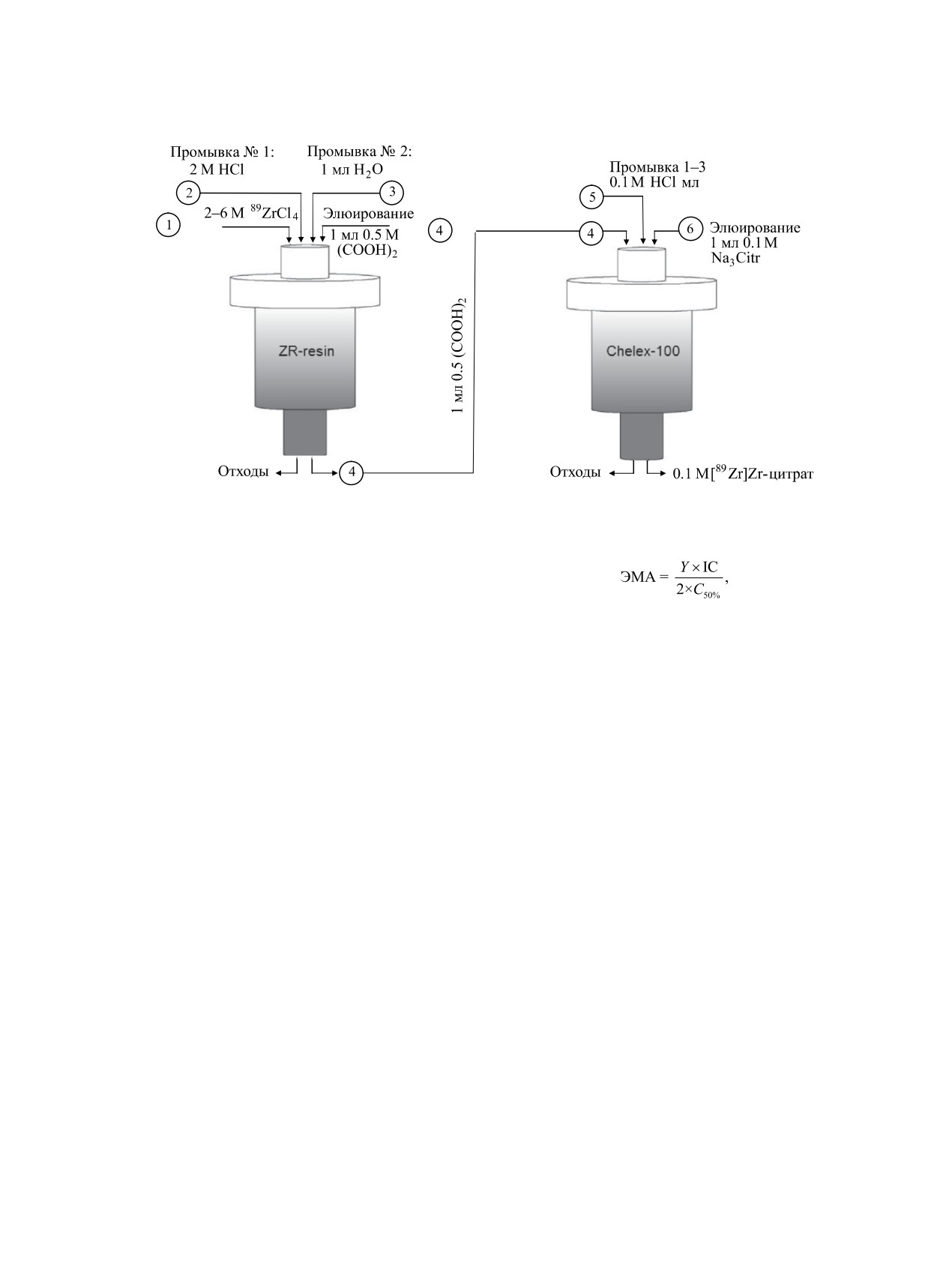
Рис. 8. Метод получения [89Zr]Zr-цитрата.
двухступенчатой очистки: на первой стадии прово-
дится высокоселективная очистка на гидроксамат-
ной смоле ZR-resin, после чего получаемый [89Zr]
где Y - выход изотопа, МБк/(мкA·ч); IC-интеграль-
Zr-оксалат используется для сорбции на второй ко-
ный ток пучка, мкA·ч; C50% - концентрация хелато-
лонке со смолой Chelex-100. Элюирование 89Zr про-
ра, необходимая для достижения 50%-ного выхода
водится 0.1-1 М раствором цитрата натрия с высо-
комплексообразования.
ким выходом (>90%) (рис. 8). Полученный раствор
имеет концентрацию, близкую к изотонической, зна-
ЭМА также зависит от химической формы 89Zr и
чения рН, близкие к физиологическим, стабилен не
присутствия эксципиентов. Сегодня эксперименты
менее 14 сут и пригоден для синтеза РФП.
по определению ЭМА преимущественно выполне-
Одной из важнейших характеристик таргетно-
ны с [89Zr]Zr-оксалатом, в то время как для [89Zr]
го РФП в настоящее время является эффективная
Zr-хлорида получены лишь единичные данные
молярная активность (ЭМА), поскольку инъекция
(табл. 6).
РФП с низкой ЭМА может привести к насыщению
Максимально высокая ЭМА
(379
±
целевых рецепторов избытком немеченого лиганда,
23 ГБк/мкмоль) получена в настоящее время при
что приведет к снижению качества диагностиче-
фракционном элюировании [89Zr]Zr-оксалата с ги-
ского исследования. Метод расчета ЭМА для 89Zr
дроксаматной смолы [71]. Необходимо отметить,
основан, как правило, на титровании бифункцио-
что авторы лишь изредка публикуют данные по
нального хелатора дефероксамина (ДФО) и поэто-
титрованию дефероксамина и не указывают ито-
му учитывает наличие любого металла, способного
говое значение ЭМА. Так, Голланд и соавт. [54]
образовывать комплексы с ДФО [54, 106]. Стоит
сообщают о достижении C50% при концентрации
отметить, что данная величина является не идеаль-
ДФО ~9 пмоль (ЭМА 17.39-44.215 ГБк/мкмоль),
ной для сравнения чистоты полученных растворов,
Охара и соавт. [106] - C50% ~10 пмоль ДФОМ (44 ±
поскольку зависит от параметров облучения. Экс-
7 ГБк/мкмоль), Вутен и соавт. [56] - C50% =
периментально показано, что увеличение времени
0.4 нмоль DFO-NCS (4.0 ± 0.3 ГБк/мкмоль).
облучения, тока и энергии пучка приводит к увели-
чению ЭМА, равно как и увеличение толщины и/
При обсуждении ЭМА необходимо подчер-
или массы мишени снижает ЭМА [71]:
кнуть противоречивые данные, полученные для
РАДИОХИМИЯ том 63 № 3 2021
292
БУБЕНЩИКОВ и др.
Таблица 6. Сравнение ЭМА для различных форм 89Zr
Форма 89Zr
Метод получения
Метод измерения
ЭМА, ГБк/мкмоль
Ссылка
[89Zr]Zr-хлорид
TBP resin
Титрование ДОТА
0.085 ± 0.048
[63]
Гидроксаматная смола +
0.518 ± 0.056
Sep-pak QMA
Титрование ДФО
33.7-84.6
[60]
[89Zr]Zr-оксалат
Гидроксаматная смола
Титрование ДФО
0.2-13.1
[56]
Титрование DFO-NCS
4.0 ± 0.3
[57]
Титрование ДФО
17.4-44.2
[54]
36.3 ± 2.3
[67]
60 ± 70
[68]
75 ± 8
[63]
75.5-158.4
[60]
105.0 ± 70.3
[118]
51-379
[71]
Титрование ДФОМ
44 ± 7
[106]
AG MP-1M (Cl-) + гидрок-
279 ± 61
[107]
саматная смола
[89Zr]Zr-фосфат
Гидроксаматная смола
ICP-MS
41.2 ± 19.2
[112]
растворов
[89Zr]Zr-хлорида. В частности, Гра-
Таким образом, способы получения растворов
вес и соавт. [63] наблюдали отличающиеся зна-
89Zr значительное влияют на дальнейший син-
чения ЭМА для [89Zr]Zr-хлорида, которые были
тез и эффективность РФП Например, описано
получены различными методами: один обра-
несколько противоречивых результатов доклини-
зец был получен конверсией
[89Zr]Zr-оксалата
ческих исследований. Абу и соавт. [119] наблюда-
в
[89Zr]Zr-хлорид на картридже Sep-pak QMA
ли накопление [89Zr]Zr-хлорида в мягких тканях,
(518 ± 56 МБк/мкмоль), второй - на смоле TBP-
а затем в скелете, тогда как Голланд и соавт. [54]
Resin
(85
± 48 МБк/мкмоль). Для определения
отмечают высокое накоплении
[89Zr]Zr-хлорида
ЭМА использовали хелатор ДОТА, и реакцию
в печени. Аналогичным примером является ре-
комплексообразования проводили в достаточно
зультаты, представленные в работах [35, 119]. Абу
жестких условиях (pH 5.0-7.5, 90°С, 45 мин), од-
и соавт. [119] обнаружили высокое накопление
нако авторы отмечают значительный гидролиз
[89Zr]Zr-фосфата в печени (~60%/г) и селезенке, со-
[89Zr]Zr-хлорида, а природа различий между об-
храняющееся в течение 6 сут. Однако данные, пред-
разцами остается невыясненной. Еще одним при-
ставленные Бансал и соавт. [35] показывают, что
мером является работа [60], в которой сообщается
после внутривенного введения [89Zr]Zr-фосфата на-
о близких значениях ЭМА для [89Zr]Zr-оксалата
копление активности происходит главным образом
(75.5-158.4 ГБк/мкмоль) и
[89Zr]Zr-хлори-
в скелете. Наиболее вероятным объяснением данных
да, полученного на картридже Sep-pak QMA
фактов является присутствие 89Zr в коллоидной фор-
(33.7-84.6 ГБк/мкмоль). Кроме того, авторы ука-
ме. Таким образом, помимо исследования методов
зывают, что в конечном растворе [89Zr]Zr-хло-
получения радионуклида необходим тщательный
рида были обнаружены оксалат-ионы
(1.55
±
0.37 мг/мл). Мы считаем, что данные различия
подход к разработке и постадийному контролю каче-
ЭМА для [89Zr]Zr-хлорида вызваны неполной
ства как исходных субстанций, так и готовых РФП
очисткой от щавелевой кислоты на картридже
на основе 89Zr, поскольку даже для радионуклидов,
Sep-pak QMA, поскольку присутствие даже сле-
которые уже прочно вошли в мировую клиническую
довых количеств щавелевой кислоты приводит
практику, например, 68Ga, все же существуют неко-
к изменению хроматографического поведения
торые неясности и особенности в анализе радиохи-
[89Zr]Zr-хлорида [92].
мической чистоты его препаратов [120].
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
293
ЗАКЛЮЧЕНИЕ
nndc.bnl.gov (дата обращения: 1.02.2020).
10. Nayak T.K., Brechbiel M.W. // Bioconjugate Chem.
2009. Vol. 20, N 5. P. 825-841.
В последнее десятилетие наблюдается значи-
11. Lubberink M., Van Schie A., de Jong H.W. et al. //
тельный прогресс в области разработки и синтеза
J. Nucl. Med. 2006. Vol. 47, N 8. P. 1375-1381.
РФП на основе 89Zr. Несмотря на многообещающие
12. Börjesson P.K., Jauw Y.W., Boellaard R. et al. // Clin.
результаты, полученные при проведении клиниче-
Cancer Res. 2006. Vol. 12,. N 7. P. 2133-2140.
ских и доклинических исследований, имеется ряд
13. Börjesson P.K., Jauw Y.W., de Bree R. et al. // J. Nucl.
проблем, связанных со сложностью выделения,
Med. 2009. Vol. 50, N 11. P. 1828-1836.
хелатирования, синтеза конъюгатов и контроля ка-
14. Menke-van der Houven C.W., van Oordt E.C.G.,
чества полученных РФП. Использование гидрокса-
Huisman M.C. et al. // Oncotarget. 2015. Vol. 6, N 30.
матных смол значительно упростило технологию
P. 30384.
получения растворов 89Zr, позволяя эффективно
15. Pandit-Taskar N., O’Donoghue J.A., Durack J.C.
очищать 89Zr от мишенного иттрия и различных ме-
et al. // Clin. Cancer Res. 2015. Vol. 21, N
23.
P. 5277-5285.
таллических примесей, однако данный метод имеет
16. Pandit-Taskar N., O’Donoghue J.A., Beylergil V.
существенный недостаток - основным элюентом
et al. // Eur. J. Nucl. Med. 2014. Vol. 41, N 11.
является щавелевая кислота. В связи с этим весь-
P. 2093-2105.
ма перспективной химической формой для синтеза
17. den Hollander M.W., Bensch F., Glaudemans A.W.
РФП и является цитрат циркония-89. Мы надеем-
et al. // J. Nucl. Med. 2015. Vol. 56, N 9. P. 1310-1314.
ся, что разработка технологии получения исходных
18. Lamberts L.E., Menke-van der Houven C.W.,
растворов даст толчок к развитию технологии РФП
ter Weele E.J. et al. // Clin. Cancer Res. 2016. Vol. 22,
89Zr в целом, и разработанные препараты займут
N 7. P. 1642-1652.
свое место в клинической практике.
19. Dijkers E.C., Kosterink J.G., Rademaker A.P. et al. //
J. Nucl. Med. 2009. Vol. 50, N 6. P. 974-981.
КОНФЛИКТ ИНТЕРЕСОВ
20. Dijkers E.C., Oude Munnink T.H., Kosterink J.G.
et al. // Clin. Pharmacol. Ther. 2010. Vol. 87, N 5.
Авторы заявляют об отсутствии конфликта
P. 586-592.
интересов.
21. Gebhart G., Lamberts L.E., Wimana Z. et al. // Ann.
Oncol. 2015. Vol. 27, N 4. P. 619-624.
СПИСОК ЛИТЕРАТУРЫ
22. Muylle K., Flamen P., Vugts D.J. et al. // Eur. J. Nucl.
Med. Mol. Imaging. 2015. Vol. 42, N 8. P. 1304-1314.
23. Rizvi S.N., Visser O.J., Vosjan M.J. et al. // Eur. J. Nucl.
1.
Zeglis B.M., Lewis J.S. // Dalton Trans. 2011. Vol. 40,
Med. Mol. Imaging. 2012. Vol. 39, N 3. P. 512-520.
N 23. P. 6168-6195.
24. Gaykema S.B., Brouwers A.H., Lub-de Hooge M.N.
2.
Holland J.P., Williamson M.J., Lewis J.S. // Mol.
et al. // J. Nucl. Med. 2013. Vol, 54. N 7. P. 1014-1018.
Imaging. 2010. Vol. 9, N 1. P. 7290-2010.
25. Bahce I., Huisman M.C., Verwer E.E. et al. // EJNMMI
3.
Sánchez-Crespo A., Andreo P., Larsson S.A. // Eur. J.
Res. 2014. Vol. 4, N 1. P. 35.
Nucl. Med. Mol. Imaging. 2004. Vol. 31, N 1. P. 44-51.
26. Oosting S.F., Brouwers A.H., van Es S.C. et al. // J. Nucl.
4.
Conti M., Eriksson L. // EJNMMI Physics. 2016. Vol. 3,
Med. 2015. Vol. 56, N 1. P. 63-69.
N 1. P. 8.
27. van Asselt S.J., Oosting S.F., Brouwers A.H.
5.
Disselhorst J.A., Brom M., Laverman P. // J. Nucl. Med.
et al. // J. Nucl. Med. 2014. Vol. 55, N 7. P. 1087-1092.
2010. Vol. 51, N 4. P. 610-617.
28. Viola-Villegas N.T., Sevak K.K., Carlin S.D.
6.
Moses W.W. // Nucl. Instrum. Meth. Phys. Res., Sect. A.
et al. // Mol. Pharmaceutics. 2014. Vol. 11, N 11.
2011. Vol. 648, N 1. P. 236-240.
P. 3965-3973.
7.
Laboratoire National Henri Becquerel [Электронный
29. Vosjan M.J., Vercammen J., Kolkman J.A. et al. // Mol.
Cancer Ther. 2012. Vol. 11, N 4. P. 1017-1025.
1.02.2020).
30. Nagengast W.B., Lub-de Hooge M.N., Oosting S.F.
8.
Grignon C., Barbet J., Bardiès M., Carlier T. // Nucl.
et al. // Cancer Res. 2011.Vol. 71, N 1. P. 143-153.
Instrum. Meth. Phys. Res., Sect. A. 2007. Vol. 571,
31. Hoeben B.A., Kaanders J.H., Franssen G.M.
N 1-2. P. 42-145.
et al. // J. Nucl. Med. 2010. Vol. 51, N 7. P. 1076-1083.
9.
National Nuclear Data Center, Brookhaven National
32. Jacobson O., Zhu L., Niu G. et al. // Mol. Imaging Biol.
2011. Vol. 13, N 6. P. 1224-1233.
РАДИОХИМИЯ том 63 № 3 2021
294
БУБЕНЩИКОВ и др.
33. Charoenphun P., Meszaros L.K., Chuamsaamarkkee K.
57. Queern S.L., Aweda T.A., Massicano A.V.F.
et al. // Eur. J. Nucl. Med. Mol. Imaging. 2015. Vol. 42,
et al. // Nucl. Med. Biol. 2017. Vol. 50. P. 11-16.
N 2. P. 278-287.
58. Dabkowski A.M., Probst K., Marshall C. // AIP Conf.
34. Sato N., Wu H., Asiedu K. O. et al. // Radiology. 2015.
Proc. 2012. Vol. 1509, N 1. P. 108-113.
Vol. 275, N 2. P. 490-500.
59. Tang Y., Shuntao L., Yang Y. et al. // Appl. Radiat. Isot.
35. Bansal A.,
Pandey M.K., Demirhan Y.E.
2016. Vol. 118. P. 326-330.
et al. // EJNMMI Res. 2015. Vol. 5, N 1. P. 19.
60. Lin M., Mukhopadhyay U., Waligorski G.J.,
36. Heneweer C., Holland J.P., Divilov V. et al. // J. Nucl.
Balatoni J.A. // Appl. Radiat. Isot. 2016. Vol. 107.
Med. 2011.Vol. 52, N 4. P. 625-633.
P. 317-322.
37. Heuveling D.A., Visser G.W., Baclayon M. et al. //
61. Link J.M., Krohn K.A., Eary J.F. et al. // J. Label. Compd.
J. Nucl. Med. 2011. Vol. 52, N 10. P. 1580-1584.
Radiopharm. 1986. Vol. 23. P. 1297-1298.
38. Ruggiero A., Villa C.H., Holland J.P. et al. // Int. J.
62. Link J.M., Krohn K.A., O’Hara M.J. // Appl. Radiat.
Nanomed. 2010.Vol. 5, P. 783-802.
Isot. 2017. Vol. 122. P. 211-214.
39. Keliher E.J., Yoo J., Nahrendorf M. et al. // Bioconjugate
63. Graves S.A., Kutyreff C., Barrett K.E. et al. // Nucl. Med.
Biol. 2018. Vol. 64-65. P. 1-7.
Chem. 2011. Vol. 22, N 12. P. 2383-2389.
64. Dejesus O.T., Nickles R.J. // Appl. Radiat. Isot. 1990.
40. Deri M.A., Zeglis B.M., Francesconi L.C.,
Vol. 41, N 8. P. 789-790.
Lewis J.S. // Nucl. Med. Biol. 2013. Vol, 40. N 1. P. 3-14.
65. Ciarmatori
A.,
Cicoria
G.,
Pancaldi
D.
41. Fischer
G.,
Seibold
U.,
Schirrmacher R.
et al. // Radiochim. Acta. 2011. Vol. 99, N
10.
et al. // Molecules. 2013. Vol. 18, P. 6469-6490.
P. 631-634.
42. Marquez-Nostra B.V., Viola N. The Radiopharmaceutical
66. Walther M., Gebhardt P., Grosse-Gehling P.
Chemistry of Zirconium-89 // Radiopharmaceutical
et al. // Appl. Radiat. Isot. 2011. Vol. 69, N
6.
Chemistry / Eds J. Lewis, A. Windhorst, B. Zeglis.
P. 852-857.
Cham: Springer, 2019. P. 371-390.
67. Scharli R.K., Price R.I., Chan S. et al. // AIP Conf. Proc.
43. Bhatt N.B., Pandya D.N., Wadas T.J. // Molecules. 2018.
2012. Vol. 1509, N 1. P. 101-107.
Vol. 23, N 3. P. 638.
68. Ellison P.A., Valdovinos H.F., Graves S.A. et al. // Appl.
44. Heskamp S., Raavé R., Boerman O. et al. // Bioconjugate
Radiat. Isot. 2016. Vol. 118, P. 350-353.
Chem. 2017. Vol. 28, N 9. P. 2211-2223.
69. Zweit J., Downey S., Sharma H.L. // Appl. Radiat. Isot.
45. Vugts D.J., Van Dongen G. // Drug Discov. Today. 2011.
1991. Vol. 42, N 8. P. 199-201.
Vol. 8, N 2-4. P. 53-61.
70. Kandil S.A., Scholten B., Saleh Z.A. et al. // J. Radioanal.
46. Audi G., Wapstra A.H., Thibault C. // Nucl. Phys. A.
Nucl. Chem. 2007. Vol. 274, N 1. P. 45-52.
2003. Vol. 729, N 1. P. 337-676.
71. Alnahwi A., Tremblay S., Guérin B. // Appl. Sci. 2018.
47. Saha G.B., Porile N.T., Yaffe L. // Phys. Rev. 1966.
Vol. 8. N 9. P. 1579.
Vol. 144, N 3. P. 962-971.
72. Verel I., Visser G.W., Boellaard R. et al. // J. Nucl. Med.
48. Kandil S.A., Spahn I., Scholten B. et al. // Appl. Radiat.
2003. Vol. 44. N 8. P. 1271-1281.
Isot. 2007. Vol. 65, N 5. P. 561-568.
73. Rowshanfarzad P., Jalilian A., Sabet M. // Nukleonika.
49. Laforest R., Lapi S. E., Oyama R. et al. // Mol. Imaging
2005. Vol. 50, N 3. P. 97-103.
Biol. 2016. Vol. 16, N 6. P. 952-959.
74. Khandaker M.U., Kim K., Lee M.W. et al. // Nucl.
50. Lewis V.E., Zieba K.J. // Nucl. Instrum. Meth. 1980.
Instrum. Meth. Phys. Res., Sect. B. 2012. Vol. 271,
Vol. 174, N 1-2. P. 141-144.
P. 72-81.
51. Semkova V., Bauge E., Plompen A.J.M.,
75. Uddin M.S., Khandaker M.U., Kim K.S. et al. // Nucl.
Smith D.L. // Nucl. Phys. A. 2010. Vol. 832, N 3-4.
Instrum. Meth. Phys. Res., Sect. B. 2008. Vol. 266, N 1.
P. 149-169.
P. 13-20.
52. Omara H.M., Hassan K.F., Kandil S.A.
76. Levkovski V.N. Cross Sections of Medium Mass Nuclide
et al.
// Radiochim. Acta.
2009. Vol.
97, N
7.
Activation (A = 40-100) by Medium Energy Protons
P. 467-471.
and Alpha Particles (E = 10-50 MeV). Moscow: Inter-
53. Kasbollah A., Eu P., Cowell S., Deb P. // J. Nucl. Med.
Vesi, 1991.
Technol. 2013. Vol. 41, N 1. P. 35-41.
77. Sharifian M., Sadeghi M., Alirezapour B. // Appl. Radiat.
54. Holland J.P., Sheh Y., Lewis J.S. // Nucl. Med. Biol.
Isot. 2017. Vol. 127. P. 161-165.
2009. Vol. 36. P. 729-739.
78. Taghilo M., Kakav T., Rajabifar S., Sarabadani P. // Int.
55. Meijs W.E., Herscheid J.D.M., Haisma H.J. // Appl.
J. Phys. Sci. 2012. Vol. 7, N 9. P. 1321-1325.
Radiat. Isot. 1994. Vol. 45, N 12. P. 1143-1147.
79. Mustafa M.G., West H.I., Jr., O’Brien H. et al. // Phys.
56. Wooten A., Madrid E., Schweitzer G.D. et al. // Appl.
Rev. 1988. Vol. 38, N 4. P. 1624.
Sci. 2013. Vol. 3, N 3. P. 593-613.
80. Infantino A., Cicoria G., Pancaldi D. et al. // Appl.
РАДИОХИМИЯ том 63 № 3 2021
ПОЛУЧЕНИЕ Р
АСТВОРОВ 89Zr
295
Radiat. Isot. 2011. Vol. 69, N 8. P. 1134-1137.
Nucl. Chem. 1997. Vol. 218, N 2. P. 229-231.
81. Uddin M. S., Baba M., Hagiwara M. et al. // Radiochim.
104. Baroncelli F., Grossi G. // J. Inorg. Nucl. Chem. 1965.
Acta. 2007. Vol. 95, N. 4. P. 187-192.
Vol. 27, N. 5. P. 1085-1092.
82. Manenti S., Haddad F., Groppi F. // Nucl. Instrum. Meth.
105. Guérard F., Lee Y.S., Tripier R. et al. // Chem. Commun.
Phys. Res., Sect. B. 2019. Vol. 458. P. 57-60.
83. Lebeda O., Štursa J., Ráliš, J. // Nucl. Instrum. Meth.
2013. Vol. 49, N 10. P. 1002-1004.
Phys. Res., Sect. B. 2015. Vol. 360. P. 118-128.
106. O’Hara M.J., Murray N.J., Carter J.C. et al. // Appl.
84. Shannon R. D. // Acta Crystallogr., Sect. A.
1976.
Radiat. Isot. 2018. Vol 132. P. 85-94.
Vol. 32, N 5. P. 751-767.
107. O’Hara M.J., Murray N.J., Carter J.C.
85. Соловкин А.С., Цветкова З.Н. // Успехи химии. 1962.
Т. 31, N 11. С. 1394-1416.
et al. // J. Chromatogr. A. 2018. Vol. 1567. P. 37-46.
86. Ekberg C., Källvenius G., Albinsson Y., Brown P. L. //
108. O’Hara M.J., Murray N.J., Carter J.C.,
J. Solution Chem. 2004. Vol. 33, N 1. P. 47-79.
Morrison S.S.// J. Chromatogr. A. 2018. Vol. 1545.
87. Mayer A., Bradshaw G. // Analyst. 1952. Vol. 77, N 918.
P. 48-58.
P. 476-483.
109. ZR Resin: Product sheet. Triskem International. P. 2-4.
88. Benedict J.T., Schumb W.C., Coryell C.D. // J. Am.
Chem. Soc. 1954. Vol. 76, N. 8. P. 2036-2040.
110. TrisKem International, posters and presentations
89. Aja S.U., Wood S.A., Williams-Jones A.E. // Appl.
Geochem. 1995. Vol. 10, N 6. P. 603-620.
international.com/posters-and-presentations.php (дата
90. Ryabchikov D.I., Marov I.N., Ermakov A.N.,
обращения: 1.02.2020).
Belyaeva V.K. // J. Inorg. Nucl. Chem. 1964. Vol. 26, N 6.
P. 965-980.
111. Pandya D.N., Bhatt N., Yuan H. et al. // Chem. Sci.
91. Thomas A.W., Owens H.S. // J. Am. Chem. Soc. 1935.
2017. Vol. 8. P. 2309-2314.
Vol. 57, N 10. P. 1825-1828.
112. Pandey M.K., Bansal A., Engelbrecht H.P.
92. Larenkov A., Bubenschikov V., Makichyan A. et al. //
et al. // Nucl. Med. Biol. 2016. Vol. 43, N
1.
Molecules. 2019. Vol. 24, N 8. P. 1534. doi: 10.3390/
P. 97-100.
molecules24081534.
93. Kobayashi T., Sasaki T., Takagi I., Moriyama H. //
113. Baur
B.,
Andreolli
E.,
Al-Momani E.
J. Nucl. Sci. Technol. 2009. Vol. 46, N 2. P. 142-148.
et al. // J. Radioanal. Nucl. Chem. 2014. Vol. 299, N 3.
94. Bunney L.R., Ballou N.E., Pascual J., Foti S. // Anal.
P. 1715-1721.
Chem. 1959. Vol. 31, N 3. P. 324-326.
114. Severin G.W., Jorgensen J.T., Wiehr S. et al. // Nucl.
95. Wish L. // Anal. Chem. 1959. Vol. 31, N 3. P. 326-330.
Med. Biol. 2015. Vol. 42, N 4. P. 360-368.
96. Coleman G.H. The Radiochemistry of Plutonium,
115. Schmuckler G.
// Talanta.
1965. Vol.
1, N
3.
National Academy of Sciences, National Research
Council, 1965.
P. 281-290.
97. Nelson F., Murase T., Kraus K.A. // J. Chromatogr. 1964.
116. El-Sweify F.H., Shabana R., Abdel-Rahman N.,
Vol. 13. P. 503-535.
Aly H.F. // Radiochim. Acta. 1985. Vol. 38, N 4.
98. Das S.S., Chattopadhyay S., Barua L. // J. Radioanal.
P. 211-214.
Nucl. Chem. 2017. Vol. 313, N 3. P. 1-5.
117. El-Sweify F. // J. Radioanal. Nucl. Chem.
1997.
99. Ivanov P. I., Jerome S. M., Bozhikov G. A. et al. // Appl.
Radiat. Isot. 2014. Vol. 90. P. 261-264.
Vol. 222, N 1-2. P. 55-59.
100. Dutta B., Maiti M., Lahiri S. // J. Radioanal. Nucl.
118. Pandey M. K., Engelbrecht H. P., Byrne J. F. et al. //
Chem. 2009. Vol. 281, N 3. P. 663.
Nucl. Med. Biol. 2014. Vol. 41, N 4. P. 309-316.
101. Mathev V.J., Khopkar S.M. // Chem. Anal.
1997.
119. Abou D.S., Ku T., Smith-Jones P.M. // Nucl. Med. Biol.
Vol. 42, N 5. P. 651-658.
2011. Vol. 38, N 5. P. 675-681.
102. Lahiri S., Mukhopadhyay B., Das N.R. // Appl. Radiat.
Isot. 1997. Vol. 48, N 7. P. 883-886.
120. Ларенков А.А., Марук А.Я., Кодина Г.Е. // Радиохи-
103. Lahiri S., Mukhopadhyay B., Das N.R. // J. Radioanal.
мия. 2018. Т. 60, № 6. С. 535-542.
РАДИОХИМИЯ том 63 № 3 2021