РАДИОХИМИЯ, 2022, том 64, № 1, с. 60-64
УДК 544.58+661.876.6
ИЗУЧЕНИЕ СОРБЦИИ 90Y НАНОАЛМАЗАМИ КАК
ПОТЕНЦИАЛЬНЫМИ НОСИТЕЛЯМИ В СОСТАВЕ
РАДИОФАРМПРЕПАРАТОВ
© 2022 г. А. Г. Казаковa,*, Ю. С. Бабеняa, М. К. Ивановаa,
С. Е. Винокуровa, Б. Ф. Мясоедовa, б
a Институт геохимии и аналитической химии им. В.И. Вернадского РАН,
119991, Москва, ул. Косыгина, д. 19
б Межведомственный центр аналитических исследований в области физики, химии и биологии РАН,
117997, Москва, ул. Профсоюзная, д. 65, стр. 6
*e-mail: adeptak92@mail.ru
Поступила в редакцию 18.11.2020, после доработки 25.11.2020, принята к публикации 30.11.2020
Изучена сорбция 90Y наноалмазом (НА) и НА с окисленной поверхностью (НА-ок) для их последующего
применения в составе радиофармпрепаратов для β-терапии в ядерной медицине. Исследована кинетика
сорбции в зависимости от рН и солевого фона водных растворов. Установлено, что оптимальными
средами сорбции 90Y являются водные растворы с рН от 5 до 7, а также 0.9%-ный раствор NaCl и фосфатно-
солевой буфер; при этом показано, что присутствие солевого фона не оказывает существенного влияния
на сорбцию. При изучении стабильности конъюгатов 90Y с НА и НА-ок в модельной биологической
среде (эмбриональной телячьей сыворотке) установлено, что десорбция не превышает 27% за 24 ч для
исследованных образцов НА.
Ключевые слова: 90Y, наноалмаз, сорбция, десорбция, ядерная медицина, радиофармпрепарат.
DOI: 10.31857/S0033831122010051
В настоящее время методы ядерной медицины,
ностью изотопа: 90Y может быть легко выделен из
основанные на использовании излучения радио-
растворов материнского 90Sr (T1/2 = 28.8 года), об-
изотопов, широко применяются для диагностики
разующегося при делении урана в ходе эксплуата-
и лечения различных заболеваний, прежде всего
ции ядерных реакторов [11-15]. Для получения 90Y
онкологических. Одной из основных задач иссле-
также рассматривается его наработка в реакторе по
дований в области ядерной медицины является
реакции 89Y(n,γ)90Y [13], однако данный метод не
разработка радиофармпрепаратов (РФП), которые
получил широкого распространения.
в большинстве случаев представляют собой рас-
Среди носителей для адресной доставки радио-
твор радионуклида, связанного с органическим или
нуклидов в ядерной медицине рассматривают угле-
неорганическим лигандом, расположенным в том
родные наноматериалы, в том числе наноалмазы
числе и на поверхности сорбента, или с нанораз-
(НА) [16, 17]. К преимуществам применения НА
мерным носителем.
как носителей радионуклидов относятся высокая
90Y является одним из наиболее широко приме-
удельная поверхность, биологическая совмести-
няемых β-излучателей для терапии в ядерной ме-
мость и нетоксичность, возможность направленно
дицине [1, 2]. Ядерно-физические характеристики
изменять физико-химические свойства поверхности
90Y (Emax, β = 2280 кэВ, T1/2 = 64 ч [3]) определяют
с помощью химической обработки, а также высокая
эффективность его использования в терапии круп-
радиационная стойкость [18-20]. На сегодняшний
ных опухолей. Так, применяют несколько видов
день НА исследуются как носители для адресной
препаратов на его основе для лечения рака печени
доставки лекарств и как компоненты конъюгатов с
[4-6], для радиоиммунной терапии [7, 8] и для ле-
противораковыми, антибактериальными, противо-
чения болезней коленного и голеностопного суста-
воспалительными агентами и др. [21, 22]. В то же
вов [9, 10]. Отмеченное многообразие препаратов
время сведения в литературе по использованию НА
на основе 90Y обусловлено прежде всего доступ-
в ядерной медицине ограничены. Так, в работе [23]
60
ИЗУЧЕНИЕ СОРБЦИИ
90Y НАНОАЛМАЗАМИ
61
рассмотрено биораспределение НА, меченных 18F,
Использованные образцы НА и их физико-
с помощью позитронно-эмиссионной томографии.
химические свойства. В качестве сорбентов
Нами ранее в работах [24-28] продемонстриро-
использовали образцы НА марки УДА-ТАН (СКТБ
вана способность НА сорбировать различные ра-
«Технолог», Россия), а также образцы с окисленной
дионуклиды для диагностики и лечения, а также
поверхностью, которые получали обработкой НА
показана устойчивость полученных конъюгатов в
смесью концентрированных H2SO4 и HNO3 (3 : 1 по
модельных биологических средах. Было установ-
объему) при 120°С в течение 24 ч.
лено, что НА с окисленной поверхностью (НА-
ок), как правило, обладает большей сорбционной
Физико-химические свойства НА и НА-ок
способностью и большей прочностью связывания
были определены нами ранее в работе [24]. По-
радионуклидов по сравнению с НА. В настоящей
казано, что НА и НА-ок содержат на поверхно-
работе подробно изучены условия сорбции 90Y на
сти 330 и 990 мкмоль/г карбоксильных групп, 7.7
НА и НА-ок с целью получения устойчивых конъ-
и 9.9 ат. % кислорода и в водной среде находятся
югатов для возможного применения в составе РФП
в виде агрегатов с размером 100 и 95 нм соответ-
в β-терапии.
ственно.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Изучение сорбции и десорбции
90Y
использованными образцами НА. Сорбцию
Выделение и детектирование 90Y. Все исполь-
90Y образцами НА и НА-ок проводили из водных
зованные в работе химические реагенты имели чи-
растворов с рН от 3 до 7, которые получали
стоту не ниже х.ч.
добавлением растворов HCl или NH3, а также из
90Y выделяли из раствора 90Sr методом экстрак-
раствора 0.9% NaCl (физиологического раствора)
ционной хроматографии с использованием коммер-
и из фосфатно-солевого буфера (ФБ) с рН 7.3; рН
ческого сорбента RE (основа - трибутилфосфат и
контролировали рН-метром «Эксперт» (Эконикс-
октил(фенил)-N,N-диизобутилкарбамоилметилфос-
Эксперт, Россия). В пробирки типа Eppendorf
финоксид, размер частиц 100-150 мкм, TrisKem Int.,
Франция), по методике, описанной в работе [29].
вносили по 100 мкл суспензии НА или НА-ок с
Для этого сорбент выдерживали в 6 М HNO3 в тече-
содержанием 1 мг/мл, добавляли аликвоты раствора
ние 24 ч, затем заполняли им колонку (h = 5.5 см, d =
90Y, после чего объем доводили до 1 мл раствором
0.6 см, V = 1.6 см3). 4 мл раствора 90Sr и 90Y в 6 М
изучаемой среды для сорбции. Затем проводили
HNO3 помещали на колонку, при этом 90Y сорбиро-
перемешивание на термошейкере (TS-100, Biosan,
вался на колонке, а 90Sr оставался в растворе. 90Sr
Латвия) при скорости
1100 об/мин при
25°С
затем элюировали 8 мл раствора 6 М HNO3, после
(температуру контролировали термоприставкой
чего 90Y элюировали 6 мл раствора 0.05 М HNO3.
шейкера) в течение выбранного в экспериментах
Элюат, содержащий 90Y, выпаривали досуха, сухой
времени. Фазы разделяли центрифугированием
остаток растворяли в воде, а затем повторно выпа-
в течение 15 мин при 18000 g с использованием
ривали досуха для удаления остатков HNO3. Для
центрифуги CM-50 (Eppendorf, США), из раствора
контроля степени очистки 90Y от 90Sr фракции 90Y
отбирали аликвоты объемом 500 мкл и определяли
выдерживали в течение месяца для полного распада
содержание 90Y.
90Y, после чего по скорости счета препарата опре-
При определении прочности сорбции 90Y на НА
деляли активность стронция, которая составила не
и НА-ок использовали эмбриональную телячью
более 0.2% от общей активности. Для эксперимен-
тов по изучению сорбции и десорбции 90Y к сухому
сыворотку (ЭТС). Для этого НА или НА-ок с 90Y,
остатку, полученному после упаривания, добавляли
предварительно сорбированным из ФБ, встряхива-
бидистиллированную воду (рН 6.0), после чего ис-
ли в течение заданного времени с ЭТС при 37°С,
пользовали аликвоты полученного раствора.
затем снова центрифугировали, отбирали 500 мкл
Содержание 90Y в растворах определяли мето-
супернатанта, измеряли содержание 90Y в растворе
дом жидкостной сцинтилляционной спектрометрии
методом ЖСС. В предварительных экспериментах
(ЖСС, GreenStar, Россия) с использованием сцин-
было показано, что в условиях центрифугирования
тиллятора UltimaGold (Perkin Elmer).
белки ЭТС не осаждаются.
РАДИОХИМИЯ том 64 № 1 2022
62
КАЗАКОВ и др.
(а)
(б)
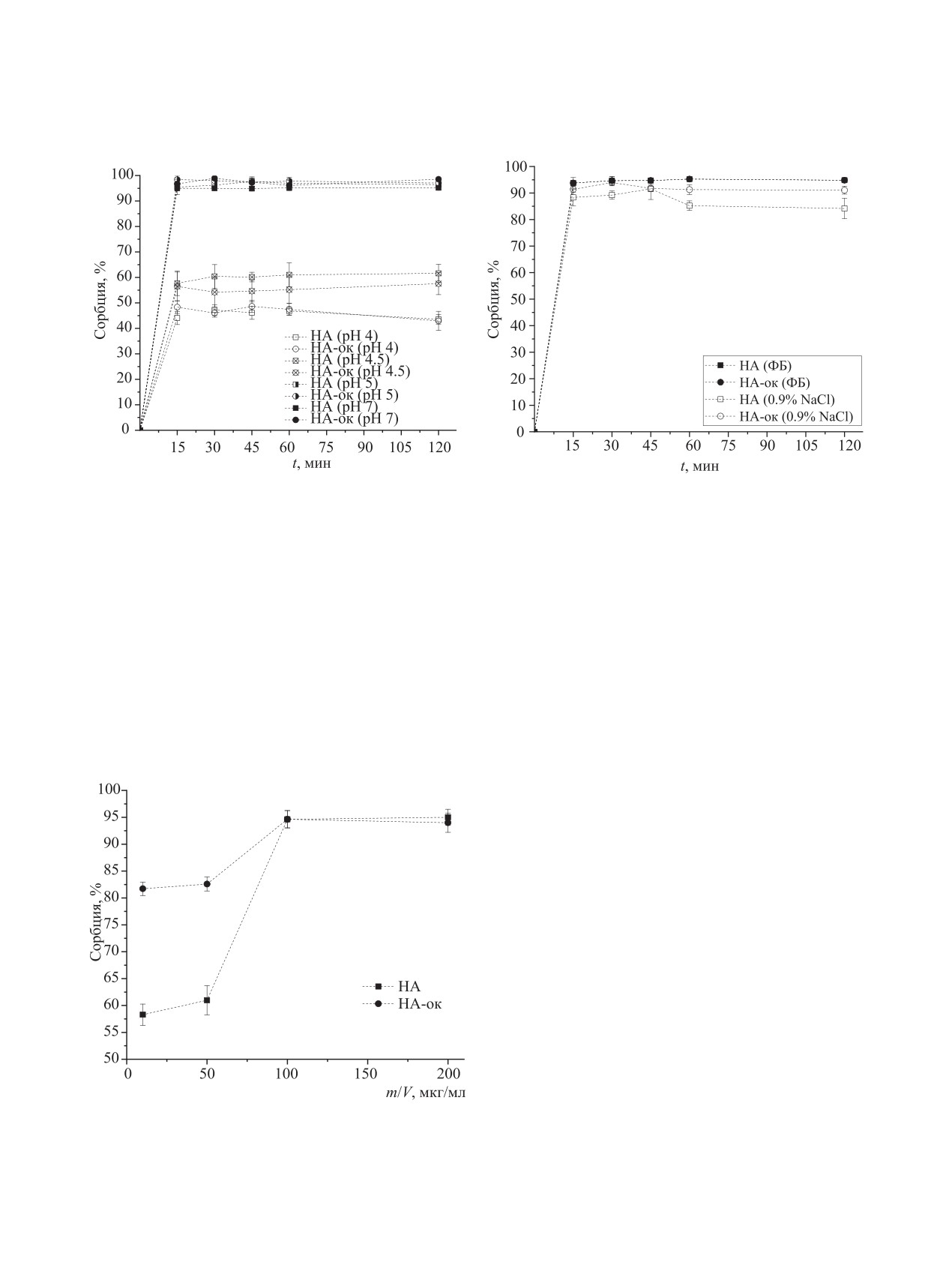
Рис. 1. Кинетика сорбции 90Y образцами НА и НА-ок из водных растворов при рН 4-7 (а), а также из 0.9%-ного раствора
NaCl и ФБ (б). Условия: 25°С, m/V 100 мкг/мл.
Все эксперименты по сорбции или десорбции
90Y не сорбируется обоими образцами НА. Данные
90Y проводили не менее двух раз до получения схо-
по сорбции при рН 4-7 приведены на рис. 1, а.
дящихся результатов.
Из этих данных видно, что при рН 4 НА и НА-
ок сорбируют около 45% 90Y, при рН 4.5 сорбция
возрастает до ~60%, а при увеличении рН до 5-7
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
сорбция становится практически количественной
(>95%). При этом для всех изученных значений
Зависимость степени сорбции 90Y от рН и
рН сорбционное равновесие устанавливается
солевого фона раствора. Изучена сорбция 90Y
уже за
15 мин. Уменьшение степени сорбции
НА и НА-ок из водных растворов при рН 3-7, из
при повышении кислотности растворов можно
0.9%-ного раствора NaCl и из ФБ. Также исследована
объяснить доминирующей ролью карбоксильных
кинетика сорбции. Установлено, что при рН 3 за 1 ч
групп на поверхности НА и НА-ок в сорбции
90Y, как было нами ранее продемонстрировано
при изучении сорбции других радионуклидов
аналогичными образцами НА
[24-28]. Важно
отметить, что сорбция 90Y в отличие от сорбции
68Ga [26] или 207Bi [24] на аналогичных образцах НА
и НА-ок не зависит от количества карбоксильных
групп на поверхности наночастиц.
При этом также установлено, что присутствие
солевого фона не оказывает существенного влияния
на сорбцию 90Y. Из данных по сорбции 90Y из 0.9%-
ного раствора NaCl и ФБ (рис. 1, б) видно, что мак-
симальное извлечение 90Y в водном растворе с рН 7
и в ФБ на обоих образцах НА составляет 90-95%,
а в 0.9%-ном NaCl незначительно снижается и для
НА составляет 84, а для НА-ок - 91%, при этом рав-
новесие устанавливается за 15 мин.
Зависимость степени сорбции 90Y от соотно-
шения массы сорбента к объему раствора (m/V).
Исследована зависимость степени сорбции 90Y об-
Рис. 2. Зависимость степени сорбции 90Y образцами НА
и НА-ок в ФБ при 25°С от соотношения m/V.
разцами НА и НА-ок от отношения m/V в растворах
РАДИОХИМИЯ том 64 № 1 2022
ИЗУЧЕНИЕ СОРБЦИИ
90Y НАНОАЛМАЗАМИ
63
достигается за 15 мин, а десорбция составляет око-
ло 10% за 1 ч. Таким образом, изученные в работе
конъюгаты НА и НА-ок с сорбированным 90Y мож-
но использовать для приготовления РФП в случае
возможности их доставки к пораженным органам за
время не более 2-3 ч, и при этом десорбция соста-
вит не более 15%.
ФОНДОВАЯ ПОДДЕРЖКА
Исследование выполнено за счет гранта Россий-
ского научного фонда (проект № 18-13-00413).
КОНФЛИКТ ИНТЕРЕСОВ
Авторы заявляют об отсутствии конфликта ин-
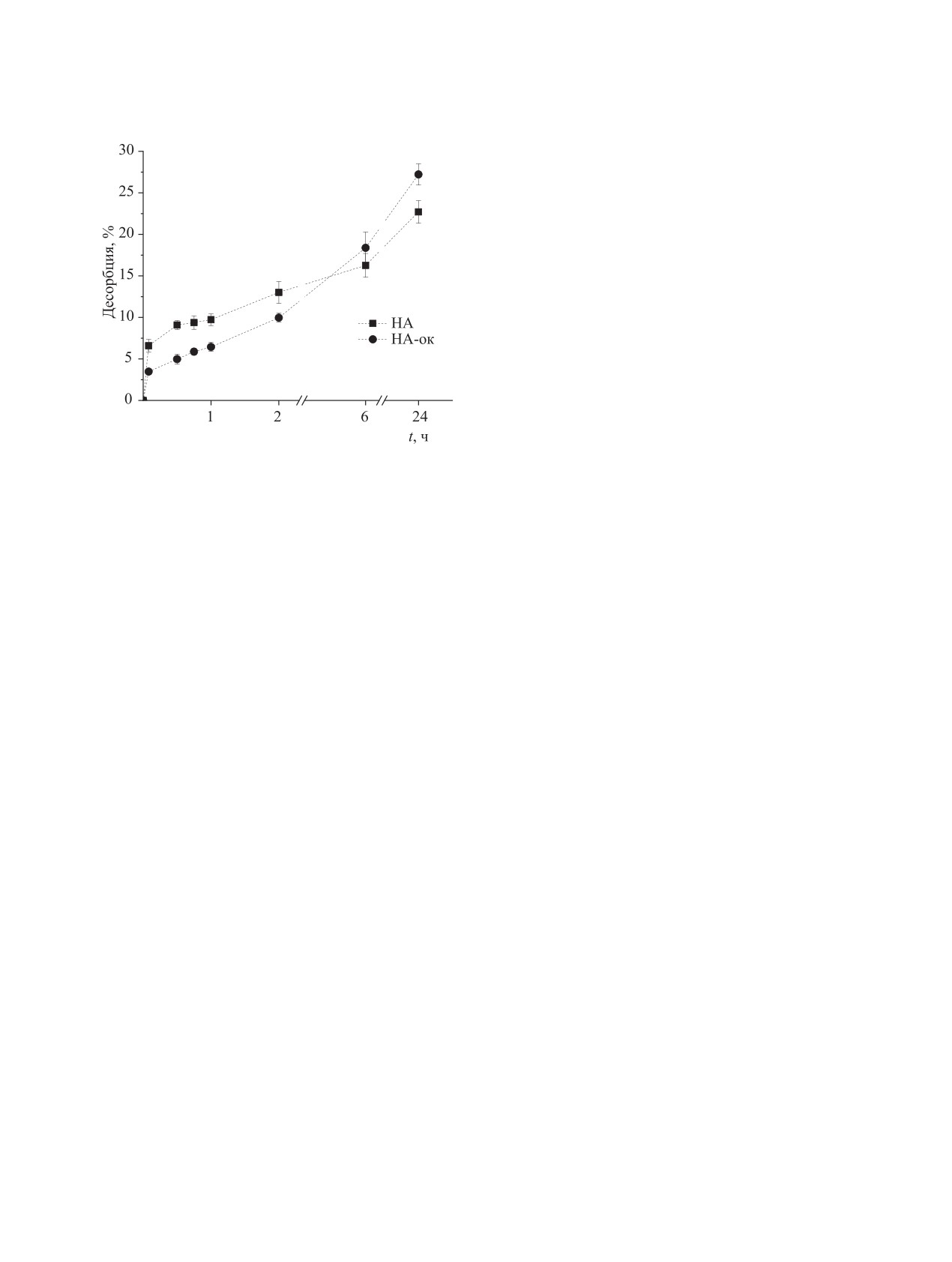
Рис. 3. Кинетика десорбции 90Y с НА и НА-ок в ЭТС при
37°С.
тересов.
ФБ; полученные данные представлены на рис. 2.
Из этих данных видно, что при m/V 10 мкг/мл сте-
СПИСОК ЛИТЕРАТУРЫ
пень сорбции 90Y на НА и НА-ок составила 58 и
82% соответственно, при увеличении отношения
1.
Asadian S.,
Mirzaei
H.,
Kalantari
B.A.,
до 50 мкг/мл она изменяется незначительно, а при
Davarpanah M.R., Mohamadi M., Shpichka A.,
Nasehi L., Es H.A., Timashev\ P., Najimi M., Gheibi N.,
увеличении содержания наночастиц до 100 мкг/мл
Hassan M., Vosough M.
// Pharmacol. Res.
2020.
сорбция 90Y на обоих образцах возрастает до 95% и
Vol. 160. Paper 105070.
не изменяется при дальнейшем увеличении указан-
ного соотношения до 200 мкг/мл. Таким образом,
2.
Datta P., Ray S. // J. Label. Compd. Radiopharm. 2020.
Vol. 63. P. 333-355.
оптимальное соотношение m/V для извлечения 90Y
составляет 100 мкг/мл, так как при этом значении
3.
Chu S.Y.F., Ekström L.P., Firestone R.B. // Table of
Radioactive Isotopes, Database Version 1999-02-28.
достигается максимальное значение степени сорб-
[Electronic resource].
ции 90Y изучаемыми образцами при минимальном
nuclear.lu.se
содержании НА и НА-ок в растворе.
4.
Carr B.I., Kondragunta V., Buch S.C., Branch R.A. //
Десорбция 90Y с изученных образцов нано-
Cancer. 2010. Vol. 116. P. 1305-1314.
алмазов. Для изучения устойчивости конъюгатов
5.
d’Abadie P., Hesse M.,Louppe A., Lhommel R., Walrand
НА и НА-ок с 90Y в модельной среде крови нами
S., Jamar F. // Molecules. 2021. Vol. 26. Paper 3966.
исследована десорбция в ЭТС при 37°С; результа-
ты приведены на рис. 3. Из этих данных видно, что
6.
Sarwar A., Kudla A., Weinstein J.L., Ali A., Malik R.,
десорбция 90Y составляет в первый час 10% для НА
Bullock A., Khwaja K.O., Curry M., Faintuch S.,
и 7% для НА-ок, а затем медленно возрастает до 27
Ahmed M. // Eur. Radiol. 2021 V. 31(3), P. 1316-1324.
и 23% за 24 ч соответственно. Таким образом, при
использовании в РФП изученных конъюгатов НА
7.
Wiseman G.A., Witzig T.E.
//
Cancer Biother.
или НА-ок с 90Y необходимо их применение для те-
Radiopharm. 2005. Vol. 20. P. 185-188.
рапии опухолей в случае быстрого (не более 2-3 ч)
8.
Borghaei H., Schilder R.J. // Semin. Nucl. Med. 2004.
распределения РФП к пораженным органам или
Vol. 34. P. 4-9.
тканям для минимизации выхода десорбированного
9.
Miszczyk M., Jochymek B., Miszczyk L., Matysiakiewicz
90Y в кровь пациента.
J., Spindel J., Jabłońska I., Mrożek T., Chrobok A.,
Таким образом, установлено, что оптимальными
Tomasik P., Zakrzewski T., Tukiendorf A. // Ann. Nucl.
растворами для сорбции 90Y являются водные рас-
Med. 2020. Vol. 34. P. 94-101.
творы с рН от 5 до 7 или раствор, содержащий 0.9%
10. Magalhães A.F., de Oliveira L.C.O., Pitella F.A.,
NaCl или ФБ, при этом количественная сорбция 90Y
Wichert-Ana L., Engel E.E., Barbieri C.H. // Hematol.
наблюдалась как на НА, так и на НА-ок. При этом
Transfus. Cell Ther. 2021, V. 43 (1), P. 15-20.
равновесное распределение 90Y на обоих образцах
РАДИОХИМИЯ том 64 № 1 2022
64
КАЗАКОВ и др.
11. Шаповалов В.В., Мельниченко Н.А., Нерозин Н.А.,
22. Tinwala H., Wairkar S. // Mater. Sci. Eng. C. 2019.
Ткачев С.В., Тогаева Н.Р., Хамьянов С.В. // Радиохи-
Vol. 97. P. 913-931.
мия. 2012. Т. 54, № 4. С. 357-359.
23. Rojas S., Gispert J.D., Martín R., Abad S., Menchón C.,
12. Muchtaridi M., Kamal E., Subarnas A., Mutalib A. //
Pareto D., Víctor V.M., Álvaro M., García H.,
Indones. J. Chem. 2017. Vol. 17. P. 15-21.
Herance J.R. // ACS Nano. 2011. Vol. 5. P. 5552-5559.
13. Qaim S.M., Scholten B., Neumaier B. // J. Radioanal.
Nucl. Chem. 2018. Vol. 318. P. 1493-1509.
24. Kazakov A.G., Garashchenko B.L., Yakovlev R.Y.,
14. Dietz M.L., Horwitz E.P. // Int. J. Radiat. Appl. Instrum.
Vinokurov S.E., Kalmykov S.N., Myasoedov B.F. // Diam.
1992. Vol. 43. P. 1093-1101.
Relat. Mater. 2020. Vol. 104. Paper 107752.
15. Chakravarty R., Pandey U., Manolkar R.B., Dash A.,
25. Казаков А.Г., Гаращенко Б.Л., Яковлев Р.Ю., Виноку-
Venkatesh M., Pillai M.R.A. // Nucl. Med. Biol. 2008.
ров С.Е., Калмыков С.Н., Мясоедов Б.Ф. // Радиохи-
Vol. 35. P. 245-253.
мия. 2020. Т. 62, № 5. С. 396-401.
16. Majkowska-Pilip A., Gawęda W., Żelechowska-
Matysiak K., Wawrowicz K., Bilewicz A. // Nanomaterials.
26. Kazakov A.G., Garashchenko B.L., Ivanova M.K.,
2020. Vol. 10. Paper 1366.
Vinokurov S.E., Myasoedov B.F. // Nanomaterials. 2020.
17. Xing Y., Dai L. // Nanomedicine. 2009. Vol. 4. P. 207-
Vol. 10. Paper 1090.
218.
27. Казаков А.Г., Гаращенко Б.Л., Яковлев Р.Ю., Виноку-
18. Schrand A.M., Hens S.A.C., Shenderova O.A. // Solid
State Mater. Sci. 2009. Vol. 34. P. 18-74.
ров С.Е., Мясоедов Б.Ф. // Радиохимия. 2020. Т. 62,
19. Lam R., Ho D. // Expert Opin. Drug Deliv. 2009. Vol. 6.
№ 6. С. 519-525.
P. 883-895.
28. Казаков А.Г., Гаращенко Б.Л., Бабеня Ю.С.,
20. Uthappa U.T., Arvind O.R., Sriram G., Losic D., Ho-
Иванова М.К., Винокуров С.Е., Мясоедов Б.Ф. //
Young-Jung, Kigga M., Kurkuri M.D. // J. Drug Deliv.
Вопр. радиац. безопасности. 2020. № 3. С. 72-82.
Sci. Technol. 2020. Vol. 60. Paper 101993.
21. Mochalin V.N., Shenderova O., Ho D., Gogotsi Y. // Nat.
29. Pichestapong P., Sriwiang W., Injarean U. // Energy
Nanotechnol. 2012. Vol. 7. P. 11-23.
Procedia. 2016. Vol. 89. P. 366-372.
РАДИОХИМИЯ том 64 № 1 2022