РАСПЛАВЫ
1 · 2019
УДК 544.971
АНОМАЛИИ ТЕРМОДИНАМИЧЕСКИХ ПАРАМЕТРОВ
ГЕТЕРОГЕННОЙ СИСТЕМЫ Li2CO3-Na2CO3-K2CO3-НАНОПОРОШОК MgO
© 2019 г. И. Д. Закирьяноваa, b, *, И. В. Корзунa
aИнститут высокотемпературной электрохимии УрО РАН,
620000 Россия, Екатеринбург, ул. Академическая, 20
bУральский федеральный университет им. первого Президента России Б.Н. Ельцина,
620002 Россия, Екатеринбург, ул. Мира, 19
*e/mail: optica96@ihte.uran.ru
Поступила в редакцию 15.07.2018
Методом дифференциальной сканирующей калориметрии (ДСК) получены све"
дения о термодинамических параметрах гетерогенной системы Li2CO3-Na2CO3-
K2CO3-нанопорошок MgO. Установлено аномальное уменьшение температуры и
приведенной энтальпии плавления солевой фазы при увеличении содержания в
композите оксида магния.
Ключевые слова: гетерогенные системы, нанопорошок MgO, карбонаты щелочных
металлов, композит.
DOI: 10.1134/S0235010619010249
ВВЕДЕНИЕ
Исследование физико"химических свойств высокотемпературных гетерогенных
систем ионная соль-нанодисперсный оксид необходимо для создания композицион"
ных материалов различных электрохимических устройств [1]. В частности, сведения о
влиянии нанопорошка MgO на температуру и энтальпию плавления смеси Li2CO3-
Na2CO3-K2CO3 будут полезны при разработке оптимальных рабочих сред карбонат"
ных топливных элементов [2].
ЭКСПЕРИМЕНТ
Подготовка образцов для исследования (солевая композиция Li2CO3-Na2CO3-
K2CO3 эвтектического состава и оксид магния), их аттестация методами РФА, ВЕТ,
ИК" и КР"спектроскопии описаны в [3]. Для исследования использовали оксид маг"
ния различной дисперсности: со средним размером кристаллитов 95 нм и удельной
площадью поверхности (S) 9.35 ± 0.07 м2/г и с размером кристаллитов 25 нм и S =
= 15.02 ± 0.13 м2/г.
Измерения температур фазовых превращений и сопутствующих тепловых эффек"
тов проводили на синхронном термоанализаторе STA 449C Jupiter фирмы NETZSCH
(Германия). Необходимые количества карбонатной эвтектики и оксида магния пере"
тирали в агатовой ступке и помещали в тигли из сплава Pt-Rh. Измерения осуществ"
ляли в атмосфере чистого аргона (99.998%) со скоростью нагрева образца 10 град/мин.
Погрешность измерения температуры фазовых переходов не превышала 1 K.
При ДСК измерениях гетерогенных систем получали воспроизводимые результаты,
при этом для анализа использовали данные второго и последующих нагревов образцов.
68
И. Д. Закирьянова, И. В. Корзун
ДСК, мВт/мг
1
3.5
↓экз
о
2
3.0
4
2.5
3
2.0
1.5
1.0
0.5
5
0
500
600
700
800
800
900
Температура, °C
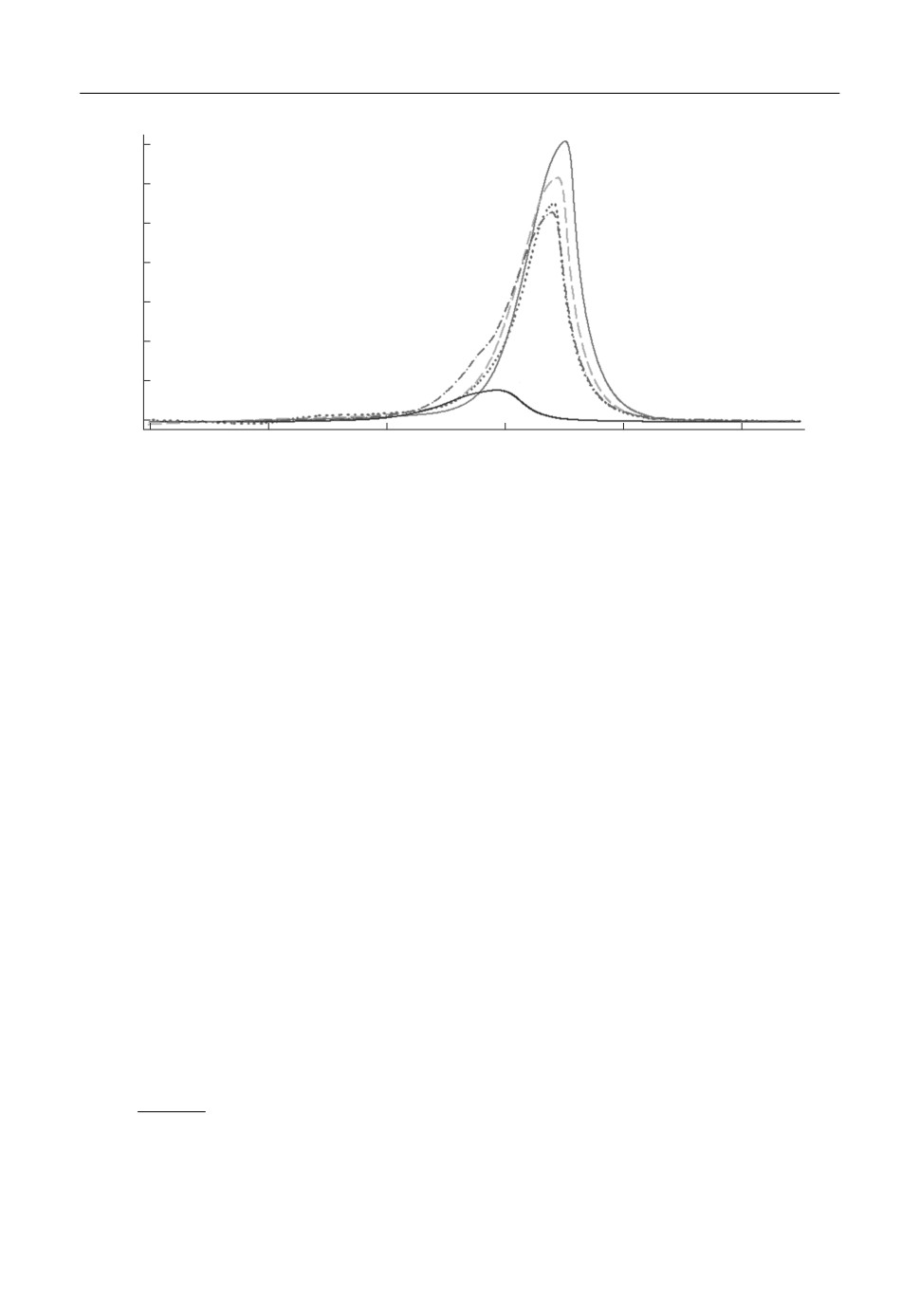
Рис. 1. Кривые ДСК гетерогенной системы (Li2CO3-Na2CO3-K2CO3)-MgO, S = 9.35 м2/г. Содержание
MgO (об. %): 0 - 1; 4.8 - 2; 11.1 - 3; 29.7 - 4; 70.1 - 5.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рис. 1 приведены экспериментальные кривые, полученные методом ДСК, гете"
рогенных систем (Li2CO3-Na2CO3-K2CO3)-MgO, содержание оксида магния (S =
= 9.35 м2/г) в которых составляет до 70 об. %. Полученные из эксперимента темпера"
тура и энтальпия плавления смеси Li2CO3-Na2CO3-K2CO3 эвтектического состава
(398°С и 277 Дж/г соответственно) согласуются с литературными данными [4]. При
увеличении содержания нанопорошка MgO отмечено уменьшение температуры и эн"
тальпии плавления ионной соли (рис. 1). Аналогичные результаты получены для гете"
рогенных систем, содержащих оксид магния с удельной площадью поверхности
15.02 м2/г. Интересно отметить, что при увеличении удельной площади поверхности
частиц нанопорошка MgO возрастают отклонения приведенной энтальпии плавления
солевой фазы от аддитивных значений (рис. 2). Это прямо указывает на влияние меж"
фазной границы соль - оксид на термодинамические параметры ионной соли.
Чтобы отследить изменения термодинамических свойств гетерогенных систем, со"
держащих частицы твердой фазы различной морфологии с различными геометриче"
скими параметрами (удельная площадь поверхности, средний размер кристаллитов),
мы использовали подход, предложенный в [5, 6] для описания физико"химических
свойств солевых расплавов, содержащих наноразмерный оксидный наполнитель. По"
лученные зависимости температуры и приведенной энтальпии плавления от эффек"
тивной толщины прослойки солевой фазы между частицами оксида магния (d) приве"
дены на рис. 3. Параметр d рассчитывали по соотношению
V
эвт
d
=
,
S⋅m
MgO
где Vэвт - объем солевой композиции, mMgO - масса оксида магния.
Из рисунка видно, что при значениях параметра d менее 100 нм в гетерогенной си"
стеме наблюдается резкое уменьшение температуры плавления солевой композиции и
приведенной энтальпии фазового перехода.
Аномалии термодинамических параметров гетерогенной системы
69
ΔH/ΔHэвт, %
ΔH/ΔHэвт, %
100
2
1
100
80
80
60
60
40
40
20
20
0
20
40
60
80
100
0
20
40
60
80
100
Содержание Li2CO3-Na2CO3-K2CO3, об. %
Рис. 2. Отклонения приведенной энтальпии плавления солевой фазы от аддитивных значений в гетероген"
ных системах (Li2CO3-Na2CO3-K2CO3)-MgO: S = 9.35 м2/г - 1; S = 15.02 м2/г - 2.
Tпл, °С
ΔH/ΔHэвт, %
400
100
395
80
2
1
390
60
385
40
380
20
375
0
0
100
200
300
400
500
600
0
100
200
300
400
500
600
d, нм
d, нм
Рис. 3. Зависимости Тпл и приведенной энтальпии плавления гетерогенных систем (Li2CO3-Na2CO3-
K2CO3)-нанопорошок MgO от параметра d (S = 9 м2/г - квадраты, S = 15 м2/г - треугольники).
При температурах ниже Тпл исследуемую гетерогенную систему можно рассматри"
вать как нанокомпозит [1], состоящий из матрицы карбонатов щелочных металлов, в
которую введен нанопорошок оксида магния. Известно, что наличие межфазных гра"
ниц вносит вклад в дефектность кристалла, что отражается на изменении термодина"
мических параметров фазовых переходов. В частности температура и энтальпия плав"
ления несут информацию о разупорядочении кристалла при температуре плавления
[1]. Значительное уменьшение этих параметров солевой системы при образовании на"
нокомпозита можно связать с увеличением концентрации дефектов в кристалличе"
ской решетке карбонатов щелочных металлов.
ВЫВОДЫ
Впервые с использованием метода ДСК получены сведения о термодинамических
параметрах гетерогенных систем Li2CO3-Na2CO3-K2CO3-нанопорошок MgO, содер"
жащих до 70 об. % оксида магния. Установлено, что при увеличении удельной площа"
70
И. Д. Закирьянова, И. В. Корзун
ди поверхности частиц нанопорошка MgO возрастают отклонения приведенной эн"
тальпии плавления солевой композиции от аддитивных значений. Обнаружено ано"
мальное уменьшение температуры и приведенной энтальпии плавления солевой фазы
при увеличении содержания в композите оксида магния.
СПИСОК ЛИТЕРАТУРЫ
1. Ув а р о в Н . Ф . Композиционные твердые электролиты. Новосибирск: изд"во СО
РАН. 2008. 258 с.
2. R e m i c k R . Molten Carbonate and Phosphoric Acid Stationary Fuel Cells: Overview and
Gap Analysis, National Renewable Energy Laboratory Technical Report NREL/TP"560"49072. 2010.
46 p.
3. Z a k i r ’ y a n o v a I . D . In situ Raman spectroscopic investigation of salvation in the disperse
system Li2CO3-Na2CO3-K2CO3"melt-MgO"nanopowder // J. of Applied Spectroscopy. 2018. 85.
P. 611-615.
4. J a n z G . J . Thermodynamic and Transport properties for molten Salts // J. Phys. Chem. Ref.
Data. 1988. 17. P. 3-325.
5. M i z u h a t a M . , H a r a d a Y. , C h a G . , B é l é k é A . , D e k i S . Physicochemical
properties of molten alkali metal carbonates coexisting with inorganic powder // J. Electrochem. Soc.
2004. 151. P. 179-185.
6. B é l é k é A . B . , M i z u h a t a M . , D e k i S . Anomalous properties of molten alkali ni"
trates coexisting with aluminum oxides by hetero"phase effect // Vibr. Spectrosc. 2006. 40. P. 66-79.
Thermodynamic Parameters Anomalies
of the Heterogeneous System Li2CO3-Na2CO3-K2CO3-Nanopowder MgO
I. D. Zakiryanova1, 2, I. V. Korzun1
1Institute of High Temperature Electrochemistry, Ural Branch of Russian Academy of Sciences,
620990 Russia, Yekaterinburg, Akademicheskaya st., 20
2Ural Federal University named after the first President of Russia B.N. Yeltsin,
620002 Russia, Yekaterinburg, Mira st., 19
The method of the differential scanning calorimetry (DSC) has received data on thermo"
dynamic parameters of the heterogeneous system Li2CO3-Na2CO3-K2CO3-nanopowder
MgO. Abnormal reduction of temperature and the relative enthalpy of melting of a salt
phase at increase in contents in a magnesium oxide composite is established.
Keywords: heterogeneous systems, nanopowder MgO, carbonates of alkaline metals,
composite
REFERENCES
1. Uvarov N.F. Composite solid electrolytes [Compozicionny tverdy electrolity]. Novosibirsk: Sib.
Br. RAS. 2008. 258 p. [in Rus.].
2. Remick R. Molten Carbonate and Phosphoric Acid Stationary Fuel Cells: Overview and Gap
Analysis, National Renewable Energy Laboratory Technical Report NREL/TP"560"49072. 2010,
46 p.
3. Zakir’yanova I.D. In situ Raman spectroscopic investigation of salvation in the disperse system
Li2CO3-Na2CO3-K2CO3"melt-MgO"nanopowder // J. of Applied Spectroscopy. 2018. 85. P. 611-
615.
4. Janz G.J. Thermodynamic and Transport properties for molten Salts // J. Phys. Chem. Ref. Da"
ta. 1988. 17. P. 3-325.
5. Mizuhata M., Harada Y., Cha G., Béléké A., Deki S. Physicochemical properties of molten al"
kali metal carbonates coexisting with inorganic powder // J. Electrochem. Soc. 2004. 151. P. 179-185.
6. Béléké A.B., Mizuhata M., Deki S. Anomalous properties of molten alkali nitrates coexisting
with aluminum oxides by hetero"phase effect // Vibr. Spectrosc. 2006. 40. P. 66-79.