РАСПЛАВЫ
2 · 2019
УДК 544.654.2
ЭНЕРГИЯ СВЯЗЕЙ В РАСПЛАВЛЕННЫХ СИСТЕМАХ
M-Al-Zr-O-F (M = Li, Na, K)
© 2019 г. А. С. Воробьевa, А. В. Суздальцевa, *, А. Е. Галашевa
aИнститут высокотемпературной электрохимии УрО РАН,
ул. Академическая, 20, Екатеринбург, 620990 Россия
*e+mail: suzdaltsev_av@mail.ru
Поступила в редакцию 20.07.2018
После доработки 29.07.2018
Принята к публикации 05.08.2018
Методом первопринципной молекулярной динамики, реализованном с помо"
щью программы Siesta, рассчитана энергия связи в комплексных анионах, образо"
ванных из компонентов: Al-F, Zr-F, Al-O-F и Zr-O-F, формирование которых
связано с растворением оксидов ZrO2 и Al2O3 во фторидных расплавах MF-AlF3 (где
M = Li, Na, K). Определено влияние элементного состава анионов и катиона из вто"
рой координационной сферы на энергию связи комплексных анионов. Показано,
что среди кислород"содержащих анионов наибольшей стабильностью обладают
2-
2−
анионы
Al
2
O
2
F
6
и
Zr
2
O
2
F
6
При идентичных условиях, самой низкой энергией,
определяющей связи, обладают анионы, образуемые цирконием. Замена катиона во
второй координационной сфере в ряду от K к Li приводят к снижению энергии свя"
зей в анионах M2Al2O2F6 и M2Zr2O2F6.
Ключевые слова: оксидно"фторидный расплав, анионы, цирконий, алюминий, моле"
кулярно"динамическое моделирование, энергия связи, стабильность.
DOI: 10.1134/S0235010619020063
1. ВВЕДЕНИЕ
Мелкозернистая структура получаемого литьем алюминия желательна, т.к. она при"
водит к улучшению его механических свойств и эксплуатационных характеристик
благодаря лучшей гомогенности и пониженной пористости. Измельчение зерна в
алюминии и его сплавах обычно осуществляется с помощью добавления металлов"из"
мельчителей зерен. В качестве зерновых измельчителей для алюминия и алюминие"
вых сплавов используются переходные металлы, такие как Ti, Sс, Zr, V, Cr и др. [1-3].
В частности уже очень незначительные добавки циркония в алюминий (не более
0.28 мас. %) дают очень мелкое, близкое по размерам зерно. Цирконий может быть
введен в расплавленный алюминий перед литьем путем добавления солей циркония
(K2ZrF6, NaZrF4) в покровный солевой флюс [4, 5]. Однако использование такого хи"
миката приводит к непредсказуемым и пагубным последствиям, таким как выделение
в атмосферу газообразных фторидных составляющих (AlF3, ZrF4).
Более перспективными представляются способы получения сплавов и лигатур Al-
Zr с использованием оксида ZrO2. В частности известны исследования процесса алю"
минотермического восстановления ZrO2 в системах: CaO-CaF2 при 1600°С [6, 7];
KClO3-S или NaNO3-S при 1725°С [8]; KF-AlF3 при 750-800°С [9, 10]. Благодаря вы"
сокому выходу циркония (до 99.5%), низкой температуре и возможности организации не"
прерывного получения сплавов и лигатур Al-Zr с содержанием циркония до 15 мас. %
наиболее энергоэффективным представляется восстановление оксида ZrO2 алюмини"
Энергия связей в расплавленных системах M-Al-Zr-O-F
157
ем в условиях электролиза в оксидно"фторидных расплавах на основе систем KF-AlF3
и NaF-AlF3 с добавками оксидов Al2O3 и ZrO2 [11-14]. Однако кинетика восстановле"
ния и параметры синтеза во многом зависят от состава комплексных соединений цир"
кония, образующихся при растворении ZrO2 в оксидно"фторидном расплаве.
Поиски альтернативных способов электролитического получения алюминия приве"
ли к необходимости исследования стабильности оксихлорида алюминия и оксида алю"
миния [15], а также анализу роли аниона фтора в условной растворимости оксида алю"
миния в хлоридных расплавах [16]. Также появилась идея возможного электровыделе"
ния алюминия из хлоридно"фторидно"оксидных расплавах [17]. Все эти исследования
страдают от недостатка информации о структурах появляющихся ионных комплексов.
Методы моделирования выглядят очень перспективным инструментом для получе"
ния структурных и энергетических свойств, а также информации о вибрациях в ком"
плексных анионах. Использование программного обеспечения для выполнения вычис"
лений по теории функционала плотности (DFT) позволяет прямо учитывать обменные
и корреляционные эффекты, при этом на два порядка снижая объем вычислений по
сравнению с методом Хартри-Фока. Причем, пользуясь методом DFT можно выпол"
нять все геометрические оптимизации без какой"либо фиксированной симметрии.
Проведение оптимизации геометрии анионов показало, что атом алюминия всегда
пятикратно скоординирован, т.е. находится в окружении четырех атомов фтора и од"
ного атома кислорода [17].
Чтобы сравнить все энергии всех комплексов, мы предпочтительно рассчитать при"
сущие им энергии связи. На основании таких расчетов можно сравнивать относитель"
ную стабильность комплексов непосредственно. В работах [17, 18] всесторонне рас"
смотрены комплексные соединения алюминия, благодаря чему, имеется возможность
верифицировать полученные в настоящей работе данные.
Цель настоящей работы - выявление наиболее стабильных комплексных соедине"
ний в расплавленных системах M-Al-Zr-O-F (M = Li, Na, K) путем расчета энергии
связи и сравнение полученных данных с энергиями связи комплексных соединений
алюминия.
В последнее время при помощи модельных расчетов решается значительное число
научно"технических вопросов о влиянии того или иного фактора на процессы при элек"
тролитическом получении алюминия [19-21]. Следовательно, помимо расширения
представлений о комплексообразовании в расплавах KF-AlF3, NaF-AlF3 и LiF-AlF3 с
добавками оксидов Al2O3 и ZrO2 полученные в работе данные могут быть использованы
при моделирования процессов, протекающих в расплаве и на электродах в традицион"
ном криолит"глиноземном расплаве с добавками (примесями) LiF, KF, ZrO2.
2. МЕТОДИКА РАСЧЕТОВ
Наиболее эффективным подходом к расчету энергии связи, а также динамики ре"
шетки кристаллов является метод функционала плотности, предложенный в работах
Кона, Хоэнберга и Шэма [22, 23]. Суть данного метода определяется следующей тео"
ремой: энергия основного состояния системы взаимодействующих электронов в поле
атомных ядер является однозначным функционалом распределения электронной
плотности ρ(r) (функционал Кона-Шэма). При варьировании ρ(r) этот функционал
достигает своего экстремума (минимума), равного энергии основного состояния си"
стемы, на правильном распределении электронной плотности. Это положение можно
записать в виде следующего условия:
δE[ρ]
=
0.
(1)
δρ
158
А. С. Воробьев, А. В. Суздальцев, А. Е. Галашев
Для вычисления полной энергии системы необходимо определить набор волновых
функций
i r
, которые минимизируют функционал Кона-Шэма. Они определяются
из условия (1). Обменно"корреляционный потенциал
V rXC
можно определить через
функциональную производную:
δE
XC
[ρ]
∂[ρ(r)ε
XC
(r)]
V
XC
r
=
=
,
(2)
δρ(r
)
∂ρ(r)
где
ε
XC
r
=ε om ρ [
XC
(r)];
εhomXC
- обменно"корреляционная энергия однородного элек"
тронного газа с плотностью ρ, приходящаяся на один электрон.
В итоге мы имеем приближение локальной плотности, в котором плотность обмен"
но"корреляционной энергии в точке r равна плотности обменно"корреляционной
энергии в однородном электронном газе с той же плотностью ρ(r).
Более точным приближением для обменно"корреляционной энергии является
обобщенное градиентное приближение (GGA). В этом случае обменно"корреляцион"
ный функционал зависит не только от плотности, но и от ее первой пространственной
производной:
3
E
XC
ρ]= ∫ρ()ε [ρ
[ r r
XC
∇ρ(r)]d
r
(3)
Для расчета электронных свойств твердых тел часто используется конкретная фор"
ма приближения GGA, предложенная Perdew и др. в работе [24]. Мы использовали
стандартную процедуру разложения орбиталей по базису, в качестве которого были
выбраны плоские волны. В этом случае волновые функции могут быть записаны в ви"
де разложения:
Ψ
i
(r)
=
∑Ci,
k
+G
exp[i(k
+
G
)⋅
r].
(4)
G
В результате уравнения Кона-Шэма принимают вид системы линейных алгебраиче"
ских уравнений, определяющих коэффициенты
i,k
+G
C
:
2
⎡
ℏ
2
⎤
k
+
G
δ
+V
(G
-
G')
+V
(G
-
G')
+V
(G
-
G')
C
=ε
C
,
(5)
∑
⎢
GG'
ion
H
XC
⎥
i,k+G'
i
i,k+G
⎣
2m
⎦
G
'
гдеVion
- статический электрон"ионный потенциал,
V
- потенциал Хартри для элек"
H
тронов,
- собственное значение уравнения Кона-Шэма [23]. Данная система урав"
εi
нений представляет собой стандартную задачу линейной алгебры на нахождение соб"
ственных значений.
Расчеты были выполнены с использованием программного пакета Siesta. Геометри"
ческая оптимизация была проведена с использованием GGA в форме Perdew"Burke"
Ernzerhof, методом диагонализации без закрепления координат. Для всех расчетов был
использован трехэкспоненциальный базис и поляризационные функции. В обратном
пространственном разложении плотности заряда использовалось обрезание по сетке
равное 300 Ry. Критерий сходимости по энергии цикла самосогласованного поля
(SCF) был выбран равным 10-3 эВ. Энергии связи были рассчитаны по формуле:
E
bind
=
E
OMF
-
N
EM M
-
N
F F
E
-
N EO,
(6)
где
EOMF
,
EM,
EF
и
EO
- полная энергия комплекса, единичного атома металла (Al3+,
Zr4+), фтора (F-) и кислорода (O2-), соответственно;
NM,
NF,
NO
- количество атомов
металла, фтора и кислорода в системе соответственно.
Энергия связей в расплавленных системах M-Al-Zr-O-F
159
Таблица 1
Энергии связи для различных Al8 и Zr8содержащих комплексов в эВ,
где x - количество атомов фтора в комплексе
x
Комплекс
1
2
3
4
5
6
7
8
9
−
–
-
-65.0
-69.5
-69.6
-63.0
-
-
-
AlFzx
-
–
-
-
-92.0
-98.6
-97.5
-
-
-
ZrFzx
−
–73.9
-80.0
-79.7
-72.4
-
-
-
-
-
AlOFzx
−
–89.8
-103.1
-109.1
-107.7
-
-
-
-
-
ZrOFzx
−
–
-
-
-142.7
-149.1
-151.0
-146.7
-138.4
Al
2
OFzx
-
–
-
-
-173.3
-189.9
-202.2
-207.6
-209.3
-206.3
Zr
2
OFzx
−
–
-153.4
-158.4
-158.6
-156.2
-150.8
-
-
-
Al
2
O
2
Fzx
-
–
-183.8
-199.5
-209.5
-219.2
-220.1
-216.5
-
-
Zr
2
O
2
Fzx
−
–
-
-
-160.1
-172.5
-179.1
-180.4
-176.3
-171.1
AlZrOFzx
−
–
-170.9
-181.5
-186.4
-190.7
-186.2
-177.3
-
-
AlZrO
2
Fzx
Все полученные энергии связи для комплексов, образуемых катионами Al и Zr,
представлены в табл. 1. Там же приведены значения энергии связей для гипотетиче"
ских комплексов, образуемых одновременно Zr и Al.
3. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
−
−
3.1. Энергия связи в комплексах
AlF
и
Zr
y
Энергия связи эквивалентна энергии,
необходимой для разборки всей системы на отдельные части. Связанная в комплекс
система обычно имеет более низкую потенциальную энергию, чем сумма ее составля"
ющих частей. Другими словами, с помощью этой энергии части системы удерживают"
ся вместе. Часто это означает, что энергия выделяется при создании связанного состо"
яния. Соединение устойчиво, если суммарная потенциальная энергия его частей от"
рицательна. Именно такого определения энергии связи (см. выражение (6)) мы будем
придерживаться в этой работе.
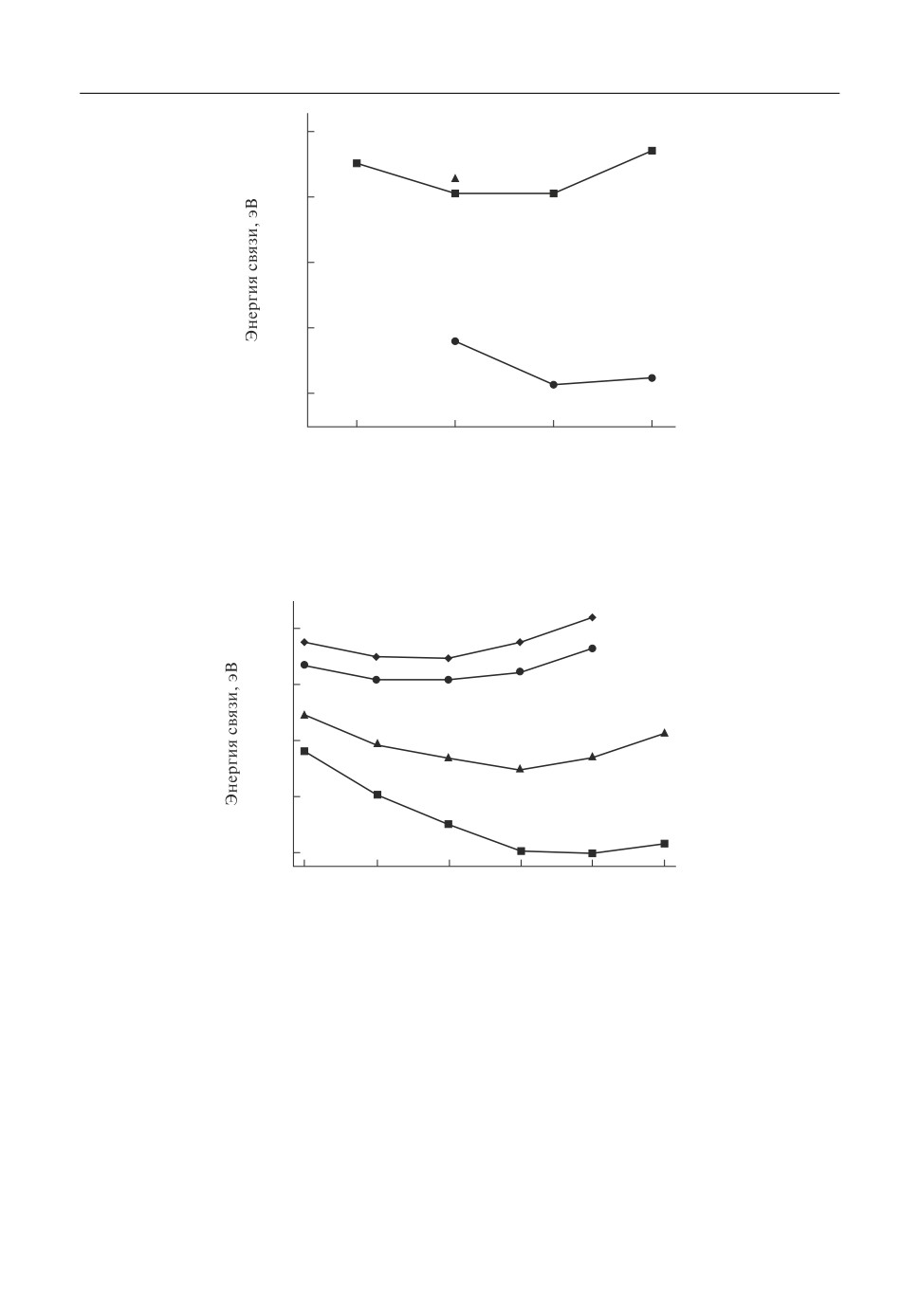
На рис. 1 представлены полученные зависимости энергий связи для комплексов
z
-
z
AlF
и
ZrF
−.
Также приведено значение для энергии связи комплекса
AlF
−,
полу"
x
x
4
ченное в работе [17]. Незначительное отклонение в значениях Ebind, вызвано использо"
ванием в настоящей работе иного программного комплекса и отличного от применяе"
мого в работе [17] обменно"корреляционного потенциала.
На основе зависимостей показанных на рис. 1 можно сделать следующие выводы.
Во"первых, наиболее стабильными из всех приведенных комплексов алюминия явля"
−
2−
ются
AlF
(-69.51 эВ) и
AlF
(-69.56 эВ), что согласуется с данными полученными
4
5
Робертом и др. [18]. Результат, полученный в работе [18] свидетельствует в пользу того,
что расплавленные смеси MF-AlF3 (где M = Li, Na, K) состоят в основном из ком"
160
А. С. Воробьев, А. В. Суздальцев, А. Е. Галашев
60
70
-j- Al
80
-d- Zr
-m- Picard G.S.
90
100
-z
-z
-z
-z
XF3
XF4
XF5
XF6
Рис. 1. Рассчитанные энергий связи комплексных анионов AlFx ( ) и ZrFx ( ). Данные для AlFx сопоставле"
ны с результатами работы [17] ( ).
140
160
180
200
220
-z
-z
-z
-z
-z
-z
X2O2F2
X2O2F3
X2O2F4
X2O2F5
X2O2F5
X2O2F7
–j- Zr
-d- Al
-m- ZrAl
-r- Picard G.S.
2−
Рис. 2. Энергия связи комплексов
где X2 - Zr2 ( ), Al2( ) или ZrAl ( ).
2
2
X
O
F
,
y
2
плексов
AlF
-,
AlF
−.
Во"вторых, комплексы циркония обладают более прочной свя"
4
5
зью (более отрицательной энергией связи) по сравнению с аналогичными алюминие"
выми комплексами. В"третьих, самой прочной связью (и самой низкой энергией, ха"
−
рактеризующей связи) обладает комплекс
ZrF
(-98.57 эВ).
5
3.2. Энергия связи комплексов
X
O
Fz-y
На рис. 2 представлены величины энергии
2
2
z
связи комплексов
X
O
F
−,
где X2 - комплексообразователь (Zr2, Al2, ZrAl), y - коли"
2
2
y
z
-
чество атомов фтора. Полученные энергии связи алюминиевых комплексов
Al
O
F
2
2
y
Энергия связей в расплавленных системах M-Al-Zr-O-F
161
F
-2
OZrF3-1
OZr2F8
Zr
O
0.2
0.1
0
0
-0.1
-0.2
0.2
-0.2
-0.1
0.1
0
0
0
0
-0.1
0.3
0.1
0.2
O2Zr2F6-2
Li2Zr2O2F6
F
Zr
O
0.2
0.2
Li
0
0
-0.2
-0.2
0.2
-0.3
0.1
0
0
0
0
0.3
0.3
–0.1
-0.2
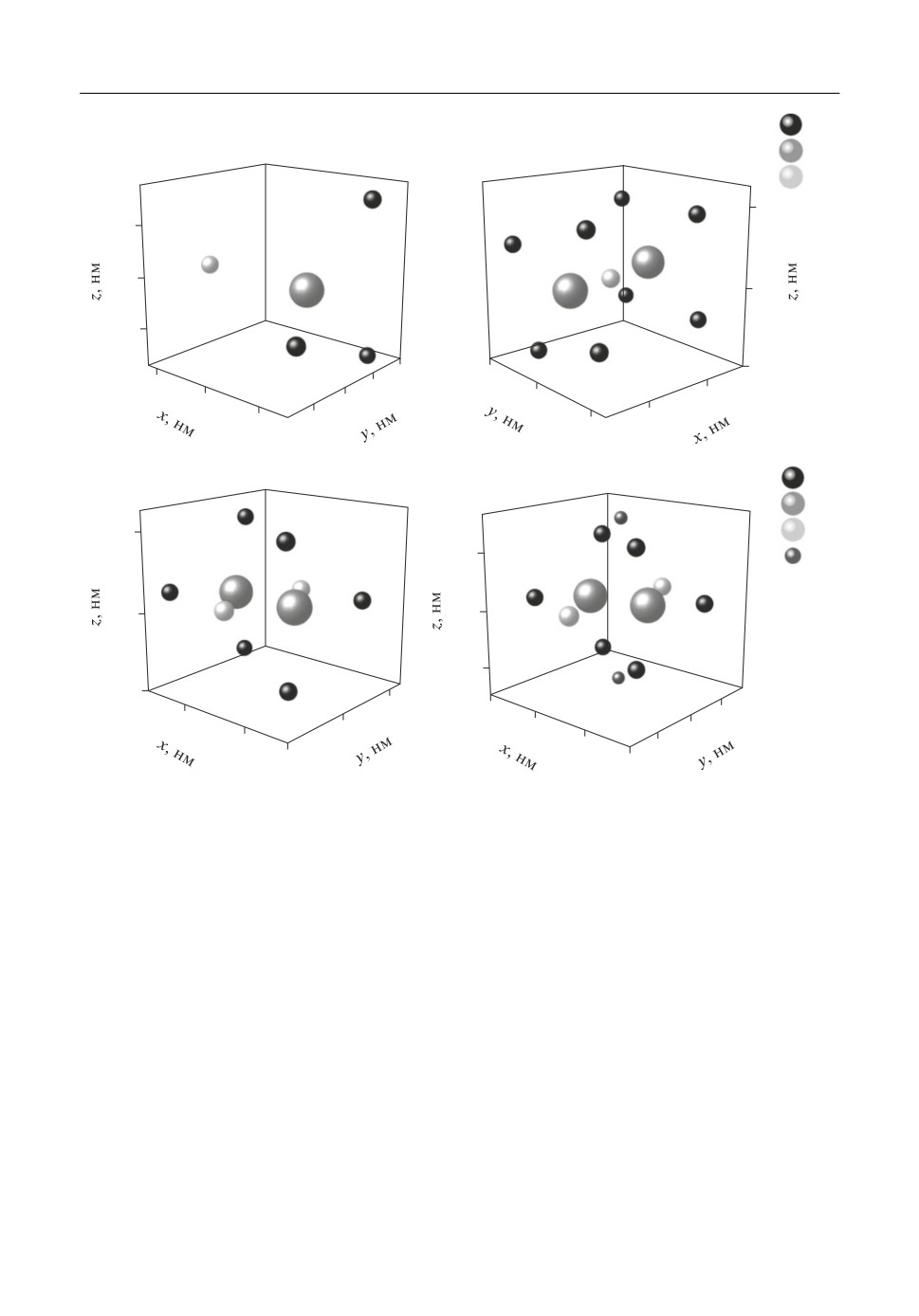
Рис. 3. 3D структура некоторых комплексных анионов.
имеют более низкие значения (на 5-7%), чем значения энергии связи соответствую"
щих комплексов, определенные в работе [17]. Однако местоположение минимума
энергии связи и общий вид зависимости для данного комплексного соединения сов"
падают c аналогичными характеристиками, приведенными в работе [17].
Из полученных на рис. 2 зависимостей можно сделать следующие выводы. Во"пер"
2
вых, самой прочной связью (-220.14 эВ) обладает комплексный анион
Во"
-.
2
2
6
Zr
O
F
z
вторых, сравнение энергии связи комплексных соединений
где X2 = Al2, Zr2,
−,
2
2
y
X
O
F
ZrAl при равных y показывает, что связи становятся слабее (абсолютное значение
энергии связи увеличивается) при переходе от соединений циркония к смешанным
алюминиево"циркониевые соединениям, и, далее, к алюминиевым комплексным со"
единениям. Как видно из табл. 1, это соотношение справедливо для всех рассмотрен"
ных случаев. В"третьих, для всех рассмотренных групп комплексов обнаружены ми"
нимумы энергии связи в области значений y = 4...6.
3.3. Структура наиболее стабильных комплексов. На рис. 3 приведены 3D структуры
2
2−
четырех комплексных соединений циркония:
ZrOF
3
−,
Zr
2
OF
8
−,
Zr
2
O
2
F
6
и Li2Zr2O2F6.
Данные соединения являются наиболее стабильными соединения своей группы и
162
А. С. Воробьев, А. В. Суздальцев, А. Е. Галашев
140
160
180
200
220
240
-Z
X2O2F6-Z Li2X2O2F6-Z Na2X2O2F6-Z
K2X2O2F6
Zr
Al
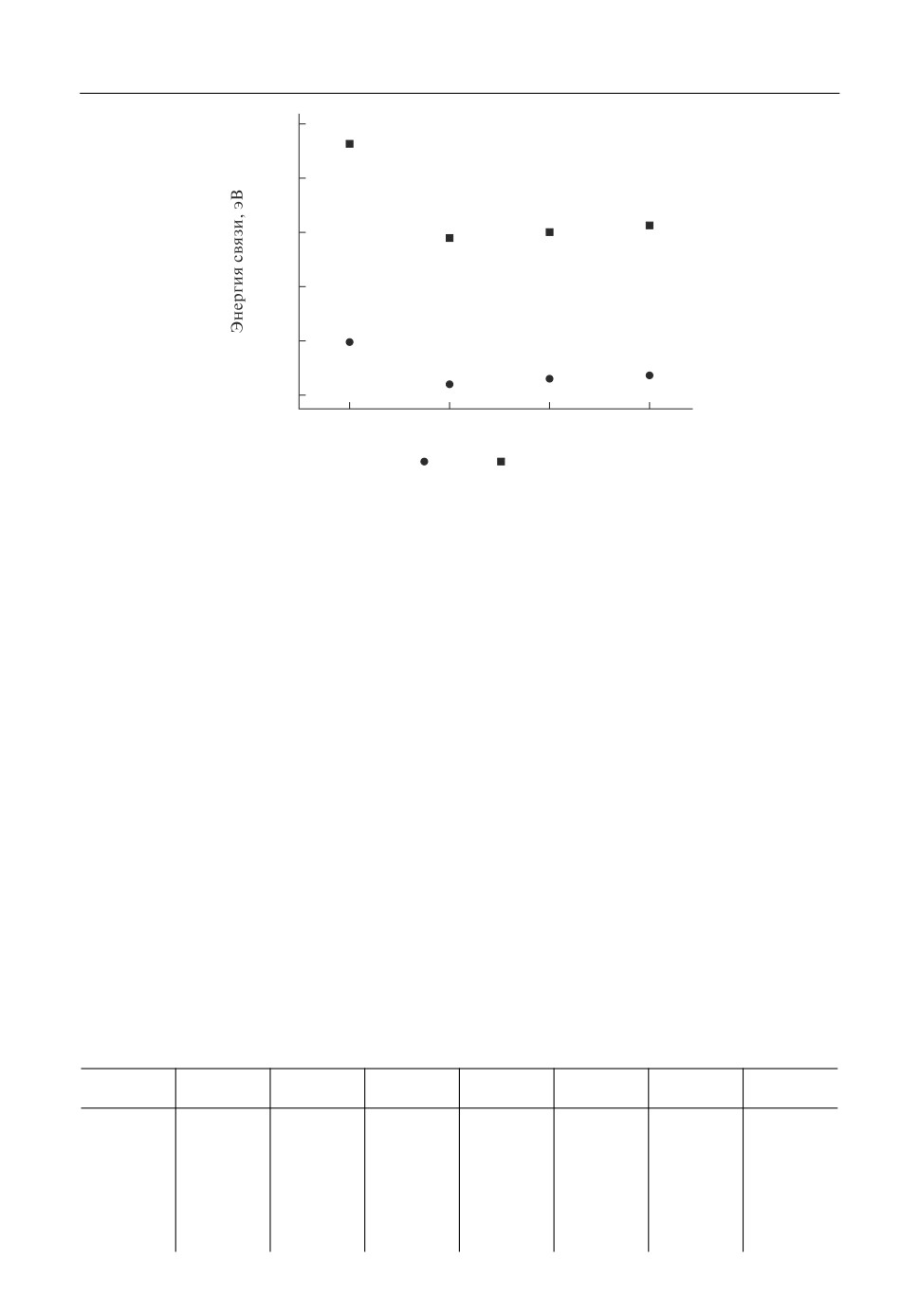
Рис. 4. Энергия связи комплексов M2Al2O2F6 и M2Zr2O2F6, где M = K, Na, Li, а X - Zr ( ) или Al ( ), рас"
считанная с учетом геометрических соседей из второй координационной сферы.
имеют самую низкую энергию связи, что видно из табл. 1. Рассчитанные длины связи
для этих соединений, представленные в табл. 2. На основании полученных данных
можно сделать следующие выводы: 1) каждое из рассматриваемых соединений обла"
дает ярко выраженной симметрией; 2) центром всех соединений являются ионы Zr4+;
3) длины связей Zr-F и Zr-O во всех рассмотренных соединениях имеют достаточно
близкое значение.
3.4. Влияние второй координационной сферы. Рисунок 4 отражает влияние второй
координационной сферы (химического потенциала катиона в системе) на энергию
связи в системах M2Al2O2F6 и M2Zr2O2F6, где M = K, Na, Li. Как видно из этого рисун"
ка внедрение атомов M приводит к уменьшению энергии связи. Данный факт объяс"
няется изменением геометрической структуры данных комплексных соединений (см.
рис. 2), которое можно видеть на примере соединения Li2Zr2O2F6. Гипотетическое объ"
2-
единение щелочного металла и соединения
Zr
2
O
2
F
6
заметно снижает энергию связи
комплекса. Наиболее сильное снижение энергии связи происходит при внедрении в
комплекс атомов Li.
Таблица 2
−1
−2
2
Длина связи для комплексов
ZrOF
3
,
Zr
2
OF
8
,
Zr
2
O
2 6
F-
и Zr2Li2O2F6 в ангстремах
Zr-Zr
Zr-F
Zr-O
F-F
F-O
O-O
F-Li
−
-
2.07
1.88
2.88
3.09
-
-
ZrOF
3
2−
–
2.02
1.99
2.73
3.13
-
-
Zr
2
OF
8
2−
3.10
2.03
1.97
2.87
2.94
2.65
-
Zr
2
O
2
F
6
Li2Zr2O2F6
3.07
1.98
1.92
2.93
2.84
2.676
1.80
Энергия связей в расплавленных системах M-Al-Zr-O-F
163
На основе данных, отображаемых на рис. 4, можно сделать следующие выводы. Во"
первых, сохраняется соотношение между энергиями связи для циркония и алюминия:
циркониевые комплексы также обладают более низкой энергией связи, чем аналогич"
ные алюминиевые соединения. Во"вторых, каждый добавочный катион вносит свое
изменение в энергию связи: самая низкая энергия связи оказывается у Li, а наиболее
высокая - у K. В"третьих, наибольшей стабильностью обладают литий"содержащие
комплексы, имеющие энергию связи -182.153 эВ для алюминиевого соединения
(Li2Al2O2F6) и -235.705 эВ для циркониевого соединения (Li2Zr2O2F6).
4. ВЫВОДЫ
Настоящее исследование позволяет расширить представления о процессах ком"
плексообразования в расплавах на основе систем KF-NaF-AlF3-ZrO2, используемых
для получения сплавов и лигатур Al-Zr. Полученные результаты могут быть кратко
обобщены в следующем виде:
- наименьшей энергией связи, без учета влияние второй координационной сферы,
из всех рассмотренных комплексных соединений циркония обладает соединение
2
-;
2
2
6
Zr
O
F
- комплексные соединения циркония обладают наибольшей стабильностью в срав"
нении с аналогичными комплексными соединениями алюминия-циркония и алюми"
ния;
- в соединении с двумя комплексообразователями Al и Zr энергия связи меньше
аналогичных алюминиевых комплексов;
z
- добавление катионов Li+, Na+ или K+ в соединение
X
O
F
−,
где X2 = Al2, Zr2, при"
2
2
6
водит к увеличению стабильности системы, как для циркониевых, так и для алюмини"
евых комплексов, наиболее низкую энергию связи имеют комплексы, включающие
Li, а наиболее высокой энергией связи обладают комплексы, содержащие K;
- во всех группах систем имеются комплексы, обладающие самой низкой энергией
связи, отражаемой минимумом на соответствующей энергетической зависимости;
- наибольшую прочность связи среди представленных в данной работе комплексов
показывает соединение Li2Zr2O2F6 (-235.705 эВ).
Работа выполнена при финансовой поддержке Министерства образования РФ (согла"
шение № 14.607.21.0146), уникальный идентификатор проекта RFMEFI60716X0146.
СПИСОК ЛИТЕРАТУРЫ
1. О г о р о д о в Д . В . , П о п о в Д . А . , Тр а п е з н и к о в А . В . Способы получения ли"
гатуры Al-Zr (обзор) // Труды ВИАМ. 2015. № 11. С. 2-11.
2. K n i p l i n g K . E . , S e i d m a n D . N . , D u n a n d D . C . Ambient" and high"temperature
mechanical properties of isochronally aged Al-0.06Sc, Al-0.06Zr and Al-0.06Sc-0.06Zr (at %) al"
loys // Acta Materialia. 2011. 59. P. 943-954.
3. Га с и к М . И . , Л я к и ш е в Н . П . , Е м л и н Б . И . Теория и технология производ"
ства ферросплавов. М.: Металлургия. 1988. 784 с.
4. Я ц е н к о С . П . , О в с я н н и к о в Б . В . , А р д а ш е в М . А . , С а б и р з я н о в А . Н .
Цементационное получение "мастер"сплава" из фторидно"хлоридных расплавов // Расплавы.
2006. № 5. С. 29-36.
5. Н а п а л к о в В . И . , М а х о в С . В . Легирование и модифицирование магния и алю"
миния // М.: МИСИС. 2002. 376 с.
6. К р а с и к о в С . А . , А г а ф о н о в С . Н . , Ч е н ц о в В . П . , Ж и л и н а Е . М . Влия"
ние фазообразования на характер межфазных взаимодействий при алюмотермическом вос"
становлении циркония из его диоксида // Расплавы. 2015. № 2. С. 60-64.
7. А г а ф о н о в С . Н . , К р а с и к о в С . А . , П о н о м а р е н к о А . А . , О в ч и н н и к о "
ва Л.А. Фазообразование при алюмотермическом восстановлении ZrO2 // Неорганические
материалы. 2012. 48. С. 927-934.
164
А. С. Воробьев, А. В. Суздальцев, А. Е. Галашев
8. J u n e j a J . M . Preparation of aluminium"zirconium master alloys // Indian J. Engineering &
Materials Sciences. 2002. 9. P. 187-190.
9. П е р ш и н П . С . , Ф и л а т о в А . А . , С у з д а л ь ц е в А . В . , З а й к о в Ю . П . Алю"
мотермическое получение сплавов Al-Zr в расплаве KF-AlF3 // Расплавы. 2016. № 5. С. 413-
421.
10. Pershin P.S ., K ataev A .A ., F ilatov A .A ., S uzdaltsev A .V., Z aikov Yu .P.
Synthesis of Al-Zr alloys via ZrO2 aluminium"thermal reduction in KF-AlF3"based melts // Metal"
lurgical and Materials Transactions B. 2017. 48. P. 1962-1969.
11. Ф и л а т о в А . А . , П е р ш и н П . С . , Н и к о л а е в А . Ю . , С у з д а л ь ц е в А . В .
Получение сплавов и лигатур Al-Zr при электролизе расплавов KF-NaF-AlF3-ZrO2 // Цвет"
ные металлы. 2017. № 11. С. 27-31.
12. K u b i n a k o v a E . , D a n i e l i k V. , H i ve s J . Advanced technology for Al-Zr alloy
synthesis: Electrochemical investigation of suitable low"melting electrolytes // J. Alloys and Com"
pounds. 2018. 738. P. 151-157.
13. С у з д а л ь ц е в А . В . , Ф и л а т о в А . А . , Н и к о л а е в А . Ю . , П а н к р а т о в А . А . ,
Молчанова Н.Г., Зайков Ю.П. Извлечение скандия и циркония из их оксидов при
электролизе оксидно"фторидных расплавов // Расплавы. 2018. № 1. С. 5-13.
14. F i l a t o v A . A . , Pe r s h i n P. S . , S u z d a l t s e v A . V. , N i k o l a e v A . Yu . ,
Z a i k ov Yu . P. Synthesis of Al-Zr master alloys via the electrolysis of KF-NaF-AlF3-ZrO2 melts //
J. Electrochemical Society. 2018. 165. № 2. P. E28-E34.
15. P i c a r d G . S . , S e o n F. , Tr e m i l l o n B . Oxoacidity reactions in molten lithium chlo"
ride + potassium chloride eutectic (at 470°C): potentiometric study of the equilibria of exchange of
oxide ion between aluminum(III) systems and carbonate and water systems // J. Electroanalytical
Chemistry and Interfacial Electrochemistry. 1979. 102. № 1. P. 65-75.
16. P i c a r d G . S . , S e о n F. , Tr e m i l l o n B . , B e r t a u d Y. Effect of the addition of
fluoride on the conditional solubility of alumina in lithium chloride-potassium chloride eutectic melt //
Electrochim. Acta. 1980. 25. P. 1453-1462.
17. P i c a r d G . S . , B o u y e r F. C . , L e r o y M . , B e r t a u d Y. , B o u ve t S . Structures
of oxyfluoroaluminates in molten cryolite-alumina mixtures investigated by DFT"based calculations //
J. Molecular Structure (Theochem). 1996. 368. P. 67-80.
18. R obert E ., O lsen J.E ., D anek V., Tixhon E ., O stvold T., G ilbert B .
Structure and thermodynamics of alkali fluoride"aluminum fluoride"alumina melts. Vapor pressure,
solubility, and Raman spectroscopic studies // J. Phys. Chem. B. 1997. 101. P. 9447-9456.
19. T h o r n e R . J . , S o m m e r s e t h C . , R a t v i k A . P. , R o r v i k S . , S a n d n e s E . ,
L o s s i u s L . P. , L i n g H . , S ve n s s o n A . M . Correlation between coke type, microstructure
and anodic reaction overpotential in aluminium electrolysis // J. Electrochemical Society. 2015. 162.
№ 12. P. E296-E306.
20. G a l a s h e v A . Y. , R a k h m a n o v a O . R . Computer modeling of oxygen migration ac"
companying aluminum production // Letters on materials. 2017. 7. № 4. P. 373-379.
21. G a l a s h e v A . Y. , R a k h m a n o v a O . R . Computer study of oxygen release from Al
melts // Modelling and Simulation in Materials Science and Engineering. 2017. 26. 025003.
22. H o h e n b e r g P. , K o h n W. Inhomogeneous electron gas // Physical Review B. 1964.
136. P. 864-871.
23. K o h n W. , S h a m L . J . Self"consistent equations including exchange and correlation ef"
fects // Physical Review A. 1965. 140. P. 1133-1138.
24. Pe r d e w J . P. , B u r k e K . , E r n z e r h o f M . Generalized gradient approximation
made simple // Physical Review Letters. 1996. 77. P. 3865-3868.
Bond Energies in the Molten M-Al-Zr-O-F Systems (M = Li, Na, K)
A. S. Vorobiov1, A. V. Suzdaltsev1, A. E. Galashev1
1Institute of High Temperature Electrochemistry, Ural Branch of Russian Academy of Sciences,
Akademicheskaya st., 20, Yekaterinburg, 620990 Russian Federation
The bond energies in complex anions formed from the components Al-F, Zr-F, Al-OF,
and Zr-OF were calculated in Siesta program using first"principle molecular dynamics.
These anions are formed at the dissolution of ZrO2 and Al2O3 oxides in fluoride MF"AlF3
Энергия связей в расплавленных системах M-Al-Zr-O-F
165
melts (where M = Li, Na, K). An influence of anions composition as well as the cation na"
ture in the second coordination sphere on the bond energies in the anions was determined. It
2-
2−
was shown that the
Al
2
O
2
F
6
and
Zr
2
O
2
F
6
anions are most stable among analyzed oxygen"
containing anions. At the same time anions formed by zirconium have the lowest bond ener"
gies. Replacement of the cation in the second coordination sphere of the M2Al2O2F6 and
M2Zr2O2F6 anions in the range from K to Li leads to a decrease in the bond energy.
Keywords: oxide"fluoride melt, anions, zirconium, aluminum, molecular dynamics sim"
ulation, bond energy, stability
REFERENCES
1. Ogorodov D.V., Popov D.A., Trapeznikov A.V. Methods of preparing аluminum"zirconium
master alloy (review) [Sposoby polucheniya ligatury Al-Zr (obzor)]. 2015. № 11. Р. 2-11. [In Rus.].
2. Knipling K.E., Seidman D.N., Dunand D.C. Ambient" and high"temperature mechanical
properties of isochronally aged Al-0.06Sc, Al-0.06Zr and Al-0.06Sc-0.06Zr (at. %) alloys // Acta
Materialia. 2011. 59. P. 943-954.
3. Gasik M.I., Lyakishev N.P., Emlin B.I. Theory and practice of ferroalloys production [Teoriya i
tekhnologiya proizvodstva ferrosplavov]. M.: Metallurgia. 1988. 784 p. [In Rus.].
4. Yatsenko S.P., Ovsyannikov B.V., Ardashev M.A., Sabirzyanov A.N. Precipitated receipt of
"master"alloy" from fluoride"chloride melts [Tsementatsionnoye polucheniye "master+splava" iz ftorid+
no+khloridnykh rasplavov] // Rasplavy. 2006. № 5. P. 29-36. [In Rus.].
5. Napalkov V.I., Makhov S.V. Alloying and modifying of aluminium and magnesium [Legiro+
vaniye i modifitsirovaniye magniya i alyuminiya]. Moscow: MISiS. 2002. 376 p. [In Rus.].
6. Krasikov S.A., Agafonov S.N., Chentsov V.P., Zhilina E.M. The effect of phase formation on
the character of inter"phase interaction at alumo"thermic reduction of zirconium from its dioxide
[Vliyaniye fazoobrazovaniya na kharakter mezhfaznykh vzaimodeystviy pri alyumotermicheskom
vosstanovlenii tsirkoniya iz yego dioksida] // Rasplavy. 2015. № 2. P. 60-64. [In Rus.].
7. Agafonov S.N., Krasikov S.A., Ponomarenko A.A., Ovchinnikova L.A. Phase relations in the
aluminothermic reduction of ZrO2 [Fazoobrazovaniye pri alyumotermicheskom vosstanovlenii ZrO2] //
Inorganic Materials. 2012. 48. P. 927-934. [In Rus.].
8. Juneja J.M. Preparation of aluminium"zirconium master alloys // Indian J. Engineering & Ma"
terials Sciences. 2002. 9. P. 187-190.
9. Pershin P.S., Filatov A.A., Suzdaltsev A.V., Zaikov Yu.P. Aluminum"thermal receiving of Al-Zr
alloys in KF-AlF3 melt [Alyumotermicheskoye polucheniye splavov Al-Zr v rasplave KF-AlF3] // Ras"
plavy. 2016. № 5. P. 413-21. [In Rus.].
10. Pershin P.S., Kataev A.A., Filatov A.A., Suzdaltsev A.V., Zaikov Yu.P. Synthesis of Al-Zr al"
loys via ZrO2 aluminium"thermal reduction in KF-AlF3"based melts // Metallurgical and Materials
Transactions B. 2017. 48. P. 1962-1969.
11. Filatov A.A., Pershin P.S., Nikolaev A.Yu., Suzdaltsev A.V. Synthesis of Al"Zr alloys and mas"
ter"alloys during the electrolysis of KF-NaF-AlF3-ZrO2 melts [Polucheniye splavov i ligatur Al-Zr
pri elektrolize rasplavov KF-NaF-AlF3-ZrO2] // Tsvetnye metally. 2017. № 11. P. 27-31. [In Rus.].
12. Kubinakova E., Danielik V., Hives J. Advanced technology for Al-Zr alloy synthesis: Electro"
chemical investigation of suitable low"melting electrolytes // J. Alloys and Compounds. 2018. 738.
P. 151-157.
13. Suzdaltsev A.V., Filatov A.A., Nikolaev A.Yu., Pankratov A.A.,Molchanova N.G., Zaikov
Yu.P. Extraction of scandium and zirconium from their oxides during the electrolysis of oxide-fluo"
ride melts // Russian Metallurgy (Metally). 2018. V. 2018. № 2. P. 133-138.
14. Filatov A.A., Pershin P.S., Suzdaltsev A.V., Nikolaev A.Yu., Zaikov Yu.P. Synthesis of Al-Zr
master alloys via the electrolysis of KF-NaF-AlF3-ZrO2 melts // J. Electrochemical Society. 2018.
165. № 2. P. E28-E34.
15. Picard G.S., Seon F., Tremillon B. Oxoacidity reactions in molten lithium chloride + potassi"
um chloride eutectic (at 470°C): potentiometric study of the equilibria of exchange of oxide ion be"
tween aluminum(III) systems and carbonate and water systems // J. Electroanalytical Chemistry and
Interfacial Electrochemistry. 1979. 102. № 1. P. 65-75.
166
А. С. Воробьев, А. В. Суздальцев, А. Е. Галашев
16. Picard G.S., Seоn F., Tremillon B., Bertaud Y. Effect of the addition of fluoride on the condi"
tional solubility of alumina in lithium chloride-potassium chloride eutectic melt // Electrochim. Acta.
1980. 25. P. 1453-1462.
17. Picard G.S., Bouyer F.C., Leroy M., Bertaud Y., Bouvet S. Structures of oxyfluoroaluminates
in molten cryolite-alumina mixtures investigated by DFT"based calculations // J. Molecular Struc"
ture (Theochem). 1996. 368. P. 67-80.
18. Robert E., Olsen J. E., Danek V., Tixhon E., Ostvold T., Gilbert B.. Structure and thermody"
namics of alkali fluoride"aluminum fluoride"alumina melts. Vapor pressure, solubility, and Raman
spectroscopic studies // J. Phys. Chem. B. 1997. 101. P. 9447-9456.
19. Thorne R.J., Sommerseth C., Ratvik A.P., Rorvik S., Sandnes E., Lossius L.P., Ling H., Svens"
son A.M. Correlation between coke type, microstructure and anodic reaction overpotential in alumin"
ium electrolysis // J. Electrochemical Society. 2015. 162. № 12. P. E296-E306.
20. Galashev A.Y., Rakhmanova O.R. Computer modeling of oxygen migration accompanying
aluminum production // Letters on materials. 2017. 7. № 4. P. 373-379.
21. Galashev A.Y., Rakhmanova O.R. Computer study of oxygen release from Al melts // Model"
ling and Simulation in Materials Science and Engineering. 2017. 26. 025003.
22. Hohenberg P., Kohn W. Inhomogeneous electron gas // Physical Review B. 1964. 136. P. 864-
871.
23. Kohn W., Sham L.J. Self"consistent equations including exchange and correlation effects //
Physical Review A. 1965. 140. P. 1133-1138.
24. Perdew J.P., Burke K., Ernzerhof M. Generalized gradient approximation made simple //
Physical Review Letters. 1996. 77. P. 3865-3868.