РАСПЛАВЫ
6 · 2019
УДК 544.2:546.05:54.31
МОДИФИЦИРОВАНИЕ КАТИОННОГО СОСТАВА НАНОПОРОШКОВ LiNbO3
И LiTaO3 В КАЛЬЦИЙСОДЕРЖАЩИХ ХЛОРИДНЫХ РАСПЛАВАХ
© 2019 г. В. А. Хохловa, b, *, Н. А. Вьюгинa, В. Н. Докутовичa,
И. Д. Закирьяноваa, b, Б. Д. Антоновa
aИнститут высокотемпературной электрохимии УрО РАН, Екатеринбург, Россия
bУральский федеральный университет им. первого Президента России Б.Н. Ельцина,
Екатеринбург, Россия
*e7mail: v.khokhlov@ihte.uran.ru
Поступила в редакцию 17.06.2019 г.
После доработки 28.06.2019 г.
Принята к публикации 15.07.2019 г.
Ионный состав нанопорошков метаниобата и метатанталата лития модифициро
ван в кальцийсодержащих хлоридных расплавах. Исследования продуктов реакции
методами рентгеновской дифрактометрии, спектроскопии комбинационного рассе
яния света, сканирующей электронной микроскопии, энергодисперсионной рентге
новской спектроскопии и элементного химического анализа показали, что поверх
ностный слой модифицированных малоразмерных частиц порошков ниобата или
танталата лития обогащен метаниобатом или метатанталатом кальция (CaNb2O6,
CaTa2O6), образованными в результате реакции изоморфного гетеровалентного за
мещения ионов лития ионами кальция в расплавленных смесях LiCl-CaCl2 и KCl-
CaCl2 при температурах 700 и 750°C.
Ключевые слова: функциональные оксидные материалы, неорганический синтез, мо
дифицирование химического состава, хлоридный расплав, метаниобат и метатанта
лат лития, нанопорошки.
DOI: 10.1134/S0235010619060069
ВВЕДЕНИЕ
Ниобаты и танталаты щелочных и щелочноземельных металлов являются практи
чески важными оптоэлектрическими материалами и сегнетоэлектриками [1, 2], вслед
ствие чего представляет интерес разработка новых методов получения их стехиомет
рических и допированных разными элементами мелкодисперсных порошков для со
здания специальных керамик с заданными эксплуатационными свойствами. В
последние годы предложены и испытаны более совершенные способы синтеза мета
ниобатов и метатанталатов MNbO3, MTaO3, MeNb2O6, MeTa2O6 (M - щелочной ме
талл, Me - щелочноземельный металл) в виде нанопорошков с различной морфологи
ей частиц (1d наностержней, 2d наноразмерных пластин, 3d объемных нанокристал
лов), среди которых особый интерес вызывают различные модификации методов,
связанных с использованием расплавленных солей [3, 4]. Эти методы позволяют сни
зить температуру получения малоразмерных стехиометрических ниобатов и тантала
тов щелочных и щелочноземельных металлов на сотни градусов по сравнению с их
твердофазным синтезом из соответствующих оксидов, обеспечить однородность рас
пределения исходных оксидных частиц в реакционной среде, повышающую скорость
процесса синтеза, контролировать морфологию и размер частиц, снизить их склон
ность к агломерации.
Из за уникальных оптических и диэлектрических свойств ниобаты и танталаты ще
лочных и щелочноземельных металлов могут быть использованы для создания новых
590
В. А. Хохлов, Н. А. Вьюгин, В. Н. Докутович и др.
оптоэлектронных устройств [5-7]. Интересен опыт формирования на основе кристал
лов танталата лития оптических волноводов с широким диапазоном показателей пре
ломления и точек Кюри, которые образованы за счет реакций гетеровалентного обме
на в расплавах, содержащих соли двухвалентных металлов (Zn2+
→
2Li+, Ni2+
→
2Li+,
Mn2+
→
2Li+, Fe2+
→
2Li+, Co2+
→
2Li+, Ca2+
→
2Li+, Mg2+
→
2Li+) [8, 9]. Порошки
твердых растворов замещения с катионными вакансиями (Li1 - xMex/2VLix/2NbO3 и
Li1⎯ xMex/2VLix/2TaO3, где Мe - ионы двухвалентных металлов), образующихся в резуль
тате подобных реакций при обработке мелкокристаллических ниобата и танталата ли
тия соответствующими солевыми расплавами, могут быть использованы для изготов
ления керамик с хорошей протонной проводимостью во влажных атмосферах.
Судя по опубликованным результатам, практически во всех исследованиях на раз
ных этапах получения ниобатов и танталатов щелочных и щелочноземельных метал
лов в качестве хотя бы одного из базовых жидкосолевых прекурсоров или вспомога
тельного вещества используются термически нестойкие соли кислородсодержащих
кислот. Часто получение конечного продукта было связано с синтезом нескольких
промежуточных прекурсоров. Для этого применялись разные методы: от высокотем
пературных твердофазных до гидротермальных. Это снижало положительный эффект
от использования солевых расплавов и существенно усложняло процесс синтеза слож
ных оксидов, в частности ниобатов и танталатов щелочных и щелочноземельных метал
лов, и модифицирования их химического состава. В ряде наших работ [10-14] показано,
что использование в качестве прекурсоров расплавов термостойких солей, например,
галогенидов щелочных, щелочноземельных и переходных металлов, подвергнутых пря
мому окислению кислородом воздуха, создает благоприятные условия для синтеза на
норазмерных частиц сложных оксидов. Логическим развитием этих исследований яв
ляется использование термостойких галогенидных расплавов для изменения химиче
ского состава сложных оксидов.
В данном сообщении приведены результаты исследования модифицирования кати
онного состава нанопорошков метаниобата и метатанталата лития в кальцийсодержа
щих хлоридных расплавах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез исходных малоразмерных порошков метаниобата и метатанталата лития
(LiNbO3 и LiTaO3) основан на взаимодействии оксидов лития, ниобия и тантала, in situ
образованных в результате реакций гомогенных смесей расплавленного хлорида ли
тия и пентахлоридов ниобия или тантала, с кислородом воздуха. В некоторых случая в
качестве прекурсоров вместо хлоридов ниобия и тантала были использованы их мел
кодисперсные оксиды Nb2O5 и Ta2O5. Все соли и оксиды, использованные для получе
ния ниобата и танталата лития, имели квалификацию не хуже “ч. д. а.” и не подверга
лись дополнительной обработке. Синтез проводили при температуре 700°C, более
низкой, чем в классическом способе твердофазного спекания оксидов, в том числе об
разованных в результате термического разложения нестойких солей лития, ниобия
или тантала (карбонатов, нитратов, ацетатов, формиатов и др.) [1, 13, 14]. Подробно
метод синтеза порошков LiNbO3 и LiTaO3 обоснован и описан в нашей статье [12]. Полу
ченные для данного исследования ниобат и танталат лития аттестованы методами рент
генофазового анализа (РФА), колебательной (ИК и КРС) спектроскопии, сканирующей
электронной микроскопиии (СЭМ) и энергодисперсионной спектроскопии (ЭДС).
Для модифицирования катионного состава нанопорошков ниобата и танталата ли
тия в кальцийсодержащих хлоридных расплавах был использован простой способ их
Модифицирование катионного состава нанопорошков LiNbO
3
и LiTaO3
591
4
Ar
Воздух
3
3
1
1
2
2
5
5
6
6
7
7
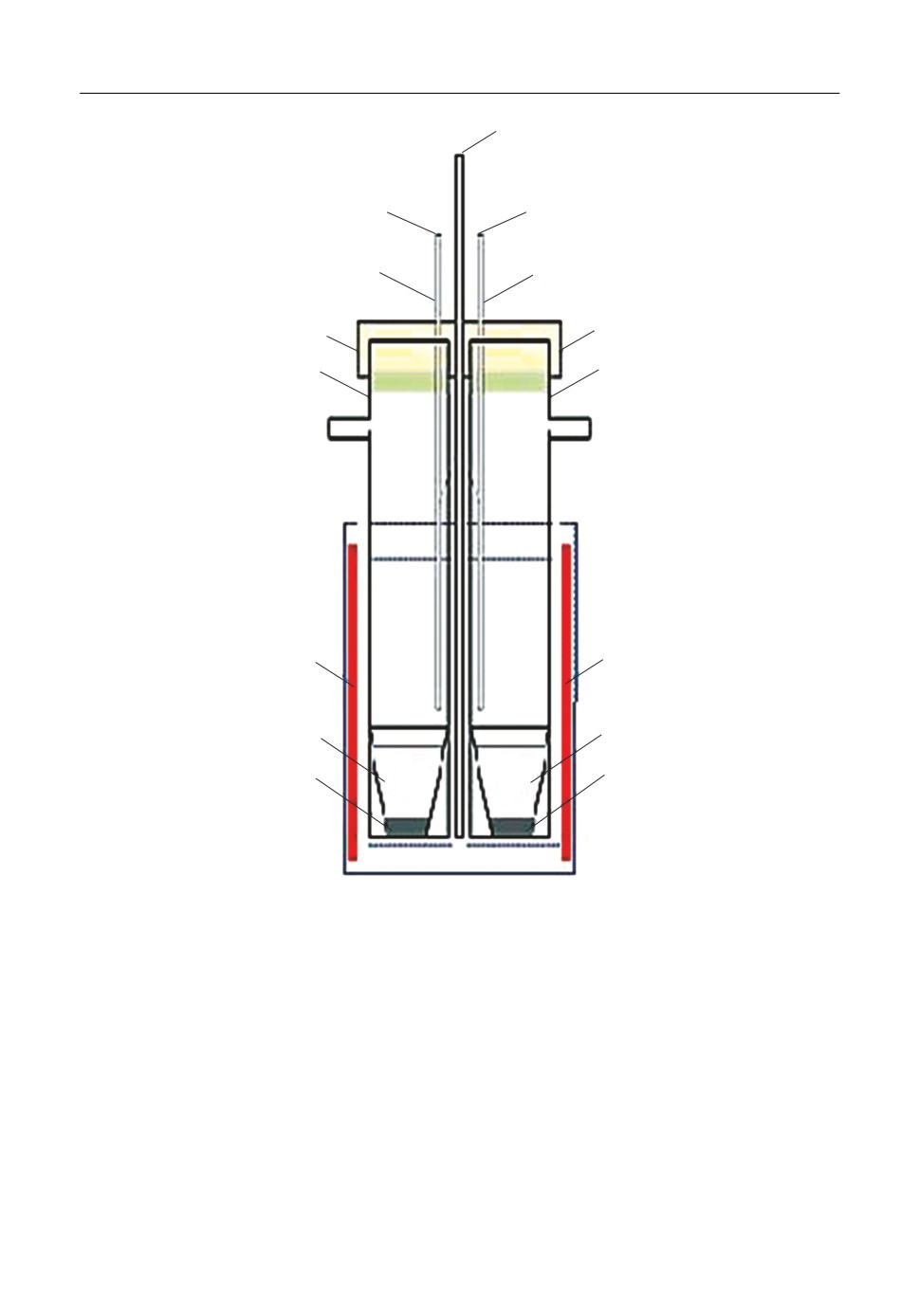
Рис. 1. Схема реактора для модифицирования химического состава ниобата и танталата лития в солевых
расплавах: 1 - пробка; 2 - кварцевая пробирка; 3 - трубка для подачи газа; 4 - термопара; 5 - электриче
ская печь сопротивления; 6 - хлоридный расплав; 7 - порошок LiNbO3 (LiTaO3).
изотермической выдержки в реакторе, схематически изображенном на рис. 1. Он поз
волял проводить эксперименты в разных газовых атмосферах (инертной аргоновой и
воздушной) при одной той же температуре для того, чтобы установить возможное вли
яние кислородсодержащих компонентов воздуха (кислорода, углекислого газа, следов
воды) на состав и стехиометрию конечных оксидных продуктов реакции гетеровалент
ного замещения лития в его ниобате или танталате. В качестве реакционных сред - мо
дификаторов были выбраны расплавленные смеси (0.35CaCl2-0.65LiCl) и (0.40CaCl2-
0.60KCl) с приблизительно одинаковым мольным содержанием хлорида кальция.
Предварительно было изучено взаимодействие ниобата и танталата лития с эвтектиче
592
В. А. Хохлов, Н. А. Вьюгин, В. Н. Докутович и др.
ской смесью хлоридов лития и калия. Безводные реактивы (LiCl, KCl и CaCl2) квали
фикации “х. ч.”, использованные для приготовления реакционных смесей, не подвер
гались дополнительной обработке. Эксперименты с расплавами LiCl-KCl и LiCl-
CaCl2 эвтектического состава выполнены при 700°С, а с реакционной смесью KCl-
CaCl2, плавящейся при 717°С, опыты проведены при 750°С.
Возможность изоморфного гетеровалентного замещения лития кальцием была оце
нена по энергии Гиббса (ΔG) реакции:
2LiNbO3(тв) + CaCl2(ж) = CaO · Nb2O5(тв) + 2LiCl(ж),
для которой в базе данных программы для расчета термодинамических параметров
HSC Chemistry 7.1 есть все необходимые сведения. Судя по величинам ΔG при 700 и
750°С, равным -9.65 и -14.56 кДж/моль, соответственно, реакция должна протекать.
Для танталата лития расчеты не проведены из за отсутствия термодинамических па
раметров танталата кальция (CaO · Ta2O5). Каких либо термодинамических данных
для пирониобата (танталата) и ортониобата (танталата) кальция в литературе также не
приводится, что не позволяет предсказать вероятность их образования в упомянутых
реакциях изоморфного замещения.
После опытов охлажденные до комнатной температуры оксидно солевые смеси
растворяли в дистиллированной воде. Осадок продуктов реакций отделяли фильтро
ванием, промывали, высушивали и исследовали.
Для идентификации и исследования свойств исходных LiNbO3, LiTaO3 и продуктов
реакции были использованы различные весьма информативные методы. Структурно
фазовый анализ был проведен на автоматизированном рентгеновском дифрактометре
Rigaku D/MAX 2200VL/PC с CuKα1 источником радиации и графитовым монохрома
тором. Идентификация дифрактограмм проводилась по базе данных MDI/JADE6.
Элементный химический состав солевых реакционных сред определялся на эмисси
онном спектрометре Optima 4300 DV с индуктивно связанной плазмой. Информация
о микроскопической структуре порошков была получена методом комбинационного
рассеяния света с использованием оптоволоконного спектрометрического комплекса
Avantes Ava Raman, оснащенного лазерным источником монохроматического света с
длиной волны λ = 532 нм. Морфологические особенности и полуколичественный хи
мический состав порошков были изучены сканирующем электронном микроскопе с
энергодисперсионным рентгеновским детектором X act ADD + JSM 5900LV, снаб
женном волновым дисперсионным микроанализатором, шлюзовой камерой и устрой
ством для подавления электромагнитных помех INCA Energy 250 and INCA Wave 500.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
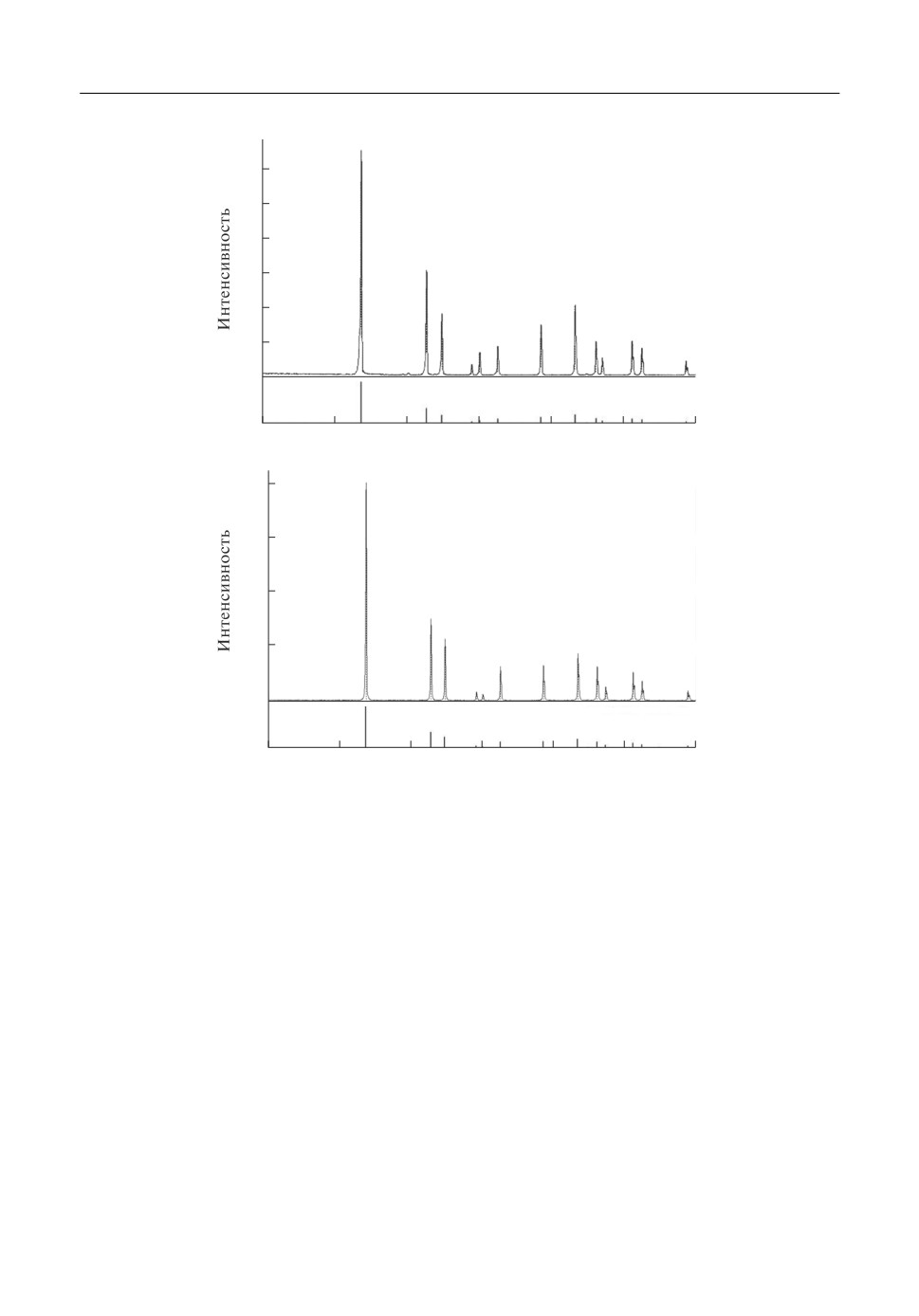
По данным РФА исходные порошки LiNbO3 и LiTaO3 представляют собой однофаз
ные мелкокристаллические ниобат и танталат лития ромбоэдрической модификации
(рис. 2), о чем свидетельствует проведенная с их использованием оценка размеров
кристаллитов. Для обоих случаев они находились в пределах от 500 до 540 Å. ИК и
КРС спектры чистых ниобата и танталата лития, приведенные в нашей ранее опубли
кованной работе [12], указывают на их принадлежность к пространственной группе
с точечной симметрией 3m [15, 16].
R
3
c
Предварительные эксперименты по изотермической обработке этих порошков в
расплавленной эвтектической смеси LiCl-KCl при 700°С в течение 5 ч показали, что
метаниобат и метатанталат лития не взаимодействуют с этим расплавом, о чем свиде
тельствуют результаты исследования методами РФА (дифрактограмма аналогична
Модифицирование катионного состава нанопорошков LiNbO
3
и LiTaO3
593
а
12
10
8
5
4
2
· 103
LiNbO3 - ниобат лития
10
20
30
40
50
60
70
2θ
20
б
15
10
5
· 103
LiTaO3 - танталат лития
10
20
30
40
50
60
70
2θ
Рис. 2. Дифрактограммы ниобата лития (a) и танталата лития (б), синтезированных в расплавленном хлори
де лития при 700°С и использованных в экспериментах по модифицированию их катионного состава.
приведенной на рис. 2б), СЭМ (рис. 3) и ЭДС (табл. 1). В качестве примера приведены
данные, полученные для порошка танталата лития. Полученные сведения были от
правной точкой и оказались весьма полезными в последующей работе с хлоридными
расплавами модификаторами (0.35CaCl2-0.65LiCl) и (0.40CaCl2-0.60KCl). Поскольку
в отличие от калия сродство к кислороду у кальция больше, чем у лития, ожидалось,
что при контакте ниобата и танталата лития с кальцийсодержащими расплавами будет
протекать реакция изоморфного гетеровалентного замещения ионов лития ионами
кальция в микрокристаллах LiNbO3 и LiTaO3 с образованием метаниобата или мета
танталата кальция (CaNb2O6, CaTa2O6) и их твердых растворов с катионными ваканси
ями: Li1 - xCax/2VLix/2NbO3 и Li1 - xCax/2VLix/2TaO3.
Первоначально эксперименты с этими расплавами были выполнены в инертной
(аргон) и воздушной газовых средах, для того чтобы оценить возможное влияние кис
лорода воздуха и присутствующих в нем следов влаги на процесс изоморфного заме
594
В. А. Хохлов, Н. А. Вьюгин, В. Н. Докутович и др.
2
1
5 мкм
Рис. 3. Микрофотография СЭМ порошка танталата лития после его изотермической обработки в эвтектиче
ской смеси хлоридов лития и калия при 700°С.
щения, состав и структуру конечного продукта. Из приведенных в качестве типичного
примера сведений о химическом составе водного раствора охлажденной реакционной
солевой смеси 0.4CaCl2-0.6KCl после ее взаимодействия с танталатом лития при
750°С в течение 5 и ч (табл. 2) следует, что в том и другом случаях произошла реакция
изоморфного замещения. Отношение концентраций оставшегося в расплаве кальция
и появившегося в нем лития в результате прошедшей в инертной и воздушной газовых
атмосферах реакции было приблизительно одинаковым (192.3 в воздушной и 231.0 в
аргоновой атмосфере). Поэтому последующие исследования проводились, как прави
ло, в воздушной атмосфере. Было установлено также, что обработка ниобата и танта
лата лития в разных по катионному составу калийсодержащих хлоридных расплавах
не влияла на химический состав конечных продуктов реакций гетеровалентного заме
щения. Более точная и надежная информация о химическом и фазовом составах, а
также о морфологии и структуре модифицированных в солевых расплавах ниобата и
танталата лития была получена с помощью рентгенофазового анализа, спектроскопии
комбинационного рассеяния света, сканирующей электронной микроскопии и рент
геновской энергодисперсионной спектроскопии.
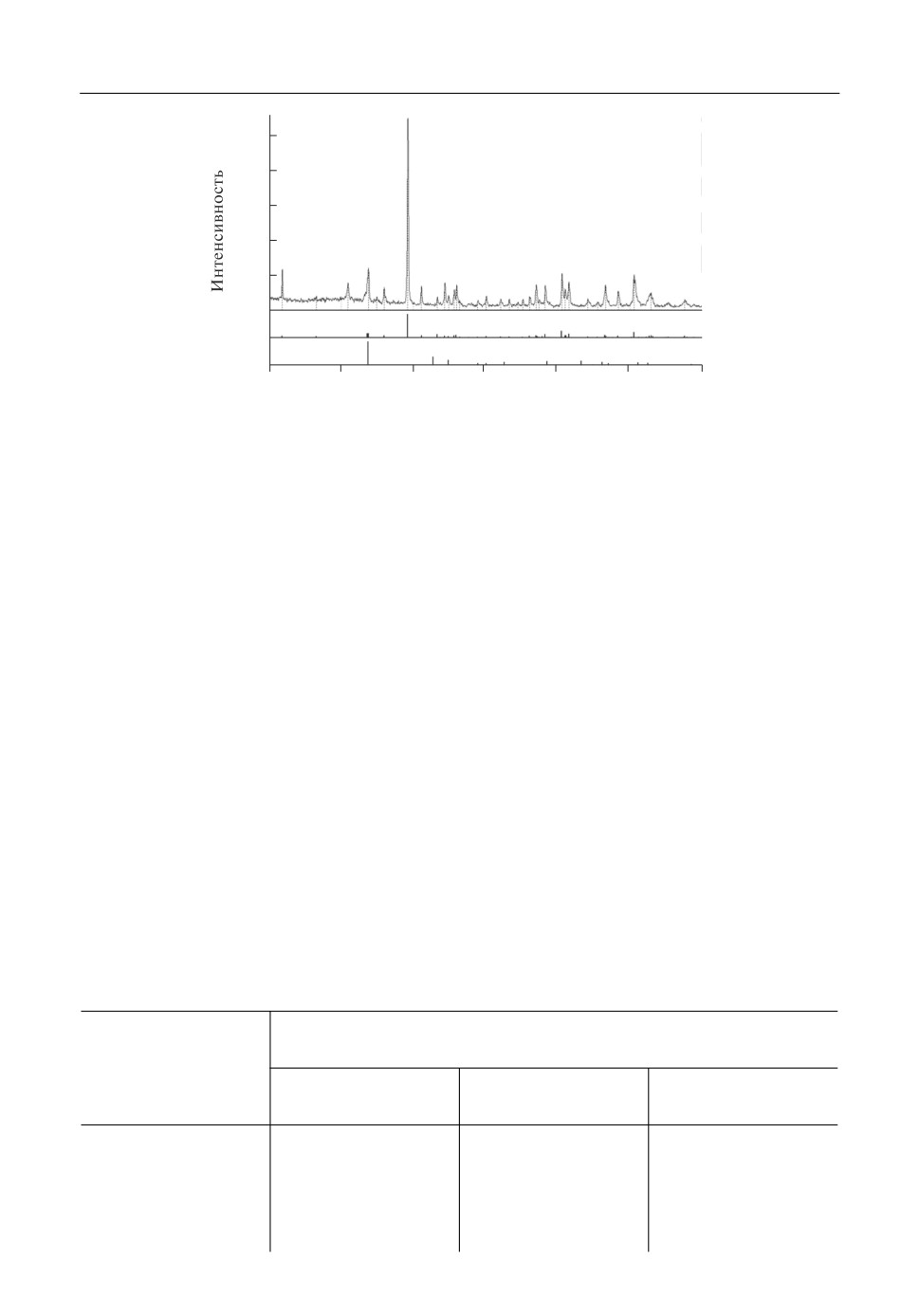
Из рентгенограммы модифицированного в расплаве (0.35CaCl2-0.65LiCl) порошка
ниобата лития (рис. 4) видно, что при изоморфном гетеровалентном замещении про
Таблица 1
Концентрация элементов (ат. %) в точках поверхности порошка танталата лития после его изотермической
обработки в эвтектической смеси хлоридов лития и калия, отмеченных на рис. 3, по результатам ЭДС
№ позиции
O
Cl
K
Ta
1
76.05
0.00
0.00
23.95
2
75.88
0.00
0.00
24.12
Модифицирование катионного состава нанопорошков LiNbO
3
и LiTaO3
595
1250
1000
750
500
250
0
39-1392 > Ферсмит - CaNb2O6
74-2238 > LiNbO3 - ниобат лития
10
20
30
40
50
60
70
2θ
Рис. 4. Дифрактограмма ниобата лития, модифицированного в расплавленной смеси хлоридов лития и
кальция при 700°С.
дуктом реакции был бипирамидальный метаниобат кальция (CaNb2O6) с орторомби
ческой структурой типа ферсмита, кристаллизующейся в пространственной группе
Pbcn. В то же время сопоставительный анализ проявляющихся на этой рентгенограм
ме остаточных пиков ниобата лития и рентгенограммы чистого LiNbO3 (pис. 2а) показал
увеличение параметров кристаллической решетки a и c, а также объема элементарной
ячейки V в модифицированном порошке (a = 5.19630 Å, c = 13.95273 Å, V = 326.27 Å3) по
сравнению с исходным ниобатом (a = 5.15252 Å, c = 13.87072 Å, V = 318.91 Å3). Это
свидетельствует не только об образовании новой фазы (CaNb2O6), но и твердого рас
твора замещения (Li1 - xCax/2VLix/2NbO3).
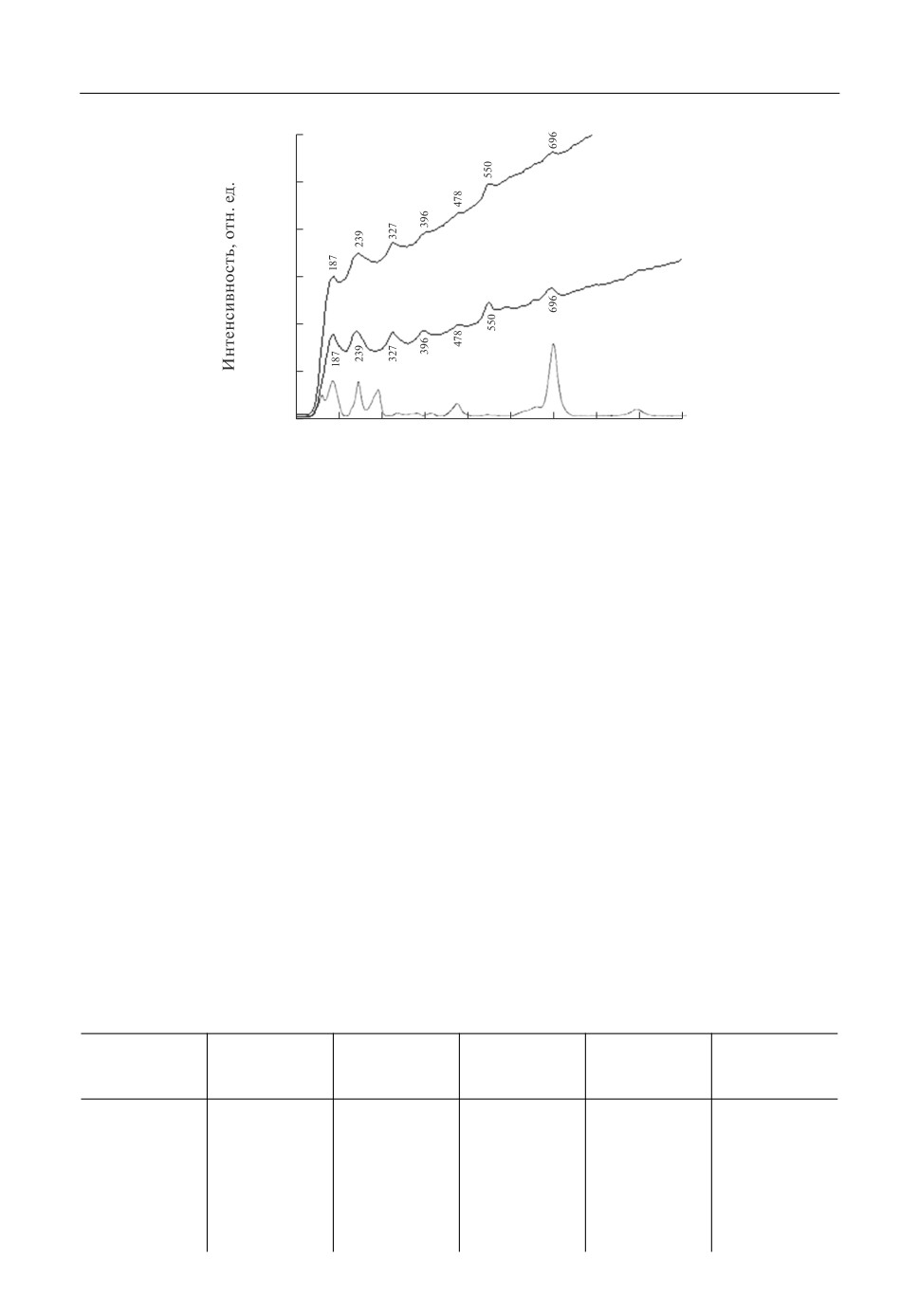
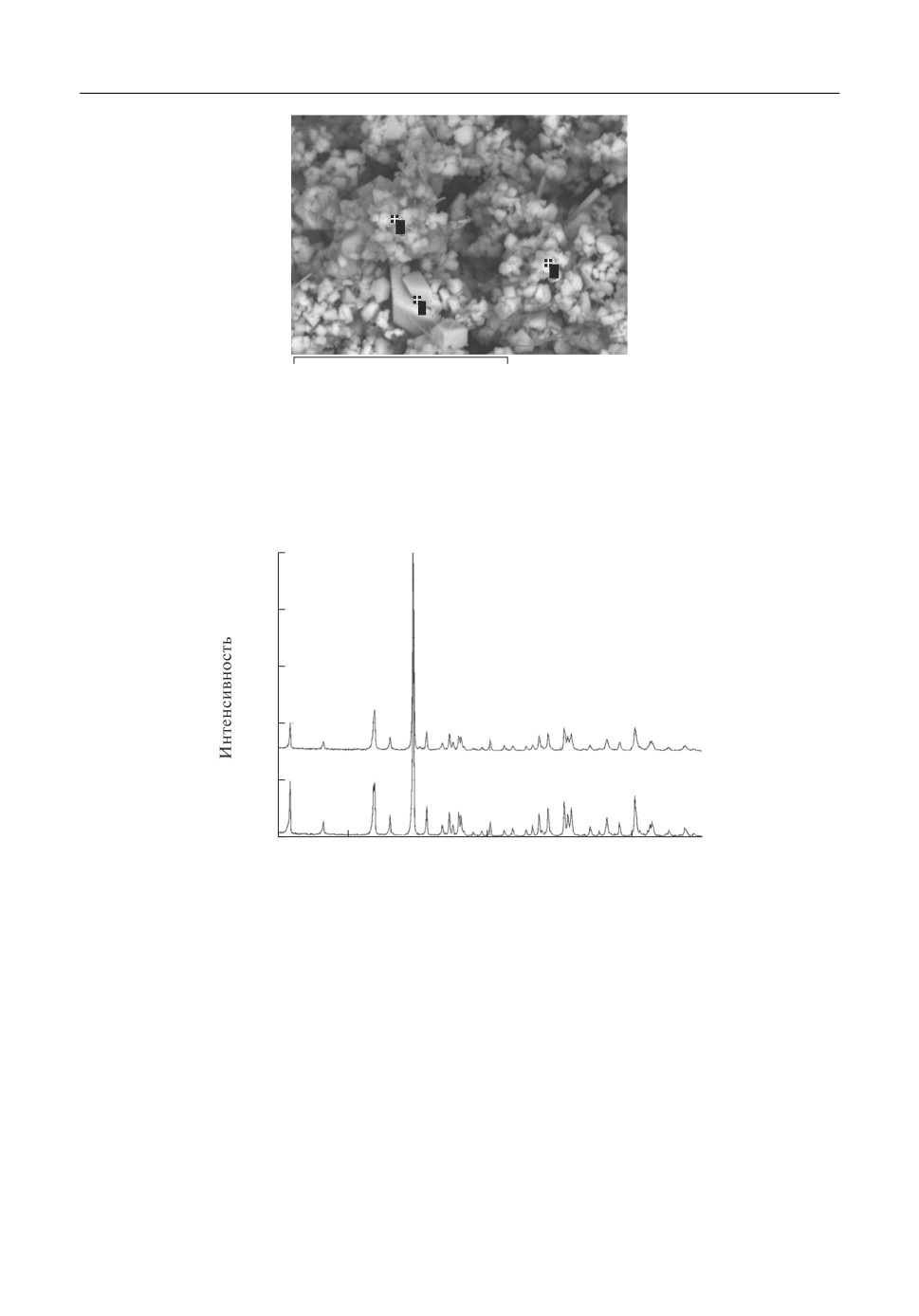
Для модифицированного в расплаве (0.4CaCl2-0.6KCl) танталата лития характерно
образование CaTa2O6, о чем свидетельствуют спектры КРС (рис. 5), и полученные ме
тодом СЭМ (рис. 6) изображения поверхности порошка во вторичных электронах,
глубина проникновения которых в микрокристаллы не превышает 50 нм, а также дан
ные рентгеновской ЭДС по элементному составу поверхностного слоя (табл. 3).
Таблица 2
Элементный состав водного раствора охлажденной реакционной солевой смеси
0.4CaCl2-0.6KCl после ее взаимодействия с порошком танталата лития
Концентрация элементов в водном растворе реакционной солевой среды, мг/л
Элемент
исходный расплав
после опыта в воздухе
после опыта в аргоне
K
3583.00
4024.00
6016.00
Li
0.11
14.80
19.90
Ca
2480.00
2847.00
4240.00
596
В. А. Хохлов, Н. А. Вьюгин, В. Н. Докутович и др.
1
60 000
50 000
40 000
2
30 000
20 000
10 000
0
300
400
600
800
1000
Волновое число, 1/см
Рис. 5. Спектры КРС поверхности порошков LiTaO3, обработанных расплавом (0.4CaCl2-0.6KCl) в аргоно
вой (1) и воздушной (2) газовой атмосфере при 750°С. Здесь же показаны для сравнения справочные данные
для спектра CaTa2O6 [15].
Спектры КРС демонстрируют идентичность продуктов, получаемых в инертной и
кислородсодержащей газовых атмосферах, а также их хорошее согласие с литератур
ными данными (нижняя вкладка на рис. 5) для неориентированного образца минера
ла ринерсонита [15].
В отличие от порошков чистых ниобата и танталата лития, морфологические черты
которых можно видеть на примере LiTaO3 после термической обработки при 700°С в
эвтектике LiCl-KCl (рис. 3), их порошки, обогащенные продуктами изоморфного за
мещения ионов лития ионами кальция, более разнообразны по форме и размерам об
разующих их частиц (рис. 6). Хорошо видны наноразмерные пластинки и нити.
При увеличении времени изотермической выдержки ниобата и танталата лития в
кальцийсодержащих хлоридных расплавах можно добиться контролируемого изо
морфного замещения вплоть до полной замены лития кальцием. В качестве иллю
Таблица 3
Концентрация элементов (ат. %) в точках поверхности порошка танталата лития после его изотермической
обработки в расплавленной смеси хлоридов калия и кальция, отмеченных на рис. 6, по результатам ЭДС
№ позиции
O
Cl
K
Сa
Ta
1
68.15
2.89
0.00
10.88
18.08
2
56.40
2.55
0.00
14.96
26.10
3
60.77
4.00
0.00
12.85
22.38
Модифицирование катионного состава нанопорошков LiNbO
3
и LiTaO3
597
3
2
1
10 мкм
Рис. 6. Микрофотография СЭМ порошка танталата лития после его изотермической обработки в расплав
ленной смеси хлоридов калия и кальция при 750°С.
1000
800
600
2
400
200
1
0
20
40
60
2θ
Рис. 7. Дифрактограммы ниобата лития, модифицированного в хлоридных расплавах 0.35CaCl2-0.65LiCl
при 700°С (1) и 0.4CaCl2-0.6KCl при 750°С (2) в течение 7 ч.
страции на рис. 7 приведены рентгенограммы продуктов взаимодействия ниобата ли
тия с расплавами (0.35CaCl2-0.65LiCl) и (0.40CaCl2-0.60KCl) в течение 7 и ч. Видно,
что литий полностью замещен кальцием с образованием однофазного порошкообраз
ного метаниобата кальция стехиометрического состава.
Таким образом, все рассмотренные выше примеры иллюстрируют простой способ
модифицирования химического состава мелкокристаллических порошков ниобата
или танталата лития (LiNbO3, LiTaO3) в кальцийсодержащих хлоридных расплавах при
температурах, не превышающих 800°С, основанный на реакции изоморфного гетеро
валентного замещения. Ее продуктами являются метаниобат или метатанталат каль
ция (CaNb2O6, CaTa2O6) вне зависимости от состава использованного в работе распла
598
В. А. Хохлов, Н. А. Вьюгин, В. Н. Докутович и др.
ва модификатора и газовой атмосферы над оксидно хлоридной реакционной средой.
Результаты исследования продемонстрировали также возможность частичной или
полной замены ионов лития в кристаллической решетке его ниобата или танталата на
ионы кальция и существенного изменения морфологии продуктов изоморфного гете
ровалентного замещения.
Авторы искренне благодарят сотрудников ЦКП “Состав вещества” Института вы
сокотемпературной электрохимии УрО РАН А.А. Панкратова и Н.И. Москаленко за
анализ состава и морфологии модифицированных оксидных продуктов.
Работа выполнена при частичной финансовой поддержке Российского фонда фун
даментальных исследований (проект № 18 03 00475а).
СПИСОК ЛИТЕРАТУРЫ
1. Ку з ь м и н о в Ю . С . Ниобат и танталат лития - материалы для нелинейной оптики.
М.: Наука, 1975.
2. П а л а т н и к о в М . Н . , С и д о р о в Н . В . , К а л и н н и к о в В . Т. Сегнетоэлектри
ческие твердые растворы на основе оксидных соединений ниобия и тантала. Санкт Петер
бург: Наука, 2002.
3. K i m u r a T. Molten salt synthesis of ceramic powders. in: advances in ceramics - synthesis
and characterization, processing and specific applications. Prof. Costas Sikalidis, Ed., In Tech. 2011.
P. 75-100.
4. L i L . , D e n g J . , C h e n J . , X i n g X . // Chem. Sci. 2016. 7. P. 855-865.
5. N a k a y a m a Y. , Pa u z a u s k i e P. J . , R a d e n o v i c A . , O n o r a t o R . M ,
S ay k a l l y R . J . , L i p h a r d t J ., Ya n g P. // Nature. 2007. 447. P. 1098-1101.
6. X u C h Y. , Z h e n L . , Ya n g R . , Wa n g Z . L . // J. Am. Chem. Soc. 2007. 129.
P. 15444-15445.
7. S ubhan F., Azam S., Khan G., Irfan M., Muhammad S., Al Sehemi A.G.,
N a q i b S . H . , K h e n a t a R . , K h a n S . , K i t y k i I . V. , A m i n B . // J. Alloys and Compd.
2019. 785. P. 232-239.
8. F e d o r o v V. A . , G a n s h i n V. A . , K o r k i s h k o Yu . N . , M o r o z o v a T. V. // Fer
roelectrics. 1993. 138. P. 23-36.
9. H s u W. T. , C h e n Z . B . , W u C . C . , C h o u b e y R . K . , L a n C . W. Optical prop
erties of Mg, Fe, Co doped near stoichiometric LiTaO3 single crystals / Materials. 2012. 5. P. 227-
238.
10. K h o k h l o v V . , M o d e n o v D . , D o k u t o v i c h V . , K o c h e d y k o v V . ,
Zakir’yanova I., Vovkotrub E., Beketov I. Lithium oxide solution in chloride melts
as a medium to prepare LiCoO2 nanoparticles // MRS Communications. 2014. 4. P. 15-18.
11. M o d e n o v D . V. , D o k u t o v i c h V. N . , K h o k h l o v V. A . , A n t o n o v B . D . ,
K o c h e d y k ov V. A . , Z a k i r ’ ya n ova I . D . // Russian Metallurgy. 2013. № 2. P. 86-89.
12. K h o k h l o v V. A . , D o k u t o v i c h V. N . , V i u g i n N . A . , B o b r o v a K . O . // Rus
sian Metallurgy. 2019. № 2. P. 90-96.
13. Z h u Y. , L i n S . , L i u Y. , M a D . , Wa n g B . // Materials and Manufacturing Pro
cesses. 2015. 30. P. 1342-1347.
Модифицирование катионного состава нанопорошков LiNbO
3
и LiTaO3
599
14. Ya n g T. , L i u Y. , Z h a n g L . , H u M . , Ya n g Q . , H u a n g Z . , Fa n g M . //
Advanced Powder Technology. 2014. 25. P. 933-936.
Сation Composition Modifying of LiNbO3 and LiTaO3 Nanopowder
in Calciumcontaining Chloride Melts
V. A. Khokhlov1, 2, N. A. Viugin1, V. N. Dokutovich1, I. D. Zakir’yanova1, 2, B. D. Antonov1
1Institute of High7Temperature Electrochemistry UB RAS, Yekaterinburg, Russia
2The Ural Federal University named after the first President of Russia B.N. Yeltsin, Yekaterinburg, Russia
Ionic composition of lithium metaniobate and metatantalate nanopowders is modified in
calciumcontaining chloride melts. Investigation of the reaction products by the methods of
X ray diffractometry, Raman spectroscopy, scanning electron microscopy, energy dispersion
X ray spectroscopy and elemental chemical analysis showed that surface layer of the modi
fied small dimension particles of lithium niobate and tantalate powders is enriched with the
calcium metaniobates or metatantalate (CaNb2O6, CaTa2O6) formed in the result of the iso
morphic heterovalent substitution reaction of lithium ions by calcium ions in molten LiCl-
CaCl2 and KCl-CaCl2 mixtures at the temperatures of 700 и 750°C.
Keywords: functional oxide materials, inorganic synthesis, chemical composition modi
fying, chloride melt, lithium metaniobate and metatantalate, nanopowders
REFERENCES
1. Kuz’minov Yu.S. Niobat i tantalat litiya - materialy dlya nelineynoy optiki [Lithium niobate
and tantalate - materials for nonlinear optics]. M: Nauka Publ., 1975. (in Russian).
2. Palatnikov M.N., Sidorov N.V., Kalinnikov V.T. Segnetoelektricheskie tvjerdye rastvory na os
nove oksidnykh soedineniy niobiya i tantala [Ferroelectric solid solutions based on oxide compounds
of niobium and tantalum]. St. Petersburg: Nauka Publ. 2002. (in Russian).
3. Kimura T. Molten salt synthesis of ceramic powders. in: advances in ceramics - synthesis and
characterization, processing and specific applications. Prof. Costas Sikalidis, Ed., InTech. 2011.
P. 75-100.
4. Li L., Deng J., Chen J., Xing X. // Chem. Sci. 2016. 7. P. 855-865.
5. Nakayama Y., Pauzauskie P.J., Radenovic A., Onorato R.M, Saykally R.J., Liphardt J., Yang P. //
Nature. 2007. 447. P. 1098-1101.
6. Xu Ch Y., Zhen L., Yang R., Wang Z.L. // J. Am. Chem. Soc. 2007. 129. P. 15444-15445.
7. Subhan F., Azam S., Khan G., Irfan M., Muhammad S., Al Sehemi A.G., Naqib S.H., Khenata R.,
Khan S., Kityki I.V., Amin B. // J. Alloys and Compd. 2019. 785. P. 232-239.
8. Fedorov V.A., Ganshin V.A., Korkishko Yu.N., Morozova T.V. // Ferroelectrics. 1993. 138.
P. 23-36.
9. Hsu W.T., Chen Z.B., Wu C.C., Choubey R. K., Lan C.W. Optical properties of Mg, Fe, Co
doped near stoichiometric LiTaO3 single crystals / Materials. 2012. 5. P. 227-238.
10. Khokhlov V., Modenov D., Dokutovich V., Kochedykov V., Zakir’yanova I., Vovkotrub E.,
Beketov I. Lithium oxide solution in chloride melts as a medium to prepare LiCoO2 nanoparticles //
MRS Communications. 2014. 4. P. 15-18.
600
В. А. Хохлов, Н. А. Вьюгин, В. Н. Докутович и др.
11. Modenov D.V., Dokutovich V.N., Khokhlov V.A., Antonov B.D., Kochedykov V.A.,
Zakir’yanova I.D. // Russian Metallurgy. 2013. № 2. P. 86-89.
12. Khokhlov V.A., Dokutovich V.N., Viugin N.A., Bobrova K.O. // Russian Metallurgy. 2019.
№ 2. P. 90-96.
13. Zhu Y., Lin S., Liu Y., Ma D., Wang B. // Materials and Manufacturing Processes. 2015. 30.
P. 1342-1347.
14. Yang T., Liu Y., Zhang L., Hu M., Yang Q., Huang Z., Fang M. // Advanced Powder Technol
ogy. 2014. 25. P. 933-936.