Российская сельскохозяйственная наука, 2020, № 3
УДК.633.18:631.527.7:581.143.6(571.6)
DOI:10.31857/S2500262720030047
ФОРМИРОВАНИЕ ТЕТРАПЛОИДОВ РИСА В АНДРОГЕНЕЗЕ in vitro
М.В. Илюшко, кандидат биологических наук,
М.В. Ромашова, кандидат сельскохозяйственных наук
Федеральный научный центр агробиотехнологий Дальнего Востока имени А.К. Чайки,
692539, Приморский край, п. Тимирязевский, ул. Воложенина, 30
E-mail: ilyushkoiris@mail.ru
Получение тетраплоидного риса - перспективное направление в повышении урожайности культуры. В настоящее время
отсутствуют коммерческие сорта риса из-за слабой озерненности метелки, которая обусловлена низкой фертильно-
стью пыльцы. В научной литературе отмечено, что в андрогенезе in vitro в качестве дополнительного исходного ма-
териала получаются тетраплоидные растения. Целью исследования было изучение особенностей каллусов в культуре
пыльников in vitro риса, на которых формируются тетраплоидные растения, и характеристика тетраплоидных ре-
генерантов этой культуры. Исследования проведены на 15 гибридах F2 риса Oryza sativa L. подвида japonica Kato трех
гибридных комбинаций. Показано, что андрогенез in vitro - надежный способ получения полиплоидных регенерантов у
большинства генотипов: 59 растений (1,9% от всех зеленых регенерантов) являются тетраплоидными. Доля каллусов
с тетраплоидами составляет 17,6%. Каллусы, на которых формировались тетраплоидные растения, характеризуются
снижением числа гаплоидов и увеличением бессемянных растений негаплоидного происхождения. Максимальное число
тетраплоидов на каллусный агрегат составляет 12 шт. Тетраплоиды, полученные в андрогенезе in vitro, имеют неболь-
шую озерненность метелки (в среднем 1,0-6,0 шт. на главной метелке), что типично для полиплоидного риса.
RICE TETRAPLOID FORMATION IN ANDROGENESIS in vitro
Ilyushko M.V., Romashova M.V.
Federal Scientific Centre of Agrobiotechnology of the Far East named A.K. Chaika,
692539, Primorskiy kray, p. Timiryasevskiy, ul. Volozhenina, 30
Е-mail:ilyushkoiris@mail.ru
Obtaining tetraploid rice is considered as a promising direction in increasing crop yields. There are currently no commercial rice
varieties due to poor panicle grazing due to low pollen fertility. In the scientific literature it is stated that in androgenesis in vitro
tetraploid plants are obtained as an additional starting material. The aim of the study was to study the characteristics of callus in
anther culture of rice in vitro, on which tetraploid plants are formed, and the characteristics of rice tetraploid regenerants. Studies
were performed on 15 rice hybrids F2 Oryza sativa L. subspecies japonica Kato of three hybrid combinations. In vitro androgenesis
is a reliable way to obtain polyploid regenerants in most genotypes: 59 plants (1.9% of all green regenerants) are tetraploid. The
proportion of calli with tetraploids is 17.6%. Calli, on which tetraploid plants were formed, are characterized by a decrease in
the number of haploids and an increase in seedless plants of non-haploid origin. The maximum number of tetraploids per callus
aggregate is 12 pcs. Tetraploids obtained in androgenesis in vitro have a slight grazing of the panicle (on average 1.0-6.0 pcs. оn the
main panicle), which is typical for polyploid rice.
Ключевые слова: Oryza sativa, андрогенез in vitro, каллус, Key words: Oryza sativa, androgenesis in vitro, callus, tetraploid
тетраплоид
Полиплоидия сыграла важнейшую роль в эволюции
[11]. Перевод гибридов риса O. sativa с диплоидного
растений и селекции культурных видов [1, 2]. Множе-
уровня на тетраплоидный путем обработки колхи-
ство полиплоидов успешно используют в сельскохо-
цином способствует формированию остистых форм
зяйственном производстве и цветоводстве, так как они
растений, даже если исходная форма была безостой.
обеспечивают более высокий урожай и декоративные
Длина остей зависит от наличия их у исходного гибри-
качества в сравнении с диплоидными видами [2, 3].
да [6]. Культура пыльников in vitro также обеспечива-
Рис Oryza sativa L. - широко распространенная дипло-
ла получение остистых тетраплоидных регенерантов
идная культура (основное число хромосом 2n=24), ко-
риса из безостых растений сорта Каскад [10]. Открыта
торую выращивают на пяти континентах, крупой риса
полиплоидная мейотическая стабильность (Polyploidy
питается половина человечества [4]. Полиплоидный,
meiosis stability - PmeS), различающаяся у тетраплоид-
в частности тетраплоидный рис, рассматривают как
ных линий, что ведет к дифференциации показателей
один из источников увеличения урожайности данного
фертильности пыльцы и завязываемости семян от 37
вида [5-7]. Тетраплоидный рис впервые был получен в
до 80% [8]. Получен нео-тетраплоидный рис, кото-
1933 г. и с 1953 г. в Китае включен в селекционный про-
рый при скрещивании с тетраплоидным дает высо-
цесс [8]. Однако из-за низкой фертильности пыльцы,
кую фертильность. Методом секвенирования выявили
обусловленной отклонениями от нормального мейоти-
большую изменчивость ДНК и дифференциально экс-
ческого деления клеток [9], на метелках формируется
прессирующиеся гены в стадии мейоза у трех нео-те-
небольшое число семян [8, 10]. Поэтому коммерческо-
траплоидных линий по сравнению с родителями [12].
го применения тетраплоидный рис пока не нашел [7].
Увеличение числа бивалентов приводит к повышению
Современные исследования тетраплоидного риса
семенной продуктивности, а фертильность 2n-пыльцы
немногочисленны. Изучена генетическая и морфоло-
маскируется нейтральными генами. Определено, что
гическая изменчивость O. sativa с использованием 99
мейоз-связанные гены и мейоз-специфические гены
SSR маркеров и агрономических признаков. Оказа-
также отвечают за метаболизм сахаров и синтез крах-
лось, что изменчивость тетраплоидного риса выше,
мала и экспрессируются у гибридов полиплоидного и
чем диплоидного, и получен гетерозисный эффект от
нео-тетраплоидного риса в течение различных стадий
межподвидовой гибридизации полиплоидного риса
развития [7].
14
Российская сельскохозяйственная наука, 2020, № 3
Андрогенез in vitro успешно применяют в селекции
шт. (1,9%) были тетраплоидами. Каллусные агрегаты
риса для получения гомозиготных линий удвоенных
одной каллусной линии имеют разную регенерацион-
гаплоидов [13]. В качестве побочного материала об-
ную способность: в отдельных случаях регенерации не
разуются также гаплоиды, триплоиды, тетраплоиды,
происходит, на других каллусных агрегатах существу-
пентаплоиды, анеуплоиды [14, 15]. Доля тетраплоид-
ет морфогенетический ответ [19]. Различия закономер-
ных регенерантов в культуре пыльников составляет
ны, так как каждая недозрелая микроспора пыльника
0,9-16,0% в зависимости от протокола исследования
может дать начало каллусу [17]. В связи с этим даль-
[14, 16]. Известно, что 17,4% каллусов, полученных
нейшие расчеты проводили в среднем на каллусный
в культуре пыльников риса, в конце первого пассажа
агрегат.
имеют тетраплоидные клетки, доля которых может
Тетраплоиды образовались на 16 каллусных агрега-
увеличиваться при более длительном пассировании
тах 9 гибридов (табл.), 5 из них не имели регенерантов
[17]. Однако, не все генетические и геномные наруше-
без семян. Формирование тетраплоидов шло на кал-
ния, которые накапливаются в культуре in vitro на кле-
лусных агрегатах 1-го, 2-го и 4-го порядка. Также бес-
точном уровне, могут пройти через этап морфогенеза и
семянные регенеранты встречались на каллусных агре-
не всегда можно получить регенеранты и их потомство
гатах любого порядка. С бессемянными растениями
[18]. Упоминаний об особенностях формирования по-
образовалось 25 каллусов, в 44% случаев регенерация
липлоидных растений или о дальнейшем селекцион-
заканчивалась тетраплоидией. Корреляции между чис-
ном применении тетраплоидов, полученных в андроге-
ленностью тетраплоидных и бессемянных растений на
незе in vitro риса, в литературе не обнаружено. Целью
каллусе не выявлено. Доля каллусов с тетраплоидами
исследования было изучение особенностей каллусных
составляла 17,6%, что совпадает с данными С. Сhen
линий в культуре пыльников in vitro риса, на которых
and С. Chen [17], у которых 17,4% всех каллусов обра-
формируются тетраплоидные растения, и характери-
зовали тетраплоидные клетки.
стика тетраплоидных регенерантов риса.
Большинство каллусов с тетраплоидами не имело
Методика. Исследования проведены на гибридах
гаплоидов (9 шт.), 5 каллусных агрегатов образовали
F2 риса Oryza sativa L. подвида japonica Kato сле-
один или два гаплоида, и только на двух морфогене-
дующих гибридных комбинаций: Романика×(Дарий
тический ответ проявился во множественной гаплои-
122×Краснодар 9167) - Р×Д×67; Дон 4237×(Зарваси
дии - 17 и 121 гаплоид/каллус. Три каллуса с тетра-
70× Хейлудзян) - Д×З×Х; Китаец×(ВНИИР 3223×Кен-
плоидами были без удвоенных гаплоидов, на других
зо) - К×23×К. Использовано по пять растений каждой
каллусных агрегатах сформировались 3-93 удвоенных
гибридной комбинации. Исходные растения выращи-
гаплоидов. Каллусы, где представлены исключительно
вали на вегетационной площадке в сосудах до периода
тетраплоиды, отсутствовали.
сбора метелок. Методики холодовой обработки пыль-
Провели сравнительную характеристику всех кал-
ников, культивирования пыльников, каллусов и регене-
лусных агрегатов и каллусов с тетраплоидами (рис.),
рантов в условиях in vitro приведены ранее [19].
из анализа исключили каллусный агрегат с 121 гапло-
Под термином «каллусная линия» понимали все
идом как нетипичный. На каллусах с тетраплоидами
каллусные агрегаты, сформированные на одном пыль-
было на порядок меньше гаплоидов, чем в среднем на
нике. Каллусные агрегаты (каллусы) размером 2-5 мм
всех каллусных агрегатах (при p=0,05), а число бессе-
пересаживали из индукционной питательной среды на
мянных растений - больше в 2 раза (при р=0,02). Стати-
регенерационную с интервалом в семь дней с присво-
стически значимых различий по удвоенным гаплоидам
ением порядкового номера. Зеленые регенеранты R0 с
и погибшим растениям не выявлено, по тетраплоидам
развитой корневой системой высаживали в горшечную
подтверждены (р=0,0001). При использовании в рас-
культуру и продолжали выращивать в условиях куль-
четах всех 16 каллусных агрегатов с тетраплоидами
туральной комнаты. Все регенеранты разделяли на
сохранялась тенденция уменьшения среднего числа га-
пять групп по морфологическим признакам: гаплои-
ды (стерильные растения с очень мелкими цветками);
удвоенные гаплоиды (растения с семенами); тетрапло-
иды (растения с очень крупными немногочисленны-
ми семенами, выраженным килем и ребристостью на
цветочной чешуе); растения без семян (формировали
цветки нормального или большего размера, но не об-
разовывали семена на двух и более метелках); расте-
ния, погибшие на ранних этапах роста и развития. При
сравнении с данными по содержанию ядерной ДНК в
регенерантах риса ошибка отнесения растений к соот-
ветствующей группе составляла 4,5% [14].
Статистические расчеты (средние значения призна-
ков, ошибка средней, коэффицинт корреляции, t-крите-
рий Сьюдента) проведены с использованием програм-
мы Statistica.
Результаты и обсуждение. В культуру in vitro было
введено 2700 пыльников. Каллусообразование соста-
вило 6,04%. Образовалось 65 каллусных линий с зеле-
ными регенерантами 12 гибридных растений; 21 кал-
лусная линия сформировала по несколько каллусных
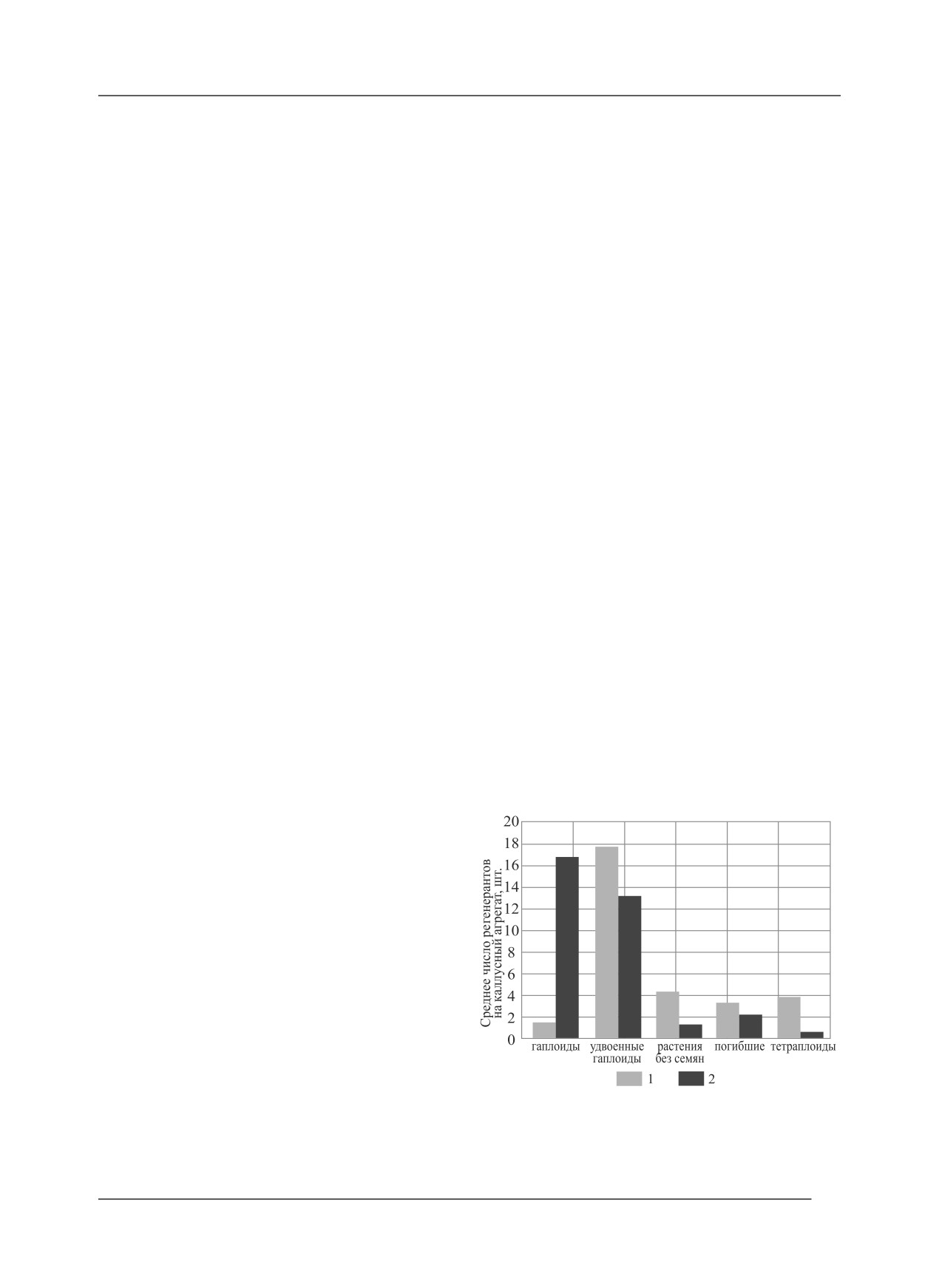
Сравнительная характеристика регенерационной
агрегатов: 12 линий по 2 каллуса, 4 линии с тремя и
способности каллусных агрегатов риса, полученных
четырьмя каллусными агрегатами и одна линия с пя-
в андрогенезе in vitro:
тью каллусными агрегатами. В эксперименте получено
1 - каллусные агрегаты с тетраплоидами (15 шт.),
2 - все каллусные агрегаты в эксперименте (91 шт.).
3115 зеленых регенерантов с 91 каллусом, из них 59
15
Российская сельскохозяйственная наука, 2020, № 3
Характеристика семенной продуктивности тетрапло-
каллусов риса O. sativa (74%) в кон-
идных растений, полученных в андрогенезе in vitro
це первого пассажа миксоплоидна:
различные сочетания одно-, двух-,
Гибрид
Каллусный
Число
Максимальное
Среднее
Стандартная
четырех- и восьмиядерных клеток
агрегат
тетраплоид-
число семян
число семян
ошибка
[17]. Доказано одноклеточное проис-
ных расте-
главной
главной ме-
средней
ний, шт.
метелки, шт.
телки, шт.
хождение гаплоидов в андрогенезе
Р×Д×67 (1)
62.2.1
3
6
4,0
1,0
in vitro у пшеницы [24]. Каллусы, не-
сущие четырехядерные клетки, могут
62.2.4
2
8
6,0
2,0
стать основоположниками тетрапло-
Р×Д×67 (2)
109.2.1
5
4
2,2
0,6
идов. Но не каждая клетка в условиях
in vitro даст начало новому растению,
Д×З×Х (1)
193.2.1
2
1
1,0
0,0
только часть генетических изменений
реализуется у растений-регенеран-
Д×З×Х (2)
161.2.1
3
5
4,5
0,5
тов [18]. Вероятно, по этой причине
Д×З×Х (3)
128.2.1
1
5
5
-
несколько меньшее число каллусных
агрегатов в эксперименте (57%) име-
Д×З×Х (4)
117.2.1
12
13
5,8
1,4
ло сочетание регенерантов различной
118.2.1
1
1
1
-
плоидности (гаплоиды и удвоенные
гаплоиды, удвоенные гаплоиды и те-
Д×З×Х (5)
59.2.1
4
7
3,0
1,4
траплоиды, 3 типа регенерантов вме-
сте).
60.2.2
1
4
4
-
Спонтанное удвоение хромосом
72.1.1
1
10
10
-
клеток в культуре пыльников in vitro
88.2.2
9
11
5,3
1,0
идет за счет слияния ядер и эндоми-
тозов [15, 17, 23], в том числе и крат-
97.1.1
1
3
3
-
ное увеличение плоидности более
высоких порядков
[17]. Формиро-
К×23×К (1)
80.2.2
4
8
5,3
1,3
вание триплоидных клеток каллуса
80.2.4
8
9
4,4
0,8
возможно за счет слияния низкопло-
идных клеток или редукции имею-
К×23×К (2)
112.2.2
2
2
1,5
0,5
щихся хромосом у тетраплоидов [17].
Преобладание каллусных агрегатов с
плоидов/каллус: их было в 2 раза меньше, чем в сред-
бессемянными растениями и общего их числа над те-
нем на всех каллусах, но без достоверных различий.
траплоидами прежде всего свидетельствует о слиянии
У бессемянных растений, полученных в андрогене-
гаплоидных и дигаплоидных клеток, что привело к сте-
зе in vitro, отмечена высокая вариабельность по содер-
рильности регенерантов.
жанию ядерной ДНК, выявленной методом проточной
У растений 2n гаметы могут образовываться с очень
цитометрии. У них обнаружено содержание ДНК, ха-
высокой частотой - до 14-36%, что ведет к формиро-
рактерное для растений с двойным набором хромосом,
ванию полиплоидов в естественных условиях [25] и
триплоидов, тетраплоидов и пентаплоидов, вероятно,
дигаплоидов в андрогенезе in vitro [23]. В более ред-
среди них встречались неуплоиды, что не позволило
ких случаях в результате аномального цитокинеза об-
им дать семенное потомство [14]. Формирование те-
разуются 3n и 4n пыльцевые материнские клетки [25].
траплоидов и бессемянных растений сопровождалось
Это также может объяснить происхождение три- и
увеличением погибших растений: в среднем на всех
тетраплоидов в культуре пыльников in vitro [15]. Тем
каллусах - на 1,32 шт., на каллусах с тетраплоидами
не менее спонтанное удвоение хромосом считаем ли-
и регенерантами без семян (всего 31 каллусный агре-
дирующим фактором изменения плоидности клеток в
гат) - в среднем на 3,87 шт. (различия статистически
андрогенезе in vitro. Выявлена слабая отрицательная
значимы при р=0,008). В андрогенезе in vitro растения,
корреляция (r= - 0,3 при р=0,05) между числом преоб-
в генотипе которых содержится много леталей, полуле-
ладающих регенерантов на каллусе и их плоидностью.
талей и субвиталей, погибают на ранних стадиях раз-
Это означает, что с увеличением числа хромосом в
вития. Выживают только те особи, которым в результа-
клетках, которые перед этим прошли слияние ядер или
те мейоза не досталось «вредных» генов или их было
эндомитоз, уменьшается число регенерантов соответ-
очень мало [20]. В нашем случае погибло в среднем
ствующей плоидности. Поэтому тетраплоидов на кал-
1,32 растений/каллус. Увеличение этого показателя в
лусе формируется относительно немного (до 12 шт.),
3 раза возможно связано не только с комплексом генов
значительно больше удвоенных гаплоидов - до 125 шт.,
погибших растений, но и с хромосомными изменения-
а максимальное число гаплоидов на каллусе составляет
ми, которые при благоприятных перестройках реали-
346 растений [26]. Поддержание и размножение гапло-
зовались в тетраплоидные регенеранты.
идных клеток в культуре in vitro идет быстрее и легче,
Причины формирования гаплоидных и дигапло-
чем клеток с иным набором хромосом, поскольку они
идных растений в андргенезе in vitro в значительной
обладают значительной устойчивостью и конкуренто-
степени изучены. У риса регенерация идет через кал-
способностью к полиплоидным, двуядерным и анеу-
лусогенез, на ранних стадиях деления клеток они спон-
плоидным клеткам. Это обеспечивается, вероятно, бы-
танно удваиваются [15], что приводит к формированию
стрым делением клеток, более коротким митотическим
до 72-95% дигаплоидов от всех зеленых регенерантов
циклом, быстрой элиминацией или дифференциацией
[21,22]. Интенсивность этого процесса зависит от ге-
поврежденных клеток [27].
нотипа растения-донора [21,22] и условий культиви-
На каллусном агрегате может сформироваться до 12
рования исходных растений, каллусов и регенерантов
тетраплоидных растений (табл.) и до 26 бессемянных рас-
in vitro [23]. Известно, что большая часть андрогенных
тений. Регенеранты, полученные в андрогенезе in vitro,
16
Российская сельскохозяйственная наука, 2020, № 3
имеют низкую озерненность метелки: в среднем до
swquecing and transcriptome analysis reveal rich DNA
6,0 шт., максимум - 13 семян, что согласуется с лите-
vatiations and differential expressions of fertility-related
ратурными данными о низкой озерненности метелок
genes in neo-tetraploid rice // PloS ONE. - 2019. - Vol.
тетраплоидного риса [5] и результатами наших опытов,
14, №4. - 23 p.
полученных на других гибридах и сорте Каскад в ан-
13. Mishra R., Rao G.J.N. In-vitro androgenesis in rice:
adventages, constraints and future prospects. // Rice
дрогенезе in vitro [10]. Культура тканей in vitro в целом
Scienc. - 2016. - 23(2). - P.57-68.
ведет к высокой стерильности полученных регенеран-
14. Илюшко М.В., Скапцов М.В., Ромашова М.В. Содер-
тов [28]. Снижение семенной продуктивности при по-
жание ядерной ДНК в регенерантах риса, полученных
вышении уровня плоидности встречается на многих
в культуре пыльников in vitro // Сельскохозяйственная
культурах, и опыт показывает, что последующим отбо-
биология. - 2018. - Т. 53. - №3. - С. 531-538.
ром возможно увеличить фертильность [3], в том числе
15. D`Amato F. Cytogenetics of plant cell and tissue cultures
у риса, на 70% [5, 6]. Выращивание регенерантов, сле-
and their regenerates // Critical Reviews in Plants
дующих за поколением R0, также позволяет значитель-
Sciences. - 1985. - Vol. 3, № 1. - P. 73-112.
но снизить стерильность пыльцы [29].
16. Mishra R., Rao G.J.N., Rao R.N., Kaushal P. Development
Таким образом, в андрогенезе in vitro полиплоиды
and characterization of elite doubled haploid lines from
формируются на регулярной основе. Этот метод можно
two Indica rice hybrids // Rice Science. - 2015. - 22(6).
рассматривать как один из эффективных для получе-
- P.290-299.
ния тетраплоидных растений для селекции риса. Пути
17. Chen C.C., Chen C.-M. Changes in chromosome number
формирования тетраплоидов на каллусах требуют до-
in microspore callus of rice during successive subculrures
полнительного изучения.
// Can. J. Genet. Cytol. - 1980. - Vol. 22. - P. 607-614.
18. Кузнецова О.И., Аш О.А., Харитонов Г.А., Гостим-
Литература.
ский С.А. Исследование растений-регенерантов
1. Stebbins G.L. Variation and evolution in plants: progress
гороха (Pisum sativum L.) с помощью молекулярных
during the past twenty years // Essays in evolution and
RAPD- и ISSR-маркеров // Генетика. - 2005. - Т. 41. -
genetics in honor of Theodosius Dobzhansky / M.K.
№1. - С. 71-77.
Hecht, C.S. William (ed.). - Springer, US, 1970. - Ch.
19. Илюшко М.В., Ромашова М.В. Регенерационная спо-
6. - P. 173-208.
собность каллусных трансплантантов риса в куль-
2. Жученко А.А. Адаптивная селекция растений (эколо-
туре пыльников in vitro // Аграрный вестник Примо-
го-генетические основы) : монография в 2-х т. - М. :
рья. - 2018. - № 1 (9). - С. 5-8.
Изд-во РУДН, 2001. Т. II. - 708 с.
20. Гончарова Ю.К. Использование метода культуры
3. Хафетов Э.Б., Щербак В.С. Автополиплоидия - как
пыльников в селекции риса. - Краснодар: ВНИИ
эффективный механизм в селекции сельскохозяй-
риса, 2012. - 91 с.
ственых растений // Международные научные ис-
21. Datta S.K. Androgenic haploids: factors controlling
следования. - 2016. - Т. 8. - № 3. - С. 281-284.
development and its ap-plication in crop improvement.
4. Ляховкин А.Г. Рис. Мировое производство и гено-
// Current Science. - 2005. - 89(11). - P.1870-1878.
фонд. - СПб.: «Профи-информ», 2005. - 288 с.
22. Сартбаева И.А., Усенбеков Б.Н., Рысбекова А.Б.,
5. Tu S., Luan L., Liu Y., Long W., Kong F., He T., Xu Q.,
Мухина Ж.М., Казкеев Д.Т., Жамбакин К.Ж., Жан-
Yan W., Yu M. Production and heterosis analysis of rice
дырбаев Е.А., Беркимбай Х.А., Ахметова Д.Ш., Мел-
autotetraploid hybrids // Crop Science. - 2007. - Vol.
дебекова А.А. Получение дигаплоидных линий для се-
47. - P. 2356-2363.
лекции глютинозного риса // Биотехнология. - 2018.
6. Song Z.-J., Du C.-Q., Zhang X.-H., Chen D.-L., He Y.-
- Т. 34. - № 2. - С. 26-36.
C., Cai D-T. Studies on awns in polyploidy rice (Oryza
23. Segui-Simarro J.M., Nuez F. Pathways to doubled
sativa L.) and preliminary cross experiments of a special
haploidy: chromosome doubling during androgenesis //
awnlew tetraploid rice // Genet. Resour. Crop. Evol. -
Cytogenetics and Plant Breeding. - 2008. - Vol. 120. - P.
2014. - Vol. 61, № 4. - P. 797-807.
358-369.
7. Chen L., Yuan Y., Wu J., Chen Z., Wang L., Shahid
24. Сельдимирова О.А, Круглова Н.Н. Андроклинный эм-
M.Q., Liu X. Carbohydrate metabolism and fertility
бриогенез in vitro злаков // Успехи современной биоло-
related genes high expression levels promote heterosis
гии. - 2014. - Т. 134. - №5. - С. 476-487.
in autotetraploid rice harboring double neutral genes //
25. Цаценко Л.В., Мосунов С.А. Гаметы с соматическим
Rice. - 2019. - Vol. 12. - 34 p.
числом хромосом: механизмы их формирования и
8. He Y., Ge J., Wei Q., A.-M., Gan L., Song Z.-J.,Cai D.-T.
роль в эволюции автополиплоидных растений (обзор
Jiang. Using a polyploidy meiosis stability (PMeS) line
иностранной литературы) // Сельскохозяйственная
as a parent improves embryo development and the seed
биология. - 2008. - № 1. - С. 16-25.
set rate of a tetraploid rice hybrid // Canadian Journal
26. Илюшко М.В. Регенерационный максимум в адроген-
of Plant Sciences. - 2011. - Vol. 91. - P. 325-335.
ных каллусных линиях риса Oryza sativa L. in vitro //
9. Luan L., Wang X., Long W.B., Liu Y.H., Tu S.B., Xiao X.Y.,
Рисоводство. - 2019. - №2 (43). - С. 29-32.
Kong F.L. A comparative cytogenetic study of the rice
27. Тырнов В.С., Давоян Н.И. Цитогенетика соматиче-
(Oryza sativa L.) autotetraploid restorers and hybrids //
ских тканей гаплоидов / Глава в книге Гаплоидия и
Генетика. - 2009. - Т. 4. - № 9. - С. 1225-1233.
селекция - М.: Наука, 1976. - С. 57-65.
10. Илюшко М.В., Ромашова М.В., Гученко С.С. Тетра-
28. Давоян Э.И. Мутагенез в культуре ткани риса и по-
плоидный рис в культуре пыльников in vitro // Дальне-
лучение на его основе нового исходного материала //
восточный аграрный вестник. - 2018. - №3(47). - С.
Генетика. - 1983. - Т. XIX. - №10. - С. 1714-1719.
18-25.
29. Гостимский С.А., Багрова А.М., Ежова Т.А. Обна-
11. Wu J., Hu C., Shahid M., Guo H.-B., Zeng Y.-X., Liu X.-
ружение и цитогенетический анализ изменчивости,
D. Analysis on genetic diversification and heterosis in
возникающей при регенерации растений из культу-
autotetraploid rice // SpringerPlus. - 2013. - Vol. 2. - 12 p.
ры тканей посевного гороха // Доклады академии
12. Bei X., Shahid M.Q., Wu J., Chen Z., Wang L., Liu X. Re-
наук. - 1985. - Т. 283. - № 4. - С. 1007-1011.
Поступила в редакцию 26.11.19
После доработки 05.12.19
Принята к публикации 15.01.20
17