Химия твердого топлива, 2019, № 2, стр. 23-29
ЗАВИСИМОСТЬ РЕАКЦИОННОЙ СПОСОБНОСТИ ОТ СТРУКТУРНЫХ И ФИЗИКО-ХИМИЧЕСКИХ ХАРАКТЕРИСТИК СОСТАВЛЯЮЩИХ ТЯЖЕЛЫХ ВЫСОКОВЯЗКИХ НЕФТЕЙ
А. Л. Лапидус 1, А. М. Гюльмалиев 2, *, О. Ю. Полетаева 3, **, Г. Ю. Колчина 3, ***, С. Н. Гусейнова 3, ****, Э. М. Мовсумзаде 3, *****
1 ФГБУН Институт органической химии имени Н.Д. Зелинского РАН
119991 Москва, Россия
2 ФГБУН Институт нефтехимического синтеза имени А.В. Топчиева РАН
119991 Москва, Россия
3 ФГБОУ ВО Уфимский государственный нефтяной технический университет
450062 Уфа, Россия
* E-mail: gyulmaliev@ips.ac.ru
** E-mail: ol612@mail.ru
*** E-mail: kolchina.gyu@mail.ru
**** E-mail: guseynovas@yandex.ru
***** E-mail: eldarmm@yahoo.com
Поступила в редакцию 07.03.2018
После доработки 15.08.2018
Принята к публикации 24.10.2018
Аннотация
Проведен квантово-химический анализ растворимости высокомолекулярных компонентов тяжелой нефти, содержащей ароматические и парафиновые фрагменты, а также гетероатомы N, О и S. Получены результаты расчетов теплот образования ΔН298 модельных соединений и их комплексов по методу РМЗ, калиброванному по тестовым молекулам. Показано, что димеры макромолекул, содержащие алкильные группы, а также гетероатомы, более устойчивы и лучше сольватируются в гептане, чем в бензоле. Между свободными энергиями сольватации модельных соединений в бензоле и гептане имеется линейная зависимость. Согласно термодинамическим расчетам равновесного состава реакции, между донором и акцептором водорода возможно образование новых сложных структур.
В связи с истощением запасов нефти в настоящее время ее переработка в основном направлена на разработку новых технологических процессов получения синтетической нефти с помощью гидрогенизационной переработки угля, сланцев и биомассы, а также гидроконверсии тяжелых нефтей и нефтяных остатков. Вследствие высокой плотности и высокодисперсности тяжелых нефтей при их транспортировке и переработке для снижения вязкости используют смесь двух или нескольких нефтей различного состава. Нефть является многокомпонентной, высокодисперсной и термодинамически нестабильной системой с отличающимися локальными плотностями. Из-за неустойчивости структур и свойств дисперсных систем в условиях транспортировки и переработки фазовый состав смеси нефтей может претерпевать существенные изменения.
Компоненты дисперсной системы отличаются по элементному составу, плотности и надмолекулярными образованиями. В такой системе за счет энергий межмолекулярных взаимодействий формируется фазовый состав, приводящий к межфазным взаимодействиям, – адгезии. В результате нескомпенсированности поверхностных энергий в конденсированных фазах молекулы, находящиеся на поверхности фаз, обладают большей энергией, чем молекулы в объеме. Процессы идут самопроизвольно – разрушаются существующие и образовываются новые фазы до тех пор, пока их химические потенциалы не станут равны. Следовательно, неустойчивость состава нефти обусловлена самопроизвольно идущими процессами: растворением и осаждением макрокомпонентов.
Асфальтены и смолы – высокомолекулярные компоненты тяжелой нефти с полиароматической структурой и температурой кипения выше 500°С [1–4]. При наличии в системе растворителей (бензола, толуола и т.д.) асфальтены с плотностью около 1.1 г/см3 растворяются, а при наличии осадителей (гексана, гептана и т.д.) – осаждаются. Следовательно, в нефти различные соединения могут выступать как в качестве растворителей, так и осадителей.
Углеводородный состав нефти в основном состоит из трех классов соединений: парафиновых, нафтеновых и ароматических [2]. Стабильность нефти зависит от соотношения этих трех структурных составляющих. Нефть с большим содержанием ароматических структур более стабильна из-за их низкой реакционной способности. Асфальтены состоят из конденсированных ароматических колец и алкильных заместителей с длиной цепи до С30. Гетероатомы N, О, S находятся в определенных положениях: азот связан в виде пиррола и пиридина, сера – в виде бензтиофеновых колец, меркаптанов, тиоэфиров и кислород – в виде кетонов, фенолов, карбоновых кислот [5].
В настоящее время предлагаются многочисленные структурные модели асфальтенов и смол и на их основе – методы описания свойств [1], но сложность структуры и простота применяемых расчетных методов не позволяют на количественном уровне оценить их свойства. По этой же причине отсутствуют достоверные экспериментальные данные, что интерпретация их структурных особенностей приводит к малоубедительным, а иногда к противоречивым выводам.
Основными факторами, которые могут привести к структурным изменениям при мягких условиях смешивания при транспортировке и переработке нефти, являются различие в элементных и фракционных составах нефтей, а также наличие соединений, выступающих в качестве растворителей и осадителей.
В работе был проведен теоретический анализ растворимости высокомолекулярных компонентов нефти при их сольватации в гептане и бензоле, которые присутствуют в бензиновой фракции.
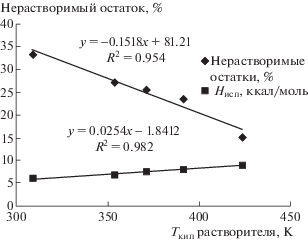
Рассмотрим эмпирические зависимости растворимости асфальтенов от физико-химических параметров растворителей. В табл. 1 приведены экспериментальные данные по нерастворимым остаткам асфальтенов в различных растворителях [1]. На рис. 1 представлены зависимости нерастворимых остатков от температуры кипения растворителей Ткип и их теплоты испарения ΔНv. Как следует из рис. 1, с ростом температуры кипения растворителя количество нерастворимых остатков линейно уменьшается. Поскольку теплота испарения коррелирует с температурой кипения, то и в случае зависимости нерастворенных остатков от теплоты испарения имеется линейная зависимость. Приведенные примеры показывают, что различие в растворимости компонентов нефти, естественно, является следствием структурных особенностей, как самих компонентов, так и растворителей. Но эта зависимость не простая, например чем больше разветвлен парафиновый углеводород, тем выше его растворяющая способность [6]. Однако, с другой стороны, с ростом разветвленности парафинов температура кипения уменьшается. Следует отметить, что теория растворимости органических макромолекул пока мало изучена. Различные подходы к расчету растворимости изложены в работе [7]. В работе [8] предложен метод выбора структурных параметров органических молекул произвольной структуры, которые могут быть использованы для полуэмпирического описания их растворимости в различных растворителях.
Таблица 1.
Свойства некоторых растворителей и растворимость в них асфальтена
| Растворитель | Ткип, К [9] | ΔНv, ккал/моль [9] | Нерастворимый остаток, % |
|---|---|---|---|
| н-Пентан | 309.22 | 6.16 | 33.5 |
| Изооктан | 390.8 | 8.08 | 32.2 |
| 2,2,3-Триметилбутан | 354.02 | 6.918 | 27.2 |
| н-Гептан | 371.58 | 7.575 | 25.7 |
| 3-Метилгептан | 392.07 | 8.1 | 23.6 |
| н-Нонан | 423.96 | 9.03 | 15.1 |
| 1,3-Диметилциклопентан | 364.87 | 7.361 | 0 |
| Метилциклогексан | 374.08 | 7.58 | 0 |
| Этилциклогексан | 404.93 | 8.29 | 0 |
| Циклогексан | 353.88 | 7.19 | 0 |
| Бензол | 353.25 | 7.353 | 0 |
Рис. 1.
Зависимости нерастворимых остатков асфальтенов от физико-химических показателей растворителей: температуры кипения и теплоты испарения.
Сольватация является следствием межмолекулярных взаимодействий в растворителях и растворенных веществах. Обозначим молекулу растворителя Р, растворенного вещества В и реакцию сольватацию запишем в следующем виде:
По формуле (1) можно вычислить энергию сольватации, если принять энергию взаимодействия двух молекул растворителя Е(Р–Р), двух молекул растворенного вещества Е(В–В) и молекулы растворителя с молекулой растворенного вещества Е(P – В). Тогда
Учитывая, что энергии взаимодействия величины отрицательные, реакция сольватации возможна при ΔЕ < 0.
Энергия межмолекулярных взаимодействий (ЭМВ) соединений зависит от их состава, строения и молекулярной массы. Следовательно, у различных классов соединений ЭМВ будут зависеть только от их строения. Рассмотрим этот вопрос более подробно на модельных соединениях. В качестве их энергетических характеристик можно использовать теплоты образования в стандартных условиях ΔН298. Для расчета теплоты образования модельных соединений использовали квантово-химический метод РМЗ [10]. Для повышения точности расчета энергетических характеристик соединений провели калибровку метода по линейному уравнению (3), используя экспериментальные значения теплоты образования тестовых молекул
(3)
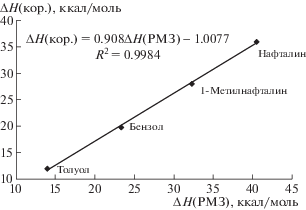
$\Delta {{Н }_{{298}}}({\text{к о р }}{\text{.}}) = n[\Delta {{Н }_{{298}}}({\text{Р М 3}})] + m.$Коэффициенты n и m определяли корреляцией экспериментальных значений теплоты образования ΔН298 (эксп.) с расчетными данными ΔН298 (РМЗ) молекул (ккал/моль): бензола (19.82), толуола (11.95), нафталина (36.08) и 1-метилнафталина (27.93) [9]. Зависимость представлена на рис. 2.
Результаты расчетов теплоты образования при стандартных условиях тестовых молекул приведены в табл. 2, из которой следует, что корреляционное уравнение (3) удовлетворительно воспроизводит литературные данные по ΔН298 [9]. Тестированный метод применяли для расчета энергетических характеристик ряда соединений и их комплексов, моделирующих структурные фрагменты макромолекул нефти. В табл. 2 приведены вычисленные по уравнению (3) ΔН298 для модельных соединений.
Таблица 2.
Результаты расчета теплоты образования соединений при стандартных условиях по корреляционному уравнению (3) и методу РМЗ
| Соединение | ΔН298, ккал/моль | |
|---|---|---|
| по уравнению (1) * | по методу РМЗ | |
| Бензол (С6Н6) | 20.14 (19.82) | 23.29 |
| Толуол (С6Н5СН3) | 11.62 (11.95) | 13.91 |
| Нафталин (C10H8) | 35.69 (36.08) | 40.42 |
| 1-Метилнафталин (С10Н7СН3) | 28.32 (27.93) | 32.30 |
| Декан (С10Н22) | –57.3 (–59.67) | –62.00 |
| Пирен (С16Н10) | 56.90 | 63.77 |
| Тетрадекан (С14Н30) | –77.13 (–79.38) | –83.84 |
| Коронен (С24Н12) | 77.95 | 86.96 |
| Ди-пирен. 2(C16H10) | 115.15 | 127.93 |
| Ди-коронен. 2(С10Н12) | 157.63 | 174.71 |
| Тетра-коронен. 4(С24Н12) | 316.22 | 349.37 |
| Модель -I (С28Н34) | –2.13 | –1.24 |
| Модель-II (C27NH33) | 4.32 | 5.87 |
| Модель-III (C54N2H66) | –15.71 | –16.19 |
| Модель-IV (C29N2H32SO3) | –63.60 | –68.93 |
| Модель-V (C58N4H64S206) | –130.28 | –142.37 |
* В скобках приведены данные из [9].
По данным табл. 2, вычисленным по уравнению (3), найдены энтальпии образования молекулярных комплексов (рис. 3):
Рис. 3.
Структура модельных соединений: I – C28H34, II – C27NH33, III – C54N2H66, IV – C29N2H32SO3, V – C58N4H64S2O6.
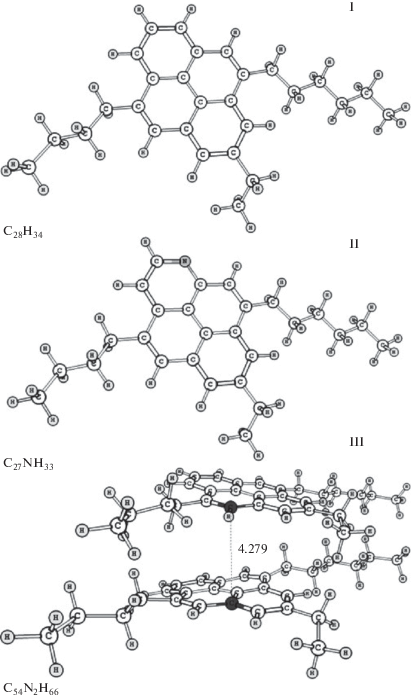
Рис. 3.
Окончание
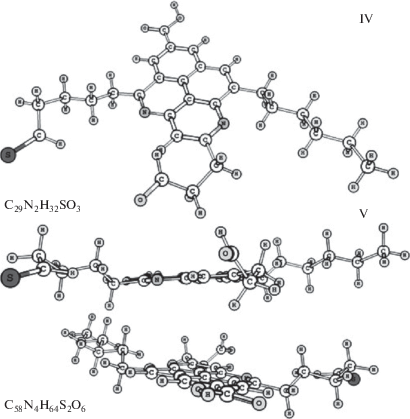
Пирен + Пирен = Ди-Пирен. ΔН298 = = 1.35 ккал/моль.
Коронен + Коронен = Ди-Коронен. ΔН298 = = 1.73 ккал/моль.
Ди-Коронен + Ди-Коронен = Тетра-Коронен. ΔН298 = 4.42 ккал/моль.
Модель-II + Модель-II = Модель-III. ΔН298 = = –7.07 ккал/моль.
Модель-IV + Модель-IV = Модель-V. ΔН298 = = –3.08 ккал/моль.
Приведенные данные показывают, что реакции образования димеров пирена и коронена, а также тетрамера коронена эндотермичны, но реакции образования больших молекул, содержащих ароматические и алкильные группы, а также гетероатомы, экзотермичны.
Квантово-химическое моделирование энергии растворимости асфальтенов в органических растворителях – гептане и бензоле. Взаимосвязь растворимости и сольватации растворителя и растворенного вещества следует из уравнений (1), (2). Энергию сольватации соединений представленных в табл. 2, в гептане и бензоле оценили квантово-химическим методом. При расчете энергии сольватации отдельных классов органических соединений в различных органических средах часто используют “модель поляризованного континуума” (РСМ). В этой модели расчеты выполняются как для вакуума, так и с учетом растворителя [10]. Растворитель представляется как континуум, обладающий определенными значениями диэлектрической проницаемости и поляризуемости. В модели РСМ энергия сольватации рассчитывается как сумма трех вкладов:
где Ecav – кавитационная энергия, т.е. энергия образования полости в растворителе, где помещается молекула растворенного соединения; Eel – энергия электростатического взаимодействия между собственными и наведенными зарядами растворенного соединения и молекулами растворителя; Edisp – дисперсионная составляющая энергии взаимодействия, учитывающая ван-дер-ваальсовское взаимодействие.В модели РСМ молекулярная свободная энергия вычисляется как сумма трех членов:
где es – электростатические, dr – дисперсионно-отталкивающие вклады в свободную энергию, cav – энергия кавитации (каверны).Можно показать, что полная свободная энергия сольватации Gsol равна сумме электростатического и неэлектростатического вкладов.
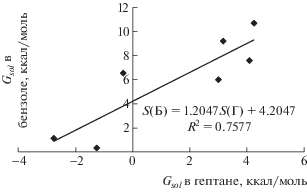
Результаты расчетов по методу HF/6-31g(d) представлены в табл. 3, из которой видно, что по величине свободной энергии Гиббса все рассмотренные молекулы лучше сольватируются в гептане, чем в бензоле; энергия кавитации в гептане меньше, чем в бензоле, а дипольный момент в бензоле незначительно больше; дисперсионная энергия в случае гептана больше, чем в бензоле. Следовательно, рассмотренные вещества лучше должны растворяться в гептане, чем в бензоле. С другой стороны, согласно рис. 4, энергия сольватации модельных соединений в бензоле коррелирует с энергией сольватации в гептане. Отметим, что, согласно предложенной в [11] модели строения асфальтенов, выпадение их в осадок гептаном объясняется тем, что смолы, которые хорошо растворяются в гептане, выступают в роли поверхностно-активного вещества для асфальтенов. Далее, после растворения смол в гептане, асфальтены выпадают в осадок, что свидетельствует о сложных самопроизвольных процессах в нефти [12].
Таблица 3.
Параметры сольватации структур I и II, вычисленные по методу HF/6-31g(d) [10]
| Соединение | Сольватация | |||||||
|---|---|---|---|---|---|---|---|---|
| в гептане | в бензоле | |||||||
| Gsol | Gcav | Gdr | μ | Gsol | Gcav | Gdr | μ | |
| ккал/моль | Дебай | ккал/моль | Дебай | |||||
| Гептан | 2.98 | 18.39 | –17.12 | 0.136 | 5.98 | 21.84 | –18.88 | 0.137 |
| Бензол | –1.28 | 10.55 | –12.02 | 0.001 | 0.29 | 12.62 | –13.33 | 0.001 |
| Коронен | –2.77 | 27.19 | –30.14 | 0.001 | 1.11 | 32.65 | –33.35 | 0.001 |
| Модель I – (С28Н34) | 4.25 | 44.99 | –42.47 | 0.573 | 10.77 | 53.55 | –47.23 | 0.584 |
| Модель II–(C27NH33) | 3.15 | 44.40 | –42.40 | 3.344 | 9.24 | 52.95 | –46.99 | 3.469 |
| Модель IV–(C29N2Н32SO3) | –0.34 | 51.05 | –49.73 | 7.743 | 6.55 | 61.05 | –55.37 | 7.914 |
| Дигексил | 4.06 | 24.08 | –21.97 | 0.0 | 7.60 | 28.58 | –24.48 | 0.0 |
Рис. 4.
Зависимость энергии сольватации модельных соединений в гептане от энергии сольватации их в бензоле.
Реакции диспропорционирования водорода. В нефти между гидроароматическими и ароматическими фрагментами возможны реакции передачи водорода от донора к акцептору [12]. На рис. 5 приведены модельные гидроароматические и ароматические соединения.
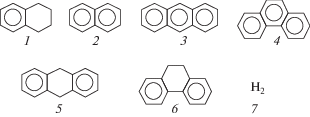
Рис. 5.
Ароматические молекулы и их гидропроизводные: 1 – тетралин (С10Н12), 2 – нафталин (С10Н8), 3 – антрацен (С14Н10), 4 – фенантрен (С14Н10), 5 – 9,10-дигидроантрацен (С14Н12), 6 – 9,10-дигидрофенантрен (С14Н12), 7 – водород.
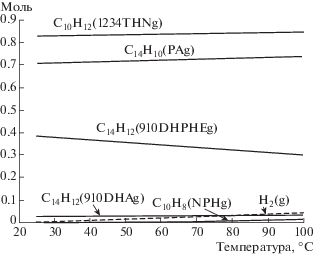
Методами химической термодинамики [13] при давлении Р = 0.1 МПа вычислена температурная зависимость равновесного числа молей компонентов по схеме:
Тетралин + Антрацен → {Тетралин, Нафталин, Антрацен, Фенантрен. 9,10-Дигидроантрацен, 9,10-Дигидрофенантрен, Водород}.
Результаты расчета представлены на рис. 6, из которого видно, что с ростом температуры равновесная концентрация тетралина и фенантрена увеличивается, а 9,10-дигидрофенантрена – падает. Видно, что в присутствии водородо-донорных и водородо-акцепторных фрагментов возможно протекание сложных реакций передачи водорода от донора к акцептору.
Таким образом, результаты квантово-химических расчетов энергии межмолекулярных взаимодействий модельных соединений, состоящих из парафиновых и ароматических фрагментов, показывают, что димеры макромолекул, содержащие алкильные группы, более устойчивы и лучше сольватируются в гептане, чем в бензоле, при этом растворимости в бензоле и гептане имеют линейную зависимость. Согласно термодинамическим расчетам равновесного состава реакции, между донором и акцептором водорода возможны образования новых структур. Сделан вывод о том, что смешивание нефтей при транспортировке может привести к реакциям сольватации, растворения и диспропорционирования водорода, а также к существенным структурным изменениям.
Список литературы
Большая энциклопедия нефти и газа. http://www.e-reading.mobi/chapter.php/1006958/15/Sklyarov-Sensacionnaya_istoriya_Zemli.html
Горбунова Л.В., Филимонова Т.А., Камьянова В.Ф. Химический состав высших ногонов нефтей и нефтяных остатков. М.: ЦНИИТЭнефтехим, 1986. 96 с.
Dekkers C., Daan R. // Oil and Gas. 1999. V. 97. № 9. P. 41.
Movsumzade E.M., Poletaeva O.Yu., Kolchina G.Yu., Leontev A.Yu. // DGMK Tagungsbericht. 2017. P. 227.
Сафиева Р.З. Физикохимия нефти. Физико-химические основы технологии переработки нефти. М.: Химия, 1998. 448 с.
Шкаликов Н.В., Васильев С.Г., Скирда В.Д. // Коллоидный журн. 2010. Т. 72. № 1. С. 120.
Аскадский А.А., Матвеев Ю.И. Химическое строение и физические свойства полимеров. М.: Химия, 1983. 248 с.
Яркова Т.А., Гюльмалиев А.М. // ХТТ. 2018. № 2. С. 17.
Сталл Д., Вестрам Э., Зинке Г. Химическая термодинамика органических соединений. М.: Мир, 1971. 807 с.
Granovsky A.A. GAMESS. V. 7.1. http://classic.chem.msu. su/gran/gamess/index.html
Сафиева Р.З. Химия нефти и газа. Нефтяные дисперсные системы: состав и свойства. Ч. 1. Учебное пособие. М.: РГУ нефти и газа имени И.М. Губкина, 2004. 112 с.
Гюльмалиев А.М., Головин Г.С., Гладун Т.Г. Теоретические основы химии угля. М.: Изд-во МГГУ, 2003. 556 с.
HSC Chemistry 6. http://www.hsclchemistry.net/
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива