Расплавы, 2021, № 6, стр. 601-604
Термодинамические свойства растворов серебра в калии
В. М. Ивенко a, *, В. Ю. Шишкин a
a Институт высокотемпературной электрохимии УрО РАН
Екатеринбург, Россия
* E-mail: Ivenko@ihte.uran.ru
Поступила в редакцию 10.06.2021
После доработки 19.06.2021
Принята к публикации 12.07.2021
Аннотация
Используя данные по растворимости серебра в калии и уравнение Шредера, были получены значения коэффициентов активности серебра и парциальная энтальпия смешения серебра и его парциальная избыточная энтропия.
Растворимость металлов в жидких щелочных металлах изучена недостаточно. Это вызвано как заметной агрессивностью щелочных металлов, так и их летучестью, что требует подбора материалов невзаимодействующих с щелочными и с исследуемыми металлами, и изготовления герметичных, находящихся в изотермических условиях, приборов [1]. В настоящее время для растворов серебра в калии кроме нашей работы по растворимости серебра [2], имеется работа по растворимости многих металлов в жидких щелочных металлах при одной температуре – 873 К [3], значение растворимости из которой для этой температуры совпадают с нашими данными [2]. Имеется работа А. Пелтона [4], который предположил растворимость Ag в К, равной 1 мол. % серебра при температуре плавления серебра. По нашим данным для температуры меньше температуры плавления на 31°С растворимость серебра больше 8 мол. %. Также имеется в литературе (построенная по данным А. Пелтона в программе FactSage 8.1) фазовая диаграмма Ag–K [5]. Кроме фазовой диаграммы программа FactSage 8.1 рассчитывает и термодинамические характеристики растворов.
Нами для расчета термодинамических функций растворенного серебра было использовано уравнение Шредера [6], используемое Козиным Л.Ф. для нахождения термодинамических функций растворов металлов в ртути. Уравнение выведено для идеальных растворов в предположении независимости энтальпии плавления растворяемого металла от температуры.
(1)
${\text{ln}}{{N}_{{{\text{Ag}}}}} = {{\Delta {{H}_{{{\text{пл}}}}}_{{{\text{Ag}}}}} \mathord{\left/ {\vphantom {{\Delta {{H}_{{{\text{пл}}}}}_{{{\text{Ag}}}}} {R \cdot ({1 \mathord{\left/ {\vphantom {1 {{{T}_{{{\text{пл}}}}}_{{{\text{Ag}}}}}}} \right. \kern-0em} {{{T}_{{{\text{пл}}}}}_{{{\text{Ag}}}}}} - {1 \mathord{\left/ {\vphantom {1 T}} \right. \kern-0em} T})}}} \right. \kern-0em} {R \cdot ({1 \mathord{\left/ {\vphantom {1 {{{T}_{{{\text{пл}}}}}_{{{\text{Ag}}}}}}} \right. \kern-0em} {{{T}_{{{\text{пл}}}}}_{{{\text{Ag}}}}}} - {1 \mathord{\left/ {\vphantom {1 T}} \right. \kern-0em} T})}}.$В уравнение Шредера для идеальной растворимости серебра входят две константы, взятые из работы [7]. ∆HплAg = 11 296 Дж/моль, TплAg = 1234.93 К и универсальная газовая постоянная R = 8.31441 Дж/(моль · К).
Данные по растворимости серебра в калии из работы [2] и данные, рассчитанные по уравнению Шредера, приведены в табл. 1. Там же приведены значения коэффициентов активности серебра, рассчитанные как отношения значений растворимости в идеальных растворах к значениям растворимости в реальных растворах.
(2)
${{N}_{{{\text{Ag}}}}}{\text{ид}}{\text{.}}{{{\text{р}}{\kern 1pt} {\text{ - }}{\kern 1pt} {\text{р}}} \mathord{\left/ {\vphantom {{{\text{р}}{\kern 1pt} {\text{ - }}{\kern 1pt} {\text{р}}} {{{N}_{{{\text{Ag}}}}}}}} \right. \kern-0em} {{{N}_{{{\text{Ag}}}}}}} = {{y}_{{{\text{Ag}}}}}.$Таблица 1.
Значения растворимости серебра в калии из работы [2] и рассчитанная по уравнению Шредера
| T, C | NAg (мол. доля) |
ln(NAg) | Т, К | 1/Т | ln(NAg) ид. р-р | NAg ид. р-р | yAg | ln(yAg) |
|---|---|---|---|---|---|---|---|---|
| 500 | 0.00695 | –4.9697 | 773.16 | 0.001293 | –0.657122 | 0.5183 | 74.64 | 4.31261 |
| 550 | 0.00896 | –4.7145 | 823.16 | 0.001215 | –0.550376 | 0.5767 | 64.34 | 4.16413 |
| 600 | 0.01285 | –4.3547 | 873.16 | 0.001145 | –0.455856 | 0.6339 | 49.35 | 3.89887 |
| 650 | 0.01859 | –3.9851 | 923.16 | 0.001083 | –0.371575 | 0.6896 | 37.10 | 3.61354 |
| 700 | 0.02620 | –3.6421 | 973.16 | 0.001028 | –0.295955 | 0.7438 | 28.39 | 3.34616 |
| 750 | 0.03567 | –3.3336 | 1023.16 | 0.000977 | –0.227725 | 0.7963 | 22.33 | 3.10583 |
| 800 | 0.04700 | –3.0577 | 1073.16 | 0.000932 | –0.165853 | 0.8472 | 18.03 | 2.89180 |
| 850 | 0.06019 | –2.8102 | 1123.16 | 0.00089 | –0.109490 | 0.8963 | 14.89 | 2.70072 |
| 900 | 0.07525 | –2.5870 | 1173.16 | 0.000852 | –0.057931 | 0.9437 | 12.54 | 2.52902 |
| 930 | 0.08518 | –2.4630 | 1203.16 | 0.000831 | –0.029052 | 0.9714 | 11.40 | 2.43397 |
| 961.8 | 0.09643 | –2.3389 | 1234.96 | 0.00081 | 0.000027 | 1.0000 | 10.37 | 2.33894 |
Вид зависимостей идеальной и экспериментальной растворимости серебра в калии от температуры показан на рис. 1. Видно, что в идеальном растворе серебра растворяется больше. Рассчитанные по ур. (2) значения коэффициента активности серебра логарифмировали и получали зависимость логарифма коэффициента активности серебра от температуры.
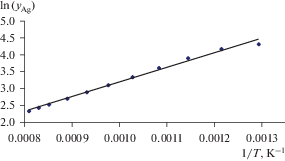
Из рис. 2 видно, что наиболее сильно отличаются от аппроксимирующей прямой значения коэффициента активности серебра при низких температурах.
Значения логарифма коэффициента активности серебра от температуры можно аппроксимировать следующим уравнением:
(3)
${\text{ln(}}y{\text{Ag)}} = 4322.6 \cdot {1 \mathord{\left/ {\vphantom {1 Т}} \right. \kern-0em} Т} - 1.1327{\text{ }}\cdot{{R}^{2}} = 0.9924.$Коэффициент активности серебра связан с парциальными избыточными термодинамическими функциями следующим образом:
(4)
$\Delta {{\bar {G}}_{{{\text{изб}}{\kern 1pt} {\text{Ag}}}}} = R \cdot T \cdot {\text{ln}}{{y}_{{{\text{Ag}}}}} = \Delta {{\bar {H}}_{{{\text{Ag}}}}} - T \cdot \Delta {{\bar {S}}_{{{\text{изб}}{\kern 1pt} {\text{Ag}}}}},$(5)
${\text{ln}}{{y}_{{{\text{Ag}}}}} = {{\Delta {{{\bar {H}}}_{{{\text{Ag}}}}}} \mathord{\left/ {\vphantom {{\Delta {{{\bar {H}}}_{{{\text{Ag}}}}}} {(R \cdot T)}}} \right. \kern-0em} {(R \cdot T)}} - {{\Delta {{{\bar {S}}}_{{{\text{изб}}{\kern 1pt} {\text{Ag}}}}}} \mathord{\left/ {\vphantom {{\Delta {{{\bar {S}}}_{{{\text{изб}}{\kern 1pt} {\text{Ag}}}}}} R}} \right. \kern-0em} R}.$Используя ур. (3) и (5), можно рассчитать $\Delta {{\bar {H}}_{{{\text{Ag}}}}}$ и $\Delta {{\bar {S}}_{{{\text{изб}}{\kern 1pt} {\text{Ag}}}}}$. Они соответственно равны: $\Delta {{\bar {H}}_{{{\text{Ag}}}}}$ = 35 941 Дж/моль и $\Delta {{\bar {S}}_{{{\text{изб}}{\kern 1pt} {\text{Ag}}}}}$ = 9.4186 Дж/(моль · К).
ВЫВОДЫ
Используя экспериментальные данные по растворимости серебра в калии и уравнение Шредера для этих растворов, были рассчитаны коэффициенты активности серебра.
Получено аппроксимирующее уравнение для температурной зависимости коэффициента активности серебра.
Используя уравнение Шредера, были рассчитаны парциальная энтальпия смешения серебра и парциальная избыточная энтропия серебра.
Список литературы
Ивенко В.М. Исследование взаимодействия серебра и меди с расплавами K–KCl и K–KI // Расплавы. 2008. № 6. С. 32–39.
Ивенко В.М., Шишкин В.Ю. Растворимость твердого серебра в жидком калии // Расплавы. 2020. № 2. С. 205–207.
Borgstedl H.U., Guminski C. Solubilities and Solutions Chemistry in Liguid Alkali Metals // Monatshefte fur Chemie. 2000. 131. P. 917–930.
Pelton A.D. The Ag–K (Silver–Potassium) System // Bulletin of Alloy Phase Diagrams. 1986. 7. № 3. P. 223.
FactSage 8.1. https://www.factsage.com/.
Козин Л.Ф. Амальгамная пирометаллургия. Алма-ата: Наука Казахской ССР, 1973.
Barin I. Thermochemical Data of Pure Substances. VCH Verlags Gesellschaft, Weinheim. 1995.
Дополнительные материалы отсутствуют.