Расплавы, 2022, № 3, стр. 291-300
Коррозия меди в расплаве фторидов лития, натрия, калия, содержащем фториды актинидов либо их имитаторы
Э. А. Карфидов a, b, Е. В. Никитина a, b, *, Ю. П. Зайков a, b, К. Е. Селиверстов a, b, П. Н. Мушников a, b
a Уральский федеральный университет
Екатеринбург, Россия
b Институт высокотемпературной электрохимии УрО РАН
Екатеринбург, Россия
* E-mail: neekeetina@mail.ru
Поступила в редакцию 24.12.2021
После доработки 15.01.2022
Принята к публикации 30.01.2022
- EDN: VNJEHD
- DOI: 10.31857/S0235010622030033
Аннотация
Расплавленные галогениды щелочных металлов, особенно фториды, являются чрезвычайно агрессивной коррозионной средой. Инженерная реализация жидкосолевого реактора (ЖСР) существенно зависит от того, насколько успешно может быть решена проблема подбора и создания соответствующих конструкционных материалов. Материалов, устойчивых в этих средах, до сих пор не создано, и актуальными становятся другие способы защиты конструкционных элементов высокотемпературных технологических устройств. Способы защиты от коррозии в расплавленных солях немногочисленны, как в силу внешних факторов коррозии (температура, радиация), так и внутренних – возможности фазовых переходов, модифицирования и деградации материалов при высоких температурах). В представленной работе коррозионное поведение меди (М1) было изучено в расплаве фторидов лития, натрия, калия, содержащем добавки фторидов неодима, церия в качестве имитаторов фторидов актинидов и фторида урана от 0 до 5 мас. % в атмосфере аргона высокой чистоты при 550 и 800°С в течение 100 ч. Гравиметрия, энергодисперсионный анализ поверхности и шлифов поперечного сечения образцов были использованы для оценки коррозионной стойкости меди. Представлены зависимости скорости коррозии материала от температуры и концентрации добавок фторидов имитаторов актинидов и фторида урана. Представлена морфология поверхности и шлифа поперечного сечения в зависимости от состава расплава. По совокупности данных гравиметрического анализа, атомно-абсорбционного и микрорентгеноспектрального методов исследования установлено, что медь проявляет себя как материал, устойчивый во фторидах лития, натрия, калия.
ВВЕДЕНИЕ
Успешное использование расплавленных фторидов щелочных металлов требует создания таких реакторных материалов, которые обладают высокой коррозионной стойкостью в расплавах с характерными для жидкосолевого реактора (ЖСР-С) составами [1–9]. Коррозия является одной из важнейших нерешенных проблем, при этом также чрезвычайно важны конструкционные характеристики используемых материалов, которые, помимо прочности, также должны легко обрабатываться, подвергаться сварке для получения изделий достаточно сложной конфигурации и быть устойчивыми в широком температурном диапазоне и при радиационном воздействии.
Инженерная реализация ЖСР существенно зависит от того, насколько успешно может быть решена проблема подбора и создания соответствующих конструкционных материалов [10–23]. И поскольку подбор сплава с идеальным составом практически невозможен, помимо легирования необходимо использовать и другие способы защиты от коррозии.
Исследование индивидуальных фторидов актинидов и их смесей можно заменить исследованиями близких по физико-химическим, термодинамическим и другим свойствам аналогов – лантанидов. Известно [24], что имитаторами фторидов актинидов –плутония и урана, америция являются фториды церия и неодима.
Целью исследований является исследование механизма процесса коррозии меди [25], анализ коррозионных характеристик процесса взаимодействия в системе медь–фторидный расплав солей щелочных металлов, содержащий добавки соединений f-элементов (фторидов урана, неодима, церия как имитатора фторида плутония). В перспективе предполагается изучение стойкости нанесенных медных высокотехнологичных покрытий на конструкционные материалы в расплавах фторидов щелочных металлов.
Неоспоримо электрохимический механизм коррозии в расплавленных солях принципиально отличается от коррозионного разрушения в низкотемпературных средах [26–29]. Способы защиты от коррозии в расплавленных солях немногочисленны, как в силу внешних факторов коррозии (температура, радиация), так и внутренних – возможности фазовых переходов, модифицирования и деградации материалов при высоких температурах).
Один из эффективных способов снижения коррозионных потерь – создание на поверхности материала слоя, защищающего металл от коррозионного воздействия окружающей среды.
Защитный слой может быть как металлическим, так и из неорганического материала, химически стойкого в данной агрессивной среде.
Достаточно сложно создать пассивирующий слой продуктов коррозии, обладающий хорошей адгезией к основе, непосредственно во фторидном расплаве. Целесообразно рассмотреть возможность покрытия кандидатных материалов металлами, обладающими высокой химической стойкостью во фторидных расплавах, но неприемлемыми в чистом виде по прочностным и другим механическим свойствам.
При рассмотрении коррозионных свойств кандидатных материалов в расплаве фторидов лития, натрия, калия в первую очередь надо сфокусировать внимание на коррозионно-электрохимическом поведении основных компонентов конструкционных материалов и их бинарных сплавов для уточнения состава и структуры образующихся продуктов коррозии.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ. МАТЕРИАЛЫ И МЕТОДЫ
Исследовано коррозионное поведение металлической меди при взаимодействии с эвтектическим солевым расплавом KF–LiF–NaF, содержащем фториды актиноидов либо их имитаторы.
Исследования проводились в перчаточном боксе, в котором постоянно поддерживалась инертная атмосфера аргона с влажностью не более 2 ppm и содержанием кислорода 2–9 ppm. Коррозионные испытания проводились в запатентованной экспериментальной установке, рис. 1. Данная установка предполагает возможность пробоотбора электролита в течение коррозионных испытаний, а также поддержание требуемой температуры в рабочей зоне нагрева с образцами с погрешностью ≤1°С, за счет присутствия в непосредственной близости к тиглю платино-платинородиевой термопары. Регулирование температуры осуществлялось посредством терморегулятора Варта ТП 703.
Рис. 1.
Конструкция используемой в перчаточном боксе сборной установки для изучения высокотемпературной коррозии: 1, 2, 3 – трубы различной высоты диаметром 52 мм; 4 – поперечные теплоотражающие диски; 5 – шпили с резьбой М6; 6 – нижняя платформа; 7 – втулки с внутренней резьбой М6; 8 – тарельчатые шайбы; 9 – конструктивная крышка с двумя отверстиями; 10 – конструктивные крышки с одним отверстием.

Расплав фторидов щелочных металлов предварительно очищали электролизом, используя графитовые стрежни в качестве электродов, в токе кислорода. После коррозионной выдержки готовили шлифы и травили полученную поверхность 50% раствором азотной кислоты.
Испытания образцов исследуемых материалов осуществляли в параллели по 5 образцов. Предварительно материалы нарезали на образцы, равные по размерам, обрабатывались шлифовальной бумагой различной зернистости.
После этого образцы промывали, обезжиривали, сушили. После стадии сушки образцы незамедлительно отправлялись в бокс на хранение, для избегания формирования на поверхности оксидного слоя под действием окислительной атмосферы воздуха.
Также производили замер габаритных размеров для последующего расчета площади контакта материала с расплавленным солевым электролитом цифровым штангенциркулем, производилось многократное взвешивание образцов.
Исследуемые образцы были аттестованы на соответствие структуры и состава заявленным по ГОСТ с помощью методов микрорентгеноспектрального, рентгенофазового и металлографического анализа.
После эксперимента образцы отмывали от остатка фторидных солей в термостате с перемешиванием горячим раствором борной кислоты (температура – 80°С, время отмывки – 90 мин, концентрация в пересчете на ортоборную кислоту 5 мас. %. Данная промывочная жидкость оптимальна по составу и концентрации с учетом температурной зависимости растворимости фторидов и позволяет избежать дополнительного коррозионного воздействия на материалы, ранее контактировавшие с расплавленными фторидами. При выборе оптимальной методики рассматривались также такие варианты растворителей как дистиллированная вода (фторид натрия практически не растворим) и раствор фторида аммония при кипячении (образование дополнительных нерастворимых продуктов), отмывка хлоридным расплавом с последующей отмывкой в воде (оказание чужеродного влияния на коррозию в расплавленных фторидах), нагрев образца под вакуумом (наличие местной коррозии, образование в ходе взаимодействия с фторидным расплавом подповерхностных пустот делало неприемлемым данный метод), таким образом, был выбран единый оптимальный режим отмывки изучаемых образцов различных металлических материалов.
Изменение морфологии образцов в результате коррозионной выдержки фиксировалось с помощью метода микрорентгеноспектрального анализа. Металлографический анализ осуществлялся как на поверхности образцов, так и на поперечном сечении (шлиф поперечного сечения).
Образцы меди марки “М00б” представляли собой бруски с прямоугольным сечением длиной от 6.12 до 6.76 мм, шириной от 4.10 до 4.12 мм и толщиной от 2.35 до 2.37 мм.
По совокупности данных гравиметрического анализа, атомно-абсорбционного и микрорентгеноспектрального методов исследования, можно сделать вывод, что медь является наиболее стойким материалом при температуре 550°С в расплаве FLiNaK. В связи с этим было решено провести 100-часовые испытания этого материала, перспективного для создания защитного металлического покрытия, в диапазоне температур 550–800°С в расплаве FLiNaK, содержащем добавки фторидов урана, неодима и церия как имитатора трифторида плутония (1 и 5 мас. %).
В табл. 1 представлены скорости коррозии меди марки М1, рассчитанные по данным гравиметрических измерений.
Таблица 1.
Скорость коррозии медных образцов выдержанных в расплаве фторидов щелочных металлов с различными добавками, г/м2 ч
| Исследуемый фторидный солевой расплав | Температура, °С | ||
|---|---|---|---|
| 550 | 650 | 800 | |
| FLiNaK | 0.177 ± 0.009 | 0.201 ± 0.010 | 0.269 ± 0.013 |
| FLiNaK + 1% UF4 | 0.209 ± 0.010 | 0.244 ± 0.012 | 0.327 ± 0.016 |
| FLiNaK + 5% UF4 | 0.278 ± 0.014 | 0.370 ± 0.019 | 0.537 ± 0.027 |
| FLiNaK + 1% СеF3 | 0.237 ± 0.012 | 0.301 ± 0.015 | 0.359 ± 0.018 |
| FLiNaK + 5% СеF3 | 0.283 ± 0.014 | 0.364 ± 0.018 | 0.540 ± 0.027 |
| FLiNaK + 1% NdF3 | 0.203 ± 0.010 | 0.230 ± 0.012 | 0.279 ± 0.014 |
| FLiNaK + 5% NdF3 | 0.247 ± 0.012 | 0.309 ± 0.015 | 0.434 ± 0.022 |
На рис. 2–7 представлены данные микрорентгеноспектрального анализа образцов меди после коррозионных испытаний в зависимости от температуры и состава расплава.
Рис. 2.
Образцы меди, выдержанные в расплаве FLiNaK при температуре 550°С. а – Поверхность; б – шлиф поперечного сечения.

Рис. 3.
Образцы меди, выдержанные в расплаве FLiNaK + 1% UF4 при температуре 550°С. а – Поверхность; б – шлиф поперечного сечения.

Рис. 4.
Образцы меди, выдержанные в расплаве FLiNaK + 5% UF4 при температуре 550°С. а – Поверхность; б – шлиф поперечного сечения.
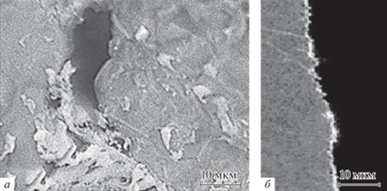
Рис. 5.
Образцы меди, выдержанные в расплаве FLiNaK при температуре 800°С. а – Поверхность; б – шлиф поперечного сечения.

Рис. 6.
Образцы меди, выдержанные в расплаве FLiNaK + 1% UF4 при температуре 800°С. а – Поверхность; б – шлиф поперечного сечения.

Рис. 7.
Образцы меди, выдержанные в расплаве FLiNaK + 5% UF4 при температуре 800°С. а – Поверхность; б – шлиф поперечного сечения.

Рис. 8.
Образцы меди, выдержанные в расплаве FLiNaK + 5% CeF3 при температуре 550°С. а – Поверхность; б – шлиф поперечного сечения.

Рис. 9.
Образцы меди, выдержанные в расплаве FLiNaK + 5% NdF3 при температуре 550°С. а – Поверхность; б – шлиф поперечного сечения.
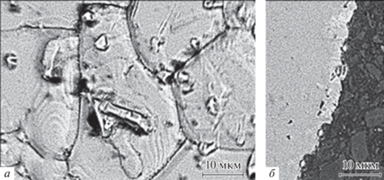
По данным микрорентгеноспектрального анализа поверхности и металлографического исследования шлифов поперечного сечения медных образцов можно сделать вывод, что введение добавок фторидов f-элементов приводит к возникновению незначительной межкристаллитной коррозии, наиболее отчетливо наблюдаемой при введении в исследуемый расплав фторида церия. В целом, морфология меди практически не подверглась каким-либо значительным изменениям в ходе 100 часовой выдержки. Глубина коррозионных очагов не превышает 2.1–3.4 мкм (5.0–6.8 мкм при добавке фторида церия). Повышение температуры несколько увеличивает скорость коррозии. Другими словами, медь демонстрирует значительную коррозионную стойкость в исследуемых крайне агрессивных условиях.
Исследование выполнено при финансовой поддержке РФФИ и Госкорпорации “Росатом” в рамках научного проекта № 20-011-70 001.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 20-21-00022.
Список литературы
LeBlanc D. Molten salt reactors: A new beginning for an old idea // Nucl. Eng. Des. 2010. 240. P. 1644–1656.
Комаров В.Е., Смоленский В.В., Афоничкин В.К. Перспективы использования расплавов солей в радиохимических технологиях // Расплавы. 2000. № 2. С. 59–65.
Khokhlov V., Ignatiev V., Afonichkin V. // J. Fluor. Chem. 2009. 130. P. 30–37. https://doi.org/10.1016/j.jfluchem.2008.07.018
Ignatiev V.V., Kormilitsyn M.V., Kormilitsyna L. Molten-salt reactor for nuclear fuel cycle closure on all actinides // At. Energy. 2018. 125. P. 251–255.
Ignatiev V., Feynberg O., Gnidoi I., Merzlyakov A. Molten salt actinide recycler and transforming system without and with Th-U support: Fuel cycle flexibility and key material properties // Ann. Nucl. Energy. 2014. 64. P. 408–420.
Ponomarev L.I., Belonogov M.N., Volkov I.A., Simonenko V.A., Sheremet’eva U.F. LiF–NaF–KF eutectic based fast molten-salt reactor as Np, Am, Cm transmuter // At. Energy. 2019. 126. P. 139–149.
Ignat’ev V.V., Feinberg O.S., Smirnov V.P., Vanyukova G.V., Lopatkin A.V. Analysis of the fuel-loop characteristics of a molten-salt nuclear reactor with a cavity core // At. Energy. 2019. 126. P. 156–162.
Dolan T.J. Molten salt reactors and thorium energy // Woodhead Publishing: Sawston, Cambridge, USA, 2017. 1. P. 452–540.
Sridharan K., Allen T.R.R. Corrosion in molten salts // Elsevier Inc.: Amsterdam, 2013. 1. P. 241–267.
Ignatiev V., Surenkov A. 5–corrosion phenomena induced by molten salts in Generation IV nuclear reactors // Struct. Mater. Gener. IV Nucl. React. 2017. 1. P. 153–189.
Raiman S.S., Sangkeun L. Aggregation and data analysis of corrosion studies in molten chloride and fluoride salts // J. Nucl. Mater. 2018. 511. P. 523–535.
Guo S., Zhang J., Wub W., Zhou W. Corrosion in the molten fluoride and chloride salts and materials development for nuclear applications // Prog. Mater. Sci. 2018. 97. P. 448–487.
Wang Y., Zhang S., Ji X., Wang P., Li W. Material corrosion in molten fluoride salts // Int. J. Electrochem. Sci. 2018. 13. P. 4891–4900.
Wagner C. The formation of thin oxide films on metals // Corros. Sci. 1973. 13. P. 23–52.
Young D.J. High Temperature oxidation and corrosion of metals // Elsevier Science: Oxford, UK, 2016. P. 320–355.
Azhazha V.M., Andriiko A.A., Bakai A.S., Volkov S.V., Devyatkin S.V., Dovbnya A.N., Lavrienenko S.D., Omelchuk A.A., Shirokov B.M. Corrosion of irradiated Ni-Mo alloys in sodium fluoride-zirconium fluoride melt // Quest. Atom. Sci. Tech. 2005. 3. P. 134–139.
Бакай А.С., Чечкин А.В., Жук В.В. Механические, физические, коррозионные и радиационные свойства сплавов типа Хастеллой Н в расплавах фторидных солей: Обзор. Харьков: ННЦ ХФТИ, 2005.
Serp J., Allibert M., Beneš O., Delpech S., Feynberg O., Ghetta V., Heuer D., Holcomb D., Ignatiev V., Kloosterman J.L. The molten salt reactor (MSR) in generation IV: Overview and perspectives // Prog. Nucl. Energy. 2014. 77. P. 308–319.
Williams D.F. Assessment of candidate molten salt coolants for the advanced high-temperature reactor (AHTR) // Ridge National Laboratory, Oak Ridge, TN, USA: 2006.
Hogerton J.F. Reactor Handbook: Materials // Technical Information Service, U.S. Atomic Energy Commission, Geneva, 1955.
Manly W.D., Coobs J.H., DeVan J.H., Douglas D.A., Inui H., Patriarca P., Roche T., Scott J. Metallurgical problems in molten fluoride system // Nucl. Fuel React. Mater. 1959. 6. P. 36–52.
Manly W.D., Adamson G.M., Coobs J.H., DeVan J.H., Douglas D.A., Hoffman E.E., Patriarca P. Aircraft reactor experiment-metallurgical aspects // Ridge National Laboratory, Oak Ridge, TN, USA, 1957.
Ignatiev V., Surenkov A., Gnidoi I., Fedulov V., Uglov V., Afonichkin V., Bovet A., Subbotin V., Panov A., Toropov A. Compatibility of selected Ni-based alloys in molten Li,Na,Be/F Salts with PuF3 and tellurium additions // Nucl. Technol. 2008. 164. P. 130–142.
Lizin A.A., Tomilin S.V., Gnevashov O.E., Gazizov R.K., Osipenko A.G., Kormilitsyn M.V., Baranov A.A., Zaharova L.V., Naumov V.S., Ponomarev L.L. PuF3, AmF3, CeF3 and NdF3 solubility in LiF–NaF–KF melt // At. Energy. 2013. 115. P. 11–17.
Басоло Ф., Пирсон Р. Механизмы неорганических реакций. М.: Изд-во “Мир”, 1971.
Шрайвер Д., Эткинс П. Неорганическая химия. М.: Мир, 2004. 1. С. 645–648.
Третьяков Ю.Д. Неорганическая химия. Том 3. Химия переходных элементов. М.: Академия, 2007. С. 230–242.
Кузнецов С.А., Кузнецова С.В., Глаголевская А.Л. Каталитическое саморастворение меди в расплаве эквимольной смеси NaCl–KCl, содержащей комплексы тугоплавких металлов // Расплавы. 1994. № 3. С. 38–47.
Karfidov E., Nikitina E. Corrosion behavior of candidate functional materials for molten salts reactors in LiF–NaF–KF containing actinide fluoride imitators // Materials. 2022. 15. № 3. P. 761.
Ерженков М.В., Борисов Г.В., Зайков Ю.П., Никитина Е.В., Дедюхин А.Е., Карфидов Э.А. Патент на изобретение № 2 021 108 248 “Установка для определения скорости коррозии материалов в расплавленных солях”. 29.03.21.
Дополнительные материалы отсутствуют.


