Расплавы, 2022, № 3, стр. 276-290
Изотермические и политермические сечения системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}$
З. Н. Вердиева a, А. В. Бурчаков b, *, А. Б. Алхасов a, Н. Н. Вердиев a, c, **, И. М. Кондратюк b
a Институт проблем геотермии и возобновляемой энергетики –
филиал Объединенного института высоких температур РАН
Махачкала, Россия
b Самарский государственный технический университет
Самара, Россия
c Дагестанский государственный университет
Махачкала, Россия
* E-mail: turnik27@yandex.ru
** E-mail: verdiev55@mail.ru
Поступила в редакцию 13.12.2021
После доработки 23.01.2022
Принята к публикации 25.01.2022
- EDN: FUEKQS
- DOI: 10.31857/S0235010622030112
Аннотация
На основе данных о составах и температурах плавления двух- и трехкомпонентных эвтектик, сформирована пространственная модель фазового комплекса трехкомпонентной системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}$ в программе КОМПАС 3D. Модель построена в координатах “состав–температура”, в основании которого лежит треугольник составов системы, по оси аппликата отложена температура в диапазоне 500–800°С. Структура модели предполагает использование понятия “базовый геометрический элемент фазовой области” для понимания геометрического строения пространственной диаграммы, где каждая фазовая область является локальным объемом с ограниченными поверхностями. На основе модели получены изотермы поверхности ликвидуса, изотермические и политермические сечения, рассчитан материальный баланс равновесных фаз для произвольно выбранных фигуративных точек системы. Показана возможность расчета материального баланса произвольно выбранной фигуративной точки равновесно сосуществующих фаз при заданной температуре и в интервале температур, основываясь на геометрии построенной 3D модели исследуемой системы. Соотношения равновесных фаз рассчитаны с использованием уравнений математических матриц. 3D модели многокомпонентных систем (МКС), построенные на основе информации об элементах меньшей мерности, позволяют определить принадлежность нонвариантного состава к соответствующему симплексу без проведения эксперимента. При исследовании поверхности ликвидуса многокомпонентной системы, ограничиваются выявлением нонвариантных составов, кристаллизующиеся при более низких температурах, чем исходные ингредиенты. Однако, для многих технологических процессов необходим интервал температур. Наличие 3D модели и T–x–y диаграммы состояния МКС позволяет с помощью изотермических и политермических сечений выбрать заданный интервал температур. Предлагаемый подход в отличие от традиционных методов проще и нагляднее, что делает возможным его широкое применение в физико-химическом анализе МКС.
ВВЕДЕНИЕ
Одним из направлений современного материаловедения является исследование фазовых равновесий многокомпонентных систем (МКС), с целью дальнейшей разработки материалов с регламентируемыми свойствами. Энергоемкие солевые эвтектические смеси востребованы в возобновляемой энергетике, их используют в качестве теплонакопителей и теплоносителей в устройствах, аккумулирующих тепловую энергию, в ядерной энергетике, для поддержания температурного режима химических процессов [1–7]. Основой подбора солевых смесей для химико-технологических процессов являются диаграммы состояния. При исследовании МКС наряду с экспериментальными методами применяются расчетные методы, пакеты программ, позволяющие ограничить область проведения эксперимента [8–11]. В последние годы используют компьютерное моделирование, позволяющее оптимизировать планирование эксперимента, формировать изотермические, политермические сечения, выполнять виртуальный эксперимент с прогнозом температур фазовых переходов и фазового состава произвольно выбранной фигуративной точки системы [12–19].
Целью настоящей работы является моделирование фазового комплекса трехкомпонентной системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}~$ в программе КОМПАС 3D в координатах “состав– температура” на базе данных о составах и температурах кристаллизации двух- и трехкомпонентных эвтектик.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Данные о нонвариантных составах двух- и трехкомпонентной систем послужили основой для построения 3D компьютерной модели трехкомпонентной системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }}{\text{,MoO}}_{4}^{{2 - }}~$ в программе КОМПАС 3D [15]:
${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }}$ [20]. Эвтектика при 580°С и 40 мол. % фторида калия;
${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}$ [21]. В системе образуется конгруэнтное соединение ${{{\text{K}}}_{3}}{\text{FMo}}{{{\text{O}}}_{4}}$ c температурой плавления 754°C, эвтектическим точкам отвечают составы 29 и 57 мол. % молибдата калия, плавящиеся при 722 и 745°С, соответственно;
${{{\text{K}}}^{ + }}{\text{||B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}$ [22]. Эвтектика при 625°С и 35 мол. % молибдата калия.
${\text{KBr}}{\kern 1pt} - {\kern 1pt} {{{\text{K}}}_{3}}{\text{FMo}}{{{\text{O}}}_{4}}$ [23]. Эвтектика при 574°С и 50 мол. % бромида калия.
${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }}{\text{,MoO}}_{4}^{{2 - }}$ [23]. Эвтектика Е1 при 556°С и 35 мол. % фторида калия, 53 мол. % бромида калия, 12 мол. % молибдата калия. Эвтектика Е2 при 568°С и 23 мол. % фторида калия, 50 мол. % бромида калия, 27 мол. % молибдата калия.
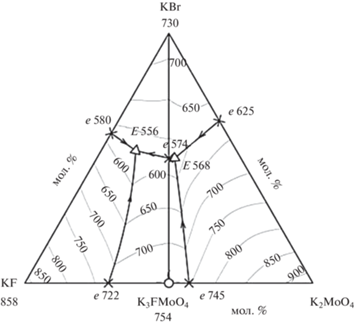
Диаграмма построена в координатах “состав–температура”, в основании лежит треугольник составов системы, по оси аппликата откладывается температура в диапазоне 500–800°С (рис. 1). Модель представляет собой совокупность точек, линий и поверхностей, которые предопределяются исходя из базовых геометрических элементов фазовых областей (табл. 1). Эти области выявлены из проекции поверхности ликвидуса системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }},$ в соответствии с методикой предложенной [16, 24, 25].
Рис. 1.
Проекция 3D модели фазового комплекса системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}.$
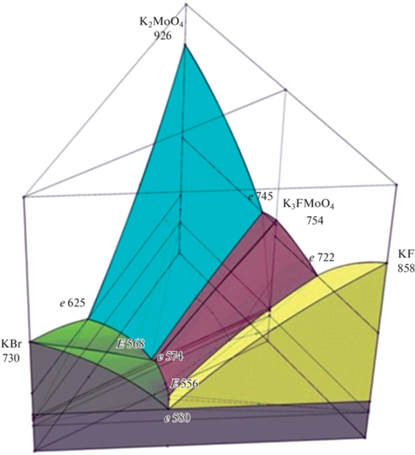
Таблица 1.
Базовые и дополнительные геометрические элементы модели фазового комплекса системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}$
| Фазовая область | Число равновесных фаз, Ф | Степень
свободы, С: С = К-Ф + 1 = = 4-Ф |
Базовые геометрические элементы фазовой области | Дополнительные геометрические элементы фазовой области |
|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 |
| ж + K2MoO4 | 2 | 2 | Две поверхности: (K2MoO4-е 625-Е 568-е 745- K2MoO4), вторая вырождена в отрезок |
Две линейчатые поверхности, две плоские боковые грани |
| ж + KF | 2 | 2 | Две поверхности: (KF-е 722-Е 556-е 580-KF), вторая вырождена в отрезок |
Две линейчатые поверхности, две плоские боковые грани |
| ж + KBr (две области) |
2 | 2 | Две поверхности: (KBr-е 625-Е 568-е 574-E 556-e 580-KBr), вторая вырождена в отрезок |
Две линейчатые поверхности, две плоские боковые грани |
| ж + K3FMoO4 (две области) |
2 | 2 | Две поверхности: (K3FMoO4-е 745-Е 568-е 574-E 556-e 722-K3FMoO4), вторая вырождена в отрезок |
Две линейчатые поверхности, две плоские боковые грани |
| ж + KF + KBr | 3 | 1 | Три линии: одна линия е 580–Е 556, две вырождены в отрезки |
Три линейчатые поверхности, нижняя плоская грань |
| ж + KBr + + K3FMoO4 | 3 | 1 | Три линии: одна линия е 574–Е 556, две вырождены в отрезки |
Три линейчатые поверхности, нижняя плоская грань |
| ж + KBr + + K3FMoO4 | 3 | 1 | Три линии: одна линия е 574–Е 568, две вырождены в отрезки |
Три линейчатые поверхности, нижняя плоская грань |
| ж + KBr + + K2MoO4 |
3 | 1 | Три линии: одна линия е 625–Е 568, две вырождены в отрезки |
Три линейчатые поверхности, нижняя плоская грань |
| ж + K2MoO4 + + K3FMoO4 |
3 | 1 | Три линии: одна линия е 745–Е 568, две вырождены в отрезки |
Три линейчатые поверхности, нижняя плоская грань |
| ж + KF + + K3FMoO4 |
3 | 1 | Три линии: одна линия е 722–Е 556, две вырождены в отрезки |
Три линейчатые поверхности, нижняя плоская грань |
| KF + KBr + + K3FMoO4 | 3 | 1 | Три линии, вырожденные в отрезки | Три линейчатые поверхности, нижняя и верхняя плоские грани |
| K2MoO4 + KBr + + K3FMoO4 | 3 | 1 | Три линии, вырожденные в отрезки | Три линейчатые поверхности, нижняя и верхняя плоские грани |
| ж = KF + KBr + + K3FMoO4 | 4 | 0 | Четыре точки: одна Е 556, три образуют вершины треугольника |
Плоскость треугольника |
| ж = K2MoO4 + + KBr + K3FMoO4 | 4 | 0 | Четыре точки: одна Е 568, три образуют вершины треугольника |
Плоскость треугольника |
Каждая фазовая область является, по сути, локальным объемом, ограниченным поверхностями (рис. 2). Фазовая область характеризуется своим фазовым состоянием. Модель предоставляет наглядную информацию о фазовом комплексе системы в объеме. Сечением элементов модели горизонтальной плоскостью с заданной координатой аппликаты получают изотермический разрез. Совокупность изотермических линий поверхности ликвидуса, спроецированных на треугольник составов (рис. 3), дает представление о крутизне поверхности и градиенте температур начала кристаллизации в системе.
Рис. 2.
Локальные объемы пространственных областей фазового комплекса системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}.$
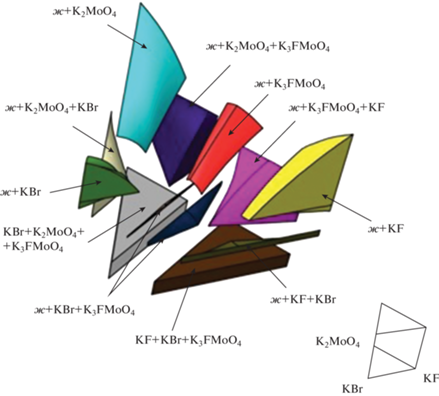
Рис. 3.
Изотермы поверхности ликвидуса системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}.$
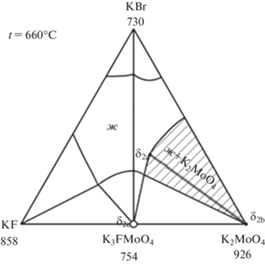
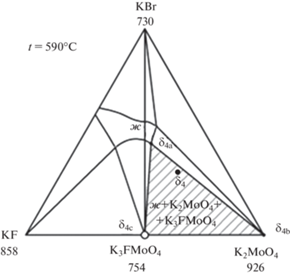
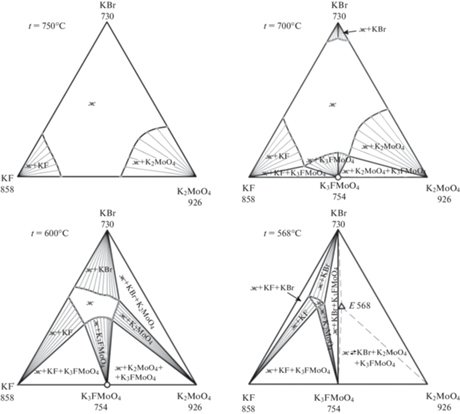
Анализируя изотермические сечения системы, выявленные с помощью 3D модели (рис. 4), можно заключить, что при понижении температуры уменьшается область жидкости, и увеличиваются двухфазные, а затем и трехфазные области. Конноды-отрезки характеризуют своими вершинами составы равновесных сосуществующих фаз в двухфазных областях, трехфазные области с фазами постоянного состава представляют собой треугольники.
Рис. 4.
Изотермические сечения системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}.$
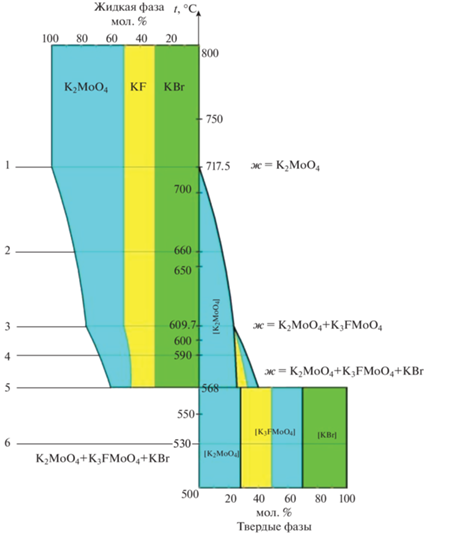
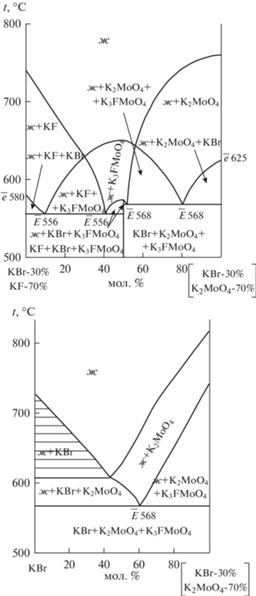
Сечением модели вертикальными плоскостями выявлены политермические разрезы, фиксирующие направления на трехкомпонентные эвтектики $\bar {E}~556$ и $\bar {E}~568$ (рис. 5).
Рис. 5.
Политермические сечения системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}.$
Осуществлен расчет материального баланса равновесных фаз для смеси δ в диапазоне температур 500–800°С с использованием 3D модели геометрическим методом. Состав смеси δ, мол. %: KF – 21, K2MoO4 – 49, KBr – 30. Результаты расчета сведены в табл. 2.
Таблица 2.
Составы равновесных фаз для смеси δ системы ${{{\text{K}}}^{ + }}{\text{||}}{{{\text{F}}}^{ - }},{\text{B}}{{{\text{r}}}^{ - }},{\text{MoO}}_{4}^{{2 - }}$
| № | t, °C | Равновесная фаза | Точка на диаграмме | Содержание фазы в образце, мол. % | Соотношение компонентов в фазе, мол. % | Абсолютное состав фазы относительно смеси, мол. % | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| KF (α) | K2MoO4 (β) | KBr (γ) | KF (α) | K2MoO4 (β) | KBr (γ) | |||||
| 0 | 800 | Ж | δ0 | 100 | 21 | 49 | 30 | 21 | 49 | 30 |
| 1 | 717.5 | Ж (a) | δ1 | 100 | 21 | 49 | 30 | 21 | 49 | 30 |
| K2MoO4 (b) | δ1b | 0 | 0 | 100 | 0 | 0 | 0 | 0 | ||
| 2 | 660 | Ж (a) | δ2a | 84.3 | 24.92 | 39.48 | 35.6 | 21.00756 | 33.28164 | 30.0108 |
| K2MoO4 (b) | δ2b | 15.7 | 0 | 100 | 0 | 0 | 15.7 | 0 | ||
| 3 | 609.7 | Ж (a) | δ3a | 76.6 | 27.29 | 33.56 | 39.15 | 20.90414 | 25.70696 | 29.9889 |
| K2MoO4 (b) | δ3b | 23.4 | 0 | 100 | 0 | 0 | 23.4 | 0 | ||
| D (c) | δ3c | 0 | 50 | 50 | 0 | 0 | 0 | 0 | ||
| 4 | 590 | Ж (a) | δ4a | 67.7 | 25.19 | 30.51 | 44.3 | 17.05363 | 20.65527 | 29.9911 |
| K2MoO4 (b) | δ4b | 24.4 | 0 | 100 | 0 | 0 | 24.4 | 0 | ||
| D (c) | δ4c | 7.9 | 50 | 50 | 0 | 3.95 | 3.95 | 0 | ||
| 5 | 568 | Ж (a) | δ5a | 60 | 23 | 27 | 50 | 13.8 | 16.2 | 30 |
| K2MoO4 (b) | δ5b | 25.6 | 0 | 100 | 0 | 0 | 25.6 | 0 | ||
| D (c) | δ5c | 14.4 | 50 | 50 | 0 | 7.2 | 7.2 | 0 | ||
| 5' | 568 | K2MoO4 (b) | δ5'b | 28 | 0 | 100 | 0 | 0 | 28 | 0 |
| D (c) | δ5'c | 42 | 50 | 50 | 0 | 21 | 21 | 0 | ||
| KBr (d) | δ5'd | 30 | 0 | 0 | 100 | 0 | 0 | 30 | ||
| 6 | 530 | K2MoO4 (b) | δ6b | 28 | 0 | 100 | 0 | 0 | 28 | 0 |
| D (c) | δ6c | 42 | 50 | 50 | 0 | 21 | 21 | 0 | ||
| KBr (d) | δ6d | 30 | 0 | 0 | 100 | 0 | 0 | 30 | ||
Температуры фазовых переходов определены геометрическим способом при пересечении вертикального луча имеющем (х, у) координаты, отвечающие составу смеси δ с границами пространственных фазовых областей 3D модели фазовой диаграммы (рис. 1). Каждый температурный отрезок внутри фазовой области разбит на два участка (табл. 2).
Используя принцип треугольника Розебома, выявлены геометрически координаты вершин коннодной фигуры. Для двухфазной области это коннода-отрезок, например, отрезок δ2a–δ2 на рис. 6 для смеси δ, а для трехфазной области – это коннода-треугольник δ4a–δ4b–δ4c на рис. 7. Координаты этих точек соответствуют составу равновесных сосуществующих фаз, области которых примыкают к точкам. Таким образом, определены соотношения компонентов в фазе (табл. 2). Соотношения равновесных фаз рассчитаны, используя уравнение математических матриц:
(1)
$\left( {\begin{array}{*{20}{c}} {{{{\{ {\text{Ж}}\} }}_{{\delta i}}}}&{{{{\{ {{{\text{K}}}_{{\text{2}}}}{\text{Mo}}{{{\text{O}}}_{4}}\} }}_{{\delta i}}}}&{{{{\{ D\} }}_{{\delta i}}}} \end{array}} \right) = \left( {\begin{array}{*{20}{c}} {\alpha _{{\delta i}}^{'}}&{\beta _{{\delta i}}^{'}}&{\gamma _{{\delta i}}^{'}} \end{array}} \right) \times {{\left( {\begin{array}{*{20}{c}} {{{\alpha }_{{\delta ia}}}}&{{{\beta }_{{\delta ia}}}}&{{{\gamma }_{{\delta ia}}}} \\ {{{\alpha }_{{\delta ib}}}}&{{{\beta }_{{\delta ib}}}}&{{{\gamma }_{{\delta ib}}}} \\ {{{\alpha }_{{\delta ic}}}}&{{{\beta }_{{\delta ic}}}}&{{{\gamma }_{{\delta ic}}}} \end{array}} \right)}^{{ - 1}}},$где:
$\left( {\begin{array}{*{20}{c}} {{{{\{ {\text{Ж}}\} }}_{{\delta i}}}}&{{{{\{ {{{\text{K}}}_{{\text{2}}}}{\text{Mo}}{{{\text{O}}}_{4}}\} }}_{{\delta i}}}}&{{{{\{ D\} }}_{{\delta i}}}} \end{array}} \right)$ – матрица соотношения равновесных фаз жидкости, твердых фаз молибдата калия и соединения фторида-молибдата калия для смеси δ в фигуративной точке δi, где i характеризует температуру (табл. 2, первый столбец);
$(\begin{array}{*{20}{c}} {\alpha _{{\delta i}}^{'}}&{\beta _{{\delta i}}^{'}}&{\gamma _{{\delta i}}^{'}} \end{array})$ – мольное процентное содержание компонентов KF (α), K2MoO4 (β) и KBr (γ) в фигуративной точке δi;
${{\left( {\begin{array}{*{20}{c}} {{{\alpha }_{{\delta ia}}}}&{{{\beta }_{{\delta ia}}}}&{{{\gamma }_{{\delta ia}}}} \\ {{{\alpha }_{{\delta ib}}}}&{{{\beta }_{{\delta ib}}}}&{{{\gamma }_{{\delta ib}}}} \\ {{{\alpha }_{{\delta ic}}}}&{{{\beta }_{{\delta ic}}}}&{{{\gamma }_{{\delta ic}}}} \end{array}} \right)}^{{ - 1}}}$ – обратная матрица преобразования, содержащая эквивалентные доли компонентов KF, K2MoO4 и KBr в точках δia, δib и δiс – точечных базисах равновесных фаз жидкости, твердых фаз молибдата калия и соединения фторида-молибдата калия.
Далее выявлен абсолютный состав равновесных фаз в пересчете на всю смесь как произведение относительного состава на содержание фазы в смеси (табл. 2, последние 3 столбца).
На основании абсолютного состава фаз построена диаграмма материального баланса сосуществующих фаз в диапазоне температур 500–800°С (рис. 8). Она построена, опираясь на принцип непрерывного изменения свойств внутри фазовой области, т.е. реализовано плавное соединение составов равновесных фаз сплайн-линией.
ЗАКЛЮЧЕНИЕ
Планирование эксперимента при определении фазовых равновесных состояний в МКС связано с построением древ фаз и древ кристаллизаций. Древа фаз формируются теоретическими расчетами по выявлению стабильного секущего комплекса системы и экспериментальному подтверждению рентгенофазовым анализом их правомерности. Для построения древа кристаллизаций в каждом симплексе комплексным дифференциальным термическим анализом исследуют по одному равномассовому составу, и сравнением температур исчезновения жидкой фазы определяю принадлежность нонвариантного состава к соответствующему симплексу. Наличие компьютерной 3D модели фазового комплекса МКС с соединениями позволяет на основе анализа информации о системах меньшей мерности оптимизировать эксперимент, т.е. позволяет прогнозировать характер, наличие, принадлежность нонвариантного состава к соответствующему симплексу, моделировать политермические и изотермические разрезы, а диаграмма материального баланса позволяет выявить составы равновесных фаз в заданном температурном диапазоне.
Список литературы
Манякова А.А., Егорова Е.М., Гаркушин И.К. Исследование стабильного треугольника четырехкомпонентной взаимной систем Li, Na, Cs||F, I // Расплавы. 2018. № 2. С. 188–193.
Shashkov M.O., Garkushin I.K. Experimental determination of eutectic compositions in the quinary reciprocal system Li, K||F, Br, VO3, MoO4 // Russian J. Inorganic Chemistry. 2019. 64. № 2. P. 251–256.
Trifonov K.I., Zabotin I.F., Krotov V.E., Nikiforov A.F. Density and molar volume of molten GdCl3–NaCl and GdCl3–KCl binary mixtures // Russian metallurgy. 2019. № 8. P. 838–841.
Maltsev D.S., Volkovich V.A., Vasin B.D. Diffusion coefficients of the uranium(III) and (IV) ions in the LICl–KCl–CsCl eutectic melt // Russian metallurgy. 2016. № 8. P. 722–728.
Benes O., Konings R.J.M. Actinide burner fuel: Potential compositions based on the thermodynamic evaluation of MF–PuF3 (M = Li, Na, K, Rb, Cs) and LaF3–PuF3 systems // J. Nuclear Materials. 2008. 377. № 3. C. 449–457.
Никитина Е.В., Карфидов Э.А., Зайков Ю.П. Коррозия перспективных металлических материалов во фторидных расплавах для жидкосолевых реакторов // Расплавы. 2021. № 1. С. 21–45.
Ламуева М.В., Зеленая А.Э., Луцык В.И. Тройные и четверные галогенидные системы для ядерного реактора 4-го поколения // Сб. статей. Бурятский госуниверситет. Улан-Удэ. 2020. С. 137–146.
Моргунова О.Е. Методология автоматизированного комплексного исследования многокомпонентных систем с применением моделирования и специализированного программного обеспечения // Сб. трудов Х Межд. Курнаковского совещания по физико-химическому анализу. В 2-х т. Самара: Сам. ГТУ. 2013. 1. С. 154–156.
Lutsyk V.I., Zelenaya A.E. T–x–y diagram of the MgO–SiO2–Al2O3 system: computer model assembly // Russian J. Inorganic Chemistry. 2018. 63. № 7. C. 966–973.
Афанасьева О.С., Егорова Г.Ф, Моргунова О.Е., Трунин А.С. Методика расчета тройных эвтектик по данным об элементах огранения систем низшей мерности // Вестник Самарского гос. техн. ун-та. Сер. Физ.-мат. науки. 2007. № 1. С. 182–183.
Афиногенов Ю.П., Гончаров Е.Г., Семенова Г.В. Физико-химический анализ многокомпонентных систем: учеб. пособие для студентов вузов, обучающихся по направлению и специальности “Химия”. М.: МФТИ; Воронеж: Воронежский гос. ун-т. 2006.
Лупейко Т.Г., Тарасов Н.И., Зяблин В.Н. Моделирование фазовых систем: монография. Ростов н/Д: ЮФУ. 2010.
Mazunin S.A., Noskov M.N., Elsukov A.V. Efficient methods to study phase equilibria in multinary aqueous systems // Russian J. Inorganic Chemistry. 2017. 62. № 5. P. 539–544.
Черкасов Д.Г., Ильин К.К. Аппроксимация данных для построения бинодальной кривой фазовых диаграмм некоторых тройных систем соль–вода–изопропиловый (н. пропиловый) спирт // Изв. Саратовского университета. Серия: Химия. Биология. Экология. 2019. 19. № 3. С. 274–283.
Зиновьев Д. Основы проектирования в КОМПАС-3D. V16 1-е изд. Студия Vertex. 2017.
Nipan G.D., Aronov A.N. Splitting of the chalcopyrite polyhedron in an isothermal Zn–Cd–Ge–As tetrahedron // Inorganic Materials. 2020. 56. № 2. P. 111–115.
Verdiev N.N., Garkushin I.K., Burchakov A.V., Verdieva Z.N., Alkhasov A.B., Musaeva P.A., Kondratyuk I.M., Egorova E.M. Phase Equilibria in the NaF–NaCl–NaBr–Na2CrO4 System // Inorganic Materials. 2020. 56. № 11. P. 1179–1187.
Vorob’eva V.P., Zelenaya A.E., Lutsyk V.I., Lamueva M.V. 3D computer models of the T–x–y diagrams, forming the LiF–NaF–CaF2–LaF3T–x–y–z diagram // Nanosystems: Physics, Chemistry, Mathematics. 2020. 11. № 3. P. 345–354.
Ламуева М.В., Зеленая А.Э., Луцык В.И. Компьютерная модель фазовой диаграммы системы LiF–PuF3–KF // Новые материалы и перспективные технологии. VI междисциплинарный научный форум с межд. участием. Москва. 2020. С. 128–133.
Справочник по плавкости систем из безводных неорганических солей // Под ред. Воскресенской Н.К. Двойные системы. М.–Л.: Изд-во АН СССР. 1961.
Посыпайко В.И., Алексеева Е.А., Васина Н.А. Диаграммы плавкости солевых систем: Справочник. Двойные системы с общим катионом. М.: Металлургия. 1977. III.
Вердиев Н.Н., Искендеров Э.Г., Арбуханова П.А., Амадзиев А.М. Фазовые равновесия в системе KBr–K2MoO4 // Изв. ВУЗов. Химия и химическая технология. 2006. 49. № 9. С. 26–28.
Вердиев Н.Н., Арбуханова П.А., Искендеров Э.Г., Зейналов М.Ш. Трехкомпонентная система KF–KBr–K2MoO4 // Изв. вузов. Химия и химическая технология. 2007. 50. № 12. С. 15–18.
Бурчаков А.В., Гаркушин И.К., Милов С.Н., Сухаренко М.А. Прогнозирование фазовых равновесий в системе NaCl–Na2MoO4–Na2WO4 на границе “жидкость–твердое тело” // Бутлеровские сообщения. 2019. 60. № 10. С. 124–139.
Вердиева З.Н., Бурчаков А.В., Вердиев Н.Н., Алхасов А.Б., Магомедбеков У.Г. Моделирование фазовых реакций в многокомпонентных системах // Вестник Тверского госуниверситета. 2019. № 3. С. 31–45.
Дополнительные материалы отсутствуют.