Агрохимия, 2019, № 3, стр. 3-18
ВЛИЯНИЕ ТЕМПЕРАТУРЫ, ВЛАЖНОСТИ И ВНЕСЕНИЯ СОЛОМЫ НА ДИНАМИКУ МИНЕРАЛИЗАЦИИ ОРГАНИЧЕСКОГО ВЕЩЕСТВА И ПОЧВЕННЫЕ ПУЛЫ УГЛЕРОДА И АЗОТА
А. С. Тулина *
Институт физико-химических и биологических проблем почвоведения РАН
142290 Московская обл., Пущино, ул. Институтская, 2, Россия
* E-mail: atulina@yandex.ru
Поступила в редакцию 10.09.2018
После доработки 01.10.2018
Принята к публикации 10.12.2018
Аннотация
Изучено влияние температуры (8, 18 и 28°С), влажности (10, 25 и 40 вес. %) и внесения зрелой пшеничной соломы (1% от массы почвы) на динамику продуцирования С-СО2 образцами 3-х пахотных почв в течение 150-суточной инкубации. Наиболее значимым фактором, определяющим изменчивость пулов общего органического, потенциально-минерализуемого и микробного углерода и общего азота являлось внесение соломы. Изменчивость пула минерального азота определялась температурой. К концу эксперимента при 18 и 28°С в почвах накапливалось в среднем в 2 раза больше минерального азота, чем при 8°С, а при 25%-ном увлажнении – в 1.5 раза больше, чем при увлажнении 10 и 40 вес.%. В почвах с соломой при 8°С обнаружена нетто-иммобилизация, а при 18 и 28°С – нетто-минерализация азота.
ВВЕДЕНИЕ
Минерализация органического вещества в почве определяется количеством, качеством и защищенностью его составляющих, а также природными и антропогенными факторами [1]. Важнейшими природными абиотическими факторами являются температура и влажность: они влияют на скорость процессов в почве и преобразование содержащихся в почве и поступающих в нее веществ и материалов, и, как следствие, на эмиссию парниковых газов и содержание минеральных форм азота, необходимых для роста и развития растений. Для прогнозирования влияния температуры и влажности на почвенные процессы и пулы различных элементов необходимы специальные исследования, проводимые при разных гидротермических условиях, что особенно актуально при наблюдающихся климатических изменениях последних десятилетий.
Распространенной практикой современного земледелия является возвращение в почву побочной продукции сельскохозяйственных культур, основная доля в которой принадлежит соломе [2]. Солома становится значимым удобрительным ресурсом в связи с переходом на бесподстилочное содержание скота, ее внесение в почву менее затратно по сравнению с уборкой с поля. Систематическое применение соломы обеспечивает улучшение структуры и водно-физических свойств почвы, способствует оптимизации гумусного статуса пахотных почв и повышению содержания в них питательных элементов [3–7]. Солома является эффективным источником формирования активного пула почвенного азота, стимулируя функциональную активность почвенного микробного сообщества [8, 9]. Усиление иммобилизации азота при внесении соломы способствует уменьшению газообразных и инфильтрационных потерь азота [10–13], что особенно важно в отсутствие вегетирующих растений в безморозный период года.
Внесение соломы изменяет азотный режим почвы. С одной стороны, с соломой в почву поступает дополнительное количество азота, также возможно усиление несимбиотической азотфиксации, связанное с применением соломы [6, 14]. С другой стороны, широкое соотношение углерода и азота (С : N), свойственное соломе, способствует поглощению микроорганизмами минерального азота, содержащегося в почве, и преобладанию иммобилизации над минерализацией органических соединений азота [15, 16]. В этой связи важным представляется выявление условий, способствующих минерализации органических азотсодержащих соединений.
Цель работы – изучить влияние температуры, влажности и внесения соломы на динамику минерализации органического вещества (ОВ) и оценить воздействие этих факторов на общий органический (Сорг), потенциально-минерализуемый (Спм), микробный (Смб) пулы углерода, а также общий (Nобщ) и минеральный (Nмин) пулы азота в пахотных почвах 3-х типов.
МЕТОДИКА ИССЛЕДОВАНИЯ
Характеристика почв. Исследования проводили с образцами серой лесной среднесуглинистой почвы (Московская обл.), оподзоленного тяжелосуглинистого чернозема (Тульская обл.) и темно-каштановой легкосуглинистой почвы (Оренбургская обл.), отобранными на пахотных участках из 0–20 см слоя. Почвы имели следующие исходные показатели: серая лесная почва: ${\text{p}}{{{\text{H}}}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}$ – 6.7, содержание Сорг – 0.92%, Nобщ – 1170, обменного аммония (N-NH4) – 7, нитратов (N-NO3) – 13 мг/кг; оподзоленный чернозем: ${\text{p}}{{{\text{H}}}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}$ – 7.2, Сорг – 2.5%, Nобщ – 2190, N-NH4 – 13, N-NO3 – 4 мг/кг; темно-каштановая почва: ${\text{p}}{{{\text{H}}}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}$ – 7.6, Сорг – 1.12%, Nобщ – 1390, N-NH4 – 22, N-NO3 – 12 мг/кг.
Основная инкубация. Зрелую пшеничную солому, содержащую 40.5% Сорг и 0.86% Nобщ, размалывали и смешивали с почвой в дозе 1% от массы почвы. Образцы почв без соломы и с соломой помещали в стеклянные флаконы, увлажняли и инкубировали в термостатах при постоянной температуре (8, 18 и 28°С) и влажности (10, 25, 40 вес. %) в течение 150 сут. Образцы соломы инкубировали также в течение 150 сут при температуре 8, 18 и 28°С и влажности 10, 40, 80, 120 и 160 вес. %. Опыт провели в трехкратной повторности.
Повторная инкубация. Образцы почв с соломой и без соломы, ранее проинкубированные при разных гидротермических условиях, подвергали повторной инкубации при одинаковой температуре (22°С) и влажности (25 вес. %) в течение 14 сут.
Измерение СО2. В течение инкубации образцов почвы, соломы и почвы с соломой ежедневно в течение первой недели эксперимента, затем 3, 2 и 1 раз в неделю определяли количество продуцируемого диоксида углерода (СО2). Измерения концентрации СО2 проводили на хроматографе “Кристалл Люкс 4000М”.
Для оценки воздействия температуры и влажности на размер фактической минерализации органического вещества (Сфм), оцениваемой по продуцированию углерода, входящего в состав диоксида (С-СО2), были использованы температурные (Q10) и влажностные (W10) коэффициенты, которые вычисляли по уравнениям (1) и (2) соответственно [17]:
(1)
${{Q}_{{10}}} = {{({{Х }_{2}}{\text{/}}{{Х }_{1}})}^{{10/({{{\text{T}}}_{2}} - {{{\text{T}}}_{{\text{1}}}})}}},$Температурный коэффициент показывает, во сколько раз изменяется кумулятивное количество С-СО2, выделившееся из образцов почвы, соломы и почвы с соломой при минерализации ОВ за определенный период времени при увеличении температуры на 10°С, а влажностный коэффициент – при увеличении влажности на 10 вес. %.
Минерализацию соломы в почвах оценивали по разности кумулятивного продуцирования С-СО2 образцами почвы с соломой и почвы без соломы за 150 сут инкубации.
Оценка минерализуемого пула органического вещества и микробной биомассы биокинетическим методом. Величину пула потенциально-минерализуемого углерода рассчитывали по кумулятивному продуцированию С-СО2 за 150 сут инкубации в соответствии с методом биокинетического фракционирования органического вещества [18]. Кумулятивные кривые продуцирования С-СО2 рассчитывали по кинетике первого порядка:
где Ct – кумулятивное количество выделившегося С-СО2 за время t, мг С/кг почвы. Спм – пул потенциально-минерализуемого углерода, мг С/кг почвы, k – константа скорости минерализации Спм, сут–1.Среднее время оборачиваемости Спм (ТТ) рассчитывали как ТТ = 1/k, а интенсивность минерализации (ИМ) – как ИМ = Спмk.
Содержание микробной биомассы определяли по количеству С-СО2, выделившемуся за 14 сут повторной инкубации (уравнение (4)):
где Ct – кумулятивное количество C-СО2 (мг/кг), выделившегося за время t (сут), Cмб – содержание углерода микробной биомассы (мг/кг), k – константа скорости, сут–1, 0.45 – доля углерода почвенного субстрата, минерализованного микроорганизмами до C-СО2, B – константа, показывающая скорость продукции C-CO2 при равновесном состоянии прироста и отмирания биомассы после полной утилизации начального запаса субстрата [18].Вычисления проводили методом нелинейной оценки с использованием программы Statistica 6.0. Коэффициенты с уровнем значимости P > 0.05 отвергали.
Микробный метаболический или дыхательный коэффициент (qСО2) рассчитывали как отношение скорости дыхания микроорганизмов к их биомассе [19].
Определение содержания углерода и азота в почве. После окончания инкубации образцы почвы и почвы с соломой высушивали в течение 1 сут при 65°С, определяли содержание в них Сорг и Nобщ на CHNS-анализаторе “Elementar Vario”, N-NH4, N-NO3, суммы нитратов и обменного аммония (Nмин) – по методу Кудеярова. Величину нетто-минерализации и нетто-иммобилизации минерального азота рассчитывали как разницу содержания Nмин в почве после 150 сут инкубации и в исходных образцах.
Математическая обработка результатов. Вклад изученных факторов (температуры, влажности и внесения соломы) в изменчивость пулов углерода и азота в почвах рассчитывали с использованием программы Microsoft Excel.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Оценка фактической минерализации органического вещества. Минерализация ОВ больше зависела от гидротермических условий, при которых проходила инкубация, и от внесения соломы, чем от свойств почв. Содержание Сорг в черноземе было в 2.2 и 2.7 раза больше, чем в темно-каштановой и серой лесной почвах, соответственно, а количество органического вещества, фактически минерализованного до С-СО2 за 150 сут инкубации – лишь в 1.2 раза больше (рис. 1), тогда как при повышении увлажнения с 10 до 40 вес. % размер Сфм увеличился в 1.8 раза, при повышении температуры с 8 до 28°С – в 2.6 раза, а при внесении соломы – в 4.4 раза в среднем в эксперименте.
Рис. 1.
Количество фактически минерализованного углерода органического вещества до С-СО2 (Сфм, мг/кг) в течение 150-суточной инкубации серой лесной почвы (I), оподзоленного чернозема (II) и темно-каштановой почвы (III) без соломы и с соломой при разных гидротермических условиях. На гистограммах приведены средние величины и стандартные отклонения. То же на рис. 2–4.

Чувствительность минерализации органического вещества к изменению температуры на разных этапах инкубации значительно различалась. В почвах без соломы в первые 14 сут эксперимента коэффициент Q10 в интервале 8–28°С составил 1.26, в последние 14 сут – 2.22 в среднем для 3-х почв (табл. 1). В начале эксперимента преимущественно минерализовались наиболее доступные микроорганизмам и наименее термочувствительные соединения легко минерализуемой фракции минерализуемого пула почвенного органического вещества (ПОВ), тогда как в конце – менее доступные и более термочувствительные вещества трудно минерализуемой фракции. При внесении соломы, напротив, чувствительность минерализации к изменению температуры в начале эксперимента была больше (Q10 = 2.28), чем в конце (Q10 = 1.71). Это объясняется наличием лаг-фаз (lag – задержка, запаздывание), обнаруженных в ходе минерализации при 8°С в почвах с соломой при анализе динамики продуцирования С-СО2 (рис. 2). В среднем за 150 сут инкубации различий термочувствительности минерализации в почвах с соломой и без соломы выявить не удалось: коэффициенты Q10 составили 1.61 в среднем для 3-х почв.
Таблица 1.
Температурные коэффициенты (Q10) фактической минерализации органического вещества в почвах без соломы и с соломой за первые и последние две недели инкубации и за весь период инкубации, рассчитанные для температурного диапазона 8–28°С
| Почва | Без соломы | С соломой | ||||
|---|---|---|---|---|---|---|
| период оценки продуцирования С-СО2, сут | ||||||
| 0–14 | 137–150 | 0–150 | 0–14 | 137–150 | 0–150 | |
| Серая лесная | 1.18 | 1.86 | 1.40 | 1.95 | 1.68 | 1.42 |
| Чернозем оподзоленный | 1.33 | 2.73 | 1.85 | 2.46 | 1.96 | 1.88 |
| Темно-каштановая | 1.28 | 2.07 | 1.57 | 2.42 | 1.50 | 1.52 |
Рис. 2.
Динамика кумулятивного продуцирования С-СО2 в течение 150-суточной инкубации серой лесной почвы, чернозема оподзоленного и темно-каштановой почвы без соломы и с соломой в разных гидротермических условиях: 8, 18 и 28°C – температура, 10, 25 и 40 вес. % – влажность.


Чувствительность минерализации к изменению влажности в почвах с соломой и без соломы в начале инкубации различалась несущественно, а с течением времени эти различия проявились (табл. 2). Величины влажностных коэффициентов W10 для интервала увлажнения 10–40 вес. % за весь период инкубации в почвах без соломы составили в среднем 1.15, а в почвах с соломой – 1.24, т.е. для обеспечения эффективной минерализации при внесении соломы возрастала потребность в увлажнении.
Таблица 2.
Влажностные коэффициенты (W10) фактической минерализации органического вещества в почвах без соломы и с соломой за первые и последние 2 нед инкубации и за весь период инкубации, рассчитанные для диапазона увлажнения 10–40 вес. %
| Почва | Без соломы | С соломой | ||||
|---|---|---|---|---|---|---|
| период оценки продуцирования С-СО2, сут | ||||||
| 0–14 | 137–150 | 0–150 | 0–14 | 137–150 | 0–150 | |
| Серая лесная | 1.09 | 1.11 | 1.09 | 1.03 | 1.30 | 1.20 |
| Чернозем оподзоленный | 1.22 | 1.17 | 1.20 | 1.29 | 1.29 | 1.34 |
| Темно-каштановая | 1.17 | 1.16 | 1.17 | 1.11 | 1.19 | 1.18 |
Характеристика потенциально-минерализуемого органического вещества почв и соломы. Размер фактической минерализации указывал на суммарное количество углерода в составе СО2, образовавшегося при минерализации органического вещества за определенное время. Вычисления, произведенные по методу биокинетического фракционирования, позволили определить размер пула потенциально-минерализуемого углерода и установить характеризующие его параметры: константу скорости минерализации, среднее время оборачиваемости и интенсивность минерализации. При оценке минерализации ОВ значение имеет не только размер минерализуемого пула, но и скорость, с которой минерализация происходит. Минерализуемый пул может быть “большим и медленным” или “небольшим, но быстрым”. Размеры потерь углерода из почв в виде СО2 за время инкубации, определенные на газовом хроматографе, соотносились с расчетными величинами пула Спм, который был в среднем в 1.2 раза больше, чем Сфм.
В изученных почвах без соломы содержание Спм при 8°С практически не различалось, а повышение температуры инкубации выявило различия в пуле потенциально-минерализуемого углерода в почвах разных типов (табл. 3). В почвах с соломой, напротив, существенные различия наблюдали при 8°С: пул Спм темно-каштановой почвы был в 2–3 раза больше, а ТТ – в 3 раза продолжительнее, чем в серой лесной почве и черноземе, что объясняется наличием лаг-фаз различной продолжительности, тогда как повышение температуры эти различия нивелировало.
Таблица 3.
Характеристика минерализуемого пула (Спм) почв с соломой и без соломы при разных гидротермических условиях
| Почва | Влажность, весовые % | 8°С | 18°С | 28°С | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| мг/кг | % от Сорг | ТТ, сут. | мг/кг | % от Сорг | ТТ, сут. | мг/кг | % от Сорг | ТТ, сут. | ||
| Почва без соломы | ||||||||||
| Серая лесная почва | 10 | 251 ± 4 | 2.7 | 48 | 653 ± 11 | 7.1 | 99 | 731 ± 59 | 7.9 | 124 |
| 25 | 357 ± 6 | 3.9 | 40 | 803 ± 20 | 8.7 | 122 | 820 ± 28 | 8.9 | 112 | |
| 40 | 333 ± 7 | 3.6 | 41 | 965 ± 22 | 10.5 | 150 | 883 ± 10 | 9.6 | 105 | |
| Среднее | 314 | 3.4 | 43 | 807 | 8.8 | 124 | 811 | 8.8 | 114 | |
| Чернозем оподзоленный | 10 | 184 ± 1 | 0.7 | 38 | 731 ± 8 | 2.9 | 106 | 988 ± 43 | 4.0 | 141 |
| 25 | 287 ± 3 | 1.1 | 39 | 953 ± 11 | 3.8 | 82 | 1360 ± 20 | 5.4 | 124 | |
| 40 | 321 ± 5 | 1.3 | 34 | 1070 ± 20 | 4.3 | 79 | 1480 ± 1 | 5.9 | 104 | |
| Среднее | 264 | 1.0 | 37 | 917 | 3.7 | 89 | 1270 | 5.1 | 123 | |
| Темно-каштановая почва | 10 | 217 ± 1 | 1.9 | 32 | 480 ± 6 | 4.3 | 88 | 489 ± 3 | 4.4 | 86 |
| 25 | 241 ± 2 | 2.2 | 41 | 533 ± 9 | 4.8 | 76 | 747 ± 31 | 6.7 | 72 | |
| 40 | 285 ± 3 | 2.5 | 38 | 648 ± 5 | 5.8 | 71 | 982 ± 2 | 8.8 | 78 | |
| Среднее | 248 | 2.2 | 37 | 554 | 4.9 | 78 | 739 | 6.6 | 79 | |
| Среднее | 275 ± 57 | 2.2 ± 1.1 | 39 ± 5 | 759 ± 203 | 5.8 ± 2.5 | 97 ± 26 | 942 ± 310 | 6.8 ± 2.1 | 105 ± 23 | |
| Почва с соломой | ||||||||||
| Серая лесная почва | 10 | 1230 ± 20 | 9.3 | 68 | 1940 ± 50 | 14.7 | 57 | 1880 ± 10 | 14.3 | 51 |
| 25 | 1690 ± 20 | 12.8 | 81 | 3520 ± 180 | 26.6 | 101 | 3160 ± 2 | 24.0 | 78 | |
| 40 | 1960 ± 50 | 14.9 | 96 | 4080 ± 150 | 30.9 | 115 | 4570 ± 100 | 34.6 | 101 | |
| Среднее | 1630 | 12.3 | 82 | 3180 | 24.1 | 91 | 3210 | 24.3 | 77 | |
| Чернозем оподзоленный | 10 | 650 ± 13 | 2.2 | 93 | 1910 ± 80 | 6.6 | 70 | 2330 ± 30 | 8.0 | 78 |
| 25 | 1390 ± 10 | 4.7 | 66 | 4140 ± 200 | 14.3 | 79 | 4560 ± 60 | 15.7 | 80 | |
| 40 | 1980 ± 3 | 6.8 | 129 | 4231 ± 190 | 14.6 | 71 | 4950 ± 40 | 17.1 | 69 | |
| Среднее | 1340 | 4.6 | 96 | 3430 | 11.8 | 73 | 3950 | 13.6 | 76 | |
| Темно-каштановая почва | 10 | 2770 ± 50 | 18.2 | 246 | 2110 ± 50 | 13.9 | 67 | 2500 ± 10 | 16.4 | 61 |
| 25 | 3700 ± 130 | 24.4 | 260 | 4180 ± 250 | 27.5 | 101 | 3880 ± 70 | 25.6 | 70 | |
| 40 | 4500 ± 330 | 29.6 | 330 | 3810 ± 110 | 25.0 | 69 | 4520 ± 40 | 29.7 | 68 | |
| Среднее | 3660 | 24.1 | 279 | 3370 | 22.2 | 79 | 3630 | 23.9 | 66 | |
| Среднее | 2210 ± 1240 | 13.7 ± 9.2 | 152 ± 99 | 3320 ± 1030 | 19.4 ± 8.3 | 81 ± 20 | 3600 ± 1150 | 20.6 ± 8.4 | 73 ± 14 | |
Влагоемкость соломы была в 2–3 раза больше влагоемкости почв, поэтому при 10%-м увлажнении минерализация соломы лимитировалась влажностью (табл. 4). При влажности 10 вес. % и 8°С Спм практически отсутствовал, а минерализация проходила с крайне низкой скоростью. При 18 и 28°С минерализуемый пул углерода соломы также был крайне мал, и фактически был представлен лишь легко минерализуемой фракцией, время оборачиваемости которой не превышало 10 сут. Коэффициент W10 в интервале увлажнения 10–40 вес. % составил в среднем 2.91. Для сравнения, W10 для легко- и трудно минерализуемых фракций изученных почв в этом диапазоне были равны в среднем 1.22 и 1.03 соответственно [17]. Дальнейшее повышение влажности не привело к значительным изменениям минерализации. В отсутствии лимитирования минерализации соломы влажностью (при 40, 80, 120 и 160%-ном увлажнении) ее скорость примерно соответствовала скорости разложения целлюлозного пула [11]. При 40%-ном увлажнении коэффициент Q10 в интервале 8–28°С был равен 1.80.
Таблица 4.
Потенциально-минерализуемый углерод (Спм) соломы без смешивания ее с почвами и время оборачиваемости (ТТ) в зависимости от температуры и влажности
| Влажность, вес. % | 8°С | 18°С | 28°С | |||
|---|---|---|---|---|---|---|
| Спм, % от исходного | ТТ, сут | Спм, % от исходного | ТТ, сут | Спм, % от исходного | ТТ, сут | |
| 10 | 0.04 ± 0.02 | 184 | 0.43 ± 0.15 | 9 | 0.62 ± 0.07 | 7 |
| 40 | 4.98 ± 0.04 | 51 | 10.51 ± 0.39 | 27 | 16.05 ± 0.61 | 27 |
| 80 | 5.57 ± 0.07 | 49 | 11.47 ± 0.28 | 29 | 17.40 ± 0.77 | 29 |
| 120 | 5.87 ± 0.30 | 45 | 11.09 ± 0.51 | 33 | 16.29 ± 1.06 | 26 |
| 160 | 5.63 ± 0.39 | 48 | 10.07 ± 0.40 | 31 | 14.51 ± 1.14 | 23 |
По доступности микроорганизмам фракции органического вещества изученных почв [17] и вносимой соломы можно расположить в ряд по убыванию: легко минерализуемая фракция (ТТ < < 10 сут) > солома (ТТ ≈ 30 сут) > трудно минерализуемая фракция (ТТ = 100–1000 сут), по чувствительности к повышению температуры в ряд по возрастанию: легко минерализуемая фракция (Q10 = 0.91) < солома (Q10 = 1.80) < трудно минерализуемая фракция (Q10 = 2.40), т.е., чем пул углерода доступнее микроорганизмам, тем он менее термочувствителен, и, наоборот, чем углеродный пул устойчивее к микробному разложению, тем его термочувствительность выше. Солома характеризовалась средней термочувствительностью и средней доступностью микроорганизмам.
Продуцирование СО2 характеризует минерализацию всех органических соединений, присутствующих в почве, а их вклад в общий поток диоксида углерода может меняться с течением времени и зависит от факторов, лимитирующих минерализацию. Запаздывание минерализации, проявившееся в обнаруженных лаг-фазах, в почвах с соломой при температуре 8°С могло происходить из-за того, что в начале инкубации минерализовалась преимущественно легко минерализуемая фракция ПОВ, наименее чувствительная к температуре и наиболее доступная для микробного разложения, а активизация минерализации соломы запаздывала тем значительнее, чем больше в почве содержалось легко минерализуемой фракции, данные о размере которой приведены в нашей предыдущей работе [20]. Следует отметить, что при сравнении интенсивности минерализации (Спмk) существенных различий между почвами разных типов не выявлено.
Внесение соломы увеличивало исходное содержание Сорг в серой лесной почве на 44%, в черноземе – на 16%, в темно-каштановой почве – на 36% и увеличило долю потенциально-минерализуемого углерода в общем органическом углероде этих почв в среднем в эксперименте с 7 до 20, с 3 до 10, с 5 до 23% соответственно. К концу инкубации солома минерализовалась на 21–74% в серой лесной почве, на 9–87% – в черноземе и на 25‒84% – в темно-каштановой почве. Минерализация соломы вне почв не превышала 17%, поскольку она лимитировалась минеральным азотом, количество которого в соломе с течением времени инкубации истощалось, тогда как при минерализации соломы в почвах микроорганизмам были доступны почвенные источники азота.
При внесении соломы не только многократно увеличивался минерализуемый пул органического вещества в почвах, но и изменялась скорость минерализации, что отчетливо проявилось в разных условиях инкубации. Если в почвах без соломы при 8°С минерализовались наиболее доступные и наименее термочувствительные соединения, на что указывало короткое ТТ (39 ± 5 сут), то по мере увеличения температуры ТТ становилось почти в 3 раза продолжительнее, что свидетельствовало о включении в процесс минерализации менее доступных микроорганизмам и более термочувствительных органических веществ в составе ПОВ. При внесении соломы, напротив, при 8°С ТТ в среднем составило 152 ± 99 сут, а при повышении температуры инкубации среднее время оборачиваемости сокращалось в 2 раза. В почве без соломы минерализовались вещества различного генезиса, защищенности, доступности микроорганизмам, обладающие разной термочувствительностью. В почве с соломой основной вклад в минерализацию принадлежал свежевнесенной соломе, представляющей собой незащищенный, относительно гомогенный углеродсодержащий субстрат со средней доступностью микроорганизмам и средней термочувствительностью, поэтому повышение температуры вполне закономерно увеличило скорость ее минерализации. Весьма продолжительные ТТ, отмеченные в ходе инкубации почв с соломой при 8°С, были связаны с вышеописанными лаг-фазами, которые составили от 2–3 нед в серой лесной почве и оподзоленном черноземе до 6 нед в темно-каштановой почве.
Содержание Сорг и Nобщ в почве. Чем интенсивнее проходила минерализация ОВ, тем меньше содержалось в почвах общего органического углерода через 150 сут, как показали данные, полученные на CHNS-анализаторе (рис. 3). В вариантах без внесения соломы убыль содержания Сорг в разных гидротермических условиях составила в среднем для 3-х почв от 2 до 11% от исходного его количества. Внесение соломы, не смотря на бoльшие газообразные потери углерода при ее минерализации, позволило компенсировать потери Сорг в течение инкубации при температуре 28°С и увеличить его содержание на конец инкубации при температуре 18°С и 8°С по сравнению с исходным его количеством в почвах.
Рис 3.
Содержание: (а) – общего органического углерода (Сорг), (б) – общего азота (Nобщ), (в) – их соотношение (Сорг : Nобщ) в исходных образцах (исх.) серой лесной почвы (I), оподзоленного чернозема (II), темно-каштановой почвы (III) и после 150 сут инкубации без соломы и с соломой при разных гидротермических условиях.

Содержание общего азота в почвах в результате инкубации изменялось в меньшей степени, чем содержание общего органического углерода. Применение соломы увеличило пул Nобщ в среднем на 5%, а повышение температуры и влажности сказалось на содержании Nобщ не столь существенно. Соотношение Сорг : Nобщ в почвах при повышении температуры и влажности инкубации значительно уменьшалось, внесение соломы расширяло это соотношение, причем гидротермические условия оказывали большее влияние на изменение соотношения Сорг : Nобщ, чем внесение соломы. О преобладании потерь углерода над потерями азота в результате продолжительной инкубации в разных гидротермических условиях также свидетельствовали результаты других авторов [21].
Минеральный азот в почве. В отличие от Nобщ, содержание Nмин в почвах к концу эксперимента изменялось весьма значительно (рис. 4). Доля минерального азота в пуле общего азота через 150 сут составила в вариантах без внесения соломы: в серой лесной почве – 3–6%, в оподзоленном черноземе – 2–4%, темно-каштановой почве – 4–8%, при внесении соломы: 1–2, 1–3, 1–6% соответственно.
Рис. 4.
Содержание: (а) – обменного аммония (N-NH4), (б) – нитратного азота (N-NO3), (в) – их суммы (Nмин) в исходных образцах (исх.) серой лесной почвы (I), оподзоленного чернозема (II), темно-каштановой почвы (III) и после 150 сут инкубации без соломы и с соломой при разных гидротермических условиях.
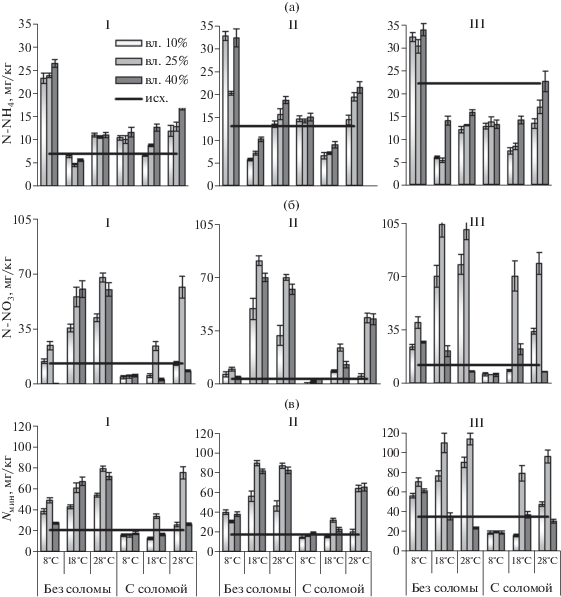
Изменение содержания минерального азота в почвах зависело от одновременно проходящих разнонаправленных процессов – минерализации и иммобилизации. Если минерализация шла быстрее, чем иммобилизация, то наблюдали увеличение содержания Nмин по сравнению с исходным содержанием минерального азота в почве, или нетто-минерализацию, если иммобилизация проходила быстрее, чем минерализация, то отмечали убыль содержания Nмин в почве по сравнению с его исходным содержанием, или нетто-иммобилизацию. Следует подчеркнуть, что в настоящей статье оценили результирующую величину процессов минерализации и иммобилизации, каковой является нетто-величина изменения Nмин, а реальную интенсивность этих 2-х процессов можно оценить лишь при помощи изотопной индикации. Размер нетто-минерализации (накопления в почве Nмин в отсутствие растений) характеризует потенциальную доступность растениям азота почвы [22, 23], поэтому накопление в почвах Nмин оценивали за время, сопоставимое с продолжительностью вегетационного периода.
Накопление минерального азота в почвах больше зависело от температуры, при которой осуществлялась инкубация, чем от влажности и внесения соломы. Прямая зависимость нетто-минерализации азота от температуры почвы установлена также в полевых условиях [24]. Нетто-минерализация в почвах без соломы при 8 и 28°С составила в среднем в серой лесной почве 90 и 230% от исходного содержания Nмин, в черноземе – 100 и 330%, в темно-каштановой почве – 70 и 110%, т.е. в результате минерализации при 8°С высвободилось в 2 раза больше доступного растениям азота, чем можно судить по его содержанию в исходных образцах почвы, а при 28°С – до 4-х раз больше.
Накопление в почве Nмин при увеличении влажности изменялось нелинейно. При оптимальном увлажнении (25 вес. %) в почвах накапливалось в среднем в 1.5 раза больше Nмин, чем при недостаточном (10 вес. %) и избыточном (40 вес. %) увлажнении. Недостаточное увлажнение могло подавлять микробные процессы в почве, избыточное – усиливать газообразные потери минерального азота, что подтверждено убылью пула общего азота.
Уменьшение активности минерализации органических азотсодержащих соединений почвы может быть одной из причин снижения урожайности сельскохозяйственных культур в холодные и (или) засушливые годы из-за ухудшения условий азотного питания растений. Применение азотных удобрений уменьшает климатические риски при возделывании зерновых культур [25], что может быть связано с восполнением дефицита азота, минерализуемого из почвенного органического вещества с меньшей скоростью при неблагоприятных гидротермических условиях.
В почвах с соломой при 8°С наблюдали нетто-иммобилизацию азота, которая в серой лесной почве составила 30, черноземе – 10, темно-каштановой почве – 50% от исходного Nмин, тогда как при 18 и 28 °С имела место нетто-минерализация, которая была наибольшей при увлажнении 25 вес. %, достигая соответственно 70 и 270% в серой лесной почве, 90 и 280% – в черноземе, 130 и 170% – в темно-каштановой почве. Иммобилизованный на ранних этапах инкубации азот подвергался повторной минерализации (реминерализации), а минерализация азота более чувствительна к температуре, чем иммобилизация. В среднем в опыте, в вариантах с применением соломы в почвах накапливалось Nмин на 30 мг/кг меньше, чем в почвах без соломы.
Микробная иммобилизация содержащегося в почве минерального азота при применении соломы может привести к снижению урожайности культур, что наиболее вероятно при ее внесении незадолго перед началом активной вегетации растений. Максимальная иммобилизация, как правило, происходит в первый месяц после внесения соломы, а затем возможна его повторная минерализация [14]. Чтобы синхронизировать превращения азота в почве и его потребление растениями, важно не столько ограничить иммобилизацию азота, сколько обеспечить его реминерализацию [2]. Повторной минерализации азота способствует повышение температуры. Как показали результаты, полученные в полевых опытах, внесение соломы осенью после уборки урожая не привело к снижению урожайности культур, выращенных на следующий год на черноземах [26, 27], и повышало ее на дерново-подзолистой почве [28], что можно отчасти объяснить реминерализацией ранее иммобилизованного азота.
Известно, что чем больше в почве содержится нитратов, тем выше риск потерь азота из почвы, как газообразных, так и инфильтрационных. Наши результаты показали, что соотношение нитратов и обменного аммония зависело от гидротермических условий, при этом содержание аммонийного азота изменялось менее значительно, чем содержание нитратного. В результате инкубации при 8°С в пуле минерального азота преобладал аммонийный азот, а при 18 и 28°С – нитратный. Содержание N-NO3 в почвах увеличилось в диапазоне увлажнения 10–25 вес. % и уменьшилось в диапазоне 25–40 вес. %. Относительно небольшую долю N-NO3 в Nмин при недостаточном увлажнении можно объяснить невысокой скоростью нитрификации, а снижение содержания N-NO3 при избыточном увлажнении – усилением денитрификации. Внесение соломы снижало долю нитратного азота в пуле минерального азота. Следовательно, повышение температуры и влажности в отсутствие вегетирующих растений способствовало увеличению риска потерь азота из почвы, а внесение соломы было эффективным способом биологического связывания минерального азота в почве, который способствует уменьшению потерь азота и не препятствовал повторной минерализации органических азотсодержащих соединений.
Соотношение количества С-СО2, продуцированного почвами за 150 сут и содержания минерального азота к концу основной инкубации (Сфм : Nмин) в почвах без соломы в среднем составило 10. Внесение соломы способствовало расширению соотношения Сфм : Nмин до 82 как за счет увеличения минерализации органических углеродсодержащих соединений, так и за счет усиления иммобилизации Nмин органотрофными микроорганизмами. Это согласовалось с выводом о том, что продуцирование почвой СО2 более объективно отражает минерализационно-иммобилизационный цикл азота в целом, а не отдельные слагающие его процессы [29].
Влияние длительной инкубации почвы на микробный пул углерода. Почвенные микроорганизмы, использующие Cорг в качестве источника энергии и питания, выступают главным биотическим агентом трансформации органического вещества, а микробная биомасса является основным компонентом минерализуемого пула ПОВ [30]. В нашем эксперименте в результате повышения температуры и влажности основной инкубации содержание микробной биомассы при повторной инкубации уменьшилось, а внесение соломы увеличило долю Смб в Сорг с 1–2 до 2–4% (табл. 5). Практически двукратное увеличение микробного пула в результате внесения соломы было отмечено нами ранее и для почв, отобранных в полевых опытах [31].
Таблица 5.
Характеристика микробного пула почв (Смб) после 150 сут инкубации без соломы и с соломой при разных температуре и влажности
| Почва | Влажность основной инкубации, весовые % | Температура основной инкубации | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 8°С | 18°С | 28°С | ||||||||
| Смб | qCO2, мг С-СО2 в час/г Смб | Смб | qCO2, мг С-СО2 в час/г Смб | Смб | qCO2, мг С-СО2 в час/г Смб | |||||
| мг/кг | % от Сорг | мг/кг | % от Сорг | мг/кг | % от Сорг | |||||
| Почва без соломы | ||||||||||
| Серая лесная почва | 10 | 254 ± 1 | 2.8 | 1.96 | 225 ± 4 | 2.5 | 1.51 | 270 ± 20 | 3.1 | 0.91 |
| 25 | 177 ± 10 | 2.0 | 2.52 | 228 ± 9 | 2.6 | 0.97 | 227 ± 3 | 2.6 | 0.78 | |
| 40 | 180 ± 12 | 2.0 | 2.38 | 220 ± 8 | 2.6 | 0.93 | 183 ± 6 | 2.2 | 0.63 | |
| Среднее | 204 | 2.3 | 2.29 | 224 | 2.6 | 1.14 | 227 | 2.7 | 0.77 | |
| Чернозем оподзоленный | 10 | 228 ± 7 | 0.9 | 2.71 | 268 ± 5 | 1.1 | 1.88 | 266 ± 3 | 1.2 | 1.09 |
| 25 | 250 ± 1 | 1.0 | 1.84 | 234 ± 12 | 1.0 | 1.32 | 207 ± 1 | 0.9 | 0.92 | |
| 40 | 234 ± 4 | 1.0 | 1.66 | 238 ± 5 | 1.0 | 1.10 | 179 ± 4 | 0.8 | 0.91 | |
| Среднее | 237 | 1.0 | 2.07 | 247 | 1.0 | 1.43 | 217 | 1.0 | 0.97 | |
| Темно-каштановая почва | 10 | 345 ± 1 | 3.1 | 1.32 | 219 ± 1 | 2.0 | 2.25 | 328 ± 3 | 3.2 | 1.07 |
| 25 | 234 ± 6 | 2.1 | 1.39 | 272 ± 5 | 2.5 | 1.02 | 229 ± 14 | 2.3 | 1.11 | |
| 40 | 226 ± 3 | 2.1 | 1.62 | 239 ± 2 | 2.3 | 1.18 | 184 ± 19 | 1.9 | 1.23 | |
| Среднее | 268 | 2.4 | 1.44 | 243 | 2.3 | 1.48 | 247 | 2.5 | 1.14 | |
| Среднее | 236 | 1.9 | 1.93 | 238 | 2.0 | 1.35 | 230 | 2.0 | 0.96 | |
| Почва с соломой | ||||||||||
| Серая лесная почва | 10 | 351 ± 10 | 2.9 | 3.70 | 432 ± 5 | 3.6 | 1.27 | 440 ± 9 | 4.2 | 1.01 |
| 25 | 459 ± 18 | 3.8 | 1.87 | 407 ± 30 | 3.7 | 0.56 | 286 ± 15 | 2.9 | 0.62 | |
| 40 | 450 ± 4 | 4.3 | 1.68 | 407 ± 5 | 4.2 | 0.65 | 307 ± 0 | 3.3 | 0.65 | |
| Среднее | 420 | 3.7 | 2.42 | 415 | 3.8 | 0.83 | 344 | 3.4 | 0.76 | |
| Чернозем оподзоленный | 10 | 343 ± 1 | 1.2 | 4.56 | 359 ± 5 | 1.3 | 1.52 | 463 ± 1 | 1.7 | 1.15 |
| 25 | 438 ± 8 | 1.6 | 1.76 | 440 ± 4 | 1.7 | 1.24 | 337 ± 11 | 1.4 | 0.89 | |
| 40 | 380 ± 13 | 1.4 | 2.10 | 395 ± 16 | 1.6 | 1.12 | 239 ± 1 | 1.0 | 0.89 | |
| Среднее | 387 | 1.4 | 2.81 | 398 | 1.6 | 1.29 | 346 | 1.4 | 0.98 | |
| Темно-каштановая почва | 10 | 486 ± 13 | 3.5 | 3.45 | 599 ± 2 | 4.5 | 1.16 | 279 ± 2 | 2.2 | 0.99 |
| 25 | 506 ± 12 | 3.8 | 1.71 | 469 ± 11 | 3.9 | 1.00 | 302 ± 5 | 2.6 | 0.95 | |
| 40 | 516 ± 1 | 3.9 | 1.86 | 400 ± 3 | 3.4 | 1.31 | 335 ± 7 | 3.0 | 0.77 | |
| Среднее | 502 | 3.7 | 2.34 | 489 | 3.9 | 1.16 | 305 | 2.6 | 0.90 | |
| Среднее | 437 | 2.9 | 2.52 | 434 | 3.1 | 1.09 | 332 | 2.5 | 0.88 | |
Коэффициент qСО2 может служить для оценки устойчивости микробного сообщества, а значит и почвы в целом, к различным воздействиям [32], а также быть индикатором состояния почвы как биологического объекта [33]. Предполагается, что чем меньше величина qСО2, тем устойчивее данное сообщество микроорганизмов. Наши результаты показали, что длительное предшествовавшее воздействие температуры и влажности привело к снижению qСО2 при повторной инкубации, а внесение соломы – к повышению этих коэффициентов, т.е. чем выше была температура и влажность основной инкубации, тем устойчивее было в последующем микробное сообщество, а внесение соломы приводило к обратному результату.
Размер и устойчивость микробного пула может зависеть от доступности микроорганизмам углерода и азота. Как показали наши результаты, чем выше была температура и влажность на протяжении основной инкубации, тем активнее расходовался минерализуемый пул углерода, и тем больше в почвах накапливалось минерального азота. В результате внесения соломы, напротив, количество доступного микроорганизмам углеродного субстрата увеличивалось, а содержание Nмин уменьшалось. Доступность микроорганизмам углерода и азота сказалась на размере микробного пула и величинах дыхательного коэффициента qСО2.
После инкубации почв без соломы при 28°С и увлажнении 40 вес. % содержание в почвах Смб при повторной инкубации было самым низким в опыте и в среднем для 3-х почв составило 182 мг/кг, qСО2 был наименьшим, равняясь 0.92, т.е. истощение пула доступного углерода привело к уменьшению микробной биомассы, а накопление доступного азота способствовало созданию благоприятных, “комфортных” условий для микроорганизмов. После инкубации почв с соломой при 8°С и влажности 10 вес. %, напротив, содержание Смб было наибольшим и составило в среднем 393 мг/кг, qСО2 был самым высоким, равняясь 3.90. В таких гидротермических условиях солома в почвах разлагалась лишь на 9–25% от внесенной дозы, а в ходе повторной инкубации в условиях, не лимитирующих минерализацию (22°С и влажности 25 вес. %), неразложившаяся ранее солома активно минерализовалась, что привело к увеличению микробной биомассы. Крайне низкое содержание Nмин и качество углеродного субстрата, представленного в основном соломой, способствовали созданию “некомфортных”, стрессовых условий для микробного сообщества в этих вариантах опыта.
Оценка вклада температуры, влажности и внесения соломы в изменчивость почвенных пулов углерода и азота. Установлено, что наиболее значимым фактором, определяющим изменчивость пулов общего, потенциально-минерализуемого и микробного углерода и общего азота было внесение соломы в дозе 1% от массы почвы (табл. 6). Изменчивость пула минерального азота, микробный метаболический коэффициент и соотношение Сорг : Nобщ определялись повышением температуры основной инкубации с 8 до 28°С. Вклад влажности в изменчивость изученных показателей не был определяющим в условиях обсуждаемого эксперимента.
Таблица 6.
Вклад изученных факторов (температуры, влажности и внесения соломы) в изменчивость пулов углерода и азота в почвах, %
| Показатель пулов углерода или азота | Т, °С | Влажность, вес. % | Внесение соломы |
|---|---|---|---|
| Сорг, мг/кг | 20.0 (–1.07) | 7.8 (–1.05) | 47.9 (+1.13) |
| Nобщ, мг/кг | 17.8 (+1.02) | 1.5 (–1.01) | 44.7 (+1.10) |
| Сорг : Nобщ | 43.2 (–1.13) | 11.6 (–1.06) | 19.7(+1.08) |
| Спм, мг/кг | 16.4 (+1.79) | 12.7 (+1.88) | 56.2 (+4.71) |
| Смб, мг/кг | 7.7 (–1.16) | 17.6 (–1.31) | 52.0 (+1.61) |
| qCO2, мг С-СО2/ч/г Смб | 55.6 (–2.57) | 10.1 (–1.46) | 5.5 (+1.30) |
| N-NH4, мг/кг (вл. 10–25 вес. %) | 28.7 (–1.47) | 0.9 (+1.01) | 25.7 (–1.48) |
| N-NH4, мг/кг (вл. 25–40 вес. %) | 11.3 (–1.25) | 8.2 (+1.19) | 17.2 (–1.34) |
| N-NO3, мг/кг (вл. 10–25 вес. %) | 65.0 (+4.42) | 9.5 (+1.96) | 19.3 (–1.97) |
| N-NO3, мг/кг (вл. 25–40 вес. %) | 54.3 (+4.59) | 18.8 (–2.16) | 8.6 (–1.76) |
| Nмин, мг/кг (вл. 10–25 вес. %) | 40.3 (+2.09) | 13.4 (+1.54) | 25.2 (–1.77) |
| Nмин, мг/кг (вл. 25–40 вес. %) | 49.6 (+2.11) | 16.7 (–1.50) | 15.8 (–1.59) |
ЗАКЛЮЧЕНИЕ
Минерализация органического вещества в почвах 3-х типов больше зависела от внесения соломы и от гидротермических условий, в которых проходила инкубация, чем от содержания Сорг в почвах (0.9–2.5%). По влиянию на минерализацию изученные факторы образовывали следующий ряд: внесение соломы (1% от массы почвы) > > температура (8–28°С) > влажность (10–40 вес. %). Различия скорости минерализации и зависимости ее от температуры на разных этапах 150-суточной инкубации можно объяснить преимущественным использованием микроорганизмами наиболее доступного и наименее термочувствительного субстрата, по мере расходования которого возрастает вклад в продуцирование СО2 менее доступных и более термочувствительных соединений.
Вклад температуры, влажности и внесения соломы в изменчивость размера потенциально-минерализуемого пула углерода составил соответственно 16, 13 и 56% в среднем в опыте. Внесение соломы увеличило содержание Сорг в почвах в начале инкубации в 1.2–1.4 раза, долю Спм в Сорг – в 3–5 раз. За 150 сут инкубации в почвах в разных гидротермических условиях минерализовалось от 9–25 до 74–87% внесенной соломы. Вклад внесения соломы в изменчивость Сорг и Nобщ в конце инкубации также был наибольшим из изученных факторов, однако абсолютное увеличение этих пулов было незначительным. Чем выше была температура и влажность, тем меньше становилось соотношение Сорг : Nобщ в почвах через 150 сут инкубации.
Основным фактором, влияющим на изменчивость пула минерального азота в почвах, являлась температура. За 150 сут при 18 и 28°С в почвах в среднем в опыте накопилось в 2 раза больше Nмин, чем при 8°, при 25%-ном увлажнении – в 1.5 раза больше, чем при увлажнении 10 и 40 вес.%. Уменьшение активности минерализации органических азотсодержащих соединений почвы может быть одной из причин снижения урожайности сельскохозяйственных культур в холодные и (или) засушливые годы из-за ухудшения условий азотного питания растений. Повышение температуры способствовало повторной минерализации азота, иммобилизованного при внесении соломы.
Изменение доступности углерода и азота в результате 150-суточной инкубации почвенных образцов с внесением и без внесения соломы в разных гидротермических условиях сказалось на размере микробного пула и величине дыхательного коэффициента qСО2, которые были установлены в ходе повторной инкубации при одинаковой температуре и влажности. Размер микробной биомассы зависел от доступности микроорганизмам углерода, а создание благоприятных, “комфортных” условий для микроорганизмов было связано с содержанием минерального азота в почве.
Благодарность. Изучение почвенных пулов углерода проведено при поддержке РФФИ, грант №17-04-00707_а, почвенных пулов азота – при поддержке государственного задания рег. № АААА-А18-118013190177-9.
Список литературы
Семенов В.М., Когут Б.М. Почвенное органическое вещество. М.: ГЕОС, 2015. 233.
Семенов В.М., Ходжаева А.К. Агроэкологические функции растительных остатков в почве // Агрохимия. 2006. № 7. С. 63–81.
Русакова И.В. Теоретические основы и методы управления плодородием почв при использовании растительных остатков в земледелии. Иваново: Издательско-полиграфический комплекс “ПрессСто”, 2016. 131 с.
Чуян Н.А., Чуян О.Г., Брескина Г.М. Агрофизические показатели чернозема типичного в условиях использования побочной продукции на удобрение при разных уровнях удобренности // Достиж. науки и техн. АПК. 2013. № 2. С. 3–5.
Six J., Bossuyt H., Degryze S., Denef K. A history of research on the link between (micro)aggregates, soil biota, and soil organic matter dynamics // Soil Tillage Res. 2004. V. 79. № 1. P. 7–31.
Серая Т.М., Богатырева Е.Н., Бирюкова О.М., Мезенцева Е.Г. Высвобождение элементов питания при заделке соломы в дерново-подзолистые почвы в зависимости от ее видового состава и удобрения азотом // Агрохимия. 2013. № 3. С. 52–59.
Шарков И.Н., Самохвалова Л.М., Мишина П.В., Шепелев А.Г. Влияние пожнивных остатков на состав органического вещества чернозема выщелоченного Западной Сибири // Почвоведение. 2014. № 4. С. 473–479.
Семенов В.М., Кузнецова Т.В., Иванникова Л.А., Семенова Н.А., Лисова Е.П. Участие растительной биомассы в формировании активной фазы почвенного азота // Агрохимия. 2001. № 7. С. 5–12.
Русакова И.В. Биологические свойства дерново-подзолистой супесчаной почвы при длительном использовании соломы на удобрение // Почвоведение. 2013. № 12. С. 1485–1493.
Семенов В.М., Кузнецова Т.В., Ходжаева А.К., Семенова Н.А., Кудеяров В.Н. Почвенная эмиссия закиси азота: влияние природных и агрогенных факторов // Агрохимия. 2004. № 1. С. 30–39.
Hadas A., Kautsky L., Goek M., Kara E.E. Rates of decomposition of plant residues and available nitrogen in soil, related to residue composition through simulation of carbon and nitrogen turnover // Soil Biol. Biochem. 2004. V. 36. № 2. P. 255–266.
Jensen L.S., Mueller T., Magid J., Nielsen N.E. Temporal variation of C and N mineralization, microbial biomass and extractable organic pools in soil after oilseed rape straw incorporation in the field // Soil Biol. Biochem. 1997. V. 29. № 7. P. 1043–1055.
Korsaeth A., Henriksen T.M., Bakken L.R. Temporal changes in mineralization and immobilization of N during degradation of plant material: implications for the plant N supply and nitrogen losses // Soil Biol. Biochem. 2002. V. 34. № 6. P. 789–799.
Использование соломы как органического удобрения / Под ред. Мишустина Е.Н. М.: Наука, 1980. 270 с.
Семенов В.М., Семенов А.М., Ван Бругген А.Х., Феррис Х., Кузнецова Т.В. Трансформация азота почвы и растительных остатков сообществом микроорганизмов и микроскопических животных // Агрохимия. 2002. № 1. С. 5–11.
Recous S., Robin D., Darwis D., Mary B. Soil inorganic N availability: effect on maize residue decomposition // Soil Biol. Biochem. 1995. V. 27. № 12. P. 1529–1533.
Тулина А.С., Семенов В.М. Оценка чувствительности минерализуемого пула почвенного органического вещества к изменению температуры и влажности // Почвоведение. 2015. № 8. С. 952–962.
Семенов В.М., Иванникова Л.А., Кузнецова Т.В., Семенова Н.А., Тулина А.С. Минерализуемость органического вещества и углеродсеквестрирующая емкость почв зонального ряда // Почвоведение. 2008. № 7. С. 819–832.
Anderson T.-H., Domsch K.H. Maintenance requirements of actively metabolizing microbial populations under in situ conditions // Soil Biol. Biochem. 1985. V. 17. № 2. P. 197–203.
Тулина А.С., Семенов В.М., Розанова Л.Н., Кузнецова Т.В., Семенова Н.А. Влияние влажности на стабильность органического вещества почв и растительных остатков // Почвоведение. 2009. № 11. С. 1333–1340.
Ларионова А.А., Мальцева А.Н., Лопес де Гереню В.О., Квиткина А.К., Быховец С.С., Золотарева Б.Н., Кудеяров В.Н. Влияние температуры и влажности на минерализацию и гумификацию лиственного опада в модельном инкубационном эксперименте // Почвоведение. 2017. № 4. С. 438–448.
Andersen M.K., Jensen L.S. Low soil temperature effects on short-term gross N mineralization-immobilisation turnover after incorporation of a green manure // Soil Biol. Biochem. 2001. V. 33. P. 511–521.
Brye K.R., Norman J.M., Nordheim E.V., Gower S.T., Bundy L.G. Refinements to an in-situ soil core technique for measuring net nitrogen mineralization in moist, fertilized agricultural soil // Agron. J. 2002. V. 94. P. 864–869.
Кузякова И.Ф., Штар К. Изучение динамики нетто-минерализации азота в катене на лессовидных отложениях с помощью анализа временных рядов // Почвоведение. 2006. С. 443–449.
Романенков В.А., Павлова В.Н., Беличенко М.В. Оценка климатических рисков при возделывании зерновых культур на основе региональных данных и результатов длительных опытов Геосети // Агрохимия. 2018. № 1. С. 77–86.
Колсанов Г.В. Солома как удобрение в зернопропашном севообороте на черноземе лесостепи Поволжья // Агрохимия. 2006. № 5. С. 30–40.
Шарков И.Н., Колбин С.А., Прозоров А.С., Самохвалова Л.М. Плодородие чернозема выщелоченного и урожайность яровой пшеницы при многолетнем удалении соломы с поля в лесостепи Западной Сибири // Агрохимия. 2016. № 11. С. 12–18.
Серая Т.М., Богатырева Е.Н., Кирдун Т.М., Бирюкова О.М., Белявская Ю.А., Торчило М.М. Влияние запашки побочной продукции и минеральных удобрений на продуктивность звена севооборота и агрохимические показатели дерново-подзолистой супесчаной почвы // Агрохимия. 2015. № 11. С. 32–38.
Кузнецова Т.В., Тулина А.С., Розанова Л.Н., Семенов В.М., Кудеяров В.Н. О сопряженности процессов метаболизма углерода и азота в почве // Почвоведение. 1998. № 7. С. 832–839.
Семенов В.М., Тулина А.С. Сравнительная характеристика минерализуемого пула органического вещества в почвах природных и сельскохозяйственных экосистем // Агрохимия. 2011. № 12. С. 53–63.
Семенов В.М., Когут Б.М., Лукин С.М., Шар-ков И.Н., Русакова И.В., Тулина А.С., Лазарев В.И. Оценка обеспеченности почв активным органическим веществом по результатам длительных полевых опытов // Агрохимия. 2013. № 3. С. 19–31.
Anderson T.-H., Domsch K.H. Application of eco-physiological quotients (qCO2 and qD) on microbial biomasses from soils of different cropping histories // Soil Biol. Biochem. 1990. V. 22. № 2. P. 251–255.
Ананьева Н.Д., Благодатская Е.В., Демкина Т.С. Пространственное и временное варьирование микробного метаболического коэффициента в почвах // Почвоведение. 2002. № 10. С. 1233–1241.
Дополнительные материалы отсутствуют.
Инструменты
Агрохимия


