Агрохимия, 2020, № 12, стр. 50-63
Подвижность и параметры миграции Zn в системе чернозем типичный–растения ячменя
В. С. Анисимов 1, *, Л. Н. Анисимова 1, Л. М. Фригидова 1, А. И. Санжаров 1, Ю. Н. Корнеев 1, Р. А. Фригидов 1, Д. В. Дикарев 1
1 Всероссийский научно-исследовательский институт радиологии и агроэкологии
249030 Калужская обл., Обнинск, Киевское шоссе, 109 км, Россия
* E-mail: vsanisimov@list.ru
Поступила в редакцию 03.03.2020
После доработки 18.05.2020
Принята к публикации 11.09.2020
Аннотация
В вегетационных опытах с ячменем на черноземе типичном, в который дополнительно вносили Zn, установлено, что концентрация металла в почвенном растворе уменьшалась со временем, а относительное содержание подвижных форм Zn достоверно не изменялось, но оно возрастало с увеличением концентрации металла в почве. На основании данных динамики прироста биомассы ячменя, накопления и выноса Zn разными органами растений установлены и формализованы закономерности, параметры которых отражают особенности динамики накопления биомассы и выноса Zn ячменем. Установлено, что с ростом количества внесенного Zn доля выноса металла в результате конвективного переноса снижалась. Изучено изменение кислотности почвенных растворов, извлеченных из чернозема разных вариантов опыта.
ВВЕДЕНИЕ
Корневое поглощение микроэлементов растениями зависит как от эдафических, так и биологических факторов и является “одним из важнейших факторов жизнедеятельности растений” [1]. Для количественного описания подобных процессов наряду с простыми эмпирическими моделями, имеющими ограниченное применение, широко используются полумеханистические модели поглощения элементов питания и микроэлементов растениями [1–6]. Хотя в этих моделях исследователи и стараются учесть механизмы процессов, происходящих при корневом поглощении микроэлементов растениями, полностью освободиться от необходимости использования эмпирических зависимостей не удается [1, 7]. К основным механизмам относятся: процессы сорбции–десорбции ионов микроэлементов на границе раздела твердой и жидкой фаз, конвективно-диффузионное передвижение ионов к поверхности корня, поглощение их апопластом и переход в симпласт с реализацией механизмов активного и пассивного переноса через плазмаллемму, рост корневой системы и изменение площади рабочей поверхности корней [1, 7]. Скорость поступления ионов в растения контролируется главным образом скоростью их вступления в контакт с поглощающей поверхностью корней, а последняя, в свою очередь, зависит от интенсивности 3-х процессов [2]: роста корней, сопровождающегося изменением их рабочей поверхности и проникновением в новые участки слоя почвы, конвективного и диффузионного массопереноса ионов через поверхность раздела почвенный раствор–поверхность корня.
В работах [1, 2] была предложена достаточно простая конвективно-диффузионная полумеханистическая модель корневого поглощения ионов ТМ. В ней количественно описано поглощение ионов, обусловленное 3-мя вышеуказанными процессами, исходя из линейного конвективно-диффузионного потока ионов к рассматриваемой в виде плоскости поглощающей поверхности корней, площадь которой изменяется во времени.
Используя подходы, предложенные вышеупомянутыми исследователями, были заложены вегетационные опыты с внесением в почву различных доз Zn для изучения в динамике процессов прироста биомассы тест-растений, изменения концентрации металла в надземных частях и корнях растений, изменения площади рабочей поверхности корней, выноса Zn с надземной биомассой и корнями. Также были исследованы динамика содержания доступных растениям форм Zn в почве и переход его в почвенный раствор. Цель работы – оценка в контролируемых условиях вегетационного опыта параметров процесса массопереноса ионов цинка в корни и надземные органы растений ячменя.
МЕТОДИКА ИССЛЕДОВАНИЯ
Поведение Zn в системе почва–растение изучали в вегетационных опытах в контролируемых тепличных условиях: температура 20–27°С, относительная влажность воздуха 60–70%, влажность почвы 64% ПВ (при более низкой влажности почвы возникали сложности с отбором центрифужных почвенных растворов (ЦПР)). Объектом исследования служил ячмень (Hordeum vulgare L.) сорта Зазерский 85, выращиваемый на черноземе типичном (Курская обл., Медвенский р-н). Физические и химические показатели почвы (табл. 1) определяли общепринятыми методами [8, 9]: pHKCl (pH$_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}$) – потенциометрическим методом в суспензии почвы в 1 М растворе KCl (дистиллированной воде) при соотношении твердой и жидкой фаз 1 : 2.5, гранулометрический состав почв – пипеточным методом Качинского [8, 10], содержание гумуса – по методу Тюрина, гидролитическую кислотность – по Каппену, сумму поглощенных оснований – по Каппену–Гильковицу, содержание подвижных форм P2O5 – по Чирикову и K2O – по Масловой. Предварительная подготовка чернозема перед определением исходных физико-химических характеристик включала доведение его до воздушно-сухого состояния и просеивание через сито с диаметром отверстий 1 мм. Растения выращивали в пластиковых сосудах, содержащих 5 кг (в пересчете на абсолютно-сухую массу) чернозема типичного. В почву были высажены пророщенные 3-суточные семена в количестве 25 шт./сосуд. Перед посевом в почву вносили Zn (в виде водного раствора нитрата) при тщательном перемешивании и разминании образующихся почвенных комочков в количестве 100, 250, 500 мг/кг почвы. Затем аналогичным образом добавляли питательные элементы в виде водных растворов солей (NH4NO3, KH2PO4, K2SO4) из расчета N200P100K100. При этом в каждом варианте, включая контрольный, количество внесенного азота корректировали с помощью азотнокислого аммония до указанной величины содержания его в почве (в варианте с максимальной дозой Zn содержание азота, внесенного в виде Zn(NO3)2, составляло 215 мг/кг и корректировку дозы не проводили).
Таблица 1.
Основные характеристики чернозема типичного
| Показатель | Величина показателя |
|---|---|
| pHKCl | 5.49 ± 0.01 |
| pH$_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}$ | 6.23 ± 0.02 |
| Гумус, % | 5.13 ± 0.19 |
| Массовая доля фракции (мм) в почве, % | |
| 1–0.25 | 0.77 |
| 0.25–0.05 | 0.47 |
| 0.05–0.01 | 50.6 |
| 0.01–0.005 | 10.7 |
| 0.005–0.001 | 8.52 |
| <0.001 | 29.0 |
| Физическая глина (<0.01 мм) | 48.1 |
| Илистая фракции (<2 μм), % | 33.4 |
| Hг, мг-экв/100 г почвы | 3.17 ± 0.01 |
| Сумма обменных оснований, мг-экв/100 г почвы | 34.4 ± 0.2 |
| Обменный K2O, мг/кг (по Масловой) | 124 ± 2.4 |
| Подвижный P2O5, мг/кг (по Чирикову) | 120 ± 1.3 |
| Валовое содержаниеZn в нативной почве, мг/кг | 55.7 ± 2.2 |
После внесения растворов солей почву в сосудах инкубировали, поддерживая заданную в эксперименте влажность в течение 21 сут перед посадкой проростков ячменя. Выбор доз Zn обусловлен соответствием их ранее установленному диапазону оптимальных концентраций металла в исследованной почве [11, 12], при которых не отмечены эффекты фитотоксичности, в то же время фиксировали достаточно высокие концентрации Zn в разных частях растений и квазиравновесных почвенных растворах, позволяющие надежно детектировать в них металл. Контролем для каждого из вариантов Zn0, Zn100, Zn250, Zn500 являлся соответствующий вариант без растений (черный пар).
Отдельные показатели регистрировали в динамике. Для этого из сосудов через 7, 14, 21, 30, 45 и 70 сут отбирали по 2 растения и проводили анализ морфометрических показателей надземных органов. В корнях определяли содержание Zn, а также их сырую и сухую массу (после размывания в сосуде и отмывания от почвенных частиц деионизированной водой). Параллельно из почв извлекали ЦПР. Концентрацию Zn в растениях, содержание подвижных и кислоторастворимых форм элемента в почвах определяли в соответствии с методикой [14], а также с помощью ее модификаций, изложенных в работах [15, 16]. Содержание подвижных форм ТМ определяли экстракцией с помощью ацетатно-аммонийного буфера (pH 4.8) и вытяжки 1 M HCl. Валовое количество цинка в почве определяли по методу Обухова–Плехановой [17]. Воздействие загрязнения чернозема Zn на состояние растений оценивали в динамике.
После уборки урожая были определены морфометрические показатели: длина растений, количество стеблей на одно растение, количество колосьев, масса корней, соломы и колоса, было определено содержание макро- и микроэлементов в зеленой массе, в соломе, корнях и зерне.
Ежедневно проводили контроль массы сосудов с вегетирующими растениями и без них, долив их дистиллированной водой до влажности, соответствующей 64% ПВ. Формирующийся суточный дефицит массы почвы в последних был обусловлен физическим испарением, а различия в массе сосудов с вегетирующими растениями за 1 сут были связаны с эвапотранспирацией. Дефицит влаги в сосудах с растениями, обусловленный совместными процессами десукции и транспирации рассчитывали по разности между дефицитом влаги, обусловленным эвапотранспирацией (в вариантах с растениями) и физическим испарением (в вариантах исследованных почв без растений). Опыты проводили в четырехкратной повторности. Квазиравновесные почвенные растворы были получены с помощью центрифугирования в соответствии с методикой [18]. Использовали центрифужные стаканы с вкладышами (куда помещалась влажная почва), изготовленные из тефлона (ПТФЭ). Вкладыши имели перфорированное дно. В извлеченных почвенных растворах определяли pH, содержание Zn, микро- и макроэлементов. Концентрацию Zn в анализированных растворах определяли методом ICP-OES на приборе Liberty II фирмы “Varian” в соответствии с [19].
Прирост надземной биомассы растений описывали с помощью логистической (S-образной) функции [18, 20–22]
где Mmax – максимальная возможная масса 1 растения, г; M0 – начальная масса 1-го растения (расчетная величина), г; μ – удельная скорость прироста биомассы растения, сут–1; t – время, сут.Зависимость изменения концентраций Zn в вегетативных органах растений от времени аппроксимировали с помощью уравнения Вуда [23]:
где а (мг кг–1 сут–b), b и c (сут–1) – параметры.Динамику выноса Zn с биомассой описывали с помощью логистической функции:
где Wmax – максимально возможный вынос Zn одним растением, мкг; W0 – начальный вынос (расчетная величина); u – константа выноса Zn с биомассой, сут–1, t – время, сут.Величины параметров уравнений (1), (2) и (3) Mmax, M0, Wmax, W0, u, μ, a, b и c подбирали с использованием модуля “Поиск решения” программы Excel. При этом применяли алгоритм последовательных итераций, использующий минимизацию ошибки E = Σ[Kc(расч) – Kc(измерен)]2. Статистический анализ экспериментальных данных проводили стандартными методами с использованием MS-Excel в соответствии с требованиями, изложенными в работах [24, 25].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В течение вегетационного периода из почвенных сосудов сразу после высаживания пророщенных семян ячменя (на 21-е сут после внесения Zn в почву), а также соответственно на 51-, 71-, 83- и 120-е сут после внесения Zn в почву извлекали квазиравновесные почвенные растворы методом центрифугирования. Динамика изменения концентрации Zn в них представлена на рис 1. Установлено, что уменьшение концентрации Zn в почвенном растворе в зависимости от времени можно удовлетворительно описать (после исключения промахов) степенными уравнениями:
Рис. 1.
Динамика концентрации Zn в квазиравновесном почвенном растворе, извлеченном из типичного чернозема вариантов “черный пар” и “ячмень”, мг/дм3: (а) – Zn0, (б) – Zn100, (в) – Zn250, (г) – Zn500. То же на рис. 2–9. Горизонтальные сплошные линии на графиках – средние концентрации цинка в почвенных растворах за период проведения опытов.
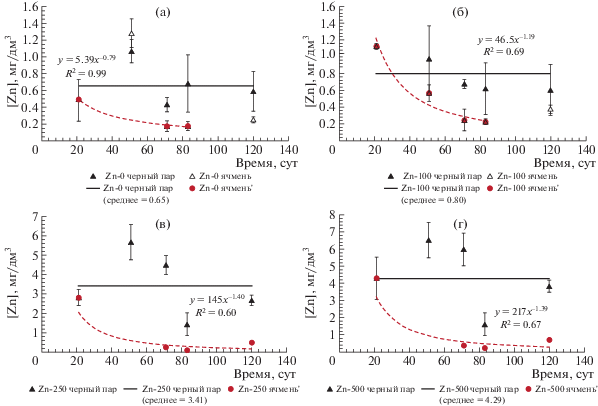
Снижение концентрации Zn в почвенных растворах, отобранных из сосудов с вегетирующими растениями особенно заметное в сравнении с концентрацией металла в почвенных растворах, извлеченных из вариантов опыта с черным паром, связано как с истощением запаса водорастворимых форм Zn в почве в результате непрерывного поглощения корнями растений, не компенсируемого десорбцией Zn из почвенного поглощающего комплекса (ППК) в почвенный раствор, так и с процессами возможной трансформации подвижных (доступных растениям) форм нахождения металла в малоподвижные (“фиксации” Zn). На кривых зависимостей [Zn]почв.р-р = f(t), полученных для вариантов опыта с растениями отмечено увеличение концентрации металла в почвенных растворах на 120-е сут с начала инкубации Zn в почве (100-е сут с момента посадки проростков, фаза развития ячменя – восковая спелость) по сравнению с 83-ми сут (фаза развития ячменя – предмолочная спелость). Это объясняется значительным снижением в первом случае поступления ионов цинка в корни растений ввиду засыхания последних и, как следствие, преобладания процессов десорбции Zn из ППК в почвенный раствор по сравнению с поглощением металла растениями. В ходе экспериментов проводили изучение динамики трансформации подвижных (извлекаемых 1 M CH3COONH4, pH 4.8) форм нахождения Zn в типичном черноземе. Результаты представлены на рис. 2. Графический анализ полученных результатов показал, что отрицательная динамика исследованного показателя прослежена лишь в качестве тенденции, не подкрепленной достоверными статистическими данными.
Рис. 2.
Динамика содержания подвижного Zn (извлекаемого 1 M CH3COONH4, pH 4.8) в типичном черноземе вариантов “черный пар” и “ячмень”, мг/кг.
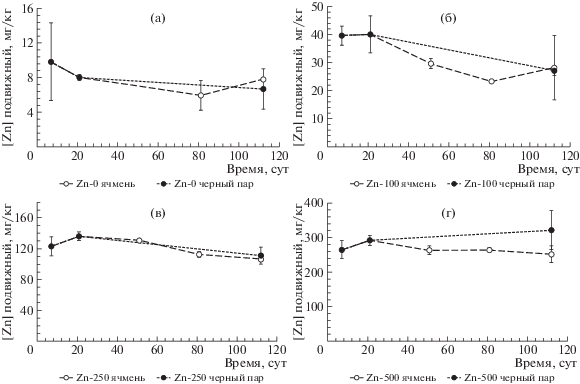
В целом содержание подвижных форм Zn в почве (в % от общего содержания) возрастало с увеличением количества внесенного в почву металла. Полученная зависимость хорошо описывается с помощью уравнения асимптоты (рис. 3): Znподв.(%) = Znподв.,max(%) × (1 – exp(–a × [Zn]вал.), где Znподв.(%) – содержание подвижного цинка в почве; Znподв., max(%) – максимальное содержание подвижного цинка в почве – расчетная величина (параметр); a – параметр, (кг мг–1); [Zn]вал. – общее содержание цинка в почве, (мг кг–1) – независимая переменная. Величины параметров, подобранные по критерию минимизации ошибки между расчетными и экспериментальными данными Znподв.(%) (E = Σ[Kc(расч) – Kc(измерен)]2), составили: Znподв.,max(%) = 61.5 ± 9.8% (t = 6.27, p = = 0.024 при ν = 2), a = 3.1 × 10–3 кг мг–1 (t = 6.27, p = 0.024 при ν = 2); t – критерий значимости параметра, p – уровень значимости при числе степеней свободы, равном ν.
Рис. 3.
Среднее (для всех сроков отбора) содержание подвижного Zn, (извлекаемого 1 M CH3COONH4, pH 4.8) в типичном черноземе, % от валового.
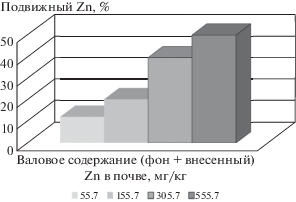
Данные прироста надземной массы ячменя аппроксимировали с помощью уравнения логистической кривой (рис. 4). Величины параметров логистической кривой Mmax (г) M0 (г), μ (сут–1) для типичного чернозема при различных дозах внесенного в почву Zn представлены в табл. 2. Положительная динамика изменения биомассы отмечена приблизительно до 75-ти сут, после чего увеличение биомассы не наблюдали.
Рис. 4.
Динамика изменения надземной биомассы ячменя, выращенного на черноземе типичном до фазы созревания, в пересчете на одно растение, г × растение–1.
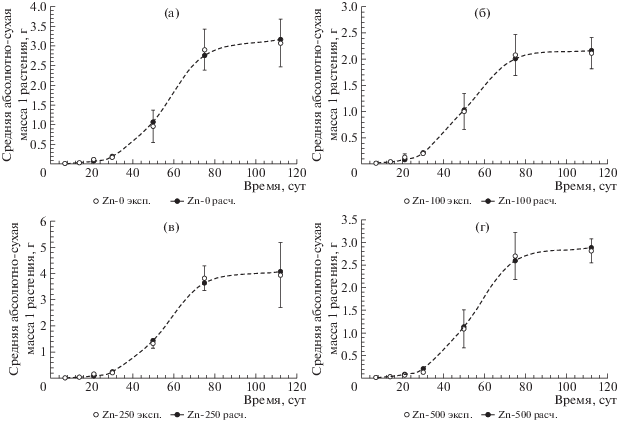
Таблица 2.
Количественные параметры логистических кривых изменения сухой надземной биомассы ячменя (в пересчете на одно растение), выращенного на черноземе типичном до фазы созревания зерна
| Вариант | ν* | Mmax, г | t; p** | M0, г | t; p | μ, сут–1 | t; p |
|---|---|---|---|---|---|---|---|
| Zn0 | 4 | 3.12 ± 0.07 | 46.1; 1 × 10–6 | 0.003 ± 0.002 | 1.41; 0.23 | 0.13 ± 0.01 | 9.15; 8 × 10–4 |
| Zn100 | 4 | 2.16 ± 0.05 | 45.8; 1 × 10–6 | 0.008 ± 0.004 | 1.87; 0.13 | 0.11 ± 0.01 | 9.94; 6 × 10–4 |
| Zn250 | 4 | 4.00 ± 0.09 | 47.0; 1 × 10–6 | 0.002 ± 0.002 | 1.13; 0.32 | 0.14 ± 0.02 | 7.73; 1.5 × 10–3 |
| Zn500 | 4 | 2.83 ± 0.03 | 103.6; 1 × 10–7 | 0.002 ± 0.001 | 2.48; 0.07 | 0.13 ± 0.01 | 16.4; 8 × 10–5 |
В целом можно выделить тенденцию к увеличению надземной биомассы по мере роста количества внесенного в чернозем цинка до дозы Zn500 (при последней дозе металла наблюдали уменьшение биомассы). Снижение надземной биомассы ячменя при дозе Zn100, начиная с 50-х сут (табл. 2, рис. 4) было обусловлено однократным негативным неконтролируемым внешним воздействием, вызвавшем в дальнейшем угнетение растений данного варианта.
Полученные данные динамики накопления (концентрации) Zn в надземных органах ячменя показали, что содержание Zn (равно как и других двухвалентных катионов) в растениях в целом увеличивалось в ходе онтогенеза. Зависимость изменения концентраций Zn в вегетативных органах растений (мг/кг сухой массы) от времени (рис. 5) имеет вид одновершинной кривой с выраженной положительной ассиметрией (крутая левая ветвь и полого падающая правая). Ввиду сложного характера экспериментально установленной зависимости [Zn]раст. = f(t) для надземной биомассы ячменя подобрать идеальное уравнение для аппроксимации затруднительно. Тем не менее, подобная зависимость, как отмечено выше, может быть описана уравнением Вуда [23], отражающим взаимодействие конкурирующих процессов накопления в фитомассе и перераспределения Zn между разными органами растений. С использованием уравнения (2) удалось объяснить 62% вариабельности результативного признака в варианте Zn0 и 77, 51, 73% – в вариантах Zn100, Zn250, Zn500 соответственно.
Рис. 5.
Динамика накопления Zn в надземной фитомассе ячменя (в пересчете на сухую массу) до фазы созревания, выращенного на типичном черноземе, мг/кг.
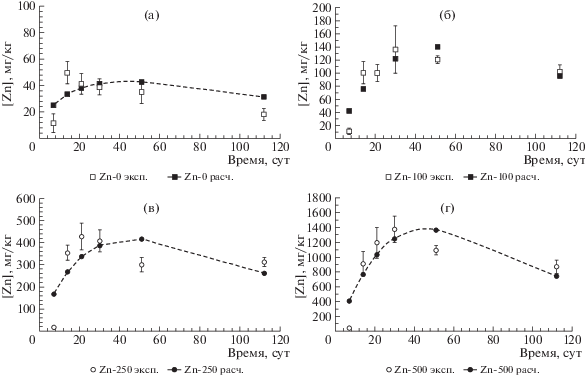
Величины параметров а (мг кг–1 сут–b), b и c (сут–1), рассчитанные для разных вариантов опыта на черноземе типичном представлены в табл. 3. Динамика выноса Zn с надземной биомассой в пересчете на одно растение представлена на рис. 6. Величины параметров полученной логистической кривой Wmax (мкг) W0 (мкг), u (сут–1) для типичного чернозема при различных дозах внесенного в почву Zn представлены в табл. 4. С использованием уравнения (2) и подобранных параметров удалось объяснить 93 (вариант Zn0) и 99% вариабельности результативного признака (варианты Zn100, Zn250, Zn500).
Таблица 3.
Количественные параметры кривых, аппроксимирующих концентрации Zn в сухой надземной биомассе ячменя, выращенного на черноземе типичном до фазы созревания, от времени
| Вариант | a, мг кг–1 сут–b | b | c, сут–1 |
|---|---|---|---|
| Zn0 | 5.05 | 0.88 | 0.03 |
| Zn100 | 6.50 | 1.04 | 0.02 |
| Zn250 | 34.8 | 0.88 | 0.02 |
| Zn500 | 51.0 | 1.16 | 0.02 |
Рис. 6.
Динамика выноса Zn надземной фитомассой ячменя, выращенного на типичном черноземе до фазы созревания, мкг/растение.
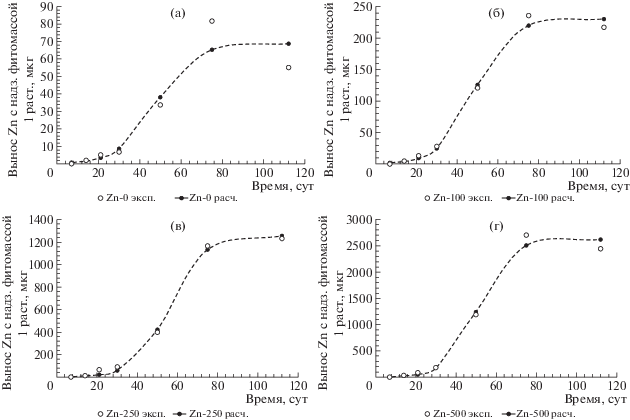
Таблица 4.
Количественные параметры логистических кривых, описывающих динамику выноса Zn надземной фитомассой ячменя (мкг/растение), выращенного на типичном черноземе до фазы созревания
| Вариант | ν | Wmax, мкг | t; p | W0, мкг | t; p | U, сут–1 | t; p |
|---|---|---|---|---|---|---|---|
| Zn0 | 4 | 68.9 ± 7.93 | 8.7; 3.3 × 10–4 | 0.375 | –; – | 0.11 ± 0.01 | 9.2; 2.6 × 10–4 |
| Zn100 | 4 | 231 ± 10 | 24.0; 2 × 10–5 | 0.72 ± 0.81 | 0.89; 0.43 | 0.12 ± 0.02 | 5.03; 7 × 10–3 |
| Zn250 | 4 | 1260 ± 40 | 31.6; 6 × 10–6 | 1.11 ± 1.09 | 1.02; 0.37 | 0.12 ± 0.02 | 6.63; 2.7 × 10–3 |
| Zn500 | 4 | 2600 ± 1 | 23.9; 2 × 10–5 | 0.46 | –; – | 0.17 ± 0.08 | 2.12; 0.10 |
В ходе вегетационного опыта были оценены количественные параметры конвективного потока влаги из почвы в корни растений и сопряженного с ним массопереноса ионов цинка. На основании полученных данных была оценена скорость транспирации влаги растениями ячменя. Полученные опытные данные удалось удовлетворительно аппроксимировать с помощью логистической функции (рис. 7):
(4)
$T(t) = \frac{{{{T}_{{\max }}}}}{{1 + \frac{{{{T}_{{\max }}}}}{{{{T}_{0}}}}\exp ( - \gamma t)}},$(5)
$T({{t}_{{(i)}}} - {{t}_{{(55)}}}) = \frac{{T_{{\max }}^{'}}}{{1 + \frac{{T_{{\max }}^{'}}}{A}\exp [\lambda ({{t}_{{(i)}}} - {{t}_{{(55)}}})]}},$Рис. 7.
Динамика транспирации влаги надземными органами ячменя, выращенного на черноземе типичном до фазы созревания (в пересчете на одно растение), мл × раст–1 × сут–1.
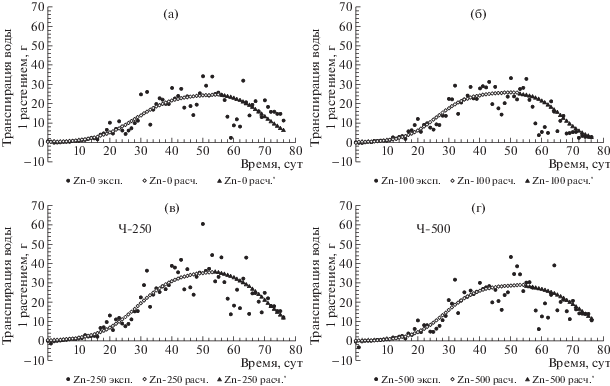
Таблица 5.
Количественные параметры транспирации влаги надземными частями ячменя, выращенного на черноземе типичном, на этапе роста транспирации до фазы цветения
| Вариант | Tmax | T0 | γ, сут–1 |
|---|---|---|---|
| мл H2O/(растение × сут) | |||
| Zn0 | 25.0 | 0.26 | 0.161 |
| Zn100 | 26.0 | 0.17 | 0.193 |
| Zn250 | 36.5 | 0.36 | 0.159 |
| Zn500 | 29.5 | 0.13 | 0.186 |
Таблица 6.
Количественные параметры транспирации влаги надземными частями ячменя, выращенного на черноземе типичном, на этапе уменьшения транспирации до фазы созревания зерна
| Вариант | $T_{{\max }}^{'}$ | A | λ, сут–1 |
|---|---|---|---|
| мл H2O/(растение × сут) | |||
| Zn0 | 25.9 | 470 | 0.155 |
| Zn100 | 26.3 | 310 | 0.230 |
| Zn250 | 37.9 | 490 | 0.165 |
| Zn500 | 29.9 | 580 | 0.170 |
Вынос Zn из почвы с конвективным потоком влаги в пересчете на одно растение можно получить, используя данные транспирации воды растениями ячменя в течение вегетационного периода, представленные на рис. 7, формализованные с помощью логистических уравнений, параметры которых приведены в табл. 5, 6, и данных динамики концентрации [Zn] в почвенных растворах в течение вегетационного периода (рис. 1).
С использованием данных о транспирации воды растениями и концентрациях Zn в почвенных растворах для разных вариантов опыта были построены кумулятивные кривые выноса Zn из типичного чернозема растениями с конвективным потоком влаги (рис. 8 – заштрихованные точки), а также рассчитаны величины максимального выноса Zn ячменем с конвективным потоком влаги, мкг/растение: 228 (Zn0), 350 (Zn100), 654 (Zn250), 1080 (Zn500). Динамика массы корней ячменя оценена в рамках специального эксперимента с разборными вегетационными сосудами, где почву, загрязненную Zn в дозах, равных тем, что были использованы в стандартных вегетационных сосудах-лизиметрах Митчерлиха, отделяли от растущих корней с помощью биофильных мембран. Дизайн этих сосудов, изготовленных из плексигласа, описан ранее в работе [26]. На определенной стадии развития растений (синхронно с отбором растений из вегетационных сосудов-лизиметров) плексигласовые сосуды разбирали и анализировали соотношение масс надземной части растений и корней. Было установлено, что эти соотношения в зависимости от времени и количества внесенного в почву Zn можно в первом приближении удовлетворительно описать с помощью линейных регрессионных уравнений: mн.ч./mкорни = 0.066t, R2 = 0.77 (вариант Zn0); mн.ч./mкорни = 0.053t, R2 = 0.85 (вариант Zn100); mн.ч./mкорни = 0.039t, R2 = 0.96 (вариант Zn250); mн.ч./mкорни = 0.027t, R2 = 0.99 (вариант Zn500). Рассчитанные соотношения вместе с известными массами надземных частей растений и концентрацией Zn в корнях ячменя, выращенного в вегетационных сосудах-лизиметрах, позволили рассчитать вынос Zn корнями в динамике с помощью аппроксимирующих регрессионных уравнений, параметры которых представлены в табл. 7 и 8.
Рис. 8.
Динамика выноса Zn из типичного чернозема растениями в течение вегетационного периода (в пересчете на одно растение), мкг × растение–1: с конвективным потоком влаги (заштрихованные точки, расчетные величины), общего, включающего диффузионную и конвективную компоненты (открытые точки, экспериментально установленные величины).
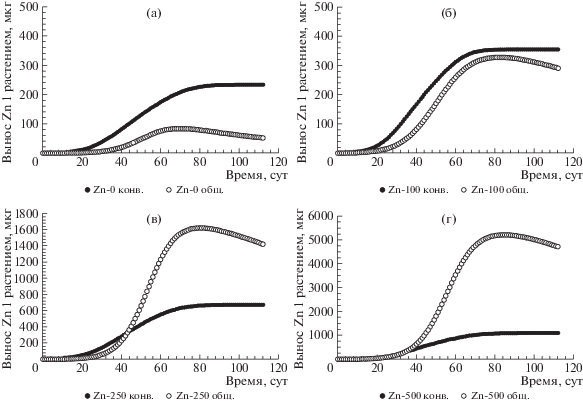
Таблица 7.
Количественные параметры логистических кривых изменения сухой массы корней ячменя (в пересчете на одно растение), выращенного на черноземе типичном до фазы созревания зерна
| Вариант | Mmax | M0 | μ, сут–1 |
|---|---|---|---|
| г | |||
| Zn0 | 0.50 | 0.006 | 0.105 |
| Zn100 | 0.45 | 0.007 | 0.120 |
| Zn250 | 1.10 | 0.008 | 0.116 |
| Zn500 | 1.12 | 0.014 | 0.112 |
Таблица 8.
Количественные параметры логистических кривых изменения концентрации Zn в сухой надземной биомассе корней ячменя, выращенного на черноземе типичном до фазы созревания
| Вариант | [Zn]max, корни | [Zn]min, корни | Β, сут–1 |
|---|---|---|---|
| мг/кг | |||
| Zn0 | 35.0 | 1.32 | 0.059 |
| Zn100 | 209 | 6.28 | 0.056 |
| Zn250 | 488 | 11.6 | 0.053 |
| Zn500 | 1110 | 27.4 | 0.049 |
Общий вынос Zn растениями из почвы складывался из суммы выносов металла корнями и надземными органами (теоретически соотношение Wконв./Wобщ. должно быть <1). В настоящей работе приведены данные общего выноса металла корнями и надземными органами ячменя. Общий вынос Zn из почвы, по существу, объединяющий диффузионную и конвективную компоненты, в динамике также представлен на рис. 8 (кривые с открытыми точками). Обращает на себя внимание следующая закономерность: с ростом количества внесенного в почву Zn доля выноса металла в результате конвективного переноса неуклонно снижалась. Однако для варианта Zn0, Wконв./Wобщ. = 4.4 (рис. 8а), что, безусловно, вызывало вопросы и могло быть связано как с кумулятивным эффектом ошибок при определении параметров регрессионных уравнений [Zn]почв.раствор = = f(t) и T = f(t) в условиях чрезвычайно низких концентраций Zn в почвенных растворах (и высочайшей их вариабельности), так и с недоучетом потерь цинка в результате листового опада и перераспределения металла между вегетативными и генеративными органами растений. Для вариантов Zn100, Zn250 и Zn500 величины Wконв./Wобщ. соответственно были равны 1.2, 0.5 и 0.2. Прояснить подобное миграционное поведение Zn в системе почва–растение помогают данные изменения концентрации ионов оксония в почвенных растворах, приведенные на рис. 9. Из этого следуют несколько закономерностей:
Рис. 9.
Динамика изменения pH почвенных растворов, извлеченных из типичного чернозема (варианты – “с растениями” и “черный пар”) в течение вегетационного периода.
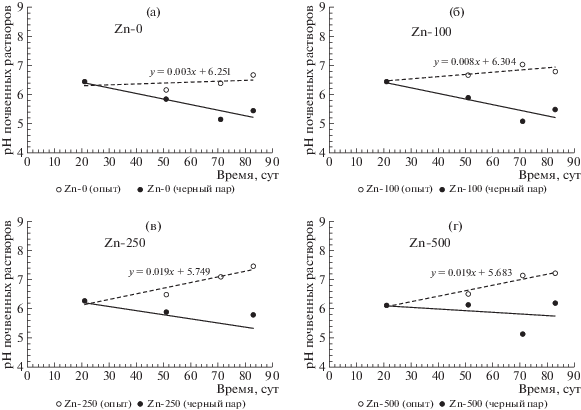
– при выращивании ячменя в течение вегетационного опыта наблюдали положительную динамику величин pH (причем значимость ее возрастала с увеличением количества Zn, внесенного в почву);
– в вариантах “черный пар”, наоборот, отмечена отрицательная динамика величин pH;
– величины показателя pH в квазиравновесных почвенных растворах, отобранных в вариантах опыта “черный пар” были практически на 1 ед. меньше величины pH образцов, отобранных в вариантах с растениями. Связано это с хорошо известным и многократно описанным в научной литературе фактом эквивалентного обмена нитрат-ионов при корневом их поглощении из почвенного раствора на присутствующие в цитозоле гидрокарбонат- и гидроксид-ионы, что приводит к подщелачиванию системы почва–почвенный раствор в прикорневой зоне, и как следствие, уменьшению подвижности в ней ионов тяжелых металлов, включая Zn. Соответственно, снижается количество металла, поступающего в растения с конвективным потоком влаги. В темное время суток устьица, расположенные на листьях растений, закрываются, массоперенос элементов с конвективным потоком влаги снижается до нуля. Однако в то же время создаются благоприятные условия для диффузии тяжелых металлов от поверхности ППК к корневому поглощающему комплексу (КПК). Эффективность данного процесса существенно возрастает в ранние утренние часы благодаря выделению корнями ячменя естественных водорастворимых полидентантных лигандов различной природы – фитосидерофоров в прикорневой зоне. Известно, что значительная часть однодольных растений (пшеница, кукуруза, ячмень и др.) выделяет в почву хелатирующие лиганды, называемые фитосидерофорами (ФС) из семейства мугеневых кислот для извлечения железа и цинка из почвы (стратегия II извлечения микроэлементов) [27–31]. После высвобождения в ризосферу ФС связывают и переводят в водорастворимую форму Fe, Zn и др. микроэлементы из почвы путем образования водорастворимых полидентатных комплексов с металлами, которые легко поглощаются злаковыми растениями. Для многих культурных злаковых видов (в том числе пшеницы и ячменя) экссудация ФС в основном происходит в апикальной зоне корней, подчиняясь циркадному ритму: начинается после наступления светлого времени суток и достигает максимума через 4–6 ч [27]. ФС также способны эффективно извлекать и связывать в виде водорастворимых комплексных соединений катионы металлов, связанные с природными водонерастворимыми органо-минеральными соединениями (например, гуматами). Одновременно с восходом солнца происходит раскрытие устьиц листьев и возобновляется процесс конвективного массопереноса элементов с “обогащенным” металлами благодаря фитосидерофорам почвенным раствором. Однако раствор в прикорневой зоне быстро “истощается”, поскольку: а) растения через несколько часов перестают выделять фитосидерофоры и б) конвективный поток влаги возрастает в течение дня с ростом температуры и увеличением инсоляции, вовлекая сравнительно “бедный” металлами почвенный раствор из дальних частей прикорневой зоны. Поскольку отбор проб из вегетационных сосудов для извлечения почвенных растворов проводили ближе к полудню, то фиксировали заниженные концентрации в них металлов (включая Zn). Это могло приводить к недооценке конвективной составляющей массопереноса Zn в растения, особенно в вариантах опыта с большими дозами внесенного Zn, где наблюдали более сильное подщелачивание среды. Изложенная гипотеза, безусловно, требует тщательной проверки с использованием специальных методов отбора образцов квазиравновесных почвенных растворов (в динамике) и применения ВЭЖХ-хроматографии.
ЗАКЛЮЧЕНИЕ
Для всех вариантов опыта установлено, что концентрация цинка в почвенном растворе уменьшалась со временем в соответствии с обратной степенной зависимостью вследствие процесса истощения запаса водорастворимых форм Zn в почве в результате непрерывного поглощения корнями растений.
Эмпирически установленные закономерности прироста биомассы и выноса металла разными органами растений описывается логистическими функциями с 3-мя параметрами: Mmax (г), M0 (г), μ (сут–1) – для накопления биомассы; Wmax (мкг), W0 (мкг), u (сут–1) – для выноса Zn. Накопление Zn вегетативными органами ячменя удовлетворительно аппроксимируется уравнением Вуда (одновершинной кривой с выраженной положительной ассиметрией) с 3-мя параметрами, а (мг кг–1 сут-b), b и c (сут–1). Величины этих параметров отражают особенности динамики накопления биомассы, накопления и перераспределения Zn между разными органами растений, а также выноса Zn ячменем в условиях различного загрязнения чернозема исследованным элементом. Графический анализ динамики трансформации подвижных (извлекаемых 1 M CH3COONH4, pH 4.8) форм нахождения Zn в типичном черноземе показал, что отрицательная динамика исследованного показателя прослежена лишь в качестве тенденции, не подкрепленной достоверными статистическими данными. В то же время содержание подвижных форм Zn в почве (в % от валового содержания) возрастало с увеличением количества внесенного в почву металла. Полученная зависимость может быть удовлетворительно аппроксимирована с помощью уравнения асимптотической функции: Znподв.(%) = 61.5(1 – exp(–0.0031[Zn]вал.).
Были рассчитаны общий вынос Zn из почвы, включающий диффузионную и конвективную компоненты, а также вынос металла из почвы условно “конвективной” составляющей массопереноса. Выявлена следующая закономерность: с ростом количества внесенного в почву Zn доля выноса металла в результате “конвективного” переноса неуклонно снижалась. Например, для варианта Zn0, Wконв./Wобщ. = 4.5, для вариантов Zn100, Zn250 и Zn500, величины Wконв./Wобщ. Соответственно были равны 1.2, 0.5 и 0.2.
Изучено изменение концентрации ионов оксония в почвенных растворах, извлеченных из чернозема разных вариантов опыта. Выявлено несколько закономерностей:
– при выращивании ячменя в течение вегетационного опыта наблюдали положительную динамику величин pH (причем значимость ее возрастала с увеличением количества Zn, внесенного в почву);
– в вариантах “черный пар”, наоборот, отмечена отрицательная динамика величин pH;
– величины показателя pH в квазиравновесных почвенных растворах, отобранных из вариантов опыта “черный пар” были практически на 1 ед. меньше величин pH образцов, отобранных в вариантах с растениями. Связано это с хорошо известным и многократно описанным в научной литературе фактом экивалентного обмена нитрат-ионов при корневом их поглощении из почвенного раствора на присутствующие в цитозоле гидрокарбонат- и гидроксил-ионы, что приводит к подщелачиванию системы почва–почвенный раствор в прикорневой зоне, и как следствие, уменьшению подвижности в ней ионов тяжелых металлов, включая Zn.
Список литературы
Фрид А.С. Математическая модель как метод изучения корневого поглощения веществ растениями //Агрохимия. 1974. № 3. С. 122–131.
Прохоров В.М. Математическая модель поглощения элементов растениями из почвы // Агрохимия. 1970. № 7. С. 126–136.
Най П.Х., Тинкер П.Б. Движение растворов в системе почва–растение. М.: Колос, 1980. 368 с.
Barber S.A. Soil nutrient bioavailability: a mechanistic approach (second edition). N.Y.: John Wiley & Sons, 1995. 384 p.
Barber S.A., Chen J.-H. Using a mechanistic model to evaluate the effect of soil pH on phosphorus uptake // Plant and Soil. 1990. V. 124. P. 183–186.
Adhikari T., Rattan R.K. Modelling zinc uptake by rice crop using a Barber-Cushman approach // Plant and Soil. 2000. V. 227. P. 235–242.
Фрид А.С. Миграционная концепция доступности веществ почвы корням растений // Агрохимия. 1996. № 3. С. 29–37.
Агрохимические методы исследования почв. М.: Наука, 1975. 656 с.
Практикум по агрохимии / Под ред. Минеева В.Г. М.: Изд-во МГУ, 2001. 689 с.
Вадюнина А.Ф., Корчагина З.А. Методы исследования физических свойств почв. М.: Агропромиздат, 1986. 416 с.
Анисимов В.С., Санжарова Н.И., Анисимова Л.Н., Гераськин С.А., Дикарев Д.В., Фригидова Л.М., Фригидов Р.А., Белова Н.В. Оценка миграционной способности и фитотоксичности Zn в системе почва–растение // Агрохимия. 2013. № 1. С. 64–74.
Анисимов В.С., Кочетков И.В., Дикарев Д.В., Анисимова Л.Н., Корнеев Ю.Н., Фригидова Л.М. Влияние физико-химических характеристик почв на биологическую доступность природного и радиоактивного цинка // Почвоведение. 2016. № 8. С. 942–954. https://doi.org/10.7868/S0032180X16080025
Колосов И.И. Поглотительная деятельность корневых систем растений. М.: Изд-во АН СССР, 1962. 388 с.
Методические указания по определению тяжелых металлов в почвах сельхозугодий и продукции растениеводства (изд. 2-е, перераб. и доп.). М.: ЦИНАО, 1992. 61 с.
Анисимов В.С., Анисимова Л.Н., Фригидова Л.М., Дикарев Д.В., Фригидов Р.А., Корнеев Ю.Н., Санжаров А.И., Арышева С.П. Оценка миграционной способности Zn в системе почва–растение // Почвоведение. 2018. № 4. С. 427–438.
Minkina T.M., Mandzhieva S.S., Burachevskaya M.V., Bauer T.V., Sushkova S.N. Method of determining loosely bound compounds of heavy metals in the soil // MethodsX. 2018. V. 5. P. 217–226. https://doi.org/10.1016/j.mex.2018.02.007
Обухов А.И., Плеханова И.О. Атомно-абсорбционный анализ в почвенно-биологических исследованиях. М.: Изд-во МГУ, 1991. 184 с.
Анисимов В.С., Анисимова Л.Н., Фригидова Л.М., Корнеев Ю.Н., Фригидов Р.А., Санжаров А.И., Дикарев Д.В., Кочетков И.В. Исследование миграционной способности Zn в системе дерново-подзолистая почва–кормовые бобы в условиях вегетационного опыта // Агрохимия. 2019. № 3. С. 72–84.
Количественный химический анализ почв. Методика выполнения измерений содержания металлов в твердых объектах методом спектрометрии с индуктивно-связанной плазмой. ПНДФ 16.1:2.3:3.11–98. М., 1998. (изд-е 2005 г). 28 с.
Рашкович Н.Л. Моделирование показателей минерального питания растений методом регрессионного анализа // Агрохимия. 1995. № 6. С. 97–106.
Дричко В.Ф., Изосимова А.А. Влияние возрастающих доз извести на урожай и скорость роста растений рапса и овса // Агрохимия. 2005. № 8. С. 19–23.
Витковская С.Е., Дричко В.Ф., Хофман О.В. Оценка скорости нарастания биомассы сельскохозяйственных культур // Докл. РАСХН. 2014. № 1. С. 50–53.
Франс Дж., Торнли Дж.Х.М. Математические модели в сельском хозяйстве. М.: Агропромиздат, 1987. 400 с.
Лакин Г.Ф. Биометрия. М.: Высш. шк., 1990. 352 с.
Дрейпер Н., Смит Г. Прикладной регрессионный анализ. Множественная регрессия. 3-е изд. М.: Диалектика, 2007. 912 с.
Анисимов В.С., Анисимова Л.Н., Фригидова Л.М., Дикарев Д.В., Фригидов Р.А., Кочетков И.В., Санжарова Н.И. Оценка миграционной способности Zn в системе почва–растение // Biogeosyst. Technique. 2015. V. 4. № 2. P. 153–163. https://doi.org/10.13187/bgt.2015.4.153. www. ejournal19.com
Takagi S., Nomoto K., Takemoto T. Physiological aspect of mugineic acid, a possible phytosiderophore of graminaceous plants // J. Plant Nutr. 1984. V. 7. P. 469–477. https://doi.org/10.1080/01904168409363213
Marschner H., Römheld V., Kissel M. Different strategies in higher–plants in mobilization and uptake of iron. // J. Plant Nutr. 1986. V. 9. P. 695–713.
Suzuki M., Takahashi M., Tsukamoto T., Watanabe S., Matsuhashi S., Yazaki J., Kishimoto N., Kikuchi S., Nakanishi H., Mori S., Nishizawa N.K. Biosynthesis and secretion of mugineic acid family phytosiderophores in zinc-deficient barley // Plant J. 2006. V. 48 P. 85–97. https://doi.org/10.1111/j.1365-313X.2006.02853.x
Медведев С.С. Физиология растений. СПб.: Изд-во СПбГУ, 2004. 336 с.
Walter M., Oburger E., Schindlegger Y., Hann S., Puschenreiter M., Kraemer S.M., Schenkeveld W.D.C. Retention of phytosiderophores by the soil solid phase – adsorption and desorption // Plant Soil. 2016. V. 404. P. 85–97. https://doi.org/10.1007/s11104-016-2800-x
Дополнительные материалы отсутствуют.


