Агрохимия, 2021, № 4, стр. 22-26
ЯМР-спектроскопия гуминовых кислот почв термокарстовых понижений и бугров пучения
Е. Ю. Мильхеев 1, *, Ю. Б. Цыбенов 1
1 Институт общей и экспериментальной биологии СО РАН
670047 Улан-Удэ, ул. Сахьяновой, 6, Россия
* E-mail: evg-milh@rambler.ru
Поступила в редакцию 25.09.2020
После доработки 19.11.2020
Принята к публикации 11.01.2021
Аннотация
Биоклиматические условия почвообразования в зоне криоаридного климата Забайкалья определяют специфический состав гуминовых веществ (ГВ), однако гетерогенность этих соединений, а также широко используемые классические методы анализа органического вещества не позволяют с достаточной степенью уверенности судить о структуре высокомолекулярных органических соединений в почвах криолитозоны. Спектроскопия 13С-ЯМР препаратов гуминовых кислот (ГК) исследованных почв (криоморфозов) позволила выделить диапазоны химических сдвигов, принадлежащих атомам углерода различных функциональных групп и молекулярных фрагментов. Сравнительный анализ молекулярного состава ГК исследованных почв показал, что при переходе от бугров пучений к термокарстовым понижениям происходит трансформация структурно-функциональных параметров гуминовых кислот, которая выражается в уменьшении доли ароматических фрагментов и увеличении лабильных углеводных, аминокислотных и метоксильных остатков. Возрастание доли алифатических структур и снижение доли ароматических фрагментов в составе препаратов ГК позволяют говорить об упрощении строения молекулы гуминовой кислоты, что может быть обусловлено снижением микробиологической активности в термокарстовом понижении в условиях их постоянного переувлажнения.
ВВЕДЕНИЕ
Судьба природного органического вещества и особенно гуминовых веществ (ГВ) в последние десятилетия привлекает все больший интерес ученых, представляющих различные дисциплины. ГВ, являясь важнейшим компонентом почвенного гумуса, характеризуется нестехиометричностью состава, нерегулярностью строения, полидисперсностью и гетерогенностью структурных элементов. Гетерогенная химическая природа ГВ играет многофункциональную роль в окружающей среде, контролируя биогеохимический цикл углерода, обеспечивая растения питательными веществами и биостимуляторами роста и взаимодействуя с неорганическими и органическими загрязнителями.
Компонентный состав органического вещества почв – динамический показатель, отражающий влияние экологических условий на геохимический цикл углерода экосистемы. Основными механизмами стабилизации биомолекул органических остатков в аэробных условиях являются гумификация и органо-минеральные взаимодействия [1]. В силу исторически сложившихся традиций в основу классификации ГВ положено их различие, связанное с извлечением этих специфических соединений из природных объектов теми или иными растворителями. По общепринятой классификации гуминовые вещества делят на гуминовые кислоты (ГК) (растворимы в щелочных растворах), фульвокислоты (ФК) (растворимы во всем диапазоне pH) и гумины (нерастворимы во всем диапазоне pH).
Гуминовые кислоты – природные высокомолекулярные системы нерегулярного строения, являются одним из главных компонентов органического вещества почв, торфов, природных вод, морских и озерных донных отложений. Они накапливают элементы минерального питания, обеспечивая их постепенное поступление в живые организмы, отвечают за структурообразование почв и их благоприятные водно-физические свойства, снижают негативное действие токсичных веществ [1]. Существуя в почвах тысячи лет, ГК придают им стабильность, своеобразную буферность, определенный биохимический фон [2].
В настоящее время специалистов в области химии природного органического сырья привлекают уникальные возможности спектроскопии ядерного магнитного резонанса (ЯМР) 13С для количественного анализа и изучения строения многокомпонентных систем, в том числе и гуминовых кислот [3]. Применимость данного метода исследования в изучении функционального состава ГК подтверждена неоднократно [3–5]. Использование сверхпроводящих магнитов и преобразования Фурье позволило не только разделять сигналы при высоком уровне шумов или при их наложении, но и выполнять расчет интегральной интенсивности сигналов [6, 7].
Комплексное изучение высокомолекулярных органических соединений криогенных форм рельефа (бугров пучений и термокарстовых понижений), сформированных в условиях ультраконтинентального климата Бурятии и относительно близко залегающих многолетнемерзлых пород, с использованием высокочувствительных спектроскопических методов будет способствовать пониманию фундаментальных процессов гумусообразования и созданию новых представлений о сложных по составу и структуре природных высокомолекулярных соединений почв в зоне криогенеза.
Цель работы – изучение химического строения гуминовых кислот почв термокарстовых понижений и бугров с использованием 13С ядерного магнитного резонанса. Выявление структурных особенностей ГК криоморфозов по 13С-ЯМР-спектрам позволяет установить закономерности изменения структурного состава гуминовых кислот почв различного криогенеза.
МЕТОДИКА ИССЛЕДОВАНИЯ
Район исследования расположен в Еравнинской котловине юга Витимского плоскогорья, где многолетняя мерзлота достигает максимальной мощности 120–130 м, в среднем составляя 80–85 м [8, 9]. Верхняя границы мерзлоты залегает на глубине 1.5–3.0 м от дневной поверхности, местами – на глубине <1 м.
Объектами исследования послужили образцы ГК, полученные из верхних генетических горизонтов почв бугров пучения и термокарстовых понижений. Гуминовые кислоты были выделены по стандартной методике [10] экстракцией 0.1 н. NaOH, препараты ГК очищали путем переосаждения 20%-ным раствором HCl до величины pH 1.5–2.0 и многократного центрифугирования. Осадок промывали 0.1 н. HCl, затем дистиллированной водой, высушивали и растирали до состояния пудры. Спектры ядерно-магнитного резонанса 13С-ЯМР были сняты на спектрометре Avance 300 MHz “Вruкеr” (Германия) с рабочей частотой 100.53 МГц с использованием твердофазной методики CP-MAS. Частота вращения образца 6 kHz, время контакта 5 мс, время релаксации 5 с, количество накоплений 3500–13 000 сканов. Химические сдвиги представлены относительно тетраметилсилана со сдвигом 0 ppm, в качестве стандарта использовали пик адамантана (в слабом поле) при 38.48 ppm. Для количественной обработки применяли численное интегрирование по областям, соответствующим расположению функциональных групп и молекулярных фрагментов.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
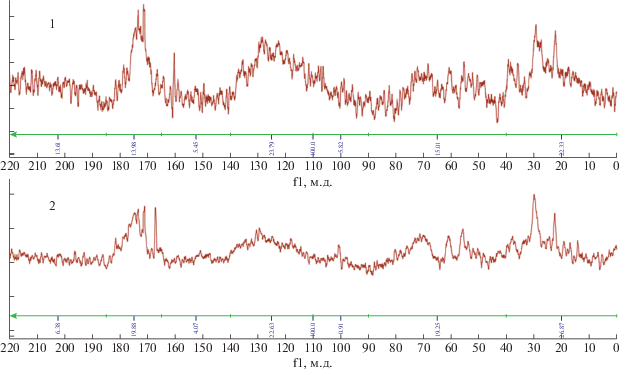
Для изучения особенностей структурно-функциональных параметров органического вещества почв бугров и понижений были сняты 13С-ЯМР-спектры (техника CP-MAS) препаратов гуминовых кислот. Все полученные спектры ГК характеризовались широкими полосами поглощения, обусловленными перекрыванием нескольких сигналов (рис. 1).
Ввиду сильного перекрывания пиков, отнесение сигналов в твердофазных 13С-ЯМР-спектрах возможно только по диапазонам химического сдвига, согласно положению резонансов атомов со сходным химическим окружением (табл. 1).
Таблица 1.
Содержание молекулярных фрагментов гуминовых кислот
| Химический сдвиг, м.д. | Тип молекулярных фрагментов* | Интегральная интенсивность, % | |
|---|---|---|---|
| бугор пучения | термокарстовое понижение | ||
| 0–40 | Cалк | 22.3 | 26.9 |
| 40–90 | Cалк–O | 15.0 | 19.3 |
| 90–110 | Cар | 5.8 | 0.9 |
| 110–140 | Cар–CH | 23.8 | 22.6 |
| 140–165 | Сар–O | 5.5 | 4.1 |
| 165–185 | CCOOH + CCOOR | 14.0 | 19.9 |
| 185–220 | CC=O | 13.6 | 6.4 |
По характеру спектров ЯМР 13С видно, что в химическом строении углеродного скелета ГК бугров и понижений в сопоставимых количествах содержатся как ароматические, так и алифатические компоненты. Относительно острый пик, сосредоточенный в области 30 м.д., может быть отнесен к метиленовым атомам углерода в положениях α, β, δ и ε от концевых метильных групп (15 м.д.) в алкильных цепочках [11]. Эти метиленовые атомы углерода, как предполагается некоторыми исследователями, могут являться результатом накопления воскосмол, липидов и субериновых структур из растений [12–15].
Также все спектры имели сигнал в диапазоне 47–60 м.д., который некоторые авторы связывают с метоксильными группами, обусловленными присутствием лигниновых фрагментов – сирингил- и гваяцилпропановых единиц [16, 17]. Однако в этой области химических сдвигов можно также наблюдать и сигналы от атомов углерода в α положении в полипептидах (–C(O)–C*(R)H–NH–)n [14, 18]. Высокий коэффициент корреляции между интенсивностью сигнала в диапазоне 47–60 м.д. и массовой долей азота в составе исследованных гуминовых веществ косвенно подтверждал последнее предположение. Количественная оценка их ядерных сигналов показала, что содержание Слигн в препаратах, выделенных из бугра, больше, чем в понижении. На состав ГК, возможно, повлияла высокая лигнинофицированность первичных источников гумуса, различия в видовом составе травянистой растительности.
Интенсивный пик при 71 м.д. в 13С-ЯМР-спектрах характерен для CH(О)-групп кольцевых атомов углерода в углеводах [11]. Сигнал в этой области спектра распространяется от 64 до 90 м.д., который, вероятно, происходит от различных HC–OH-групп целлюлозных или других углеводных фрагментов [14]. Слабый сигнал ≈62 м.д. типичен для CH2O-групп гексоз из полисахаридных фрагментов [19]. Наличие слабо интенсивного сигнала при 101 м.д., который является представительным для аномерных (полуацетальных) атомов углерода, также подтверждал присутствие углеводных фрагментов в структуре ГК.
В области ароматических фрагментов сигнал в пределах 90–165 м.д. могут давать незамещенные и/или алкил-замещенные ароматические атомы углерода. Пик при 147–149 м.д. типичен в спектрах структурных блоков лигнина, и его приписывают к кислородзамещенным атомам углерода ароматических колец – сирингил- и гваяцилпропановых единиц [14, 20]. ЯМР-спектры ГК бугра пучения имели более интенсивные сигналы в этой области по сравнению с термокарстовым понижением.
Многие свойства ГК определяются типом и количеством функциональных групп в их составе. В области карбоксильной группы (165–185 м.д.) наблюдали максимум при 171–173 м.д., в значительной степени относимый к углероду карбоксильных групп [21], но также он может принадлежать и карбонильной группе амидов и полипептидов [14]. Преобладание карбоксильных групп (–СООН) служит основанием для причисления гуминовых веществ к кислотам, в частности к высокомолекулярным ароматическим оксикарбоновым кислотам. Атомы углерода хинонных фрагментов и карбонильных групп альдегидов и кетонов вносили свой вклад в слабые сигналы в области 185–220 м.д., и невысокое их содержание (6.4–13.6), вероятно, связано с понижением биохимической активности почв понижений.
Кроме рассмотренных соотношений важным свойством ГК является соотношение в их составе гидрофильных и гидрофобных компонентов. К гидрофильным компонентам относим активные функциональные кислородсодержащие группы (С=О, СООН, Cалк–O-фрагменты), а гидрофобную часть представляют С- и Н-замещенные ароматические и алкильные фрагменты (СарСН и Салк) гуминовых кислот. Доля гидрофильных фрагментов в исследованных препаратах, которая отвечает за реакционную способность ГК, составляла 42.6–45.6%.
Сравнительный анализ молекулярного состава ГК исследованных почв показал, что при переходе от бугров пучений к термокарстовым понижениям происходила трансформация структурно-функциональных параметров гумусовых кислот, которая выражалась в уменьшении доли ароматических фрагментов и увеличении лабильных углеводных, аминокислотных и метоксильных остатков. Основными факторами, влияющими на строение и свойства высокомолекулярных органических соединений почв, являются климатические условия (температурный и водный режимы) обусловливающие специфику растительности и микробиологической активности исследованных криогенных экосистем.
Анализируя полученные результаты, можно сделать вывод, что избыточное увлажнение заметно влияет не только на количество накапливаемых гумусовых соединений, но и оказывает воздействие на их молекулярную структуру, а именно, обусловливает накопление в полугидроморфных почвах гумусовых веществ, обогащенных алифатическими цепочками. Переувлажнение, в совокупности с анаэробными условиями и низкой микробиологической активностью заметно снижает скорость трансформации почвенного органического вещества и приводит к увеличению доли не окисленных алифатических фрагментов в структуре гуминовых кислот.
ЗАКЛЮЧЕНИЕ
Таким образом, в спектрах 13С-ЯМР гуминовых кислот (ГК) бугров пучений доминирует сигнал углерода ароматического ряда, в ГК термокарстовых понижений – алифатического. Эти данные полностью совпадают с результатами элементного состава, величинами отношения Н : С. Выявленные различия в содержании атомов углерода, входящих в состав структурных фрагментов в составе макромолекул ГК, свидетельствуют о разных условиях почвообразования и гумификации. Возрастание доли алифатических структур и снижение доли ароматических фрагментов в составе препаратов ГК позволяют говорить об упрощении строения молекулы гуминовой кислоты, что может быть обусловлено снижением микробиологической активности в термокарстовом понижении в условиях их постоянного переувлажнения.
Список литературы
Орлов Д.С. Гумусовые кислоты почв и общая теория гумификации. М.: Изд-во МГУ, 1990. 324 с.
Дергачева М.И. Методы почвоведения в археологических исследованиях. Новосибирск: Новосибирск. гос. ун-т, 2007. 96 с.
Калабин Г.А., Каницкая Л.В., Кушнарев Д.Ф. Количественная спектроскопия ЯМР природного органического сырья и продуктов его переработки. М.: Химия, 2000. 407 с.
Федорова Т.Е. Количественная спектроскопия ЯМР 13С, 17О и физиологическая активность гуминовых кислот: Автореф. дис. … канд. хим. наук. Иркутск, 2000. 24 с.
Ковалевский Д.В. Исследование структуры гуминовых кислот методами спектроскопии ЯМР 1Н и 13C. Дис. … канд. хим. наук. М., 1998. 140 с.
Simpson A.J., Burdon J., Graham C.L. Interpretation of heteronuclear and multidimensional NMR spectroscopy of humic substances // Eur. J. Soil Sci. 2001. V. 52. P. 495–509.
Schilling M., Cooper W.T. Effects of chemical treatments on the quality and quantitative reliability of solid-state 13C NMR spectroscopy of mineral soils // Analyt. Chim. Acta. 2004. V. 508. P. 207–216.
Мельничук Н.Л. Геокриологические условия южной части Витимского плоскогорья // Геокриологические условия Забайкалья и Прибайкалья. М.: Наука, 1967. С. 71–79.
Цыбенов Ю.Б., Чимитдоржиева Г.Д., Чимитдоржиева Э.О., Егорова Р.А., Мильхеев Е.Ю., Давыдова Т.В., Корсунова Ц.Д.-Ц. Морфологические и физические свойства почвенной массы из криогенных трещин мерзлотных лугово-черноземных почв Забайкалья // Почвоведение. 2016. № 8. С. 975–981.https://doi.org/10.7868/S0032180X16080153
Орлов Д.С., Гришина Л.А. Практикум по химии гумуса. М.: Изд-во МГУ, 1981. 271 с.
Simpson A.J., Simpson M.J. Nuclear magnetic resonance analysis of natural organic matter // Biophysic-chemical processes involving natural nonliving organic matter in environmental systems / Eds. Senesi N., Xing B., Huang P.M. New Jersey: John Wiley & Sons Inc., 2009. P. 589–650.
Lodygin E.D., Beznosikov V.A. Influence of soil moisture on concentrations and 13C NMR profiles of lipids in three Albeluvisols // Geoderma. 2005. V. 127. № 3–4. P. 253–262.https://doi.org/10.1016/j.geoderma.2004.12.004
Winkler A., Haumaier L., Zech W. Insoluble alkyl carbon components in soils derive mainly from cutin and suberin // Org. Geochem. 2005. V. 36. P. 519–529.
Keeler C., Kelly E.F., Maciel G.E. Chemical-structural information from solid-state 13C NMR studies of a suite of humic materials from a lower montane forest soil, Colorado, USA // Geoderma. 2006. V. 130. P. 124–140.
Alarcón-Gutiérrezet E., Floch C., Augur C., Petit J.L., Ziarelli F., Criquet S. Spatial variations of chemical composition, microbial functional diversity, and enzyme activities in a Mediterranean litter (Quercus ilex L.) profile // Pedobiologia, 2009. V. 52. P. 387–399.
Tadini A.M., Pantano G., Toffoli A.L., Fontaine B., Spaccini R., Piccolo A., Moreira A.B., Bisinoti M.C. Off-line TMAH-GC/MS and NMR characterization of humic substances extracted from river sediments of northwestern São Paulo under different soil uses. Original research article // Sci. Total Environ. 2015. V. 506–507. P. 234–240.https://doi.org/10.1016/j.scitotenv.2014.11.012
Ковалева Н.О., Ковалев И.В. Лигниновые фенолы в почвах как биомаркеры палеорастительности // Почвоведение. 2015. № 9. С. 1073–1086.https://doi.org/10.7868/S0032180X15090063
Knicker H., Hilscher A., González-Vila F.J., Almendros G. A new conceptual model for the structural properties of char produced during vegetation fires // Org. Geochem. 2008. V. 39. P. 935–939.
Duarte R.M.B.O., Silva A.M.S., Duarte A.C. Two-dimensional NMR studies of water-soluble organic matter in atmospheric aerosols // Environ. Sci. Technol. 2008. V. 42. P. 8224–8230.
Ковалева Н.О., Ковалев И.В. Биотрансформация лигнина в лесных почвах // Лесоведение. 2006. № 3. С. 57–63.
Лодыгин Е.Д., Безносиков В.А. Изучение молекулярной структуры гумусовых кислот подзолистых и болотно-подзолистых почв методом 13C-ЯМР спектроскопии // Почвоведение. 2003. № 9. С. 1085–1094.
Дополнительные материалы отсутствуют.