Журнал аналитической химии, 2019, T. 74, № 10, стр. 784-800
Потенциометрические сенсоры и мультисенсорные системы для определения лантанидов
И. С. Ярошенко a, *, М. Ю. Аляпышев b, В. А. Бабаин a, b, А. В. Легин a, Д. О. Кирсанов a
a Санкт-Петербургский государственный университет
198504 Санкт-Петербург, Петродворец, Университетский просп., 26, Россия
b ООО “ТриАркМайнинг”
198216 Санкт-Петербург, просп. Народного Ополчения, 10, Россия
* E-mail: irina.s.yaroshenko@gmail.com
Поступила в редакцию 29.10.2018
После доработки 15.11.2018
Принята к публикации 27.04.2019
Аннотация
Рассмотрены проблемы разработки потенциометрических сенсоров и мультисенсорных систем для определения содержания редкоземельных элементов в водных растворах. Продемонстрирована эффективность подхода к созданию сенсоров, основанного на применении веществ и закономерностей, используемых в жидкостной экстракции. Показаны возможности мультисенсорных систем для селективного определения отдельных лантанидов в сложных смесях.
Одна из основных тенденций в развитии современной аналитической химии связана с автоматизацией методов анализа. Особую популярность приобрели химические сенсоры, основанные на различных принципах получения сигнала. Сенсорные методы отличаются простотой приборного оформления, широкими возможностями автоматизации и миниатюризации. Особенно интенсивно исследуются потенциометрические сенсоры, что связано с возможностью управления их сенсорными свойствами путем направленного изменения состава потенциометрической мембраны. В то время как твердотельные потенциометрические мембраны на основе поликристаллов и халькогенидных стекол давно коммерциализованы и прочно вошли в повседневную аналитическую практику, исследования в области полимерных пластифицированных мембран ведутся и в настоящее время. Классические полимерные мембранные композиции, например, для определения ионов калия, аммония, нитрата, катионов щелочноземельных металлов [1] также коммерчески доступны и успешно применяются в лабораториях. Между тем существует ряд аналитов, для определения которых не созданы надежные потенциометрические сенсоры с удовлетворительными эксплуатационными характеристиками. Помимо целого ряда гидрофильных анионов (таких как фосфаты, карбонаты, сульфаты) сюда относятся и лантаниды. Сложность определения лантанидов связана с тем, что в большинстве случаев они присутствуют в растворе в виде смесей [2]. Поскольку свойства лантанидов близки, одновременное определение нескольких лантанидов – непростая задача. Выделение и разделение смесей лантанидов требует разработки способов их совместного определения. Определить содержание каждого элемента можно с помощью таких методов, как атомно-эмиссионная спектроскопия [3] или масс-спектрометрия с индуктивно связанной плазмой [4, 5], чаще с предварительным разделением хроматографическими или электрофоретическими методами. Несмотря на высокую точность таких методов, они обладают рядом существенных ограничений: длительность анализа и невозможность проведения его в режиме реального времени, высокая стоимость оборудования и расходных материалов, высокая квалификация персонала. Создание простых и недорогих химических сенсоров с подходящими аналитическими характеристиками стало бы существенным шагом вперед на пути разработки методов, контролирующих процессы разделения лантанидов в режиме реального времени. Такие методы востребованы также при анализе растворов переработки облученного ядерного топлива (ОЯТ). Следует отметить, что к измерительным устройствам для анализа таких сред, помимо чувствительности и селективности к целевым аналитам, предъявляются некоторые специфические требования: радиационная стойкость сенсорных материалов и способность функционировать при низких значениях рН.
Довольно большое число работ посвящено созданию потенциометрических сенсоров с полимерными мембранами для определения ионов лантанидов. В качестве полимера в таких сенсорных мембранах выступает, как правило, поливинилхлорид (ПВХ). Эти материалы позволяют в широких пределах варьировать характеристики сенсора путем модификации структуры ионофора, изменения концентрационного соотношения ионофор/ионообменная добавка, применения различных растворителей-пластификаторов. Ионофоры представляют собой липофильные органические лиганды, отвечающие за селективное связывание целевого иона. Ионообменные добавки вводят для компенсации заряда комплекса ионофор–ион в фазе мембраны и для облегчения ионного обмена на фазовой границе мембрана–раствор. Более подробные сведения, касающиеся основных принципов функционирования подобных сенсоров, можно найти в обзоре [6]. Создание селективных сенсоров для определения ионов лантанидов является непростой задачей по следующим причинам: 1) невысокая электрохимическая чувствительность, поскольку большинство лантанидов в водных растворах существует в виде трехзарядных катионов, теоретическое значение потенциометрического отклика к которым составляет всего 19 мВ/дек (по сравнению с 59 мВ/дек для однозарядных катионов); 2) невысокая селективность определения лантанидов, связанная с близкими ионными радиусами соседних лантанидов, их электронной структурой и свойствами; 3) необходимость работы при низких значениях рН, связанная с гидролизом трехзарядных катионов лантанидов.
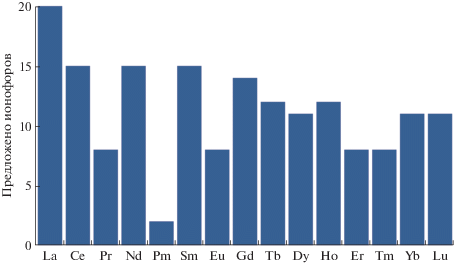
К настоящему времени предложено около 200 различных ионофоров для потенциометрических сенсоров, чувствительных к ионам лантанидов. На рис. 1 показано число ионофоров, описанных в литературе, для каждого лантанида, которые удалось найти в SCOPUS по запросу “элемент + + PVC-sensor”. Наиболее подробный список публикаций и детальное их описание приведено в пятой главе книги [7].
Так, например, для создания церийселективных сенсоров в качестве ионофоров применяли 1,3,5-тритиациклогексан [8], 2,5-диоксоимидазолидинил [9], 2,9-дигидрокси-1,10-дифенокси-4,7-дитиадекан [10] и еще более 10 соединений. Согласно литературным данным, чувствительность всех описанных сенсоров близка к теоретическому нернстовскому значению 19 мВ/дек в широком концентрационном диапазоне (10–6–0.1 М). Описанные сенсоры проявляют селективность именно к церию, что авторы цитируемых работ объясняют размером полости ионофора, подходящим только для церия. Подобные результаты представляются несколько неожиданными, принимая во внимание ионные радиусы лантанидов в водных растворах [11] и их близость. Так, например, радиус La3+ составляет 0.125 нм, радиус Ce3+ 0.122 нм, а радиус Pr3+ 0.120 нм.
Разработаны различные полимерные потенциометрические сенсоры, чувствительные к ионам лантана. 1,3,5-Тритиациклогексан, на основе которого в работе [8] изготовлены церийселективные электроды, применяли и для создания лантанселективного электрода [12] (табл. 1). Авторы обеих работ приводят коэффициент селективности для пары лантан–церий: в работе [8] он составил 5 × 10–2, т.е. чувствительный к церию сенсор фиксирует церий при 500-кратном избытке ионов лантана, а в работе [12] коэффициент селективности для поливинилхлоридного электрода, чувствительного к лантану, составил 3.5 × 10–2, т.е. предлагаемый сенсор способен определять лантан при 350-кратном избытке церия. При этом процедура приготовления сенсоров и составляющие их компоненты абсолютно аналогичны. Очевидно, что такие данные нуждаются в дополнительной проверке.
Таблица 1.
Электроаналитические характеристики поливинилхлоридных мембран на основе различных ионофоров в растворах лантанидов
| Катион | Структура ионофора | Наклон электродной функции, мВ/дек | Линейный диапазон, М |
Предел детектиро-вания, М | Коэффициент селективности | Рабочий диапазон рН | Литера-тура |
|---|---|---|---|---|---|---|---|
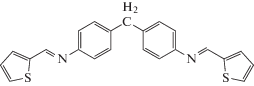
| La3+ |  |
19.6 ± 0.5 | 8.0 × 10–6–0.05 | 5.0 × 10–6 | 7.7 × 10–3 (Ag+) 3.5 × 10–3 (Zn2+) 3.5 × 10–2 (Се3+) |
5.0–8.0 | [12] |
 |
20.0 ± 0.2 | 3.2 × 10–8–0.01 | 2.5 × 10–8 | 3.2 × 10–4 (Ag+) 1.9 × 10–3 (Zn2+) 5.2 × 10–1 (Се3+) |
3.5–9.5 | [13] | |
 |
19.0 | 1.0 × 10–6–0.1 | 5.0 × 10–7 | 5.0 × 10–3 (Ag+) 1.0 × 10–2 (Pb2+) 2.5 × 10–2 (Се3+) |
4.0–9.0 | [14] | |
| Ce3+ |  |
19.4 ± 0.4 | 5.0 × 10–5–0.1 | 3.0 × 10–5 | 3.2 × 10–2 (Ag+) 6.3 × 10–2 (Zn2+) 5.0 × 10–2 (La3+) |
5.0–8.0 | [8] |
 |
19.6 ± 0.3 | 1.0 × 10–6–0.1 | 5.7 × 10–7 | 4.7 × 10–4 (Na+) 6.2 × 10–4 (Zn2+) 8.6 × 10–3 (La3+) |
3.1–9.8 | [9] | |
 |
19.3 ± 1.0 | 1.0 × 10–8–0.1 | 2.1 × 10–9 | 1.1 × 10–5 (Ag+) 1.0 × 10–6 (Zn2+) 1.0 × 10–7 (Al3+) |
5.0–8.0 | [10] | |
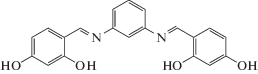
| Pr3+ |  |
19.9 ± 0.3 | 2.5 × 10–7–0.1 | 9.0 × 10–8 | 1.5 × 10–5 (Na+) 2.9 × 10–3 (Zn2+) 4.0 × 10–4 (Nd3+) |
3.5–7.5 | [15] |
 |
19.8 ± 0.4 | 1.0 × 10–6–0.01 | 5.7 × 10–7 | 2.4 × 10–4 (Na+) 4.6 × 10–4 (Pb2+) 8.2 × 10–4 (Nd3+) |
3.1–9.8 | [16] | |
 |
20.5 ± 0.2 | 1.0 × 10–7–0.5 | 5.2 × 10–8 | 4.7 × 10–6 (Na+) 1.6 × 10–3 (Pb2+) 6.3 × 10–3 (Nd3+) |
3.0–8.8 | [17] | |
| Nd3+ | 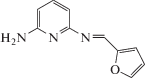 |
19.6 ± 0.3 | 1.0 × 10–5 –0.01 | 7.0 × 10–6 | 2.5 × 10–3 (Na+) 1.0 × 10–2 (Cu2+) 2.5 × 10–2 (La3+) 3.1 × 10–2 (Sm3+) |
4.0–8.0 | [18] |
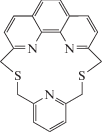 |
20.0 ± 0.2 | 1.0 × 10–6 –0.01 | 7.9 × 10–7 | 1.3 × 10–3 (Na+) 1.6 × 10–2 (Zn2+) 4.0 × 10–2 (La3+) 2.5 × 10–2 (Sm3+) |
4.0–6.5 | [19] | |
 |
19.6 ± 0.3 | 1.0 × 10–5–0.01 | 2.0 × 10–6 | 2.1 × 10–3 (Na+) 8.9 × 10–3 (Cu2+) 2.7 × 10–2 (Ce3+) |
3.5–8.5 | [20] | |
| Pm3+ |  |
20.0 ± 0.5 | 4.5 × 10–7–0.01 | 3.2 × 10–7 | 5.9 × 10–5 (Na+) 5.5 × 10–5 (Pb2+) 3.5 × 10–2 (Nd3+) 3.3 × 10–2 (Sm3+) |
4.0–7.5 | [21] |
 |
19.5 ± 0.5 | 3.5 × 10–6–0.1 | 2.3 × 10–6 | 7.2 × 10–5 (Na+) 6.0 × 10–5 (Pb2+) 3.2 × 10–2 (Nd3+) 3.0 × 10–2 (Sm3+) |
4.0–6.5 | ||
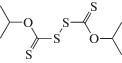
| Sm3+ |  |
19.35 ± 0.2 | 1.0 × 10–7–0.1 | 1.0 × 10–7 | 1.6 × 10–4 (Na+) 3.2 × 10–4 (Pb2+) 1.0 × 10–3 (Eu3+) |
3.0–8.0 | [22] |
 |
19.5 ± 0.4 | 1.0 × 10–5–0.1 | 3.1 × 10–6 | 6.3 × 10–3 (Na+) 4.4 × 10–2 (Pb2+) 7.9 × 10–2 (Gd3+) |
4.0–7.0 | [23] | |
 |
19.8 ± 0.4 | 1.0 × 10–6–0.01 | 5.0 × 10–7 | 8.5 × 10–4 (Na+) 7.6 × 10–3 (Pb2+) 5.6 × 10–3 (Nd3+) 8.5 × 10–3 (Eu3+) |
3.7–8.2 | [24] | |
| Eu3+ | 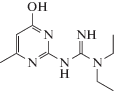 |
19.8 ± 0.1 | 7.0 × 10–5–0.1 | 5.0 × 10–5 | 1.2 × 10–3 (Ag+) 1.0 × 10–2 (Zn2+) 2.8 × 10–2 (Gd3+) |
3.0–7.0 | [25] |
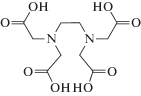 |
19.7 ± 0.5 | 1.0 × 10–6–0.01 | 7.2 × 10–7 | 7.8 × 10–4 (Na+) 2.7 × 10–3 (Pb2+) 5.7 × 10–3 (Gd3+) |
2.5–9.1 | [26] | |
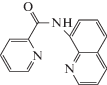 |
19.8 ± 0.3 | 1.0 × 10–6 –0.01 | 6.4 × 10–7 | 3.2 × 10–4 (Na+) 4.1 × 10–4 (Pb2+) 7.6 × 10–3 (Gd3+) |
2.4–7.4 | [27] | |
| Gd3+ |  |
19.95 ± 0.3 | 3.0 × 10–7–0.1 | 3.0 × 10–7 | 5.0 × 10–6 (Na+) 2.3 × 10–5 (Pb2+) 3.0 × 10–4 (Eu3+) |
4.0–9.0 | [28] |
 |
19.5 ± 0.5 | 9.4 × 10–7–0.1 | 5.0 × 10–7 | 7.5 × 10–3 (Na+) 8.4 × 10–4 (Zn2+) 1.9 × 10–2 (Nd3+) |
3.5–8.5 | [29] | |
 |
19.8 ± 0.4 | 1.0 × 10–7–0.01 | 7.3 × 10–8 | – | 2.9–8.4 | [30] | |
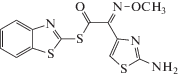
| Tb3+ |  |
19.6 ± 0.2 | 1.0 × 10–5–0.1 | 7.0 × 10–6 | 1.2 × 10–4 (Cs+) 6.3 × 10–3 (Pb2+) 7.9 × 10–3 (Gd3+) 1.4 × 10–2 (Dy3+) |
3.5–7.7 | [31] |
 |
19.5 ± 0.1 | 1.5 × 10–7 –0.01 | 9.3 × 10–8 | 3.2 × 10–5 (Na+) 3.2 × 10–6 (Zn2+) 1.6 × 10–5 (Gd3+) |
1.5–7.5 | [32] | |
 |
19.7 ± 0.4 | 1.0 × 10–6–0.1 | 8.0 × 10–7 | 3.0 × 10–4 (Na+) 7.3 × 10–4 (Pb2+) 6.8 × 10–3 (Gd3+) 2.1 × 10–3 (Yb3+) |
3.5–8.0 | [33] | |
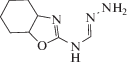
| Dy3+ |  |
20.6 ± 0.2 | 1.0 × 10–5–0.1 | 6.0 × 10–6 | 3.9 × 10–3 (Cs+) 5.0 × 10–3 (Pb2+) 2.5 × 10–2 (Gd3+) |
3.5–8.0 | [34] |
 |
19.5 ± 0.4 | 1.0 × 10–6–0.1 | 4.7 × 10–7 | 6.5 × 10–4 (Na+) 6.7 × 10–4 (Pb2+) 1.5 × 10–4 (Gd3+) |
3.3–8.4 | [35] | |
 |
19.8 ± 0.6 | 1.0 × 10–6–0.01 | 5.5 × 10–7 | 6.7 × 10–4 (Na+) 3.3 × 10–3 (Pb2+) 2.2 × 10–3 (Ho3+) |
2.4–8.9 | [36] | |
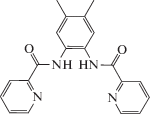
| Ho3+ |  |
19.7 ± 0.2 | 1.0 × 10–5–0.01 | 7.0 × 10–6 | 4.0 × 10–2 (Na+) 4.5 × 10–2 (Pb2+) 4.0 × 10–3 (Er3+) |
4.0–9.5 | [37] |
 |
19.8 ± 0.3 | 1.0 × 10–6–0.01 | 5.8 × 10–7 | 2.5 × 10–3 (Na+) 6.4 × 10–3 (Pb2+) 4.2 × 10–3 (Er3+) |
2.5–9.8 | [38] | |
 |
20.1 ± 0.2 | 1.0 × 10–6–0.01 | 5.0 × 10–7 | 5.9 × 10–4 (Na+) 7.4 × 10–3 (Cu2+) 2.5 × 10–4 (Dy3+) 8.2 × 10–3 (Er3+) |
3.5–9.4 | [39] | |
| Er3+ |  |
21.0 ± 0.5 | 1.0 × 10–7–0.01 | 7.0 × 10–8 | 1.3 × 10–5 (Na+) 2.9 × 10–5 (Pb2+) 3.4 × 10–4 (Ho3+) |
3.2–8.9 | [40] |
 |
19.6 ± 0.6 | 1.0 × 10–6–0.01 | 6.6 × 10–7 | 3.2 × 10–4 (Na+) 4.5 × 10–4 (Pb2+) 2.5 × 10–3 (Ho3+) |
2.8–9.3 | [41] | |
 |
20.5 ± 0.4 | 1.0 × 10–6–0.01 | 6.3 × 10–7 | 3.4 × 10–4 (Na+) 3.9 × 10–4 (Pb2+) 1.8 × 10–3 (Ho3+) |
2.5–10.6 | [42] | |
| Tm3+ |  |
19.5 ± 0.3 | 1.0 × 10–5–0.01 | 8.0 × 10–6 | 2.0 × 10–3 (K+) 7.0 × 10–3 (Pb2+) 3.0 × 10–3 (Yb3+) |
3.0–12.0 | [43] |
 |
21.2 ± 0.3 | 1.0 × 10–7–0.1 | 9.0 × 10–8 | 1.0 × 10–5 (Na+) 1.7 × 10–5 (Pb2+) 1.0 × 10–5 (Er3+) |
3.6–9.0 | [44] | |
 |
19.5 ± 0.2 | 1.0 × 10–6–0.01 | 8.7 × 10–7 | 8.3 × 10–4 (Na+) 3.4 × 10–4 (Pb2+) 6.7 × 10–3 (Yb3+) |
3.2–9.5 | [45] | |
| Yb3+ |  |
19.7 ± 0.5 | 1.0 × 10–6–0.01 | 4.4 × 10–7 | 6.8 × 10–4 (Na+) 2.3 × 10–3 (Pb2+) 6.8 × 10–4 (Tb3+) |
3.5–8.4 | [46] |
 |
19.3 ± 0.2 | 1.0 × 10–6–0.01 | 5.0 × 10–7 | 1.0 × 10–3 (Na+) 4.0 × 10–5 (Pb2+) 7.9 × 10–3 (Dy3+) |
3.5–9.0 | [47] | |
 |
19.5 ± 0.3 | 1.0 × 10–6–0.1 | 4.6 × 10–7 | 1.0 × 10–3 (Na+) 5.0 × 10–4 (Pb2+) 1.2 × 10–3 (Tb3+) |
3.3–8.0 | [48] | |
| Lu3+ | 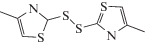 |
19.6 ± 0.4 | 1.0 × 10–6–0.01 | 6.8 × 10–7 | 7.3 × 10–4 (Na+) 7.6 × 10–4 (Co2+) 3.8 × 10–3 (Yb3+) |
2.7–9.6 | [49] |
 |
20.5 ± 0.4 | 1.0 × 10–6–0.01 | 8.0 × 10–7 | 3.2 × 10–4 (Na+) 7.9 × 10–4 (Pb2+) 5.3 × 10–3 (Yb3+) |
4.5–8.0 | [50] | |
 |
19.8 ± 0.5 | 1.0 × 10–6–0.01 | 7.2 × 10–7 | 8.7 × 10–4 (Na+) 5.8 × 10–3 (Yb3+) 2.3 × 10–2 (Ho3+) |
2.7–10.6 | [51] |
Имеются подобные публикации для всех лантанидов, что демонстрирует табл. 1. Приведены лишь отдельные примеры для каждого из лантанидов. Применяемые в сенсорах ионофоры (в некоторых публикациях употребляется название “селектофоры”) имеют самые разнообразные структуры, включающие различные функциональные группы.
Обращает на себя внимание тот факт, что величины коэффициентов селективности для описанных в литературе сенсоров на лантаниды (табл. 1) в присутствии соседних по ряду элементов неожиданно велики. Если такую селективность относительно одно- и двухзарядных катионов металлов можно было бы объяснить разницей в химической природе, то для соседних лантанидов полученные значения вызывают недоумение. Так, например, в работе [32] авторы сообщают о разнице в селективности к тербию и гадолинию практически в пять порядков (логарифм коэффициента селективности в паре тербий–гадолиний равен –4.8). В работе [35] разница между коэффициентами селективности к диспрозию и гадолинию составила около четырех порядков, в исследовании [44] обнаружена разница между коэффициентами селективности к тулию и эрбию в пять порядков. Такие поразительные результаты, противоречащие природе лантанидов, к сожалению, авторами не объясняются. Попытки нашего коллектива воспроизвести эти результаты, например, для самария на основе коммерчески доступного ионофора 1-циклогексил-3-{4-[2-(5-метилпиразин-2-карбоксамидо)этил]фенилсульфонил}мочевины, который по данным авторов работы [52] проявлял селективность к самарию при стократном избытке лантана в анализируемом растворе, не увенчались успехом. Изготовленные нами сенсоры не проявляли заявленной селективности и чувствительности к самарию.
В табл. 1 приведены рабочие диапазоны значений рН для различных сенсоров на лантаниды. Для большинства описанных в литературе сенсоров они составляют 5–6 ед. рН и захватывает щелочную область. Однако ни в одной работе не указано, что при рН > 4 катионы лантанидов значительно гидролизуются, образуя гидроксокатионы, дигидроксокатионы, гидроксиды и т.д. (рис. 2) [53]. В связи с этим не всегда понятно, к какой именно ионной форме лантанида имеют отклик разработанные сенсоры. Кроме того, такие диапазоны рН функционирования сенсоров ставят под вопрос возможность их применения для анализа технологических растворов цикла переработки ОЯТ, которая происходит в сильнокислых водных растворах, содержащих до 7 М HNO3.
Рис. 2.
Диаграмма распределения форм церия в водном растворе (воспроизведено из [53] с разрешения правообладателя. © 2004, Elsevier Masson SAS, all rights reserved).

Помимо этого в некоторых случаях (например, работы [13, 30]) предложенные структуры ионофоров подразумевают их заметную растворимость в воде, что приведет к их быстрому вымыванию из фазы полимерной мембраны при измерениях в водных образцах.
Таким образом, характеристики подавляющего большинства описанных в литературе сенсоров вызывают целый ряд вопросов и их применение для контроля реальных технологических процессов вряд ли возможно.
Обойти ограничения, связанные с селективностью отдельных сенсоров, успешно позволяет мультисенсорный подход [54], который заключается в применении массива перекрестно-чувствительных сенсоров в сочетании с методами хемометрики. Каждый отдельный сенсор массива обладает выраженной чувствительностью сразу к нескольким компонентам анализируемого раствора (и не обладает высокой селективностью), при этом для различных сенсоров характер этой чувствительности в ряду одних и тех же веществ должен существенным образом различаться. Например, если речь идет о растворах лантанидов, то часть сенсоров массива должна обеспечивать более высокую чувствительность к легким лантанидам, а другая часть – к тяжелым лантанидам. При этом селективность любого сенсора в паре двух соседних лантанидов может быть незначительной или отсутствовать вовсе. Для массива в целом, разумеется, крайне желательно использовать сенсоры с максимальной вариабельностью чувствительности к определяемым элементам. В сложных многокомпонентных растворах такой массив сенсоров дает отклик, подобный неразрешенному электрохимическому “спектру” образца. Обработка “спектра” современными методами многомерной статистки позволяет строить математические модели, связывающие отклики сенсоров с качественным и количественным составом анализируемых растворов (проводить многомерную градуировку массива). Стандартная схема применения мультисенсорных систем заключается в подборе подходящего набора сенсоров, серии измерений с этим массивом в градуировочных образцах с известным содержанием целевых компонентов и последующей многомерной градуировке с помощью методов хемометрики. Для создания таких сенсоров, обладающих выраженной чувствительностью к лантанидам, нашей исследовательской группой предложено использовать вещества и закономерности, ранее изученные при жидкостной экстракции для разделения и концентрирования лантанидов и актинидов. Сама идея заимствования лигандов из экстракции для создания, например, ионселективных электродов, разумеется, не нова. Так, одно из первых исследований на эту тему, опубликованное более 50 лет назад [55], было посвящено разработке кальцийселективного электрода. При разработке экстракционных систем для обращения с ОЯТ новые лиганды проходят проверку на устойчивость к радиолизу и кислотному гидролизу, поэтому их использование в сенсорах для определения лантанидов в технологических растворах представляется вполне логичным.
В первых наших работах [56, 57], использующих описанный подход, были изучены электрохимические характеристики полимерных пластифицированных мембран, содержащих бидентатные нейтральные фосфорорганические соединения (рис. 3). Интересной особенностью этих работ является то, что в качестве катионообменной добавки в разработанных сенсорах предложено использовать не традиционные для ионометрии производные тетрафенилбората, а стабильный по отношению к кислотному гидролизу хлорированный дикарболлид кобальта (ХДК), широко применяемый в экстракции [58].
Разработанные таким образом сенсоры проявляли высокую чувствительность к трехзарядным катионам редкоземельных элементов в кислых растворах (рН 2, по азотной кислоте). В некоторых случаях электроды проявляли супер-нернстовскую чувствительность (29.5 мВ/дек), характерную для двухзарядных катионов. Этот факт можно объяснить тем, что трехзарядный катион лантанида в присутствии значительных количеств бифункциональных нейтральных фосфорорганических соединений может присоединять к себе один нитрат-анион, а соединение состава Ln(NO3)2+ имеет формальный заряд 2+. Такое явление зафиксировано при масс-спектрометрических исследованиях с электроспрей ионизацией [59]. Следует отметить, что, в отличие от цитируемых в книге [7] работ, нам не удалось зарегистрировать значительной разности в электродных чувствительностях этих сенсоров к соседним лантанидам. Так, например, во всех случаях чувствительность к празеодиму и неодиму практически одинакова, что логично при их соседстве в Периодической системе и хорошо согласуется с данными по коэффициентам распределения лантанидов.
В наших работах [60–62] перечень лигандов был расширен за счет фосфорилсодержащих подандов и диамидов различных органических кислот. Предприняты первые попытки [62] использования разработанных сенсоров в составе мультисенсорной системы для селективного определения отдельных лантанидов в двойных и тройных смесях. В состав мультисенсорной системы вошли 12 разработанных сенсоров с различной перекрестной чувствительностью. Были приготовлены модельные растворы, содержащие четыре трехзарядных катиона: церий и неодим, самарий и гадолиний. Эти ионы присутствуют в растворах, образующихся в процессе переработки облученного топлива. Церий и неодим выбраны как присутствующие в наибольших концентрациях по сравнению с остальными лантанидами, а самарий и гадолиний, хотя и присутствуют в заметно меньших количествах, являются нейтронными ядами и их концентрацию следует контролировать. Достигнута приемлемая точность при определении неодима в смеси с церием и гадолиния в смеси с самарием. В случае использования мультисенсорных систем возможность селективного определения отдельных лантанидов достигается за счет определенных различий в характере чувствительности отдельных сенсоров, составляющих систему, к различным лантанидам. Эти различия учитываются в ходе хемометрической обработки получаемых данных.
В работе [63] нами изучено влияние модификации нижнего и верхнего ободов каликсаренового ионофора фосфиноксидными и диамидными группами на чувствительность соответствующих сенсоров к лантанидам в кислых водных растворах. Показано, что каликсарен, содержащий фосфиноксидные группы на верхнем ободе, обладает как более высокой экстракционной способностью, так и более высокой чувствительностью соответствующих сенсоров по сравнению с простыми фосфиноксидными лигандами. В то же время модификация каликсарена по верхнему ободу диамидными группами приводила к некоторому выравниванию чувствительности сенсоров в ряду лантанидов.
Работа [64] посвящена синтезу и изучению экстракционных и сенсорных свойств диамидов 2,2'-дипиридил-6,6'-дикарбоновой кислоты. Новые лиганды оказались пригодными для жидкостной экстракции лантанидов из азотнокислых растворов, однако сенсоры на основе этих лигандов не проявили чувствительности к трехзарядным катионам в кислых водных растворах. Между тем отдельные разработанные сенсоры продемонстрировали высокую селективность к кадмию [65].
В работе [66] изучены диамиды дипиколиновой кислоты. Все сенсоры, разработанные на основе этих соединений, обладали высокой чувствительностью ко всем изученным лантанидам: La, Ce, Pr, Nd, Sm, Eu, Gd, Lu. Наклоны электродных функций, полученные в азотнокислой среде при рН 2, составили 16–28 мВ/дек.
Нами изучены также диамиды 1,10-фенантролин-2,9-дикарбоновой кислоты [67]. Несмотря на то, что эти соединения продемонстрировали интересные экстракционные свойства при разделении лантанидов и актинидов, сенсоры на их основе заметной чувствительности к лантанидам не проявили.
В работе [68] мультисенсорную систему на основе 14 разработанных ранее сенсоров исследовали в тройных смесях редкоземельных элементов в диапазонах концентраций 10–5–10–3 М (иттрий–лантан–гадолиний, а также неодим–самарий–гадолиний) с добавлением урана и тория (как аналога плутония) в концентрации 10–4 М. Состав смесей моделировал типичные технологические растворы с различных этапов цикла переработки ОЯТ. Использование метода проекций на латентные структуры для обработки данных от массива сенсоров позволило определять концентрации отдельных элементов в сложных смесях с точностью, приемлемой для технологических нужд. Полученные данные представлены в табл. 2.
Таблица 2.
Характеристики разработанных сенсоров и мультисенсорных систем в растворах лантанидов
| Аналит | Ионофоры и добавки | Диапазон чувствительности, мВ/дек | Линейный диапазон, М | рН | Литература |
|---|---|---|---|---|---|
| La3+ Pr3+ Nd3+ Eu3+ | Фосфиноксиды, с добавкой ХДК (рис. 3) |
18–34 | 1 × 10–7–0.01 | 2 | [56, 57] |
| Ce3+ Nd3+ Sm3+ |
Фосфиноксиды, диамиды органических кислот, ХДК, TБФБ | 10–31 | 1 × 10–6–0.01 | 1.6 | [60] |
| La3+– Lu3+ | Фосфиноксиды, ХДК, TБФБ, ТОДГА | 15–41 | 1 × 10–7–1 × 10–3 | 2 | [61] |
| Ce3+ Nd3+ Sm3+ Gd3+ | Фосфиноксиды, ХДК, диамиды орг. кислот, фосфорилсодержащие поданды | 12–29 | 1 × 10–5–1 × 10–3 | 2 | [62] |
| La3+– Lu3+ | Каликсарены, НФОЭ, ТОДГА, ХДК | 11–25 | 1 × 10–7–0.01 | 2 | [63] |
| La3+– Lu3+ | Диамиды дипиколиновой кислоты, НФОЭ, ХДК, TБФБ | 16–28 | 1 × 10–6–1 × 10–3 | 2 | [66] |
| Y3+ La3+ Gd3+ Nd3+ Sm3+ |
Фосфиноксиды, диамиды орг. кислот, каликсарены, диамиды дипиколиновой кислоты | 13–24 | 1 × 10–5–1 × 10–3 | 1.5 | [68] |
Сравнение полученных нами и приведенных в литературе данных по индивидуальными сенсорам для определения лантанидов (табл. 1) позволяет отметить ряд преимуществ нашего подхода. Во-первых, чувствительность сенсоров в наших исследованиях определяется при рН ≤ 2; при этом в водных растворах преобладает трехзарядная негидролизованная форма катиона лантанида. Такие условия ближе к составу реальных технологических растворов, в которых определяют лантаниды, чем применяемые в других работах водные растворы с рН ≥ 4. Во-вторых, достигнутые нами величины электродной чувствительности для ряда разработанных мембранных композиций существенно превышают величины 19–20 мВ/дек, приведенные в литературе. Несмотря на супер-нернстовский характер отклика некоторых сенсоров на основе лигандов, заимствованных из жидкостной экстракции, он хорошо воспроизводим, и разработанные сенсоры пригодны для практического применения. Следует отметить, что величины чувствительности получены нами в жестких для потенциометрических сенсоров условиях (сильнокислые водные растворы). В‑третьих, несмотря на имеющиеся литературные данные по селективным сенсорам для отдельных катионов ряда лантанидов, на достаточно широком круге лигандов с различными функциональными группами нами показано, что высокой селективности к отдельным лантанидам добиться практически не-возможно. Селективно определять лантаниды в смесях потенциометрическими сенсорами можно только с помощью мультисенсорного подхода.
Результаты описанного цикла исследований нашей группы позволяют говорить о перспективности подхода к разработке сенсоров и мультисенсорных систем для определения лантанидов. Использование лигандов, ранее изученных в жидкостной экстракции, оказалось эффективным при создании перекрестно-чувствительных сенсоров, пригодных для количественного определения лантанидов в кислых водных растворах. Так, например, при экстракции лантанидов с помощью ТОДГА тяжелые лантаниды экстрагируются лучше легких. В то же время соответствующие потен-циометрические сенсоры более чувствительны к тяжелым лантанидам, чем к легким [61].
Аналогия экстракционных свойств и свойств мембраны, содержащей ионофор, наблюдается далеко не всегда. Для некоторых лигандов изменение чувствительности сенсоров в ряду РЗЭ совпадает с полученным при экстракции. В то же время для амидов 1,10-фенантролин-2,9-дикарбоновой и 2,2'-дипиридил-6,6'-дикарбоновой кислот эти зависимости резко отличаются: они проявляют экстракционную способность по отношению к лантанидам, но у соответствующих сенсоров отсутствует электрохимическая чувствительность к лантанидам [64, 67]. Однако при этом можно получить полимерные пластифицированные мембраны с высокой селективностью к ионам переходных металлов, таких, например, как свинец [69] и кадмий [65].
В настоящее время в нашей группе активно продолжаются исследования по разработке новых перекрестно-чувствительных сенсоров и мультисенсорных систем, усложняются составы модельных растворов, которые приближаются к составу реальных сред.
* * *
Описан подход к разработке мультисенсорных систем для определения лантанидов в сложных смесях, основанный на использовании веществ, предложенных в жидкостной экстракции для разделения и концентрирования лантанидов и актинидов, в качестве мембраноактивных компонентов в полимерных пластифицированных мембранах потенциометрических сенсоров. Применение массивов таких сенсоров с последующей хемометрической обработкой получаемых данных позволяет количественно определять лантаниды в кислых водных растворах, моделирующих состав технологических сред цикла переработки ОЯТ.
Публикация подготовлена при финансовой поддержке проекта РНФ 18-19-00151.
Список литературы
Власов Ю.Г. Химические сенсоры / Проблемы аналитической химии. Т. 14. М.: Наука, 2010. 399 с.
Fisher A., Kara D. Determination of rare earth elements in natural water samples – a review of sample separation, preconcentration and direct methodologies // Anal. Chim. Acta. 2016. V. 935. P. 1.
Betti M., Menichetti L., Barrero Moreno J.M., Fuoco R. A preliminary study for the determination of long-lived radionuclides (second transition group 4-d) in environmental samples by ion chromatography inductively coupled plasma-mass spectrometry (IC-ICP-MS) // Microchem. J. 2000. V. 67. P. 285.
Pitois A., Las Heras L.A., Betti M. Determination of fission products in nuclear samples by capillary electrophoresis-inductively coupled plasma mass spectrometry (CE-ICP-MS) // Int. J. Mass. Spectrom. 2008. V. 270. P. 118.
Becker J.S. Recent developments in isotope analysis by advanced mass spectrometric techniques // J. Anal. A-tom. Spectrom. 2005. V. 20. P. 1173.
Михельсон К.Н., Пешкова М.А. Химические сенсоры на основе ионофоров: достижения и перспективы // Успехи химии. 2015. Т. 84. № 6. С. 555.
Ganjali M.R., Gupta V.K., Faridbod F., Norouzi P. Lanthanides Series Determination by Various Analytical Methods. Amsterdam: Elsevier, 2016. 448 p.
Shamsipur M., Yousefi M., Ganjali M.R. PVC-based 1,3,5-trithiane sensor for cerium(III) ions // Anal. Chem. 2000. V. 72. P. 2391.
Abedi M.R., Zamani H.A., Ganjali M.R., Norouzi P. Determination of cerium(III) ions in soil and sediment samples by Ce(III) PVC-based membrane electrode based on 2,5-dioxo-4-imidazolidinyl // Int. J. Environ. Anal. Chem. 2008. V. 88. № 5. P. 353.
Rounaghi G., Kakhki R.M.Z., Sadeghian H. A new cerium(III) ion selective electrode based on 2,9-dihydroxy-1,10-diphenoxy-4,7-dithia decane, a novel synthetic ligand // Electrochim. Acta. 2011. V. 56. P. 9756.
D’Angelo P., Zitolo A., Migliorati V., Chillemi G., Duvail M., Vitorge P., Abadie S., Spezia R. Revised ionic radii of lanthanoid(iii) ions in aqueous solution // Inorg. Chem. 2011. V. 50. P. 4572.
Shamsipur M., Yousefi M., Hosseini M., Ganjali M.R. Lanthanum(III) PVC membrane electrodes based on 1,3,5-trithiacyclohexane // Anal. Chem. 2002. V. 74. P. 5538.
Jain A.K., Singh A.K., Mehtab S., Saxena P. Rubeanic acid as novel carrier in construction of selective membrane sensor for La(III) // Anal. Chim. Acta. 2005. V. 551. P. 45.
Mittal S.K., Kumar S.K.A., Sharma H.K. PVC-based dicyclohexano-18-crown-6 sensor for La(III) ions // Talanta. 2004. V. 62. P. 801.
Ganjali M.R., Khoshsafar H., Faridbod F., Shirzadmehr A., Javanbakht M., Norouzi P. Room temperature ionic liquids (RTILs) and multiwalled carbon nanotubes (MWCNTs) as modifiers for improvement of carbon paste ion selective electrode response; a comparison study with PVC membrane // Electroanalysis. 2009. V. 21. P. 2175.
Zamani H.A., Arvinfar A., Rahimi F., Imani A., Ganjali M.R., Meghdadi S. Praseodymium analysis in aqueous solution by Pr3+-PVC membrane sensor based on N,N'-bis(4-hydroxysalicylidene)-1-3-phenylenediamine // Mater. Sci. Eng. C. 2011. V. 31. P. 307.
Pourjavid M.R., Rezaee M., Hosseini M.H., Razavi T. Monitoring of praseodymium(III) ions in aqueous solutions, soil and sediment samples by a PVC membrane sensor based on a furan-triazole derivative // Quim. Nova. 2012. V. 35. P. 1973.
Norouzi P., Ganjali M.R., Ahmadalinezhad A., Adib M. Novel neodymium(III) membrane sensor based on N-(2-furylmethylene)pyridine-2,6-diamine // J. Braz. Chem. Soc. 2006. V. 17. P. 1309.
Shamsipur M., Hosseini M., Alizadeh K., Mousavi M.F., Garau A., Lippolis V., Yari A. PVC membrane potentiometric sensor based on 5-pyridino-2,8-dithia-9-(2,9)-1,10-phenanthroline-phane for selective determination of neodymium(III) // Anal. Chem. 2005. V. 77. P. 276.
Ganjali M.R., Ahmadalinezhad A., Norouzi P., Adib M. Nd(III)-PVC membrane sensor based on 2-{(6-aminopyridin-2-yl)imino methyl}-phenol // J. Appl. Electrochem. 2006. V. 36. P. 931.
Gupta V.K., Jain R., Hamdan A.J., Agarwal S., Bharti A.K. A novel ion selective sensor for promethium determination // Anal. Chim. Acta. 2010. V. 681. P. 27.
Ganjali M.R., Memari Z., Faridbod F., Dinarvand R., Norouzi P. Sm3+ potentiometric membrane sensor as a probe for determination of some pharmaceutics // Electroanalysis. 2008. V. 20. P. 2663.
Shamsipur M., Hosseini M., Alizadeh K., Eskandari M.M., Sharghi H., Mousavi M.F., Ganjali M.R. Polymeric membrane and coated graphite samarium(III)-selective electrodes based on isopropyl 2-(isopropoxycarbothioyl)disulfanyl ethanethioate // Anal. Chim. Acta. 2003. V. 486. P. 93.
Naddaf E., Zamani H.A. Samarium(III)-PVC-membrane sensor based on ethoxy-1-ethoxycarbonyl-1,2-dihydroquinoline // Anal. Lett. 2009. V. 42. P. 2838.
Ganjali M.R., Rahimi-Nasrabadi M., Maddah B., Moghimi A., Borhany S. An Eu(III) sensor based on N,N-diethyl-N-(4-hydroxy-6-methylpyridin-2-yl)gua-nidine // Anal. Sci. 2004. V. 20. P. 1427.
Abedi M.R., Zamani H.A. Construction of Eu3+ ion-selective electrode based on 1,2-diaminopropane-N,N,N',N'-tetraacetic acid // E-J. Chem. 2011. V. 8. P. 467.
Zamani H.A., Kamjoo R., Mohammadhosseini M., Zafero-ni M., Rafati Z., Ganjali M.R., Faridbod F., Meghdadi S. Europium(III) PVC membrane sensor based on N‑pyridine-2-carboxamido-8-aminoquinoline as a sensing material // Mater. Sci. Eng. C. 2012. V. 32. P. 447.
Ganjali M.R., Norouzi P., Alizadeh T., Tajarodi A., Ha-nifehpour Y. Fabrication of a highly selective and sensitive Gd(III)-PVC membrane sensor based on N-(2-pyridyl)-N'-(4-nitrophenyl)thiourea // Sens. Actuators B. 2007. V. 120. P. 487.
Gupta V.K., Singh A.K., Kumawat L.K. A novel gadolinium ion-selective membrane electrode based on 2-(4-phenyl-1,3-thiazol-2-yliminomethyl) phenol // Electrochim. Acta. 2013. V. 95. P. 132.
Zamani H.A., Behmadi H. Gadolinium(III) ion-selective electrode based on 3-methyl-1H-1,2,4-triazole-5-thiol // E-J. Chem. 2012. V. 9. P. 308.
Ganjali M.R., Ghesmi A., Hosseini M., Pourjavid M.R., Rezapour M., Shamsipur M., Salavati-Niasari M. Novel terbium(III) sensor based on a new bis-pyrrolidene Schiff’s base // Sens. Actuators B. 2005. V. 105. P. 334.
Gupta V.K., Singh A.K., Gupta B. Electroanalytical performance of a terbium(III)-selective sensor based on a neutral ionophore in environmental and medicinal samples // Anal. Bioanal. Chem. 2008. V. 390. P. 2171.
Zamani H.A., Ganjali M.R., Norouzi P., Tadjarodi A., Shahsavani E. Determination of terbium(III) ions in phosphate rock samples by a Tb3+-PVC membrane sensor based on N,N-Dimethyl-N',N"-bis(4-methoxyphenyl)phosphoramidate // Mater. Sci. Eng. C. 2008. V. 28. P. 1489.
Ganjali M.R., Ravanshad J., Hosseini M., Salavati-Niasari M., Pourjavid M.R., Baezzat M.R. Novel Dy(III) sensor based on a new bis-pyrrolidene Schiff’s base // Electroanalysis. 2004. V. 16. P. 1771.
Zamani H.A., Mohaddeszadeh M. Determination of dysprosium(III) ion in soil and sediment samples by an original potentiometric dysprosium(III) membrane sensor // Anal. Lett. 2008. V. 41. P. 2710.
Zamani H.A., Faridbod F., Ganjali M.R. Dysprosium selective potentiometric membrane sensor // Mater. Sci. Eng. C. 2013. V. 33. P. 608.
Ganjali M.R., Norouzi P., Adib M., Ahmadalinezhad A. A novel Holmium(III) membrane sensor based on N-(1-thien-2-ylmethylene)-1,3-benzothiazol-2-amine // Anal. Lett. 2006. V. 39. P. 1075.
Zamani H.A. N-1,N-2-Bis-1-(2-hydroxyphenyl)methylidene ethanedihydrazide as a neutral ionophore for preparation of a new Ho3+ PVC-membrane sensor // Chin. Chem. Lett. 2011. V. 22. P. 701.
Zamani H.A., Zanganeh-Asadabadi A., Rohani M., Zabihi M.S., Fadaee J., Ganjali M.R., Faridbod F., Meghdadi S. A Ho(III) potentiometric polymeric membrane sensor based on a new four dentate neutral ion carrier // Mater. Sci. Eng. C. 2013. V. 33. P. 984.
Ganjali M.R., Faridbod F., Norouzi P., Adib M. A novel Er(III) sensor based on a new hydrazone for the monitoring of Er(III) ions // Sens. Actuators B. 2006. V. 120. P. 119.
Nekoei M., Zamani H.A., Mohammadhossieni M. Erbium(III) PVC membrane ion-selective sensor based on 4-(2-thiazolylazo)resorcinol // Anal. Lett. 2009. V. 42. P. 284.
Zamani H.A. Erbium(III) PVC membrane sensor based on N-(benzyloxycarbonyloxy) succinimide as a new neutral ionophore // Chin. Chem. Lett. 2011. V. 22. P. 346.
Ganjali M.R., Rasoolipour S., Rezapour M., Norouzi P., Adib M. Synthesis of thiophene- 2-carbaldehyde-(7-methyl-1,3-benzothiazol-2-yl)hydrazone and its application as an ionophore in the construction of a novel thulium(III) selective membrane sensor // Electrochem. Commun. 2005. V. 7. P. 989.
Ganjali M.R., Norouzi P., Farrokhi R., Faridbod F., La-rijani B., Meghdadi S. Lanthanide recognition: Determination of thulium(III) ions in presence of other rare earth elements by a thulium(III) sensor based on 4-methyl-1,2-bis(2-pyridinecarboxamido)benzene as a sensing material // Anal. Lett. 2008. V. 41. P. 2322.
Zamani H.A., Nekoei M., Mohammadhosseini M., Ganjali M.R. Construction of Tm3+-PVC membrane sensor based on 1-(2-thiazolylazo)-2-naphthol as sensing material // Mater. Sci. Eng. C. 2010. V. 30. P. 480.
Ebrahimi M., Zamani H.A. Determination of ytterbium(III) ions in soil and sediment samples by a new polymeric Yb3+-PVC membrane sensor // Anal. Lett. 2009. V. 42. № 7. P. 1041.
Ganjali M.R., Rasoolipour S., Rezapour M., Norouzi P., Tajarodi A., Hanifehpour Y. Novel ytterbium(III) selective membrane sensor based on N-(2-pyridyl)-N'-(2-methoxyphenyl)-thiourea as an excellent carrier and its application to determination of fluoride in mouth wash preparation samples // Electroanalysis. 2005. V. 17. P. 1534.
Zamani H.A., Rajabzadeh G., Ganjali M.R. A new ytterbium(III) PVC membrane electrode based on 6-methy-4-{1-(1H-pyrrol-2-yl)methylidene amino}-3-thioxo-3,4-dihydro-1, 2,4-triazin-5(2H)-one // Talanta. 2007. V. 72. P. 1093.
Abedi M.R., Zamani H.A. Application of 2,2'-dithiobis(4-methylthiazole) as sensing material for construction of Lu3+ PVC-membrane sensor // Chin. Chem. Lett. 2011. V. 22. № 8. P. 977.
Ganjali M.R., Tamaddon A., Norouzi P., Adib M. Novel Lu(III) membrane sensor based on a new asymmetrically S-N Schiff’s base // Sens. Actuators B. 2006. V. 120. P. 194.
Zamani H.A., Rohani M., Zangeneh-Asadabadi A., Zabihi M.S., Ganjali M.R., Salavati- Niasari M. A novel lutetium(III) PVC membrane sensor based on a new symmetric S-N Schiff’s base for Lu(III) analysis in real sample // Mater. Sci. Eng. C. 2010. V. 30. P. 917.
Ganjali M.R., Pourjavid M.R., Rezapour M., Haghgoo S. Novel samarium(III) selective membrane sensor based on glipizide // Sens. Actuators B. 2003. V. 89. P. 21.
Bentouhami E., Bouet G.M., Meullemeestre J., Vierling F., Khan M.A. Physicochemical study of the hydrolysis of rare-earth elements(III) and thoriu (IV) // C. R. Chim. 2004. V. 7. P. 537.
Власов Ю.Г., Легин А.В., Рудницкая А.М. Мультисенсорные системы типа электронный язык – новые возможности создания и применения химических сенсоров // Успехи химии. 2006. Т. 75. № 2. С. 141.
Ross J.W. Calcium-selective electrode with liquid ion exchanger // Sci. New Series. 1967. V. 156. P. 1378.
Кирсанов Д.О., Легин А.В., Бабаин В.А., Власов Ю.Г. Полимерные сенсоры на основе экстракционных систем для определения редкоземельных металлов // Журн. прикл. химии. 2005. Т. 78. № 4. С. 575. (Kirsanov D.O., Legin A.V., Babain V.A., Vlasov Y.G. Polymeric sensors based on extraction systems for determination of rare-earth metals // Russ. J. Appl. Chem. 2005. V. 78. № 4. P. 568.)
Legin A.V., Kirsanov D.O., Babain V.A., Borovoy A.V., Herbst R.S. Cross-sensitive rare-earth metal sensors based on bidentate neutral organophosphorus compounds and chlorinated cobalt dicarbollide // Anal. Chim. Acta. 2006. V. 572. P. 243.
Rais J., Grüner B. Extractions with metal bis(dicarbollide) anions: metal bis(dicarbollide) extractants and their applications in separation chemistry // Ion Ex. Solv. 2004. V. 17. P. 243.
Галль Л.Н., Чуприков A.B., Шадрин А.Ю., Смирнов И.В. Исследование комплексных соединений в растворах методом электрораспылительной масс-спектрометрии // Докл. АН. 1992. Т. 325. № 3. С. 514.
Кирсанов Д.О., Легин А.В., Бабаин В.А., Меднова О.В., Власов Ю.Г. Новые сенсоры и мультисенсорные системы (“электронный язык”) для анализа растворов отработанного ядерного топлива // Вестн. СПбГУ. 2007. Сер. 4. № 4. С. 84.
Legin A.V., Babain V.A., Kirsanov D.O., Mednova O.V. Cross-sensitive rare earth metal ion sensors based on extraction systems // Sens. Actuators B. 2008. V. 131. P. 29.
Babain V.A., Legin A.V., Kirsanov D.O., Rudnitskaya A.M., Tatuev Y.M., Baulin V.E. New chemical sensors based on extraction systems for stable fission products analysis // Radiochim. Acta. 2009. V. 97. P. 479.
Alyapyshev M.Yu., Babain V.A., Boyko V.I., Eliseev I.I., Kirsanov D.O., Klimchuk O.V., Legin A.V., Mikhailina E.S., Rodik R.V., Smirnov I.V. Calixarenes functionalized with phosphine oxide and diamide functions as extractants and ionofores for rare-earth metals // J. Incl. Phenom. Macrocycl. Chem. 2010. V. 67. P. 117.
Alyapyshev M., Babain V., Borisova N., Eliseev I., Kirsanov D., Kostin A., Legin A., Reshetova M., Smirnova Z. 2,2'-Dipyridyl-6,6'-dicarboxylic acid diamides: Synthesis, complexation and extraction properties // Polyhedron. 2010. V. 29. P. 1998.
Легин А.В., Кирсанов Д.О., Аляпышев М.Ю., Бабаин В.А., Смирнова З.Б., Легин Е.А., Елисеев И.И., Борисова Н.Е., Решетова М.Д., Костин А.А. Состав мембраны ионоселективного электрода для определения ионов кадмия. Патент № 2428683 РФ. Заявка 2010121317/28 от 27.05.2010. Опубл. 10.09.2011.
Спиридонов И.Г., Кирсанов Д.О., Бабаин В.А., Аляпышев М.Ю., Елисеев И.И., Власов Ю.Г., Легин А.В. Полимерные сенсоры для определения ионов редкоземельных металлов на основе диамидов дипиколиновой кислоты // Журн. прикл. химии. 2011. Т. 84. № 8. С. 1289. (Spiridonov I.G., Kirsanov D.O., Babain V.A., Alyapyshev M.Yu., Eliseev N.I., Vlasov Yu.G., Legin A.V. Polymeric sensors for determination of rare-earth metal ions, based on diamides of dipicolinic acid // Russ. J. Appl. Chem. 2011. V. 84. № 8. Р. 1354.)
Alyapyshev M., Ashina J., Dar’in D., Kenf E., Kirsanov D., Tk-achenko L., Legin A., Starova G., Babain V. 1,10-Phenanthroline-2,9-dicarboxamides as ligands for separation and sensing of hazardous metals // RSC Adv. 2016. V. 6. P. 68642.
Kirsanov D., Khaydukova M., Tkachenko L., Legin A., Babain V. Potentiometric Sensor Array for Analysis of Complex Rare Earth Mixtures // Electroanalysis. 2012. V. 24. № 1. P. 121.
Кирсанов Д.О., Легин А.В., Бабаин В.А., Польшин Е.Н., Рудницкая А.М., Легин К.А., Селезнев Б.Л. Состав мембраны ионоселективного электрода для определения ионов свинца. Патент № 2315988 РФ. Заявка 2006122863/28 от 28.06.2006. Опубл. 21.01.2008.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии