Журнал аналитической химии, 2019, T. 74, № 8, стр. 624-633
Изучение подвижности наночастиц оксида церия в почвах с использованием динамического экстрагирования в микроколонке и вращающейся спиральной колонке
М. С. Ермолин a, *, Н. Н. Федюнина b, В. К. Карандашев c, П. С. Федотов a
a Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук
119991 Москва, ул. Косыгина, 19, Россия
b Национальный исследовательский технологический университет “МИСиС”
119049 Москва, Ленинский просп., 4, Россия
c Институт проблем технологии микроэлектроники и особочистых материалов Российской академии наук
142432 Московская обл., Черноголовка, ул. Институтская, 6, Россия
* E-mail: mihail.ermolin@gmail.com
Поступила в редакцию 09.04.2018
После доработки 07.05.2018
Принята к публикации 09.03.2019
Аннотация
В настоящее время наноматериалы находят широкое применение в различных сферах человеческой деятельности, что неизбежно приводит к их попаданию в окружающую среду, при этом почвы являются одним из основных резервуаров для наночастиц (НЧ). Поскольку НЧ могут быть особенно токсичными для живых организмов, разработка новых подходов к оценке их поведения и подвижности в почвах является важной задачей. В настоящей работе для оценки поведения НЧ в почвах изучены аналитические возможности динамического экстрагирования НЧ CeO2 в микроколонке (МК) и вращающейся спиральной колонке (ВСК). Построены дифференциальные и интегральные кривые элюирования НЧ CeO2 из почвы на основе данных анализа элюата методом масс-спектрометрии с индуктивно связанной плазмой. Показано, что после прокачивания 100 мл воды из почвы в МК и ВСК вымывается соответственно 0.15 и 1.37 мкг НЧ CeO2, что составляет 0.2 и 1.6% от введенных НЧ. Соотношение НЧ CeO2 и минеральных частиц почвы в 2 раза выше в элюате МК. Установлено, что ВСК позволяет оценить максимальную подвижность НЧ в почве за счет нивелирования влияния ее структуры на их транспорт. Микроколонка за счет сохранения почвенный структуры позволяет наиболее корректно оценить подвижность НЧ в реальном почвенном столбе. Изучено влияние модификации поверхности НЧ CeO2 лимонной кислотой на их подвижность в почве. Показано, что НЧ CeO2, модифицированные лимонной кислотой, обладают большей подвижностью в почве по сравнению с немодифицированными НЧ.
В настоящее время наноматериалы за счет своих уникальных химических и физических свойств находят широкое применение в различных сферах человеческой деятельности: металлургии [1], медицине [2, 3], косметологии [4, 5], научных исследованиях (в том числе и аналитической химии [6]) и т.д. Такое повсеместное применение наноматериалов неизбежно приводит к их попаданию в окружающую среду [7, 8]. Согласно последним оценкам, именно синтетические НЧ, в отличие от существующих на Земле с незапамятных времен природных наночастиц, могут быть особенно токсичными для живых организмов [9–12], что обусловливает необходимость создания новых аналитических подходов к обнаружению, количественному определению, а также к оценке поведения и подвижности синтетических НЧ в объектах окружающей среды. Возможность обнаружения и количественного определения НЧ является необходимым условием получения информации о форме их нахождения, поведении и подвижности, что в свою очередь позволяет судить о биологической доступности НЧ и, следовательно, об их потенциальной опасности для живых организмов [13].
Водные системы и почвы являются основными резервуарами для НЧ, попадающих в окружающую среду с бытовыми и технологическими стоками, атмосферными осадками и т.п. [14]. В настоящее время в большей степени изучены поведение и транспорт наночастиц в водных системах [13]. Более того, прогноз поведения частиц в данном случае может быть сделан при помощи существующих теоретических моделей коллоидной химии (например, теории Дерягина–Ландау–Фервея–Овербека) [13]. Почвы же являются значительно более сложным объектом окружающей среды, где, в отличие от водных систем, поведение и миграция наночастиц зависят от значительно большего числа параметров (например, типа и структуры почв, их минерального и гранулометрического состава, содержания органического вещества, pH и т.д.).
Помимо случайных сценариев попадания в почву, НЧ также могут намеренно добавлять в почву. Так, на сегодняшний день одной из передовых тенденций в агрохимии, направленных на повышение урожайности растений, защиту их от вредителей и болезней, а также на снижение количества химических препаратов, традиционно используемых в сельском хозяйстве, является применение так называемых “наноудобрений” и “нанопестицидов”, которые позволяют более эффективно и “адресно” выполнять свои функции [15–17]. В качестве таких нанопрепаратов, в частности, используют наночастицы металлов и оксидов металлов, таких как Ag, Au, ZnO, Cu, CeO2 и т.д.
Наночастицы CeO2 находятся в десятке самых производимых наночастиц в мире [18]. По некоторым оценкам из 10 тыс. тонн НЧ CeO2, произведенных в 2010 г., 1.4 тыс. тонн в итоге попали в почву [18]. Наряду с применением в автоиндустрии, микроэлектронике и оптике, в последние годы ведутся исследования по применению НЧ CeO2 в качестве наноудобрения. Например, показано, что добавление НЧ CeO2 в почву в концентрации 500 мкг/г приводит к улучшению роста и урожайности пшеницы [19], а также увеличению биомассы ячменя [20]. Кроме того, ряд исследований показал, что НЧ CeO2 влияют на активность ферментов-антиоксидантов в растениях. Известно, что добавление 800 мкг/г НЧ CeO2 увеличивает активность каталазы и аскорбат-пероксидазы в ростках кукурузы [21]. Сообщается [22], что при концентрации НЧ CeO2 в почве 500 мкг/г увеличивается активность аскорбат-пероксидазы, но при этом уменьшается активность каталазы в корнях риса. Помимо НЧ CeO2 с немодифицированной поверхностью, исследовали и НЧ CeO2, модифицированные лимонной кислотой (ЛК). Показано [23], что добавление в почву 500 мкг/г НЧ CeO2 и СeO2/ЛК приводит к увеличению длины стеблей томатов, при этом НЧ СeO2/ЛК повышают активность каталазы в листьях. На примере редиса также показано, что модификация поверхности НЧ CeO2 лимонной кислотой приводит к значительному уменьшению степени их поглощения растением (по сравнению с немодифицированными НЧ CeO2), что снижает потенциальную токсичность растения [24]. При этом НЧ СeO2/ЛК обладают значительно меньшим ζ-потенциалом и размером [24], что делает их более подвижными в окружающей среде.
Таким образом, проблема изучения поведения и подвижности НЧ в почвах является чрезвычайно актуальной. Данные о подвижности НЧ в почвах необходимы в контексте оценки их биологической доступности, которая обусловливает как эффективность их применения по прямому назначению, так и потенциальный риск для живых организмов вследствие токсических свойств. Ключом к пониманию поведения, связывания и миграции НЧ в почвах является создание новых аналитических подходов к их обнаружению и количественному определению [13].
При моделировании различных процессов, происходящих в почвах, проточные методы обладают неоспоримым преимуществом перед статическими, поскольку все процессы, происходящие в естественных условиях, носят динамический характер. Существуют различных варианты исполнения почвенных колонок для моделирования динамических процессов в почвах, каждый из которых имеет свои преимущества и недостатки [25]. Насыщенные почвенные колонки (полностью насыщенные элюентом, без воздуха в почвенных порах) обладают преимуществом перед ненасыщенными с точки зрения аналитических возможностей, а именно позволяют получать более воспроизводимые результаты в лабораторных условиях [25]. Эксперименты с ненасыщенными почвенными колонками позволяют наиболее точно смоделировать реальные процессы в природных условиях, однако они трудно реализуемы в лабораторных условиях, при этом их результаты плохо воспроизводимы [25].
Микроколонка и вращающаяся спиральная колонка, активно применяемые в вещественном анализе почв для выделения различных по физико-химической подвижности и потенциальной биологической доступности форм элементов [26, 27], являются насыщенными и обладают рядом преимуществ при изучении поведения НЧ в почвах. В МК, где образец почвы удерживается за счет мембранных фильтров (между которыми он находится), использование мембран с необходимым размером пор позволяет на выходе из микроколонки элюировать частицы определенного размерного диапазона. В ВСК образец почвы удерживается под действием центробежных сил в непрерывном потоке подвижной фазы, при этом варьирование скорости потока также позволяет добиться элюирования на выходе из колонки частиц необходимого размерного диапазона. Такая возможность регулирования размера вымываемых из колонки частиц позволяет учесть процессы гомо- и гетероагрегирования НЧ в почвах и таким образом оценить реальную подвижность именно НЧ, а не их агрегатов.
Цель настоящей работы – оценка поведения (подвижности и удерживания) синтетических НЧ CeO2 в почвах на основе изучения их динамического экстрагирования из почв в МК и ВСК, а также исследование влияния изменения поверхностных характеристик НЧ CeO2 (модификации лимонной кислотой) на их поведение в почвах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исследуемые образцы. Исследования проводили на примере образца типичного чернозема Курской области. Образец пахотного горизонта агрочернозема (0–10 см) пашни с традиционной обработкой был отобран в ходе полевых исследований в июне–июле 2017 г. на территории Курского научно-исследовательского института агропромышленного производства. Перед исследованиями образец почвы просеивали через сито с диаметром отверстий 1 мм.
В работе использовали наночастицы CeO2 (Sigma Aldrich) с сертифицированным размером <50 нм. Размерное распределение НЧ CeO2 дополнительно изучали методом лазерной дифракции (Shimadzu SALD-7500nano). Для модификации НЧ CeO2 использовали лимонную кислоту (Acros Organics).
На всех этапах настоящего исследования использовали деионированную воду с удельным сопротивлением 18.2 МОм см (Millipore).
Введение наночастиц CeO2 в почву. Наночастицы CeO2 добавляли в почву из расчета достижения их концентрации в почве 500 мкг/г, как наиболее часто используемой в исследованиях по применению НЧ CeO2 в качестве удобрения [19, 20, 22–24]. Готовили два образца смеси почвы с НЧ CeO2: с немодифицированными НЧ и НЧ, модифицированными ЛК. Наночастицы CeO2 модифицировали лимонной кислотой согласно методике [28]. Наночастицы CeO2 добавляли в почву в виде суспензий в воде и в 0.5 мМ растворе ЛК (pH 10). Щелочную среду раствора ЛК создавали добавлением 0.1 М раствора NaOH. Для приготовления суспензий брали навески по 7.5 мг CeO2 и приливали к ним 10 мл деионированной воды и раствора ЛК. Затем суспензии обрабатывали в ультразвуковой ванне (Bandelin DT 52) в течение 1 мин, после чего водную суспензию НЧ CeO2 сразу приливали к 15 г почвы. Суспензию НЧ CeO2 в ЛК оставляли на 1 ч для взаимодействия ЛК с поверхностью НЧ, после чего снова обрабатывали ультразвуком в течение 1 мин и приливали к 15 г почвы. Получившиеся в результате смешивания 10 мл суспензий НЧ с 15 г почвы грязеподобные смеси тщательно перемешивали шпателем, после чего оставляли до полного высыхания на 10 дней при комнатных температуре и влажности. Уплотнившиеся после высыхания образцы почв с НЧ аккуратно измельчали пестиком, после чего тщательно перемешивали.
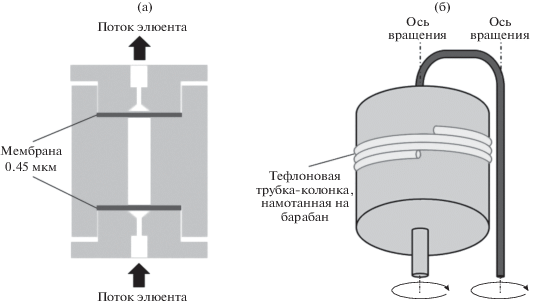
Изучение подвижности и степени удерживания наночастиц CeO2 в микроколонке и вращающейся спиральной колонке. Использовали тефлоновую МК (28 × 7 мм) объемом 1 мл, принципиальная схема которой изображена рис. 1. Соотношение диаметра и длины колонки 1 : 4 является оптимальным при исследовании почв [25]. Для удерживания образца почвы в МК использовали мембраны из смеси ацетатов целлюлозы со средним размером пор 0.45 мкм (Владипор). В ходе эксперимента навеску образца почвы массой 0.2 г помещали в МК, после чего через колонку начинали прокачивать элюент (деионированную воду). Колонка находилась в вертикальном положении, элюент подавали в направлении снизу-вверх для вытеснения воздуха из почвы и таким образом полного ее насыщения. Через колонку с помощью перистальтического насоса (Watson Marlow) прокачивали 100 мл элюента со скоростью 1 мл/мин, при этом на выходе из колонки отбирали каждые 10 мл элюата для последующего анализа методом масс-спектрометрии с индуктивно связанной плазмой (МС-ИСП). Затем из колонки извлекали почву, центрифугировали ее в течение 60 мин при 3500 об./мин, высушивали и анализировали методом МС-ИСП после разложения. Фильтры также анализировали методом МС-ИСП (после разложения).
Для изучения подвижности и степени удерживания НЧ CeO2 в ВСК использовали планетарную центрифугу, оснащенную тефлоновой вращающейся спиральной колонкой внутренним диаметром 1.6 мм и общим объемом 25 мл (Институт аналитического приборостроения РАН). Данное устройство детально описано в работе [29].
Подвижность и степень удерживания НЧ CeO2 в ВСК изучали в двух режимах: без мембраны и с мембраной 0.45 мкм на выходе из колонки. В ходе эксперимента навеску почвы массой 0.2 г диспергировали (однократным встряхиванием пробирки) в 5 мл деионированной воды, после чего суспензию вводили в ВСК с помощью перистальтического насоса. Далее колонку приводили во вращение (800 об./мин) и начинали прокачивать элюент (деионированную воду) со скоростью 1 мл/мин. На выходе из колонки отбирали каждые 10 мл элюата для последующего анализа методом МС-ИСП. Всего через колонку прокачивали 120 мл элюента, чтобы отобрать 100 мл элюата (с учетом свободного объема колонки 25 мл и за вычетом объема введенного образца 5 мл). Затем из колонки извлекали почву, центрифугировали ее в течение 60 мин при 3500 об./мин, высушивали и анализировали методом МС-ИСП после разложения.
В качестве контрольных опытов проводили описанные выше эксперименты с почвой без добавления НЧ CeO2.
Разложение фильтров и образцов почвы. Разложение фильтров проводили партиями, состоящими из анализируемых и контрольных образцов, с использованием системы автоклавного разложения с резистивным нагревом. Образцы помещали в тефлоновые реакционные емкости автоклавов и добавляли 0.5 мл конц. HNO3 и 1 мл HCl. Реакционные емкости закрывали крышками и герметизировали в титановых кожухах аналитических автоклавов. Автоклавы помещали в электронагреватель и выдерживали по 1 ч при 160, 180 и 200°С. После охлаждения автоклавы открывали, полученные растворы переносили в полиэтиленовые бюксы, добавляли 0.2 мл раствора, содержащего 10 мг/л In (внутренний стандарт при масс-спектральных измерениях), разбавляли водой до 10 мл. В качестве контрольных опытов описанные выше процедуры проводили в тефлоновых реакционных емкостях без образца. Конечные растворы использовали как контрольные.
Применяли кислотное разложение образцов почвы в открытой системе. Методика разложения подробно описана в работе [30].
Анализ элюатов и растворов, полученных после разложения. Отобранные пробы элюата анализировали методом МС-ИСП (Agilent 7900), где определяли Ce и Al. Элюаты анализировали непосредственно после отбора проб, чтобы избежать возможного осаждения частиц. В качестве внутреннего стандарта использовали Rh с концентрацией 10 мкг/л. Внутренний стандарт подавался в распылитель в режиме on-line вместе с анализируемыми растворами. Содержание Сe и Al определяли при следующих параметрах работы спектрометра: выходная мощность генератора 1550 Вт, микроконцентрический распылитель MicroMist, кварцевая охлаждаемая распылительная камера (2°С), расход плазмообразующего потока Ar 15 л/мин, расход потока Ar в распылителе 1.05 л/мин, скорость подачи анализируемого образца 1 мл/мин, разрешение 0.8 M.
Содержание Ce и Al в растворах после разложения определяли методами атомно-эмиссионной спектрометрии с индуктивно связанной плазмой (iCAP-6500 Duo, Thermo Scientific) и МС-ИСП (Х-7, Thermo Scientific). Параметры работы приборов описаны в работе [31].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Изучение динамики элюирования наночастиц CeO2 из почвы с использованием микроколонки и вращающейся спиральной колонки. На основе результатов анализа элюатов колонок построили кривые элюирования CeO2 (рис. 2). Концентрацию НЧ CeO2 в элюате рассчитывали относительно определенной концентрации Ce за вычетом вклада минеральных частиц в количество определенного Ce, рассчитанного из контрольных опытов. Как видно из рис. 2а, в МК уже после прокачивания 20 мл воды вымывание НЧ CeO2 сводится к минимуму, при этом абсолютное количество вымытых НЧ CeO2 значительно меньше (0.15 мкг), чем при использовании ВСК (рис. 2б). Помимо особенностей процессов взаимодействия твердой и жидкой фаз в ВСК и МК, это можно объяснить наличием мембраны 0.45 мкм на выходе из МК. Мембранная фильтрация – достаточно сложный процесс, эффективность которого зависит от множества параметров [32]. В данном случае забивание пор мембраны, вероятно, снижает эффективность фильтрации и сводит ее к минимуму на определенной стадии. При использовании мембраны 0.45 мкм на выходе из ВСК элюирование НЧ CeO2 продолжалось в ходе всего эксперимента, и количество вымытых частиц после прокачивания 100 мл воды оказалось в 6 раз выше (0.92 мкг), чем в МК. Данный факт можно объяснить следующими двумя явлениями:
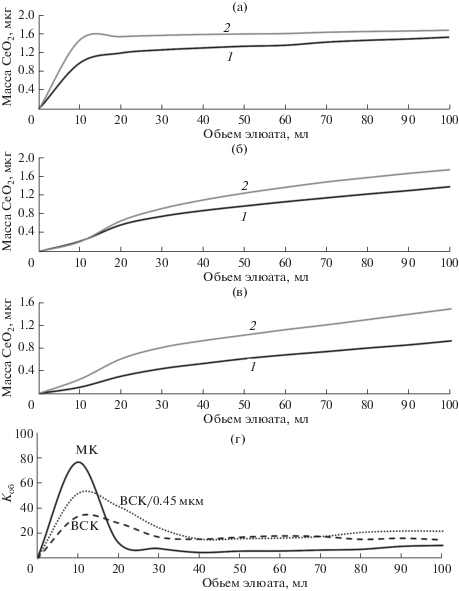
Рис. 2.
Дифференциальные (а) и интегральные (б) кривые элюирования наночастиц CeO2, а также коэффициенты обогащения элюатов колонок наночастицами CeO2 (относительно минеральных частиц почвы) при динамическом экстрагировании в микроколонке (1) и вращающейся спиральной колонке без мембраны (2) и с мембраной 0.45 мкм (3) (в).
1) в ВСК почва равномерно распределена тонким слоем вдоль стенки колонки, что упрощает переход НЧ в элюент и позволяет более эффективно вымывать НЧ из колонки по сравнению с набивной МК;
2) ВСК обладает бóльшим объемом (25 мл) по сравнению с МК (1 мл), что приводит к бóльшему разбавлению элюируемых частиц в ВСК и в свою очередь повышает эффективность мембранной фильтрации [32].
Вращающаяся спиральная колонка без мембраны на выходе показала наибольшую эффективность при элюировании НЧ CeO2 из почвы (рис. 2). После прокачивания 100 мл воды через почву в ВСК вымывается 1.37 мкг НЧ CeO2, что составляет 1.6% от введенных НЧ (рис. 2б), при этом элюирование частиц не прекращается.
Поскольку вместе с НЧ CeO2 элюируются и природные НЧ (почвенные НЧ минерального происхождения), при сравнении эффективности колонок важно оценить соотношение синтетических и природных НЧ в элюатах. Для этого рассчитали коэффициенты обогащения (Kоб) элюата церием по формуле:
Алюминий выбрали как референтный элемент, имеющий прямое отношение к минеральной составляющей элюата, поскольку основная часть почвенных коллоидных частиц представлена глинистыми минералами (алюмосиликатами). Рассчитанные значения Kоб показывают, во сколько раз элюат обогащен именно церием неприродного происхождения, т.е. добавленными НЧ CeO2. Динамика изменения Kоб элюатов различных колонок представлена на рис. 2в. Видно, что первые 10 мл элюата МК примерно в 2 раза больше обогащены НЧ CeO2, чем элюаты ВСК. При этом элюат ВСК с мембраной 0.45 мкм немного больше обогащен НЧ CeO2 по сравнению с ВСК без мембраны. Вызвано это, вероятно, уплотнением почвы в МК, что снижает транспорт минеральных частиц по сравнению с НЧ CeO2. Необходимо отметить, что подвижность частиц в почве в значительной степени обусловлена их поверхностными свойствами, которые влияют на взаимодействие с органическими и минеральными фазами. Процессы гетероагрегации играют основную роль в транспорте синтетических наночастиц. Однако в условиях настоящего исследования (изучение одного образца почвы и двух различных проточных систем) разница в транспорте частиц, очевидно, связана именно с условиями нахождения почвы в колонках. Почву в МК в некотором приближении можно рассматривать как инертную пористую матрицу, где объем порового пространства значительно меньше объема матрицы. В ВСК же, наоборот, колонку очень условно можно представить в виде большой поры, вдоль которой равномерно тонким слоем распределена почва, что обеспечивает большую площадь взаимодействия жидкой и твердой фаз, а также отсутствие пространственных ограничений для транспорта частиц. В данном случае в МК сферические НЧ CeO2 претерпевают меньше пространственных ограничений в транспорте через слой почвы, чем почвенные НЧ (прежде всего, глинистые минералы) неправильной (часто пластинчатой) формы. Кроме того, из рис. 2в видно, что в МК после прокачивания 70 мл воды Коб увеличивается с 20 до 30, что свидетельствует об уменьшении доли вымываемых минеральных частиц со временем.
Анализируя полученные результаты, можно отметить, что для ВСК (с мембраной и без нее) пик Ce (рис. 2а) приходится на 20 мл (что соответствует объему ВСК), при этом максимальное значение Kоб соответствует 10 мл элюата (рис. 2в). Для МК эти максимумы совпадают.
Проанализировали образцы почвы до и после динамического экстрагирования (табл. 1). Видно, что по результатам анализа остаточной фракции почвы (извлеченной из колонки после прокачивания элюента) невозможно корректно судить о степени удерживании НЧ CeO2 в колонке вследствие достаточно широких доверительных интервалов. Такая погрешность связана с неоднородностью смеси почвы и НЧ, а также недостаточной представительностью пробы (0.2 г). При этом результаты анализа почв все-таки подтверждают данные анализа элюатов, а именно обеспечение ВСК большего вымывания НЧ CeO2 по сравнению с МК. Анализ фильтров показал большее количество Ce на мембране МК, чем на ВСК/0.45 мкм, что, вероятно, связано с удерживанием части крупных агрегатов НЧ CeO2 в ВСК под действием центробежных сил. В МК при этом все агрегаты частиц, увлекаемые потоком, удерживаются на мембране. Необходимо отметить, что Kоб частиц на мембране МК примерно в два раза выше, чем на мембране ВСК, что также продемонстрировано для элюатов колонок (рис. 2в) и подтверждает предположение о влиянии уплотнения почвы и соотношения жидкой и твердой фаз в колонке на транспорт частиц различной формы.
Таблица 1.
Содержание (мкг) церия в почве и мембранных фильтрах после динамического экстрагирования (n = 4, P = 0.95)
| Образец | Исходная почва | Почва, извлеченная из колонки | Ретентат мембраны 0.45 мкм | Kоб | |||
|---|---|---|---|---|---|---|---|
| МК | ВСК | МК | ВСК/ 0.45 мкм | МК | ВСК/ 0.45 мкм | ||
| Почва + НЧ CeO2 | 82 | 84 ± 8 | 78 ± 14 | 0.5 ± 0.2 | 0.17 ± 0.05 | 16 | 7 |
| Почва + НЧ CeO2/ЛК | 86 | 76 ± 6 | 75 ± 7 | 0.5 ± 0.2 | 0.16 ± 0.04 | 12 | 4 |
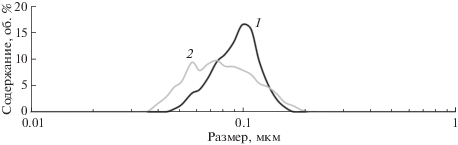
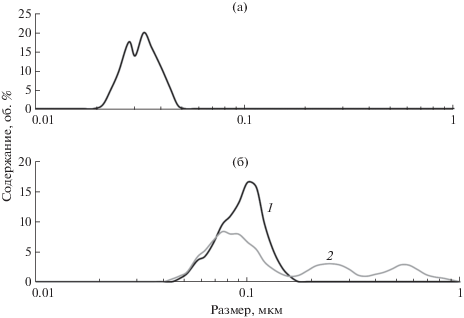
Размерное распределение частиц в элюатах колонок, а также в исходном образце CeO2 охарактеризовано методом лазерной дифракции (рис. 3). Согласно данным светорассеяния средний размер НЧ CeO2 равен 32 нм (рис. 3а). Изучение размерного распределения частиц в элюатах колонок (рис. 3б) показало, что в ВСК на выходе вымываются частицы размером до 1 мкм с преобладающим пиком (50%) в нанодиапазоне (<100 нм). Частицы в элюатах МК и ВСК/0.45 мкм имели одинаковое размерное распределение с медианой 91 нм (66% частиц имеют размер <100 нм). Таким образом, применение мембраны на выходе из колонки позволяет убрать крупные субмикронные гомо- и гетероагрегаты НЧ CeO2, что важно при оценке подвижности в окружающей среде именно тех НЧ, которые заслуживают особого внимания вследствие своих токсических свойств.
Рис. 3.
Размерное распределение исходного образца наночастиц CeO2 (а) и частиц в элюатах микроколонки (1) и вращающейся спиральной колонки (2) (б).
Сравнивая результаты, полученные в МК и ВСК, можно сделать вывод, что ВСК (за счет принципа удерживания почвы в колонке) позволяет оценить максимальную подвижность НЧ в почвах, достигаемую в условиях, при которых нивелируется влияние уплотнения почвы в колонке (плотности почвенного слоя) на подвижность НЧ, т.е. когда почвенные частицы свободно омываются элюентом и при этом нет пространственных ограничений для их элюирования.
Набивная МК, где через почвенный столб прокачивается элюент, лучше всего моделирует условия, реально имеющие место в почве, так как сохраняется структура почвенной колонки с соответствующими пространственными ограничениями для транспорта НЧ. При этом важным остается вопрос об эффективности действия мембраны на выходе из МК. Показано, например, что применение мембран в пробоподготовке при изучении НЧ в окружающей среде может приводить к заниженной оценке их реального количества вследствие ряда нежелательных процессов в ходе фильтрации [33], однако мембраны 0.45 мкм наиболее часто применяют при исследованиях в данной области; они являются неким стандартом для выделения самой тонкодисперсной фракции (НЧ) из полидисперсных образцов окружающей среды.
В настоящем исследовании меньшее абсолютное количество НЧ CeO2 на выходе из МК и ВСК/0.45 мкм частично можно объяснить удерживанием их гомо- и гетероагрегатов мембраной на выходе. С точки зрения исследований подвижности НЧ в окружающей среде это является преимуществом, поскольку агрегаты НЧ не настолько токсичны, как сами НЧ. При этом набивная МК позволяет изучать подвижность НЧ в почве, принимая во внимание ее структуру, а ВСК/0.45 – максимальную подвижность в почве.
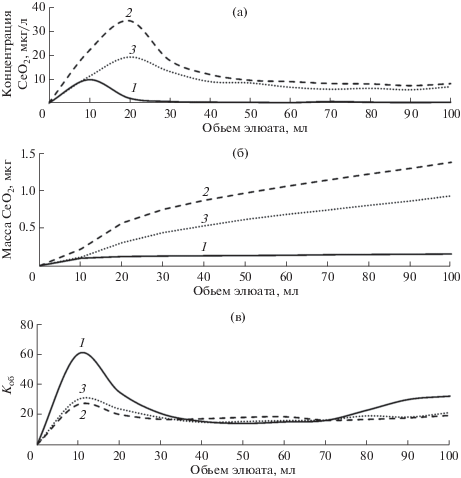
Влияние модификации поверхности наночастиц CeO2 лимонной кислотой на их подвижность в почве. Проведено сравнение подвижности НЧ CeO2 и CeO2/ЛК в почве. На рис. 4 изображены интегральные кривые элюирования НЧ, полученные с использованием разных колонок. Показано, что модификация поверхности НЧ CeO2 лимонной кислотой приводит к увеличению их подвижности, что также подтверждается результатами анализа почв (табл. 1). Коэффициенты обогащения элюатов колонок НЧ CeO2/ЛК также увеличиваются по сравнению с НЧ CeO2 (рис. 4г), что также свидетельствует об увеличении подвижности модифицированных НЧ в почве. Кроме того, модификация поверхности НЧ CeO2 лимонной кислотой приводит к уменьшению среднего размера частиц в элюате колонок (рис. 5).
* * *
Изучены особенности поведения НЧ CeO2, используемого в качестве наноудобрения, в типичной почве сельскохозяйственного назначения (черноземе) с использованием МК и ВСК. Показано, что ВСК позволяет оценить максимальную подвижность НЧ в почве за счет нивелирования влияния упаковки почвы в колонке на транспорт частиц. В свою очередь, МК за счет сохранения почвенный структуры позволяет наиболее корректно оценить подвижность НЧ в реальном почвенном столбе. Показано также, что элюат МК в большей степени обогащен НЧ CeO2 по сравнению с ВСК, что, вероятно, связано с влиянием пространственных ограничений на транспорт НЧ CeO2 и минеральных НЧ через слой почвы. В МК за счет упаковки почвы в колонке снижается транспорт минеральных частиц неправильной (часто пластинчатой) формы по сравнению со сферическими НЧ CeO2. Изучено влияние модификации поверхности НЧ CeO2 лимонной кислотой на их подвижность в почве. Показано, что НЧ CeO2/ЛК обладают большей подвижностью в почве по сравнению с немодифицированными НЧ.
Исследование выполнено за счет гранта Российского научного фонда (проект № 17-73-10338). Авторы благодарны Ольге Борисовне Роговой (Почвенный институт им. В.В. Докучаева, Москва) за предоставление образца почвы.
Список литературы
Tjong S.C. Recent progress in the development and properties of novel metal matrix nanocomposites reinforced with carbon nanotubes and graphene nanosheets // Mat. Sci. Eng. R. Rep. 2013. V. 74. № 10. P. 281
Zhang L., Gu F.X., Chan, J.M., Wang A.Z., Langer R.S., Farokhzad O.C. Nanoparticles in medicine: Therapeutic Applications and developments // Clin. Pharmacol. Ther. 2008. V. 83. № 5. P. 761.
Sanvicens N., Marco M.P. Multifunctional nanoparticles – properties and prospects for their use in human medicine // Trends Biotechnol. 2008. V. 26. № 8. P. 425.
Kokura S., Handa O., Takagi T., Ishikawa T., Naito Y., Yoshikawa T. Silver nanoparticles as a safe preservative for use in cosmetics // Nanomedicine. 2010. V. 6. № 4. P. 570.
Pardeike J., Hommoss A., Muller R.H. Lipid nanoparticles (SLN, NLC) in cosmetic and pharmaceutical dermal products // Int. J. Pharm. 2009. V. 366. № 1–2. P. 170.
Штыков С.Н. Проблемы аналитической химии. Т. 20. Нанообъекты и нанотехнологии в химическом анализе. М.: Наука, 2015. С. 430.
Nowack B., Bucheli T.D. Occurrence, behavior and effects of nanoparticles in the environment // Environ. Pollut. 2007. V. 150. № 1. P. 5.
Biswas P., Wu C.Y. 2005 critical review: Nanoparticles and the environment // J. Air Waste Manage. Assoc. 2005. V. 55. № 6. P. 708.
Buzea C., Pacheco I.I., Robbie K. Nanomaterials and nanoparticles: Sources and toxicity // Biointerphases. 2007. V. 2. № 4. P. MR17.
Soenen S.J., Rivera-Gil P., Montenegro J.M., Parak W.J., De Smedt S.C., Braeckmans K. Cellular toxicity of inorganic nanoparticles: Common aspects and guidelines for improved nanotoxicity evaluation // Nano Today. 2011. V. 6. № 5. P. 446.
Srivastava V., Gusain D., Sharma Y.C. Critical review on the toxicity of some widely used engineered nanoparticles // Ind. Eng. Chem. Res. 2015. V. 54. № 24. P. 6209.
Sharma V.K., Filip J., Zboril R., Varma R.S. Natural inorganic nanoparticles – formation, fate, and toxicity in the environment // Chem. Soc. Rev. 2015. V. 44. № 23. P. 8410.
Peijnenburg W., Praetorius A., Scott-Fordsmand J., Cornelis G. Fate assessment of engineered nanoparticles in solids dominated media – Current insights and the way forward // Environ. Pollut. 2016. V. 218. P. 1365.
Batley G.E., Kirby J.K., McLaughlin M.J. Fate and risks of nanomaterials in aquatic and terrestrial environments // Acc. Chem. Res. 2013. V. 46. № 3. P. 854.
Chhipa H. Nanofertilizers and nanopesticides for agriculture // Environ. Chem. Lett. 2017. V. 15. № 1. P. 15.
Kah M. Nanopesticides and nanofertilizers: emerging contaminants or opportunities for risk mitigation // Front. Chem. 2015. V. 3. P. 64.
Liu R., Lal R. Potentials of engineered nanoparticles as fertilizers for increasing agronomic productions // Sci. Total Environ. 2015. V. 514. P. 131.
Keller A.A., Lazareva A. Predicted releases of engineered nanomaterials: from global to regional to local // Environ. Sci. Technol. Lett. 2014. V. 1. № 1. P. 65.
Rico C.M., Lee S.C., RubeneciaR., Mukherjee A., Hong J., Peralta-Videa J.R., Gardea-Torresdey J.L. Cerium oxide nanoparticles impact yield and modify nutritional parameters in wheat (Triticum aestivum L.) // J. Agric. Food Chem. 2014. V. 62. № 40. P. 9669.
Rico C.M., Barrios A.C., Tan W., Rubenecia R., Lee S.C., Varela-Ramirez A., Peralta-Videa J.R., Gardea-Torresdey J.L. Physiological and biochemical response of soilgrown barley (Hordeum vulgare L.) to cerium oxide nanoparticles // Environ. Sci. Pollut. Res. 2015. V. 22. P. 10551.
Zhao L., Peng B., Hernandez-Viezcas J.A., Rico C., Sun Y., Peralta-Videa J.R., Tang X., Niu G., Jin L., Varela A., Zhang J., Gardea-Torresdey J.L. Stress response and tolerance of Zea mays to CeO2 nanoparticles: cross talk among H2O2, heat shock protein, and lipid peroxidation // ACS Nano. 2012. V. 6. P. 9615.
Rico C.M., Hong J., Morales M.I., Zhao L., Barrios A.C., Zhang J., Peralta-Videa J.R., Gardea-Torresdey J.L. Effect of cerium oxide nanoparticles on rice: a study involving the antioxidant defense system and in vivo fluorescence imaging // Environ. Sci. Technol. 2013. V. 47. P. 5635.
Barrios A.C., Rico C.M., Trujillo-Reyes J., Medina-Velo I.A., Peralta-Videa J.R., Gardea-Torresdey J.L. Effects of uncoated and citric acid coated cerium oxide nanoparticles, bulk cerium oxide, cerium acetate, and citric acid on tomato plants // Sci. Total Environ. 2016. V. 563–564. P. 956.
Trujillo-Reyes J., Vilchis-Nestor A.R., Majumdar S., Peralta-Videa J.R., Gardea-Torresdey J.L. Citric acid modifies surface properties of commercial CeO2 nanoparticles reducing their toxicity and cerium uptake in radish (Raphanus sativus) seedlings // J. Hazard. Mater. 2013. V. 263. Pt. 2. P. 677.
Lewis J., Sjöstrom J. Optimizing the experimental design of soil columns in saturated and unsaturated transport experiments // J. Contam. Hydrol. 2010. V. 115. P. 1.
Федотов П.С., Савонина Е.Ю., Спиваков Б.Я., Веннрих Р. Возможности гармонизации методов динамического фракционирования форм элементов в почвах и донных отложениях // Журн. аналит. химии. 2012. Т. 67. № 10. С. 948. (Fedotov P.S., Savonina E.Yu., Spivakov B.Ya., Wennrich R. Possibilities for the harmonization of methods of the dynamic fractionation of elements in soils and bottom sediments // J. Analyt. Chem. 2012. V. 67. № 10. P. 851.)
Rosende M., Savonina E.Yu., Fedotov P.S., Miro M., Cerda V., Wennrich R. Dynamic fractionation of trace metals in soil and sediment samples using rotating coiled column extraction and sequential injection microcolumn extraction: A comparative study // Talanta. 2009. V. 79. № 4. P. 1081.
Cornelis G., Ryan B., McLaughlin M.J., Kirby J.K., Beak D., Chittleborough D. Solubility and batch retention of CeO2 nanoparticles in soils // Environ. Sci. Technol. 2011. V. 45. № 7. P. 2777.
Fedotov P.S., Ermolin M.S., Katasonova O.N. Field-flow fractionation of nano- and microparticles in rotating coiled columns // J. Chromatogr. A. 2015. V. 1381. P. 202.
Карандашев В.К., Хвостиков В.А., Носенко С.Ю., Бурмий Ж.П. Использование высокообогащенных стабильных изотопов в массовом анализе образцов горных пород, грунтов, почв и донных отложений методом масс-спектрометрии с индуктивно-связанной плазмой // Заводск. лаборатория. Диагностика материалов. 2016. Т. 82. № 7. С. 6.
Ермолин М.С., Федотов П.С., Иванеев А.И., Карандашев В.К., Федюнина Н.Н., Еськина В.В. Выделение и количественный анализ наночастиц дорожной пыли // Журн. аналит. химии. 2017. Т. 72. № 5. С. 448. (Ermolin M.S., Fedotov P.S., Ivaneev A.I., Karandashev V.K., Fedyunina N.N., Eskina V.V. Isolation and quantitative analysis of road dust nanoparticles // J. Analyt. Chem. 2017. V. 72. № 5. P. 520.)
Fedotov P.S., Vanifatova N.G., Shkinev V.M., Spivakov B.Ya. Fractionation and characterization of nano- and microparticles in liquid media // Anal. Bioanal. Chem. 2011. V. 400. P. 1787.
Gimbert L.J., Haygarth P.M., Beckett R., Worsfold P.J. The influence of sample preparation on observed particle size distributions for contrasting soil suspensions using flow field flow fractionation // Environ. Chem. 2006. V. 3. P. 184.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии