Биотехнология, 2022, T. 38, № 5, стр. 73-79
Роль ингибитора апоптоза xiap в устойчивости клеток глиобластомы к действию рекомбинантного вируса осповакцины VV-GMCSF-Lact
Н. С. Васильева 1, 2, *, А. Б. Агеенко 1, О. А. Чинак 1, В. А. Рихтер 1, Е. В. Кулигина 1, 2
1 Институт химической биологии и фундаментальной медицины
Сибирского отделения Российской академии наук
630090 Новосибирск, Россия
2 Общество с ограниченной ответственностью “Онкостар”
630090 Новосибирск, Россия
* E-mail: nataly_vas@bk.ru
Поступила в редакцию 28.07.2022
После доработки 10.08.2022
Принята к публикации 23.08.2022
- EDN: SDHCHS
- DOI: 10.56304/S0234275822050155
Аннотация
Исследование механизмов резистентности глиобластомы важно для разработки эффективных препаратов для лечения этого онкологического заболевания. Вопрос о формировании устойчивости глиобластомы к онколитическим вирусам остается открытым. При глиобластоме ингибитор апоптоза XIAP в большинстве случаев высокоэкспрессирован и участвует в формировании лекарственной резистентности опухоли, наряду с другими нарушениями в каскадах программируемой клеточной гибели. Нами показано, что гибель клеток глиобластомы под действием рекомбинантного вируса осповакцины VV-GMCSF-Lact происходит преимущественно по апоптотическому пути. Однако в клетках, более устойчивых к VV-GMCSF-Lact, активация путей клеточной гибели происходит на более поздних стадиях развития вирусной инфекции. Кроме того, общий уровень белка XIAP повышен в клетках культур, устойчивых к действию вируса.
На сегодняшний день одним из наиболее перспективных подходов к лечению опухолей считается виротерапия – иммунотерапевтический метод, основанный на опосредованной вирусом гибели опухолевых клеток и индукции иммунного ответа организма [1]. В настоящее время множество онколитических вирусов проходит клинические испытания в качестве потенциальных агентов для лечения опухолей головного мозга, в том числе глиобластомы – одной из наиболее агрессивных опухолей центральной нервной системы (ЦНС). Однако пока ни один препарат не одобрен для применения в клинике. Самая большая проблема в лечении глиобластомы состоит в развитии лекарственной резистентности опухоли; при этом вопрос о формировании устойчивости к онколитическим вирусам остается открытым.
Коллективом авторов ИХБФМ СО РАН и Государственного научного центра вирусологии и биотехнологии “Вектор” (Россия) разработан рекомбинантный штамм VV-GMCSF-Lact вируса осповакцины, который содержит делеции фрагментов в генах вирусных белков: тимидинкиназы и фактора роста; в эти области встроены гены гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) человека и апоптозиндуцирующего белка лактаптина соответственно [2]. Ранее нами показано, что штамм VV-GMCSF-Lact обладает цитотоксической активностью in vitro и противоопухолевой эффективностью in vivo в отношении клеток иммортализованных и персонализированных культур клеток глиобластомы человека [3]; при этом чувствительность различных культур к действию вируса неодинакова.
Известно, что опухолевые клетки, в частности клетки глиобластомы, характеризуются нарушениями сигнальных каскадов клеточной гибели, что может в той или иной степени опосредовать эффективность терапии с помощью онколитического вируса VV-GMCSF-Lact. Изучение механизмов, определяющих устойчивость опухолевых клеток к действию онколитического вируса, позволит разработать эффективные стратегии лечения с применением соответствующих препаратов для комбинированной терапии.
Цель исследования – анализ путей гибели клеток иммортализованных и персонализированных культур глиобластомы, обладающих различной чувствительностью к VV-GMCSF-Lact, под действием вируса.
УСЛОВИЯ ЭКСПЕРИМЕНТА
Вирусный препарат
Рекомбинантный вирус осповакцины VV‑GMCSF-Lact любезно предоставлен Г.В. Кочневой (ГНЦ ВБ “Вектор” Роспотребнадзора, Новосибирская область, Россия).
Культивирование иммортализованных культур клеток U87 MG и U343 MG
Клетки иммортализованных культур U87 MG и U343 MG глиобластомы человека (Коллекция культур клеток ИХБФМ СО РАН, Новосибирск) культивировали в среде Alpha-MEM с добавлением 10% эмбриональной сыворотки крупного рогатого скота (FBS), 2 мM L-глютамина (GlutaMAX) и раствора антибиотика-антимикотика (100 ед/мл пенициллина, 100 мг/мл стрептомицина сульфата, 0.25 мкг/мл амфотерицина).
Культивирование персонализированных культур клеток BR1.20 и BR3.20
Клетки персонализированных культур BR1.20 и BR3.20 глиобластомы человека (Коллекция культур клеток ИХБФМ СО РАН) культивировали в среде IMDM с добавлением 10% FBS, 4 мM L-глютамина (GlutaMAX) и раствора антибиотика-антимикотика (100 ед/мл пенициллина, 100 мг/мл стрептомицина сульфата, 0.25 мкг/мл амфотерицина) и 5 мкл MITO + SERUM EXTENDED (SACCO system, Италия).
Анализ апоптоза в клетках глиобластомы человека под действием VV-GMCSF-Lact
В лунки 12-луночных планшетов, содержащих по 2 × 105 клеток/лунка, вносили препарат VV-GMCSF-Lact с множественностью инфекции 1 бляшкообразующая единица (БОЕ) на клетку. Клетки в присутствии вирусного препарата инкубировали при 37°С 24 ч и анализировали методом проточной цитометрии. Апоптотические клетки идентифицировали на проточном цитометре FACSCantoII с использованием коммерческого набора FITC Annexin V Apoptosis Detection kit I и программного обеспечения FACSDiva (BD Biosciences, США).
Коиммунопреципитация
В лунки 6-луночных планшетов, содержащих по 106 клеток/лунка, вносили препарат VV-GMCSF-Lact с множественностью инфекции 1 БОЕ/клетка. Клетки инкубировали при 37°С в течение 12, 24, 36, 48 и 72 ч. В качестве контроля использовали клетки, культивируемые в ростовой среде без добавления вируса. Клетки лизировали в буфере RIPA (1% NP-40, 150 мM NaCl, 0.1% SDS, 50 мM Трис-HCl, pH 7.4) в присутствии ингибиторов протеаз и фосфатаз. Коиммунопреципитацию проводили с использованием агарозных частиц Protein A/G PLUS-Agarose (Santa Cruz Biotechnology, Inc., США) и антител к каспазе-8 (Invitrogen, США) или XIAP (Invitrogen). Полученные иммунопреципитаты использовали для дальнейшего анализа.
Иммуноблотинг
Электрофоретическое разделение белков проводили в денатурирующем 10%-ном ПААГ (SDS-PAAG) с использованием камеры для вертикального электрофореза. Для переноса белков с геля на нитроцеллюлозную мембрану (0.45 мкм) использовали камеру для электропереноса (Bio-Rad, США) с использованием буфера NuPAGE Transfer Buffer (Thermo Fisher Scientific, США).
Мембраны помещали в прибор IBind Western Device (Thermo Fisher Scientific) и инкубировали сначала с антителами, специфичными к исследуемым белкам: каспазе-8, RIPK1, RIPK3, XIAP и SMAC, ‒ а затем со вторичными антителами. В качестве первичных антител использовали поликлональные кроличьи антитела к RIPK1, RIPK3, каспазе-8 и XIAP, моноклональные кроличьи антитела к SMAC (все производства Invitrogen). В качестве вторичных антител использовали конъюгированные с пероксидазой хрена (HRP) поликлональные антитела козы против IgG кролика и поликлональные антитела козы против IgG мыши соответственно. Все антитела – производства Invitrogen. После промывки мембран проводили детекцию белков с использованием набора реагентов Novex® ECL Chemiluminescent Substrate Reagent kit (Invitrogen) и системы для хемилюминесцентной детекции Amersham™ Imager 600 (GE Healthcare Life Sciences, США). Для нормирования полученных данных использовали моноклональные кроличьии антитела к β-актину (Invitrogen). Результаты иммуноблотинга анализировали в программе GelAnalyzer.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Анализ апоптоза в клетках глиобластомы человека под действием VV-GMCSF-Lact
Клетки иммортализованных (U87 MG и U343 MG) и персонализированных (BR1.20 и BR3.20) культур глиобластомы человека, обладающие различной чувствительностью к VV-GMCSF-Lact (табл. 1), инкубировали с онколитическим вирусом (MOI = 1 БОЕ/клетка) в течение 24 ч. Для исследования апоптотических процессов использовали проточную цитометрию с двойным окрашиванием: аннексином V и йодидом пропидия. Этот метод позволяет дифференцировать популяции живых и погибших клеток, а также клеток, находящихся на ранних стадиях апоптоза, и количественно определить их содержание [4].
Таблица 1.
Цитотоксическая активность VV-GMCSF-Lact в отношении клеток глиомы Table 1. Cytotoxic activity of VV-GMCSF-Lact for glioma cells
| Культура клеток | IC50*, БОЕ/клетка |
|---|---|
| U87 MG | 0.1 |
| U343 MG | 0.06 |
| BR1.20 | 0.006 |
| BR3.20 | 0.02 |
Согласно полученным данным (рис. 1), доля погибших клеток и находящихся на ранних стадиях апоптоза тем больше, чем чувствительнее культура глиомы к действию VV-GMCSF-Lact (см. табл. 1).
Рис. 1.
Анализ апоптотических процессов в клетках иммортализованных и персонализированных культур глиобластомы человека, вызванных онколитическим вирусом VV-GMCSF-Lact. Проточная цитометрия: Q2 – погибшие клетки; Q3 – клетки, находящиеся на ранних стадиях апоптоза; Q4 – живые клетки. Окрашивание Аннексином V (ось Х) и йодидом пропидия (ось Y). Fig. 1. Analysis of apoptotic processes in cells of immortalized and patient-derived human glioblastoma cultures exposed to the oncolytic virus VV-GMCSF-Lact. Flow cytometry: Q2 – dead cells; Q3 – cells at early stages of apoptosis; Q4 – living cells. Staining with Annexin V (X-axis) and propidium iodide (Y-axis).

Известно, что кроме прямого лизиса клеток, инфицированных поксвирусами, к которым относится вирус осповакцины, гибель опухолевых клеток может проходить как по пути некроптоза [5, 6], так и апоптоза [7, 8]. Ранее Bidgood & Mercer [9] показали, что лизис клеток под действием вируса осповакцины наступает через 72 ч после инфицирования, а наблюдаемая нами гибель клеток глиобластомы уже в первые сутки инкубации с VV-GMCSF-Lact может быть следствием активации программируемых путей клеточной гибели: апоптоза и некроптоза. Кроме того, ранее показано, что при воздействии VV-GMCSF-Lact на клетки трижды негативного рака молочной железы MDA-MB-231 популяция апоптотических клеток была больше, чем в клетках, инкубированных с рекомбинантным штаммом VV-GMCSF-dGF, который не экспрессировал лактаптин [2]. Как видно из данных, приведенных на рис. 1, в исследованных нами культурах превалируют клетки, позитивные только по Аннексину V (Q3), из чего можно сделать вывод о преобладании апоптотического пути гибели клеток глиобластомы под действием VV-GMCSF-Lact.
Экспрессия белков, участвующих в процессах клеточной гибели под действием VV-GMCSF-Lact
Как было отмечено ранее, вирус осповакцины может активировать различные пути клеточной гибели. Некроптоз представляет собой регулируемый некроз, опосредованный белками RIPK1 и RIPK3. RIPK1, как активатор RIPK3, будучи расщеплен каспазой-8, индуцирует ингибирование некроптоза [10–12]. Так, Nailwal & Chan сообщали [13], что инфицированные вирусом осповакцины RIPK1/3-дефицитные клетки устойчивы к некроптозу.
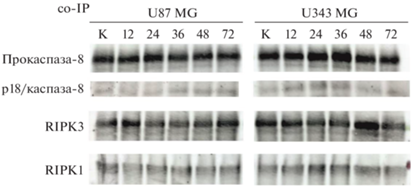
В клетках иммортализованных культур U87 MG и U343 MG и персонализированных культур BR1.20 и BR3.20 нами исследованы уровни белков RIPK1 и RIPK3, соосажденных в комплексе с каспазой-8, на разных временных интервалах инкубации клеток с VV-GMCSF-Lact. Используя технологию коиммунопреципитации и последующий анализ методом иммуноблотинга, мы обнаружили, что при обработке вирусом VV-GMCSF-Lact уровень активированной каспазы-8 в клетках U343 MG, более чувствительных к действию вируса по сравнению с U87 MG, повышался через 12 ч и снижался через 48 ч инкубации, в то время как уровень белка RIPK3, наоборот, снижался через 12 ч и возрастал к 48 ч (рис. 2). Известно, что активная каспаза-8 ингибирует некроптоз, расщепляя не только RIPK1 и RIPK3, но и CYLD [14], и c-FLIP [15], и запускает апоптотический сигналинг в клетке [16, 17]. Таким образом, снижение уровня RIPK3 может свидетельствовать о начальной стадии активации апоптоза, а его повышение – о последующей индукции некроптоза. Также в клетках U343 MG, в точках 24 и 36 ч, наблюдали повышение уровня RIPK1. В клетках U87 MG уровень каспазы-8 увеличивался только к 36 ч инкубации с вирусом, а к 72 ч повышался и уровень RIPK3, что может свидетельствовать о поздней активации сигнальных путей клеточной гибели в культуре, более устойчивой к действию онколитического вируса.
Рис. 2.
Динамика изменений уровней белков RIPK1 и RIPK3, копреципитированных (co-IP) с каспазой-8, в клетках иммортализованных культур глиобластомы человека, обработанных VV-GMCSF-Lact. Иммуноблотинг: K – лизаты контрольных клеток (не обработанных вирусом); цифрами указано время (ч) инкубации клеток с VV-GMCSF-Lact. Fig. 2. Dynamics of changes in the levels of RIPK1 and RIPK3 proteins, co-precipitated (co-IP) with caspase-8, in cells of immortalized human glioblastoma cultures treated with VV-GMCSF-Lact. Immunoblotting: K – lysates of control cells (not treated with the virus); the numbers indicate the time (h) of cell incubation with VV-GMCSF-Lact.
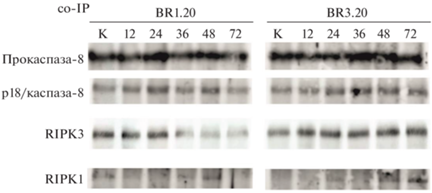
В клетках культуры BR1.20, более чувствительной к действию VV-GMCSF-Lact по сравнению с культурой BR3.20, уровень активированной каспазы-8 повышался к 24 и 48 ч инкубации с вирусом, в то же время уровень белка RIPK3 снижался к 36 ч, из чего можно сделать вывод о подавлении некроптической гибели клеток и активации апоптоза в них (рис. 3). Уровень белка RIPK1 не изменялся на протяжении всего времени инкубации с вирусом, лишь незначительно повышался в культуре BR1.20 к 48 ч и в культуре BR3.20 к 24 ч.
Рис. 3.
Динамика изменений уровней белков RIPK1 и RIPK3, копреципитированных (co-IP) с каспазой-8, в клетках персонализированных культур глиобластомы человека, обработанных VV-GMCSF-Lact. Иммуноблотинг: K – лизаты контрольных клеток (не обработанных вирусом); цифрами указано время (ч) инкубации клеток с VV-GMCSF-Lact. Fig. 3. Dynamics of changes in the levels of RIPK1 and RIPK3 proteins, co-precipitated (co-IP) with caspase-8, in cells of patient-derived human glioblastoma cultures treated with VV-GMCSF-Lact. Immunoblotting: K – lysates of control cells (not treated with the virus); the numbers indicate the time (h) of cell incubation with VV-GMCSF-Lact.
На основании полученных результатов можно говорить о том, что с увеличением времени инкубации клеток глиобластомы с VV-GMCSF-Lact повышается уровень активированной каспазы-8; при этом в клетках, более чувствительных к VV-GMCSF-Lact, активация фермента происходит уже через 24 ч инкубации. Снижение уровня RIPK1 и RIPK3 при повышении уровня каспазы-8 позволяет предположить, что VV-GMCSF-Lact активирует в клетках глиобластомы рецепторопосредованный путь апоптотической гибели; при этом в более устойчивых к действию вируса клетках активация как некроптоза, так и апоптоза, происходит на более поздних стадиях инфицирования.
Экспрессируемый VV-GMCSF-Lact лактаптин, протеолитический фрагмент каппа-казеина молока человека, как показано ранее [18, 19], индуцирует апоптоз опухолевых клеток по митохондриальному пути, что приводит к активации каспазы-3 и каспазы-7. Однако в клетках глиобластомы часто детектируют высокий уровень белка XIAP, ингибирующего эти каспазы [20]. Также на эффективность активации апоптоза, индуцируемого лактаптином, может влиять представленность в опухолевых клетках белка SMAC, который в нормальном состоянии находится в межмембранном пространстве митохондрий. При активации апоптоза по митохондриальному пути и увеличении проницаемости мембран митохондрий SMAC покидает митохондрии и участвует в связывании белков-ингибиторов каспаз, таких как XIAP [21].
Используя технологию коиммуноприципитации и последующий иммуноблотинг, мы проанализировали изменение уровня белка SMAC в комплексе с XIAP в клетках иммортализованных культур U87 MG и U343 MG и персонализированных культур BR1.20 и BR3.20 глиобластомы человека до и после воздействия VV-GMCSF-Lact.
Согласно полученным данным, уровень белка XIAP был выше в клетках U87 MG, более устойчивых к действию VV-GMCSF-Lact по сравнению с U343 MG. Уровень белка SMAC в комплексе с XIAP при этом был ниже, хотя повышался через 24 ч инкубации с вирусом (рис. 4а). В клетках U343 MG уровень SMAC, напротив, снижался через 24 ч, из чего можно сделать вывод об ингибировании апоптоза в процессе вирусной инфекции. Вирус осповакцины несет гены, кодирующие белки-гомологи Bcl-2, способные ингибировать апоптоз путем связывания Bax и Bak [22, 23]. Bax и Bak, согласно литературным данным, участвуют в повышении проницаемости митохондриальной мембраны и опосредуют выход в цитоплазму таких молекул, как SMAC, HtrA2 и цитохром с [24, 25]. Согласно полученным нами данным, несмотря на снижение уровня белка SMAC в клетках U343 MG при их инфицировании вирусом VV-GMCSF-Lact, доля клеток, находящихся на ранних стадиях апоптоза, в этой культуре была выше чем в U87 MG (рис. 1).
Рис. 4.
Анализ динамики изменений уровня белка SMAC в комплексе с XIAP в клетках иммортализованных культур U87 MG и U343 MG (а) и персонализированных культур BR1.20 и BR3.20 (b) глиобластомы человека. Иммуноблотинг: K – лизаты контрольных клеток; цифрами указано время (ч) инкубации клеток с VV-GMCSF-Lact. Fig. 4. Analysis of the dynamics of changes in the level of SMAC protein in a complex with XIAP in cells of immortalized cultures U87 MG and U343 MG (a) and patient-derived cultures BR1.20 and BR3.20 (b) of human glioblastoma. Immunoblotting: K – control cell lysates; the numbers indicate the time (h) of cell incubation with VV-GMCSF-Lact.
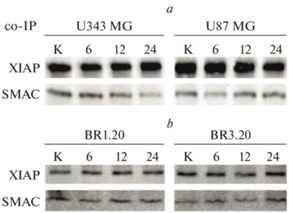
В клетках BR3.20, более устойчивых к действию VV-GMCSF-Lact по сравнению с BR1.20, уровень XIAP также был выше, а уровень SMAC повышался через 24 ч инкубации с вирусом (рис. 4b). Заметим, что уровень SMAC в комплексе с XIAP не снижался в клетках BR1.20, характеризующихся высокой чувствительностью к VV-GMCSF-Lact, что может свидетельствовать об эффективном прохождении апоптоза по митохондриальному пути.
В результате проведенного исследования нами продемонстрировано, что гибель клеток глиобластомы под действием VV-GMCSF-Lact протекает преимущественно по апоптотическому пути. И это очень важный и обнадеживающий факт с практической точки зрения, так как развитие воспалительных реакций при некрозе опухолевых клеток головного мозга относится к нежелательным процессам. Однако в культурах с повышенной устойчивостью к VV-GMCSF-Lact активация путей клеточной гибели происходит позже и менее эффективно, чем в чувствительных культурах, что может быть связано с нарушениями апоптотического сценария. В пользу этого предположения свидетельствует и повышенный уровень ингибирующего апоптоз белка XIAP в этих клетках. Уже замечено, что высокая экспрессия XIAP при глиобластоме коррелирует с низкой выживаемостью пациентов [20, 26]. Недавно в клетках глиобластомы с повышенной устойчивостью к VV-GMCSF-Lact нами зарегистрирован высокий уровень активированной киназы Akt1 [27]. А ранее сообщалось о взаимосвязи между активацией Akt1 и высокой экспрессией XIAP в опухолевых клетках [28–30]. Согласно литературным данным, нокдаун XIAP и использование низкомолекулярных ингибиторов этого белка не только приводит к индукции апоптоза, но и увеличивает чувствительность опухолевых клеток к химиотерапии [31–33]. Таким образом, XIAP можно рассматривать как потенциальную мишень, воздействие на которую позволит повысить эффективность реализации апоптотических программ, запускаемых онколитическим вирусом VV-GMCSF-Lact, в клетках глиобластомы.
Список литературы
Melcher A., Harrington K., Vile R. Oncolytic virotherapy as immunotherapy. Science, 2021, 374, 1325–1326. https://doi.org/10.1126/science.abk3436
Kochneva G., Sivolobova G., Tkacheva A., Grazhdantseva A., Troitskaya O., Nushtaeva A., Tkachenko A., Kuligina E., Richter V., Koval O. Engineering of double recombinant vaccinia virus with enhanced oncolytic potential for solid tumor virotherapy. Oncotarget, 2016, 7, 74171–74188. https://doi.org/10.18632/oncotarget.12367
Vasileva N., Ageenko A., Dmitrieva M., Nushtaeva A., Mishinov S., Kochneva G., Richter V., Kuligina E. Double recombinant vaccinia virus: a candidate drug against human glioblastoma. Life, 2021, 11, 1084. https://doi.org/10.3390/life11101084
Kabakov A.E., Gabai V.L. Cell death and survival assays. Methods Mol. Biol., 2018, 107–127. https://doi.org/10.1007/978-1-4939-7477-1_9
Whilding L.M., Archibald K.M., Kulbe H., Balkwill F.R., Öberg D., McNeish I.A. Vaccinia virus induces programmed necrosis in ovarian cancer cells. Mol. Ther., 2013, 21, 2074–2086. https://doi.org/10.1038/mt.2013.195
Koehler H.S., Jacobs B.L. Subversion of programed cell death by Poxviruses. Curr. Top. Microbiol. Immunol., 2020. https://doi.org/10.1007/82_2020_229
Greiner S., Humrich J.Y., Thuman P., Sauter B., Schuler G., Jenne L. The highly attenuated vaccinia virus strain modified virus Ankara induces apoptosis in melanoma cells and allows bystander dendritic cells to generate a potent anti-tumoral immunity. Clin. Exp. Immunol., 2006, 146, 344–353. https://doi.org/10.1111/j.1365-2249.2006.03177.x
Humlová Z., Vokurka M., Esteban M., Mělková Z. Vaccinia virus induces apoptosis of infected macrophages. J. Gen. Virol., 2002, 83, 2821–2832. https://doi.org/10.1099/0022-1317-83-11-2821
Bidgood S., Mercer J. Cloak and dagger: alternative immune evasion and modulation strategies of poxviruses. Viruses, 2015, 7, 4800–4825. https://doi.org/10.3390/v7082844
Chan FK-M., Shisler J., Bixby J.G., Felices M., Zheng L., Appel M., Orenstein J., Moss B., Lenardo M.J. A role for tumor necrosis factor receptor-2 and receptor-interacting protein in programmed necrosis and antiviral responses. J. Biol. Chem., 2003, 278, 51613–51621. https://doi.org/10.1074/jbc.M305633200
Cho Y., Challa S., Moquin D., Genga R., Ray T.D., Guildford M., Chan F.K. Phosphorylation-driven assembly of the RIP1-RIP3 complex regulates programmed necrosis and virus-induced inflammation. Cell, 2009, 137, 1112–1123. https://doi.org/10.1016/j.cell.2009.05.037
Zhang D.-W., Shao J., Lin J., Zhang N., Lu B.-J., Lin S.-C., Dong M.Q., Han J. RIP3, an energy metabolism regulator that switches TNF-induced cell death from apoptosis to necrosis. Science, 2009, 325, 332–336. https://doi.org/10.1126/science.1172308
Nailwal H., Chan FK-M. Necroptosis in anti-viral inflammation. Cell Death Differ., 2019, 26, 4–13. https://doi.org/10.1038/s41418-018-0172-x
O’Donnell M.A., Perez-Jimenez E., Oberst A., Ng A., Massoumi R., Xavier R., Green D.R., Ting A.T. Caspase 8 inhibits programmed necrosis by processing CYLD. Nat. Cell Biol., 2011, 13, 1437–1442. https://doi.org/10.1038/ncb2362
Pop C., Oberst A., Drag M., Van Raam B.J., Riedl S.J., Green D.R., Salvesen G.S. FLIPL induces caspase 8 activity in the absence of interdomain caspase 8 cleavage and alters substrate specificity. Biochem. J., 2011, 433, 447–457. https://doi.org/10.1042/BJ20101738
Kominami K., Nakabayashi J., Nagai T., Tsujimura Y., Chiba K., Kimura H., Miyawaki A., Sawasaki T., Yokota H., Manabe N., Sakamaki K. The molecular mechanism of apoptosis upon caspase-8 activation: quantitative experimental validation of a mathematical model. Biochim. Biophys. Acta, 2012, 1823, 1825–1840. https://doi.org/10.1016/j.bbamcr.2012.07.003
Kruidering M., Evan G. Caspase-8 in apoptosis: the egbinning of “the end”? IUBMB Life, 2000, 50, 85–90. https://doi.org/10.1080/713803693
Fomin A.S., Koval O.A., Semenov D.V., Potapenko M.O., Kuligina E.V., Kit Yu.Ya., Richter V. A. Analysis of biochemical markers of MCF-7 cell apoptosis induced by a recombinant analogue of lactaptin. Russ. J. Bioorg. Chem., 2012, 38, 77–82. https://doi.org/10.1134/S1068162012010086
Koval O.A., Tkachenko A.V., Fomin A.S., Semenov D.V., Nushtaeva A.A., Kuligina E.V., Zavjalov E.L., Richter V.A. Lactaptin induces p53-independent cell death associ-ated with features of apoptosis and autophagy and delays growth of breast cancer cells in mouse xenografts. PLoS One, 2014, 9, e93921. https://doi.org/10.1371/journal.pone.0093921
Lopez P.L.C., Filippi-Chiela E.C., Silva A.O., Cordero E.A.A., Garcia-Santos D., Pelegrini A.L., Reder G.M., Barbieri N.L., Lenz G. Sensitization of glioma cells by X-linked inhibitor of apoptosis protein knockdown. Oncology, 2012, 83, 75–82. https://doi.org/10.1159/000337978
Du C., Fang M., Li Y., Li L., Wang X. Smac, a mitochondrial protein that promotes cytochrome c–dependent caspase activation by eliminating IAP inhibition. Cell, 2000, 102, 33–42. https://doi.org/10.1016/S0092-8674(00)00008-8
Kvansakul M., Yang H., Fairlie W.D., Czabotar P.E., Fischer S.F., Perugini M.A., Huang D.C., Colman P.M. Vaccinia virus anti-apoptotic F1L is a novel Bcl-2-like domain-swapped dimer that binds a highly selective subset of BH3-containing death ligands. Cell Death Differ., 2008, 15, 1564–1571. https://doi.org/10.1038/cdd.2008.83
Aoyagi M., Zhai D., Jin C., Aleshin A.E., Stec B., Reed J.C., Liddington R.C. Vaccinia virus N1L protein resembles a B cell lymphoma-2 (Bcl-2) family protein. Protein Sci., 2006, 16, 118–124. https://doi.org/10.1110/ps.062454707
Dewson G., Kluck R.M. Mechanisms by which Bak and Bax permeabilise mitochondria during apoptosis. J. Cell Sci., 2009, 122, 2801–2808. https://doi.org/10.1242/jcs.038166
Elmore S. Apoptosis: a review of programmed cell death. Toxicol. Pathol., 2007, 35, 495–516. https://doi.org/10.1080/01926230701320337
Emery I.F., Gopalan A, Wood S., Chow K, Battelli C., George J., Blaszyk H., Florman J., Yun K. Expression and function of ABCG2 and XIAP in glioblastomas. J. Neurooncol., 2017, 133, 47–57. https://doi.org/10.1007/s11060-017-2422-z
Vasileva N., Ageenko A., Richter V., Kuligina E. The signaling pathways controlling the efficacy of glioblastoma therapy. Acta Naturae, 2022, 14(2), 62‒70. https://doi.org/10.32607/actanaturae.11623
Prabhu K.S., Siveen K.S., Kuttikrishnan S., Iskandarani A., Tsakou M., Achkar I.W, Therachiyil L., Krishnankutty R., Parray A., Kulinski M., Merhi M., Dermime S., Mohammad R.M., Uddin S. Targeting of X-linked inhibitor of apoptosis protein and PI3-kinase/AKT signaling by embelin suppresses growth of leukemic cells. PLoS One, 2017, 12, e0180895. https://doi.org/10.1371/journal.pone.0180895
Carter B.Z., Milella M., Tsao T., McQueen T., Schober W.D., Hu W., Dean N.M., Steelman L., McCubrey J.A., Andreeff M. Regulation and targeting of antiapoptotic XIAP in acute myeloid leukemia. Leukemia, 2003, 17, 2081–2089. https://doi.org/10.1038/sj.leu.2403113
Hussain A.R., Bu R., Ahmed M., Jehan Z., Beg S., Al-Sobhi S., Al-Dayel F., Siraj A.K., Uddin S., Al-Kuraya K.S. Role of X-linked inhibitor of apoptosis as a prognostic marker and therapeutic target in papillary thyroid carcinoma. J. Clin. Endocrinol. Metab., 2015, 100, E974–E985. https://doi.org/10.1210/jc.2014-4356
Zhang Y., Huang F., Luo Q., Wu X., Liu Z., Chen H., Huang Y. Inhibition of XIAP increases carboplatin sensitivity in ovarian cancer. Onco Targets Ther., 2018, 1, 8751–8759. https://doi.org/10.2147/OTT.S171053
Carter B.Z., Gronda M., Wang Z., Welsh K., Pinilla C., Andreeff M., Schober W.D., Nefzi A., Pond G.R., Mawji I.A., Houghten R.A., Ostresh J., Brandwein J., Minden M.D., Schuh A.C., Wells R.A., Messner H., Chun K., Reed J.C., Schimmer A.D. Small-molecule XIAP inhibitors derepress downstream effector caspases and induce apoptosis of acute myeloid leukemia cells. Blood, 2005, 105, 4043–4050. https://doi.org/10.1182/blood-2004-08-3168
Abbas R., Larisch S. Targeting XIAP for promoting cancer cell death ‒ the story of ARTS and SMAC. Cells, 2020, 9, 663. https://doi.org/10.3390/cells9030663
Дополнительные материалы отсутствуют.


